Способ получения производныхтетрагидро-1,4-бенздиазепинон-2- карбоновой -4 кислоты
Иллюстрации
Показать всеРеферат
ОП ИСАНИЕ
ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ
Союз Советски а
Социалистических
Республик
Iii 798101 (61) Дополнительное к авт. свил-ву (22) Заявлено 13.07.78 (21) 2644010/23 04, Э (5l )М. Кл.
С 07 1.) 243/28//
А 61 К 31/70 с присоединением заявки ла
Государственный коиитет (23) Приоритет
Опубликовано 23.01.81 ° Бюллетень М 3
Дата опубликования описания 25 01,81 пс делан изобретений и открытий (53) УДК 547.892. .07(088.8) О. П. Руденко, T. М. Шмигель, А. И. Лисицына и А. В. Богатский (72) Авторы изобретения
Одесский орцена Трудового Красного Знамени государственный университет им. И. И. Мечникова (71) Заявитель (54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ТЕТРАГИДРО—
-1,4-БЕНЗЙИАЗЕПИНОН-2КАРБОНОВОЙ-4-КИСЛОТ@ Я P Т )а
ФЗЦ й!- ЫИ3
Изобретение относится к способу получения новых соединений - 4- Я-аамещенных производных тетра гидро-1,4° бензциазепинонов-2 (где 4- Й -замещающей группой является остаток эфира карбоновой кислоты), которые могут найти применение в мецицине.
Известен способ, по которому получают 4- К-замешенные 5-фенил-1,3,4,5-тетра гидро-l,4-бенздиазепиноны-2, где
4- е)-заме;щающей группой является низший алкил, бенэил или замещенный бенэил. По этому способу, например, 7ме» т окси-4-метил-5-фен ил-1, 3, 4,5тетрагидро-1,4-бенэдиазепинон-2 получают посредством возцействия на соответствующий оксим 2-Я -метил-иэохииолона полифосфорной кислотой при 130йСв те чение 10 мин с послецующей обработкой реакционной смеси аммиаком. Оксим получают взаимодействием соответствующего 2-)е -метил-изохинолона с хлоргидратом гидросиламина при кипячении их растворов в присутствии ацетата натрия, Этот
2 способ основан на расширении шестичленного кольца 2-И юамещенного оксима изохинолона до семичленного 4-Й-аамещенного 1,4-бензциазелинона-2 (1J .
Известен также способ, по которому
4- )е -замешенные производные тетрагицро-1,4-бенэдиазепинонов-2 (где 4- Я-замещающей группой является низшая алкильная или алкиленовая группа) получают алкилированием галоидалкилом или галоицалкиленом 4- р1-незамещенного
1,4-бенздиаэепинона-2. Например, 1-метил-4-аллил-5-фенил-7-хлор-1, 2,4,5-. -. тетрагидро-ЗН-1,4-бенэдиазепинон-2 получают взаимодействием аллилбромида с 1-метил -фенил-7-хлор-1,2,4,5-тетра гидро-ЗН-1,4-бенздиазепиноном-2 в диметилформамиде при нагревании на водяной бане в течение 16 ч.
Аналогичные 4-Я -метильные замещенные получают взаимодействием с йоцистым метилом при нагревании в ме» таноле в течение 1,5 ч. Этот способ по- . лучения 4-т1- алкильных и 4- N-алке798101 и соон (2) 20
0OR
О О
П .б б
С и соон
OR г соон (Л
e00R
М -,"СООН (6)
C00R й
3 нильных замешенных тетрагицро-1,4-бенздиазепинонов-2 основан на алкилировании галоидным алкилом, галоицным алкиленом соответствуюших 4- М -незамещенных тетрагицро-1,4-бензциазепинонов-2 (2).
Однако известные способы не позволяют получать эфиры 5-фенил-1,3,4,5-тетрагидро-1,4-бензциазепинон-2-карбоновой 4-кислоть.
Цель изобретения — получение эфиров
5-фенил-1, 3,4,5-тетра гидро-1,4-бензциазепинон-2-карбон овой-4-кислоты, которые могут найти применение в мецицинкой практике и расширить арсенал средств воздействия на живой организм.
Указанная цель цостигается способом получением новых производных тетрагидро-1,4-бенздиазепмнон-2-карбоновой-4-кислоты. обшей формулы 1. где . Й вЂ” водород, галоиц, или низший алкил; а
Р,1- водород или ОртО мета- или парагалоид; — низший алкил c 1-4 атомами
2 углерода или бензилрацикал, заключающийся в том, что производное
Я вЂ” (2-аминобензгицрил)-глицина общей формулы 11.. подвергают взаимодействию с эфиром хлормуравьиной кислоты обшей формулы И1
25 в среде органического растворителя в присутствии органического основания при температуре от О С no — 20 С.
О 0
Целевой процукт выделяют известными приемами.
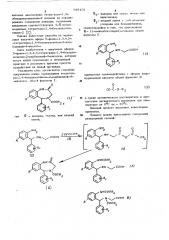
30 Процесс можно представить слецуюлей реакционной схемой.
8101.
4 мак производнык (1) присутствуют полосы поглощения валентнык колебаний карбонильной группы циаэепинового кольца в области 1650-1670 см 1, карбонильной группы 4-Ы-«эамещающего остатка при 1690-1700 см ",Я Н-групп в об4 ласти 3180-3450 см
Строение 1 подтверждают также превращением, например, бенэилового эфира
»0 5-фенил-7-клор-l,3,4,5-тетрагицро-1, 4-бенздиазеп ин он-2-к а рб онов ой«4-кислоты (la) в известное соецинение, 5-фенил-7-хл ор-l, 3, 4, 5-т е тра гидро-1,4-
:-бенэдиазепинон-2 (7):
О (7) оси с и р» М
5 79
Высокая реакционная способность смешанного ангидрида (4) в реакции внутримолекулярного аминолиза, приводящая к образованию циазепинового кольца, препятствует протеканию побочного процесса, например образованию продуктов 2- К -замещения кислоты (1). Соединения (5) и (6) в данных условиях получения не образуются.
Однородность состава (1) контролируют двумерной тонкослойной хроматографией. Строение поцтвержцают спектральными метоцами, в частности ИК-спектроскопией. Например, в ИК-спектрограмПолучение (7) из (la) осуществляют обработкой последнего бромистым водородом в ледяной уксусной кислоте при 20-22 С в течение 0,5 ч с после- 5о дующей нейтрализацией реакционной сМе« си водным раствором основания, напри мер бикарбонатом натрия или аммиаком.
Характеристики соецинения (Т.. пл., Я, ИК-спектры и ap.), полученного известным и предлагаемыми способами сов» падают. Положение 4- Й -«замешенных производных (1) подтверждают также тем, что, например, в условияк потенциометрического титрования 0,05 н раст- вором хлорной кислоты в ледяной уксусной кислоте растворы I в этой же кислоте не титруются, в то время, как 4 Я-незамещенные, например, (7) в этих условиях количественно оттитровываются по 4-Ц -положению. Известно, что азот в положении 1 диазепинового кодьца не обладает основными свойствами и в указаннык условияк не титруется, а приведенный пример поцтвержцает 4-Я-замещение производных (1). Молекулярный вес (1) подтверждают при помощи массспектроскопии.
Пример 1. Изобутиловый эфир
5-фенил-7-бром-l, 3,4,5-тетрагидро-1, 4-бензциазепинон-2-карбоновой-4«кислоты.
К раствору 3,35 г (0,01 моль)
)4 -(2-амино-5-бромбензгицрил) глицина в 40 мл безводного диметилформамида, 25 мл этилацетата и 3,5 мл триэтилами» на при (-20) - (-18)©С, прибавляют
2,8 мл (0,02 моль) изобутилхлорформиата, смесь перемешивают 0,5 ч, затем в течение 1 ч температуру повышают цо (-6) - (-5) С. После этого растворители удаляют в вакууме, остаток растворяют в 130 мл этилацетата и 15 мл воды, раствор промывают 0,1 н соляной кислотой (Зк10 мл), 57-ным раствором бикар4 боната натрия (Зх15 мл), затем водой (2к20 мл). Органический раствор обезвоживают сульфатом натрия. После отгонки растворителя в вакууме и перекристаллизации остатка из метанола получают
3,6 г (86%) эфира. Т. пл. 143-144 С, 0
Р 0,53.
Элементный анализ:
Вычислено,%: С 57,4; Н 5,0; N 6,7.
С20Н2! Мгою В
Найдено,7: С 57,2; Н 5,1; Я 6,8.
ИК-спектр 1670, 1690 (СО), 3230 и 3450 см» (g -Н).
Пример 2 . Бензиловый эфир
5 фенил-7-бром-1,3;4,5-тетрагидро-1,4-бенэдиазепинон-2-карбоновой-4-кислоты.
К раствору 3,35 r (0,01 моль)
Ц -(2-амино-5-бромбензгицрил) -глицина в 40 мл этилапетата и 10 мл триэтиламина при (-10}- (-8) С прибавляют
3,8 г (0,022 моль) бензилхлорформиата, смесь перемешивают 15-17 мин, затем
7 7981 температуру повышают цо О С и продоло жают перемэшиванке в течение 1 ч. После этого к реакционной смеси прибавляют 100 мл этклацетата, промывают 1н раствором соляной кислоты (Зх15 мл), 5%-ным раствором бикарбоната натрия (4х20 мл) и водой (3x20 мл), Этилацетатный раствор обезвоживают сульфатом натрия, затем упарквают в вакууме, остаток перекристаллизовывают кз метанола и получают 3,74 г (83%) эфира. Т. пл, 179-180 С, R 0,69. б
Элементный анализ:
Вычислено,%: С 61,2; Н 4,2; Я 6,2.
Су Н,,> К,О Вг 5
Найдено,%: С 61,0; Н 4,1; Я 6,3.
ИК-спектр 1655, 1 700 (С=О), 3180 и 3450 см" (ЦН).
Аналогично получа1от бензиловый эфир
5-фенил-7- хлор-1,3,4,5-тетрагидро- 2э
-1,4-бенздиазепинон-2-карбоновой-4-кислоты С Н М О С6(выход 82%; т. пл)
151-152 С и Р 0,69) и бензиловый эфир 5-фенил-7-метил-1,3,4,5«тетра гидро-1,4-бензциазепкнон-2-карбоновой-4- д
KNCJ1oTbl С 4 Нрр К О 3 (выход 83%1 т, пл. 192-193оС, Ру. 0,69).
ИК-спектр 1665, 1700 (C ) и
3200-3450 см (Ц-H)..
Пример 3. 5-Фенкл-7-хлор- Эо
-1,3,4;5«тетрагидро-1,4 бенздиазепинон-2.
К навеске 2 г (0,005 моль) бензилового эфира 5-фенил-7-хлор-1, 3,4,5-тетрагицро-1,4-бенздиазепкнон-2«карбоновой-4-кислоты прибавляют 7 мл 30%35 ного раствора бромистого водорода в лецяной уксусной кислоте и при 20«22 С перемешивают 0,8 ч. Затем реак0 цконный раствор выливают в 50 мл лецяной веды, нейтрализуют раствором би- О карбоната натрия, осацок отделяют, перекрксталлкзовывают из метанола и цолучают 1,05 г (77%) эфира С H>N>OCP, ) 84 1850
П р и м е ч а н и е. Значения R g в 4 системе ацетон-гексан (1:2) на пластинах "5_#_0503, ИК-спектры в таблетках
КВЧ, прибор "09A4h-РФег
01 8
Формула изобретения
Способ получения производных тетрагидро -1,4-бенздказепкнон-2-карбоновой-4-кислоты общей формулы где Я - водород, галоид, или низший алкил; - водород или орто-, мета-или парагалоиц;
- низший алкил илк бензилрадикал, отличающийся тем, что производное и -(2-амино-бензгидрил) -глицина общей формулы
СО6> (2) подвергают взаимодействию с эфиром хлормуравькной кислоты общей формулы
Cga=0 Ц (3) в среце органического растворителя и в присутствии органического основания при температуре от 0ОС цо - 2(РС.
Источники информации, принятые во внимание при экспертизе
1. Патент США % 3501474, кл. 260-239.3. опублик, 1968.
2.бег. ОИЕП No. 1445865, кл. 12 р 10/01, опублик. 1973.
Составитель Г, Коннова
Редактор Г. Кацман Техред С.Мнгунова Корректор Н.Швыдкая
Заказ 9942/27 Тираж 454 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб., д. 4/5
Филиал ППП "Патент", г. Ужгород, ул. Проектная, 4