Способ получения нитротиофе-новых , -непредельных ketohob
Иллюстрации
Показать всеРеферат
Союз Советскик
Социалистических
Республик
ОПИСАНИЕ
ИЗОБРЕТЕНИЯ
К АВТОРСКОМУ СВИ ИТИЛЬСТВУ (»)802282 (61) Дополнительное к авт. сеид-ву (22) Заявлено 010379 (21) 2725850/23-04 с присоединением заявки ¹ (23) Приоритет
Опубликовано 07.02.81. Бюллетень N9 5
Дата опубликования описания 07.0281 (51) рА. Кл.з
С 07 Э 333/12
Государственный комитет
СССР по делам изобретений и открытий (S3) УДК 547,737 .07 (088.8) (72) Авторы изобретения
Ю,Д.Чуркин и Л.В.Панфилова (71) Заявитель
Куйбышевский политехнический институт им. В.В.Куйбышева (5 4) СПОСОБ ПОЛУЧЕНИЯ НИТРОТИОФЕНОВЬй
g, P -НЕ ПРЕДЕЛЬНЫХ КЕТ0Н08
s СН=СН-Со-М q
zaex З З02 Et Н, я2
Изобретение относится к новому способу получения нитротиофеновык о -непредельных кетонов, большая
) часть иэ которых получена впервые.
Известен способ получения a p -непредельнйх iKBTDHQB с нитрогруплой в тиофеновом кольце путем кротоновой конденсации нитротиофеновых альдегндов с ароматическими и гетероциклическими метилкетонами в присутствии
30 щелочных или кислотных катализаторов.
Однако 5-нитро-2-тиофеновый альдегид нестоек в присутствии щелочей fl), Поэтому синтезировать ннтротнофеновые непредельные кетоны с использованием l$ щелочных катализаторов практически невозможно, так как реакция либо не идет совсем, либо приводит к очень низким выходам, Наиболее близким к предлагаемому 20 способу является способ получения Нитротиофеновых l,P -непредельных кетонов путем конденсации нитротиофеновых альдегидов и метилкетонов ароматического и гетероциклического рядов в среде ледяной уксусной кислоты в присутствии каталитических количеств концентрированной серной кислоты..
Выходы непредельнйх кетонов в этих .случаях 10-48% (2). Однако в ряде ЗО случаев указанный способ не позволяет получить требуемое непредельное нитротнофеновое карбонильное соединение. Так, например, провести конденсацию 5-ннтро-2-тиофенового альдегида с ацетоном нлн 2,4,б-триметоксиацето- феноном при использовании в качестве катализатора серной кислоты не удается.
Целью изобретения является разработка способа конденсации нитротио- феновых альдегидов с метилкетонами, позволяющего получать новые.тиофеновые а,рнепредельные,-кетоны, содержащие нитрогруппу в одном из положений гетероцнклического кольца, а так- же повышать выход при синтезе извест ных ннтротиофеновых непредельных кетонов, Поставленная цель достигается способом, заключающимся в том, что нитротиофеновые o(,P -непредельные кетоны общей формулы
"02282
Il B-CHg Ri 2l0g R2- a I
О- ., -, 0
C2Hg В(-КО,, З2-СН, 1 получают конденсацией нитротиофено- )g вых альдегидов с ацетоном и метилкетонами ароматического или гетероциклического рядов в среде ледяной уксусной кислоты при температуре кипения последней с использованием в качестве катализатора ацетата аммония.
Количественное соотношение конденсирующий агент (ацетат аммония): исходный нитроальдегид составляет 0,52,0. Реакцию проводят не при понижен- 20 ной температуре, как ведут реакцию кротоновой конденсации, а при нагревании реакционной смеси. Реакцию осуществляют при температуре кипения ледяной уксусной кислоты (118 C) в течение 2-20 ч (в зависимости от природы радикала R2) в кетонном компоненте реакции (см. табл. 1,2) с последующей выдержкой реакционной смеси в течение трех суток и выделением целевых соединений .известными методами, При этом выход иитротиофеновых с,p— непредельных кетонов в этих условиях достигает 40-95%.
Предлагаемый способ применения для получения a, ф -непредельных кетонов из З5 нитротиофеновых альдегидов и метилкетонов ряда бифенила и 2,2-битиенила.
В этом случае выходы целевых соединений составляют 12-38%.
Строение полученных кетонов было 4О доказано ИК-спектрами, элементным анализок, а также сравнением полученных физико-химических констант с известными в литературе (для соединений 1 а-е) . Сравнение выходов по предлагае- 4 мому способу и температур плавления веществ с литературными данными приведено в табл. 1. Физико-химические характеристики вновь синтезированных нитротиофеновых непредельных кетонов приведены в табл. 2. Чистоту полученных кетонов контролируют тонкослойной хроматографией на пластинках
"Ь tufol 0Ч=254".
" р и м е р 1. Получение 4-(5.нитротиенил-2) -бутен-3-она-2 (Ia) . $5, 1,57 г (0,01 моль) 5-иитро-2-тиофенового альдегида растворяют в минимальном количестве, ледяной уксусной кислоты, добавляют 0,39 г (0,005 моль) ацетата аммония и 0,58r (0,01 моль) ацетона. Поддерживая слабое кипение, реакционную смесь на гревают в течение 20 ч при 118 С.
После охлаждения смесь выдерживают при комнатной температуре трое суток.
Если осадок не выпадает, реакционную смесь наполовину разбавляют водой. Выпавший осадок отфильтровывают, промывают водой и перекристаллизовывают из подходящего растворителя (изопропиловый спирт или толуол) .
Выход кетона Ia составляет 1,28 г (65%), т.пл. 131,5-132,5 С.
Пример 2. Получение 3-(5-нитротиенил-2) — 1-фенилпропен-2-она-1 (соединение Ir).
0,01 моль (1,57 r) нитротиофенового альдегида (5-нитро-2-.тиофенового альдегида) растворяют в минимальном количестве ледяной уксусной кислоты, добавляют 0,02 моль (1,54 г) ацетата аммония и 0,01 моль метилкетона (1,2 г ацетофенона). Поддерживая слабое кипение, реакционную смесь нагревают в течение 2 ч при 118 С.
Далее обработку реакционной смеси ведут аналогично описанному в примере
1. Выход кетона Ir составляет 2,41 г (93%), т. пл. 180,5 С.
Пример 3. Получение 3-(5-нитротиенил-2) -1-(2,2 -битиенилил-5) -пропен-2-она-1 (Тд) .
0,01 моль (1,57 г) нитротиофенового альдегида (5-нитро-2-тиофенового альдегида) растворяют в минимальном количестве ледяной уксусной кислоты, добавляют 0,01 моль (0,77 r) ацетата аммония и 0,01 моль (2,08 г 5-ацетил-2,2-битиенила). Поддерживая слабое, кипение, реакционнцю смесь нагревают 2 ч при 1184С. Дальнейшую обработку реакционной смеси и выделение целевого продукта ведут аналогично описанному в примере 1. Выход кетона
Тд 1,05 r (30%), х,пл. 237-238 С.
Использование предлагаемого способа получения нитротиофеновых Ы>риедредельных кетонов по сравнению с существующими способами кротоновой конденсации обеспечивает следующие преимущества: синтез новых ранее недоступных тиофеновых Ы,Р --непредельных кетонон, содержащих нитрогруппу в гетероциклическом кольце (соединения Тд, té fа-е, Ia, r-e); повышение выхода при получении известных нитротиофеновых непредельных кетонов (см. табл. 1) .
Разработка такого способа получения непредельных карбонильных соединений своевременна и необходима потому, что ароматические и гетероциклические соединения, содержащие систему сопряженных СзС и СлО-кратных связей проявляют биологическую активность. Введение же нитрогруппы в гетероциклическое кольцо непредельных кетонов резко усиливает направленное биологическое действие этих препара- тов.
802282
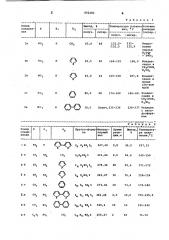
Таблица 1 в
Выход, Ф
Температура плавле ния, 4С получ. литер. получ. Iëèòåð.
131131,5,48,131,5,132,5 к02
65,0
Н
65,5 20 194-195
Й02
196, О
Тб
Й02
40,0 24 205-206
?в
N01
48 179-180
80,0
Н 30,0
Н0г
Колич.235-236
Таблица 2 ввввввввввввйвВВ
1д НО С, Н МО S 347,40 2,0
30,0
237,23
С Н9 NO> S 211,24 2,0 94,6 149-150 и а СН . ИО
Сн>
С, Н9 ИО) 5 279, 34 20 55, 4 171-172 и б сн ко
С, H9 NOy S 263 g 27 10 76 g4 158-159 и а СН МО, Ск Нн НОЗ S 273,30 10
"3 " И
73,0
179-180
С Н НО S> 361,46 2,0 14,0 235-235,5
Ид СН Но, С Н 6 ЙО> S 349 4
12
241-242
Сн и о
71-72
Иа С Н, НО, Номер соедине" ния
Номер R соединения
Брутто-форму Иолекула лярный вес
Сн Се Н 1 МО S 255,27 2
Условия реакции (литер.) Нитро вание смесью
Н25сФ
+ НМ03
Конденсация в
СНЗСоон, Н 504
207,0 Конденсация в среде
10%-ной
МаОН
180-181 Конденсация в
СНЗ СООН, Н 1504
236-237 Реакция с кетофосфораном
Выход, Температур ра плавления, С
802282
Продолжение табл.
Молеку- Вре лярный реа вес ции
Брутто-форму ла
Номер соеди нения
Щг С Н йО
287, 34 8
Ся НВ НО Я
169-170
375,48 2 с н
38,2
225-227 с н фе
Составитель Л.Иоффе
Техред M. Петко Корректор Г.Решетник
Редактор Э.Бородкина
Заказ 10500/28 Тираж 454 Подписное
ВИИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб., д. 4/5
Филиал ППП Патент, г. Ужгород, ул. Проектная, 4
/ ио
Ся Н11 ИО 5
НО 3 / / C2 Н N03 S
Формула изобретения
1. Способ получения нитротиофеновых о(р -непредельных кетонов общей фор- 20
I 3 мудилы
И1
К Í=СЫ- СО-К2 где В-вО В -Н, В—
21
R-СН51 З1 М02 З2 6К5,
A- Ор-С Я 1М g-21021 Вд-6Н
/ 3 и
363,44 10 17 233-234 отличающийся тем, что нитротиофеновые альдегиды конденсируют с ацетоном и метилкетонами ароматического или гетероциклического рядов в среде ледяной уксусной кислоты при температуре кипения последней, в присутствии в качестве катализатора ацетата аммония.
2. Способ по п. 1, о т л и ч а ю шийся тем, что количественное соотношение ацетат аммония: нитроальдегид составляет 0,5-2,0.
Источники информации, приняте во внимание при экспертизе
1. РЖ Химия, 1860, 92528.
2. Цукерман С.В.Никитченко В.М., Лаврушин В.Ф. Синтез нитропроизводных (, -HeHBckiHg&HHblx кетонов, содержащих ядра бемзола и тиофена-.ЖОХ, т. 32 с. 2324, 1962.