Четвертичные соли 2-фторалкилбензтиазолия,обладающие фунгицидной и бактерицидной активностью
Иллюстрации
Показать всеРеферат
СОЮЗ СОВЕТСНИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИН
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Н АВТОРСНОМУ СВИДЕТЕЛЬСТВУ где
ГОСУДАРСТВЕННЫЙ НОМИТЕТ СССР
ПО ДЕЛАМ ИЗОБРЕТЕНИЙ И ОТКРЫТИЙ
{ 21) 2887962/23-04 (62) 2673680/05 (22) 30.11.79 (23) 20.07.78 (46) 23,02 ° 84. Бюл. 9 7 (72) Л.И. Трушанина, Л.М. Ягупольский, T.È. Черепенко, A.Â. АгафоНов, Б.Г. Вальков и В.Н. Салеева (71) Институт органической химии
AH Украинской ССР и Волгоградский научно-исследовательский противочумный институт (53) 547.789.6.03 (088.8) (56) 1 ° Мельников H.H. Химия пестицидов. М., "Химия", 1968, с. 133.
2. Машковский M.Ä. Лекарственные средства. М., "Медицина", 1972, т.2, с. 436.
3. Там ве, с. 459.
4. Там же, с. 460. (54) четБеРтичные сОли 2-ФтОРАлкил-.
БЕНЗТИАЗОЛИЯ, ОБЛАДАЮШИЕ ФУНГИЦИДНОЙ И БАКТЕРИЦИДНОЙ АКТИВНОСТЬЮ, „„SU„„1 А
З 50, С 07 D 277/64; A 01 К 43/78;
A 61 к 31 425 (57) Четвертичные соли 2-фторалкилбенэтиаэолия формулы (1) 3
1 )к, х- „>
R" — метил(R — фторметил
R — нитрогруппау
Х вЂ” метилсульфат, или R — метил
2 (R — э я а -трифторэтил)
3 (R — водород, Х вЂ” анион хлора, или R — этил;
R — ди фтормет ил;
R — водород; 3
Х вЂ” анион хлора, обладаюцие.фунгицидной и бак герицидной активностью.
822513
Иэобретение относится к новым химическим соединениям, конкретно, к четвертичным солям 2-фторалкилбенэтиазолия, общей формулы (1)
R3 S
I a !
Rl где R — метил
2
R — фторметил)
R3 — нитрогруппа, Х вЂ” метилсульфат или R — метился
R †./3<9<6 -трифторэтил
R — водород >
Х вЂ” анион хлора
I
H JIB R — ЭТИЛ )
R — дифторметил;
R — водород;
Х вЂ” анион хлора, обладающим фунгицидной и бактериальной активностью.
Указанные свойства предполагают возможность применения нх в сельском хозяйстве и медицине.
Известен фигон-2,3-дихлорнафтохинон-1,4, проявляющий свойства фунгицида (1).
Известны также бенэолсульфохлорамид-натрий (хлорамин) (23, фенол(3) и лизол (раствор креэола в калийном мыле) (.4 ), обладающие бактерицидными свойствами.
Целью изобретения является расширение арсенала средств воздействия на живой организм.
Цель достигается четвертичными солями 2-фторалкилбензтиаэолия
Формулы (1), обладающими фунгицидной и бактерицидной активностью.
Соединения формулы (1) получают конденсацией о-алкиламинотиофенола с хлорангидридом соответствующей фторсодержащей кислоты в бензоле при температуре 0 С или алкилированием 2-фторалкилбензтиазола диметилсульфатом при 120 С.
Синтезированные четвертичные соли представляют собой кристаллические .бесцветные вещества, растворимые на холоду или при нагревании в воде, спирте, ацетоне, не растворимые в бензоле, эфире.
Пример 1. Метилсульфат 2-фторметил-3-метил-6-нитробензтиазолия (I) .
1,5 г 2-фторметил-6-нитробензтиазола, 1,5 r диметилсульфата нагревают 1,5 ч при 112-120 С. Растирают с абсолютным эфиром. Фильтруют, сушат в эксикаторе над Р2ОЗ. Выход .98,3%.T .ïë.178-180 С(с осмолением) .
Найдейо,%: F 18,24; 18,45 .
С, Н+, Н 28 О, Вйчнслено,(: Г 18,93.
Пример 4. Фунгитоксичность соединений формулы (1) определяют на конидиях гриба H. Sativum по методу контактного прорастания в водной среде. Экспозиция 19-21 ч при
23-24 С, повторность четырехкратная.
В таблице представлены минимальные, ингибирующие прорастание спор концентрации. Наиболее токсичным для спор гриба, не уступающим по активности эталону-фигону, является соединение II, Выраженной активностью обладают соединения 1, III, превы.Пример 2. Хлорид 2-(p, p,p
-трифторэтил)-3-метилбенэтиаэолия (II) .
К раствору 3,5 г хлорангидрида трифторпропионовой кислоты в 5 мл бензола добавляют при охлаждении до 0 С 3 r й-метил-о-амннотиофено- . ла. Через 2 ч отфильтровывают, промывают бензолом, ацетоном. Выход 68%. T.ïë. 160-162 С (с раэложе10 нием).
Найдено,%: F 21,05; 21,17
С о HgCIF3NS
Вычислено,%: F 21,30.
Пример 3. Хлорид 2-дифтор15 метил-3-этилбензтиаэолия (III).
Аналогично примеру 2 получают вышеуказанное соединение, Выход 24,7Ъ.
T.цл. 206 С.
Найдено,%г F 15,91; 16,09
20 C>H>CIF2NS
Вычислено,%г F 16,14
Биологические свойства новых веществ подтверждаются примерами.
Пример 4. Фунгицидные свой25 ства определяют по методу торможения роста мицелия чистых культур фитопатогенных грибов (AIternaria
radicina М.D. et Е., AspergiIIus
niger van Tiegh, ВКМГ-412; Fusarum
30 Охуэт,отищ ЯсЫесЬй ВКМГ -1182р
Helmintho sporium sativum P. К. etф, ВНПЦА 160 A, Venturia inaequaIis (cke) Kint) на твердой картофельноглюкозной среде. В расплавленный
35агаР вносят растворенную.в ацетоне навеску вещества, перемешивают и
I .Разливают в чашки Петри. После застывания инокулируют агар кусочками мицелия. Повторность четырехкратная.Через 70 ч роста при 25-26 С изме40 ряют диаметр колоний и определяют энергию роста грибов в процентах к контролю. Указанные в таблице эталонные препараты берут в концентрации-по действующему веществу.
45 В контрольные чашки вносят адекватное количество чистого ацетона.
Полученные результаты показывают
) что соединения формулы (1) .обладают выраженным фунгицидным действием, превосходящим активность хлоРамина, лизола, фигона. Наиболее активными являются соединения (I) и (II) .
822513
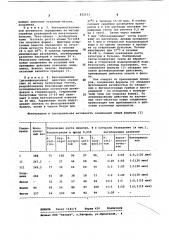
1 ость соединений общей формулы (I) Соеди- Моле- Торможение роста мицелия, Ъ к контролю Разведение (в тыс.), ление кулярКонцентрация в рреде д,05% ингибирующее развитие ный вес
Asp. F. Н. Ч. Н .
niger oxyspo shti- inae- satirum vum quaIis vum бакте- бактерицидриоста- ное тическое
А.
radiС 1115
100 96 97 96 1:2 1120 .1:0,1(20 мин) 75
388
1!20 1:50 1г1(20 мин) 96 °
27 44 98
267,5
249,5
30 64 60. 50 1z2 1:20 1г1(20 мин) 77
Хлорамии
41 33 38 18 13 1:2 1г20 1:1(10 мин)
32 31 57 . 40 94 )1:1 1:5 1:0,1(10 мин) 266
Ллзол
Фенол 94
Фигов 227
48 54 86 97 100 71:1 1:10 1:0,1(10 мин)
94 100 58 92 99 1:20
ВНИИПИ Заказ 114.1/5 Тираж 410 Подпксное
Фллкал ППП "Патент, г.ужгород, ул.Проектная, 4
Шающие действие эталонов-ли эола, хлорами на .
Пример 5. Бактериостатическую активность определяют по методу серийных разведений на питательном бульоне. Тест-объект — возбудитель чумы 3ersenia pestis штамм 72/1458 (ие споровая форма). Действие испытуемых веществ определяют по отсутствию мутности бульона в течение
24 ч при 28 С. В таблице приведены ,минимальные разведения, ингибирующие развитие бактерий в течение 24 ч.
Результаты таблицы показывают, что новые соединения не уступают или превышают действие эталонов: хлор- 15 амина, фенола, лизола. Наиболее .активным является препарат II.
Пример 6. Бактерицидное (дезинфекционное) действие опреде- 20 ляют.по методу батистовых тестов, разработанному Всесоюзным научно,исследовательским институтом дезин,фекции и стерилизации. Стерильные батистовые тесты (5-10 мм) заливают 2 мпрд бактериальной взвесью на 20 мин. Зараженные тесты подсушивают сначала на фильтровальной бумаге, затем в чашках Петри при .
,Ф
Фунгицидная и бактериальная активн
37 С в течение 15-20 мин. В колбах готовят серийное разведение препаратов и в эти растворы опускают зараженные тесты (из расчета 0,5 мл на 1 тест). Затем через каждые
5 мин "обеззараженные" тесты извлекают из растворов, дважды промывают по 5 мин в стерильной водопроводной воде и по одному засевают в пробирки со стерильным бульоном, Посевы инкубируют при 37 С в течение
24-48 ч, снимая показатели роста культуры в бульоне. Контрольные тесты подвергают таким же обработкам в стерильной водопроводной воде.
Результаты таблицы показывают, что соединения формулы (1). обладают высоким дезинфекционным действием, превышающим действие. лизола и фенола.
Как следует из приведенных примеpos, соединения формулы (1} обладают фунгицидной активностью по отношению к фитопатогенным грибам и бактерицидной — по отношению к возбудителю чумы (не споровая форма). По антимикробному действию на изученных тест-объектах новые соединения превосходят или приближаются к действию эталонных препаратов.