Электрохимический способ восстановления металлов с переменной валентностью
Иллюстрации
Показать всеРеферат
Союз Советск ин
Социапнсткческнк
Республик
ОП ИКАНИЕ
ИЗОБРЕТЕН ИЯ
К АВТОРСКОМУ СВИДЕТЕЛЬСТВУ (щ903383 (61) Дополнительное к авт. саид-ву (22) Заявлено 02.04.79 (2! ) 2746108/23-26 с присоединением заявки И (23) П риоритет
Опубликовано 07.02.82. Бюллетень №5
Дата опубликования описания 09.02.82, (5l)M. Кл.
С 25 В 1/ОО Ъеударственный комитет
СССР но делам изобретений н открытий (53) УДK621.Ç57..1 (088.8) (72) Авторы изобретения
Л. В. Опарин, B. П. Бочин, А. В. Маркешин „ и В. В; ЗМЫДИйа . 1
ВСЫ ЧЬЕ : ;
ИАткж-мо. тЕХНЧЧРИАЯ ъ
6 И БЛ И 11Ък, (71) Заявитель (54) ЭЛЕКТРОХИМИЧЕСКИЙ СПОСОБ ВОССТАНОВЛЕНИЯ
МЕТАЛЛОВ С ПЕРЕМЕННОЙ ВАЛЕНТНОСТЬЮ
Изобретение относится к гидрометаллургии металлов, обладающих переменной
1 валентностью, и может быть использовано в металлургической и химической промышленности.
В современной гидрометаллургии металлов, обладающих переменной валентностью, широко используется электрохимический способ их восстановления в водных растворах электролитов с.целью получения низких валентных форм и их
1О соединений, наиболее пригодных для аффинажных и других процессов.
Известен электрохи мический способ восстановления металлов с переменной
35 валентностью, в частности урана, в электролизере с диафрагмой, разделяющей анолит и католит, с использованием исхоаного раствора в качестве католита 311.
Для известного способа характерны следующие электрохимические реакции: на катоде: г+
UOã + e uOð
002 e uo> с последующей химической реакцией
uO + Н вЂ” uO, - гНеО на аноде: 20-Ог+4Н + ge суммарная электрохимическая реакция
uo „— u" о, В табл. 1 приведены основные показатели известного способа восстановления сульфата уранила до урана (ХУ) в еернокислом растворе с концентрацией НдS
58 г/л и концентрацией урана (ХУ)
70 г/л. при 1 = 41 С.
Данные табл. 1 показывают, что затраты электроэнергии на восстановление
1 кг () (ХУ) составляют 1,244
2,6 кВт. ч при изменении плотности тока
200 - 800 А/ма.
Однако известный электрохимический способ восстановления металлов из-за высоких затрат электроэнергии остается дорогостоящим. Снизить затраты электроэнергии за счет изменения режимов электролиза, практически невозможно.
3 9033
Пелью изобретения является сниженид напряжения на электролизере.
Указанная цель достигается электрохимическим способом восстановления металлов с переменной валентностью в 5 электролизере с диафрагмой, разделяющей анолит и католит, с использованием исходного раствора в качестве католита, причем процесс восстановления ведут при одновременной подаче сернистого ангидрида в анолит и католит.
Способ осуществляют в диафрагменном электролизере, а сернистый ангидрид подают одновременно в катодное и анодное пространство электролизера. В католит газ барботируют через раствор электролита, а в анолит через пористую стенку газопроницаемого графитного анода, рабочий слой которого промотирован платиновым катализатором от l да 2 мг о на 1 см . В качестве катода используют свинец или графтированную ткань ТВШ-800.
Электрохимический способ осуществляют согласно одновременному протеканию следующих реакций, например для восстановления сульфата уранила до урана (У1): на катоде: 00 +2a 4H — 04 -2%0 на аноде: SOg 2йф З0 Н 2е
30 .суммарная реакцйя: UO 50q U" + ЭЗ
Данные:реакции дают возможность снизить равновесный потенциал в предложенном способе более чем в два раза..
Пример 1. Электрохимическому
35 восстановлению подвергают водный раст вор католита, содержащий сульфат. уранила с концентрацией 70 г/л О (УХ) и
50-60 г/л избыточной серной кислоты, 40 через который непрерывно подают газообразный сернистый адгидрид и поддерживают концентрацию газа 5-10 г/л. В исходный раствор анолита с концентрацией 80-100 г/л Н> 5 О непрерывно подают газообразный сернистый ангидрид
45 через пористую стенку графитного анода, причем скорость его подачи определяется плотностью анодного тока. Плотность анодного. и катодного тока поддерживают в пределах 500 - 2000 Аlм, предпочтительно до 1000 Аlм . Напряжение на электролизере находится в пределах 1,4—
2,3 В при 40-50 С.
Основные показатели способа представлены в табл. 2.
FI р и м е р 2. Осуществляя операции, как указано в примере 1, подают исходный раствор католита с концентра83 4 цией Fe > (З О,) 40 г/л, серной кислоты 10-20 г/л и сернистого ангидрида на электрохимическое восстановление
Fe - Fe . В качестве анолита подают раствор, содержащий 70-80 г/л серной кислоты и газообразный ВО . Электролиз ведут при плотности тока 200—
1000 А/м и напряжении 1,2 — 2,1 В.
Затраты электроэнергии на восстановление 1 KI Г при плотности тока
500 Аlм составляют 1,27 кВт ч; при плотности тока 1000 Аlм — 1,53 кВт ч.
Р
Пример 3. Осуществляя операции, как указано в примере 1, подают исходный раствор католита с концентрацией
Сг+ 30 г/л, в виде Cv > (60+)>. Концентрация свободной серной кислоты 8010О г/л, а сернистого ангидрида 5-10г/л.
Электролиз ведут при плотности тока
300 — 1000 Аlм и напряжении 1,28—
У
1,65 В. Выход продукта по току 70—
80, а затраты 1 кг С1 до 1,51 кВт. ч.
Пример 4. Осуществляя операции, как указано в примере 1, подают исходный раствор католита с концентрацией Ti 45-50 г/л в виде сульфата титанила. Содержание свободной серной кислоты 100-125 г/л, а сернистого ангидрида 5-7,5 г/л. Электролиз ведут при плотности тока 2000 — 1000 Аlм и напряжении 0,85 — 1,24 В. Выход
Ti по току 68-75, а затраты электроэнергии на 1 кг T1 + 0,5—
0,7 кВт ч.
Пример 5. Осуществляя операции, как показано в примере 1, подают исходный раствор католита с концентрацией плутония 40-45 г/л в виде сульфата плутонила. Концентрация свободной серной кислоты в католите 85-100 г/л, а содержание сернистого ангидрида 56 г/л. Электролиз ведут при плотности тока 250 - 1000 Alì и напряжении
1,8-2,2 В.
Выход по току Рц + составляет
62, 1 -7 5, 5 ., Затраты электооэнеогии на получение 1 кг Pu+ 1,15 — 1,2 кВт ч.
Предложенный электрохимический способ восстановления ионов металлов в водных растворах электролитов позволяет в 3-4 раза снизить напряжение на электролизере и, следовательно, затраты электроэнергии по сравнению с известным способом. Кроме того, способ позволяет получать восстановленный металл высокой чистоты и одновременно серную кислоту, которая может быть использована в производстве.
903383
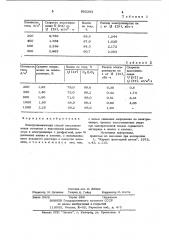
Т аблица 1
Расход электроэнергии на
1 кг 0 (ТУ), кВт ч
Плотность тока, А/м . й
Скорость восстановления 0 (YI) до
Ц (ТУ), кгlм м
200
88,5
400
87,0
600
84,5
800
80,7
Таблица 2
Плотность Среднее напрятока, жение на электАl м ролизере, В
Расход элекч роэнергии на
1 кг 0 (1У), кВт ° ÷
0,8
99,6
99,2
99,0
98,4
98,0.
0,39
0,42
1,74
0,51
3,31
4,08
0,60. 1500
1,03
2,25
Фор мула изобретения с целью снижения напряжения на электро-. лизере, процесс восстановления ведут при одновременной подаче сернистого адгидрида в анолит и католит.
Источники информации, принятые во внимание при экспертизе
1. "Журнал прикладной химии", 1972, т. 45, с. 110.
Электрохимический способ восстановления металлов с переменной валентностью в электролизере с диафрагмой, раз- 35 деляющей анолит и католит, с использованием исходного раствора в качестве католита, отличающийся тем, что, Состави.ель О. Зобнин
Редактор М. Циткина Техред И. Гайду Корректор М. Коста
Заказ 34/6 Тираж 686 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий
113035, Москва, Ж-35, Раушская наб., д. 4/5
Филиал ППП "Патент", г. Ужгород ул. Проектная, 4
200 1,35
500 1,40
800 1,60
1000 1,80
0,786
1,553
2,236
2,865
78,0
75,0
71,0
68,0
59,2
1,244
1,620
2,172
2,593
Скорость восстановления
U (УХ) до
Ц (УХ), кг/м . ч