Способ получения производных 5(10 @ 9)абеоэрголина
Иллюстрации
Показать всеРеферат
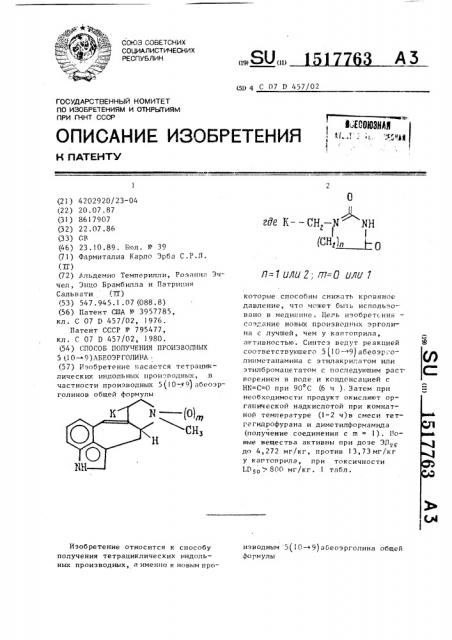
ИЗОБРЕТЕНИЕ КАСАЕТСЯ ТЕТРАЦИКЛИЧЕСКИХ ИНДОЛЬНЫХ ПРОИЗВОДНЫХ, В ЧАСТНОСТИ ПРОИЗВОДНЫХ 5(10→ 9) АБЕОЭРГОЛИНОВ ОБЩЕЙ ФОРМУЛЫ @ , КОТОРЫЕ СПОСОБНЫ СНИЖАТЬ КРОВЯНОЕ ДАВЛЕНИЕ, ЧТО МОЖЕТ БЫТЬ ИСПОЛЬЗОВАНО В МЕДИЦИНЕ. ЦЕЛЬ ИЗОБРЕТЕНИЯ - СОЗДАНИЕ НОВЫХ ПРОИЗВОДНЫХ ЭРГОЛИНА С ЛУЧШЕЙ, ЧЕМ У КАПТОПРИЛА, АКТИВНОСТЬЮ. СИНТЕЗ ВЕДУТ РЕАКЦИЕЙ СООТВЕТСТВУЮЩЕГО 5(10 → 9) АБЕОЭРГОЛИНМЕТАНАМИНА С ЭТИЛАКРИЛАТОМ ИЛИ ЭТИЛБРОМАЦЕТАТОМ С ПОСЛЕДУЮЩИМ РАСТВОРЕНИЕМ В ВОДЕ И КОНДЕНСАЦИЕЙ С HN=C=O ПРИ 90°С (6 Ч). ЗАТЕМ ПРИ НЕОБХОДИМОСТИ ПРОДУКТ ОКИСЛЯЮТ ОРГАНИЧЕСКОЙ НАДКИСЛОТОЙ ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ (1-2 Ч) В СМЕСИ ТЕТРАГИДРОФУРАНА И ДИМЕТИЛФОРМАМИДА (ПОЛУЧЕНИЕ СОЕДИНЕНИЯ С M=1). НОВЫЕ ВЕЩЕСТВА АКТИВНЫ ПРИ ДОЗЕ ЭД<SB POS="POST">25</SB> ДО 4,272 МГ/КГ, ПРОТИВ 13,73 МГ/КГ У КАПТОПРИЛА, ПРИ ТОКСИЧНОСТИ LD<SB POS="POST">50</SB>*98800 МГ/КГ. 1 ТАБЛ.
ССНОЗ СОВЕТСКИХ
СОЦИАЛИСТИЧЕСКИХ
РЕСПУБЛИК (19> SU(II) (5П 4 С 07 Р 457/02
ВьЕСОЮ3ЯЦ ц.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
К IlATEHTY
О ие к- — сн,-н нн г (Щ)л
/7=1 UJILl 7; П7=0 ЦЯЦ f
fol сн, ГОСУДАРСТВЕННЫЙ КОМИТЕТ
ПО ИЗОБРЕТЕНИЯМ И ОТКРЫТИЯМ
ПРИ ГКНТ СССР (21) 4202920/23-04 (22) 20.07.87 (31) 8617907 (32) 22.07.86 (33) СВ (46) 23.10.89. Бюл. 1"- 39 (71) Фармиталиа Карло Эрба С.P.Ë. (и) (72) Альдемио Темперилли, Розанна Эччел, Энцо Брамбилла и Патриция
Сальвати (37) (53) 547.945.1.07 (088.8) (56) Патент США Р 3957785, кл. С 07 D 457/02, 1976.
Патент СССР Р 795477, кл. C 07 D 457/02, 1980. (54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ
5 (10- 9)АБЕОЭРГОЛИНА (57) Изобретение касается тетрациклических индольных производных, в частности производных 5 I 10 9) абеоэрголинов общей формулы
Изобретение относится к способу получения тетрациклических индольных производных, а именно к новым прокоторые способны снижать кровяное давление, что может быть использовано в медипине . Цегь изобретения создание новых производных эрголина с лучшей, чем у каптоприла, активностью. Синтез ведут реакцией соответствуюшего 5 (10 — «9) абеоэр олинметанамина с этилакригатом или этилбромацетатом с последующим раст. ворением в воде и конденсацией с
HN=C=0 при 90 С (6 ч ). Затем при необходимости продукт окисляют органической надкислотой при комнатной температуре (1-2 ч)в смеси тетрггидрофурана и диметилформамида (получение соединения с m = 1). Новые вещества активны при дозе ЭД до 4,272 мг/кг, против 13,73 мг/кг у каптоприла, при токсичности
LD о 800 мг/кг. 1 табл. изводным 5(10 — 9) абеоэрголина общей формулы
1517763
О
15 гдеп= l или2, т=Оили 1 обладающих свойствами снижать давление крови.
Цель изобретения — получение новых производных эрголина, обладающих фармакологически»и преимуществами перед известным препаратом — катоприлом.
Пример 1, 1 — ((5- (!О- 9)Aáeo- 25
-9,10- дидегидроидро-6-метилэрголин-ЯР-ил) метил) -2, 4- (1Е1, ЗН) -пиримидиндион-11-.ок сид. о-6h.. 5- (10 9)Абео-9, 10-дидегидрометилэpr олин-3 3-»е танамин. 30
10,3 г трифенилфосфина, 5,4 г фта6 9 г этилазодикарбоксилата лимида и
- нии и 25 С добавляют при перемешивании и к раствору 5 r 5- (10 9)a6eo-9,10-дидегидро-6-метилэрголин-UJ3-метанола 35 в 1Об мл тетрагидрофурана. Спустя 1 ч растворитель выпаривают в вакууме, остаток растворяют в 10%-ной винной кислоте. Этот раствор повторно экстрагируют этилацетатом, затем подщела- 40 чивают его гидроксидом аммон ония и экстрагируют дихлорметаном. Пос осле выпаривания дихлорметана получается сырой остаток 6,3 r 2- ((5- (10 — 9)aáeo-9,10-дидегидро-б-метилэрголин- 6-86-ил)метил)-1Н-изоиндол-1,3-(2Н)-диона, т. пл. 174-176 С.
Это вещество растворяют в 80 мл этанола и 80 мл тетрагидрофурана, добавляют 3,15 мл гидразингидрата, и раствор кипятят 5 ч с обратным холодильником. После выпаривания растворителя остаток растворяют в воде и дихлорметане. После упаривания органического слоя остается 4 г указанного соединения (аморфное).
Б. 1 в ((5-10 — 9)Абео-9,10-дидегидро-б-метилэрголин-S -ил)метил)-2,4— (1Н,ЗН)-пиримидиндион.
Смесь 3,25 г 5- (10- 9) абео-9,10-диде гидро-6-метилэр голин-Я -метанамина и 1,45 мл этилакрилата в 50 мп этанола кипятят 6 ч с обратным холодильником. Растворитель выпаривают, остаток очищают хрвматографически на колонке с силикагелем,,используя в качестве элюента этилацетат с возрастающими количествами этанола (от 0 до 10%), получают 3,3 r сложного этилового эфира -((5-(10 - 9)абео-9,10-дидегидро-6-метилэрголин-SP-ил)-метил)-$-аланина, плавящегося при
128-130 С.
К раствору1,53 г пианата калия в
15 мл воды добавляют раствор 3,3 r сложного этилового эфира N- ((5- (1 0- 9) абео-9,10-дидегидро-б-метилэрголин-8t3-ил)метил)- 3-аланина в 60 мл воды и 18,6 мл 1 и. хлористо-водородной кислоты. Смесь нагревают в течео ние 9 ч при 90 С, затем отделившееся твердое вещество отфильтровывают и очищают хроматографически на колонке с силикагелем, используя дихлорметан с возрастающими количествами метанола (от 0 до 8%) в качестве элюента, t получают 2,1 г указанного вещества, плавящегося при 234-236 С.
B. 1 в ((5- (10 †)Лбео-9,10-дидегидро-6)метилэрголин-8й-ил)метил)-2,4- (!Н,ЗН)-пиримидиндион-N -оксид.
Раствор 1,37 г 1 — ((5- (10 — э9)абео-9, 10-дидегидро-6 -метилэрголин- "
-SJ3-ил)метил)-2,4- (1H,3Н) — пиримидиндиона в 80 мл тетрагидрофурана и 10»л! диметилформамида обрабатывают 0,84 r метахлорбензойной кислоты в 10 мл тетрагццрофурана. Этот раствор оставляют при комнатной температуре в течение I ч и затем растворитель выпаривают. При добавлении 6 мл воды, содержащей 0,42 r бикарбоната натрия, получают 1,! г укаэанного вещества, которое выделяют путем фильтрации. Т. пл. 198-200 С.
Пример 2. 1- ((5- (10 9)Абео-9,10-дидегидро-б-метилэрголин-SP-ип)метил)-2,4-имидазолидандион-N<—
-оксид.
A.. 1 в ((5-(10 †. 9} бео-9,10-дидегидро-б-метилэрголин-8Р-ил)метил)-2,4-имидазолидиндион.
Раствор 1,93 мл этилового эфира бромуксусной кислоты в 10 мл диметилформамида добавляют к охлажденной суспензии 4,3 г 5- (10 9)à6åî-9,10— дидегидро-6-метилэрголин-8!3-метил63
При оценке противогипертонической активности. Внутриартериальные измер..ния среднего давления крсви (CjJK) были осуществлены с помощью катетеров, вставленных в правую сонную артерию крысы под алотановой анестезией. Через 24 ч после хирургии животных помещали в клетки Боллмэна, причем артериальные полые трубочки соединялись через преобразователь давления с самописцем давления крови Бекмана для непрерывного слежения за средним давлением крови.
Среднее давление крови записывалось до перорального введения медикамента (базовые значения)и через
15, 30, 60, 120, 240 мин до 24 ч после лечения. Группам по 7-8 крыс задавалась перорально единичная доза испытуемого соединения или носителя, метоцела 0,5 вес/объем (0,2 мл/
/1 00 г веса) . Значения ЭД g дозы, понижающей среднее давление крови на
25 мм рт.ст.) рассчитывали для каждого соединения из линии регрессии доза-отклик.
5 15177 амина и 2,4 карбопата калия в 50 мл диметилформамида. Ilo завершении реакций раствор упаривают в- вакууме, выливают в ледяную воду и экстрагируют дихлорметаном.
Остаток органического слоя очищают хрматографически на колонке с силикагалем, используя в качестве элюента этилацетат с возрастающими ко- 10 личествами этанола (от 0 до 10%). по-, лучают 3,5 r сложного этилового эфира И- (3- (10 — 9)абео-, 10-дидегидро-6-метилэрголин-8Р-ил)метил ) глицина, который плавится при 141-142 С.
Этот сложный этиловый эфир N- (((5, — (10- 9)абео — 9,10-дидегидро-б-метилэрголин-8Р-ил)метил) глиципа (3,5 г) обрабатывают 1,67 г цианата калия, как описано в примере !Б. указанное 33 вещество получают с выходом 75%, т.пл. 170-172 С.
Б. 1 — ((5- (10 9) абео — 9,10-дидегидро-6-метилэрголин-8Р-ил)-метил)j-2,4-имидазолидиндион-Я -оксид. 25
Действуя как в примере IB, но используя 1 — ((5- (10 9) абео-9, 10-дидегидро-6-метилэрголин-8 -ил) метил)—
-2,4-имидазолидиндион, получают указанное в заголовке вещество с выхо- 30 дом 75%. Т.пл. 218-220 С.
Пример 3. 1 — ((Транс-5— (1 Π— э9 )абео- I, 6-диметилэрголин-8P-ил)-метил) — 2,4-(1Н,3H) — пиРимидин, дион. 35, ;ействуя как в примере 1, но применяя транс-5- ;10 — 9)абео-1,6-диметилэрголин-8Р-метамин вместо 5†(10 — 9)аáeo-9,lО-дидегидро-б-метил/ эрголин-8Р-метанамино, получают с выходом 55% указанное ве.це. тво, т.пл . 185-1 87 С.
Пример 4. 1 †((Транс-5-(10 9) абео-l,б-диметилэрголин-SP — ил)метил)—
-2,4- (IН,ЗН)-пиримидиндион Мб оксид 45
Действуя как в примере 1, но используя 1 в ((транс-5- (1(М9)абео-I á,-диме— тилэрголин-SP-ил)метил) — 2,4- (1Н,ЗН)—
-пиримидиндион,получают указанное вещества с выходом 83%. Т.пл.204-206 С.
Пример 5. 1 — ((Транс-5- (10 9) абео-6 -метилэрголин .-8 -ил) метил)-2,4-имида з олидиндион . та нала, получают ук ззанное вещество с выходом 55%. Т.пл. 168-! 70 С.
Пример 6. 1 — ((Транс-5— (I О=э.9) абео-6-метилэ рголин-8/3-ил) метил — 2,4-имидаэолиндиион-.1 -оксид.
Действуя как в гримере 2, но используя 1- ((транс-5- (10- 9)абео-6метилэрголин-8 -ил)метил-2,4-имидазолидиндион, получают с выходом 80% указанное соединение,т.пл.l 87189 С.
Предлагаемое вещество и их фармацевтически приемлемые соли являются полезными противогипертоническими средствами с медленным началом действия и длительным действием активно сти.
В качестве стандартного медикамента сравнения был также испытан катоприл. В таблице приведены величины
ЭД, которые были получены для исследованных соединений.
Действуя как в примере 2, но используя транс-5- (10 — 9) абео-6-метилэрголин-88-метанамин, полученный как в примере l, исходя из транс-5— (!О- 9)абео-6-метилэрголин-8 -меПри оценке токсичности трем мышам55 самцам в каждой группе давали перо-рально медикаменты с различными уровнями дозировки для ориентировочного определения токсичности. 3а мышами наблюдали в течение семи суток после
1517763 где п = 1 или 2, m - =0 или 1, о тлич ающийс я введения лекарства. Полученные данные о летальной дозе для 50Х мьппей (1Щ ) суммированы в таблице. тем, что
5 соединение формулы
Таким образом, полученные соедине- снгNH(cHz1„-gpppp ния более активны в сравнении с катоприлом.
Формула изобретения
Способ получения производных
5 (10 — 9)абеоэрголина формулы
О (ттт) О=C NH
ЛД 50 as пределы) мг/кг (пер- P = 0,05,мг/кг орально) перорально
Соединение
1, 229 (О, 661-1, 845)
0,402 (0,297-0,511) Более 800
Более 800
Более 800
Более 800
2 051 (1,180-2,971)
4,272 (3,256-5,514) Более 800 13,73 (7,86-23,04 ) Составитель И. Федосеева
Редактор Н. Бобкова Техред А.Кравчук Корректор В.Кабаций
Заказ 6404/58
Тираж 352
Подписное
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР
113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-издательский комбинат "Патент", г.ужгород, ул. Гагарина,101
FCE 24379
Пример 1Б
FCE 24778
Пример 1В
FCE 24378
Пример 2А
FCE 25068
Пример 2Б
Катоприл (стандартный медикамент) 15 где и имеет указанные значения, полученное путем взаимодействия соответствующего 5 (10- 9) абеоэрголинметанамина с этилакрилатом или этилбромацетатом, растворяют в воде
20 и подвергают конденсации с соединением формулы при 90 Г в течение 6 ч с получением о целевого соединения формулы O), m О, с последующим, при необходимости, окислением органической надкислотой при комнатной температуре в течение 1-2 ч в смеси тетрагид30 рофурана и диметилформамида с получением целевого соединения формулы (I) где m 1.