Штамм молочно-кислых бактерий lactobacillus paracasei cncm i - 2116 (ncc 2461), обладающий способностью предотвращать колонизацию кишечника патогенными бактериями, вызывающими диарею, супернатант его культуры и принимаемое внутрь средство для профилактики и/или лечения нарушений, ассоциируемых с диареей
Иллюстрации
Показать всеИзобретение относится к биотехнологии и касается штамма Lactobacillus paracasei CNCM I-2116, используемого для предупреждения диареи, вызываемой патогенными бактериями. Супернатант культуры этого штамма также обладает способностью предотвращать колонизацию кишечника патогенными бактериями, вызывающими диарею, и предназначен для получения средства для профилактики и/или лечения нарушений, ассоциированных с диареей. Принимаемое внутрь средство представляет собой терапевтически эффективное количество штамма L.paracasei CNCM I-2116 или супернатанта его культуры и приемлемый пищевой продукт. Изобретение обеспечивает повышенную жизнеспособность штамма при его использовании и эффективность в предотвращении адгезии к кишечным клеткам и инвазии в кишечные клетки патогенных микроорганизмов, вызывающих диарею. 3 н. и 2 з.п. ф-лы, 1 табл., 8 ил.
Реферат
Данное изобретение относится к области микробиологии и, в частности, к новым микроорганизмам рода Lactobacillus, используемым для предупреждения диареи, вызываемой патогенными бактериями. В частности, данное изобретение относится к использованию указанных микроорганизмов для приготовления принимаемого внутрь средства и к композиции, содержащей его.
Уровень техники
Организмы, продуцирующие в качестве основного метаболического компонента молочную кислоту, известны в течение продолжительного времени. Эти бактерии могут быть обнаружены в молоке или в обрабытывающих молоко устройствах, соответственно, живых или разлагающихся растениях, а также в кишечнике человека и животных. Эти микроорганизмы, объединяемые под термином “молочно-кислые бактерии”, представляют собой негомогенную группу и включают, например, роды Lactococcus, Lactobacillus, Streptococcus, Bifidobacterium, Pediococcus и т.д.
Молочно-кислые бактерии используют в качестве ферментирующих агентов для консервирования пищевых продуктов в условиях низкого рН и действия продуктов ферментации, образующихся во время их ферментативной активности, для ингибирования роста портящих пищевые продукты бактерий. Для этой цели молочно-кислые бактерии используют для приготовления различных пищевых продуктов из молока, таких как сыр, йогурт и другие ферментируемые молочные продукты.
Совсем недавно среди молочно-кислых бактерий были обнаружены штаммы, обладающие полезными свойствами для человека и животных при приеме внутрь. В частности, было обнаружено, что определенные штаммы родов Lactobacillus или Bifidobacterium способны заселять слизистую оболочку кишечника и способствовать поддержанию здоровья человека и животного.
В этом отношении, в ЕР 0768375 описаны специфические штаммы рода Bifidobacterium, которые способны приживаться в качестве кишечной флоры и могут прикрепляться к кишечным клеткам. Сообщается, что эти бифидобактерии способствуют иммуномодуляции, конкурентно устраняя адгезию патогенных бактерий к клеткам кишечника, способствуя поддержанию здоровья человека.
В последние несколько лет исследование сосредоточилось также на потенциальном применении молочно-кислых бактерий в качестве симбиотических агентов. Симбиотическими агентами считаются жизнеспособные микробные препараты, которые стимулируют здоровье человека путем сохранения природной микрофлоры в кишечнике. Микробный препарат может считаться симбиотическим агентом в том случае, если известны его эффективные микробы и их способ действия. Считается, что симбиотические агенты присоединяются к слизистой оболочке кишечника, заселяют кишечный тракт и, по-видимому, предотвращают прикрепление на нем вредных микроорганизмов. Критическая предпосылка для их действия заключается в том, что они должны достигать слизистой оболочки кишечника в правильной и жизнеспособной форме и не разрушаться в верхней части желудочно-кишечного тракта, в частности, под действием низкого рН, преобладающего в желудке.
В этом отношении, в WO 97/00078 в качестве симбиотического агента описан специфический штамм Lactobacillus GG (АТСС 53103). Этот микроорганизм применяют, в частности, в способе предупреждения или лечения индуцируемых пищевыми продуктами аллергических реакций, причем его вводят реципиенту вместе с пищевым продуктом, который был подвергнут гидролизной обработке пепсином и/или трипсином. Выбранный штамм Lactobacillus описан как проявляющий адгезивные и колонизирующие свойства и обнаруживающий протеазную ферментативную систему, так что белковый материал, содержащийся в пищевом продукте, который должен вводиться, дополнительно гидролизуется протеазами, секретируемыми этим штаммом Lactobacillus. Способ, обсуждаемый в этом документе, будет в конечном счете приводить к поглощению кишечником белкового материала, который не обнаруживает уже существенного количества аллергенного материала.
Кроме того, в ЕР 0577903 делается ссылка на применение молочно-кислых бактерий, способных замещать Heliobacter pylori, признанным агентом, вызывающим развитие язвы, в приготовлении носителя, предназначенного для терапевтического или профилактического лечения язвы, связанной с действием Heliobacter pylori.
Сущность изобретения
Ценные свойства молочно-кислых бактерий определяют потребность в поиске новых штаммов молочно-кислых бактерий, полезных для здоровья человека и/или животных.
Таким образом, задача настоящего изобретения состоит в поиске новых бактериальных штаммов, обладающих свойствами, полезными для человека и/или животных.
Вышеуказанная задача была решена при обнаружении новых микроорганизмов, а именно молочно-кислых бактерий, принадлежащих к роду Lactobacillus, обладающих способностью предотвращать колонизацию кишечника патогенными бактериями, вызывающими диарею.
Согласно предпочтительному варианту, обнаруженный штамм Lactobacillus способен прикрепляться к слизистой оболочке кишечника млекопитающего и расти в присутствии до 0,4% солей желчных кислот.
В соответствии с другим предпочтительным вариантом молочно-кислые бактерии выбирают из группы, состоящей из Lactobacillus rhamnosus или Lactobacillus paracasei, предпочтительно Lactobacillus paracasei, более предпочтительно Lactobacillus parasei CNCM I-2116.
Было показано, что микроорганизмы данного изобретения обладают следующими свойствами: они являются грамположительными, каталаза-отрицательными, отрицательными по NН3-форме аргинина и отрицательными по продуцирования СО2, они продуцируют L(+)-молочную кислоту, способны расти в присутствии желчных солей в концентрации до около 0,4% и могут по существу предотвращать колонизацию кишечных клеток бактериями, вызывающими диарею, такими как патогенные Е. coli, например, энтеропатогенные Е. coli (EPEC), или сальмонеллы, например, Salmonella typhimurium.
Новые микроорганизмы могут быть использованы для приготовления различных средств, в виде принимаемых внутрь материалов-носителей, таких как молоко, йогурт, творог, ферментированные разновидности молока, ферментированные продукты на основе молока, ферментированные продукты на основе зерновых продуктов, порошки на основе молока, детские смеси, и могут быть включены в такой носитель в количестве от около 105 КОЕ/г до около 1011 КОЕ/г. В контексте данного изобретения аббревиатура КОЕ означает “колониеобразующую едниницу”, которая определяется как число колоний бактериальных клеток, выросших на чашках с агаровой средой.
Данное изобретение обеспечивает также принимаемые внутрь средства в виде пищевой или фармацевтической композиции, содержащей, по меньшей мере, один из штаммов Lactobacillus, имеющий вышеуказанные признаки и/или содержащий супернатант культуры, в которой этот микроорганизм выращивался, или его фракцию, соответственно.
Для приготовления пищевой композиции данного изобретения по меньшей мере один из штаммов Lactobacillus данного изобретения включают в подходящий носитель в количестве от около 105 КОЕ/г до около 1011 КОЕ/г, предпочтительно от около 106 КОЕ/г до около 1010 КОЕ/г, более предпочтительно от около 107 КОЕ/г до около 109 КОЕ/г.
В случае фармацевтического препарата этот продукт может быть приготовлен в формах таблеток, жидких бактериальных суспензий, высушенных пероральных добавок, увлажненных пероральных добавок, сухого продукта для введения через трубку или увлажненного продукта для введения через трубку с количеством штаммов Lactobacillus, включенным в них, в диапазоне вплоть до около 1012 КОЕ/г, предпочтительно от около 107 КОЕ/г до около 1011 КОЕ/г, более предпочтительно от около 107 КОЕ/г до около 1010 КОЕ/г.
Активность средств, содержащих в качестве активных компонентов новые микроорганизмы, в кишечнике индивидуума является, конечно, зависимой от дозы. То есть, чем больше микроорганизмов включается посредством введения внутрь вышеуказанного средства пищевого материала или фармацевтической композици, тем выше защитная или лечащая активность данного средства. Поскольку новые микроорганизмы являются безвредными для людей и животных и были выделены из фекалий ребенка, в разработанные средства можно включать большие количества микробных клеток таким образом, чтобы значительная часть кишечника индивидуума была заселена (колонизирована) новыми микроорганизмами.
В соответствии с другим предпочтительным вариантом, супернатант культуры штамма Lactobacillus данного изобретения может быть использован для приготовления одного из указанных выше принимаемых внутрь средств. Супернатант может быть использован как таковой или может быть высушен в условиях, которые не разрушают метаболические соединения, секретируемые этими микроорганизмами в жидкую среду, например, таких как лиофилизация, и может быть далее введен в средство. Для минимизации числа неизвестных соединений в супернатанте штаммы Lactobacillus предпочтительно выращивают в определенных средах, состав которых является известным и не оказывает отрицательного действия на выращиваемого хозяина. Кроме того, специалист с квалификацией в данной области на основе его общих знаний может необязательно освобождать супернатант от нежелательных продуктов, например, при помощи хроматографии.
Перечень фигур
Фиг.1 показывает результаты анализа в культуре клеток на ингибирование адгезии патогенных бактерий Е. coli к эпителиальным клеткам культивируемыми клетками ST11.
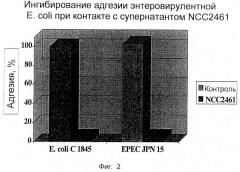
Фиг.2 показывает результаты анализа в культуре клеток на ингибирование адгезии патогенных бактерий Е. coli к эпителтальным клеткам супернатантом культуры ST11.
Фиг.3 показывает результаты анализа в культуре клеток на ингибирование инвазии Salmonella typhimurium в эпителиальные клетки культивируемыми клетками ST11.
Фиг.4 показывает результаты анализа в культуре клеток на ингибирование инвазии Salmonella typhimurium в эпителиальные клетки супернатантом культуры ST11.
Фиг.5 показывает подкисление различных сред при выращивании штамма L. casei CNCM 1-2116 (названного ST11).
Фиг.6 показывает кривую выживания L. casei ST11 при 10°С в течение 30 дней.
Фиг.7 показывает распределение мРНК IL-12 и IL-10 в мышиных прикрепленных клетках, выделенных из костного мозга, после инкубации этих клеток с серийными разведениями ST11.
Фиг.8 показывает результат дифференцировки Th2 как приводящий к уменьшенному продуцированию IL-4.
Сведения, подтверждающие возможность осуществления изобретения
Во время интенсивных исследований, приведших к данному изобретению, авторы изобретения исследовали фекалии младенцев и выделили из них множество различных бактериальных штаммов. Эти штаммы затем испытывали на их способность предотвращать колонизацию эпителиальных клеток бактериями, о которых известно, что они вызывают диарею.
Несколько бактериальных родов, включая Lactobacillus, Lactococcus и Streptococcus, скринировали на способность ингибировать диарею. Тесты на способность ингибировать диарею проводили в основном с патогенными Е. coli и Salmonella typhimurium в качестве репрезентативных бактерий для патогенных микроорганизмов, вызывающих диарею в пораженном индивидууме.
Различные молочно-кислые бактерии выращивали в подходящей среде, такой как MRS, Hugo-Jago или М17, при температуре от около 30 до 40°С, соответствующей их оптимальной температуре роста. После достижения стационарного роста бактерии собирали центрифугированием и ресуспендировали в физиологическом растворе NaCl. Полученные бактериальные клетки хранили в замороженном виде (-20°С).
Для оценки антибактериальных свойств использовали следующие методы.
Согласно одному методу, культивируемые штаммы Lactobacillus данного изобретения испытывали на их способность предотвращать адгезию патогенных бактерий, вызывающих диарею, к кишечным клеткам или инвазию их в кишечные клетки, соответственно. Для этой цели кишечные клетки инкубировали с патогенными бактериями и культивируемыми штаммами Lactobacillus данного изобретения и оценивали степень адгезии или инвазии соответственно.
Согласно второму методу, супернатант клеточной культуры штаммов Lactobacillus данного изобретения добавляли вместе с патогенными микроорганизмами к кишечным клеткам и оценивали степень адгезии или инвазии соответственно.
Таким образом, авторы смогли показать, что культивируемые штаммы Lactobacillus и супернатант оказались чрезвычайно эффективными для предотвращения как адгезии к кишечным клеткам, так и инвазии в кишечные клетки, что указывает на то, что метаболические соединения, секретируемые новыми микроорганизмами, по-видимому, отвечают за активность против диареи.
Кроме описанного выше открытия, авторам удалось также показать, что штаммы данного изобретения неожиданно проявляют также противоаллергические свойства путем определенного влияния на синтез различных иммунологических медиаторов (посредников).
Общепризнанно, что гуморальные иммунные реакции и аллергические реакции опосредуются CD4+ Т-клетками, несущими фенотип типа 2 (Th2). Тh2-клетки характеризуются продуцированием высоких уровней интерлейкина 4 (IL-4), цитокина, необходимого для секреции IgE, который является основным классом антител, участвующим в аллергических реакциях.
Дифференцировка Тh2-клеток нарушается IFN-γ, конкретным цитокином, который продуцируется взаимоисключающей Th1-субпопуляцией CD4+ Т-клеток. Указанные Th1-клетки, в свою очередь, сильно индуцируются интерлейкином 12 (IL-12). Было показано, что, в противоположность этому, IL-10, другой цитокин, оказывает сильное супрессирующее действие на пролиферацию Th1-клеток, и, следовательно, предполагается, что он играет роль в иммуносупрессивных механизмах.
В целом, как IL-12, так и IL-10 оказывают сильные модулирующие действия на развитие CD4+ Т-клеток посредством влияния на развитие Th1-субпопуляции. IL-12 является ключевым регуляторным цитокином для индукции дифференцировки Th1 и, следовательно, ингибирует генерирование Тh2-ответов. Основным путем ингибирования Тh2-клеток считается, следовательно, стимуляция синтеза IL-12 вспомогательными клетками.
Хорошо известно, что некоторые компоненты грамотрицательных бактерий, такие как LPS (липополисахарид), индуцируют высокие уровни IL-12 в прикрепленных клетках, таких как макрофаги и дендритные клетки. В соответствии с этим, было обнаружено, что грамотрицательные бактерии могут сильно смещать CD4+ Т-клеточную дифференцировку в направлении Th1-фенотипа.
Микроорганизм ST11 как пример штаммов Lactobacillus данного изобретения испытывали на потенциальную роль в индукции цитокинов, участвующих в регуляции дифференцировки CD4+ Т-клеток. В частности, исследовали действие ST11 на фенотип CD4+ Т-клеток, подвергающихся Тh2-дифференцировке.
В этой связи способность ST11 индуцировать синтез мРНК, кодирующих эти два регуляторных цитокина в мышиных прикрепленных клетках, полученных из костного мозга, сравнивали с 4 другими штаммами Lactobacillus и контрольными грамотрицательными бактериями (Е. coli K12). Количество мРНК определяли полуколичественной ОТ-ПЦР после 6 часов инкубации клеток с серийными разведениями бактерий от 107 до 109 КОЕ/мл.
Хотя все штаммы Lactobacillus в некоторой степени индуцировали транскрипцию мРНК IL-12, было показано, что ST11 является наиболее сильным индуктором, поскольку сильный сигнал ПЦР детектировался даже при самом большом разведении бактерий. Фактически, ST11 индуцирует транскрипцию мРНК IL-12 в той степени, что и Е. coli. Индукция мРНК IL-10 была обычно более низкой, чем индукция мРНК IL-12, так как сигнал удавалось детектировать только при более низких разведениях. Тем не менее, ST11 оказался наиболее сильным индуктором мРНК IL-10 по сравнению с другими штаммами Lactobacillus и Е. Coli (контроль).
Таким образом, было показано, что ST11 является эффективным индуктором иммунорегуляторных цитокинов, участвующих в дифференцировке CD4+ Т-клеток. Его значительная IL-12 индуцирующая активность делает ST11 вероятным кандидатом для ингибирования Тh2-реакций, и его IL-10 индуцирующая активность может быть использована для предотвращения воспалительных процессов.
Кроме описанного выше открытия, авторы также определяли, оказывает ли ST11 ингибирующее действие на CD4+ Т-клети, подвергающиеся Тh2-дифференцировке, и положительное действие на функции Тh1. Для решения этой задачи использовали хорошо известную культуральную систему дифференцирующихся клеток, в которой предшественник CD4+ Т-клеток поликлонально активировали и модулировали для подвергания либо Th1-, либо Th2-дифференцировке, в зависимости от типа индуктора, присутствующего в этой культуральной среде. Тh1/Тh2-дифференцировку индуцировали в 7-дневной первичной культуре, после чего клетки повторно стимулировали в течение 2 дней во вторичной культуре, содержащей только среду, а приобретение специфического фенотипа (Th1 или Th2) оценивали по количеству типичных цитокинов, продуцируемых в супернатанте (INF-γ или IL-4).
Хорошо известно, что содержащие предшественник CD4+ Т-клетки мышей BALB/ предпочтительно дифференцируются с преобладанием фенотипа Th2 (высокое содержание IL-4, низкое содержание IFN-γ во вторичных культуральных супернатантах) после активации в нейтральных условиях (только среда в первичной культуре). Этот фенотип мог быть полностью обращен в картину Th1 (высокое содержание IFN-γ, низкое содержание IL-4) при добавлении к первичной культуре блокирующего моноклонального антитела против IL-4.
Для исследования потенциальной роли ST11 в ингибировании Th2 очищенный предшественник CD4+ Т-клеток мышей BALB/c активировали в присутствии прикрепленных клеток костного мозга в качестве вспомогательных клеток в первичной культуре. Эти клетки культивировали в среде без добавок, в присутствии 1 мг/мл LPS, в присутствии 108 КОЕ/мл ST11 или в присутствии 108 КОЕ/мл другого Lactobacillus. Затем клетки промывали, CD4+ Т-клетки один раз очищали и повторно стимулировали путем вторичного культивирования в среде без добавок.
Количество цитокинов, продуцируемых дифференцированными CD4+ Т-клетками, определяли спустя 2 дня. Как и ожидалось, клетки, которые культивировали в среде без добавок, дифференцировались в доминантный фенотип Th2. Добавление ST11 к первичным культурам модулировало Тh2-фенотин, что было определено по 8-кратному уменьшению IL-4. Такое же ингибирование наблюдалось при культивировании клеток в присутствии LPS. В противоположность этому, культивирование клеток в присутствии другого штамма Lactobacillus оказывало влияния на продукцию IL-4. Интересно, что уровни IFN-γ не увеличивались при добавлении ST11 в первичные культуры.
В целом, ST11 специфически нарушал продуцирование IL-4 CD4+ Т-клетками, подвергающимися Тh2-дифференцировке, но не увеличивал значимо секрецию IFN-γ. Факт, что ST11 не увеличивал образование ifn-γ, может быть вызван его способностью индуцировать IL-10, приводящей к тому, что он может сохранять низкое воспалительное действие, несмотря на его активность против Th2.
В результате удалось показать, что ST11 представляет собой один из штаммов Lactobacillus, имеющих хороший анти-Тh2 профиль, что делает их превосходным кандидатом для их использования в качестве микроорганизмов, обладающих антиаллергической и симбиотической активностью.
Далее данное изобретение будет описано с использованием примеров без ограничения изобретения этими примерами.
Среды и растворы:
MRS (Difco)
Hugo-Jago (триптон 30 г/л (Difco), дрожжевой экстракт 10 г/л (Difco), лактоза 5 г/л (Difco), K2HPO4 6 г/л, мясной экстракт 2 г/л (Difco), агар 2 г/л (Difco))
М17 (Difco)
DMEM (модифицированная по способу Дульбекко среда Игла)
CFA (в соответствии с Ghosh et al., Journal of Clinical Microbiology, 1993 31:2163-6)
Агар Muller Hinton (Oxoid)
LB (Luria Bertami, Maniatis, A Laboratory Handbook, Cold Spring Harbor, 1992)
Антибиотики получали от Sigma
С14-ацетат (53,4 Ки/ммоль, Amersham International PLC)
PBS (NaCl 8 г/л, КСl 0,2 г/л, Na2HPO4 1,15 г/л, К2НРO4 0,2 г/л))
Раствор Трипсин-ЭДТА (Seromed)
Фетальная телячья сыворотка ФТС (Gibco)
Е. coli DAEC С 1845 получали из Washington University, Seattle, a E. coli JPN15 получали из Центра разработки вакцин университета Maryland, USA).
Пример 1
Выделение молочно-кислых бактерий из фекалий младенцев
Свежие фекалии собирали из пеленок 16 здоровых младенцев в возрасте 15-27 дней. 1 г свежих фекалий помещали в анаэробные условия для транспортировки в лабораторию и в пределах 2 часов от взятия проб серийные разведения фекалий в растворе Рингера высевали на селективные среды. Для выделения молочно-кислых бактерий использовали MRS-агар с антибиотиками (фосфомицин 80 мкг/мл, сульфаметоксазол 93 мкг/мл, триметоприм 5 мкг/мл) при инкубации 48 часов при 37°С. Колонии отбирали случайным образом и очищали. Далее проводили физиологическую и генетическую характеристику изолятов.
Пример 2
Культивирование клеток Сасо-2
Для анализов на ингибирование в качестве модели кишечника использовали клеточную линию Сасо-2. Эта клеточная линия обладает признаками, характерными для клеток кишечника, такими, как, например, поляризация, экспрессиия кишечных ферментов, продуцирование определенных структурных полипептидов и т.д.
Клетки выращивали на трех различных носителях, а именно, в пластиковых чашках (25 кв. см, Corning) для роста и размножения, в обезжиренных и стерилизованных 6-луночных стеклянных планшетах (22 × 22 мм. Corning) для тестов на адгезию и в 24-луночных стеклянных планшетах (Corning) для тестов на ингибирование.
После второго дня культивирования среду (DMEM) заменяли один раз в день. Перед использованием к среде добавляли смесь 100 Е/мл пенициллин/стрептомицин, 1 мкг/мл амфотерин и 20% ФТС, инактивированной при 56°С в течение 30 минут. Культивирование проводили при 37°С в атмосфере 10% CO2. Клетки пассировали каждые шесть дней. Для этого клетки отделяли от стенок лунок обработкой PBS с 0,25% трипсина и 3 мМ ЭДТА, рН 7,2. Для нейтрализации трипсина к полученной клеточной суспензии добавляли равный объем FCS, смесь центрифугировали 10 минут при 1000 об/мин и осадок клеток помещали в культуру. Приблизительно 3,5×105 клеток переносили в новую культуральную бутылку и культивировали до получения конфлюэнтного монослоя.
Пример 3
Культивирование бактерий
ST11:
Бактериальный штамм ST11 хранили при -20°С в MRS-среде, содержащей 15% глицерин. Штамм выращивали в анаэробных условиях в MRS и перед использованием в анализах на ингибирование переносили дважды в новую среду с интервалами 24 часа. Для анализа использовали концентрацию 2×109 КОЕ/мл.
Супернатант после центрифугирования в течение 1 часа при 20000 об/мин проверяли на присутствие бактерий.
Е. coli:
Использовали два штамма Е. Coli - Е. coli DAEC С 1845 (Е. coli с диффузной адгезией) и Е. coli JPN15 (ЕРЕС; энтеропатогенный штамм Е. coli).
Первый пассаж после оттаивания выполняли на агаре CFA-Muller Hinton, который пригоден для индукции экспрессии факторов адгезии этих бактерий.
Перед каждым экспериментом бактериальные клетки дважды инкубировали 24 ч при 37°С в новой среде. Поскольку JPN15 содержит ген устойчивости к ампициллину, этот антибиотик использовали для селекции во время выращивания.
Сальмонелла:
Для экспериментов использовали штамм Salmonella typhimurium SL1344, который предварительно выращивали в LB-среде.
Пример 4
Анализ на ингибирование для Е. coli
После второго пассажа в новой среде патогенные бактериальные штаммы метили радиоизотопами с использованием С14-ацетата при 10 мкКи/мл в LB-среде. Штаммы инкубировали в течение 18 часов при 37°С.
Затем бактериальную суспензию центрифугировали (1041 g, 15 мин) для удаления супернатанта с невключившимся С14-ацетатом. Осадок суспендировали и промывали в PBS и суспендировали клетки в концентрации приблизительно 108 клеток/мл в 1% стерильной маннозе. Известно, что манноза ингибирует неспецифическую адгезию.
Различные патогенные бактериальные штаммы (Е. coli) инкубировали с монослоем клеток Сасо-2 (37°С, 10% СO2) в течение 3 часов. Также проводили эксперименты с добавлением супернатанта (полученного центрифугированием при 20000 об/мин в течение 40 минут).
В качестве контроля патогенные бактерии инкубировали с монослоем Сасо-2 без добавления ST11 или культурального супернатанта соответственно.
После инкубации в течение 3 часов среду удаляли и монослой промывали три раза PBS. Для исключения неспецифической адгезии промывку проводили путем 20 перемешиваний PBS. Клетки лизировали добавлением 1 мл карбоната натрия и инкубировали в течение 40 минут при 37°С. После гомогенизации аликвоту (250 мкл) добавляли в 5 мл сцинтилляционной жидкости (Hionicfluor Packcard) и просчитывали (Packcard). Процент адгезии патогенных клеток к клеткам Сасо-2 рассчитывали по сравнению с контролем, который принимали за 100% (адгезии; или инвазии для примера 5).
Пример 5
Анализ на ингибирование для сальмонеллы
Сальмонелла является бактерией, которая внедряется в эпителиальные клетки и размножается в них. Для определения ингибирующей активности ST11 штамм Salmonella typhimurium SL1344 инкубировали, как описано выше, в среде, содержащей С14-ацетат, и анализировали аналогично примеру 4.
Для удаления неприкрепившихся клеток после инкубации клетки Сасо-2 промывали PBS. Затем к среде добавляли гентамицин (20 мкг/мл) и инкубировали в течение 1 часа при 37°С. Гентамицин является антибиотиком, не проникающим в кишечные клетки, таким образом все неприкрепившиеся клетки микроорганизма погибли, в то время как сальмонеллы, уже внедрившиеся в кишечные клетки, выживали. Клетки дважды промывали PBS и лизировали добавлением стерильной дистиллированной воды, после чего радиоактивность измеряли, как описано в примере 4.
Результаты экспериментов 4 и 5 показаны на фигурах 1-4. Можно видеть, что культивируемые клетки ST11 и культуральный супернатант были чрезвычайно эффективными в предотвращении адгезии к кишечным клеткам и инвазии в кишечные клетки патогенных микроорганизмов, вызывающих диарею.
Пример 6
Свойства ST11
ST11 инкубировали в модели желудочного сока. Для получения модели желудочного сока пепсин (3 г/л) суспендировали в стерильном солевом растворе (0,5% масс./об.) и доводили рН концентрированной НСl до 2,0 и 3,0 соответственно. ST11 выращивали в указанных выше средах и определяли устойчивость микроорганизмов.
Результаты приведены в таблице.
| Таблица | ||||||
| рH | КОЕ/мл Т 0 мин | КОЕ/мл T 1 мин | КОЕ/мл Т 15 мин | КОЕ/мл Т 30 мин | КОЕ/мл Т 60 мин | |
| 2,0 | 2,0×109 | 1,8×109 | 1,2×109 | 3,7×109 | 7,0×109 | |
| 3,0 | 2,0×109 | 1,9×109 | 1,7×109 | 1,7×109 | 8,4×109 |
ST11 обладал следующими свойствами, определенными в соответствии со способами, описанными в Genera of lactic acid bacteria, Ed. B.J.B.Wood and W.H.Holzapfel, Blackie A&P.
- грамположительные,
- каталаза-отрицательные,
- отрицательные по NH3-формы аргинина,
- отрицательные по продуцированию СО2,
- продуцирующие L(+)-молочную кислоту,
- растущие в присутствии солей желчных кислот в концентрации до приблизительно 0,4%.
Пример 7
Рост ST11 в различных условиях
ST11 инкубировали при 37°С в среде на основе томатов (4% порошок томатов, регидратированный в дистиллированной воде), дополненной сахарозой (0, 0,5, 1 или 2%) или соевым пептоном (0,5%) или глюкозой (0,5%), в течение различных периодов времени. Результаты показаны на фиг.5.
ST11 дополнительно добавляли в количестве 2,5% к среде, состоящей из рисовой муки (3%), пшеничной муки (2%) и сахарозы (3%), и инкубировали при 37°С до достижения рН 4,4. После охлаждения продукт упаковывали с добавлением или без добавления витамина С и хранили при 10°С.
Фиг.5 показывает данные по выживанию ST11 при 10°С в пшеничном напитке, упакованном в различные пластиковые материалы (полиэтилен высокой плотности(HDPE), полистирол, (PS).
Пример 8
Индукция синтеза мРНК IL-12 и IL-10 в мышиных прикрепленных клетках ST11
Клетки костного мозга выделяли из бедренной и большеберцовой кости 8-недельных, не содержащих конкретного патогена мышей C57BL/6, инкубировали при концентрации 2×106 клеток/мл в среде RPMI (Gibco), содержащей 10% фетальную телячью сыворотку, 1 мМ L-глутамин, 12 мМ Hepes, 0,05 мМ 2-меркаптоэтанол, 100 Е/мл пенициллина и 100 мкг/мл стрептомицина (все реагенты от Gibco), в течение 12 часов при 37°С в атмосфере 5% СO2. Неприкрепившиеся клетки удаляли 3 последовательными промывками теплой культуральной средой, а оставшиеся прикрепившиеся клетки собирали и инкубировали при концентрации 106 клеток/мл в течение 6 часов в присутствии или в отсутствие бактерий. Предварительно было определено, что 6 часов являются оптимальной временнной точкой для синтеза мРНК цитокинов в мышиных прикрепленных клетках в ответ на LPS. Бактерии добавляли при концентрациях в диапазоне от 109 до 107 КОЕ/мл. Бактерии выращивали и хранили, как указано выше.
В конце 6-часового периода культивирования клетки отделяли центрифугированием и лизировали с использованием набора реагентов TRIzol (GibcoBRL, Cat. No. 15596-018) в соответствии с инструкциями изготовителя. Тотальную РНК выделяли осаждением изопропанолом и проводили обратную транскрипцию в кДНК в течение 90 минут при 42°С с использованием 200 Е обратной транскриптазы (Superscript II, BRL) в реакционном объеме 40 мкл, содержащем 200 мМ Трис рН 8,3, 25 мМ КСl, 1 мкг/мл олиго-d(T)15 (Boehringer Mannheim), 1 мМ ДТТ (Boehringer Mannheim), 4 мМ каждого из dNTP (Boehringer Mannheim) и 40 Е/мл Rnasin (Promega). Использовали ПЦР-праймеры и условия, уже описанные в Kopf et al. (Journal of Experimental Medicine 1996 Sep. 1:184 (3):1127-36). Количества кДНК нормализовали в пробах с использованием праймеров, специфических для β-2-микроглобулина (house-keeping gene). ПЦР-продукты разделяли в 2% агарозном геле и полосы анализировали под УФ.
Как показано на фигуре 1, ST11 показал самое сильное ингибирование мРНК IL-12 и IL-10, которое сравнимо с уровнями, наблюдаемыми с положительным контролем (Е. coli). Различия лучше всего видны при самых низких концентрациях бактерий (107 КОЕ/мл).
Пример 9
Супрессия синтеза IL-4 ST11
CD4+ Т-клетки выделяли из селезенки не содержащих конкретного патогена BALB/c мышей с использованием набора Mini-MACS из Miltenui Biotec (Cat. No. 492-01). CD4+ Т-клетки культивировали при концентрации 2×105 клеток/мл в среде RPMI, содержащей 10% фатальную телячью сыворотку, 1 мМ L-глутамин, 12 мМ Hepes, 0,05 мМ 2-меркаптоэтанол, 100 Е/мл пенициллина и 100 мкг/мл стрептомицина, и активировали в течение одной недели сшиванием со связанными с планшетом моноклональными антителами против CD3 (клон 2С11) и CD28 (клон 37,51, оба антитела от Pharmingen). Во время первичной культуры CD4+ Т-клетки культивировали с прикрепленными клетками костного мозга (выделенными, как описано выше) в качестве вспомогательных клеток и с 108 КОЕ/мл La1 или 1 мг/мл LPS или с одной средой. Затем клетки промывали и CD4+ Т-клетки очищали еще раз с использованием набора MiniMACS и повторно стимулировали во вторичной культуре, содержащей только среду. Цитокины, продуцируемые дифференцированными CD4+ Т-клетками, измеряли в супернатантах после 2 дней с использованием сэндвич-ELISA (наборы от Endogen и Pharmingen).
Результаты показаны на фиг.5. Клетки, дифференцированные в присутствии только среды, проявляли доминатный фенотип Th2, характеризующийся высоким содержанием IL-4. Добавление ST11 к первичным культурам сильно модулировало дифференцировку Th2, так как оно приводило к 8-кратному уменьшению продуцирования IL-4. Подобное ингибирование наблюдалось и в культурах клеток, дифференцировавшихся в присутствии LPS. В противоположность этому, другой штамм Lactobacillus не оказывал существенного влияния на содержание IL-4. Интересно, что уровни IFN-γ не увеличивались при добавлении ST11 в первичные культуры.
Как можно видеть из приведенных выше результатов, штаммы данного изобретения могут быть использованы для приготовления пищевых и/или фармацевтических средств, использующих полезные свойства этих микроорганизмов.
Пример 10
Штамм ST11 тестировали в клинических испытаниях на жителях предместья Guatemala City на его способность влиять на передачу инфекции и протекание острой диареи дождливого сезона, которой страдает большинство детей в этой области. 203 ребенка в возрасте от 35 до 70 месяцев были зарегистрированы для этого исследования и получали целевую дозу 1010 жизнеспособных микроорганизмов (ST11) или плацебо на протяжении периода кормления 29 дней. Дети, отобранные как для введения пробы, так и для введения плацебо соответственно, имели типичные характеристики недостаточности веса и роста для соответствующего возраста, обусловленные истощением.
Перед началом испытания у дошкольников проводили оценку безопасности на основании исследований in vitro и in vivo. Исследования in vitro показали профиль устойчивости к антибиотикам, сходный с профилем других Lactobacillus, используемых в пищевых применениях, и не обнаружили способности в отношении образования биогенных аминов, в отношении деградации муцина (слизистого секрета) и в отношении деконъюгации солей желчных кислот. В клинических испытаниях с плацебо, в которых участвовали 42 взрослых волонтера, ST11 хорошо переносился и не индуцировал вредных эффектов среди потенциальных проявлений, подвергнутых мониторингу, таких как метеоризм, частота стула в день и консистенция стула; уровни белков острой фазы в сыворотке не вызывали никакого беспокойства в отношении потенциальной воспалительной реакции.
Пробы и плацебо были упакованы в виде подушечки в пакетики (sachet) на производственном предприятии Nestle Product Technology Center в Konolfingen, Switzerland и доставлены в холодильнике в Гватемалу. Каждая подушечка весом 10 г состояла из имеющего вкус шоколода ароматизированного носителя и либо 0,2 г ST11 (1010 КОЕ), либо, в случае плацебо, 0,2 г молочного порошка. Имеющий вкус шоколада ароматизированный носитель состоял из какао-порошка, сахара, лецитина сои, ванилина и корицы. Подушечки хранили при 4-6°С до двух часов перед использованием. Перед использованием подушечку нужно было растворить в 100 мл воды, обеспеченной Nestle, которая не содержала бактериального загрязнения.
В соответствии с протоколом, диарея, с которой имели дело, была определена как наличие трех или более жидких или не имеющих формы дефекаций на протяжении периода 24 часов. Диарейный приступ был определен как событие, которое давало свидетельство диареи (3 диарейных дефекации на протяжении 24 часов). Его общую продолжительность в часах рассчитывали от момента первых трех показательных дефекаций до появления первого оформленного стула или периода 24 часов без какой-либо дефекации. Для ребенка, чтобы иметь “новый” приступ, должны пройти 48 часов от конца первого приступа. Если это не происходит, то это рассматривается продолжением того же самого приступа и затем для оценки используют общую продолжительность. Был случай, когда ребенок, который испытывал один или более документированных приступа диареи на протяжении 29-дневного периода наблюдения. Интенсивность диарейного приступа основывается на общем числе производимых жидких стулов. Элементы тяжести приступа включают в себя присутствие крови, слизи или гноя в стуле, вместе с симптомами лихорадки и рвоты. Интенсивность 7 стулов за 24 часа или необходимость вмешательства профессионала в клинике, центре здоровья или больнице также классифицируют приступ как тяжелый.
Когда диарейный приступ диагностировали системой контроля, образец диарейного стула собирали для микроскопического исследования и культивирования для идентификации потенциальных этиологических патогенов для данного приступа. Образец диагностировали на ротавирусный антиген, Giardia и Е. histo-lytica, в случае дизентерийной пробы, и на бактериальные патогены, в том числе Shigella, Salmonella, Aeromonas, Plesiomonas shigelloides, E. coli и, возможно, V. cholerae.
Во время периода исследования брали пробы для испытания жизнеспособности включенных микроорганизмов во время периода введения. Удалось показать, что этот микроорганизм оставался жизнеспособным в подушечках во время всего исследования, так что также и в конце исследования подушечки были способны передавать 1010 жизнеспособных микроорганизмов при реконституировании водой.
Данное изобретение выявило, что проба, содержащая симбиотический микроорганизм, уменьшала возникновение диареи, в противоположность контрольной группе (плацебо), на приблизительно 30%. Но также контрольная группа уже проявляла уменьшенное число возникновений диареи в сравнении с нормальной популяцией, не получающей ни проб, ни плацебо соответственно. Это последнее открытие может быть час