Клеточная линия иммортализованных кератиноцитов человека (варианты) и способ иммортализации клеток кожи человека
Иллюстрации
Показать всеИзобретение относится к генной инженерии, конкретно к получению из кожных тканей здорового человека иммортализованных клеточных линий, и может быть использовано для иммунологических, фармакологических, фото- и химико-токсикологических анализов кожной реакции, для экспрессии гетерологичных генов и для конструирования искусственной кожи. Кератиноциты иммортализуют путем инфицирования кератиноцитов здорового человека. Выделяют пробу кожи человека и подготавливают эту пробу кожи для культуры in vitro. Получают кератиноциты из этой приготовленной пробы кожи человека и засевают бессывороточную среду для выращивания кератиноцитов на культуральных чашках с покрытием, облегчающим прикрепление и рост клеток. При культивировании кератиноцитов заменяют бессывороточную среду достаточным образом для получения оптимального конфлюэнтного роста клеток в культуре с непрерывным поддержанием покрытия чашки. Кератиноциты переносят в селективную бессывороточную среду на культуральных чашках с покрытием и инфицируют векторами pLXSHD+SV40(#328) и pLXSHD+E6/E7. Затем на культуральных чашках с покрытием переносят полученные иммортализованные кератиноциты в пригодную среду для пролиферации. После этого переносят полученные пролиферировавшие кератиноциты в среду для дифференцировки с высоким содержанием кальция, на культуральных камерах с покрытием. Изобретение позволяет получить клеточную линию кератиноцитов человека, которая является неонкогенной, сохраняет способность дифференцироваться и экспрессировать белки и ферменты, экспрессируемые нормальными дифференцированными кератиноцитами, даже после увеличенного числа пассажей в культуре, а также образует слоистый и поляризованный эпителий, имеющий ороговевший слой (stratum comeum), состоящий из орто-кератиноцитов, при культивировании в органотипической культуре в бессывороточной среде и без слоя питающих клеток. 3 н. и 4 з.п. ф-лы, 2 ил.
Реферат
Область техники, к которой относится изобретение
Данное изобретение относится к медицине, в частности к новым иммортализованным клеточным линиям, полученным из кожных тканей здорового человека и предоставляющим улучшенные характеристики дифференцировки, к новому способу получения этих клеточных линий и к различным их применениям, в частности в области создания искусственной кожи.
Уровень техники
Получение иммортализованных клеточных линий, происходящих из тканей кожи здорового человека, уже было описано. Как правило, способы, используемые для этой цели, включают в себя трансформацию клеток кожи человека, например кератиноцитов и меланоцитов, которые культивируют in vitro с агентами, придающими иммортализацию. Иммортализация имеет в виду получение клеток, которые могут культивироваться в течение продолжительного периода времени in vitro, теоретически в течение неограниченного периода. Эти клетки называют также непрерывными клеточными линиями. В противоположность этому неиммортализованные клетки способны размножаться только в течение определенного числа клеточных делений in vitro. Иммортализованные клетки являются чрезвычайно выгодными, так как они обеспечивают стабильный, потенциально неограниченный источник клеток, имеющих определенные характеристики. Типичными агентами для получения иммортализованных клеточных линий и иммортализованных линий клеток кожи человека являются, в частности, например, вирусы, рекомбинантные вирусы и плазмиды, содержащие последовательности ДНК, придающие свойство иммортализации.
Наиболее обычный способ получения иммортализованных клеточных линий человека включает в себя, возможно, использование последовательностей вакуолизирующего обезьяньего вируса 40 (SV40) и более конкретно ДНК большого Т-антигена (Т-Ад) SV40 в качестве агента иммортализации. Например, Steinberg et al., J. Cell Phys, 123, 117-125 (1985); патент US 4885238 (Reddel et al.); патент US 4707448 (Major); Stoner et al., Cancer Res., 51, 365-371 (1991); Chopra et al., In vitro Cell Dev. Biol., 30A, 539-546 (1994); Chopra et al., In vitro Cell Dev. Biol., 27A, 763-765 (1991); Christian et al., Cancer Res., 47, 6066-6073 (1987); Rhim et al., Science, 227, 1250-1252 (1985) и Grubman et al., Gastrointest. Liver Physiol., 29, G1060-G1070 (1994) сообщают об использовании векторов SV-40 и векторов, содержащих последовательность большого Т-антигена SV-40, для получения иммортализованных клеточных линий человека. Введение таких последовательностей выполняют обычно инфицированием вирусом SV-40 или гибридным аденовирусом 12/SV-40 или трансфекцией клеток рекомбинантной плазмодий, содержащей длинные концевые повторы вируса саркомы Рауса и регуляторный ori-район SV-40, копреципитацией в присутствии фосфата стронция (см. Brash et al., Mol. Cell Biol., 7, 2031-2034, 1987).
Другой известный способ получения иммортализованных клеточных линий и, в частности, иммортализованных кератиноцитов человека предусматривает трансфекцию или инфицирование клеток последовательностями ДНК вируса папилломы человека (ВПЧ). Например, в патенте US 5376542 (Schlegel) описана иммортализация эпителиальных клеток человека генами Е6 и Е7, выделенными из ВПЧ-16, 18, 31, 33 или 35, или одним геном Е7 для получения неонкогенных иммортализованных клеточных линий человека. Кроме того, Barbosa et al., Oncogene, 4, 1529-1532 (1989) и Munger et al., J. Virol., 63(10); 4417-4421 (1989) сообщают об использовании генов Е6 и Е7 ВПЧ-16 и ВПЧ-18 для получения иммортализованных кератиноцитов человека. Кроме того, et al., Oncogene, I, 251-256 (1987) описывает иммортализацию кератиноцитов вирусом папилломы человека типа 16.
Несмотря на то, что многочисленные группы описали иммортализованные клеточные линии кератиноцитов и их применение в анализах in vitro, эти иммортализованные клеточные линии кератиноцитов по состоянию в настоящее время обнаруживают обычно одно или несколько свойств, делающих их использование невыгодным. Например, описанные ранее имморталиэованные кератиноциты обнаруживают одно или несколько из следующих свойств: (i) уменьшение или утрату экспрессии маркеров дифференцировки, например, белков, экспрессируемых нормальными дифференцированными кератиноцитами, (ii) свойства модифицированного роста в культуре тканей и (iii) образование слоистого и поляризованного эпителия, имеющего состоящий из пара-кератиноцитов ороговевший слой (stratum corneum).
Для устранения этих недостатков в Европейском патенте ЕР780496 (Societe des Produits Nestle) предложен новый способ для иммортализации кератиноцитов или меланоцитов человека с использованием en sus новой культуральной среды, вектора pLXSHD+SV40(#328), который произведен из вируса SV-40, или равным образом вектора pLXSHD+E6/E7, который произведен из вируса папилломы человека 16 (ВПЧ-16). Иммортализованные клетки, полученные таким образом, сохраняют способность дифференцировки и экспрессии белков и ферментов, которые экспрессируются нормальными дифференцированными кератиноцитами и меланоцитами, даже после увеличенного числа пассажей в культуре.
Однако, несмотря на эти прежние описания, все еще существует важная необходимость в практической области в том, чтобы иметь иммортализованные кератиноциты человека, обладающие еще более улучшенными свойствами. Такие клетки были бы крайне выгодными для многочисленных применений, в частности, для анализов, требующих применения высокодифференцированных клеток кожи.
Сущность изобретения
Для этой цели данное изобретение относится к иммортализованной клеточной линии кератиноцитов человека, полученной с использованием по меньшей мере одного онкогенного функционального гена ретровирусного происхождения, которая характеризуется тем, что она
(1) является неонкогенной,
(2) сохраняет способность дифференцироваться и экспрессировать белки и ферменты, экспрессируемые нормальными дифференцированными кератиноцитами, после увеличенного числа пассажей в культуре ткани и
(3) образует слоистый и поляризованный эпителий, имеющий состоящий из орто-кератиноцитов ороговевший слой (stratum corneum), при культивировании в органотипической культуре в бессывороточной среде и без слоя питающих клеток.
Другой целью данного изобретения является разработка нового способа получения иммортализованных клеточных линий кератиноцитов, происходящих из нормальных кожных тканей.
Еще одной целью данного изобретения является разработка способов применения этих клеточных линий кератиноцитов в соответствии с данным изобретением, например, для иммунологических, фармакологических, фото- или химико-токсикологических анализов кожной реакции и для экспрессии гетерологичных генов.
Описание фигур
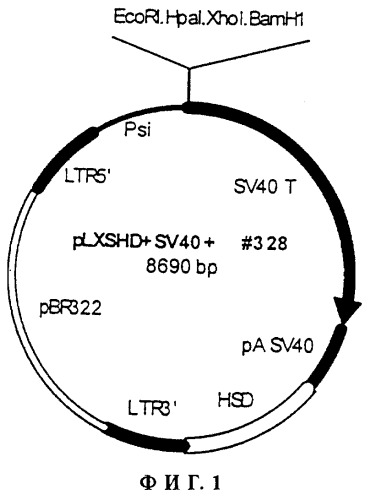
- Фигура 1 показывает конструкцию, полученную из ретровируса SV40, а именно плазмиды pLXSHD+SV40(#328), используемую для иммортализации кератиноцитов данного изобретения.
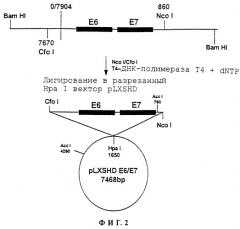
- Фигура 2 представляет конструкцию, полученную из ретровируса папилломы 16, а именно плазмиды pLXSHD+E6/E7, используемую для иммортализации кератиноцитов данного изобретения.
Подробное описание изобретения
Данное изобретение обеспечивает неонкогенные, иммортализованные клеточные линии кератиноцитов, т.е. клеточные линии, которые не образуют опухолей при инъекции под кожу животного с использованием, например, по меньшей мере 2×106 клеток для каждой инъекции.
Эти клеточные линии также сохраняют способность дифференцироваться и экспрессировать белки и ферменты, экспрессируемые нормальными кератиноцитами, после увеличенного числа пассажей. Выражение "увеличенное число пассажей" имеет в виду по меньшей мере 10 пассажей в культуре, предпочтительно по меньшей мере 20-30 пассажей, более предпочтительно по меньшей мере 50 пассажей и теоретически неограниченное число пассажей. Например, иммортализованные кератиноциты, полученные в соответствии с данным изобретением, экспрессируют белки дифференцировки, состоящие из кератина К1/10, кератина К14, инволукрина, филаггрина и лорикрина, даже после увеличенного числа пассажей в культуре тканей.
Иммортализованные кератиноциты данного изобретения имеют профиль цитохрома р450 (CYP450), который сходен, если не идентичен, с профилем нормальных кератиноцитов. Например, клетки данного изобретения экспрессируют CYP450 1А1, 2Е1, 2С18 и ЗА5. Кроме того, иммортализованные кератиноциты данного изобретения экспрессируют ферменты фазы II, например глютатион-S-трансферазу π (gsttt), сравнимым с нормальными, неиммортализо-ванными кератиноцитами образом.
Кроме того, иммортализованные кератиноциты данного изобретения экспрессируют белки и ферменты, участвующие в клеточном окислении и в воспалительных ответных реакциях, например, супероксиддисмутазу (SOD) и коллагеназу типа I и фактор некроза опухоли альфа (TNFα), после обработки форболовыми эфирами подобным или идентичным образом в сравнении с нормальными дифференцированными кератиноцитами. С учетом этих конкретных характеристик эти клеточные линии представляют собой чрезвычайно интересный, воспроизводимый источник для иммунологических, фармакологических, связанных с воспалением, фото- и химико-токсикологических исследований кожных реакций.
Кроме того, линии иммортализованных кератиноцитов данного изобретения образуют при культивировании в органотипической культуре в бессывороточной среде [например, в среде NR2 Biofluids Inc., U.S., обогащенной EGF (эпидермальным фактором роста) (5 нг/мл), витамином С (38 мкг/мл) и СаСl2 (1,5 М] и без слоя питающих клеток (без фибробластов), слоистый и поляризованный эпителий, имеющий поверхностные кератинизированные (ороговевшие) слои, обычно называемые ороговевшим слоем (stratum corneum), имеющие морфологию орто-кератиноцитов, что означает, что этот слой stratum corneum не содержит ядерных клеток, т.е. клеток, содержащих ядра.
Получение слоистого и поляризованного эпителия с иммортализованными кератиноцитами достигалось ранее в классических условиях культуры, т.е. способом с использованием среды, содержащей телячью сыворотку и слой питающих клеток (Lechner et al., Virology, 185, 536-671, 1991). Тем не менее эти иммортализованные клетки не образовывали нормальные поверхностные кератинизированные (ороговевшие) слои. Например, известно, что клеточные линии, имморталиэованные вирусом папилломы 16 или 18 или Е6/Е7, образуют очень дезорганизованные (разрушенные) эпителии (Blanton et al., Am. J. Pathol., 138, 673-685, 1991; Hudson et al., J. Virol., 64, 519-526, 1990; McCane et al., Proc. Natl. Acad. Sci., 85, 7169-7173, 1988; Woodworth et al., Oncogene, 7, 619-626, 1992).
В противоположность этому, линии, описанные в ЕР 780496 (Societe des Produits Nestle), при культивировании в органотипической культуре в бессывороточной среде и без слоя питающих клеток, образовывали слоистый и поляризованный эпителий, имеющий нормальные поверхностные кератинизированные (ороговевшие) слои, но тем не менее имеющие морфологию пара-кератиноцитов, т.е. stratum corneum (ороговевший слой) содержал все еще клетки с ядрами.
Иммортализованные кератиноциты данного изобретения также абсорбируют экзогенные незаменимые жирные кислоты (AGE) и обнаруживают ненасыщенное состояние и пролонгацию цепи AGE, совершенно соответствующие ненасыщенному состоянию и пролонгации цепи AGE нормальных кератиноцитов.
В общих чертах иммортализованные кератиноциты данного изобретения могут быть получены согласно следующему способу:
(i) получение пробы кожи человека;
(ii) подготовка этой пробы кожи для получения первичных кератиноцитов, пригодных для культивирования;
(iii) культивирование этих первичных кератиноцитов в бессывороточной среде, предпочтительно в среде NR-3 (описанной в ЕР 780496), на культуральных чашках, имеющих покрытие, облегчающее прикрепление и рост клеток, причем это покрытие содержит фибронектин, SАВ и коллаген типа I;
(iv) замена бессывороточной среды достаточным образом для получения оптимального конфлюэнтного роста кератиноцитов на культуральных чашках, причем покрытие чашки поддерживается непрерывно;
(v) отделение кератиноцитов в культуре от меланоцитов и перенос отделенных кератиноцитов в среду для инфицирования, предпочтительно в среду NR-3 и предпочтительно после обработки этих клеток композицией, содержащей трипсин и ЭДТА, с использованием культуральных чашек, покрытых покрытием таким же образом;
(vi) инфицирование клеток функциональными онкогенными генами по меньшей мере двух различных ретровирусов, таких как вирус SV40 и вирус папилломы человека;
(vii) перенос иммортализованных кератиноцитов в бессывороточную среду для пролиферации на культуральных чашках, покрытых покрытием предварительно таким же образом, предпочтительно в среды NR-2 или NR-3 (среды, описанные в ЕР 780496), состав которых включен здесь в качестве ссылки), и
(viii) перенос иммортализованных кератинсцитов после пролиферации в общепринятую среду для дифференцировки, имеющую высокое содержание кальция (1,5 М), предпочтительно в среду NR-2, обогащенную EGF (эпидермальным фактором роста) (5 нг/мл) и витамином С (38 мкг/мл).
Более подробно, стадия (i) обычно предусматривает получение проб ткани кожи человека у здоровых доноров, например, проб, получаемых во время хирургического вмешательства или педиатрического вмешательства. Иммортализация уникальной пробы кожных клеток, т.е. аутологической пробы кожных клеток, позволяет получать иммортализованные клеточные линии кератиноцитов, обнаруживающих определенные характеристики, например профиль конкретного рецептора, являющиеся характерными для конкретного донора.
Затем эту пробу кожной ткани подготавливают в стадии (ii) таким образом, чтобы она была пригодна для культуры in vitro.
Эта подготовка обычно выполняется промыванием сначала пробы кожной ткани, например, с использованием среды, используемой для культуры. Предпочтительно, эту операцию проводят в среде NR-2, которая является бессывороточной средой, точный состав которой описан в ЕР 780496, которая, как было показано, имеет преимущества для культуры нормальных кератиноцитов. После промывания пробу кожной ткани предпочтительно бреют, например, при помощи дерматома (инструмента для кожной пластики), и затем нарезают на небольшие кусочки.
Затем полученные срезы кожи разделяют предпочтительно на дерму (собственно кожу) и эпидермис (наружный (эпителиальный) слой кожи)). Это может быть достигнуто физическими и/или ферментативными способами. Например, это может быть выполнено обработкой трипсином, например, флотацией проб кожной ткани в растворе трипсина (например, приблизительно 0,5%), содержащего ЭДТА (например, приблизительно 0,1%), в течение времени, достаточного для инициации разделения клеток, например, в течение времени приблизительно 30-60 минут при температуре 37°С, или, например, в течение ночи при 4°С.
Дерму отделяют и затем эпидермис помещают в среду для получения суспензии. Предпочтительно среда для получения суспензии содержит раствор соевого ингибитора трипсина (SBTI) и ее помещают в контакт с клетками в течение времени (обычно 5 минут), достаточного для инактивации трипсина и высвобождения клеток. Затем среду для культуры ткани, предпочтительно среду NR-2, лишенную сыворотки (описанную в ЕР 780496), и фильтр (например, фильтр 100 нм) добавляют для получения целевых клеток, т.е. кератиноцитов.
Затем первичные кератиноциты, полученные в стадии (ii), используют для засева бессывороточной среды, предпочтительно среды NR-3 (описанной в ЕР780496), в подходящей концентрации клеток, предпочтительно приблизительно 1,2×104 клеток/см2, на предварительно покрытых культуральных чашках. Однако концентрация клеток может варьировать в широких пределах. Культуральные чашки предпочтительно обеспечиваются покрытием, содержащим композицию, которая, как было показано, усиливает прикрепление и рост кератиноцитов, более конкретно раствор фибронектина, ЗАВ и коллагена типа I.
В стадии (iv) культуральную среду заменяют так часто, как это необходимо для получения оптимального клеточного роста. Предпочтительно среду заменяют каждый раз после приблизительно двух дней. Однако это зависит от конкретной пробы кожной ткани. После получения почти полной конфлюэнтности, например конфлюэнтности приблизительно 90%, что имеет место после приблизительно 10-14 дней, кератиноциты и меланоциты разделяют. Это может быть выполнено любым выбранным способом, делающим возможным адекватное разделение клеток без какого-либо повреждающего влияния на меланоциты и кератиноциты. Например, это может быть выполнено дифференциальной обработкой трипсином. Предпочтительно меланоциты или кератиноциты обрабатывают раствором трипсин/ЭДТА и затем переносят в селективную среду. В случае кератиноцитов клетки предпочтительно обрабатывают в течение приблизительно 5-10 минут раствором трипсин/ЭДТА (0,025%/0,01%) и затем используют в стадии (v) для засева в среду NR-3 на предварительно покрытых чашках.
Затем кератиноциты обрабатывают агентом иммортализации. Клетки могут быть также заморожены до выполнения иммортализации, например, в жидком азоте. Инфицирование и иммортализацию предпочтительно выполняют с использованием функциональных онкогенных генов по меньшей мере двух различных ретровирусов, таких как гены Т-Аg вируса SV40 и Е6/Е7 ВПЧ-16 (HPV16). Каждый из этих генов может находиться в независимой ретровирусной конструкции, например в ретровирусном векторе pLXSHD+SV40(#328), показанном на фигуре 1 и описанном Stockshlaeder et al. (GeneBank, номер доступа М64753; Human Gen. Therapy, 2, 33-39, 1991) и ретровирусном векторе pLXSHD+E6/E7, который показан на фигуре 2.
Ретровирусный вектор pLXSHD+SV40(#328) содержит среди других последовательностей последовательность Т-Ад SV40, последовательности 5’- и 3’- длинных концевых повторов SV-40, последовательности pBR322, которые делают возможными репликацию Е.coli, цикл множественного клонирования, и последовательность полиаденилирования SV-40.
В местоположении гена, кодирующего Т-антиген, вектор pLXSHD+E6/E7 содержит NcoI/CfoI-фрагмент гена Е6/Е7, полученный из вируса папилломы человека 16.
После иммортализации клетки затем подвергают необходимому числу пассажей во время культивирования и полученные иммортализованные клетки затем переносят в среду для пролиферации на стадии (vii). Этот перенос предпочтительно выполняют во время второго пассажа. Среда для пролиферации может быть бессывороточной средой, предпочтительно средой NR-2 или NR-3. Иммортализованные клетки культивируют на предварительно покрываемых непрерывно культуральных чашках, причем покрытие опять содержит раствор фибронектина, SAB и коллагена типа I.
После размножения иммортализованных клеток в среде для пролиферации (предпочтительно NR-2) кератиноциты переносят на стадии (viii) в среду, индуцирующую дифференцировку нормальных и иммортализованных кератиноцитов, предпочтительно в среду, симулирующую (воспроизводящую) условия, преобладающие в коже, генерируя таким образом организацию кератиноцитов в слоистый и поляризованный эпителий, имеющий нормальные поверхностные кератинизированные слои. Для этой цели клетки могут культивироваться в бессывороточной среде, имеющей высокое содержание кальция, такой как NR-2, содержащей приблизительно 1,5 мМ кальций, приблизительно 5 нг/мл EGF и приблизительно 38 мкг/мл витамина С, причем культивирование выполняется на чашках в течение 2-3 недель на границе раздела (в интерфазе) воздух/жидкость, например, на чашках с 12 лунками Falcon No. 3042, причем каждая лунка имеет вкладыш Falcon No. 3180, в котором кератиноциты развиваются в интерфазе воздух/жидкость. Воздух состоит из атмосферного воздуха, содержащегося во внутреннем пространстве вкладыша, которое лишено питательной среды. Жидкостью является питательная среда, содержащаяся в лунке, причем эта среда пересекает мембрану вкладыша, на которой развиваются кератиноциты.
Что касается свойств иммортализованных кератиноцитов данного изобретения, они являются вполне пригодными для иммунологических, фармакологических, фото- и химико-токсикологических анализов кожных реакций. Например, иммортализованные клеточные линии кератиноцитов данного изобретения могут быть использованы для анализов, требующих дифференцированных кожных клеток, например, для исследований, по барьерной функции (кератинизации) реконструированной кожной ткани, исследований по метаболизму дифференцированных кератиноцитов (метаболизму жирных кислот, метаболизму антиоксидантов), исследований, касающихся влияний УФ-радиации на кожные клетки, исследований, касающихся влияний потенциальных раздражающих кожу и сенсибилизирующих кожу агентов на кожные клетки, исследований по метаболизму липидов, посредством локальной обработки и/или с использованием среды с ксенобиотическими агентами (например, косметическими маслами, путем выбора возможных защитных соединений, например, фотозащитных агентов), исследований по воспалению и раздражению кожи и т.д.
Кроме того, клеточные линии кератиноцитов, получаемые в соответствии с данным изобретением, используются для отбора потенциальных противораковых соединений и потенциальных соединений для лечения кожных болезней. Это обычно подразумевает, что эту клеточную линию выдерживают в контакте с такими соединениями во время конкретного периода времени и определяют потенциальную индукцию каких бы то ни было вредных эффектов, например, генотоксичности, образования ДНК-аддуктов, мутагенности, клеточной трансформации или цитотоксичности.
Кроме того, линии иммортализованных кератиноцитов данного изобретения могут быть использованы в анализах мутагенности ДНК, анализах для отбора кожных мутагенных агентов, анализах для идентификации агентов изменения хромосом, в исследованиях по злокачественной трансформации, исследованиях по клеточной биохимии (например, в тестах активации CYP450), в отборе соединений и композиций, например, смесей незаменимых жирных кислот, участвующих в воспалительных и аллергических реакциях, в тестах на активацию коллагеназы (в связи с воспалением), участие TNFa, и для обнаружения интерлейкина.
Что касается того факта, что клеточные линии данного изобретения образуют содержащий орто-кератиноциты ороговевший слой (stratum corneum), они особенно хорошо приспособлены для участия в получении искусственной кожи, предназначенной для исследований по мутагенности, для иммунологических, фармакологических, фото- и химико-токсикологических исследований, упомянутых выше. Эта кожа может состоять только из эпителия кератиноцитов данного изобретения, но предпочтительно она содержит также, например, коллаген, фибробласты, даже меланоциты, чтобы иметь большее сходство с кожей здорового человека.
Кроме того, клеточные линии кератиноцитов данного изобретения способны экспрессировать рекомбинантные белки, например, полипептиды и белки человека, а также продуцировать РНК и ДНК.
Среди иммортализованных клеточных линий кератиноцитов, получаемых в соответствии с данным изобретением, только клеточная линия DK7-NR была как, например, депонирована согласно условиям Будапештского договора 19 марта, 1998 года в Collection Nationale de Culture de Microorganismee (C.N.C.M.), имеющей адрес 25, rue de Docteur Roux, 75724 Paris, France, и получила депозитный номер CNCM I-1996. Это депонирование было выполнено согласно условиям Будапештского договора. Все ограничения, касающиеся доступности этой клеточной линии, будут окончательно сняты после выдачи патента в соответствии с данной заявкой или другой заявкой, заявляющей право приоритета данной заявки.
Другие признаки данного изобретения станут очевидными из нижеследующего описания примеров, которые даются для иллюстрации данного изобретения и не должны рассматриваться как ограничительные. Если нет иных указаний, манипулирование с клетками, приготовление векторов, трансформация клеток и все другие технические способы выполняются в соответствии с протоколами, описанными Sambrook et al., (Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, USA, 1989).
Пример 1: Получение и характеристика клеточных линий
Брались ткани кожи груди. После разделения дермальной и эпидермальной частей дерму нарезают на небольшие кусочки 0,2×0,2 мм и фиксируют на культуральной 6 см чашке с сывороткой. Минимальную эссенциальную среду Дульбекко (DMEM, 10% фетальная телячья сыворотка) добавляют после 2-4 часов. Эту культуру эксплантата инкубируют затем до тех пор, пока не становится видимым избыточный рост фибробластов. Культуры конфлюэнтных фибробластов отделяют и размножают для получения замороженных резервных культур.
Культуральные камеры засевают первичными клетками, покрываемыми непрерывно "коктейлем" (смесью) покрытия, описанным ранее для бронхиальных клеток (Lechner et al., J.Tiss. Cult. Meth., 9:43-49 (1985)). После достижения почти полной конфлюэнтности, например, приблизительно 90% конфлюэнтности, которая обычно имеет место после примерно 10-14 дней, кератиноциты и меланоциты разделяют. Для этой цели культуру обрабатывают раствором трипсин/ЭДТА (0,025%/0,01%) в течение 5 минут и затем собирают меланоциты, которые отделяются сначала сами от кератиноцитов. Затем первичные кератиноциты культивируют до желаемого числа клеток в среде NR-3 без сыворотки, с использованием описанных имеющих покрытие культуральных камер (среда NR-3 благоприятствует преимущественному росту кератиноцитов в сравнении с меланоцитами).
Затем клетки для инкапсулирования "ЗТЗ-фибробласты упаковочной клеточной линии" трансфицируют плазмидами pLXSHD+SV40(#328) и pLXSHD+Е6/Е7 в соответствии с протоколом Pfeifer et al. (Meth. Cell Sci., 17, 83-89, 1995) с условием, что вирус собирают после инкапсулирования его в клеточной линии, которая растет в среде DMEM с 10% фетальной телячьей сывороткой. Затем кератиноциты инфицируются этим вирусом, чтобы вызвать иммортализацию. Во время инфицирования используют также среду без сыворотки РС-1, которая описана Pfeifer et al.
После иммортализации имморталиэованные кератиноциты переносят в среду для пролиферации NR-2 или NR-3 с использованием предварительно покрытых покрытием культуральных камер. После пролиферации клеток до желаемого числа клеток эти клетки переносят в среду для дифференцировки, пригодную для культуры нормальных и иммортализованных кератиноцитов (NR-2).
Можно показать, что иммортализованные кератиноциты проявляют улучшенный рост клеток при увеличенном числе пассажей в культуре, который может быть сравнимым с ростом, описанным для клеточных линий в ЕР 780496.
Экспрессию CYP450, 1А1, 1А2, 3А5, 2Е1, 2В6, 2А6 и 2D6 анализируют в кожных клетках, состоящих их нормальных и иммортализованных кератиноцитов, при помощи ДНК-полимеразной цепной реакции при комнатной температуре (экспрессии мРНК). Профиль CYP450, экспрессируемсго иммортализованными кератиноцитами, является, в частности, сходным, даже идентичным, с профилем нормальных кератиноцитов.
Эти клеточные линии реагируют на индуцирующий агент CYP450, состоящий из бенз(а)пирена, таким же образом, каким реагируют неиммортализованные клетки, даже при увеличенном числе пассажей.
Маркеры дифференцировки анализируют с использованием специфических антител против Т-антигена (Т-Аg), инволукрина, филаггрина, лорикрина, виментина и кератинов К4, К7, К8, К10/1, К13, К14, К17, К18 и К19. Наилучшая способность для демонстрации способности дифференцировки могла быть продемонстрирована для клеточной линии DK7-NR.
Глутатион-S-трансферазу (GST) анализируют при помощи Вестерн-блота и Нозерн-блота. Все линии кератиноцитов экспрессируют в сильной степени информационную РНК (мРНК) для gstπ. Профиль экспозиции с GSTα, GSTμ и gstπ в этих клеточных линиях сходен с профилем нормальных кератиноцитов.
Для анализа и сравнения нарушения насыщенности и элонгации добавляемых к кератиноцитам AGE иммортализованные кератиноциты обрабатывают линолевой кислотой (LA, 15 мкмоль) и линоленовой кислотой (LN, 15 мкмоль). Для этих экспериментов используют среду NR-2 (Biofluids Inc.), недостаточную по AEG. Культуры клеток обрабатывают после достижения конфлюэнтности и переносят из этой среды в среду NR-2, имеющую высокое содержание кальция (1,5 мМ). Клетки обрабатывают в течение 4 дней AGE (обновляемыми после 2 дней). Анализ этих AGE выполняют посредством экстракции и отделения фосфолипидов при помощи ТСХ (тонкослойной хроматографии), а определения количества метиловых эфиров этих жирных кислот выполняют при помощи ГЖХ (газожидкостной хроматографии). Можно было показать появление снижения насыщенности и элонгации линолевой кислоты (20:4n-6 и 22:4n-6) и линоленовой кислоты (20:5n-3, 22:5n-3 и 22:6n-3). Метаболический профиль согласовался с профилем, наблюдаемым с нормальными кератиноцитами.
Все клеточные линии были гиподиплоидными с наибольшими числами хромосом в интервале диплоидных клеток. Кроме анализируемых клеток, никакие другие клетки не обнаруживались в этих культурах. Этот результат подтверждает чистоту клеточных линий и отсутствие какого-либо загрязнения, происходящего из других источников.
Онкогенность иммортализованных кератиноцитов определяют подкожной инъекцией (1-2×106 кератиноцитов) "голым" мышам. Линии испытанных кератиноцитов и, в частности, линия DK-7-NR, не были онкогенными для "голой" мыши.
Пример 2: Получение эпителия
Готовят среду NR-2, содержащую 750000 клеток клеточной линии, в соответствии с примером 1, 0,5 мл этой среды помещают во вкладыши Falcon No.3180, их помещают в лунки чашек Falcon No.3043, уже содержащие 2 мл свежей среды NR-2, кератиноциты культивируют в течение 2 дней в условиях, благоприятных для роста кератиноцитов. На третий день среду, содержащуюся во вкладыше, удаляют и клетки оставляют на свободном воздухе. Среду, содержащуюся в лунках, периодически заменяют каждые 2 дня средой NR-2, дополненной EGF (5 нг/мл), витамином С (38 мкг/мл) и СаСl2 (1,5 мМ). После 2-3 недель в культуре в интерфазе воздух-жидкость образовавшийся таким образом эпителий собирают, фиксируют пикриновой кислотой и анализируют морфологию.
Результаты показывают, что клеточная линия кератиноцитов, в частности клеточная линия DK7-NR, образуют слоистый и поляризованный эпителий, обычно называемый stratum basale (основным слоем), содержащий клетки, имеющие кубоидную морфологию, идентичную морфологии нормальных клеток. Ороговевший слой stratum corneum обнаруживает морфологию орто-кератиноцитов, которые не содержат клеток, содержащих ядро. Образование клеточного слоя орто-кератиноцитов не было возможно с другими известными иммортализованными клеточными линиями до сих пор. Например, при идентичных условиях линия DK2-NR (ЕР 780496) образует слой stratum corneum, состоящий из пара-кератиноцитов, который представляет собой слой орговевших клеток, все еще содержащих клетки с ядром. Только морфология орто-кератиноцитов stratum corneum отражает нормальную ситуацию кожи человека. Фактически орговевший слой (stratum corneum), состоящий из паракератиноцитов, характеризуется аномальной гипертрофией эпителия, приводящей к расстройствам, таким как, например, псориаз или неоплазия.
Пример 3: Тест раздражения
Клеточные линии, полученные в примере 1, в частности, линию DK7-NR, культивируют в среде NR-2. Индукцию "гена стресса" TNFα (фактора некроза опухоли альфа) после обработки кожи раздражающим агентом, состоящим из РМА (форбол-12-миристат-13-ацетата) и UV-B (радиации УФ-В), анализируют по способу Нозерн-блоттинга и при помощи биологических тестов. Результаты показывают, что эти клеточные линии и особенно клеточная линия DK7-NR, отвечают на РМД и на UV-B и экспрессируют белок TNFα, даже после увеличенного числа пассажей.
Пример 4: Конструирование искусственной кожи
Мембрану вкладыша Falcon No.3180 заменяют слоем бензилового эфира гиалуроновой кислоты (Hyaff 11). Дно вкладыша засевают первичными фибропластами человека (0,1×106 клеток в 0,2 мл среды), после 30 минут ответной реакции вкладыш заполняют средой DMEM, содержащей 10% фетальную телячью сыворотку, инкубирование проводят при 37°С в атмосфере, содержащей 5% диоксид углерода, в течение нескольких дней, вкладыш опустошают и подают 0,5 мл свежей среды NR-2, содержащей 750000 клеток клеточной линии DK7-NR, вкладыши помещают в лунки чашек Falcon No.3043, уже содержащие 2 мл свежей среды NR-2, и клетки культивируют в течение 2 дней в условиях, благоприятных для роста кератиноцитов. На третий день среду, содержащуюся во вкладыше, удаляют и клетки оставляют на воздухе. Среду в лунках заменяют периодически каждые 2 дня средой NR-2, дополненной EGF (5 нг/мл), витамином С (38 мкг/мл) и CaCl2 (1,5 мМ). После 2-3 недель культивирования в интерфазе воздух-жидкость можно наблюдать образование искусственной кожи, проявляющей характеристики нормальной кожи.
1. Клеточная линия кератиноцитов человека, иммортализованная при помощи pLXSHD+SV40(#328) и pLXSHD+E6/Е7, используемая для иммунологических, фармакологических, фото- и химико-токсикологических анализов кожной реакции и для экспрессии гетерологичных генов, отличающаяся тем, что она (1) является неонкогенной; (2) сохраняет способность дифференцироваться и экспрессировать белки и ферменты, экспрессируемые нормальными дифференцированными кератиноцитами, даже после увеличенного числа пассажей в культуре и (3) образует слоистый и поляризованный эпителий, имеющий состоящий из ортокератиноцитов ороговевший слой (stratum corneum), при культивировании в органотипической культуре в бессывороточной среде и без слоя питающих клеток.
2. Клеточная линия по п.1, используемая для получения искусственной кожи.
3. Клеточная линия иммортализованных кератиноцитов человека DK7-NR (CNCM I-1996), используемая для иммунологических, фармакологических, фото- и химико-токсикологических анализов кожной реакции и для экспрессии гетерологичных генов.
4. Клеточная линия по п.3, используемая для получения искусственной кожи.
5. Способ иммортализации клеток кожи человека для получения клеточной линии по п.1, включающий следующие стадии:
(i) выделение пробы кожи человека;
(ii) подготовка этой пробы кожи для культуры in vitro;
(iii) получение кератиноцитов из этой приготовленной пробы кожи человека и засев бессывороточной среды для выращивания указанными кератиноцитами на культуральных чашках, обеспеченных покрытием, содержащим фибронектин, коллаген типа I и BSA, которые облегчают прикрепление и рост клеток;
(iv) замена бессывороточной среды достаточным для получения оптимального конфлюэнтного роста клеток в культуре образом с непрерывным поддержанием покрытия чашки;
(v) перенос кератиноцитов в селективную бессывороточную среду на культуральных чашках, предварительно покрытых таким же образом;
(vi) инфицирование кератиноцитов с использованием функциональных опухолевых генов двух различных ДНК-вирусов;
(vii) перенос полученных иммортализованных кератиноцитов в среду для пролиферации, пригодную для пролиферации иммортализованных кератиноцитов, на культуральных чашках, покрытых таким же образом; и
(viii) перенос полученных пролиферировавших кератиноцитов в среду для дифференцировки, имеющую высокое содержание кальция, на культуральных камерах, покрытых таким же образом, отличающийся тем, что инфицирование производится двумя ретровирусными конструкциями, представляющими собой векторы pLXSHD+SV40(#328) и pLXSHD+E6/Е7.
6. Способ по п.5, отличающийся тем, что бессывороточной средой на стадиях (iii), (v) или (vii) является среда NR-3.
7. Способ по п.5, отличающийся тем, что средой для дифференцировки на стадии (viii) является модифицированная среда NR-2, имеющая содержание кальция по меньшей мере 1,5 мМ.