Способ получения (r)-5-(2-бензолсульфонилэтил)-3-n-метилпирролидин-2-илметил)-1н- индола
Иллюстрации
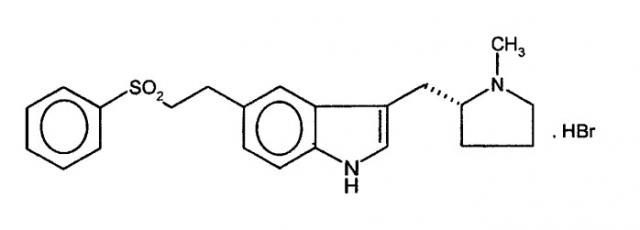
Показать всеИзобретение относится к усовершенствованному способу получения (R)-5-(2-бензолсульфонилэтил)-3-Н-метилпирролидин-2-илметил)-1Н-индола формулы (I)
или его фармацевтически приемлемой соли, который включает гидролиз соединения формулы (II)
При этом соединение формулы II получают каталитическим восстановлением соединения формулы (III)
Заявленный способ исключает образование димера в целевом продукте, используемом в медицине. 2 н. и 16 з.п. ф-лы.
Реферат
Изобретение относится к улучшенному способу получения лекарственного средства против мигрени, (R)-5-(2-бензолсульфонилэтил)-3-N-метилпирролидин-2-илметил)-1Н-индола (элетриптана), коммерчески доступного в виде гидробромидной соли:
и к получаемым при этом промежуточным продуктам, не содержащим димера.
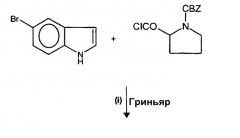
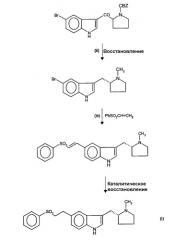
В европейском патенте № 0592438 описано получение элетриптана каталитическим восстановлением (R)-5-(2-бензолсульфонилэтенил)-3-(N-метилпирролидин-2-илметил)-1Н-индола, который получают (i) реакцией хлорангидрида N-бензилоксикарбонил-D-пролина 5-броминдолом в присутствии реактива Гриньяра, (ii) восстановлением полученного (R)-3-(N-бензилоксикарбонилпирролидин-2-илкарбонил)-5-бром-1Н-индола с образованием (R)-5-бром-3-(N-метилпирролидин-2-илметил)-1Н-индола и (iii) реакцией последнего с фенилвинилсульфоном в присутствии палладиевого катализатора, триарилфосфина и основания.
Полная последовательность реакций может быть представлена следующим образом:
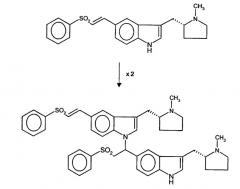
Хотя вышеупомянутая последовательность реакций дает элетриптан формулы (I) с приемлемым выходом, было обнаружено, что предшественник (R)-5-(2-бензолсульфонилэтенил)-3-(N-метилпирролидин-2-илметил)-1Н-индол склонен димеризоваться при попытках перекристаллизации в неочищенной форме и/или при сушке перед каталитическим восстановлением:
Не только образование указанной димерной примеси снижает выход элетриптана, но, возможно, что более важно, требуется дорогое и долговременное удаление указанного димера для получения достаточно чистой гидробромидной соли, чтобы удовлетворять строгим стандартам, требующимся для маркетингового одобрения.
Как следствие указанной трудности, разработан альтернативный путь получения элетриптана, который позволяет избежать применения предшественника, который склонен к димеризации. Конкретно, способ изобретения включает получение элетриптана гидролизом (R)-1-ацетил-5-(2-бензолсульфонилэтил)-3-(N-метилпирролидин-2-илметил)-1Н-индола, который может быть удобно получен (i) N-ацетилированием (R)-5-бром-3-(N-метилпирролидин-2-илметил)-1Н-индола, (ii) реакцией полученого (R)-1-ацетил-5-бром-3-(N-метилпирролидин-2-илметил)-1Н-индола с фенилвинилсульфоном в присутствии палладиевого катализатора, триарилфосфина и основания с образованием (R)-1-ацетил-5-(бензолсульфонилэтенил)-3-(N-метилпирролидин-2-илметил)-1Н-индола и (iii) каталитическим восстановлением последнего.
Полная последовательность реакций может быть представлена следующим образом:
При использовании указанного способа можно избежать образования нежелательного димера и при этом получить элетриптан с высокой степенью чистоты с хорошим выходом без последующих дорогостоящих и долговременных стадий очистки, необходимых для удаления примеси димера.
Так, в соответствии с данным изобретением предложен способ получения соединения формулы (I), который включает гидролиз соединения формулы (II), обычно в основных условиях, более конкретно карбонатом калия в смеси метанол/вода.
Согласно другому аспекту изобретения соединение формулы (II), используемое в способе, может быть получено каталитическим восстановлением соединения формулы (III), обычно с применением водорода или источника водорода в присутствии подходящего катализатора. Восстановление обычно проводят с применением водорода под давлением от 1 до 15 атмосфер или с использованием источника водорода, такого как формиат аммония или муравьиная кислота. Подходящие катализаторы включают палладий на угле, например 5% мас./мас. Pd/C, никель Ренея, оксид платины, родий или рутений. Восстановление обычно проводят в присутствии кислоты, например, метансульфоновой кислоты, уксусной кислоты или трифторуксусной кислоты. Полученное таким образом соединение формулы (II) удобно суспендировать в холодном водном тетрагидрофуране перед гидролизом до соединения формулы (I). Изобретение предлагает непосредственно вышеупомянутое соединение формулы (II), которое до сих пор не было описано.
Согласно другому аспекту изобретения соединение формулы (III), использованное в способе, может быть получено обработкой соединения формулы (IV) фенилвинилсульфоном в присутствии палладиевого катализатора, триарилфосфина и основания в соответствии со способом, описанным в примере 57 патента США 5607951.
Согласно дополнительному аспекту изобретения соединение формулы (IV), использованное в способе, может быть получено N-ацетилированием (R)-5-бром-3-(N-метилпирролидин-2-илметил)-1Н-индола, также в соответствии со способом, описанным в примере 57 вышеупомянутого патента США № 5607951.
Полученный по способу изобретения элетриптан может быть превращен в фармацевтически приемлемую кислотно-аддитивную соль обработкой соответствующей кислотой; указанное превращение может быть проведено in situ без выделения соединения формулы (I). В частности, предпочтительной солью является гидробромид, полученный обработкой бромистоводородной кислотой.
Таким образом, согласно данному изобретению предложен свободный от димера элетриптан и его фармацевтически приемлемые соли, в частности, гидробромид, и содержащие их фармацевтические композиции.
ПРИМЕРЫ
Способ изобретения может быть проиллюстрирован следующим примером получения (R)-5-(2-бензолсульфонилэтил)-3-N-метилпирролидин-2-илметил)-1Н-индола (I) и его бромистоводородной соли:
(а) Получение (R)-1-ацетил-5-(2-бензолсульфонилэтил)-3-(N-метилпирролидин-2-илметил)-1Н-индола (II)
К раствору соединения формулы (III) (200 г), полученному по способу, описанному в примере 57 вышеупомянутого патента США № 5607951, в ацетоне (2,0 л) добавляли воду (0,5 л). Добавляли по каплям метансульфоновую кислоту (43,2 г, 0,95 экв.) и полученный раствор перемешивали 5 минут перед добавлением катализатора 5% мас./мас. Pd/C (89,0 г, Johmson Mattey тип 58, 50% влажности). Раствор гидрировали при комнатной температуре и 200 фунт/кв.дюйм водорода в течение 18 часов.
Катализатор удаляли фильтрованием и фильтрат упаривали с образованием свободной от ацетона суспензии. К последней прибавляли по каплям 40% водный NaOH (30 мл) и затем воду (1,5 л). Полученную суспензию перемешивали 20 минут и дополнительно прибавляли 40% водный NaOH (20 мл). После гранулирования в течение 2 часов при активном перемешивании суспензию фильтровали и отсасывали досуха в течение 30 минут с образованием бежевого влажного твердого вещества, которое либо
(i) сушили при 45°С, получая желаемый продукт (193,0 г, выход 95%), или
(ii) обрабатывали в тетрагидрофуране (1,6 л), к которому добавляли воду (всего 1,5 л) в течение 10 минут. Полученную суспензию активно перемешивали 18 часов, фильтровали и отсасывали досуха в течение 30 минут, получая желаемый продукт в виде бежевого влажного твердого вещества (скорректированная масса 129,0 г, выход 67%).
Любая форма может быть использована непосредственно на стадии (b):
(b) Получение (R)-5-(2-бензолсульфонилэтил)-3-N-метилпирролидин-2-илметил)-1Н-индолa (I)
К раствору соединения формулы (II) (95,9 г) со стадии (а)(i) или (ii) в ацетоне (1 л) и метаноле (0,1 л) добавляли К2СО3 (46,8 г, 1,5 экв.) и полученную смесь перемешивали 24 часа. К последней прибавляли древесный уголь (50 г) и затем через один час безводный MgSO4 (300 г). Полученную суспензию перемешивали в течение 1 часа и фильтровали. Фильтрат упаривали, получая влажное твердое вещество, которое сушили в вакууме при 45°С, получая желаемый продукт (79,3 г, 91,8%).
В случае, если соединение формулы (I) должно быть превращено в фармацевтически приемлемую кислотно-аддитивную соль, выделения соединения формулы (I) можно избежать обработкой раствора, полученного при гидролизе, соответствующей кислотой, например, бромистоводородной кислотой, с образованием бромистоводородной соли.
(с) Получение (R)-5-(2-бензолсульфонилэтил)-3-N-метилпирролидин-2-илметил-1Н-индола (I) и его гидробромирование in situ
К раствору соединения формулы (II) (95,9 г) со стадии (а)(i) или (ii) в ацетоне (1 л) и метаноле (0,1 л) добавляли К2СО3 (46,8 г, 1,5 экв.) и полученную смесь перемешивали в течение 24 часов. К последней прибавляли древесный уголь (50 г) и затем через один час безводный MgSO4 (300 г). Полученную суспензию перемешивали в течение 1 часа и фильтровали.
Фильтрат частично концентрировали азеотропной перегонкой для удаления метанола и объем доводили ацетоном до 0,45 л. Добавляли по каплям раствор 48%-ной (масса/объем) HBr (33,2 г, 0,95 экв.) в ацетоне (50 мл) и полученную суспензию перемешивали в течение 72 часов. Последнюю фильтровали, отсасывали досуха в течение 30 минут и сушили в вакууме при 45°С, получая желаемый продукт в виде светло-бежевых кристаллов (71,8 г, 68,5%).
В предпочтительном выполнении изобретения некоторые стадии могут быть "телескопированы" (сокращены), чтобы уменьшить ручную обработку и сократить время процесса. Например, как показано на стадии (а)(ii), можно исключить сушку соединения формулы (II) перед гидролизом путем использования влажного материала, суспендированного в водном тетрагидрофуране. Аналогично, как показано на стадии (с), можно избежать выделения соединения формулы (I) до превращения в соль путем образования соли in situ.
1. Способ получения (R)-5-(2-бензолсульфонилэтил)-3-N-метилпирролидин-2-илметил)-1Н-индола формулы (I)
или его фармацевтически приемлемой соли, который включает гидролиз соединения формулы (II)
где полученное соединение формулы (I), в случае необходимости, превращают в фармацевтически приемлемую соль.
2. Способ по п.1, который проводят в основных условиях.
3. Способ по п.2, где указанный гидролиз проводят с применением карбоната калия в смеси метанол/вода.
4. Способ по любому из пп.1-3, где соединение формулы (II) получают каталитическим восстановлением соединения формулы (III)
5. Способ по п.4, где указанное восстановление проводят с применением водорода или источника водорода в присутствии подходящего катализатора.
6. Способ по п.5, где указанное восстановление проводят с применением водорода при давлении 1 - 15 атмосфер.
7. Способ по п.5, где указанное восстановление проводят с применением источника водорода, которым является формиат аммония или муравьиная кислота.
8. Способ по любому из пп.4-7, где указанным катализатором является палладий на угле, никель Ренея, оксид платины, родий или рутений.
9. Способ по п.8, где указанным катализатором является 5% мас./мас. палладий на угле.
10. Способ по любому из пп.4-9, где каталитическое восстановление проводят в присутствии кислоты.
11. Способ по п.10, где указанной кислотой является метансульфоновая кислота, уксусная кислота или трифторуксусная кислота.
12. Способ по любому из пп.4-11, где соединение формулы (II), полученное каталитическим восстановлением, суспендируют с холодным водным тетрагидрофураном перед гидролизом до соединения формулы (I).
13. Способ по любому из пп.4-12, где соединение формулы (III) получено обработкой соединения формулы (IV)
фенилвинилсульфоном в присутствии палладиевого катализатора, триарилфосфина и основания.
14. Способ по п.13, где соединение формулы (IV) получено N-ацетилированием (R)-5-бром-3-(N-метилпирролидин-2-илметил)-1Н-индола.
15. Способ по любому из пп.1-14, где полученное соединение формулы (I) превращают в фармацевтически приемлемую кислотно-аддитивную соль обработкой соответствующей кислотой.
16. Способ по п.15, где указанное превращение проводят in situ без выделения соединения формулы (I).
17. Способ по п.15 или 16, где кислотой является бромистоводородная кислота и получаемый солью гидробромид.
18. Соединение формулы (II):