Замещенные индольные основания манниха
Иллюстрации
Показать всеИзобретение относится к новым замещенным индольным основаниям Манниха формулы I
где R1 обозначает Н, С1-С10алкил, связанный через С1-С2алкиленовую группу незамещенный или по меньшей мере однозамещенный ОН, галогеном, CF3, CN, С1-С6алкилом, С1-С6алкоксигруппой фенил или нафтил;
R2 обозначает Н, F, Cl, Br, CF3, CN, OR10, CO(OR11), CH2CO(OR12), COR19, С1-С10алкил, незамещенный или по меньшей мере однозамещенный ОН, галогеном, CF3, CN, С1-С6алкилом, С1-С6алкоксигруппой фенил или нафтил;
R3 обозначает CH(R13)N(R14)(R15);
R4, R5, R6, R7 могут иметь идентичные либо разные значения и обозначают Н, F, Cl, Br, CF3, CN, NO2, OR10 и другие;
R10 обозначает Н, COR17, С1-С6алкил и другие;
R13 обозначает незамещенный фенил или по меньшей мере однозамещенный С1-С4алкилом, галогеном, CF3, CN, ОН фенил;
R14 и R15 могут иметь идентичные либо разные значения и обозначают разветвленный либо неразветвленный С1-С6алкил или
R14 и R15 вместе представляют собой (СН2)n, где n обозначает целое число от 3 до 6, или (СН2)2O(СН2)2;
R17 обозначает С1-С6алкил;
R19 обозначает NHR20, С1-С6алкил и другие;
R20 обозначает Н, С1-С6алкил и другие,
и/или их рацематам, энантиомерам, диастереомерам и/или соответствующим основаниям и/или соответствующим солям физиологически приемлемых кислот, за исключением рацематов ряда соединений, указанных в п.1. Описаны способы их получения и использования в качестве лекарственного средства, обладающего анальгетическим действием. 4 н. и 38 з.п. ф-лы, 2 ил., 3 табл.
Реферат
Настоящее изобретение относится к замещенным индольным основаниям Манниха, к способам их получения, к лекарственным средствам, содержащим эти соединения, а также к применению этих соединений для получения лекарственных средств.
Боль относится к основным клиническим симптомам. Несмотря на достигнутые успехи, остается актуальной потребность в разработке эффективной терапии болей. Настоятельная необходимость в целенаправленном, с учетом индивидуальных особенностей пациентов лечении хронических и нехронических болезненных состояний, причем имеется в виду успешное и удовлетворительное для пациента обезболивающее лечение, находит свое подтверждение в многочисленных опубликованных в последнее время научных работах в области прикладной анальгетики, соответственно в фундаментальных исследованиях по проблемам ноцицепции.
Классические опиоиды, такие, например, как морфин, эффективны при терапии сильных, в том числе очень сильных, болей. Однако их применение связано с нежелательными побочными действиями, такими, в частности, как депрессия дыхания, рвота, необходимость использовать седативные средства, запоры, а также развитие привыкания.
Особое место среди высокоэффективных анальгетиков занимает трамадола гидрохлорид, т.е. (1RS, 2R8)-2-[(диметиламино)метил]-1-(3-метоксифенил)циклогексанол, поскольку это активное вещество обладает выраженной способностью подавлять боль, не вызывая при этом известных побочных действий, присущих опиоидам (Journ. Pharmacol. Exptl. Ther. 267, стр. 33 (1993)). Поиски и разработка других подавляющих боль средств продолжаются повсеместно.
С учетом вышеизложенного в основу настоящего изобретения была положена задача получить новые соединения, пригодные прежде всего для применения в качестве активных веществ в соответствующих лекарственных средствах. При этом предусматривалось, что эти активные вещества должны предназначаться прежде всего для терапии болей и для лечения воспалительных и аллергических реакций, нарко- и/или алкогольной зависимости, диареи, гастрита, различных язв, сердечно-сосудистых заболеваний, недержания мочи, депрессий, шоковых состояний, мигреней, нарколепсии, избыточного веса, астмы, глаукомы, гипокинетического синдрома, болезненного безразличия (апатии), булимии, анорексии, каталепсии, для подавления чувства беспокойства и страха (анксиолиза), для повышения ясности сознания и/или для усиления либидо.
Указанная задача решается согласно изобретению благодаря замещенным индольным основаниям Манниха нижеприведенной общей формулы I, которые обладают выраженным анальгетическим действием, прежде всего и при хронических болях, и которые, кроме того, могут применяться для лечения воспалительных и аллергических реакций, нарко- и/или алкогольной зависимости, диареи, гастрита, различных язв, сердечно-сосудистых заболеваний, недержания мочи, депрессий, шоковых состояний, мигреней, нарколепсии, избыточного веса, астмы, глаукомы, гипокинетического синдрома, болезненного безразличия (апатии), булимии, анорексии, каталепсии, для подавления чувства беспокойства и страха (анксиолиза), для повышения ясности сознания и/или для усиления либидо.
Объектом изобретения в соответствии с этим являются замещенные индольные основания Манниха общей формулы I
в которой R1 обозначает Н, C1-С10алкил или связанный через C1-С6алкиленовую группу арил либо гетероарил, предпочтительно Н, C1-С6алкил или связанный через C1-С2алкиленовую группу арил, особенно предпочтительно Н или C1-С2алкил,
R2 обозначает Н, F, Cl, Br, CF3, CN, NO2, NHR8, SR9, OR10, SO2NH2, SO2NHR21, CO(OR11), CH2CO(OR12), COR19, C1-С10алкил, арил, гетероарил либо связанный через C1-С6алкиленовую группу арил или гетероарил, предпочтительно Н, Cl, F, NO2, OR10, CO(OR11), C1-С6алкил либо связанный через C1-С2алкиленовую группу арил, особенно предпочтительно Н, C1-С2алкил или незамещенный фенил,
R3 обозначает CH(R13)N(R14)(R15),
R4, R5, R6, R7 могут иметь идентичные либо разные значения и обозначают Н, F, Cl, Br, CF3, CN, NO2, NHR8, SR9, OR10, SO2NH2, SO2NHR21, CO(OR11), CH2CO(OR12), COR19, C1-С10алкил, арил, гетероарил либо связанный через C1-С6алкиленовую группу арил или гетероарил, предпочтительно Н, Cl, F, NO2, OR10, CO(OR11), арил, C1-С6алкил либо связанный через C1-С2алкиленовую группу арил, особенно предпочтительно Н, NO2, C1-С2алкил или незамещенный фенил,
R8 обозначает Н, COR16, C1-С10алкил или арил, предпочтительно C1-С6алкил,
R9 обозначает Н, C1-С10алкил или арил, предпочтительно C1-С6алкил или фенил,
R10 обозначает Н, COR17, C1-С10алкил, арил либо связанный через C1-С6алкиленовую группу арил или гетероарил, предпочтительно Н, C1-С6алкил либо связанный через C1-С2алкиленовую группу арил,
R11 обозначает Н, C1-С10алкил или арил, предпочтительно Н или C1-С6алкил,
R12 обозначает Н, C1-С10алкил или арил, предпочтительно C1-С6алкил,
R13 обозначает незамещенный фенил либо по меньшей мере однозамещенный C1-С4алкилом, C1-С3алкоксигруппой, галогеном, CF3, CN, O-фенилом или ОН фенил, предпочтительно незамещенный фенил либо по меньшей мере однозамещенный метилом, трет-бутилом, метоксигруппой, F, Cl, Br или CF3 фенил, особенно предпочтительно незамещенный фенил или 2-метоксифенил, 3-метоксифенил, 4-метоксифенил, 2-метилфенил, 3-метилфенил, 4-метилфенил, 2-трет-бутилфенил, 3-трет-бутилфенил, 4-трет-бутилфенил, 2-фторфенил, 3-фторфенил, 4-фторфенил, 2-хлорфенил, 3-хлорфенил, 4-хлорфенил, 2-бромфенил, 3-бромфенил, 4-бромфенил, 5-бром-2-фторфенил, 2-хлор-4-фторфенил, 2-хлор-5-фторфенил, 2-хлор-6-фторфенил, 4-бром-2-фторфенил, 3-бром-4-фторфенил, 3-бром-2-фторфенил, 2,3-дихлорфенил, 2,4-дихлорфенил, 2,5-дихлорфенил, 3,4-дихлорфенил, 2,3-диметилфенил, 2,4-диметилфенил, 2,5-диметилфенил, 2,3-диметоксифенил, 2,4-диметоксифенил, 2,5-диметоксифенил, 3,4-диметоксифенил, 3,4,5-триметоксифенил, 2-трифторметилфенил, 3-трифторметилфенил или 4-трифторметилфенил, наиболее предпочтительно незамещенный фенил,
R14, R15 могут иметь идентичные либо разные значения и обозначают неразветвленный либо разветвленный, насыщенный либо ненасыщенный, незамещенный либо по меньшей мере однозамещенный C1-С6алкил или незамещенный либо по меньшей мере однозамещенный фенил, бензил или фенетил, предпочтительно насыщенный, незамещенный либо по меньшей мере однозамещенный C1-С6алкил, особенно предпочтительно СН3, или
R14, R15 оба вместе представляют собой (СН2)n, где n обозначает целое число от 3 до 6, или (СН2)2O(СН2)2, предпочтительно (СН2)n, где n обозначает 4 или 5,
R16 обозначает C1-С10алкил, арил или гетероарил, предпочтительно C1-С6алкил,
R17 обозначает C1-С10алкил, предпочтительно C1-С6алкил,
R18 обозначает C1-С10алкил, арил, гетероарил или нафтил, предпочтительно C1-С6алкил,
R19 обозначает Н, NHNH2, NHR20, C1-С10алкил, арил, гетероарил или связанный через C1-С6алкиленовую группу арил либо гетероарил, предпочтительно C1-С6алкил или связанный через C1-С2алкиленовую группу арил,
R20 обозначает Н, C1-С10алкил, арил, гетероарил либо связанный через C1-С6алкиленовую группу арил или гетероарил, предпочтительно C1-С6алкил или связанный через C1-С2алкиленовую группу арил,
R21 обозначает Н, COR17, C1-С10алкил, арил либо связанный через C1-С6алкиленовую группу арил или гетероарил, предпочтительно Н, C1-С6алкил либо связанный через C1-С2алкиленовую группу арил,
и/или их рацематы, энантиомеры, диастереомеры и/или соответствующие основания и/или соответствующие соли физиологически приемлемых кислот, за исключением рацематов соединений, в которых R3 обозначает CH(R13)N(R14)(R15) и соответственно R4-R7 и R2 обозначают Н, R13 обозначает фенил, R14 и R15 вместе обозначают (СН2)5 и R1 обозначает Н, СН3 или бензил или
R4-R7 и R2 обозначают Н, R13 обозначает фенил, R14, R15 каждый обозначает СН3 и R1 обозначает Н, СН3 или бензил или
R4-R7 и R1 обозначают Н, R13 обозначает 2-хлорфенил, R14 и R15 каждый обозначает СН3 или R14 и R15 вместе представляют собой (СН2)2O(СН2)2, R2 обозначает COOR11 и R11 обозначает C2H5, а также соответствующие гидрохлориды или
R4-R7 и R1 обозначают Н, R13 обозначает фенил, R14 и R15 вместе представляют собой (СН2)5, R2 обозначает COOR11 и R11 обозначает СН3 в виде гидрохлорида или
R4-R7 и R2 обозначают Н, R13 обозначает фенил, R14 и R15 вместе представляют собой (CH2)4, R1 обозначает Н, СН3, СН2-СН=СН2 или 4-хлорбензил и при значении R1СН3 также соответствующий гидрохлорид соединения или
R4-R7, R1 и R2 обозначают Н, R13 обозначает фенил, R14 обозначает фенил и R15 обозначает 4-этоксифенил или
R4-R7 обозначают Н, R13 обозначает 2,4,6-триметоксифенил, R14 и R15 вместе представляют собой (CH2)2O(CH2)2, R1 обозначает СН3 и R2 обозначает фенил или
R4-R7 и R1 обозначают Н, R13 обозначает фенил, 2-гидроксифенил или 2-гидрокси-5-метилфенил, R14 и R15 вместе представляют собой (СН2)5 и R2 обозначает СН3, а при значении R13 фенил также соответствующий гидросульфат или
R4-R7 и R1 обозначают Н, R13 обозначает фенил, R14 и R15 вместе представляют собой (СН2)2O(СН2)2 и R2 обозначает СН3, а также соответствующий гидросульфат соединения или
R4-R7 и R1 обозначают Н, R13 обозначает фенил, R14 и R15 вместе представляют собой (СН2)5, R2 обозначает COOR11 и R11 обозначает СН3 в виде гидрохлорида или
R1, R4, R6, R7 обозначают Н, R2 обозначает COOR11, R11 обозначает С2Н5, R14 и R15 каждый обозначает СН3, R13 обозначает 2-хлорфенил и R5 обозначает этиловый эфир 3-[(2-хлорфенил)диметиламинометил]-5-метилен-1Н-индол-2-карбоновой кислоты или этиловый эфир 3-[(2-хлорфенил)диметиламинометил]-5-гидроксат-1Н-индол-2-карбоновой кислоты.
Под алкильными радикалами имеются в виду предпочтительно по меньшей мере однозамещенные галогеном, ОН, CN, CF3, особенно предпочтительно F, Cl, Br или ОН, углеводороды. Если алкильные радикалы содержат более одного заместителя, то эти заместители могут быть идентичными или разными. Алкильные радикалы могут быть разветвленными, неразветвленными или циклическими. Особенно предпочтительны в качестве алкильных радикалов метил, этил, пропил, 1-метилэтил, бутил, 1-метилпропил, 2-метилпропил, 1,1-диметилпропил, 1,2-диметилпропил, 2,2-диметилпропил, гексил, 1-метилпентил, гептил, нонил или деканил.
Под арильными радикалами имеются в виду предпочтительно по меньшей мере однозамещенные ОН, галогеном, предпочтительно F, Cl либо Br, CF3, CN, C1-С6алкилом, C1-С6алкоксигруппой либо фенилом фенил или нафтил. Незамещенные или замещенные фенильные радикалы могут быть сконденсированы также с другими кольцами. К предпочтительным арильным радикалам относятся 2-, 3-, 4-бромфенил, 4-бром-2-фторфенил, 5-бром-2-фторфенил, 3-бром-4-фторфенил, 4-трет-бутилфенил, 2-хлор-4-фторфенил, 2-хлор-6-фторфенил, 4-цианофенил, 2,3-дихлорфенил, 2,4-дихлорфенил, 2,6-дихлорфенил, 3,4-дихлорфенил, 2,3-диметоксифенил, 3,4-диметоксифенил, 2,4-диметилфенил, 2,5-диметилфенил, 2-, 3-, 4-фторфенил, 2-метоксифенил, 2-, 3-, 4-метилфенил, 3-феноксифенил, 2-, 4-трифторметилфенил или 3,4,5-триметоксифенил.
Под гетероарильными радикалами имеются в виду ароматические соединения, которые содержат по меньшей мере один гетероатом, предпочтительно азот и/или кислород и/или серу, особенно предпочтительно азот и/или кислород, и которые предпочтительно могут быть замещены галогеном, CN, CF3 или ОН. Наиболее предпочтительным гетероарильным радикалом является замещенный или незамещенный тиофен, пирролил или фурфурил.
Наиболее предпочтительны следующие замещенные индольные основания Манниха:
этиловый эфир 3-(диметиламинофенилметил)-1Н-индол-2-карбоновой кислоты,
3-(диметиламинофенилметил)-1Н-индол-2-карбоновая кислота,
[(5-фтор-1Н-индол-3-ил)фенилметил]диметиламин,
[(1-этил-2-фенил-1Н-индол-3-ил)фенилметил]диметиламин,
[(5-метокси-1Н-индол-3-ил)фенилметил]диметиламин,
3-(диметиламинофенилметил)-5-гидрокси-1Н-индол-2-карбоновая кислота,
диметил[(2-метил-1Н-индол-3-ил)фенилметил]амин,
3-(диметиламинофенилметил)-1Н-индол-4-ол,
диметил[(4-метил-1Н-индол-3-ил)фенилметил]амин,
[(5-хлор-1Н-индол-3-ил)фенилметил]диметиламин,
[(5-бензилокси-1Н-индол-3-ил)фенилметил]диметиламин,
3-(диметиламинофенилметил)-1Н-индол-4-иловый эфир уксусной кислоты,
{[2-(4-хлорфенил)-1Н-индол-3-ил]фенилметил}диметиламин,
5-бензилокси-3-(диметиламинофенилметил)-1Н-индол-2-карбоновая кислота,
диметил[(2-метил-5-нитро-1Н-индол-3-ил)фенилметил]амин,
диметил[(2-метил-6-нитро-1Н-индол-3-ил)фенилметил]амин,
[(6-фтор-2-метил-1Н-индол-3-ил)фенилметил]диметиламин,
{[2-(4-фторфенил)-1Н-индол-3-ил]фенилметил}диметиламин,
{[2-(3-хлор-4-фторфенил)-1Н-индол-3-ил]фенилметил}диметиламин,
[(7-этил-1Н-индол-3-ил)фенилметил]диметиламин,
3-(диметиламинофенилметил)-1Н-индол-6-карбоновая кислота,
диметил[(1-метил-1Н-индол-3-ил)фенилметил]амин,
1-метил-3-(морфолин-4-илфенилметил)-1Н-индол,
3-[(2-метоксифенил)пирролидин-1-илметил]-1-метил-1Н-индол,
1-этил-2-фенил-3-(пирролидин-1-ил-о-толилметил)-1Н-индол,
3-[(2-хлорфенил)пиперидин-1-илметил]-1-этил-2-фенил-1Н-индол,
1-этил-2-фенил-3-(фенилпирролидин-1-илметил)-1Н-индол,
1-этил-3-[(2-метоксифенил)пирролидин-1-илметил]-2-фенил-1Н-индол,
2-фенил-3-(пирролидин-1-ил-о-толилметил)-1Н-индол,
2-фенил-3-(пиперидин-1-ил-о-толилметил)-1Н-индол,
3-[(2-хлорфенил)пиперидин-1-илметил]-2-фенил-1Н-индол,
диметил[(2-фенил-1Н-индол-3-ил)-о-толилметил]амин,
2-фенил-3-(фенилпирролидин-1-илметил)-1Н-индол,
3-[(2-метоксифенил)пирролидин-1-илметил]-2-фенил-1Н-индол,
4-метил-3-(пиперидин-1-ил-о-толилметил)-1Н-индол,
3-[(2-метоксифенил)пирролидин-1-илметил]-4-метил-1Н-индол,
5-бензилокси-3-(фенилпиперидин-1-илметил)-1Н-индол,
[(5-бензилокси-1Н-индол-3-ил)-о-толилметил]диметиламин,
7-этил-3-[(2-метоксифенил)морфолин-4-илметил]-1Н-индол,
3-[(2-метоксифенил)пиперидин-1-илметил]-2-фенил-1Н-индол,
5-хлор-3-[(2-метоксифенил)пиперидин-1-илметил]-1Н-индол,
5-хлор-3-[(2-метоксифенил)пирролидин-1-илметил]-1Н-индол,
5-бензилокси-3-[(2-метоксифенил)пирролидин-1-илметил]-1Н-индол,
[(2-метоксифенил)-(2-метил-1Н-индол-3-ил)метил]диметиламин,
{[1-(4-метоксибензил)-1Н-индол-3-ил]фенилметил}диметиламин,
3-(фенилпиперидин-1-илметил)-1Н-индол,
1-метил-3-(фенилпиперидин-1-илметил)-1Н-индол,
3 -(фенилпирролидин-1-илметил)-1Н-индол,
[(1Н-индол-3-ил)фенилметил]диметиламин,
5-бензилокси-3-(фенилпирролидин-1-илметил)-1Н-индол,
[(5-бром-2-фторфенил)-(4-нитро-1Н-индол-3-ил)метил]диметиламин,
[(5-бром-2-фторфенил)-(1-метил-1Н-индол-3-ил)метил]диметиламин,
[(2-хлор-6-фторфенил)-(2-фенил-1Н-индол-3-ил)метил]диметиламин,
[(2-хлор-6-фторфенил)-(1-этил-2-фенил-1Н-индол-3-ил)метил]диметиламин,
[(2-хлор-6-фторфенил)-(4-нитро-1Н-индол-3-ил)метил]диметиламин,
[(2-хлор-6-фторфенил)-(1-метил-1Н-индол-3-ил)метил]диметиламин,
[(2-бромфенил)-(4-нитро-1Н-индол-3-ил)метил]диметиламин,
[(2-бромфенил)-(1-метил-1Н-индол-3-ил)метил]диметиламин,
[(3-бромфенил)-(7-этил-1Н-индол-3-ил)метил]диметиламин,
[(3-бромфенил)-(1-метил-1Н-индол-3-ил)метил]диметиламин,
[(4-трет-бутилфенил)-(2-метил-1Н-индол-3-ил)метил]диметиламин,
[(4-трет-бутилфенил)-(1-этил-2-фенил-1Н-индол-3-ил)метил]диметиламин,
[(4-трет-бутилфенил)-(1-метил-1Н-индол-3-ил)метил]диметиламин,
[(2-хлор-4-фторфенил)-(4-нитро-1Н-индол-3-ил)метил]диметиламин,
[(2-хлор-4-фторфенил)-(4-метил-1Н-индол-3-ил)метил]диметиламин,
[(2-хлор-6-фторфенил)-(2-фенил-1Н-индол-3-ил)метил]диметиламин,
{(2-хлор-6-фторфенил)-[2-(4-хлорфенил)-1Н-индол-3-ил]метил}диметиламин,
[(2-хлор-6-фторфенил)-(1-метил-1Н-индол-3-ил)метил]диметиламин,
[(3-хлорфенил)-(1-метил-1Н-индол-3-ил)метил]диметиламин,
[(2,3-дихлорфенил)-(1-метил-1Н-индол-3-ил)метил]диметиламин,
[(2,4-дихлорфенил)-(1-метил-1Н-индол-3-ил)метил]диметиламин,
[(4-трет-бутилфенил)-(1-этил-2-фенил-1Н-индол-3-ил)метил]диметиламин,
[(2-хлор-4-фторфенил)-(2-метил-1Н-индол-3-ил)метил]диметиламин,
[(2-хлор-6-фторфенил)-(2-метил-1Н-индол-3-ил)метил]диметиламин,
[(2,3-диметоксифенил)-(4-нитро-1Н-индол-3-ил)метил]диметиламин,
3-[(2,3-диметоксифенил)диметиламинометил]-4,7-дигидро-1Н-индол-6-карбоновая кислота,
3-[(2,3-диметоксифенил)диметиламинометил]-5-гидрокси-1Н-индол-2-карбоновая кислота,
[(3,4-диметоксифенил)-(2-метил-1Н-индол-3-ил)метил]диметиламин,
[[2-(4-хлорфенил)-1Н-индол-3-ил]-(3,4-диметоксифенил)метил]диметиламин,
[(3,4-диметоксифенил)-(1-этил-2-фенил-1Н-индол-3-ил)метил]диметиламин,
[(3,4-диметоксифенил)-(7-этил-1Н-индол-3-ил)метил]диметиламин,
[(3,4-диметоксифенил)-(1-метил-1Н-индол-3-ил)метил]диметиламин,
[(3,4-диметоксифенил)-[2-(4-фторфенил)-1Н-индол-3-ил]метил]диметиламин,
[[2-(3-хлор-4-фторфенил)-1Н-индол-3-ил]-(3,4-диметоксифенил)метил]диметиламин,
[(5-хлор-1Н-индол-3-ил)-(2-фторфенил)метил]диметиламин,
[(4-фторфенил)-(4-метил-1Н-индол-3-ил)метил]диметиламин,
[(7-этил-1Н-индол-3-ил)-(2-метоксифенил)метил]диметиламин,
диметил[(2-метил-1Н-индол-3-ил)-о-толилметил]амин,
[(7-этил-1Н-индол-3-ил)-о-толилметил]диметиламин,
диметил[(1-метил-1Н-индол-3-ил)-о-толилметил]амин,
[(5-хлор-1Н-индол-3-ил)-о-толилметил]диметиламин,
[(5-хлор-1Н-индол-3-ил)-м-толилметил]диметиламин,
диметил[(2-метил-1Н-индол-3-ил)-n-толилметил]амин,
[(5-хлор-1Н-индол-3-ил)-п-толилметил]диметиламин,
диметил[(2-метил-1Н-индол-3-ил)-(3-феноксифенил)метил]амин,
[(1-этил-2-фенил-1Н-индол-3-ил)-(3-феноксифенил)метил]диметиламин,
[(7-этил-1Н-индол-3-ил)-(3-феноксифенил)метил]диметиламин,
диметил[(1-метил-1Н-индол-3-ил)-(3-феноксифенил)метил]амин,
[[2-(4-фторфенил)-1Н-индол-3-ил]-(3-феноксифенил)метил]диметиламин,
[[2-(3-хлор-4-фторфенил)-1Н-индол-3-ил]-(3-феноксифенил)метил]диметиламин,
диметил[(4-метил-1Н-индол-3-ил)-(3-феноксифенил)метил]амин,
[(5-хлор-1Н-индол-3-ил)-(2-трифторметилфенил)метил]диметиламин,
диметил[(2-метил-1Н-индол-3-ил)-(4-трифторметилфенил)метил]амин.
Еще одним объектом изобретения являются способы получения замещенных индольных оснований Манниха общей формулы I, которые отличаются тем, что ароматические альдегидные соединения общей формулы II
где R13 имеет значения, указанные для общей формулы I,
в растворенном виде, предпочтительно в органическом растворителе, особенно предпочтительно в толуоле, в присутствии основания, предпочтительно карбоната калия или ангидрида борной кислоты, при температуре предпочтительно в интервале от -10 до +110°С подвергают взаимодействию с вторичными аминами общей формулы III
в которых R14 и R15 имеют значения, указанные для общей формулы I,
с получением аминальных соединений общей формулы IV
далее эти аминальные соединения общей формулы IV без последующей очистки под действием соответствующего хлорангидрида кислоты, предпочтительно ацетилхлорида, в абсолютном растворителе, предпочтительно в диэтиловом эфире, превращают в соли иминия общей формулы V
затем эти соли иминия общей формулы V без последующей очистки в растворенном виде, предпочтительно в ацетонитриле и/или толуоле, подвергают взаимодействию с индолом и/или замещенными индольными соединениями общей формулы VI
в которых R3 обозначает Н, a R1, R2, R4-R12 и R16-R21 имеют значения, указанные для общей формулы I,
и полученные таким образом индольные основания Манниха общей формулы I очищают путем промывки и/или экстракции, предпочтительно путем промывки ацетоном, и выделяют с помощью обычных методов.
Еще одним объектом изобретения являются также альтернативные способы получения замещенных индольных оснований Манниха общей формулы I, в которых R1 не обозначает Н, a R2-R21 имеют значения, указанные для общей формулы I, которые (способы) отличаются тем, что ароматические альдегидные соединения общей формулы II
где R13 имеет значения, указанные для общей формулы I,
в растворенном виде, предпочтительно в органическом растворителе, особенно предпочтительно в толуоле, в присутствии основания, предпочтительно карбоната калия или ангидрида борной кислоты, при температуре предпочтительно в интервале от -10 до +110°С подвергают взаимодействию с вторичными аминами общей формулы III
в которых R14 и R15 имеют значения, указанные для общей формулы I,
с получением аминальных соединений общей формулы IV
далее эти аминальные соединения общей формулы IV без последующей очистки под действием соответствующего хлорангидрида кислоты, предпочтительно ацетилхлорида, в абсолютном растворителе, предпочтительно в диэтиловом эфире, превращают в соли иминия общей формулы V
затем эти соли иминия общей формулы V без последующей очистки в растворенном виде, предпочтительно в ацетонитриле и/или толуоле, подвергают взаимодействию с индолом и/или замещенными индольными соединениями общей формулы VI
в которых R1 и R3 обозначают Н, a R2, R4 - R12 и R16 - R21 имеют значения, указанные для общей формулы I, и полученные таким путем соединения общей формулы VI, в которых R1 обозначает Н, a R2 - R21 имеют значения, указанные для общей формулы I, в растворенном виде, предпочтительно в диметилсульфоксиде, при температуре предпочтительно в интервале от 10 до 150°С в присутствии соответствующего основания, предпочтительно триэтиламина или трет-бутилата калия, подвергают взаимодействию с соединениями общей формулы XR22, где R22 представляет собой C1-С10алкил либо связанный через C1-С6алкиленовую группу арил или гетероарил, предпочтительно C1-С6алкил либо связанный через C1-С2алкиленовую группу арил, а Х обозначает Cl, Br или I, предпочтительно Cl, и полученные таким образом соединения общей формулы I, в которых R1 представляет собой C1-С10алкил либо связанный через C1-С6алкиленовую группу арил или гетероарил, а остальные радикалы R2-R21 имеют значения, указанные для общей формулы I, очищают путем фильтрации, предпочтительно через смолу-поглотитель, особенно предпочтительно путем фильтрации через иммобилизованный на полимере трис(2-аминоэтил)амин (фирма Novabiochem, Бад Соден) и/или 3-(3-меркаптофенил)пропанамидометилполистирол (фирма Argonaut, Муттенц, Швейцария), и в завершение выделяют с помощью обычных методов.
Синтез предлагаемых в изобретении замещенных индольных оснований Манниха предпочтительно осуществлять по описанной ниже технологии в автоматизированной установке фирмы Zymark, представленной на фиг.1 и 2.
Замещенные индольные основания Манниха общей формулы I согласно изобретению по известным специалистам в данной области методам могут переводиться в их соли с физиологически приемлемыми кислотами, предпочтительно с соляной кислотой, бромистоводородной кислотой, серной кислотой, метансульфоновой кислотой, муравьиной кислотой, уксусной кислотой, щавелевой кислотой, янтарной кислотой, винной кислотой, миндальной кислотой, фумаровой кислотой, молочной кислотой, лимонной кислотой, глутаминовой кислотой и/или аспарагиновой кислотой. Процесс образования солей предпочтительно проводить в соответствующем растворителе, особенно предпочтительно в диэтиловом эфире, диизопропиловом эфире, алкиловом эфире уксусной кислоты, ацетоне и/или 2-бутаноне. Наиболее предпочтительно образовывать соли с помощью триметилхлорсилана в метилэтилкетоне.
Предлагаемые в изобретении замещенные индольные основания Манниха общей формулы I токсикологически безопасны и могут применяться поэтому в качестве фармацевтически активных веществ.
Еще одним объектом изобретения в соответствии с этим являются также лекарственные средства, содержащие в своем составе в качестве активного вещества по меньшей мере одно замещенное индольное основание Манниха общей формулы I и необязательно другие активные вещества и/или вспомогательные вещества. В ряде случаев лекарственное средство предпочтительно может содержать в качестве активного вещества также смесь энантиомеров по меньшей мере одного замещенного индольного основания Манниха общей формулы I, при этом энантиомеры в смеси представлены предпочтительно не в эквимолярных количествах. Особенно предпочтительно относительная доля одного из энантиомеров составляет от 5 до 45 мол.%, наиболее предпочтительно от 10 до 40 мол.%, в пересчете на общее количество смеси энантиомеров.
Предпочтительно лекарственные средства по изобретению предназначаются для терапии болей, прежде всего для лечения хронических болей, и/или воспалительных реакций и/или аллергических реакций и/или наркотической зависимости и/или алкогольной зависимости и/или диареи и/или гастрита и/или различных язв и/или сердечно-сосудистых заболеваний и/или недержания мочи и/или депрессий и/или шоковых состояний и/или мигреней и/или нарколепсии и/или избыточного веса и/или астмы и/или глаукомы и/или гипокинетического синдрома и/или болезненного безразличия (апатии) и/или булимии и/или анорексии и/или каталепсии и/или для анксиолиза и/или для повышения ясности сознания и/или для усиления либидо.
Объектом настоящего изобретения является также применение по меньшей мере одного замещенного индольного основания Манниха общей формулы I по изобретению для получения соответствующего лекарственного средства, предназначенного для терапии болей, прежде всего для лечения хронических болей, и/или воспалительных реакций и/или аллергических реакций и/или наркотической зависимости и/или алкогольной зависимости и/или диареи и/или гастрита и/или различных язв и/или сердечно-сосудистых заболеваний и/или недержания мочи и/или депрессий и/или шоковых состояний и/или мигреней и/или нарколепсии и/или избыточного веса и/или астмы и/или глаукомы и/или гипокинетического синдрома и/или болезненного безразличия (апатии) и/или булимии и/или анорексии и/или каталепсии и/или для анксиолиза и/или для повышения ясности сознания и/или для усиления либидо.
Для приготовления соответствующих фармацевтических композиций наряду с по меньшей мере одним замещенным индольным основанием Манниха общей формулы I используют носители, наполнители, растворители, разбавители, красители и/или связующие. Выбор вспомогательных веществ зависит от того, предназначено ли лекарственное средство для перорального, внутривенного, интраперитонеального, интрадермального, внутримышечного, назального, буккального или местного применения, например, при кожных инфекциях, инфекциях слизистых оболочек и при глазных инфекциях. Для перорального введения пригодны композиции в форме таблеток, драже, капсул, гранул, капель, настоек и сиропов, для парентерального, местного и ингаляционного применения могут назначаться растворы, суспензии, легко восстанавливаемые сухие композиции, а также аэрозоли. Пригодными для интрадермального введения являются композиции из предлагаемых индольных оснований Манниха общей формулы I в депо-форме в растворенном виде или заделанными в пластырь, необязательно с добавками средств, способствующих пенетрации. Из применяемых для перорального или интрадермального введения лекарственных форм предлагаемые соединения общей формулы I могут высвобождаться постепенно, с замедлением, т.е. обладать пролонгированным действием.
Фармакологические исследования
1. Тестирование in vitro.
Всестороннее тестирование предлагаемых в изобретении индольных оснований Манниха на их эффективность проводили по обычным методам высокоэффективного скрининга, описанным John P. Devlin в High Throughput Screening, изд-во MarcEI Dekker Inc. (1997). Тем самым эти методы включены в настоящее описание в качестве ссылки.
Действие индольных оснований Манниха по изобретению определяли прежде всего по степени сродства к семейству NMDA-рецепторов (N-метил-D-аспартатных рецепторов), к α-адренорецепторам и к опиоидным рецепторам.
Исследования с целью выявить подавление обратного захвата серотонина (обратный захват 5-НТ (5-гидрокситрипталин)) проводили с помощью методов, описанных M.Ch. Frink, H.-H.-Hennies, W. Englberger», M. Haurand и В. Wilffert в Arzneim.-Forsch./Drug. Res. 46 (III), 11, 1996, стр. 1029-1036. Названные методы включены в настоящее описание в качестве ссылки.
Для проведения указанных исследований из соответствующих участков головного мозга крыс выделяли свежие синаптосомы. В каждом случае использовали так называемую Р2-фракцию, которую препарировали согласно рекомендациям E.G. Gray и V.P. Whittaker, описанным в Journ. Anat. 76, стр. 79-88 (1962). Данная публикация включена в этой части в настоящее описание в качестве ссылки. Для определения обратного захвата 5-НТ эти везикулярные частицы выделяли из стволового отдела головного мозга и продолговатого мозга (Pons- и Medulla oblongata) самцов крыс. Для 5-НТ-переносчика были выявлены следующие характеристики:
обратный захват 5-НТ: Кm=0,084±0,011 мкМ,
Vmax: 38,13±4,52 пмоль/мин/мг белка.
Результаты исследований представлены соответственно в виде средних значений, полученных в двух повторностях.
2. Исследование анальгезии на мышах в тесте на болевой синдром.
Углубленное исследование соединений по изобретению на их анальгетическую эффективность проводили на мышах, изучая их поведенческую реакцию в тесте на болевой синдром, индуцированный фенилхиноном (модифицированный метод согласно I.C. Hendershot, J. Forsaith, описанный в Journ. Pharmacol. Exp. Ther., том 125, стр. 237-240 (1959)). В этих целях в качестве подопытных животных использовали самцов мышей линии NMRI весом по 25-30 г. Группам по 10 особей в каждой, отобранным для испытания одной дозы тестируемой субстанции, через 10 мин после внутривенной инъекции такой субстанции вводили интраперитонеально в дозировке 0,3 мл/мышь 0,02%-ный водный раствор фенилхинона (фенилбензохинон, фирма Sigma, Дейзенхофен; приготовление раствора с добавлением 5% этанола и выдержкой в водяной бане при 45°С). Животных помещали поодиночке в специальные клетки для наблюдения и с помощью кнопочного счетчика в интервалы времени от 5 до 20 минут после введения фенилхинона подсчитывали число индуцированных болью разгибательных движений (так называемые поведенческие реакции на болевой синдром, т.е. в данном случае прогибание тела с вытягиванием задних конечностей). В качестве контроля служили животные, которым вводили только физиологический раствор поваренной соли.
Все субстанции тестировали в стандартной дозировке 10 мг/кг. Степень подавления реакции на болевой синдром (% подавления) в результате введения соответствующей субстанции рассчитывали по следующей формуле:
Ниже изобретение более подробно поясняется на примерах, которые не ограничивают его объема.
Примеры
Общие рекомендации по синтезу аминальных соединений общей формулы IV
Общие рекомендации по синтезу 1
К 2,7 эквивалента 40%-ного раствора соответствующего вторичного амина общей формулы III медленно при перемешивании добавляли по каплям при 20°С 1,0 эквивалент соответствующего ароматического альдегидного соединения общей формулы II. Затем раствор продолжали перемешивать в течение последующих 30 мин при 80°С, после чего охлаждали до комнатной температуры и смешивали с 0,57 эквивалента карбоната калия. При этом образовывались две фазы, которые разделяли, и водную фазу трижды экстрагировали порциями по 100 мл уксусного эфира. Объединенные органические фазы сушили над карбонатом калия и растворитель удаляли. Полученные таким путем аминальные соединения общей формулы IV использовали затем без дальнейшей очистки в последующих реакциях.
Общие рекомендации по синтезу 2
К раствору 1,0 эквивалента соответствующего ароматического альдегидного соединения общей формулы II в 80 мл абсолютного толуола добавляли 1,6 эквивалента ангидрида борной кислоты. Затем при интенсивном перемешивании добавляли раствор 2,4 эквивалента вторичного амина общей формулы III в 85 мл абсолютного толуола. Начало реакции сопровождалось заметным повышением температуры. Далее реакционный раствор продолжали перемешивать в течение последующих 2 часов при температуре в интервале от 45 до 50°С. После охлаждения до комнатной температуры избыточный ангидрид борной кислоты отделяли и из фильтрата удаляли растворитель. Полученные таким путем аминальные соединения общей формулы IV без дальнейшей очистки использовали в последующих реакциях.
Общие рекомендации по синтезу солей иминия общей формулы V
Общие рекомендации по синтезу 3
Раствор 1,0 эквивалента ацетилхлорида в абсолютном диэтиловом эфире медленно при перемешивании добавляли по каплям к 1,0 эквиваленту охлажденного льдом раствора соответственно суспензии полученного согласно рекомендации по синтезу 1 или 2 аминаля общей формулы III. Затем реакционную смесь продолжали перемешивать в течение ночи при приблизительно 20°С. При этом образовывался осадок, который отфильтровывали в атмосфере азота с помощью нутч-фильтра, после чего сушили в вакууме, создаваемом масляным насосом. Полученные таким путем соли иминия общей формулы V без дальнейшей очистки использовали в последующих реакциях.
Общие рекомендации по синтезу индольных оснований Манниха общей формулы I
Общие рекомендации по синтезу 4
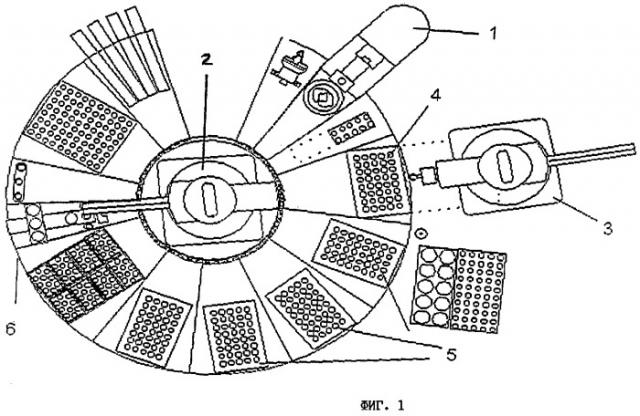
Синтез предлагаемых в изобретении индольных оснований Манниха осуществляли с помощью автоматизированной установки фирмы Zymark, представленной на фиг.1 и 2.
На фиг.1 показаны позиция укупорки (позиция 1) реакционных трубок, робот 1 (позиция 2) и робот 2 (позиция 3), первый из которых (робот 1) перемещает реакционные трубки, а второй (робот 2) пипетирует реагенты в реакционные трубки, а также показаны устанавливаемый на работу в заданном температурном режиме реакторный модуль (позиция 4), модули перемешивания (позиция 5) и позиция фильтрации (позиция 6), где реакционный раствор отфильтровывают.
На фиг.2 также показаны робот 1 (позиция 1) и робот 2 (позиция 2), перемещающие сосуды с реакционными продуктами на соответствующие позиции, на которых продукты синтеза, полученные в автоматизированной установке по фиг.1, подвергаются дальнейшей переработке. При этом указанные продукты синтеза смешивают с помощью циклонного смесителя (позиция 3) с ацетоном, перемешивают в центробежном реакторном модуле (позиция 4) и в завершение ацетон декантируют.
Для проведения синтеза круглодонную снабженную резьбой трубку из стекла (диаметром 16 мм и длиной 125 мм) вручную оснащали мешалкой и на позиции укупорки (позиция 1) закрывали навинчивающейся крышкой с мембранной прокладкой. Эту трубку с помощью робота 1 (позиция 2) помещали в установленный на работу в температурном режиме 0°С реакторный модуль. Робот 2 (позиция 3) последовательно пипетировал следующие реагенты:
1) 1 мл 0,1-молярного раствора индола или замещенного индольного соединения общ