Набор праймеров для детекции и/или идентификации трансгенных последовательностей днк в растительном материале и его содержащих продуктах (варианты), праймер (варианты), пара праймеров (варианты), способ детекции и/или идентификации с их использованием (варианты) и устройство для осуществления способа
Иллюстрации
Показать всеИзобретения относятся к биотехнологии, в частности к генной инженерии, и могут найти применение для мониторинга биобезопасности пищевых, кормовых продуктов и других товаров массового потребления. Изобретения представляют собой наборы праймеров, пары праймеров и отдельные праймеры для детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах, способы детекции и/или идентификации с их использованием и устройство для осуществления одного из способов. Праймеры комплементарны 5-ти типичным маркерным генам и регуляторным последовательностям ДНК - гену gus из бактерии E/coli, гену nptII из транспазона Tn5, 35S-промоторному участку вируса мозаики цветной капусты, терминаторным участкам гена nos и гена ocs из A. tumefaciens, наиболее часто содержащимся в генетических конструкциях самых распространенных на мировом рынке сортов трансгенных растений, и имеют нуклеотидные последовательности, указанные в SEQ ID Nos. 1-10. Способы включают экстракцию ДНК из растительного материала и его содержащих продуктов, проведение асимметричной или симметричной ПЦР, в том числе мультиплексной, с участием экстрагированной ДНК и набора праймеров, разделение амплифицированных продуктов реакции с последующей их детекцией и/или идентификацией путем гибридизации их с иммобилизованными на биологическом микрочипе олигонуклеотидами или методом гель-электрофореза, или при помощи амплификатора в режиме реального времени. Оригинальный подбор праймеров и введение в их последовательности корректирующих нуклеотидных замен обеспечивают сходство их термодинамических параметров и полную совместимость в наборах, что позволяет им эффективно работать в одних и тех же реакционных условиях и существенно увеличивает специфичность, чувствительность и достоверность способов детекции и/или идентификации трансгенных последовательностей ДНК с их участием. Использование в способе при гибридизационном анализе результатов ПЦР специально разработанных биологических микрочипов БМ «Трэссиген»-аминированных стекол с иммобилизованными непосредственно на их поверхности олигонуклеотидами с нуклеотидными последовательностями, указанными в SEQ IN Nos 11-15, а также аппаратно-программного комплекса «Дегмиген» существенно повышает специфичность, экономичность и технологичность процесса. 21 н. и 33 з.п.ф-лы, 5ил., 1табл.
Реферат
Область техники, к которой относятся изобретения
Изобретения относятся к биотехнологии, в частности к генной инженерии, касаются экологии в части биологической безопасности пищевых, кормовых продуктов и представляют собой наборы праймеров, пары праймеров и отдельные праймеры для детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах, способы детекции и/или идентификации с их использованием и устройство для осуществления одного из способов.
Изобретения могут найти применение для мониторинга биобезопасности пищевых продуктов, кормов и других товаров массового потребления.
Уровень техники
В настоящее время для обнаружения трансгенных компонентов генетически модифицированных растительных организмов используются два альтернативных метода, основанных на детекции и/или идентификации модифицированных биополимеров этих организмов - белков или нуклеиновых кислот.
Известен способ идентификации трансгенных белков растений с использованием соответствующих антител (Stave J.W., Food Control, 1999, vol.10, pp.367-374), а также способ детекции генетически модифицированных растений, содержащих NPT II белок, с использованием канамицина и/или паромомицина (US 2003/ 0017599 A1).
Известным способам присущи существенные недостатки. Во-первых, белки являются весьма лабильными биополимерами, способными изменять как конформацию молекулы, так и вторичную структуру при различного рода физических и химических воздействиях. Вследствие этого обнаружение чужеродных белков указанными способами в продуктах, прошедших глубокую термическую, химическую или микробиологическую обработку, становится практически невозможным.
Во-вторых, чувствительность известных способов не всегда достаточна для достоверной детекции малых количеств чужеродных белков в трансгенных продуктах.
В-третьих, осуществление указанных способов занимает много времени и требует значительных материальных затрат в связи применением дорогостоящих реагентов, в частности, специфических антител и антибиотиков.
Альтернативным методом, основанным на детекции и/или идентификации трансгенных последовательностей нуклеиновых кислот генетически модифицированных растительных организмов, является анализ, в частности, их ДНК с использованием полимеразной цепной реакции (ПЦР). Данный метод обладает рядом существенных преимуществ.
Во-первых, анализируемый биополимер (ДНК) значительно более стабилен по сравнению с белком, поэтому исследование его возможно и в продуктах, прошедших глубокую технологическую переработку. Кроме того, даже в случае разрушения первичной структуры биополимера, а именно деградации ДНК до фрагментов длиной 150-200 пар оснований, данный метод является пригодным.
Во-вторых, метод обладает более широкими возможностями и позволяет выявлять не только экспрессирующиеся участки генома, но и вспомогательные, такие как промоторы и терминаторы транскрипции.
В-третьих, метод обладает высокой чувствительностью и позволяет достоверно детектировать трансгенные последовательности при содержании в пробе менее 10-15 - 10-14 г анализируемой ДНК.
Известны способы обнаружения генетически модифицированных растений путем детекции одной трансгенной последовательности их ДНК, а именно маркерного гена gus из бактерии Escherichia coli (JP 2000197486), терминаторного участка гена nos из Agrobacterium tumefaciens (JP 2000210092) и 35S - промоторного участка вируса мозаики цветной капусты (KR 1020030003785 А).
При этом в первых двух случаях полученные в результате проведения симметричной ПЦР с участием экстрагированной ДНК и пары праймеров амплифицированные продукты разделяют методом гель-электрофореза и детектируют путем окрашивания их в геле флуоресцентным красителем; в последнем же случае амплифицированные продукты, содержащие флуоресцентную метку, идентифицируют в режиме реального времени путем измерения интенсивности флуоресцентного сигнала.
Используемые в известных способах для ПЦР - амплификации трансгенных последовательностей ДНК праймеры имеют следующие нуклеотидные последовательности:
- праймеры для маркерного гена gus из бактерии Escherichia coli:
(5') d - GTAGAAACCC CAACCCGTG (3')...............(1)
(5') d - CGTTGTTCAC ACAAACGGTG (3')...............(2)
- праймеры для терминаторного участка гена nos из Agrobacterium tumefaciens
(5') d - TCATGATCAGATTGTCGTTT (3')............(1)
(5') d - CGGATAAACC TTTTCACGCC (3')........................(2)
- праймеры для 35S - промоторного участка вируса мозаики цветной капусты
(5') d - TAGTGGAAAA GGAAGGTGGC (3')............(2)
(5') d-AGATATCACATCAATCCACT (3')..............................(3)
(5') d - ATTGCCCCAG CTATCTGTCA С (3').....................(4)
(5') d - ATCACATCAA TCCACTTDC (3')...............(5)
(5') d - TAGTGGAAAA GGAAGGTGGC (3')...............(6)
(5') d - AGGATAGTGG GATTGTGC (3')..................(7)
Однако значение изменения свободной энергии взаимодействия 3' - концевых нуклеотидов с матричной ДНК (в дальнейшем - изменение свободной энергии) обоих праймеров (1 и 2) для маркерного гена gus весьма низко (ΔG=-9,9 ккал/моль, значения ΔG и Tm для праймеров рассчитаны с помощью программы OLIGO), что обусловливает повышенную вероятность их неспецифического связывания с анализируемой ДНК. Кроме того, праймер (2) образует внутрипраймерную шпильку с Tm=55°С, что затрудняет его взаимодействие с анализируемой ДНК.
Значение изменения свободной энергии 3' - концевых нуклеотидов праймера (1) для терминаторного участка гена nos слишком низко (ΔG=-11,1 ккал/моль) и приводит к неспецифическому взаимодействию его с матричной ДНК. Что касается праймера (2), то его температура плавления (Tm=44,8°С), определяющая температуру отжига, недопустимо низка, что существенно увеличивает фон неспецифических реакций. Кроме того, 3' - концевой тетрамерный участок нуклеотидной последовательности праймера (2) - GTTT комплементарен гомологичному тетрамерному участку нуклеотидной последовательности праймера (1) - АААС, что является причиной межпраймерных взаимодействий.
В отношении 3-х пар праймеров для 35S - промоторного участка вируса мозаики цветной капусты прежде всего следует отметить, что последовательность матричной ДНК для их отбора не соответствует используемой в наиболее распространенных сортах трансгенной сои. Кроме того, ампликоны, получаемые при участии в ПЦР всех 3-х пар праймеров, содержат тугоплавкую шпильку с Tm=86,0°С, которая препятствует процессу амплификации.
Праймер (2) включает слишком тугоплавкий 3'-концевой тетрамерный участок с ΔG=-9,4 ккал/моль, что обусловливает его неспецифическое взаимодействие с анализируемой ДНК. Легкоплавкость праймеров (3), (5) и (7) [Tm (3) = 40,0 °C, Tm (5) = 44,7°С и Tm (7)=43,8°С] существенно увеличивает фон неспецифических реакций.
Известен способ обнаружения генетически модифицированных растений путем детекции 2-х трансгенных последовательностей их ДНК, а именно 35S - промоторного участка вируса мозаики цветной капусты и терминаторного участка гена nos из Agrobacteriun tumefaciens, рекомендованный Постановлением Европейского Парламента и Совета №1829/2003 от 22.09.2003 г. "О генетически модифицированной пище и кормах" (Lipp M., Brodmann P., Pietsch К., Pauwels J., Anklam E. Journal of АОАС International, 1999, vol. 82, №4, pp.923-928) и включенный в национальный стандарт РФ (ГОСТ Р 52173-2003).
Полученные в известном способе в результате проведения симметричной ПЦР с участием экстрагированной ДНК и 2-х пар праймеров амплифицированные продукты разделяют методом гель-электрофореза и детектируют и/или идентифицируют путем окрашивания их в геле флуоресцентным красителем.
Используемые в данном способе праймеры имеют следующие нуклеотидные последовательности:
- праймеры для 35S - промоторного участка вируса мозаики цветной капусты
(5') d - GCTCCTACAA ATGCCATCA (3')...............(1)
(5') d - GATAGTGGGA TTGTGCGTCA (3')...............(2)
- праймеры для терминаторного участка гена nos из Agrobacterium
tumefaciens
(5') d - GAATCCTGTT GCCGGTCTTG (3')............(1)
(5') d - TTATCCTAGT TTGCGCGCTA (3')...........................(2)
Однако праймер (1) для 35S - промоторного участка имеет слишком низкую расчетную температуру отжига (45,8°С) и включает нуклеотидную замену (Т→С), которая характерна для нуклеотидной последовательности 35S, используемой для получения трансгенных растений, но отсутствует в наиболее распространенных сортах генетически модифицированных организмов. Кроме того, у того же праймера 3' - конец накладывается на матричную шпильку с Tm=79°С, а праймер (2) гибридизуется с участком матричной ДНК, содержащим шпильку с Tm=70°С. В ампликоне, получаемом с участием данной пары праймеров, содержится тугоплавкая шпилька с Tm=86°С, а для проведения процесса амплификации в данном случае необходимо использовать низкую температуру отжига, при которой очень высока вероятность появления неспецифичных фрагментов ДНК.
Что касается пары праймеров для терминаторного участка гена nos, то оптимальная для них температура отжига слишком низка (<50°С), а праймер (2) самокомплементарен, так как содержит триплет, комплементарный собственной 3' - концевой нуклеотидной последовательности и, кроме того, гибридизуется с участком матричной ДНК, содержащим две тугоплавкие шпилечные структуры с Tm=61°С и Tm= 86°С.
Указанные недостатки известных праймеров и их наборов существенно снижают специфичность, чувствительность и достоверность известных способов с их использованием.
Ближайшим аналогом заявленным изобретениям в части набора праймеров для детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах, способа детекции и/или идентификации с их использованием и устройства для осуществления способа является национальный стандарт РФ (ГОСТ Р 52174-03) "Продукты пищевые. Биологическая безопасность. Генетически модифицированные организмы и источники. Метод идентификации генетически модифицированных растений и продуктов на их основе", разработанный Институтом молекулярной биологии им. В.А. Энгельгардта РАН и Институтом физиологии растений им. К.А. Тимирязева РАН, принятый и введенный в действие Постановлением Госстандарта России №403-ст от 29.12.2003 г.
Используемые в указанном стандарте праймеры имеют следующие нуклеотидные последовательности:
- праймеры для 35S - промоторного участка вируса цветной капусты
(5') d - CCTCCTCGGA TTCCATTGCC CAG (3')............(1)
(5') d - GTCCATCTTT GGGACCACTG TCGG (3')..................(2)
- праймеры для маркерного гена gus из бактерии Escherichia coli
(5') d - AAGCCGGGCAATTGCTGTGC CA (3')...........................(1)
(5') d - GACCGCATCG AAACGCAGCA CG (3')..................(2)
- праймеры для терминаторного участка гена nos из Agrobacterium tumefaciens
(5') d - CGATGACGCG GGACAAGCCG Т (3')............(1)
(5') d - GACCTTAGGC GACTTTTGAA CGCGC (3')..................(2)
- праймеры для маркерного гена npt II из транспозона Тn5
(5') d - GTGTTCCGGC TGTCAGCGCA GG (3')..................(1)
(5') d - CGCAAGGAAC GCCCGTCGTG G (3')...............(2)
- праймеры для терминаторного участка гена osc из Agrobacterium tumefaciens
(5') d - GAAACCGGCG GTAAGGATCT GAGC (3')...............(1)
(5') d - GCGAGACGCC TATGATCGCA TGAT (3').....................(2)
Способ детекции генетически модифицированных растений и продуктов на их основе с участием указанных праймеров включает:
- экстракцию из них ДНК;
- проведение мультиплексной асимметричной ПЦР с участием экстрагированной ДНК и набора из 10-ти (5-ти пар) известных праймеров, в котором один из составляющих пару праймеров содержит флуоресцентную метку;
- получение амплифицированных продуктов реакции;
- разделение амплифицированных продуктов путем гибридизации их с комплементарными иммобилизованными дезоксирибоолигонуклеотидами;
- детекцию и/или идентификацию трансгенных последовательностей ДНК.
Устройство для осуществления известного способа представляет собой биологический микрочип, поверхность которого сформирована из массива микроскопических ячеек полиакриламидного гидрогеля. Пять ячеек гидрогеля, расположенных на микрочипе в заданном порядке, содержат иммобилизованные олигонуклеотиды, комплементарные нуклеотидным последовательностям 35S - промоторного участка вируса мозаики цветной капусты, маркерного гена gus из бактерии Escherichia coli, терминаторного участка гена nos из Agrobacterium tumefaciens, маркерного гена npt II из транспозона Тn5, терминаторного участка гена ocs из Agrobacterium tumefaciens и имеющие следующие нуклеотидные последовательности:
(5') d-GCC ATC ATT GCG АТА AAG G (3')
(5') d-CTG GTA TCA GCG CGA A (3')
(5') d-GCT AAG CAC ATA CGT CAG AA (3')
(5') d-GGC AGC GCG GCT ATC (3')
(5') d-TTC TGT TGT GCA CGT TGT A (3') соответственно.
Гелевые ячейки наносятся на стеклянную подложку с помощью роботов и представляют собой полусферу диаметром до 250 мкм и периодом около 300 мкм.
Известные праймеры имеют ряд существенных недостатков. Так, праймер (2) для 35S - промоторного участка содержит тугоплавкую шпильку на 5' -конце, наличие которой приводит к образованию не участвующих в ПЦР и в гибридизации шпилечных побочных продуктов полимеразного синтеза. Кроме того, значения изменения свободной энергии 3' - концевых нуклеотидов обоих праймеров для 35S - промоторного участка слишком низки [ΔG (1)= -9,7 ккал/моль; ΔG (2)= -9,6 ккал/моль], что обусловливает неспецифическое праймирование. Значения изменения свободной энергии 3'-концевых нуклеотидов обоих праймеров для маркерного гена gus также недопустимо низки [ΔG (1)= -10,0 ккал/моль; ΔG (2)= -9,9 ккал/моль]; при этом оба праймера при большой длине (22 нуклеотида) имеют высокие температуры плавления [Tm (1)=67,0°С; Tm (2)=66,2°С], что существенно снижает специфичность амплификации.
Изменения свободной энергии 3'-концевых нуклеотидов праймеров (1) и (2) для терминаторного участка гена nos имеют экстремально низкие значения [ΔG (1)= -11,1 ккал/моль; ΔG (2)= -13,4 ккал/моль], вследствие чего процесс амплификации матричной ДНК должен протекать крайне неспецифично. Кроме того, оба праймера содержат внутренние шпильки с Tm (1)= 61°С и Tm (2)= 65°С, что препятствует связыванию праймеров с матричной ДНК. Более того, нуклеотидная последовательность праймера (1) частично перекрывается с тугоплавкой (Tm= 96°С) шпилькой матричной ДНК, вследствие чего его гибридизация с матричной ДНК существенно затруднена; праймер же (2) самокомплентарен по 3'-концевому тугоплавкому "квартету" - GCGC и должен формировать при амплификации праймерные димеры. Оба праймера (1) и (2) для маркерного гена npt II гибридизуются с участками матричной ДНК, содержащими тугоплавкие шпилечные структуры, что снижает чувствительность процесса амплификации. Кроме того, те же праймеры содержат очень тугоплавкие 3'-концевые нуклеотиды [ΔG (1)= -9,7 ккал/моль; ΔG (2)= -9,9 ккал/моль], а ампликон, получаемый с их участием, является чрезвычайно тугоплавким, поскольку включает 64,6% "дуплета" GC, что существенно снижает эффективность ПЦР.
Хотя изменения свободной энергии 3' - концевых нуклеотидов обоих праймеров для терминаторного участка гена ocs имеют вполне приемлемые значения [ΔG (1)= -8,2 ккал/моль; ΔG (2)= -6,5 ккал/моль], праймер (2) содержит тугоплавкую (Tm= 72,0°С) шпильку на 5' - конце, которая входит в состав матричной шпильки с Tm= 81,0°С, а 3' - конец праймера (1) перекрывается с тугоплавкой матричной шпилькой с Tm=71,0°С, общим следствием чего является снижение чувствительности ПЦР.
Указанные недостатки известных праймеров свидетельствуют об их неудовлетворительной совместимости в наборе, не позволяющей им эффективно работать при одних и тех же реакционных условиях, что существенно снижает специфичность, чувствительность и достоверность известного способа с их участием.
Таким образом, при использовании набора известных праймеров в известном способе возможно получение не более чем удовлетворительных результатов лишь в модельных экспериментальных условиях (при высоких концентрациях очищенной матричной ДНК), однако при массовом скрининге различного растительного материала и его содержащих продуктов очень высока вероятность появления ложноотрицательных результатов.
Кроме того, использование в известном способе для осуществления процедуры гибридизации биочипов из массива ячеек гидрогеля снижает специфичность, экономичность и технологичность процесса вследствие
- повышения вероятности неспецифического связывания амплифицированных продуктов с иммобилизованными олигонуклеотидами по причине недостаточной длины последних (от 15 до 19 нуклеотидов);
- замедления процедуры гибридизации (до 18 часов) и увеличения времени анализа;
- необходимости применения весьма дорогостоящих лазерных сканеров для детекции и/или идентификации результатов гибридизации вследствие микроразмеров ячеек гидрогеля с иммобилизованными зондами (D<250 мкм);
- повышенной вероятности нарушения технологического процесса в части полимеризации массива гидрогеля при формировании биочипов и получения брака вследствие попадания кислорода в атмосферу рабочей камеры робота.
Раскрытие изобретений
Задачей заявленных изобретений является разработка высокоэффективных новых наборов праймеров, пар праймеров и праймеров для детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах, а также высокотехнологичных, экономичных и экологически безопасных способов массового скрининга растительного сырья и продуктов на его основе с их использованием и устройства для осуществления одного из способов.
Задача изобретений в части набора праймеров решена тем, что создан оригинальный высокоспецифичный набор из 10-ти (5-ти пар) дезоксирибоолигонуклеотидов, комплементарных нуклеотидным последовательностям, наиболее часто содержащимся в генетических конструкциях самых распространенных на мировом рынке сортов трансгенных растений (James С. Preview: Global status of commericalized transgenic crops: 2003. ISAAA Briefs. No 30. ISAAA: Ithaca, NY.), а именно нуклеотидным последовательностям 35S -промоторного участка вируса мозаики цветной капусты, маркерного гена gus из бактерии Escherichia coli, терминаторного участка гена nos из Agrobacterium tumefaciens, маркерного гена npt II из транспозона Тn5 и терминаторного участка гена ocs из Agrobacterium tumefaciens и имеющих нуклеотидные последовательности, указанные в SEQ ID NOs. 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10.
Вариантом набора праймеров для детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах является набор, включающий по меньшей мере 2, но не более 10-ти дезоксирибоолигонуклеотидов, выбранных из группы, содержащей праймеры с нуклеотидными последовательностями, указанными в SEQ ID NOs. 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10.
При использовании данного варианта набора праймеров в случае необходимости подбирают любым способом, как минимум, один недостающий для образования пары праймер.
Техническими результатами заявленных изобретений в части наборов праймеров являются:
- повышение специфичности амплификации анализируемой ДНК;
- полная совместимость в наборах всех 10-ти заявленных праймеров, позволяющая им эффективно работать при одних и тех же реакционных условиях;
- расширение возможностей детекции и/или идентификации амплифицированных продуктов путем использования различных физико-химических методов.
Указанные технические результаты достигаются следующим:
- все заявленные праймеры имеют легкоплавкие 3'-концы с ΔG>-9,0 ккал/моль, что существенно снижает фон неспецифических взаимодействий;
- заявленные праймеры характеризуются повышенным содержанием пуриновых оснований (А и G) на 3' - концах, что повышает специфичность их взаимодействия с анализируемой ДНК;
- практически исключена вероятность межпраймерных и внутрипраймерных взаимодействий путем введения в нуклеотидные последовательности ряда праймеров корректирующих замен, позволяющих устранить как эти взаимодействия, так и нежелательное формирование шпилечных структур;
- температуры плавления (Tm) всех заявленных праймеров превышают 65°С и у большинства праймеров составляют около 70°С, так как в нуклеотидные последовательности ряда праймеров введены 5'-концевые замены, повышающие их Tm;
- заявленные праймеры не формируют шпилек с Tm>30°С;
- комплементарные заявленным праймерам участки анализируемой ДНК не участвуют в формировании тугоплавких шпилечных структур;
- межпраймерные участки ампликонов, получаемых с участием заявленных праймеров, не содержат тугоплавких шпилечных структур;
- пары заявленных праймеров подобраны таким образом, что различия в размерах получаемых с их участием ампликонов позволяют дифференцировать их различными физико-химическими методами, включающими электрофоретическое разделение.
Для детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах может использоваться отдельно каждая из 5-ти заявленных пар праймеров. Пара праймеров включает 2 дезоксирибоолигонуклеотида, комплементарных нуклеотидной последовательности 35S - промоторного участка вируса мозаики цветной капусты или маркерного гена gus из бактерии Escherichia coli, или терминаторного участка гена nos из Agrobacterium tumefaciens или маркерного гена npt II из транспозона Тn5, или терминаторного участка гена ocs из Agrobacterium tumefaciens, обладающих активностью прямого или обратного праймеров в ПЦР и имеющих нуклеотидные последовательности, указанные в SEQ ID NOs. 1 и 2, 3 и 4, 5 и 6, 7 и 8, 9 и 10.
Для детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах может использоваться отдельно каждый из 10-ти заявленных праймеров, комплементарный нуклеотидной последовательности 35S - промоторного участка вируса мозаики цветной капусты или маркерного гена gus из бактерии Escherichia coli, или терминаторного участка гена nos из Agrobacterium tumefaciens, или маркерного гена npt II из транспозона Тn5, или терминаторного участка гена ocs из Agrobacterium tumefaciens и представляющий собой нуклеотидную последовательность, указанную в SEQ ID NOs. 1 или 2, или 3, или 4, или 5, или 6, или 7, или 8, или 9, или 10.
При использовании какого-либо из заявленных праймеров недостающий для образования пары праймер подбирают любым способом.
Вышеуказанные технические результаты достигаются при использовании заявленных изобретений (наборов праймеров, пар праймеров и праймеров) не только с нуклеотидными последовательностями, указанными в SEQ ID NOs. 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10, но и с последовательностями, гомологичными им, как минимум, на 75%, или с их вариантами, включающими делеции, инсерции по 3' и/или 5' - концу и/или нуклеотидные замены не более 5-ти нуклеотидов в указанных последовательностях.
Техническими результатами заявленных изобретений в части способа детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах являются:
- повышение специфичности процесса;
- повышение чувствительности процесса;
- увеличение достоверности и улучшение воспроизводимости получаемых в процессе результатов, что позволяет беспрепятственно использовать его для массового скрининга растительного материала и его содержащих продуктов;
- повышение экономичности и технологичности процесса вследствие использования в нем, в частности, специально разработанных биологических микрочипов БМ «Трэссиген» и аппаратно-программного комплекса «Дегмиген»;
- расширение возможностей детекции и/или идентификации амплифицированных продуктов путем использования различных физико-химических методов.
Способ детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах, согласно изобретению, включает:
(а) экстракцию из них ДНК;
(в) проведение асимметричной ПЦР, в том числе мультиплексной, с участием экстрагированной ДНК, определяемой метки и от 1-го до 10-ти олигонуклеотидов-праймеров, выбранных из группы, включающей праймеры с нуклеотидными последовательностями, указанными в SEQ ID NOs. 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10; или с участием экстрагированной ДНК и тех же праймеров, в которых, по меньшей мере, один из составляющих пару праймеров содержит определяемую метку; или с участием экстрагированной ДНК и тех же праймеров; при этом в случае необходимости в реакционную смесь вносят, как минимум, один недостающий для образования пары праймер, подобранный любым способом;
(c) получение амплифицированных продуктов реакции;
(d) разделение амплифицированных продуктов путем гибридизации их с комплементарными иммобилизованными дезоксирибоолигонуклеотидами или методом гель-электрофореза;
(e) детекцию и/или идентификацию трансгенных последовательностей ДНК.
При этом определяемая метка является как радиоактивной, так и нерадиоактивной; предпочтительно метка представляет собой каталитическую, лигандную или флуоресцентную молекулу.
Иммобилизованные дезоксирибоолигонуклеотиды комплементарны нуклеотидным последовательностям 35S - промоторного участка вируса мозаики цветной капусты или маркерного гена gus из бактерии Escherichia coli, или терминаторного участка гена nos из Agrobacterium tumefaciens, или маркерного гена npt II из транспозона Тn5, или терминаторного участка гена ocs из Agrobacterium tumefaciens и предпочтительно имеют нуклеотидные последовательности, указанные в SEQ ID NOs. 11 или 12, или 13, или 14, или 15 соответственно.
При этом иммобилизованные дезоксирибоолигонуклеотиды локализованы на твердой фазе, представляющей собой стекло или полимеры, или металлы, или керамику, или полупроводники, или слюду. Предпочтительно поверхность твердой фазы сформирована в виде устройства, представляющего собой биологический микрочип. В качестве биологического микрочипа может использоваться устройство БМ «Трэссиген».
Детекцию и/или идентификацию трансгенных последовательностей ДНК целесообразно осуществлять путем сравнительного анализа уровня сигналов-люминесцентных или хромогенных, или радиоактивных, полученных в результате гибридизации с иммобилизованными дезоксирибоолигонуклеотидами исследуемого образца и положительного и отрицательного контролей.
Сравнительный анализ результатов гибридизации исследуемого образца и контролей предпочтительно осуществлять путем преобразования вышеуказанных сигналов в цифровые данные с последующей их математической обработкой с помощью аппаратно-программного комплекса и программы для ЭВМ.
В качестве аппаратно-программного комплекса можно использовать детектор-идентификатор биологических микрочипов «Дегмиген-001» или «Дегмиген-002», или «Дегмиген-003».
Детекцию и/или идентификацию трансгенных последовательностей ДНК при разделении амплифицированных продуктов, содержащих определяемую метку, методом гель-электрофореза осуществляют при ультрафиолетовом освещении или инфракрасном освещении, или освещении видимым светом.
Детекцию и/или идентификацию трансгенных последовательностей ДНК при разделении амплифицированных продуктов, не содержащих определяемую метку, методом гель-электрофореза осуществляют при ультрафиолетовом освещении в геле, содержащем флуоресцентный краситель, или после окрашивания амплифицированных продуктов в геле флуоресцентным красителем.
При этом в качестве флуоресцентного красителя может использоваться бромид этидия или иодид пропидия, или SYBR Green I.
Для документирования результатов детекции и/или идентификации трансгенных последовательностей ДНК в том и другом случае целесообразно использовать цифровую фотокамеру.
Кроме того, детекцию и/или идентификацию трансгенных последовательностей ДНК можно осуществлять в процессе разделения амплифицированных продуктов методом капиллярного гель-электрофореза.
Вариантом заявленного способа детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах является способ, включающий:
(а) экстракцию из них ДНК;
(в) проведение симметричной ПЦР, в том числе мультиплексной, с участием экстрагированной ДНК и от 1-го до 10-ти олигонуклеотидов-праймеров, выбранных из группы, включающей праймеры с нуклеотидными последовательностями, указанными в SEQ ID NOs. 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10, при этом в случае необходимости в реакционную смесь вносят, как минимум, один недостающий для образования пары праймер, подобранный любым способом;
(c) получение амплифицированных продуктов реакции;
(d) разделение амплифицированных продуктов методом гель-электрофореза;
(e) детекцию и/или идентификацию трансгенных последовательностей ДНК.
Детекцию и/или идентификацию трансгенных последовательностей ДНК осуществляют аналогично описанным в предыдущем варианте способа для случая разделения амплифицированных продуктов, не содержащих определяемую метку, методом гель-электрофореза.
Другим вариантом заявленного способа детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах является способ, включающий:
(а) экстракцию из них ДНК;
(в) проведение ПЦР, в том числе мультиплексной, с участием экстрагированной ДНК и от 1-го до 10-ти олигонуклеотидов-праймеров, выбранных из группы, включающей праймеры с нуклеотидными последовательностями, указанными в SEQ ID NOs. 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10, а также компонентов, обеспечивающих детекцию и/или идентификацию амплифицированных продуктов в режиме реального времени, при этом в случае необходимости в реакционную смесь вносят, как минимум, один недостающий для образования пары праймер, подобранный любым способом;
(с) детекцию и/или идентификацию амплифицированных продуктов в режиме реального времени.
При этом в качестве компонентов, обеспечивающих детекцию и/или идентификацию амплифицированных продуктов, можно использовать как флуоресцентные красители, так и флуоресцентные зонды.
В качестве флуоресцентного красителя целесообразно использовать SYBR Green I, а в качестве флуоресцентных зондов - зонды типа Tag Man или Molecular Beacons.
Детекцию и/или идентификацию амплифицированных продуктов в режиме реального времени предпочтительно осуществлять при помощи 6-канального амплификатора LightCycler фирмы Roche Applied Science.
Техническими результатами заявленных изобретений в части устройства для детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах являются:
- повышение специфичности гибридизации амплифицированных продуктов с иммобилизованными олигонуклеотидами вследствие оптимальной длины последних (до 40 нуклеотидов);
- ускорение процедуры гибридизации (до 1 часа) и сокращение времени анализа;
- использование для детекции и/или идентификации результатов гибридизации обычных оптических (не лазерных) сканеров, в частности, аппаратно-программного комплекса «Дегмиген», вследствие макроразмеров зон гибридизации;
- снижение себестоимости микрочипов вследствие упрощения и повышения надежности технологического процесса их изготовления, в частности, иммобилизации олигонуклеотидов непосредственно на поверхности твердой фазы.
Устройство для детекции и/или идентификации трансгенных последовательностей ДНК в растительном материале и его содержащих продуктах, согласно изобретению, представляет собой поверхность твердой фазы с локализованными на ней в заданном порядке от 1-го до 5-ти иммобилизованными олигонуклеотидами, выбранными из группы, включающей олигонуклеотиды, комплементарные нуклеотидным последовательностям 35S-промоторного участка вируса мозаики цветной капусты или маркерного гена gus из бактерии Escherichia coli, или терминаторного участка гена nos из Agrobacterium tumefaciens, или маркерного гена nptII из транспозона Тn5, или терминаторного участка гена ocs из Agrobacterium tumefaciens и имеют нуклеотидные последовательности, указанные в SEQ ID Nos. 11 или 12, или 13, или 14, или 15 соответственно.
При этом твердая фаза может представлять собой стекло, полимеры, металлы, керамику, полупроводники или слюду. Поверхность твердой фазы может быть сформирована в виде биологического микрочипа. Предпочтительно биологическим микрочипом является БМ «Трэссиген».
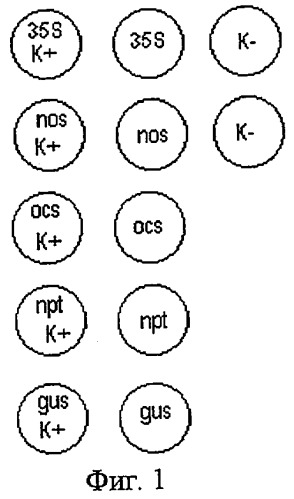
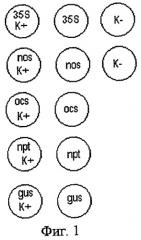
Схема расположения зон гибридизации на биологическом микрочипе представлена на фиг.1.
Вышеуказанные технические результаты в части способа детекции и/или идентификации и устройства для его осуществления достигаются при использовании заявленных изобретений - наборов праймеров, пар праймеров и праймеров, а также иммобилизованных дезоксирибоолигонуклеотидов не только с нуклеотидными последовательностями, указанными в SEQ ID NOs. 1-15, но и с последовательностями, гомологичными им, как минимум, на 75%, или с их вариантами, включающими делеции, инсерции по 3' и/или 5' -концу и/или нуклеотидные замены не более 5-ти нуклеотидов в указанных последовательностях.
Краткое описание фигур
В дальнейшем заявленные изобретения поясняются фигурами, при этом Фиг.1 иллюстрирует схему расположения зон гибридизации на биологическом микрочипе, где
К+ обозначают зонды, комплементарные нуклеотидным последовательностям меченых праймеров (положительный контроль);
К- обозначают зонды, комплементарные нуклеотидным последовательностям генов зеина и лектина кукурузы и сои соответственно (отрицательный контроль);
35S, nos, osc, npt, gus обозначают соответствующие зонды, предназначенные для гибридизации с амплифицированной анализируемой ДНК (опыт).
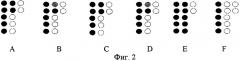
Фиг.2 иллюстрирует результаты гибридизации на биологическом микрочипе продукотв асимметричной ПЦР - амплификации трансгенной ДНК, выделенной из соевой муки, где
А - результаты гибридизации продуктов ПЦР - амплификации с участием набора праймеров с нуклеотидными последовательностями, указанными в SEQ ID NOs. 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10;
В - то же, что А, но с заменой праймера с нуклеотидной последовательностью, указанной в SEQ ID NO:l его укороченным производным с делецией пяти 5'-концевых нуклеотидов;
С - то же, что А, но с заменой праймера с нуклеотидной последовательностью, указанной в SEQ ID NO:l его удлиненным производным, содержащим инсерцию пяти 5'-концевых нуклеотидов;
D - то же, что А, но с заменой биотинилированного праймера с нуклеотидной последовательностью, указанной в SEQ ID NO:2, гомологичной ей на 75% последовательностью нуклеотидов;
Е - результаты гибридизации продуктов ПЦР - амплификации с участием контрольной ДНК, содержащей все пять детерминант трансгенности, и набора праймеров с нуклеотидными последовательностями, указанными в SEQ ID NOs. 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10 (положительный контроль);
F - отрицательный контроль.
Фиг.3 иллюстрирует результаты гибридизации на биологическом микрочипе продуктов асимметричной ПЦР - амплификации трансгенной ДНК, выделенной из картофеля сорта Desiree, где
А - результаты гибридизации продуктов ПЦР-амплификации с участием набора праймеров с нуклеотиднымми последовательностями, указанными в SEQ ID NOs. I, 2, 3, 4, 5, 6, 7, 8, 9 и 10;
В - то же, что А, но с заменой меченого праймера с нуклеотидной последовательностью, указанной в SEQ ID NO: 6, его укороченным производным с делецией пяти 5'-концевых нуклеотидов;
С - то же, что А, но с заменой меченого праймера с нуклеотидной последовательностью, указанной в SEQ ID NO: 6, его удлиненным производным, содержащим инсерцию пяти 5'-концевых нуклеотидов;
D - то же, что А, но с заменой меченого праймера с нуклеотидной последовательностью, указанной в SEQ ID NO: 6, его производным, включающим нуклеотидную замену 5-ти нуклеотидов;
Е - то же, что А, но с заменой меченого праймера с нуклеотидной последовательностью, указанной в SEQ ID NO: 6, гомологичной ей на 75% последовательностью нуклеотидов;
F - положительный контроль;
G - отрицательный контроль.
Фиг.4 представляет собой электрофореграмму продуктов симметричной ПЦР-амплификации с участием трансгенной ДНК, выделенной из листьев табака, и различных наборов праймеров, где
1 - электрофореграмма продуктов ПЦР-амплификации, полученных с участием набора праймеров с нуклеотидными последовательностями, указанными в SEQ ID NOs. 1 и 2;
2 - то же, что 1, но с участием набора праймеров с нуклеотидными последовательностями, указанными в SEQ ID NOs. 3 и 4;
3 - то же, что 1, но с участием набора праймеров с нуклеотидными последовательностями, указанными в SEQ ID NOs. 9 и 10;
4 - то же, что 1, но с участием набора праймеров с нуклеотидными последовательностями, указанными в SEQ ID NOs. 5 и 6;
5 - то же, что 1, но с участием набора праймеров с нуклеотидными последовательностями, указанными в SEQ ID NOs. 7 и 8;
6 - то же, что 1, но с участием набора праймеров с нуклеотидными последовательностями, указанными в SEQ ID NOs. 1 и 2, 3 и 4, 5 и 6, 7 и 8, 9 и 10.
Фиг.5 иллюстрирует изменение интенсивности флуоресценции красителя SYBR Green I при ПЦР-амплификации трансгенной ДНК, выделенной из картофеля сорта Desiree, с различными наборами праймеров в режиме реального времени, где
1 - кривая интенсивности флуоресценции, полученная с участ