Производные хиназолина или хинолина и лекарственные средства на их основе
Иллюстрации
Показать всеПредложено анальгетическое средство, обладающее анальгетическим действием, эффективное против боли, путем действия на ноцицептиновый рецептор. Анальгетическое средство в качестве активного ингредиента содержит соединение, представленное общей формулой (1) или его соль. X, Y, Е, Q, А1, A2, R1, R3, R4, R5, R2A, R2C, R2D, R2B определены в формуле изобретения. 3 табл.
Реферат
Настоящее изобретение относится к фармацевтически полезному новому гетероциклическому производному или его соли и к фармацевтической композиции, содержащей их в качестве активного ингредиента.
В качестве анальгетика используют наркотический анальгетик (такой как морфин), ненаркотический анальгетик (такой как аспирин или индометацин) или наркотическо-антагонистический анальгетик (такой как пентазоцин). Наркотический анальгетик оказывает анальгетическое действие главным образом путем ингибирования центральной болевой передачи возбуждения. Ненаркотический анальгетик оказывает анальгетическое действие главным образом благодаря ингибированию продуцирования периферического вызывающего боль вещества. Наркотическо-антагонистический анальгетик оказывает анальгетическое действие по механизму, аналогичному механизму действия наркотического анальгетика.
Однако отсутствует анальгетик, который является эффективным против хронической боли, которая не подавляется морфином, при аллодинии, сопровождающейся опоясывающим лишаем, или при повышенной болевой чувствительности и было бы желательно разработать превосходный анальгетик.
Ноцицептин представляет собой нейропептид, относящийся к разнообразной нервной активности, включая болевую чувствительность in vivo. В не прошедшей экспертизу патентной публикации Японии №10-212290 описано, что агонист и/или антагонист ноцицептина может оказаться эффективным при лечении психического расстройства, невропатии и физиологических нарушений и особенно эффективен для снижения беспокойства и стресса, депрессии, травматического нарушения, амнезии вследствие болезни Альцгеймера или другого слабоумия, симптомов эпилепсии и спазма, острой и/или хронической боли, симптомов при прекращении приема наркотиков, для контроля за балансом воды, для выделения Na+, нарушения артериального давления крови и при расстройстве питания, таком как ожирение.
В качестве непептидного соединения, воздействующего на ноцицептиновый рецептор, известны лофентанил, бензоилгидразон налоксона и производное 2-оксоимидазола (Международная публикация WO 9854168). Однако данные соединения все еще находятся на стадии фундаментального исследования и ни одно из них не является коммерчески доступным.
В качестве соединения, аналогичного производному хиназолина в гетероциклических производных соединений в соответствии с настоящим изобретением, известны различные соединения (Международная Публикация WO 9307124, публикация прошедшего экспертизу патента Японии №2923742, 9720821, Международная Публикация WO 9850370, Международная Публикация WO 9909986, не прошедшая экспертизу патентная публикация Японии №47-2927, Международная Публикация WO 9817267 и тому подобные). Среди них в Международной Публикации WO 9720821 описано, что производное 2-ациламинохиназолина обладает ингибирующим действием на подтип-Y5 нейропептидного Y(NPY) рецептора и является эффективным для уменьшения интенсивности повышенной чувствительности к боли или амнезии.
Задачей настоящего изобретения является разработка нового соединения, обладающего превосходным анальгетическим действием. Более конкретно настоящее изобретение относится к новому анальгетику (болеутоляющему средству), обладающему анальгетическим действием, который очень эффективен против хронической боли или аллодинии, сопровождающейся опоясывающим лишаем, путем воздействия на ноцицептиновый (болевой) рецептор.
Задача настоящего изобретения достигается соединением, представленным следующей общей формулой (1), являющимся агонистом и/или антагонистом ноцицептинового рецептора и обладающим превосходным анальгетическим действием.
Соответственно настоящее изобретение относится к соединению, представленному следующей общей формулой (1):
или его соли.
В формуле Х и Y являются одинаковыми или различными, и каждый представляет собой атом азота или СН;
R1 представляет собой атом водорода или алкил;
А1 и А2 являются одинаковыми или различными, и каждый представляет собой (1) одинарную связь или (2) двухвалентную алифатическую углеводородную группу, которая может быть замещенной и может включать 1-3 ненасыщенные связи в любом положении (такая алифатическая углеводородная группа может содержать один гетероатом, выбранный из группы, состоящей из -NH-, О и S);
Q представляет собой (1) одинарную связь, (2) необязательно замещенную 3-8-членную циклоалкиленовую группу, (3) необязательно замещенную фениленовую группу или (4) необязательно замещенную 4-8-членную двухвалентную гетероциклическую группу;
R2А, R2С и R2D являются одинаковыми или различными, и каждый представляет собой атом водорода, алкил или фенил, R2B представляет собой атом водорода, алкил, циано, нитро или фенил, или два атома азота гуанидино-группы образуют цикл вместе с одним или двумя ее заместителями R2B, R2C и R2D с образованием насыщенного или ненасыщенного 5-или 6-членного кольца;
или взяты вместе в виде -N(R1)-A1-Q-A2-N(R2A)- с образованием 5-7-членного кольца;
Е представляет собой (1) этенилен, (2) -NRCO-, (3)
-NRCONH-, (4) -CONR-, (5) этинилен, (6) -NRSO2- или (7) аминоалкилен (где R представляет собой водород или необязательно замещенный алкил);
R3 представляет собой необязательно замещенную фенильную группу или гетероциклическую группу;
R4 и R5 (1) являются одинаковыми или различными, и каждый представляет собой атом водорода, алкил, алкокси, аралкилокси, галоген, нитро, гидрокси, алкоксикарбонил, -NR6R7, -NR6COR7, -NR6SO2R7, -CONR6R7 (в которых R6 и R7 являются одинаковыми или различными, и каждый представляет собой атом водорода или алкил), или (2) когда они являются смежными друг с другом, то взятые вместе образуют -O(СН2)nО (где n представляет собой целое число 1 или 2) или -СН=СН-СН=СН-.
Предпочтительно в формуле (1) каждый Х и Y представляет собой атом азота или СН;
R1 представляет собой атом водорода или алкил;
А1 и А2 являются одинаковыми или различными, и каждый представляет собой (1) одинарную связь или (2) алкилен, который может быть замещен алкилом, карбамоилом, моноалкилкарбамоилом, диалкилкарбамоилом, гидрокси, алкокси или трифторметилом и может содержать 1-3 ненасыщенные связи в любых положениях;
Q представляет собой (1) одинарную связь, (2) 3-8-членную циклоалкиленовую группу, которая может быть замещена алкилом, алкоксикарбонилом, карбамоилом, моноалкилкарбамоилом, диалкилкарбамоилом или алкокси, (3) фениленовую группу, которая может быть замещена алкилом, алкокси, алкоксикарбонилом, карбамоилом, моноалкилкарбамоилом, диалкилкарбамоилом, сульфамоилом, моноалкилсульфамоилом, диалкилсульфамоилом, амино, моноалкиламино, диалкиламино, нитро, галогеном, циано или трифторметилом, или (4) 4-8-членную двухвалентную гетероциклическую группу, которая может быть замещена алкилом, алкокси, алкоксикарбонилом, карбамоилом, моноалкилкарбамоилом, диалкилкарбамоилом, амино, моноалкиламино или диалкиламино;
R2A, R2C и R2D являются одинаковыми или различными, и каждый представляет собой атом водорода, алкил или фенил, R2B представляет собой атом водорода, алкил, цианогруппу, нитрогруппу или фенил, или два атома азота гуанидино-группы циклизованы вместе с одним или двумя ее заместителями R2B, R2C и R2D с образованием насыщенного или ненасыщенного 5-или 6-членного кольца;
или взяты вместе в виде -N(R1)-A1-Q-A2-N(R2A)- с образованием 5-7-членного кольца;
Е представляет собой (1) этенилен, (2) -NRCO-, (3) -NRCONH-, (4) -CONR-, (5) этинилен, (6) -NRSO2- или (7) аминоалкилен (в котором R представляет собой водород или необязательно замещенный алкил);
R3 представляет собой необязательно замещенную фенильную группу или гетероциклическую группу, которая может быть замещена алкилом, алкокси, алкоксикарбонилом, карбамоилом, моноалкилкарбамоилом, диалкилкарбамоилом, сульфамоилом, моноалкилсульфамоилом, диалкилсульфамоилом, алкилсульфониламино, N-(алкил)алкилсульфониламино, амино, моноалкиламино, диалкиламино, нитро, галогеном, циано, гидрокси или трифторметилом, и
R4 и R5 (1) являются одинаковыми или различными, и каждый представляет собой атом водорода, алкил, алкокси, аралкилокси, галоген, нитро, гидрокси, алкоксикарбонил, -NR6R7, -NR6COR7, -NR6SO2R7, -CONR6R7 (в которых R6 и R7 являются одинаковыми или различными, и каждый представляет собой атом водорода или алкил) или (2) когда они являются смежными друг с другом, то взятые вместе образуют -O(СН2)nО (где n представляет собой целое число 1 или 2) или -СН=СН-СН=СН-.
Более предпочтительное соединение представлено общей формулой (1), где каждый Х и Y представляет собой атом азота, R1 представляет собой атом водорода или алкил, А1 и А2 являются одинаковыми или различными, и каждый представляет собой (1) одинарную связь или (2) необязательно замещенный алкилен, Q представляет собой (1) одинарную связь, (2) необязательно замещенную 4-8-членную циклоалкиленовую группу, (3) необязательно замещенную фениленовую группу или (4) необязательно замещенную 5-7-членную двухвалентную гетероциклическую группу, R2A, R2B, R2C и R2D являются одинаковыми или различными, и каждый представляет собой атом водорода, алкил или фенил, или взятые вместе в виде -N-(R1)-A1-Q-A2-N-(R2A)- образуют 5-7-членное кольцо, Е представляет собой (1) этенилен, (2) -NRCO- или (3) -CONR-, и R4 и R5 (1) являются одинаковыми или различными, и каждый представляет собой атом водорода, алкил, алкокси, аралкилокси, галоген, нитро, гидрокси или алкоксикарбонил, или (2) когда они являются смежными друг с другом, то взятые вместе образуют -O(СН2)nО- (где n представляет собой целое число 1 или 2) или -СН=СН-СН=СН-.
Дополнительное предпочтительное соединение представлено общей формулой (1), где каждый Х и Y представляет собой атом азота, R1 является водородом. А1 и А2 являются одинаковыми или различными, и каждый представляет собой (1) одинарную связь или (2) необязательно замещенный алкилен, Q представляет собой (1) одинарную связь, (2) необязательно замещенную 5-7-членную циклоалкиленовую группу, (3) необязательно замещенную фениленовую группу, R2A, R2B, R2C и R2D являются одинаковыми или различными, и каждый представляет собой атом водорода, алкил или фенил, Е представляет собой (1) этенилен, (2) -NRCO-, и R4 и R5 являются одинаковыми или различными, и каждый представляет собой атом водорода, алкил, алкокси, аралкилокси, галоген или нитро.
Кроме того, настоящее изобретение относится к фармацевтической композиции, включающей любое из вышеуказанных соединений или его соль, и более конкретно к анальгетику.
Структурными признаками соединения настоящего изобретения являются следующие: присутствие гуанидиновой группы на конце заместителя, -N(R1)-A1-Q-A2-, в 4-положении хиназолиновой или хинолиновой структуры или в 1-положении изохинолиновой структуры; или циклизация двух NH групп в гуанидиновой группе вместе с заместителем после этого.
Соединение согласно настоящему изобретению, которое имеет описанную выше характерную особенность, представляет собой новое соединение, которое не было раскрыто в ссылках. Соединение согласно настоящему изобретению действует на ноцицептиновый рецептор, оказывая тем самым превосходное анальгетическое действие.
Далее настоящее изобретение будет описано подробно.
Примеры «алкила» в настоящем изобретении могут включать линейный или разветвленный алкил, имеющий от 1 до 6 атомов углерода, например метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, 5-изопентил, н-гексил, изогексил и тому подобные. В частности, предпочтительным является алкил, содержащий от 1 до 4 атомов углерода.
Примеры «алкокси» могут включать линейную или разветвленную алкокси-группу, содержащую от 1 до 6 атомов углерода, например метокси, этокси н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, н-пентилокси, изопентилокси, н-гексилокси, изогексилокси и тому подобные. В частности, предпочтительным является алкокси, содержащий от 1 до 4 атомов углерода.
Примеры «аралкилокси» могут включать аралкилокси, содержащий от 7 до 10 атомов углерода, например бензилокси, фенэтилокси и тому подобные. В частности, предпочтительным является бензилокси.
Примеры «двухвалентной алифатической углеводородной группы» могут включать линейный или разветвленный алкилен, содержащий от 1 до 6 атомов углерода (например, метилен, этилен, триметилен, тетраметилен, пентаметилен, гексаметилен, 2-этилтриметилен и 1-метилтетраметилен), линейный или разветвленный алкенилен, содержащий от 2 до 6 атомов углерода (например, винилен или пропенилен) или линейный или разветвленный алкинилен, содержащий от 2 до 6 атомов углерода (например, этинилен). Такая алифатическая углеводородная группа может содержать один гетероатом, выбранный из группы, состоящей из NH, атома кислорода и атома серы.
Примеры алкилена в «аминоалкилене» могут включать алкилен, перечисленный в «двухвалентной алифатической углеводородной группе».
Примеры «циклоалкилена» могут включать циклоалкилен, содержащий от 3 до 8 атомов углерода, например циклопропилен, циклобутилен, циклопентилен, циклогексилен, циклогептилен и циклооктилен. Такой циклоалкилен может содержать 1-2 заместителя, и примеры таких заместителей могут включать алкил, алкоксикарбонил, карбамоил, моноалкилкарбамоил, диалкилкарбамоил или алкокси. Он также может содержать ненасыщенную связь, и примеры циклоалкилена, содержащего такую ненасыщенную связь, включают циклогексенилен, циклогептенилен, циклооктенилен и тому подобные.
Примеры «галогена» могут включать атомы фтора, хлора, брома и иода.
Примеры гетероциклического кольца в «гетероциклической группе» и «двухвалентной гетероциклической группе» могут включать 4-8-членное моноциклическое или конденсированное кольцо, которое содержит 1-2 гетероатома, выбранные из группы, состоящей из NH, атома кислорода и атома серы, и которое может содержать 1-4 ненасыщенные связи. Примеры R3 могут включать 2-пиридил, 3-пиридил, 4-пиридил, 2-пиримидинил, 4-пиримидинил, 5-пиримидинил, 3-пиридазинил, 4-пиридазинолил, 2-пиразинил и 3-пиразинил. Такая гетероциклическая группа может содержать 1-2 заместителя и примеры заместителей могут включать алкил, алкокси, алкоксикарбонил, карбамоил, моноалкилкарбамоил, диалкилкарбамоил, сульфамоил, моноалкилсульфамоил, диалкилсульфамоил, алкилсульфониламино, N-(алкил) алкилсульфониламино, амино, моноалкиламино, диалкиламино, нитро, галоген, циано, гидрокси или трифторметокси. Примеры гетероциклического кольца в гетероциклической группе Q могут включать пиридин, пиримидин, пиперазин, гомопиперазин, фуран, тиофен и тому подобные. Гетероциклическая группа Q может содержать 1-2 заместителя, и примеры таких заместителей могут включать алкил, алкокси, алкоксикарбонил, карбамоил, моноалкилкарбамоил, диалкилкарбамоил, амино, моноалкиламино или диалкиламино.
«Фениленовая группа» может содержать 1-2 заместителя, и примеры таких заместителей могут включать алкил, алкокси, алкоксикарбонил, карбамоил, моноалкилкарбамоил, диалкилкарбамоил, сульфамоил, моноалкилсульфамоил, диалкилсульфамоил, амино, моноалкиламино, диалкиламино, гидрокси, нитро, галоген, циано и трифторметил.
Пример кольца, представленного -N(R1)-A1-Q-A2-N(R2A)- могут включать 5-7-членное насыщенное кольцо, такое как пиперазино или гомопиперазино.
Примеры «соли» соединения (1), охватываемые настоящим изобретением, могут включать соль неорганической кислоты, такой как хлористоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, фтористоводородная кислота или бромистоводородная кислота, или соль органической кислоты, такой как уксусная кислота, винная кислота, молочная кислота, лимонная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, толуолсульфоновая кислота, нафталинсульфоновая кислота или камфорсульфоновая кислота.
Примеры особенно предпочтительного соединения могут включать дигидрохлорид (1S,2R)-N-амидино-2-{[2(4-хлорбензоиламино)-6-метоксихиназолин-4-ил]амино} циклогексиламина, тригидрохлорид N-амидино-2-[6-метокси-4-{2-[2-(2-пиридил)этенил]хиназолин-4-ил)аминоэтил]фенилэтиламина, тригидрохлорид цис-4-гуанидинометил-цис-2-метил-N-{6-метокси-2-[2-{2-пиридил)этенил]хиназолин-4-ил}циклогексиламина, тригидрохлорид N-амидино-N'-{6-метил-2-[2-(2-пиридил)этенил] хиназолин-4-ил}-1,6-гександиамина, дигидрохлорид (1S,2R)-цис-N-амидино-2-{[2-(4-хлорстирил)-6-метоксихиназолин-4-ил]амино} циклогексиламина и тригидрохлорид N-амидино-N'-{6-метокси-2-[2-(2-пиридил)этенил]хиназолин-4-ил}-1,6-гександиамина.
Соединение согласно настоящему изобретению может существовать в виде цис (Z-форма) изомера или транс (Е форма) изомера, и каждый изомер и их смесь также включены в настоящее изобретение.
Некоторые соединения согласно настоящему изобретению могут иметь асимметрические атомы углерода и каждый оптический изомер и их рацематы также включены в настоящее изобретение. Оптический изомер можно получать, например, исходя из рацемата, полученного как описано выше, с использованием его основных свойств, используя оптически активную кислоту (винную кислоту, дибензоилвинную кислоту, миндальную кислоту, 10-камфорсульфоновую кислоту и тому подобные) известным способом для осуществления оптического разделения, или исходя из предварительно полученного оптически активного соединения.
Соединение (1) согласно настоящему изобретению может быть получено, например, следующими способами.
Способ получения А
(где X, Y, R1, R2A R2B, R2c, R2D, R3, R4, R5, A1, A2, Q и Е имеют описанные выше значения. R2b и R2c являются одинаковыми или разными, и каждый представляет собой атом водорода, алкил, фенил, циано, нитро или защитную группу. L представляет собой уходящую группу.)
Примеры защитной группы могут включать трет-бутоксикарбонил, бензилоксикарбонил, бензил и тому подобные. Примеры уходящей группы могут включать пиразол-1-ил, метилтио, метокси, галоген и тому подобные. Соединение (2) подвергают взаимодействию с соединением (3) в количестве от одного эквивалента до избыточного количества в углеводородах, таких как бензол и толуол, простых эфирах, таких как диоксан и тетрагидрофуран, галогенированных углеводородах, таких как хлороформ, хлористый метилен и 1,2-дихлорэтан, или в N,N-диметилформамиде при температуре от 0°С до температуры кипения используемого растворителя в течение от нескольких часов до нескольких дней с последующим снятием защитных групп R2b и R2c, когда они присутствуют в качестве защитных групп, с использованием известного самого по себе способа, получая таким образом соединение (1). Особенно предпочтительно использовать пиразол-1-ил в качестве уходящей группы L в соединении (3) и трет-бутоксикарбонил в качестве защитной группы, 1,2-дихлорэтан в качестве растворителя и проводить реакцию при комнатной температуре в течение от 1 до 48 часов с последующим снятием защиты хлористоводородной кислотой.
Способ получения В (где R2B в соединении (1) представляет собой атом водорода)
(где X, Y, R1, R2A, R2B, R2C, R2D, R4, R5, A1, A2, Q и Е имеют описанные выше значения.
Соединение (1a) может быть получено взаимодействием соединения (2) с R2CR2DN-CN по известному способу (J. Med. Chem., 18, 90, 1975 и тому подобные).
Способ получения С (где R2D в соединении (1) представляет собой атом водорода)
(где X, Y, R1, R2A, R2B, R2C, R3, R4, R5, A1, A2, Q и Е имеют описанные выше значения.
Соединение (1b) может быть получено взаимодействием соединения (2) с R2B-N=C=N-R2C по известному способу (J. Am.Chem. Soc., 3673, 1962 и тому подобные).
Способ получения D
(где X, Y, R1, R2A, R2B, R2C, R2D, R3, R4, R5, A1, A2, Q и Е имеют описанные выше значения. R8 представляет собой алкил).
Соединение (1) может быть получено из соединения (120) известным способом (Synthesis, 6, 460, 1988 и тому подобные). Алкил в качестве R8 представляет собой алкил, имеющий от 1 до 4 атомов углерода и предпочтительно представляет собой метил.
Способ получения Е
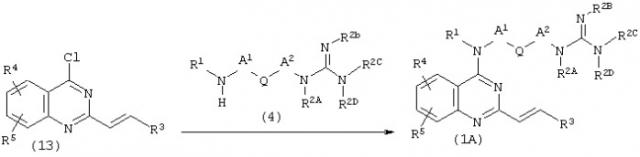
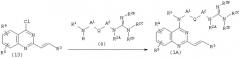
Соединение (1А), которое представляет собой соединение (1), где Е представляет собой этенилен, оба Х и Y представляют собой N, может быть получено по представленной ниже реакции:
(где R1, R2A, R2B, R2C, R2D, R3, R4, R5, A1, A2, R2b, R2c и Q имеют описанные выше значения).
Соединение (13) подвергают взаимодействию с амином (4) в количестве от одного эквивалента до избыточного количества в присутствии основания, такого как гидрид натрия или N,N-диизопропилэтиламин, в растворителе, имеющем высокую температуру кипения, таком как 1-пентанол, N,N-диметилформамид или фенол, при температуре от 50°С до температуры кипения используемого растворителя в течение от нескольких часов до нескольких суток с последующим снятием защитных групп R2b и R2c, когда они присутствуют в качестве защитных групп, с использованием известного способа, получая таким образом соединение (1А). Предпочтительно взаимодействие проводят в феноле при 150-180°С в течение 5-24 часов с последующим снятием защиты с использованием хлористоводородной кислоты, получая соединение (1А).
Способ получения F
Соединение (1Z), которое представляет собой соединение (1), где Е представляет собой -NRCO-, и оба Х и Y представляют собой N, также может быть получено представленным ниже реакционным способом:
(где R, R1, R2A, R2B, R2C, R2D, R3, R4 R5, A1, A2, R2b, R2c и Q имеют описанные выше значения).
Соединение (37В) подвергают взаимодействию с соединением (3) в количестве от одного эквивалента до избыточного количества в углеводородах, таких как бензол и толуол, простых эфирах, таких как диоксан и тетрагидрофуран, галогенированных углеводородах, таких как хлороформ, хлористый метилен и 1,2-дихлорэтан, или в N,N-диметилформамиде при температуре от 0°С до температуры кипения используемого растворителя в течение от нескольких часов до нескольких дней, получая таким образом соединение (37А). Особенно предпочтительно использовать пиразол-1-ил в качестве уходящей группы L в соединении (3), трет-бутоксикарбонил в качестве защитной группы и 1,2-дихлорэтан в качестве растворителя.
Соединение (37А) подвергают взаимодействию с хлорангидридом кислоты в количестве от одного эквивалента до избыточного количества в углеводородах, таких как бензол и толуол, простых эфирах, таких как диоксан и тетрагидрофуран, галогенированных углеводородах, таких как хлористый метилен, 1,2-дихлорэтан и хлороформ, в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин или пиридин, с использованием при необходимости катализатора, такого как 4-диметиламинопиридин, при температуре от комнатной до температуры кипения используемого растворителя в течение от нескольких часов до нескольких дней с последующим снятием защитных групп R2b и R2c, когда они присутствуют в качестве защитных групп, с использованием известного способа, получая таким образом соединение (1Z).
Полученное таким образом соединение (1) может быть выделено и очищено известными методами, такими как концентрирование, преобразование жидкой фазы, разделение, экстракция растворителем, кристаллизация, перекристаллизация, фракционная перегонка или хроматография.
Исходное соединение (2) может быть получено в соответствии со следующей реакционной схемой.
(а) Когда Е представляет собой этенилен, и оба Х и Y представляют собой N в соединении (2):
(где R1, R2, R3, R4, R5, А1, А2 и Q имеют описанные выше значения. Р1 представляет собой защитную группу).
Примеры защитной группы могут включать трет-бутоксикарбонил, бензилоксикарбонил и тому подобные.
Соединение (13) (полученное аналогично описанному на стр.13-15 в Международной Публикации WO 9909986) подвергают взаимодействию с амином (14) в количестве от одного эквивалента до избыточного количества в углеводородах, таких как бензол и толуол, простых эфирах, таких как диоксан и тетрагидрофуран, спиртах, таких как этанол и изопропанол, или в органическом растворителе, таком как N,N-диметилформамид, при необходимости в присутствии основания, такого как триэтиламин или N,N-диизопропилэтиламин, при температуре от комнатной температуры до температуры кипения используемого растворителя в течение от нескольких часов до нескольких дней с последующим снятием защиты хлористоводородной кислотой, трифторуксусной кислотой или путем гидрирования с использованием палладия-на-углероде, получая таким образом соединение (2А). Особенно предпочтительно, чтобы соединение (13) подвергали взаимодействию с 1-2 эквивалентами амина (14), в котором Р1 представляет собой трет-бутоксикарбонил, в толуоле в качестве растворителя в присутствии триэтиламина (ТЭА) при 100-130°С в течение 24-48 часов, а затем снятие защиты осуществляли хлористоводородной кислотой.
(b) Когда Е представляет собой этенилен, Х представляет собой СН, Y представляет собой N в соединении (2):
(где R1, R2A, R3, R4, R5, А1, A2, Q и Р1 имеют описанные выше значения).
Для получения соединения (19) используют известный способ (JACS 70, 4065 (1948); JACS 70, 2402 (1948); JOC 12, 456 (1947) и тому подобные), исходя из соединения (16).
Соединение (19) подвергают взаимодействию с альдегидом (11) в растворителе, таком как уксусный ангидрид, уксусная кислота или трифторуксусная кислота при температуре от комнатной температуры до температуры кипения используемого растворителя в течение 1-48 часов, предпочтительно в уксусном ангидриде в качестве растворителя при 80-100°С в течение 5-24 часов, получая таким образом соединение (20). Альдегид (11) может быть коммерчески доступным или может быть получен известным способом.
Соединение (20) подвергают взаимодействию с хлорирующим агентом, таким как оксихлорид фосфора или пентахлорид фосфора, без использования какого-либо растворителя или в растворителе, таком как толуол, ксилол или 1,2-дихлорэтан, при температуре от комнатной температуры до температуры кипения используемого растворителя или при температуре от комнатной температуры до температуры кипения используемого хлорирующего агента в том случае, когда растворитель не используется, в течение 1-24 часов, получая таким образом соединение (21). При такой методике при необходимости может присутствовать третичный амин, такой как диметиланилин или триэтиламин.
Соединение (21) подвергают взаимодействию с амином (14) в количестве от одного эквивалента до избыточного количества, так как описано выше в (а), а затем, при необходимости, проводят снятие защиты с использованием известного способа, получая соединение (2В). Особенно предпочтительно, чтобы соединение (21) взаимодействовало с 1-2 эквивалентами амина (14), в котором Р1 представляет собой трет-бутоксикарбонил, в толуоле в качестве растворителя в присутствии триэтиламина при 100-130°С в течение 24-48 часов, давая соединение (22), в котором затем снимают защиту с помощью трифторуксусной кислоты в хлористом метилене.
(с) Когда Е представляет собой этенилен, Х представляет собой N, и Y представляет собой СН в соединении (2):
(где R1, R2A, R3, R4, R5, А1, A2, Q и Р1 имеют описанные выше значения).
Исходя из соединения 23, используя известный способ (J. Chem. Soc. Perkin Trans., 1, 1990, 1770), получают соединение (24).
Соединение (24) подвергают взаимодействию с 1-3 эквивалентами диоксида селена в простых эфирах, таких как диоксан и тетрагидрофуран, или спиртах, таких как этанол и изопропанол, при температуре от комнатной температуры до температуры кипения используемого растворителя в течение от нескольких часов до нескольких дней, предпочтительно в диоксане при 50-100°С в течение 5-48 часов, получая таким образом соединение (25).
Соединение (25) подвергают взаимодействию с соединением (26) или соединением (27) в растворителе, который не участвует в реакции, таком как диоксан или тетрагидрофуран, в присутствии основания, такого как н-бутиллитий, гидрид натрия или гексаметилдисилазид натрия, при температуре от -78°С до температуры кипения используемого растворителя в течение от нескольких часов до нескольких дней, предпочтительно в тетрагидрофуране при температуре от -20°С до комнатной температуры в течение 1-5 часов, получая таким образом соединение (28).
Аналогично методике описанной выше в части (b) соединение (28) взаимодействует с хлорирующим агентом, таким как оксихлорид фосфора или пентахлорид фосфора, в течение 1-24 часов, давая соединение (29). Соединение (29) взаимодействует с амином (14) в количестве от одного эквивалента до избыточного количества, как описано выше в части (а), а затем при необходимости проводят снятие защитных групп известным самим по себе способом, получая соединение (2С).
(d) Когда Е представляет собой -NRCO-, и оба Х и Y представляют собой N в соединении (2):
(где R, R1, R2A, R3, R4, R5, A1, A2, Q и Р1 имеют описанные выше значения. X представляет собой гидроксильную группу или аминогруппу. Р2 представляет собой атом водорода или защитную группу, такую как бензил или 4-метоксибензил).
Соединение (34) может быть получено из соединений (31) и (32) в соответствии с известным способом (патент Японии №2923742).
Соединение (34) подвергают взаимодействию с амином (14) в количестве от одного эквивалента до избыточного количества в таком же растворителе, как в описанной выше части (а), при необходимости в присутствии основания, такого как триэтиламин или N,N-диизопропилэтиламин, при температуре от 0°С до температуры кипения используемого растворителя в течение от нескольких часов до нескольких дней, предпочтительно в присутствии триэтиламина при комнатной температуре в течение 5-48 часов, получая при этом соединение (35).
Соединение (35) подвергают взаимодействию с амином (36) в количестве от одного эквивалента до избыточного количества в растворителе, имеющем высокую температуру кипения, таком как фенол или дифениловый простой эфир, при необходимости в присутствии основания, такого как триэтиламин или N,N-диизопропилэтиламин, при температуре от комнатной температуры до температуры кипения используемого растворителя в течение от нескольких часов до нескольких дней, или в углеводородах, таких как бензол, толуол и ксилол, простых эфирах, таких как диоксан и тетрагидрофуран, в присутствии металлического катализатора, такого как ацетат палладия, лиганда, такого как 2,2'-бис(дифенилфосфино)-1,1'-бинафтил, и основания, такого как трет-бутоксид натрия, при температуре от комнатной температуры до температуры кипения используемого растворителя в течение от нескольких часов до нескольких дней с последующим снятием защитной группы Р2, когда она присутствует в качестве защитной группы, с использованием способа, не оказывающего действия на Р1, при этом получая соединение (37).
Соединение (37) подвергают взаимодействию с хлорангидридом кислоты в количестве от одного эквивалента до избыточного количества в углеводородах, таких как бензол и толуол, простых эфирах, таких как диоксан и тетрагидрофуран, галогенированных углеводородах, таких как хлористый метилен, 1,2-дихлорэтан и хлороформ, в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин или пиридин, при необходимости с использованием катализатора, такого как 4-диметиламинопиридин, при температуре от комнатной температуры до температуры кипения используемого растворителя в течение от нескольких часов до нескольких дней, получая таким образом соединение (38). Для получения соединения (2D) в соединение (38) снимают защитную группу с помощью известного самого по себе способа. Особенно предпочтительно проводить взаимодействие с использованием хлористого метилена в качестве растворителя в присутствии триэтиламина, используя каталитическое количество 4-диметиламинопиридина, при комнатной температуре в течение 24-48 часов. Хлорангидрид кислоты может быть коммерчески доступным или может быть получен известным способом.
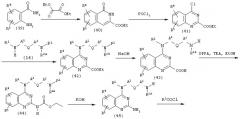
(е) Когда Е представляет собой -NHCO-, и оба Х и Y представляют собой N в соединении (2):
(где R1, R2A, R3, R4, R5, A1, A2, Q и Р1 имеют описанные выше значения).
Исходя из соединения (39), для получения соединения (41) используют известный способ (см. JOC, 27, 4672 (1962).
Соединение (41) подвергают взаимодействию с амином (14) в количестве от одного эквивалента до избыточного количества аналогично описанному выше в части (а), получая соединение (42). Особенно предпочтительно проводить взаимодействие соединения (41) с 1-2 эквивалентами амина (14) в толуоле в качестве растворителя в присутствии триэтиламина (ТЭА) при 100-130°С в течение 24-48 часов.
Гидролизом соединения (42) известным способом получают соединение (43). Особенно предпочтительно проводить взаимодействие соединения (42) в этаноле в присутствии 1н. водного раствора гидроксида натрия при температуре от комнатной температуры до 60°С в течение 1-3 часов.
Соединение (43) подвергают взаимодействию с дифенилфосфорилазидом (DPPA) в спиртах, таких как этанол и бензиловый спирт, в присутствии основания, такого как триэтиламин или N,N-диизопропилэтиламин, при температуре от комнатной температуры до температуры кипения используемого растворителя в течение от нескольких часов до нескольких дней, получая таким образом соединение (44). Особенно предпочтительно проводить взаимодействие соединения (43) в кипящем с обратным холодильником этаноле в присутствии триэтиламина в течение 24-48 часов.
Соединение (44) гидролизуют известным способом, который не оказывает воздействия на Р1, получая таким образом соединение (45). Особенно предпочтительно проводить взаимодействие соединения (44) в метаноле в присутствии гидроксида калия при температуре от комнатной температуры до 60°С в течение 1-3 часов.
Соединение (45) подвергают взаимодействию с хлорангидридом кислоты в количестве от одного эквивалента до избыточного количества в углеводородах, таких как бензол и толуол, простых эфирах, таких как диоксан и тетрагидрофуран, галогенированных углеводородах, таких как хлористый метилен и 1,2-дихлорэтан, в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин или пиридин, при необходимости с использованием катализатора, такого как 4-диметиламинопиридин, при температуре от комнатной температуры до температуры кипения используемого растворителя в течение от нескольких часов до нескольких дней, получая таким образом соединение (46). Особенно предпочтительно проводить взаимодействие с использованием хлористого метилена в качестве растворителя в присутствии триэтиламина, используя каталитическое количество 4-диметиламинопиридина, при комнатной температуре в течение 24-48 часов.
В соединении (46) известным способом снимают защитные группы, получая соединение (2Е). Когда Р1 представляет собой трет-бутоксикарбонил, предпочтительным является проводить взаимодействие с трифторуксусной кислотой в хлористом метилене при комнатной