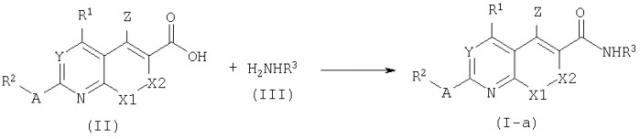Бициклические гетероароматические соединения, фармацевтическая композиция на их основе и применение
Иллюстрации
Показать всеИзобретение относится к новым бициклическим гетероароматическим соединениям общей формулы (I) где R1 представляет фенил, необязательно замещенный NHR5 или OR5; R2 представляет С1-С4алкил или фенил; R5 представляет фенилкарбонил, С4-С6 гетероциклоалкилкарбонил, C2-C8 алкенилсульфонил и др.; Y представляет N; Z представляет NH2 или ОН; А представляет S или связь; В представляет N(H) или О; X1-Х2 представляет С=С, NH-C(O), C=N и др. Указанные соединения обладают агонистической активностью в отношении LH рецептора и могут найти применение в медицине. 4 н. и 6 з.п. ф-лы.
Реферат
Изобретение относится к соединениям, обладающим агонистической или антагонистической активностью в отношении гликопротеинового гормона, в частности к соединениям, обладающим агонистической активностью в отношении лютеинизирующего гормона (LH). Кроме того, изобретение относится к бициклическим гетероароматическим производным, содержащим их фармацевтическим композициям, а также к применению данных соединений в медицинской терапии, в частности для использования для регулирования фертильности.
Гонадотропины выполняют важные функции во множестве функций тела, включая метаболизм, температурную регуляцию и репродуктивный процесс. Гипофизарный гонадотропин FSH, например, играет основную роль в стимуляции развития и созревании фолликула, тогда как LH индуцирует овуляцию (Sharp R.M. Clin. Endocrinol. 33:787-807, 1990; Dorrington and Armstrong, Recent Prog.Horm.Res. 35:301-342, 1979). В настоящее время LH применяется клинически, в сочетании с FSH, для стимуляции яичников, например, для гиперстимуляции яичников для оплодотворения in vitro (IVF) и индуцирования овуляции у бесплодных неовулирующих женщин (Insler V., Int.J.Fertility 33:85-97, 1988, Navot and Rosenwaks, J.Vitro Fert. Embryo Transfer 5:3-13, 1988), а также при недоразвитии половой системы у мужчин и мужском бесплодии.
Гонадотропины действуют на специфические гонадные типы клеток для инициирования яичниковой и тестикулярной модификации и стероидогенеза. Действие данных слизистых и плацентарных гормонов опосредовано специфическими плазматическими мембранными рецепторами, которые принадлежат к большому семейству G-протеин-связанных рецепторов. Они состоят из единственного полипептида с семью трансмембранными доменами и способны взаимодействовать с Gs белком, приводя к активации аденилциклазы.
Гонадотропины, предназначенные для терапевтических целей, могут быть выделены из мочи человека в качестве источников и имеют низкую чистоту (Morse et al., Amer.J.Reproduct. Immunol. And Microbiology 17:143, 1988). Альтернативно, они могут быть получены в качестве рекомбинантных гонадотропинов.
Как и в случае других терапевтических белков, гонадотропины необходимо вводить либо подкожно, либо внутримышечно. Однако было бы предпочтительно активировать рецептор маленькими молекулами, которые можно было бы вводить, например, пероральным или чрескожным путями.
В настоящем изобретении описано получение таких низкомолекулярных аналогов гормонов, которые селективно активируют один из гонадотропиновых рецепторов, что является одним из основных преимуществ настоящего изобретения.
Таким образом, изобретение относится к бициклическим гетероароматическим производным общей формулы I или их фармацевтически приемлемым солям
где
R1 представляет собой С3-С8циклоалкил, С2-С7гетероциклоалкил, С6-С14арил или С4-С13гетероарил; предпочтительно R1 представляет собой С6-С14арил или С4-С13гетероарил;
R2 представляет собой С1-С4алкил, С2-С4алкенил, С2-С4алкинил, С6-С14арил или С4-С13гетероарил;
R3 представляет собой С1-С8алкил, С3-С8циклоалкил, С2-С7гетероциклоалкил, С6-С14арил или С4-С13гетероарил;
Y представляет собой СН или N;
Z представляет собой NH2 или ОН;
А представляет собой S, N(H), N(R4), O или связь;
R4 может быть выбран из групп, которые описаны для R2, и В представляет собой N(H), О или связь.
Кольцевая система в R1 необязательно может быть замещена одним или несколькими заместителями, выбранными из R5,N(R4)R5, NHR5, OR5 и/или SR5, в которых R5 представляет собой С6-С14арил, С4-С13гетероарил, С6-С14арилкарбонил, С2-С7гетероциклоалкил, С3-С8циклоалкил, С6-С14арилсульфонил, С6-С14ариламинокарбонил, С6-С14арилоксикарбонил, С6-С14ариламиносульфонил, С6-С14арилоксисульфонил, С2-С8алкенил, С2-С8алкинил, С2-С7гетероциклоалкилкарбонил, С2-С8алкенилсульфонил, С2-С8алкеноксикарбонил, или С1-С8алкил, С1-С8алкилкарбонил, С1-С8алкилсульфонил, С1-С8(ди)алкиламинокарбонил, С1-С8алкоксикарбонил, С1-С8(ди)алкиламиносульфонил или С1-С8алкоксисульфонил, алкильная группа в которых необязательно может быть замещена одним или несколькими заместителями, выбранными из гидроксила, С1-С8алкокси, С2-С7гетероциклоалкил(С1-С8)алкокси, С3-С8циклоалкил(С1-С8)алкокси, С6-С14арил(С1-С8)алкокси, С4-С13гетероарилС1-С8алкокси, С2-С7гетероциклоалкила, С3-С8циклоалкила, С6-С14арила, С4-С13гетероарила, С1-С8алкоксикарбонила, С6-С14арилоксикарбонила, С1-С8алкилкарбонилокси, С6-С14арилкарбонилокси, С1-С8алкилкарбонила, С6-С14арилкарбонила, амина, С1-С8алкиламинокарбонила, С6-С14ариламинокарбонила, С1-С8алкилкарбониламино, С6-С14арилкарбониламино, С6-С14(ди)ариламино, (ди)[С1-С3алкокси(С1-С3)алкил]амино и/или С1-С8(ди)алкиламино. Предпочтительно заместители в R1 выбирают из NHR5 или OR5. R5 в любом из заместителей при R1 предпочтительно представляет собой С2-С7гетероциклоалкилкарбонил, С6-С14арилкарбонил или С1-С8алкил, С1-С8алкилкарбонил или С1-С8(ди)алкиламинокарбонил, алкильная группа в которых необязательно может быть замещена С2-С7гетероциклоалкилом, С4-С13гетероарилом, С1-С8алкоксикарбонилом, С1-С8алкиламинокарбонилом, С1-С8алкилкарбониламино, С6-С14арилкарбониламино, амином, и/или С1-С8(ди)алкиламино. Наиболее предпочтительные заместители в алкильной группе представляют собой С2-С7гетероциклоалкил, С1-С8(ди)алкиламино, амин и С1-С8(ди)алкиламинокарбонил.
Наиболее предпочтительным в R1 является фенил, необязательно замещенный одним из выше указанных заместителей, предпочтительно замещение осуществлено в мета-положении.
В соединениях изобретения Х1-Х2 представляет собой С=С, C(O)-NH, NH-C(O), C(O)-О, O-C(O), C=N или N=C. Если R5 представляет собой С1-С8алкилсульфонил, С6-С14арилсульфонил, С1-С8(ди)алкиламинокарбонил, С6-С14ариламинокарбонил, С1-C8алкоксикарбонил, С6-С14арилоксикарбонил, С1-С8(ди)алкиламиносульфонил, С6-С14ариламиносульфонил, С1-С8алкоксисульфонил, С2-С7гетероциклоалкилкарбонил, С2-С8алкенилсульфонил, С2-С8алкеноксикарбонил или С6-С14арилоксисульфонил, то Х1-Х2 дополнительно могут представлять собой S или О.
Предпочтительными соединениями согласно изобретению являются соединения общей формулы I, где В представляет собой N(H) или связь, и/или Z представляет собой NH2. Среди таких предпочтительных соединений особенно предпочтительными являются те, в которых В представляет собой N(H) или связь, и Z представляет собой NH2. Более предпочтительными являются соединения, в которых предпочтительно в дополнение к указанным отмеченным определениям В и Z, R1 определятся как С6-С14арил или С4-С13гетероарил, необязательно замещенный одним или несколькими заместителями, выбранными из N(R4)R5, NHR5, R5, OR5 и/или SR5, предпочтительно NHR5 или OR5.
Предпочтительно, во всех вышеуказанных соединениях Y представляет N, предпочтительным для В является N(H) или связь. Если В представляет собой связь, то R3 предпочтительно представляет собой C2-C7гетероциклоалкил.
Кроме того, во всех вышеуказанных соединениях Х1-Х2 предпочтительно представляет собой С=С, C=N или N=C, наиболее предпочтительно С=С.
Если R5 представляет собой С1-С8алкилсульфонил, С6-С14арилсульфонил, С1-С8(ди)алкиламинокарбонил, С6-С14ариламинокарбонил, С1-С8алкоксикарбонил, С6-С14арилоксикарбонил, С1-С8(ди)алкиламиносульфонил, С6-С14ариламиносульфонил, С1-С8алкоксисульфонил, C2-C7гетероциклоалкилкарбонил, С2-С8алкенилсульфонил, С2-С8алкеноксикарбонил или С6-С14арилоксисульфонил, тогда предпочтительным для Х1-Х2, в дополнение к вышеуказанным группам, также является S.
Наиболее предпочтительными являются соединения, выбранные из группы, включающей трет-бутил 5-амино-2-метилтио-4-(3-((N,N-диэтиламино)карбонилокси)фенил)тиено[2,3-d]пиримидин-6-карбоксамид, трет-бутил 5-амино-2-метилтио-4-(3-(метоксикарбониламино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид, трет-бутил 5-амино-2-метилтио-4-(3-(аллилоксикарбонил-амино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид, трет-бутил 5-амино-2-метилтио-4-(3-(этоксикарбониламино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид, трет-бутил 5-амино-2-метилтио-4-(3-((морфолин-4-ил)карбониламино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид, трет-бутил 5-амино-2-метилтио-4-(3-(1,2,3,6-тетрагидропиридино-карбониламино)фенил)тиено[2,3-d]пиримидин-6-карбоксамид, трет-бутил 5-амино-2-фенил-4-(3-((N,N-диметиламино)карбонилокси)фенил)тиено[2,3-d]пиримидин-6-карбоксамид.
Такие соединения как этил 5-гидрокси-2-метил-4-(пиперидин-1-ил)-пиридо[2,3-d]пиримидин-6-карбоксилат, этил 5-гидрокси-2-метил-4-(морфолин-4-ил)-пиридо[2,3-d]пиримидин-6-карбоксилат или этил 5-гидрокси-2-метил-4-(пирролидин-1-ил)пиридо[2,3-d]пиримидин-6-карбоксилат исключены из объема настоящего изобретения.
Исключение связано с раскрытием данных соединений в Chem. Pharm. Bull., 18(7), 1385-1393 (1970).
Термин С1-С8алкил, как он использован в определении формулы I, означает разветвленную или неразветвленную алкильную группу, имеющую 1-8 атомов углерода, например, метил, этил, пропил, изопропил, бутил, втор-бутил, трет-бутил, гексил и октил. C1-C6Алкильные группы являются предпочтительными, C1-C3алкильные группы являются наиболее предпочтительными.
Термин С2-С8алкенил означает разветвленную или неразветвленную алкенильную группу, имеющую 2-8 атомов углерода, такую как этенил, 2-бутенил и т.д. C1-C6Алкенильные группы являются предпочтительными, C1-C3алкенильные группы являются наиболее предпочтительными.
Термин С2-С8алкинил означает разветвленную или неразветвленную алкинильную группу, имеющую 2-8 атомов углерода, такую как этинил и пропинил. Наиболее предпочтительными являются C2-C4алкинильные группы.
Термин С6-С14арил означает ароматическую углеводородную группу, имеющую 6-14 атомов углерода, такую как фенил, нафтил, тетрагидронафтил, инденил, антрацил, которые необязательно могут быть замещены одним или несколькими заместителями, такими как, но не ограничиваясь ими, гидрокси, галоген, нитро, трифторметил, циано, С1-С8алкилкарбониламино, С1-С8алкиламинокарбонил или С1-С8(ди)алкиламино, алкильные фрагменты имеют такое же значение, как определено ранее. Более предпочтительными являются С6-С10арильные группы. Наиболее предпочтительной ароматической углеводородной группой является фенил.
Термин С3-С8циклоалкил означает циклоалкильную группу, содержащую 3-8 атомов углерода, представляющую собой циклопропил, циклобутил, циклопентил, циклогексил, циклогептил или циклооктил.
Термин C2-C7гетероциклоалкил означает гетероциклоалкильную группу, имеющую 2-7 атомов углерода, предпочтительно 2-5 атомов углерода, и по крайней мере включающую один гетероатом, выбранный из N, O или S. Предпочтительными гетероатомами являются N или О. Азот-содержащие гетероциклоалкильными группы могут быть связаны через атома углерода или азота. Наиболее предпочтительными гетероциклоалкильными группами являются пиперидин, морфолин и пирролидин.
Термин C2-C7гетероциклоалкилкарбонил означает гетероциклоалкильную группу, имеющую 2-7 атомов углерода, как определено ранее, соединенную с карбонильной группой.
Термин С1-С8алкокси означает алкоксильную группу, имеющую 1-8 атомов углерода, алкильный фрагмент имеет значения, определенные ранее. C1-C6Алкоксильные группы являются предпочтительными, C1-C3алкоксильные группы являются наиболее предпочтительными.
Термин С1-С8алкоксикарбонил означает алкоксикарбонильную группу, алкильная группа в которой содержит 1-8 атомов углерода и имеет значение, определенное ранее. C1-C6Алкоксикарбонильные группы являются предпочтительными, C1-C3алкоксикарбонильные группы являются наиболее предпочтительными.
Термин С1-С8алкеноксикарбонил означает алкеноксикарбонильную группу, алкенильная группа в которой содержит 2-8 атомов углерода и имеет значение, определенное ранее. С2-С6Алкеноксикарбонильные группы являются предпочтительными, С2-С3алкеноксикарбонильные группы являются наиболее предпочтительными.
Термин С1-С8алкоксисульфонил означает алкоксисульфонильную группу, алкильная группа в которой содержит 1-8 атомов углерода и имеет значение, определенное ранее. C1-C6Алкоксисульфонильные группы являются предпочтительными, C1-C3алкоксисульфонильные группы являются наиболее предпочтительными.
Термин С1-С8(ди)алкиламино означает (ди)алкиламиногруппу, имеющую 1-8 атомов углерода, алкильный фрагмент в которой имеет значение, определенное ранее. Более предпочтительными являются C1-C6(ди)алкиламино группы.
Термин ди[C1-C3алкоксиC1-C3алкил]амино означает (ди[алкоксиалкил]амино группу, в которой как алкильный, так и алкоксильный фрагменты имеют 1-3 атома углерода и значения, определенные ранее.
Термин С6-С14(ди)ариламино означает (ди)ариламиногруппу, имеющую 6-14 атомов углерода, арильный фрагмент имеет значение, определенное ранее. Более предпочтительными являются С6-С10(ди)ариламино группы. Наиболее предпочтительной (ди)ариламино группой является (ди)фениламино.
Термин С1-С8алкилтио означает алкилтио группу, имеющую 1-8 атомов углерода, алкильный фрагмент имеет значение, определенное ранее. Наиболее предпочтительными являются С1-С4алкилтио группы.
Термин С6-С14арилоксикарбонил означает арилоксикарбонильную группу, арильная группа в которой содержит 5-14 атомов углерода, более предпочтительно 6-10 атомов углерода и имеет значение, определенное ранее. Наиболее предпочтительными являются феноксикарбонильные группы.
Термин С6-С14арилоксисульфонил означает арилоксисульфонильную группу, арильная группа в которой содержит 6-14 атомов углерода, более предпочтительно 6-10 атомов углерода и имеет значение, определенное ранее. Наиболее предпочтительными являются феноксисульфонильные группы.
Термин С6-С14арилС1-С8алкил означает арилалкильную группу, имеющую 7-22 атома углерода, где алкильная группа представляет собой С1-С8алкильную группу, и арильная группа представляет собой С6-С14арильную группу, как определено ранее. Более предпочтительными являются С6-С10арилС1-С4алкильные группы. ФенилС1-С4алкильные группы, такие как бензил, являются наиболее предпочтительными аралкильными группами.
Термин С4-С13гетероарил означает замещенную или незамещенную ароматическую группу, имеющую 4-13 атомов углерода, предпочтительно 4-9, и включающую по крайней мере один гетероатом, выбранный из N, O и/или S, такую как имидазолил, тиенил, бензтиенил, хинолил, тетрагидрохинолил, изохинолил, тетрагидроизохинолил, индолил, акридинолил, фурил или пиридил. Заместители гетероарильной группы могут быть выбраны из группы заместителей, перечисленных для арильной группы. Предпочтительными гетероарильными группами являются тиенил, фурил, пиридил и пиримидил. Азот-содержащие гетероарильные группы могут быть связаны посредством атома углерода или азота.
Термин галоген означает фтор, хлор, бром или иод.
Термин C2-C7гетероциклоалкилС1-С8алкокси означает гетероциклоалкильную группу, содержащую 2-7 атомов углерода, как определено ранее, присоединенную к С1-С8алкоксильной группе, алкоксильный фрагмент имеет значение, определенное ранее. Более предпочтительными являются C2-C5гетероциклоалкилC1-C4алкоксильные группы.
Термин С3-С8циклоалкилС1-С8алкокси означает циклоалкильную группу, содержащую 3-8 атомов углерода, как определено ранее, присоединенную к С1-С8алкоксильной группе, алкоксильный фрагмент имеет значение, определенное ранее. Более предпочтительными являются C3-C6циклоалкилC1-C4алкоксильные группы.
Термин С6-С14арилС1-С8алкокси означает арильную группу, содержащую 6-14 атомов углерода, как определено ранее, присоединенную к С1-С8алкоксильной группе, алкоксильный фрагмент имеет значение, определенное ранее. Более предпочтительными являются C6-C10арилC1-C4алкоксильные группы, фенилC1-C4алкоксильные группы являются наиболее предпочтительными. C4-C13ГетероарилС1-С8алкоксильные группы являются аналогами С6-С14арилС1-С8алкоксильных групп, включающими по крайней мере один гетероатом, выбранный из N, O и S в гетероарильном кольце. Более предпочтительными являются С4-С9гетероарилC1-C4алкоксильные группы.
Термин С1-С8алкилкарбонил означает алкилкарбонильную группу, алкильная группа в которой содержит 1-8 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C1-C6алкилкарбонильные группы, C1-C4алкилкарбонильные группы являются наиболее предпочтительными.
Термин С6-С14арилкарбонил означает арилкарбонильную группу, арильная группа в которой содержит 6-14 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C6-C10арилкарбонильные группы, фенилкарбонильные группы являются наиболее предпочтительными.
Термин С1-С8алкилсульфонил означает алкилсульфонильную группу, алкильная группа в которой содержит 1-8 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C1-C6алкилсульфонильные группы, C1-C4алкилсульфонильные группы являются наиболее предпочтительными.
Термин С2-С8алкенилсульфонил означает алкенилсульфонильную группу, алкенильная группа в которой содержит 2-8 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C2-C6алкенилсульфонильные группы, C2-C4алкенилсульфонильные группы являются наиболее предпочтительными.
Термин С6-С14арилсульфонил означает арилсульфонильную группу, арильная группа в которой содержит 6-14 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C6-C10арилсульфонильные группы, фенилсульфонильные группы являются наиболее предпочтительными.
Термин С1-С8алкилкарбонилокси означает алкилкарбонилокси группу, алкильная группа в которой содержит 1-8 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C1-C6алкилкарбонилокси группы. Более предпочтительными являются C1-C4алкилкарбонилокси группы.
Термин С6-С14арилкарбонилокси означает арилкарбонилокси группу, арильная группа в которой содержит 6-14 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C6-C10арилкарбонилокси группы, фенилкарбонилокси группы являются наиболее предпочтительными.
Термин С1-С8(ди)алкиламинокарбонил означает (ди)алкиламинокарбонильную группу, алкильная группа в которой содержит 1-8 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C1-C6(ди)алкиламинокарбонильные группы, C1-C4(ди)алкиламинокарбонильные группы являются наиболее предпочтительными.
Термин С6-С14(ди)ариламинокарбонил означает (ди)ариламинокарбонильную группу, арильная группа в которой содержит 6-14 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C6-C10(ди)ариламинокарбонильные группы, (ди)фениламинокарбонильные группы являются наиболее предпочтительными.
Термин С1-С8 (ди)алкиламиносульфонил означает (ди)алкиламиносульфонильную группу, алкильная группа в которой содержит 1-8 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C1-C6(ди)алкил-аминосульфонильные группы, C1-C4(ди)алкиламиносульфонильные группы являются наиболее предпочтительными.
Термин С6-С14(ди)ариламиносульфонил означает (ди)ариламиносульфонильную группу, арильная группа в которой содержит 6-14 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C6-C10(ди)ариламиносульфонильные группы, (ди)фениламиносульфонильные группы являются наиболее предпочтительными.
Термин С1-С8алкилкарбониламино означает алкилкарбониламино группу, алкильная группа в которой содержит 1-8 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C1-C6алкилкарбониламино группы, C1-C4алкилкарбониламино группы являются наиболее предпочтительными.
Термин С6-С14арилкарбониламино означает арилкарбониламино группу, арильная группа в которой содержит 6-14 атомов углерода и имеет значение, определенное ранее. Более предпочтительными являются C6-C10арилкарбониламино группы, фенилкарбониламино группы являются наиболее предпочтительными.
Термин C2-C7гетероциклоалкилокси означает гетероциклоалкильную группу, содержащую 2-7 атомов углерода, как определено ранее, присоединенную к атому кислорода. Наиболее предпочтительными являются C2-C5гетероциклоалкилокси группы.
Термин С3-С8циклоалкилокси означает циклоалкильную группу, содержащую 3-8 атомов углерода, как определено ранее, присоединенную к атому кислорода.
Термин С6-С14арилокси означает арильную группу, содержащую 6-14 атомов углерода, как определено ранее, присоединенную к атому кислорода. Более предпочтительными являются C6-C10арилокси группы, феноксигруппы являются наиболее предпочтительными. С4-С13Гетероарилокси группы являются аналогами С6-С14арилокси группы, включающими по крайней мере один гетероатом, выбранный из N, O и S в гетероарильном кольце. Более предпочтительными являются С4-С9гетероарилокси группы.
Было показано, что соединения указанной выше формулы I способны связываться с LH рецептором и проявляют агонистическую активность в отношении LH.
Изобретение дополнительно относится к фармацевтической композиции, включающей бициклическое гетероароматическое производное или его соли, имеющие общую формулу I.
Таким образом, соединения согласно изобретению могут использоваться в терапии. Дополнительный аспект изобретения относится к применению бициклического гетероароматического соединения, имеющего общую формулу I для получения лекарственного средства для регулирования фертильности. Предпочтительно настоящие соединения используют для активации LH-рецептора.
Бициклические гетероароматические производные по данному изобретению могут иметь один или несколько хиральных атомов углерода. Следовательно, соединения могут быть получены в виде хирально чистых соединений или в виде смеси диастереоизомеров и/или энантиомеров. Способы получения хирально чистых соединений хорошо известны в данной области, например, кристаллизация или хроматография.
Для терапевтического применения соли соединений формулы I являются такими солями, где противоион является фармацевтически приемлемым. Однако также могут найти применение, например, при получении или очистке фармацевтически приемлемого соединения, кислотно-аддитивные соли оснований соединений формулы I. Все соли, являются они фармацевтически приемлемыми или не являются, включены в объем настоящего изобретения.
Примеры кислотно-аддитивных солей включают соли, полученные из минеральных кислот, таких как хлористоводородная кислота, фосфорная кислота, серная кислота, предпочтительно, полученные из хлористоводородной кислоты, и органических кислот, таких как лимонная кислота, винная кислота, уксусная кислота, молочная кислота, малеиновая кислота, малоновая кислота, фумаровая кислота, гликолевая кислота, янтарная кислота и подобные.
Подходящие пути введения соединений формулы I или их фармацевтически приемлемых солей, также упоминаемых в настоящем описании в качестве активного ингредиента, представляют собой внутримышечные инъекции, подкожные инъекции, внутривенные инъекции или внутрибрюшинные инъекции, пероральное или внутриназальное введение. Предпочтительно, соединения можно вводить перорально. Точная доза и режим введения активного ингредиента или его фармацевтической композиции определенным образом будут зависеть от желаемого терапевтического действия (лечение бесплодия, контрацепция) и могут изменяться в зависимости от конкретного соединения, способа введения, возраста и состояния индивидуального субъекта, которому вводится лекарственное средство.
В общем, при парентеральном введении требуются более низкие дозы, чем для других способов введения, которые в большей мере зависят от адсорбции. Однако доза для людей предпочтительно составляет 0,0001-25 мг на кг веса тела. Желаемая доза может быть представлена в виде единичной дозы или в виде множества разделенных доз, вводимых с подходящими интервалами в течение дня, или, в случае реципиентов женского пола, в виде доз для введения с подходящими дневными интервалами в течение менструального цикла. Доза, а также режим введения могут различаться для реципиента женского и мужского пола.
В случае in vitro или ex vivo применений, таких как IVF применения, соединения по изобретению должны использоваться в инкубационной среде в концентрации приблизительно 0,01-5 мкг/мл.
Таким образом, настоящее изобретение также относится к фармацевтическим композициям, включающим бициклическое гетероароматическое соединение формулы (I) в смеси с фармацевтически приемлемыми вспомогательными добавками и, необязательно, с другими терапевтическими агентами. Вспомогательные добавки должны быть «приемлемыми» в смысле совместимости с другими ингредиентами композиции и неопасными для реципиентов.
Фармацевтические композиции включают те, которые являются подходящими для перорального, ректального, назального, местного (включая чрескожное, буккальное и сублингвальное), вагинального или парентерального (включая подкожное, внутримышечное, внутривенное и внутрикожное) введения. Композиции могут быть получены любым способом, хорошо известным в области фармацевтики, например, с использованием способов, описанных в Gennaro et al., Remington's Pharmaceutical Science (18th ed., Mark Publishing company, 1990, смотри, в особенности, часть 8: Pharmaceutical Preparations and Their Manufacture (Фармацевтические препараты и их получение).
Такие способы включают стадию приведения в контакт активного ингредиента с любым вспомогательным агентом. Вспомогательный агент(ы), также именуемый добавочным ингредиентом, включает общепринятые в данной области (Gennaro, выше), такие как наполнители, связующие вещества, разбавители, разрыхляющие агенты, смазывающие вещества, красители, вкусовые агенты и смачивающие агенты.
Фармацевтические композиции, подходящие для перорально введения могут быть представлены в виде отдельных стандартных препаративных форм, таких как пилюли, таблетки или капсулы, или в виде порошков или гранул, или в виде раствора или суспензии. Активный ингредиент также может быть представлен в виде болюса или пасты. Композиции дополнительно могут быть переработаны в суппозитории или клизмы для ректального введения.
Для парентерального ведения подходящие композиции включают водные и неводные стерильные инъекции. Композиции могут быть представлены в виде контейнера с единичной дозой или многократной дозой, например, запаянные пробирки или ампулы и могут храниться в высушенном вымораживанием состоянии, требующем только добавления стерильного жидкого носителя, например воды, перед употреблением.
Композиции или составы, подходящие для введения посредством назальной ингаляции, включают тонкодисперсные дусты или туманы, которые могут генерироваться с помощью аэрозолей, распылителей и аппаратов для вдувания.
Бициклические гетероароматические производные по изобретению также могут вводиться в форму имплантируемых фармацевтических устройств, состоящих из ядра активного вещества, заключенного в мембрану, контролирующую скорость высвобождения. Такие имплантаты могут применяться подкожно или местно, и они будут высвобождать активный ингредиент с приблизительно постоянной скоростью в течение относительно большого промежутка времени, например, от недель до лет. Способы получения имплантируемых фармацевтических устройств, как таковых, известны в данной области, например, описаны в Европейском патенте 0303306 (AKZO N.V.).
Таким образом, соединения согласно настоящему изобретению могут использоваться в тех же клинических целях, что и природный LH, с тем преимуществом, что они обладают измененными свойствами стабильности и могут вводиться по-иному.
Соединения настоящего изобретения, где В=NH, представленные формулой (I-a) обычно могут быть получены в соответствии с известной в данной области конденсацией кислоты формулы (II) с амином формулы (III).
Вышеуказанную реакцию проводят при комнатной температуре в подходящем растворителе, например, в апротонном растворителе, таком как N,N-диметилформамид (ДМФ) или дихлорметан с использованием конденсирующего реагента, такого как тетрафторборат О-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония (TBTU) или гексафторфосфат бромтрипирродидинофосфония (PyBrOP) и основания - третичного амина, например, N,N-диизопропилэтиламина (DiPEA).
Также соединения формулы (I), где В=О, представленные формулой (I-b), могут быть получены таким же образом, как описано выше для соединений формулы (I-a), исходя из кислот общей структуры (II) и спиртов формулы (IV).
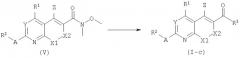
Соединения формулы (I), где В является связью, представленные формулой (I-c), могут быть получены взаимодействием подходящего металлоорганического реагента с производными формулы (V) в апротонном растворителе, таком как ТГФ. Родственные реакции замещения могут быть найдены в литературе: S.V.Frye, M.C.Johnson, N.L.Valvano, J.Org.Chem. 56:3750, 1991. Амиды Вайнреба (Weinreb) формулы (V) могут быть синтезированы из кислот формулы (II) и N-метокси-N-метиламина с использованием условий, описанных для получения амидов формулы (I-a).
Подходящим способом для получения промежуточных кислот (II) является известное в данной области омыление в основной среде этиловых сложных эфиров общей структуры (VI). Омыление происходит в присутствии основания, такого как гидроксид лития. Гидроксид калия или гидроксид натрия в водном диоксане при повышенной температуре (от 40° до температуры кипения) с последующей обработкой кислотой.
Бициклические лактамы формулы (VII) являются полезными исходными веществами для получения соответствующих иминов (VIII). В типичном эксперименте, лактам превращают в соответствующий хлоримин с использованием фосфорилхлорида при повышенной температуре (от 60° до температуры кипения) в подходящем растворителе, таком как 1,4-диоксан. При обработке восстановителем, таким как водород в присутствии подходящего катализатора в этаноле, может быть выделен целевой имин общей формулы (VIII). Родственное восстановление было описано в литературе, смотри, например: E.Bisagni, C.Landras, S.Thirot and C.Huel, Tetrahedron 52: 10427, 1996.
Бициклические лактамы общей структуры (VII) могут быть получены конденсацией кислот типа (IX) с диэтиламиномалонатом при действии конденсирующего агента, такого как TBTU/DiPEA и циклизацией промежуточных амидов в этаноле в основных условиях. Ароматизация с сопутствующим деэтоксикарбонилированием затем дает бициклы типа (VII). В альтернативном способе этиловый эфир глицина может быть использован вместо диэтиламиномалоната. Смотри, например, M.Blanco, M.G.Lorenzo, I.Perillo, C.B.Schapira, J.Heterocycl.Chem., 33:361, 1996. Циклизация промежуточных амидов также может быть выполнена под действием хлорида олова(IV). О применении хлорида олова(IV) для осуществления замыкания кольца цикла в родственных системах сообщалось: A.C.Veronese, R.Callegari, C.F.Morelli, Tetrahedron 51:12277, 1995.
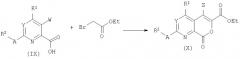
Обработка кислоты формулы (IX) этилбромацетатом в апротонном растворителе при действии не-нуклеофильного основания, такого как карбонат калия или трет-бутоксид калия может дать ароматический лактон общей структуры (Х). Родственные структуры были описаны в литературе: C.Bhakta, Indian J.Chem.Sect.B. 25:180, 1986.
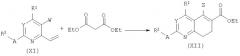
Обработка винильных производных формулы (XI) диэтилмалонатом в основных условиях дает возможность сопряженного присоединения. Промежуточный аддукт может циклизоваться в бициклы формулы (XII) посредством реакции под действием хлорида олова (IV) и последующей обработки.
Альтернативно трет-бутилэтилмалонат может быть использован в таком способе вместо диэтилмалоната.
При обработке подходящим окислителем, таким как DDQ, или палладиевым катализатором при повышенной температуре в подходящем растворителе, таком как ксилол, ароматизация производных формулы (XII) приводит к хиназолинам или хинолинам общей формулы (XIII). Смотри также: K.Kobayashi, T.Uneda, K.Takada, T.Kitamura, O.Morikawa, H.Konishi, J.Org.Chem.62:664, 1997.
При другом подходе метилпири(ми)дины общей формулы (XIV) депротонируют по метильной группе под действием сильного основания, такого как гексаметилдисилазан лития (LiHMDS) или диизопропиламид лития (LDA), в подходящем апротонном растворителе, таком как ТГФ при низкой температуре (-78°С). Анион затем взаимодействует с этил 3-этоксиакрилатом. После сопряженного присоединения происходит циклизация в хинолины или хиназолины общей формулы (XIII), как описано K.Kobayashi, K.Takada, H.Tanaka, T.Uneda, T.Kitamura, Chem.Lett.:25, 1996; K.Kobayashi, T.Uneda, K.Takada, H.Tanaka, T.Kitamura, O.Morikawa, H.Konishi, J.Org.Chem.62:664, 1997.
Обработка хлоридов общей формулы (XV) этиловым эфиром (N-алкил)-бета-аланина (XVI) в основных условиях дает бициклы общей формулы (XVII). Родственные превращения были описаны: P.Y.Boamah, N.Haider, G.Heinisch, Arch.Pharm. (Weinheim) 323:207, 1990.
Соединения формулы (XVII), где R6=H могут быть окислены до производных формулы (XVIII) с использованием палладия на активированном угле при повышенной температуре. Смотри, например, M.Onda, K.Kawakami, Chem.Pharm.Bull. 20:1484, 1972. Соединения формулы (XVII), где R6=Н или алкил, могут быть преобразованы в имины формулы (XVIII) с использованием DDQ, как описано: H.Ishii, Chem.Pharm.Bull. 26:864, 1978; J.I.DeGraw, P.H.Christie, W.T.Colwell, F.M.Sirotnak, J.Med.Chem., 35:320, 1992.
Альтернативно, имины формулы (XVIII) могут быть получены из соответствующих лактамов формулы (XIX) аналогичным образом (смотри выше) в виде их региостереоизомерных аналогов формулы (VIII), н