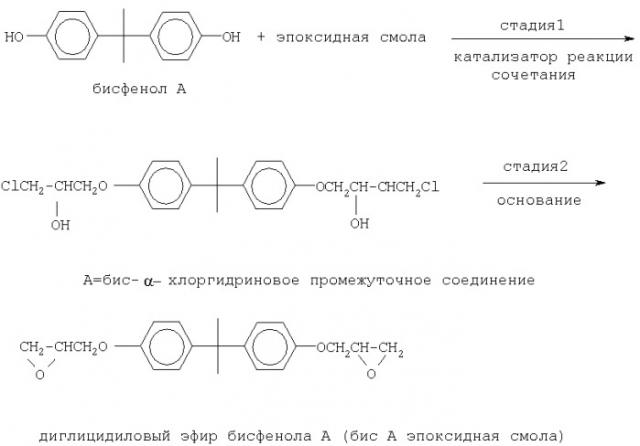
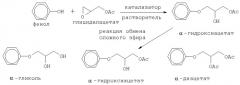
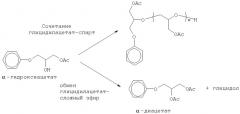
Способ получения промежуточного соединения - производного сложного гидроксиэфира и эпоксидные смолы, полученные из него
Иллюстрации
Показать всеИзобретение относится к производному сложного α-гидроксиэфира и способу его получения, к способу получения α-галогидринового промежуточного соединения и к способу получения из него эпоксидной смолы, а также к композиции на основе эпоксидной смолы. Эпоксидная смола представляет собой соединение общей формулы (R2)yAr(OR1'')z, где у принимает значения от 0 до 750; z принимает значения от 1 до 150; Ar представляет фрагмент, содержащий ароматику; R1'' представляет фрагмент, содержащий глицидил; и R2 представляет атом хлора, брома, йода, фтора, алкильную группу, циклоалифатическую группу или ароматическую группу, замещающую атом водорода на Ar фрагменте. Способ получения эпоксидной смолы включает три стадии. На первой стадии получают производное сложного α-гидроксиэфира, по крайней мере, одного или более фенолов взаимодействием, по крайней мере, одного или более фенолов со сложным глицидиловым эфиром или замещенным сложным глицидиловым эфиром. Производное сложного α-гидроксиэфира имеет формулу (R2)yAr(OR1')z, где y, z, Ar, R2 имеют вышеуказанные значения, R1' представляет фрагмент, содержащий пропиловый сложный α-гидроксиэфир. На второй стадии получают α-галогидриновое промежуточное соединение, по крайней мере, одного или более фенолов взаимодействием производного сложного α-гидроксиэфира, по крайней мере, одного или более фенолов с галоидводородом; α-галогидриновое промежуточное соединение имеет формулу (R2)yAr(OR1)z, где y, z, Ar, R2 имеют вышеуказанные значения, R1' представляет фрагмент, содержащий α-галогидринпропил. На третьей стадии проводят эпоксидирование вышеуказанного α-галогидринового промежуточного соединения, по крайней мере, одного или более фенолов. Композиция для порошкового покрытия включает, по крайней мере, два или более компонента, где, по крайней мере, один из компонентов является эпоксидной смолой. Изобретение позволяет получить эпоксидную смолу в отсутствие эпихлоргидрина, используя вышеуказанные стадии. 8 н. и 68 з.п. ф-лы, 4 табл.
Реферат
Настоящее изобретение относится к способу получения производного сложного α-галогидринового эфира, по крайней мере, одного или более фенолов, и превращения такого производного сложного α-галогидринового эфира в эпоксидную смолу.
Более конкретно, настоящее изобретение относится к способу получения производного сложного α-галогидринового эфира, по крайней мере, одного или более фенолов, превращения такого производного сложного α-галогидринового эфира в α-галогидриновое промежуточное соединение, по крайней мере, одного или более фенолов и использованию такого α-галогидринового промежуточного соединения, по крайней мере, одного или более фенолов для получения эпоксидных смол. Так, например, настоящее изобретение можно использовать для получения бисфенол А (бис А) эпоксидной смолы.
α-Галогидрины получают как реакционно-способные промежуточные соединения несколькими способами, которые хорошо известны в данной области. Обычно промежуточные α-галогидрины последовательно превращают в эпоксиды. В одном из находящих широкое применение способов α-галогидрины получают, осуществляя взаимодействие низкомолекулярных олефинсодержащих соединений, таких как пропилен, бутилен и аллилхлорид, с галогенами, такими как хлор или бром, в воде. α-Галогидрины, более конкретно α-хлоргидрины, полученные из пропилена, бутилена и аллилхлорида, используют затем для получения пропиленоксида, бутиленоксида и эпихлоргидрина (ЭХГР), соответственно, в крупных масштабах. Способ промышленной обработки пропиленоксида и ЭХГР состоит из следующей последовательности реакций: последовательности реакций (I) и последовательности реакций (II). Более конкретно, в последовательности реакций (I) представлена схема промышленного получения пропиленоксида из хлоргидринов, полученных из хлора в воде, а в последовательности реакций (II) представлена схема промышленного получения эпихлоргдрина из хлоргидринов, полученных из хлора в воде.
Последовательность реакций (I)
Последовательность реакций (II)
В хорошо известном промышленном способе получения эпоксидных смол в промышленных масштабах на первой стадии α-галоидгидрин в качестве реакционно-способного промежуточного соединения получают, осуществляя взаимодействие соединения, содержащего активный водород, такого как спирт, фенол, карбоновая кислота или амин, с эпигалоидгидрином, таким как эпихлоргидрин (ЭХГР) или эпибромгидрин. Затем на второй стадии α-галоидгидриновое промежуточное соединение превращают в глицидиловый эфир, сложный глицидиловый эфир или глицидиламин в основных условиях реакции.
Чаще всего получают особенно полезную бисфенол А (бис А) эпоксидную смолу, которую получают, осуществляя реакцию сочетания бис А и ЭХГР до образования бис(α-хлоргидрин) промежуточного соединения на первой стадии. Затем на второй стадии образования эпоксидного кольца реакцией дегидрохлорирования с основанием, бис А бис(α-хлоргидриновое) промежуточное соединение превращают в эпоксидную смолу бис А диглицидилового эфира. Такой двухстадийный способ получения эпоксидной смолы раскрыт Н. Lee и К. Neville в "Handbook of Ероху Resins", McGraw-Hill Book Co., New York, New York, 1982, Reissue, 2-3 to 2-4. Этот способ представлен ниже в последовательности реакций (III). Более конкретно, последовательность реакций (III) представляет схему реакций для двухстадийного промышленного получения бис А эпоксидной смолы реакцией бис А и ЭХГР для получения хлоргидринового промежуточного соединения.
Приведенный выше двухстадийный способ осуществления реакции сочетания бис А и ЭХГР с последующим дегидрохлорированием, обеспечивающим образование эпоксидного кольца, был также объединен в одностадийную реакцию, в которой бис(α-хлоргидриновое) промежуточное соединение бис А получают in situ и превращают в эпоксисоединение одновременно. Такой одностадийный способ получения бис А эпоксидной смолы раскрыт в патентах США 499255; 4778863 и 5028686.
Другой способ получения α-хлоргидринов в качестве реакционно-способных промежуточных соединений раскрыт в патенте США №2144612, где глицерин, который является α-гликолем, превращают в α-хлоргидрин в результате реакции с безводным хлористым водородом (HCl) в присутствии каталитического количества уксусной кислоты (АсОН). В патенте США №2144612 раскрыт способ, представленный ниже в последовательности реакций (IV) получения глицериндихлоргидрина, предшественника эпихлоргидрина из глицерин-α-гликоля. Более конкретно, в последовательности реакций (IV) представлена схема синтеза эпихлоргидрина в результате реакции глицерина с HCl и АсОН до получения глицериндихлоргидрина.
Последовательность реакций (IV)
Хотя эпихлоргидрин является важным коммерческим продуктом для получения промежуточных соединений α-хлоргидрина, и конкретно для получения бис А бис α-хлоргидриновых промежуточных предшественников бис А эпоксидной смолы, ЭХГР обеспечивает интенсивный способ с использованием хлора для получения эпоксидных смол. В превалирующем коммерческом способе получения ЭХГР ЭХГР получают из аллилхлорида, который в свою очередь получают путем термического хлорирования пропилена с использованием газообразного хлора, способом, который приводит к образованию хлорированных побочных продуктов. Обычно хлорированные побочные продукты обрабатывают как отходы.
Кроме того, при превращении аллилхлорида в α-хлоргидриновое промежуточное соединение используют большое количество воды, и эту воду необходимо в итоге также обработать как отходы. Поэтому с точки зрения окружающей среды при производстве эпоксидной смолы желательно уменьшить расход хлора и уменьшить образование хлорированных побочных продуктов и сточных вод.
Кроме того, эпоксидные смолы, получаемые из ЭХГР описанными выше или двухстадийным, или одностадийным способами, могут иметь высокое содержание органического хлора, что может быть нежелательным в некоторых применениях, например в применении в электронике.
Поэтому желательно создать способ получения эпоксидных смол, таких как бис А эпоксидная смола, без использования эпихлоргидрина. То есть желательно создать альтернативный способ получения эпоксидных смол без использования ЭХГР.
Один из способов получения эпоксидных смол без использования эпихлоргидрина раскрыт в патенте США №6001945. В способе патента США No 6001945, в качестве реагента используют глицидол для получения α-гликольного производного, которое затем превращают в α-хлоргидрин реакцией с хлористым водородом и каталитическим количеством уксусной кислоты по способу, раскрытому в патенте США No 214612. Известно, что глицидол является высоко токсичным и термически нестабильным материалом, имеющим тенденцию к взрывной самополимеризации.
При низких температурах, таких как 70°С, глицидол нестабилен, что приводит к значительным потерям содержания эпоксида. Самополимеризация глицидола снижает селективность и выход продукта в своих реакциях, и продукты самополимеризации глицидола осложняют выделение и очистку нужного продукта реакции. Эти нежелательные свойства глицидола подробно описаны A. Kleemann and R.Wagner в "Glycidol Properties, Reactions, Applications" Dr. Alfred Huthig Verlag, New York, 1981, pp.48-52. Таким образом, желательно разработать способы, с помощью которых можно было бы получать промежуточные соединения α-галогидрина в качестве предшественников для получения эпоксидных смол, которые не требовали бы использования глицидола в качестве реагента.
Один из аспектов настоящего изобретения относится к способу получения эпоксидной смолы путем превращения производного α-галогидринового сложного эфира фенола или смеси фенолов в эпоксидную смолу.
Другой аспект настоящего изобретения относится к способу получения α-галогидринового промежуточного соединения, по крайней мере, одного или более фенолов, используя in situ способ галоидзамещения - деэстерификации для превращения производного сложного α-гидроксиэфира, по крайней мере, одного или более фенолов в α-галогидриновое промежуточное соединение. Этот способ предпочтительно осуществляют в безводных условиях, используя безводный галоидводород, такой как хлористый водород, бромистый водород или йодистый водород, в качестве реагента; и необязательно способ осуществляют в присутствии растворителя.
Еще один из аспектов настоящего изобретения относится к альтернативному, без использования эпихлоргидрина, способу получения эпоксидной смолы, по крайней мере, одного или более фенолов, с использованием в качестве промежуточного продукта α-галогидринового промежуточного соединения одного или более фенолов, как раскрыто выше.
В еще одном аспекте настоящее изобретение относится к сложному α-гидроксиэфиру, по крайней мере, одного или более фенолов, который используют в указанном выше способе получения α-галогидриновых промежуточных соединений, предпочтительно получаемых в результате взаимодействия, по крайней мере, одного фенола или смеси двух или более фенолов со сложным глицидиловым эфиром, предпочтительно глицидилацетатом. Способ получения сложного α-гидроксиэфира, по крайней мере, одного фенола предпочтительно осуществляют в присутствии растворителя и катализатора.
Настоящее изобретение включает новый способ получения промежуточного α-галогидринового соединения на фенольной основе, т.е. промежуточного α-галогидринового соединения, полученного из одного фенола, или смеси α-галогидриновых промежуточных соединений, полученных из смеси двух или более различных фенолов, из производного сложного α-галогидринового эфира на фенольной основе. Затем α-галогидриновые промежуточные соединения используют для получения эпоксидных смол.
α-Галогидриновые промежуточные соединения
Обычно способ настоящего изобретения для получения α-галогидриновых промежуточных соединений включает превращение производного сложного α-гидроксиэфира, по крайней мере, одного или более фенолов в α-галогидриновое промежуточное соединение в результате in situ осуществляемого способа галоидзамещения-деэстерификации с использованием галоидводорода. Затем α-галогидриновые промежуточные соединения можно использовать для получения эпоксидных смол хорошо известными в промышленности способами, такими как, например, эпоксидирование с замыканием кольца реакцией α-галогидриновых промежуточных соединений с основанием. Более предпочтительные эпоксидные смолы, которые можно получить по способу настоящего изобретения, включают, например, эпоксидную смолу бисфенол А (бис А) диглицидилового эфира.
α-Галогидриновые промежуточные соединения, полученные по способу настоящего изобретения, представлены, например, но не ограничиваются ими, структурами формул I-V. Предпочтительный класс α-галогидриновых промежуточных соединений настоящего изобретения в общем случае представлен, например, формулой I.
Формула I
В формуле I у принимает значения от 0 до 750, и z принимает значения от 1 до 150.
В формуле I Ar представляет фрагмент, содержащий одноядерное ароматическое кольцо, такое как фенил. Ar может также представлять фрагмент, содержащий многоядерные ароматические кольца, такие как бифенил, 2,2-дифенилпропан, бисфениленоксид, 1,1,2,2-тетракисфенилэтан, стильбен, фенолформальдегидный новолак, крезолформальдегидный новолак, фенолдициклопентадиеновый новолак и гиперразветвленные ароматические фенольные дендримеры. Ar может также быть фрагментом, содержащим многоядерные конденсированные ароматические кольца, такие как нафталин, антрацен и нафталинформальдегидный новолак. Ar может также представлять фрагмент, содержащий многоядерные конденсированные ароматические кольца, содержащие один или более гетероатомов, таких как О, N, S, Si, В или Р, или любые комбинации таких гетероатомов, например, хиноксалин, тиофен и хинолин. Ar может также представлять фрагмент, содержащий одноядерное или многоядерное кольцо (кольца), конденсированное с циклоалифатическим кольцом (кольцами), такой как индан, 1,2,3,4-тетрагидронафталин и флуорен. Ar может также представлять фрагмент, содержащий ордноядерное или многоядерное ароматическое кольцо (кольца), конденсированное с циклоалифатическим кольцом (кольцами), содержащим один или более гетероатомов, таких как O, N, S, Si, В или Р, или любую комбинацию таких гетероатомов, например хроман, индолин и тиоиндан.
В формуле I Ar может также представлять фрагмент, содержащий арильные группы, в котором каждая из арильных групп соединена с олигомерными (например, полимерами со среднечисловой молекулярной массой менее 5000) или высокомолекулярными (например, со среднечисловой молекулярной массой более 5000) органосилоксановыми фрагментами. Арильные группы присоединены непосредственно к атомам кремния органосилоксановых фрагментов, или арильные группы присоединены к атомам кремния органосилоксановых фрагментов через органические алифатические фрагменты, органические циклоалифатические фрагменты, органические ароматические фрагменты, или любые их комбинации. Органические алифатические циклоалифатические или ароматические фрагменты должны содержать не более чем около 20 атомов углерода. Если Ar фрагмент содержит такие олигомерные или высокомолекулярные органосилоксановые фрагменты, тогда z предпочтительно принимает значения от 1 до 150.
В формуле I О представляет атом кислорода, замещающий атом водорода у ароматического кольца (колец) Ar фрагмента и R1 представляет фрагмент, содержащий α-галогидринпропильный фрагмент, предпочтительно выбранный из:
где Х представляет атом галогена, такой как хлор, бром или йод; и У представляет гидроксильную группу. Положения Х и Y могут быть взаимозаменяемы. R3 в формуле I предпочтительно представляет алкильную группу, содержащую от 1 до 20 атомов углерода, такую как метил, этил и пропил; циклоалифатическую группу, содержащую от 3 до 20 атомов углерода, такую как циклопентил и циклогексил; ароматическую группу, содержащую от 6 до 20 атомов углерода, такую как фенил и нафтил; или любую их комбинацию. Каждые отдельные из групп R3 могут быть одинаковыми или отличаться друг от друга.
В одном из вариантов, если R1 в формуле I представляет следующую структуру:
α-галогидрин представляет производное, содержащее фрагмент 3-гало-2-гидрокси-1-пропила, или в таком производном гидрокси и галоидные группы могут быть взаимозаменяемы с образованием производного, содержащего фрагмент 2-гало-3-гидрокси-1-пропила.
В другом варианте, если R1 в формуле I представляет следующую структуру:
α-галогидрин представляет производное, содержащее фрагмент 3-гало-2-гидрокси-2-метил-1-пропила, или в таком производном гидрокси и галоидные группы могут быть взаимозаменяемы с образованием производного, содержащего фрагмент 2-гало-3-гидрокси-2-метил-1-пропила.
В еще одном варианте, если R1 в формуле I представляет следующую структуру:
α-галогидрин представляет производное, содержащее фрагмент 3-гало-2-гидрокси-1-циклогексила, или в таком производном гидрокси и галоидные группы могут быть взаимозаменяемы с образованием производного, содержащего фрагмент 2-гало-3-гидрокси-1-циклогексила. В обоих производных пропильный фрагмент содержится в структуре циклогексильного кольца.
В формуле I R2 представляет группу, замещающую атом водорода у ароматического кольца (колец) Ar фрагмента. R2 может представлять галоген, такой как хлор, бром, йод или фтор или углеводородный радикал, такой как алкильная группа, циклоалкильная группа или ароматическая группа. R2 предпочтительно представляет алкильную группу, содержащую от 1 до 20 атомов углерода, такую как метил, этил и пропил; циклопропильную группу, содержащую от 3 до 20 атомов углерода, такую как циклопентил и циклогексил; ароматическую группу, содержащую от 6 до 20 атомов углерода, такую как фенил и нафтил; или любую их комбинацию. Указанный выше углеводородный радикал может также содержать один или более гетероатомов, таких как O, N, S, Si, В или Р, или любую комбинацию таких гетероатомов. Примерами углеводородных радикалов, содержащих гетероатом кислород, являются метоксигруппа, этоксигруппа или группа полиалкиленоксида, полученная из алкиленоксидов, таких как этиленоксид, пропиленоксид, бутиленоксид и циклогексаноксид. R2, как раскрыто выше в формуле I, может быть частично или полностью фторирован.
Более конкретные и предпочтительные примеры α-галогидриновых промежуточных соединений, которые можно использовать в настоящем изобретении, представлены формулами II-V, и их можно использовать отдельно или в виде смесей двух или более α-галогидриновых производных формул II-V, представленных ниже.
Примеры одноядерных ароматических α-галогидриновых промежуточных соединений, которые можно использовать в способе настоящего изобретения, представлены, например, формулой II:
Формула II
В формуле II у принимает значения от 0 до 5, и z принимает значения от 1 до 4. В формуле II О, R1 и R2 принимают значения, указанные выше для формулы I. α-Галогидриновые промежуточные соединения формулы II можно получить из предшественников, содержащих ароматические гидроксильные группы, таких как, например, 2-метилфенол; 4-метилфенол; 4-метоксифенол; 2,6-диметилфенол;
2,6-диизопропилфенол; 2,6-дибромфенол; 1,2-дигидроксибензол;
1,3-дигидроксибензол; 1,4-дигидроксибензол и их смеси.
Другие примеры α-галогидриновых промежуточных соединений, которые можно использовать в способе настоящего изобретения, представляют биядерные ароматические α-галогидриновые промежуточные соединения, представленные, например, следующей формулой III:
Формула III
В формуле III каждый у принимает значения от 0 до 4, и они могут быть одинаковыми или различными, и каждый z принимает значения от 0 до 3, и они могут быть одинаковыми или различными. В формуле III О, R1 и R2 имеют указанные выше для формулы I значения.
В формуле III Z может быть равно 0 или Z может быть гетероатомом, у которого могут быть (или отсутствовать) заместители для заполнения его необходимой связывающей валентности. Гетероатом выбирают из О, N, S, Si, В или Р, или любой комбинации двух или более указанных выше гетероатомов. Z может также представлять, например, -С (О)-; -S(O2)-; -C(O)NH-; -Р(O)Ar-; органический алифатический фрагмент, насыщенный или ненасыщенный, содержащий или не содержащий гетероатомы, такой как, например, оксидиметилен, метилен, 2,2-изопропилиден, изобутилен и -CR3=CH-, где R3 имеет указанные выше для формулы I значения; циклоалифатическую группу, насыщенную или ненасыщенную, содержащую или не содержащую гетероатомы, такую как, например, циклоалифатическое кольцо, содержащее более 3 атомов углерода; ароматическую группу, содержащую или не содержащую гетероатомы; или любые их комбинации. Z как раскрыто выше в формуле III, может быть частично или полностью фторированным органическим алифатическим или циклоалифатическим фрагментом, и может быть таким, как, например, 2,2-перфторизопропилиден.
Предшественники, которые можно использовать для получения α-галогидриновых промежуточных соединений формулы III, включают, например, 4,4'-дигидроксибифенил;
3,3',5,5'-тетраметил-4,4'-дигидроксибифенил;
3,3',5,5'-тетраметил-2,2',6,6'-тетрабромдигидроксибифенил;
бис(4-гидроксифенил)метан; бис(4-гидрокифенил)сульфон;
2,2-бис(3,5-дибром-4-гидроксифенил)изопропилиден;
2,2-бис(4-гидроксифенил)изопропилиден; бисфенол К;
9,9-бис(4-гидроксифенил)флуорен;
4,4'-дигидрокси-α-метилстильбен;
1,3-бис(4-гидроксифенил)адамантан и их смеси.
Другие примеры α-галогидриновых промежуточных соединений, которые можно использовать в способе настоящего изобретения, представляют многоядерные ароматические α-галогидриновые промежуточные соединения, представленные, например, следующей формулой IV:
Формула IV
В формуле IV каждый у, каждый z и Z имеют указанные выше для формулы III значения. В формуле IV m принимает значения 0,001 до 10. В формуле IV О, R1 и R2 имеют указанные выше для формулы I значения.
Предшественники, которые можно использовать для получения α-галогидриновых промежуточных соединений формулы IV, включают, например, фенолформальдегидный новолак (функциональность более 2); о-крезолформальдегидный новолак (функциональность более 2); фенолдициклопентадиенильный новолак (функциональность более 2); нафтолформальдегидный новолак (функциональность более 2) и их смеси.
Другими примерами α-галогидриновых промежуточных соединений, которые можно использовать в настоящем изобретении, являются многоядерные ароматические α-галогидриновые промежуточные соединения, представленные, например, следующей формулой V:
Формула V
В формуле V каждый y и каждый z имеют указанные выше для формулы III значения. В формуле V О, R1 и R2 имеют указанные выше для формулы I значения.
В формуле V Z' представляет органический алифатический фрагмент, насыщенный или ненасыщенный, содержащий или не содержащий гетероатомы, такие как О, N, S, Si, В или Р, или любые комбинации двух или более перечисленных выше гетероатомов, где алифатический фрагмент содержит от 1 до 20 атомов углерода, такой как, например, метин; циклоалифатический фрагмент, насыщенный или ненасыщенный, содержащий или не содержащий гетероатомы, содержащий от 3 до 20 атомов углерода, такой как, например, циклогексантриил; ароматический фрагмент, содержащий или не содержащий гетероатомы, такой как, например, бензолтриил, нафтилентриил и флуорентриил; или любые их комбинации. Z' предпочтительно содержит не более чем около 20 атомов углерода. Z', как раскрыто выше в формуле V, может быть частично или полностью фторированным органическим алифатическим или циклоалифатическим фрагментом, может быть таким, как фторметин.
В формуле V m' обычно равно 3 или 4. Однако Z' может также быть олигомерным (например, иметь среднечисловую молекулярную массу менее чем около 5000) органосилоксановым фрагментом или высокомолекулярным (например, иметь среднечисловую молекулярную массу более чем около 5000) органосилоксановым фрагментом; причем в этом случае арильные группы присоединены к атому кремния органосилоксанового фрагмента либо непосредственно, либо через алифатическую, циклоалифатическую или ароматическую группу; или любыми их комбинациями, содержащими не более чем около 20 атомов углерода. Если Z' представляет олигомерный или высокомолекулярный органосилоксановый фрагмент, m' в формуле V предпочтительно принимает значения от 1 до 150.
Предшественники, которые можно использовать для получения α-галогидриновых промежуточных соединений формулы V, включают, например, трис(4-гидроксифенил)метан, 1,1,1-трис(3,5-диметил-4-(гидроксифенил)метан; 1,1,2,2-тетракис(4-гидроксифенил) этан; и их смеси.
Предпочтительно, если α-галогидриновые промежуточные соединения настоящего изобретения включают, например, фенольные α-хлоргидриновые промежуточные соединения, полученные из фенолов, такие как 1,3-дигидроксибензол;
1,4-дигидроксибензол; 1,5-дигидроксинафталин;
2,6-дигидроксинафталин; 4,4'-дигидроксибифенил;
3,3',5,5'-тетраметил-4,4'-дигидроксибифенил;
3,3',5,5'-тетраметил-2,2',6,6'-тетрабром-4,4'-дигидроксибифенил; бис(4-гидроксифенил)метан;
2,2-бис(4-гидроксифенил)изопропилиден; фенолформальдегидный новолак (функциональность более чем 2);
о-крезолформальдегидный новолак (функциональность более чем 2); фенолдициклопентадиенильный новолак (функциональность более чем 2); нафтолформальдегидный новолак (функциональность более чем 2); 1,1,1-трис(4-гидроксифенил)метан;
1,1,2,2-тетракис(4-гидроксифенил)этан и их смеси.
Предпочтительно, если α-галогидриновые промежуточные соединения настоящего изобретения включают, например, фенольные α-хлоргидриновые промежуточные соединения, такие как 1,3-дигидроксибензолбис(3-хлор-2-гидроксипропиловый)эфир; 1,4-дигидроксибензолбис(3-хлор-2-гидроксипропиловый)эфир; 1,5-дигидроксинафталинбис(3-хлор-2-гидроксипропиловый)эфир; 2,6-дигидроксинафталинбис(3-хлор-2-гидроксипропиловый)эфир; 4,4'-дигидроксибифенилбис(3-хлор-2-гидроксипропиловый)эфир; 3,3',5,5'-тетраметил-4,4'-дигидроксибифенилбис(3-хлор-2-гидроксипропиловый)эфир; 3,3',5,5'-тетраметил-2,2',6,6'-тетрабром-4,4'-дигидроксибифенилбис(3-хлор-2-гидроксипропиловый)эфир; бис(4-гидроксифенил)метанбис(3-хлор-2-гидроксипропиловый)эфир;
2,2-бис(4-гидроксифенил)изопропилиденбис(3-хлор-2-гидроксипропиловый)эфир; фенолформальдегидный новолак(3-хлор-2-гидроксипропиловый)эфир (функциональность более чем 2);
о-крезолформальдегидный новолак(3-хлор-2-гидроксипропиловый)эфир (функциональность более чем 2);
фенолдициклопентадиенильный новолак(3-хлор-2-гидроксипропиловый)эфир (функциональность более чем 2);
нафтолформальдегидный новолак(3-хлор-2-гидроксипропиловый)эфир (функциональность более чем 2); 1,1,1-трис(4-гидроксифенил)метантрис(3-хлор-2-гидроксипропиловый)эфир;
1,1,2,2-тетракис(4-гидроксифенил)этантетракис(3-хлор-2-гидроксипропиловый)эфир и их смеси.
Кроме того, хлор и гидроксильные группы в производном, содержащем указанный выше фрагмент 3-хлор-2-гидрокси-1-пропила, могут быть взаимозаменяемыми с образованием производного, содержащего фрагмент 3-гидрокси-2-хлор-1-пропила.
α-Галогидриновые промежуточные соединения настоящего изобретения включают от около 10 до около 100 процентов, более предпочтительно от около 25 до около 100 процентов, наиболее предпочтительно от около 50 до около 100 процентов в расчете на полную массу одного или более компонентов, проиллюстрированных выше формулами I-V.
Проиллюстрированные формулами I-V α-галогидриновые промежуточные соединения настоящего изобретения получают, сначала получая производное сложного α-гидроксиэфира, по крайней мере, одного или более фенолов, и затем превращая производное сложного α-гидроксиэфира в α-галогидриновое промежуточное соединение, используя in situ способ галоидзамещения-деэстерификации. Более конкретно, α-галогидриновые промежуточные соединения настоящего изобретения получают, осуществляя взаимодействие (А) производного сложного α-гидроксиэфира, по крайней мере, одного или более фенолов с (В) галоидводородом и необязательно в присутствии (С) растворителя.
Галоидводород, компонент (В), который можно использовать для получения α-галогидриновых промежуточных соединений настоящего изобретения, может включать, например, хлористый водород, бромистый водород, йодистый водород.
Количество галоидводорода, компонента (В), которое можно использовать для получения α-галогидриновых промежуточных соединений настоящего изобретения, должно быть достаточным, чтобы обеспечить практически полное превращение производного сложного α-гидроксиэфира в α-галогидриновое промежуточное соединение. Обычно галоидводород используют в количестве от около 0,50 молей до около 20 молей галоидводорода относительно эквивалентов фрагментов сложных α-гидроксиэфиров, подвергающихся превращению в производное сложного α-гидроксиэфира, предпочтительно от около 0,75 молей до около 10 молей галоидводорода относительно эквивалентов производного сложного α-гидроксиэфира, подвергающегося превращению в производное сложного α-гидроксиэфира; и более предпочтительно от около 0,95 моля до около 5 молей галоидводорода относительно эквивалентов фрагментов сложного α-гидроксиэфира, подвергающегося превращению в производное сложного α-гидроксиэфира.
Галоидводород можно добавлять в реакцию в чистом виде, например в виде жидкости или газа. Если галоидводород в реакцию вводят в виде газа, его можно подавать в виде непрерывного потока газа. Галоидводород можно также растворить в растворителе, таком как указанно ниже для компонента (С), и подавать в реактор в виде раствора. Если используемое количество галоидводорода превышает стехиометрическое количество, необходимое для обеспечения полного превращения производного сложного α-гидроксиэфира, избыточное количество можно удалить из реакционной смеси, промывая ее водой или осторожно нейтрализуя основанием. Предпочтительно выделять и рециркулировать избыток галоидводорода путем дистилляции галоидводорода из реакционной смеси.
Растворители, необязательные компоненты (С), которые можно использовать в указанном выше способе получения α-галогидринового промежуточного соединения, могут быть, но не ограничиваются ими, алифатическими и циклическими углеводородами, такими как пентан, гексан, октан, изооктан, циклогексан и циклооктан, ароматическими углеводородами, такими как бензол, толуол и ксилол; хлорированными растворителями, такими как метилендихлорид, тетрахлорэтан и хлорбензол; апротонными растворителями, такими как ацетон, метилизобутилкетон, ацетонитрил, диметоксиэтан, 2,2'-диметоксидиэтиловый эфир, диоксан, диметилсульфоксид и 1-метокси-2-ацетоксипропан; протонными растворителями, такими как этанол, 1-пропанол, изопропиловый спирт, 1-бутанол, 2-бутанол, трет-бутанол, 1-пентанол, трет-амиловый спирт, 1-гексанол, циклогексанол и 1-метокси-2-гидроксипропан; их частично или полностью фторированные производные; и любые их комбинации. Растворитель необязательно можно использовать в присутствии воды или без нее.
Если необязательно используют протонные спиртовые растворители, предпочтительно, чтобы спиртовые растворители были вторичными или третичными спиртовыми растворителями, такими как изопропиловый спирт, 2-бутанол, трет-бутанол, трет-амиловый спирт и 1-метокси-2-гидроксипропан; их частично или полностью фторированными производными и любыми их комбинациями.
Обычно количество растворителя, необязательного компонента (С), используемого в способе настоящего изобретения, может составлять от около 0 до около 50 частей (в расчете на массу) отдельного растворителя или смеси двух или более растворителей на одну часть производного сложного α-гидроксиэфира. Более предпочтительным отношением растворителя к производному сложного α-гидроксиэфира является величина от около 0 до около 10 частей растворителя на 1 часть производного сложного α-гидроксиэфира. Наиболее предпочтительным отношением растворителя к производному сложного α-гидроксиэфира является величина от около 0 до около 5 частей растворителя на 1 часть производного сложного α-гидроксиэфира.
Температура указанной выше in situ реакции галоидзамещения-деэстерификации производного сложного α-гидроксиэфира обычно составляет от около 0°С до около 150°С; предпочтительно от около 20°С до около 130°С и более предпочтительно от около 40°С до около 110°С. При температуре ниже 0°С реакция не завершается. При температуре выше 150°С могут происходить нежелательные реакции хлорирования.
Давление, используемое в указанной выше in situ реакции галоидзамещения-деэстерификации производного сложного α-гидроксиэфира для получения α-хлоргидринового промежуточного соединения может быть атмосферным, ниже атмосферного или выше атмосферного. Величина давления не является критической и может определяться параметрами, такими как тип используемого галоидводорода, температура реакции, тип используемого растворителя или температура кипения азеотропов растворителей.
In situ реакции галоидзамещения-деэстерификации производного сложного α-гидроксиэфира для получения производного сложного α-галогидринового эфира можно осуществлять периодически или непрерывно. В периодическом способе производное сложного α-гидроксиэфира необязательно растворяют в растворителе и в реактор вводят галоидводород, как было указано выше. В периодическом способе весьма желательно проводить реакцию под давлением для поддержания галоидводорода в фазе раствора. Когда реакция в периодическом способе с использованием галоидводорода в фазе раствора завершается, избыток галоидводорода и карбоновой кислоты, образующейся при деэстерификации, можно удалить из реакционной смеси, промывая водой или осторожно нейтрализуя основанием. Или избыток галоидводорода и карбоновой кислоты можно выделить и рециркулировать, как описано ниже.
В некоторых случаях, например при использовании газообразного хлористого водорода, может оказаться выгодным непрерывно барботировать газ через реактор при эффективном смешивании или перемешивании реакционной смеси в реакторе. В этом способе газообразный хлористый водород, выходящий из реактора, собирают и рециркулируют в реактор.
В непрерывном способе галоидзамещения-деэстерификации производного сложного α-гидроксиэфира можно необязательно смешать с растворителем и затем тщательно перемешать с галоидводородом, по мере того как производное сложного α-гидроксиэфира и необязательно растворитель подают в реактор. Реакторы, которые можно использовать, хорошо известны в данной области, например, реактор может иметь трубчатую конструкцию. После того, как продукт реакции покидает реактор, продукт реакции можно обработать, используя серию стадий очистки. Например, в одном из вариантов, когда используют растворитель, температура кипения которого ниже температуры кипения получаемой карбоновой кислоты, продукт реакции можно: сначала подвергнуть перегонке для удаления избытка галоидводорода, причем галоидводород можно затем рециркулировать в реактор, где протекает реакция галоидзамещения-деэстерификации; во-вторых, подвергнуть перегонке для удаления растворителя, причем растворитель можно затем рециркулировать в реактор, где протекает реакция галоидзамещения-деэстерификации; в-третьих, подвергнуть перегонке для удаления продукта карбоновой кислоты, причем карбоновую кислоту можно затем рециркулировать в реакцию с участием аллилового сложного эфира.
В другом втором варианте, если используют растворитель, температура которого выше температуры кипения получаемой карбоновой кислоты, продукт реакции можно: сначала подвергнуть перегонке для удаления избытка галоидводорода, причем галоидводород можно затем рециркулировать в реактор, где протекает процесс галоидзамещения-деэстерификации; во-вторых, подвергнуть перегонке для удаления карбоновой кислоты - продукта деэстерификации. Во втором варианте, приведенном выше, растворитель может быть необязательно удален, например перегонкой, или если нет необходимости в удалении растворителя, в этом случае растворитель подается далее в качестве растворителя для последующей стадии эпоксидирования. Описанную выше стадию перегонки можно осуществить при атмосферном давлении, при давлении ниже или выше атмосферного, что хорошо известно в данной области.
Весьма желательно и предпочтительно осуществлять указанные выше способы, в которых α-галогидриновое промежуточное соединение можно превратить в эпоксидную смолу без дополнительной очистки.
Галоидзамещение-деэстрификацию производного сложного α-гидроксиэфира для получения α-галогидринового промежуточного соединения настоящего изобретения можно проиллюстрировать следующей последовательностью реакций (V), которая демонстрирует хлорзамещение-деацетилоксилирование α-гидроксиацетатного производного. Более конкретно, последовательность реакций (V) демонстрирует хлорзамещение-деацетилоксилирование α-гидроксиацетатного производного для получения α-хлоргидринового промежуточного соединения настоящ