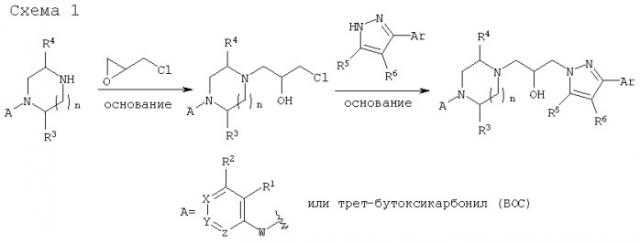
Способ лечения аллергии с использованием замещенных пиразолов
Иллюстрации
Показать всеИзобретение относится к области медицины и касается способа лечения аллергии путем введения субъекту терапевтически эффективного количества фармацевтической композиции, включающей соединение формулы I. Изобретение обеспечивает повышенную эффективность лечения. 6 з.п. ф-лы, 3 ил.
Реферат
Область изобретения
Данное изобретение относится к использованию замещенных пиразолов для лечения аллергического заболевания.
Предпосылки создания изобретения
Атопическая аллергия поражает по крайней мере 20% населения в развитых странах и включает широкий диапазон IgE-опосредованных заболеваний, таких как сенная лихорадка, астма, атопический дерматит и пищевые аллергии. Воздействие на субъекта, подверженного аллергии, соответствующих аллергенов приводит к поперечному связыванию аллерген-специфической IgE связи с тучными клетками, инициируя дегрануляцию и высвобождение провоспалительных медиаторов, таких как гистамин и эйкозаноиды, которые вызывают ответную реакцию благополучие-и-сигнал в кожном тесте. Обычно, за такой ранней ответной реакцией следует продолжительная поздняя реакция, в которой воспалительные клетки, в частности эозинофилы и активированные ТН-2 CD4 T-клетки, привлекаются в место аллергического воздействия. Воспалительные цитокины, такие как IL-4 и IL-5, оба продуцируемые ТН-2 клетками, важны для продуцирования IgE В-клетками и для эозинофилии соответственно. Было показано, что иммунотерапия, нацеленная на CD4 Т-клетки, является эффективной для снижения продуцирования IgE, активации провоспалительных клеток и высвобождения воспалительных медиаторов.
Лечение аллергии в настоящее время, нацеленное на CD4 Т-клетки, имеет смешанный успех. Уменьшение чувствительности с использованием аллергеновых экстрактов или вакцин является эффективным в случае многих аллергенов, таких как укусы насекомых Hymenoptera, которые могут вызывать угрожающие жизни аллергические реакции. Механизм может представлять собой либо индуцирование толерантности Т-клеток, либо превращение ТН-2 в ТН-1. Однако такое лечение требует продолжительного режима лечения, частых визитов лечащего врача и предварительную стабилизацию с использованием других лекарственных средств и связано с некоторой долей болезненности и редкими смертями. Альтернативно, иммуноподавляющие лекарственные средства, такие как стероиды, которые эффективно стабилизируют начинающиеся аллергические ответные реакции, часто связаны с серьезными побочными действиями.
Активация CD4 Т-клеток является основным фактором в инициировании и сохранении аллергической ответной реакции. Аллергены поглощаются специализированными антиген-представляющими клетками (APCs), такими как дендритные клетки и В-клетки. Белковые аллергены проходят через эндосомальную и лизосомальную системы, где они разрушаются различными протеазами. Такие пептидные фрагменты связываются молекулами МНС класса II, которые на клеточной поверхности представляют собой гетеротримерные комплексы, состоящие из двух трансмембранных гликопротеиновых цепей (α и β), которые образуют связывающую поддержку для третьего компонента, пептида из 11-20 аминокислот. Комплекс антиген-молекула МНС класса II распознается CD4 Т-клетками и приводит к активации Т-клетки. Активированные Т-клетки, в свою очередь, активируют несколько других компонентов иммунной системы, таких как В-клетки и макрофаги, которые являются ключевыми для ответной реакции тела на патогены, но также приводят к симптомам аллергии.
Молекулы класса II, как и другие трансмембранные белки, перемещаются в эндоплазматическую сеть (ER) после синтеза, где они связываются с третьим белком, инвариантной цепью (Ii). Инвариантная цепная молекула представляет собой трансмембранный белок типа II, который служит в качестве класс II-специфического компаньона, промотирующего выход комплексов класс II-Ii из ER и не допускающего связывания молекул класса II с пептидами и развернутыми белками в ER и секреторном пути. Целенаправляющий мотив в цитоплазматическом хвосте Ii направляет комплексы класс II-Ii из секреторного пути в эндосомальную систему.
Прежде чем молекулы МНС класса II смогут представлять собой антиген, Ii должен быть удален рядом протеаз, которые отщепляют Ii. Конечные Ii пептидные фрагменты, называемые класса II-связанные инвариантные цепные пептиды (CLIP), занимают место пептидного связывания молекулы класса II и в большинстве случаев самопроизвольно не высвобождаются. CLIP защищает связывающую зону класса II от свертывания как во время внутриклеточного транспорта, так и после Ii разрушения в эндосомальной системе. Связывание антигенных пептидов, генерированных из эндоцитозных белков, требует свободного и уже открытого сайта связывания. Следовательно, CLIP должен высвобождаться во время, когда открытый сайт связывания стабилизирован, чтобы давать возможность связывания с другими пептидами. Лейкоцитный антиген человека -DM («HLA-DM») опосредует обе такие функции, промотируя таким образом связывание антигенных пептидов. После связывания пептидов молекулы класса II транспортируются к клеточной поверхности через пути, которые большей частью не известны.
Принимая вышеизложенное во внимание, ингибирование протеолиза инвариантной цепи будет предотвращать удаление Ii из связывающей зоны класса II, что, в свою очередь, будет специфически блокировать связывание антигена с молекулой МНС класса II.
Катепсин S (CatS) представляет собой цистеинпротеазу, экспрессируемую в лимфатических тканях. CatS опосредует протеолиз инвариантной цепи, что является предпосылкой пептидного нагружения молекул класса II (Riese et al. (1996) Immunity 4:357). CatS имеет 50-60% гомологию с катепсинами L и К, но отличается от них тем, что имеет широкий оптимум рН, который расширен в щелочную область рН. CatS модулирует антигенную демонстрацию на животных моделях, и ингибиторы являются эффективными на модели астмы (Riese et al. (1998) J.Clin.Invest. 101:2351). Катепсин S-дефицитные мыши обладают ослабленной способностью представлять экзогенные белки с помощью профессиональных антиген-представляющих клеток (Nakagawa et al (1999) Immunity 10:207; Shi et al. (1999) Immunity 10:197).
Предполагается, что соединения, которые ингибируют протеолитическую активность катепсина S человека, могут найти применение для лечения хронических аутоиммунных заболеваний, включая, но не ограничиваясь ими, волчанку и ревматоидный артрит; и имеют потенциальную полезность для модулирования иммунного ответа на трансплантацию тканей. Способы модулирования аутоиммунитета с помощью агента, который модулирует активность катепсина S, например, протеолиз Ii цепи, а также способы лечения субъекта, имеющего аутоиммунное заболевание, способы оценки лечения на его способность модулировать иммунный ответ описаны в WO 99/58153.
Соединения, некоторым образом подобные соединениям настоящего изобретения, описаны в следующих ссылках.
Winters и др. ((Winters G., Sala A., Barone D., Baldoli E. J.Med.Chem., 1985, 28, 934-940; Singh P., Sharma R.C., Quant. Struct. -Act. Relat. 1990, 9, 29-32; Winters G., Sala A., Barone D. в патенте США 4500525 (1985)) описали бициклические пиразолы показанного ниже типа. Заместитель R никогда не содержит гетероциклическое кольцо, и данным молекулам не предписывается никакой ингибирующей активности в отношении протеазы; они описаны в качестве модуляторов α1-адренергических рецепторов.
Shutske и др. описали представленные ниже бициклические пиразолы. В их системе пиридиновое кольцо является ароматическим (Shutske G.M., Kapples K.J., Tomer J.D. Патент США 5264576 (1993)). Другая ссылка относится к R, являющемуся линкером для гетероцикла, формула изобретения указывает только R=водород. Соединения упоминаются в качестве ингибиторов обратного захвата серотонина.
Соединение 2-[4-[4-(3-метил-5-фенил-1Н-пиразол-1-ил)бутил]-1-пиперазинил]пиримидин известно из ЕР-382637, где описаны пиримидины, обладающие анксиолитическими свойствами. Данное соединение и его аналоги дополнительно описаны в ЕР-502786 в качестве сердечно-сосудистых агентов и агентов в отношении центральной нервной системы. Фармацевтические препараты с такими соединениями описаны в ЕР-655248 для применения при лечении желудочной секреции и в качестве противоязвенных агентов. В WO 9721439 описаны лекарственные средства с такими соединениями для лечения обцессивно-компульсивных нарушений, апноэ (отдышка) во сне, половых расстройств, рвоты и морской болезни.
Соединения 5-метил-3-фенил-1-[4-(4-фенил-1-пиперазинил)бутил]-1Н-индазол и 5-бром-3-(2-хлорфенил)-1-[4-(4-фенил-1-пиперазинил)бутил]-1Н-индазол, в частности их гидрохлоридные соли, известны из WO-9853940 и СА122:314528, где данные и подобные им соединения описаны в качестве ингибиторов киназы в первой ссылке и как обладающие сродством к бензодиазепиновым рецепторам в последней ссылке.
Краткое изложение сущности изобретения
Объектом настоящего изобретения является применение ингибиторов катепсина S для лечения аллергических заболеваний, включая, но не ограничиваясь этим, атопические аллергии. Примеры аллергического заболевания включают сенную лихорадку, астму, атопический дерматит и пищевые аллергии. Аллергены включают пыль, пыльцу, плесень и аллергию на домашних животных или шерсть домашних животных.
В одном аспекте настоящее изобретение относится к способу лечения субъекта, страдающего от аллергического заболевания, в частности от атопического аллергического заболевания, который включает введение указанному субъекту терапевтически эффективного количества фармацевтической композиции, включающей ингибитор катепсина S.
В другом аспекте настоящее изобретение относится к способу лечения субъекта, страдающего от IgE-опосредованного аллергического заболевания, в частности от атопического аллергического болезненного состояния, который включает введение указанному субъекту терапевтически эффективного количества фармацевтической композиции, включающей ингибитор катепсина S.
В третьем аспекте изобретение относится к применению или применению для получения лекарственного средства ингибитора катепсина S для лечения аллергического заболевания, более конкретно для лечения IgE-опосредованных аллергических заболеваний, еще более конкретно для лечения сенной лихорадки, астмы, атопических дерматитов или пищевых аллергий. Изобретение также относится к противоаллергическим фармацевтическим композициям, включающим в качестве активного ингредиента эффективное количество ингибитора катепсина S и фармацевтически приемлемый носитель. Активный ингредиент может быть введен в состав лекарственного средства любым способом, подходящим для конкретного аллергического заболевания, включая аэрозоль, пероральные и местные препараты и препараты замедленного высвобождения.
Настоящее изобретение касается лечения аллергического заболевания с использованием одного или нескольких соединений, которые могут быть представлены формулой (I):
где
R1 представляет собой водород, азидо, галоген, С1-5 алкокси, гидрокси, С1-5 алкил, С2-5 алкенил, циано, нитро, R7R8N, С2-8 ацил, R9OC=O, R10R11NC=O или R10R11NSO2, или R1 взят вместе с W, как описано ниже;
R2 представляет собой водород, галоген, С1-5 алкокси, С1-5 алкил, С2-5 алкенил, С1-5 галогеналкил, циано или R48R49N;
альтернативно, R1 и R2 могут быть взяты вместе с образованием необязательно замещенного 5-7-членного карбоциклического или гетероциклического кольца, указанное кольцо может быть ненасыщенным или ароматическим;
каждый R3 и R4 независимо представляет собой водород или С1-5 алкил;
каждый R5 и R6 независимо представляет собой водород, С1-5 алкил, С2-5 алкенил, С1-5 алкокси, С1-5 алкилтио, галоген или 4-7-членный карбоциклил или гетероциклил;
альтернативно, R5 и R6 могут быть взяты вместе с образованием необязательно замещенного 5-7-членного карбоциклического или гетероциклического кольца, указанное кольцо может быть ненасыщенным или ароматическим, и необязательно может быть замещено одним-тремя заместителями, независимо выбранными из галогена, циано, амино, нитро, R40, R40O-, R40S-, R40O(C1-5 алкилен)-, R40O(C=O)-, R40(C=O)-, R40(C=S)-, R40(C=O)O-, R40O(C=O)(C=O)-, R40SO2, NHR62(C=NH)-, NHR62SO2- и NHR62(C=O)-;
R40 представляет собой Н, С1-5 алкил, С2-5 алкенил, фенил, бензил, фенэтил, С1-5 гетероциклил, (С1-5 гетероциклил)С1-5 алкилен, амино или моно- или ди(С1-5 алкил)амино, или R58OR59-, где R58 представляет собой Н, С1-5 алкил, С2-5 алкенил, фенил, бензил, фенэтил, С1-5 гетероциклил или (С1-5 гетероциклил)С1-6 алкилен, и R59 представляет собой С1-5 алкилен, фенилен или двухвалентный С1-5 гетероциклил; и
R62 может представлять собой Н в дополнение к значениям для R40;
R7 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, нафтил, С1-5 гетероциклил, С2-8 ацил, ароил, R27OC=O, R28R29NC=O, R27SO, R27SO2 или R28R29NSO2;
R8 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил или С1-5 гетероциклил;
альтернативно, R7 и R8 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
R9 представляет собой С1-5 алкил, фенил, нафтил или С1-5 гетероциклил;
R21 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, нафтил, С1-5 гетероциклил, С2-8 ацил, ароил, R30OC=O, R31R32NC=O, R30SO, R30SO2 или R31R32NSO2;
R22 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил или С1-5 гетероциклил;
альтернативно, R21 и R22 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
каждый R23, R26, R27, R30, R33, R44, R45 и R50 представляет собой С1-5 алкил, фенил, нафтил или С1-5 гетероциклил;
R24 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, нафтил, С1-5 гетероциклил, С2-8 ацил, ароил, R33OC=O, R34R35NC=O, R33SO, R33SO2 или R34R35NSO2;
R25 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил или С1-5 гетероциклил;
альтернативно, R24 и R25 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
каждый R10 и R11 независимо представляет собой водород, С1-5 алкил, С2-5 алкенил, фенил или С1-5 гетероциклил;
альтернативно, R10 и R11 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
каждый R28, R29, R31, R32, R34, R35, R46, R51 и R52 независимо представляет собой водород, С1-5 алкил, фенил или С1-5 гетероциклил;
альтернативно, R28 и R29, R31 и R32,R34 и R35, R46 и R47, илиR51 и R52 независимомогут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
n равно 1 или 2;
G представляет собой С3-6 алкендиил или С3-6 алкандиил, необязательно замещенный гидрокси, галогеном, С1-5 алкилом, С1-5 алкокси, оксо, гидроксиимино, CO2R60, R60R61NCO2, (L)-C1-4 алкиленом, (L)-C1-5 алкокси, N3 или [(L)-C1-5алкилен]амино;
каждый R60 и R61 независимо представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, бензил, фенэтил или С1-5 гетероциклил;
альтернативно, R60 и R61 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
L представляет собой амино, моно- или ди-С1-5 алкиламино, пирролидинил, морфолинил, пиперидинил, гомопиперидинил или пиперазинил, где доступные кольцевые атомы азота могут быть необязательно замещены С1-5 алкилом, бензилом, С2-5 ацилом, С1-5 алкилсульфонилом или С1-5 алкоксикарбонилом;
Х представляет собой азот или R12C;
Y представляет собой азот или R13C;
Z представляет собой азот или R14C;
R12 представляет собой водород, галоген, С1-5 алкокси, С1-5 алкил, C2-5 алкенил, циано, нитро, R21R22N, C2-8 ацил, С1-5 галогеналкил, С1-5 гетероциклил, (С1-5 гетероциклил)С1-5 алкилен, R23OC=O, R23O(C=O)NH-, R23SO, R22NHCO-,, R22NH(C=O)NH-, R23(C1-4 алкилен)NHCO-, R23SO2 или R23SO2NH-;
R13 представляет собой водород, галоген, С1-5 алкокси, С1-5 алкил, C2-5 алкенил, циано, нитро, R42R43N, C2-8 ацил, С1-5 галогеналкил, С1-5 гетероциклил, (С1-5 гетероциклил)С1-5 алкилен R44OC=O, R44O(C=O)NH-, R44SO, R43NHCO-, R43NH(C=O)NH-, R44(C1-4 алкилен)NHCO-, R44SO2 или R44SO2NH-;
R14 представляет собой водород, галоген, С1-5 алкокси, С1-5 алкил, C2-5 алкенил, циано, нитро, R24R25N, C2-8 ацил, С1-5 галогеналкил, С1-5 гетероциклил, (С1-5 гетероциклил)С1-5 алкилен R26OC=O, R26O(C=O)NH-, R26SO, R25NHCO-, R25NH(C=O)NH-, R26(C1-4 алкилен)NHCO-, R26SO2 или R26SO2NH-;
альтернативно, R12 и R13 или R12 и R2, илиR13 и R14 могут быть взяты вместе с образованием необязательно замещенного 5-6-членного карбоциклического или гетероциклического кольца, указанное кольцо может быть ненасыщенным или ароматическим;
Ar представляет собой моноциклическое или бициклическое арильное или гетероарильное кольцо, необязательно замещенное 1-3 заместителями, выбранными из галогена, С1-5 алкокси, С1-5 алкила, С2-5 алкенила, циано, азидо, нитро, R15R16N, R17SO2, R17S, R17SO, R17O(C=O), R15R16NC=O, С1-5 галогеналкила, С1-5 галогеналкокси, С1-5 галогеналкилтио и С1-5 алкилтио;
R15 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, бензил, С1-5 гетероциклил, С2-8 ацил, ароил, R53OC=O, R54R55NC=O, R53S, R53SO, R53SO2 или R54R55NSO2;
R16 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, бензил или С1-5 гетероциклил;
альтернативно, R15 и R16 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
каждый R17 и R53 представляет собой С1-5 алкил, фенил или С1-5 гетероциклил;
каждый R54 и R55 независимо представляет собой водород, С1-5 алкил, С2-5 алкенил, фенил, бензил или С1-5 гетероциклил;
альтернативно, R54 и R55 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
W представляет собой SO2, C=O, CHR20 или ковалентную связь; или W и R1, взятые вместе с 6-членным кольцом, к которому оба из них присоединены, образуют одну из двух следующих формул:
где Ха представляет собой О, S или N; и Хb представляет собой О, S или SO2;
R20 представляет собой водород, С1-5 алкил, фенил, бензил, нафтил или С1-5 гетероциклил;
R42 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, нафтил, С1-5 гетероциклил, С2-8 ацил, ароил, R45OC=O, R46R47NC=O, R45SO, R45SO2 или R46R47NSO2;
R43 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил или С1-5 гетероциклил;
альтернативно, R42 и R43 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим;
R44 представляет собой С1-5 алкил, С2-5 алкенил, фенил, нафтил или С1-5 гетероциклил;
R48 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил, нафтил, С1-5 гетероциклил, С2-8 ацил, ароил, R50OC=O, R51R52NC=O, R50SO, R50SO2 или R51R52NSO2;
R49 представляет собой водород, С1-5 алкил, С3-5 алкенил, фенил или С1-5 гетероциклил;
альтернативно, R48 и R49 могут быть взяты вместе с образованием необязательно замещенного 4-7-членного гетероциклического кольца, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим; и
где каждая из вышеуказанных углеводородных или гетероуглеродных групп, если не указано иначе, и, в дополнение к любым определенным заместителям, необязательно и независимо замещена 1-3 заместителями, выбранными из метила, галогенметила, гидроксиметила, галогена, гидрокси, амино, нитро, циано, С1-5 алкила, С1-5 алкокси, -СООН, С2-6 ацила, [ди(С1-4 алкил)амино]С2-5алкилена, [ди(С1-4 алкил)амино]С2-5алкил-NH-CO- и С1-5 галогеналкокси;
или его фармацевтически приемлемой соли, амида или сложного эфира, включая их стереоизомерную форму.
Описанные соединения представляют собой ингибиторы протеолитической активности катепсина S человека с высоким сродством связывания. Для применения в медицине может оказаться желательным получение фармацевтически приемлемых солей соединений формулы (I).
Некоторые соединения настоящего изобретения могут иметь один стереогенный атом и могут существовать в виде двух энантиомеров. Некоторые соединения настоящего изобретения могут иметь два или несколько стереогенных атомов и, дополнительно, могут существовать в виде диастереомеров. Специалистам в данной области следует понимать, что все такие стереоизомеры и их смеси в любом соотношении включены в объем настоящего изобретения.
Другой аспект настоящего изобретения относится к фармацевтическим противоаллергическим композициям, включающим соединение формулы (I) и фармацевтически приемлемый носитель. Дополнительный вариант осуществления изобретения представляет собой способ получения противоаллергической фармацевтической композиции, включающий смешивание указанного соединения, описанного выше, с подходящим фармацевтически приемлемым носителем.
В изобретении также рассматриваются фармацевтические композиции, включающие более одного соединения формулы (I) и композиции, включающие соединение формулы (I) и другой фармацевтически активный агент.
Еще одним объектом изобретения является способ лечения аллергического заболевания или болезненного состояния, опосредованного ферментом катепсином S, у нуждающегося в этом субъекта, включающий введение субъекту терапевтически эффективного количества любого из соединений или фармацевтических композиций, описанных выше. При введении более одного активного агента терапевтически эффективное количество может представлять собой совместное эффективное количество. Описанные здесь соединения ингибируют протеазную активность катепсина S человека, фермента, вовлеченного в иммунную ответную реакцию. В предпочтительных вариантах осуществления ингибирование катепсина S является селективным. Как таковые описанные соединения и композиции могут использоваться для профилактики, ингибирования или лечения аллергических заболеваний, в частности атопических аллергических заболеваний.
Дополнительные отличительные признаки и преимущества изобретения будут очевидны из приведенных ниже подробного описания и примеров и прилагаемой формулы изобретения.
Краткое описание чертежей
На фиг.1 показано ингибирование пролиферативных ответных реакций Т-клеток человека на два вида пылевых клещей, Der p и Der f. Верхняя диаграмма, фиг.1А: Кривая разведения для очищенного РВМС от аллергического донора при культивировании с титрованными дозами аллергенных экстрактов, приготовленных из Der p и Der f, в течение семи дней. Пролиферацию Т-клеток оценивали в баллах путем измерения внедрения 3Н-тимидина в течение 18 часов в конце культивирования. Нижняя диаграмма, фиг.1В: Действие титрованных доз LHVS на пролиферативные ответные реакции Т-клеток на экстракты пылевых клещей.
На фиг.2 показано ингибирование пролиферативных ответных реакций Т-клеток человека на амброзию, но не ConA, с использованием LHVS. Верхняя диаграмма, фиг.2А: Кривая разведения для очищенного РВМС от аллергического донора при культивировании с титрованными дозами аллергенных экстрактов, приготовленных из Амброзии короткой и Амброзии гигантской в течение семи дней. Пролиферацию Т-клеток оценивали в баллах путем измерения внедрения 3Н-тимидина в течение 18 часов в конце культивирования. Нижняя диаграмма, фиг.2В: Действие титрованных доз LHVS на пролиферативные ответные реакции Т-клеток на экстракты амброзии.
На фиг.3 показано ингибирование пролиферативных ответных реакций Т-клеток человека на Der f, но не Con A, двумя ингибиторами катепсина S, соединениями примера 11 (фиг.3А) и примера 36 (фиг.3В). Очищенный РВМС от аллергического донора культивировали с экстрактами аллергенов, приготовленных из Der f в присутствии титрованных доз указанных соединений в течение семи дней. Пролиферацию Т-клеток оценивали в баллах путем измерения внедрения 3Н-тимидина в течение 18 часов в конце культивирования.
Подробное описание изобретения
Цель настоящего изобретения заключалась в определении, воздействует ли ингибирование катепсина S на присутствие определенных антигенов в системе человека. Согласно изобретению, в настоящее время установлено, что ингибиторы катепсина S блокируют присутствие нескольких неочищенных аллергеновых экстрактов у человека в анализе ex vivo, подтверждая, таким образом, полезность ингибиторов катепсина S для лечения таких аллергических заболеваний.
Блокирование Ii разложения должно снизить присутствие антигена в CD4 Т клетках и прервать нормальный иммунный ответ. Ингибитор катепсина S должен специфически воздействовать на активацию CD4 T клеток, таким образом, ограничивая степень сопутствующего иммуноподавления, нежелательного побочного действия при кортикостероидной терапии.
При использовании ингибиторов катепсина S в соответствии со способами настоящего изобретения иммунологический компонент аллергической реакции может быть блокирован в различной степени, обладая преимуществом по сравнению с современной терапией, заключающимся в большей селективности, наличии незначительных или сниженных побочных действий или тем и другим. Настоящее изобретение частично основано на обнаружении того факта, что ингибиторы катепсина S могут блокировать присутствие неочищенных аллергеновых экстрактов у человека в анализе ex vivo. Такая ex vivo система близко имитирует процесс, который происходит во всем теле, когда антигены входят в систему кровообращения и представлены с помощью антиген-представляющих клеток, которые, в свою очередь, активируют CD4 T клетки. В случае лечения субъекта ингибитор или его метаболит также будут присутствовать в крови, как и в анализе ex vivo.
Объектом изобретения является лечение аллергического заболевания с использованием соединений пиразола формулы (I).
А. Термины
Следующие термины, используемые в описании, определены ниже.
«Алкил» включает необязательно замещенные линейные или разветвленные углеводороды, имеющие по крайней мере один удаленный водород с образованием радикальной группы. Алкильные группы включают метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, 1-метилпропил, пентил, изопентил, втор-пентил, гексил, гептил, октил и подобные. Алкил включает циклоалкил, такой как циклопропил, циклобутил, циклопентил и циклогексил.
«Алкенил» включает необязательно замещенные линейные и разветвленные углеводородные радикалы, как указано выше, имеющие, по крайней мере, одну углерод-углеродную двойную связь (sp2). Алкенилы включают этенил (или винил), проп-1-енил, проп-2-енил (или аллил), изопропенил (или 1-метилвинил), бут-1-енил, бут-2-енил, бутадиенилы, пентенилы, гекса-2,4-диенил и подобные. Углеводородные радикалы, имеющие сочетание двойных связей и тройных связей, такие как 2-пентен-4-инил, включены в данном описании в определения алкинилов. Алкенил включает циклоалкенил. Цис- и транс- или (Е)- и (Z)-формы включены в данное изобретение.
«Алкинил» включает необязательно замещенные линейные и разветвленные углеводородные радикалы, как указано выше, имеющие, по крайней мере, одну углерод-углеродную тройную связь (sp). Алкинилы включают этинил, пропинилы, бутинилы и пентинилы. Углеводородные радикалы, имеющие сочетание двойных связей и тройных связей, такие как 2-пентен-4-инил, включены в данном описании в определения алкинилов. Алкинил не включает циклоалкинил.
«Алкокси» включает необязательно замещенную линейную или разветвленную алкильную группу с концевым кислородом, связывающим алкильную группу с остатком молекулы. Алкокси включает метокси, этокси, пропокси, изопропокси, бутокси, трет-бутокси, пентокси и подобные. «Аминоалкил», «тиоалкил» и сульфонилалкил» аналогичны алкоксильной группе, при этом концевой атом кислорода в алкокси заменен соответственно на NH (или NR), S и SO2. Гетероалкил включает алкокси, аминоалкил, тиоалкил и подобные.
«Арил» включает фенил, нафтил, бифенилил, тетрагидронафтил и подобные, каждый из которых необязательно может быть замещенным. Арил также включает арилалкильные группы, такие как бензил, фенэтил и фенилпропил. Арил включает кольцевую систему, содержащую необязательно замещенное 6-членное карбоциклическое ароматическое кольцо, указанная система может быть бициклической, мостиковой и/или конденсированной. Система может включать кольца, которые являются ароматическими или частично или полностью насыщенными. Примеры кольцевых систем включают инденил, пенталенил, 1,4-дигидронафтил, инданил, бензимидазолил, бензотиофенил, индолил, бензофуранил, изохинолинил и подобные.
«Гетероциклил» включает необязательно замещенные ароматические и неароматические кольца, имеющие атомы углерода и, по крайней мере, один гетероатом (О, S, N) или гетероатомный фрагмент (SO2, CO, CONH, COO) в кольце. Если не указано иначе, гетероциклический радикал может иметь валентность, связывающую его с остатком молекулы через атом углерода, например, 3-фурил или 2-имидазолил, или через гетероатом, например, N-пиперидил или 1-пиразолил. Предпочтительно моноциклический гетероциклил содержит от 4 до 7 кольцевых атомов или от 5 до 6 кольцевых атомов; в кольце может быть от 1 до 5 гетероатомов или гетероатомных фрагментов и предпочтительно от 1 до 3. Гетероциклил может быть насыщенным, ненасыщенным, ароматическим (например, гетероарил), неароматическим или конденсированным.
Гетероциклил также включает конденсированные, например бициклические, кольца, такие как необязательно конденсированные с необязательно замещенным карбоциклическим или гетероциклическим пяти- или шестичленным ароматическим кольцом. Например, «гетероарил» включает необязательно замещенное шестичленное гетероароматическое кольцо, содержащее 1, 2 или 3 атома азота, конденсированное с необязательно замещенным пяти- или шестичленным карбоциклическим или гетероциклическим ароматическим кольцом. Указанное гетероциклическое пяти- или шестичленное ароматическое кольцо, конденсированное с указанным пяти- или шестичленным ароматическим кольцом, может содержать 1, 2 или 3 атома азота, когда это шестичленное кольцо, или 1, 2 или 3 гетероатома, выбранных из кислорода, азота и серы, когда это пятичленное кольцо.
Примеры гетероциклилов включают тиазолил, фурил, пиранил, изобензофуранил, пирролил, имидазолил, пиразолил, изотиазолил, изоксазолил, пиридил, пиразинил, пиримидинил, пиридазинил, индолизинил, изоиндолил, индолил, индазолил, пуринил, хинолил, фуразанил, пирролидинил, пирролинил, имидазолидинил, имидазолинил, пиразолидинил, пиразолинил, пиперидил, пиперазинил, индолинил и морфолинил. Например, предпочтительные гетероциклилы или гетероциклические радикалы включают морфолинил, пиперазинил, пирролидинил, пиридил, циклогексилимино, циклогептилимино и, более предпочтительно, пиперидил.
Примерами, иллюстрирующими гетероарил, являются тиенил, фуранил, пирролил, имидазолил, оксазолил, тиазолил, бензотиенил, бензофуранил, бензимидазолил, бензоксазолил, бензотиазолил.
«Ацил» относится к карбонильной части, связанной или с атомом водорода (то есть формильная группа) или с необязательно замещенной алкильной или алкенильной цепью, или гетероциклилом.
«Гало» или «галоген» включает фтор, хлор, бром и иод, и предпочтительны в качестве заместителя хлор или бром.
«Алкандиил» или «алкилен» представляет собой линейный или разветвленный необязательно замещенный двухвалентный алкановый радикал такой как, например, метилен, этилен, пропилен, бутилен, пентилен или гексилен.
«Алкендиил» представляет собой, аналогично описанному выше, линейный или разветвленный необязательно замещенный двухвалентный алкеновый радикал, такой как, например, пропенилен, бутенилен, пентенилен или гексенилен. В таких радикалах атом углерода, связывающий азот, предпочтительно не должен быть ненасыщенным.
«Ароил» относится к карбонильной группе, связанной с необязательно замещенной арильной или гетероарильной группой, где арил или гетероарил имеют представленные выше значения. В частности, бензоил представляет собой фенилкарбонил.
Как определено в данном описании, два радикала вместе с атомом(ами), к которому они присоединены, могут образовывать необязательно замещенное 4-7-, 5-7- или 5-6-членное карбоциклическое или гетероциклическое кольцо, указанное кольцо может быть насыщенным, ненасыщенным или ароматическим. Указанные кольца могут быть такими, как определено выше в разделе «Краткое изложение сущности изобретения». Конкретные примеры таких колец такие, как указано в следующем разделе.
«Фармацевтически приемлемые соли, сложные эфиры и амиды» включают карбоксилатные соли (например, С1-8 алкил, циклоалкил, арил, гетероарил или неароматические гетероциклические), аминокислотно-аддитивные соли, сложные эфиры и амиды, которые обладают подходящим соотношением польза/риск, являются фармакологически эффективными и подходящими для контакта с тканями пациентов без чрезмерной токсичности, раздражения или ответной аллергической реакции. Примеры солей включают гидробромид, гидрохлорид, сульфат, бисульфат, нитрат, ацетат, оксалат, валерат, олеат, пальмитат, стеарат, лаурат, борат, бензоат, лактат, фосфат, тозилат, цитрат, малеат, фумарат, сукцинат, тартрат, нафтилат, мезилат, глюкогептонат, лактиобионат и лаурилсульфонат. Они могут включать катионы щелочного металла и щелочноземельного металла, такие как натрий, калий, кальций и магний, а также нетоксичные катионы аммония, четвертичного аммония и амина, такие как тетраметиламмоний, метиламин, триметиламин и этиламин. Смотри, например, публикацию S.M.Berge et al., "Pharmaceutical Salts (Фармацевтические соли)", J.Pharm.Sci., 1977, 66:1-19, включенную в данное описание в качестве ссылки. Примеры фармацевтически приемлемых амидов по изобретению включают амиды, которые получены из аммиака, первичных С1-6 алкиламинов и вторичных ди(С1-6 алкил)аминов. Вторичные амины включают 5- или 6-членные гетероциклические или гетероароматические кольцевые группы, содержащие по крайней мере один атом азота и необязательно от 1 до 2 дополнительных гетероатомов. Предпочтительные амиды получают из аммиака, С1-3 алкил первичных аминов или ди(С1-2 алкил)аминов. Примеры фармацевтически приемлемых сложных эфиров по изобретению включают С1-7 алкиловые, С5-7 циклоалкиловые, фениловые и фенил(С1-6