Соединения, которые ингибируют высвобождение воспалительных цитокинов
Иллюстрации
Показать всеНастоящее изобретение относится к соединению, в том числе ко всем их энантиомерным и диастереомерным формам и фармацевтически приемлемым солям, которые способны предотвращать внеклеточное высвобождение воспалительных цитокинов. Предлагаемые соединения имеют формулу (I), где R представляет собой: a) -OR3 или b) -NR4aR4b; R3 представляет собой замещенный или незамещенный фенил, где заместителями являются: i) галоген; ii) С1-С6 алкил; iii) трифторметил; iv) трихлорметил; v) трибромметил; vi) циано; и vii) C1-С6 алкокси; R4a и R4b представляют собой, каждый независимо: а) водород или b) -[C(R5aR5b)]xR6; индекс х равен от 0 до 5; каждый R5a и R5b представляет собой, независимо, водород, неразветвленный или разветвленный C1-C4алкил, С3-С7 циклический алкил; R6 представляет собой -OR7 или C1-C4алкил; R1 представляет собой водород или C1-C4алкил; R1 представляет собой галогензамещенный фенил; звенья R2a и R2b выбраны, каждый независимо, из группы, состоящей из: а) водорода; b) -O(CH2)jR8; с) -(CH2)jCO2R10; d) -(CH2)jCON(R10)2; e) двойной связи, когда один R2a и один R2b взяты вместе с образованием двойной связи; f) кольца, когда один R2a и один R2b взяты вместе с образованием кольца, причем указанное кольцо выбрано из группы, состоящей из: i) бензольного и ii) диоксоланового; R8 и R10 представляют собой, каждый независимо, водород или С1-С4алкил; j представляет индекс от 0 до 5; m представляет индекс от 1 до 3; n представляет индекс от 1 до 3; m+n равно 4. Объектами изобретения также являются фармацевтическая композиция на основе вышеописанных соединений, ингибирующая внеклеточное высвобождение воспалительных цитокинов, и способ регулирования внеклеточного высвобождения воспалительных цитокинов. 3 н. и 7 з.п. ф-лы, 9 табл.
Реферат
Область изобретения
Изобретение относится к соединениям, которые ингибируют внеклеточное высвобождение воспалительных цитокинов, причем указанные цитокины являются ответственными за одно или несколько патологических состояний человека или высших млекопитающих. Настоящее изобретение относится далее к композициям, включающим указанные соединения, и способу предупреждения, ослабления или регулирования иным путем действия ферментов, которые, как предполагается, являются активными компонентами, ответственными за описываемые в данном описании патологические состояния.
Предпосылки создания изобретения
Интерлейкин-1 (IL-1) и фактор-α некроза опухоли (TNF-α) среди важных биологических веществ известны совместно как «цитокины». Предполагается, что указанные молекулы опосредуют воспалительные реакции, ассоциированные с иммунологическим распознаванием инфекционных агентов.
Предполагается, что указанные провоспалительные цитокины являются важными медиаторами при многих патологических состояниях или синдромах, среди прочего, ревматоидном артрите, остеоартрите, воспалительном заболевании кишечника (IBS), септическом шоке, сердечно-легочной дисфункции, остром респираторном заболевании, кахексии и, следовательно, являются ответственными за развитие и проявление патологических состояний человека.
Поэтому имеется давно ощущаемая потребность в соединениях и фармацевтических композициях, которые включают соединения, которые могут блокировать, ослаблять, регулировать, подавлять или предупреждать высвобождение цитокинов из клеток, которые продуцируют их.
Краткое изложение сущности изобретения
Настоящее изобретение удовлетворяет вышеуказанным потребностям, поскольку неожиданно было обнаружено, что [5,6]- и [5,6,6]-конденсированные пиразолоны и их производные являются эффективными для ингибирования высвобождения воспалительных цитокинов, среди прочих, интерлейкина-1 (IL-1) и фактора некроза опухоли (TNF) из клеток и тем самым предупреждают, ослабляют или регулируют иным путем действия ферментов, которые, как предполагается, являются активными компонентами, ответственными за описанные здесь патологические состояния.
Первый аспект настоящего изобретения относится к соединениям, включающим все их энантиомерные и диастереомерные формы и фармацевтически приемлемые соли, причем соединения имеют формулу:
где R представляет собой:
а) водород;
b) -O(CH2)kR3 или
с) -NR4aR4b;
R3 представляет собой замещенный или незамещенный С1-С4алкил, замещенный или незамещенный циклический гидрокарбил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил; индекс k равен от 0 до 5;
R4a иR4b представляют собой, каждый независимо:
а) водород или
b) -[С(R5aR5b)]xR6;
каждый R5a иR5b представляет собой независимо водород, -OR7, -N(R7)2, -CO2R7, -CON(R7)2; неразветвленный, разветвленный или циклический С1-С4алкил и их смеси; R6 представляет собой водород, -OR7, -N(R7)2, -CO2R7, -CON(R7)2, замещенный или незамещенный С1-С4алкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; R7 представляет собой водород, водорастворимый катион, С1-С4алкил или замещенный или незамещенный арил; индекс х равен от 0 до 5;
R1 представляет собой:
а) замещенный или незамещенный арил или
b) замещенный или незамещенный гетероарил;
звенья R2a и R2b выбраны, каждый независимо, из группы, состоящей из:
а) водорода;
b) -O(CH2)jR8;
c) -(CH2)jN9aR9b;
d) -(CH2)jCO2R10;
e) -(CH2)jOCO2R10;
f) -(CH2)jCON(R10)2;
g) карбонила, когда два звена R2a или два звена R2b у одного и того же атома углерода могут быть взяты вместе с образованием карбонильного звена;
h) двойной связи, когда один R2a и один R2b взяты вместе с образованием двойной связи;
i) кольца, когда один R2a и один R2b взяты вместе с образованием замещенного или незамещенного кольца, включающего от 4 до 8 атомов, причем указанное кольцо выбрано из группы, состоящей из:
i) карбоциклического;
ii) гетероциклического;
iii) арильного;
iv) гетероарильного;
v) бициклического и
vi) гетеробициклического кольца
j) и их смесей;
R8, R9a, R9b и R10 представляют собой, каждый независимо, водород, С1-С4алкил и их смеси; R9a и R9b могут быть взяты вместе с образованием карбоциклического или гетероциклического кольца, включающего от 3 до 7 атомов; два звена R10 могут быть взяты вместе с образованием карбоциклического или гетероциклического кольца, включающего от 3 до 7 атомов; j представляет индекс от 0 до 5; m представляет индекс от 1 до 5; n представляет индекс от 1 до 5, m + n равно от 2 до 6.
Другой аспект настоящего изобретения относится к фармацевтическим композициям, которые могут доставлять соединения настоящего изобретения в организм человека или высшего млекопитающего, причем композиции включают:
а) эффективное количество одного или нескольких соединений настоящего изобретения и
b) один или несколько фармацевтически приемлемых эксципиентов.
Следующий аспект настоящего изобретения относится к способам борьбы с опосредованными одним или несколькими воспалительными цитокинами или модулированными воспалительными цитокинами заболеваниями или состояниями млекопитающих, причем указанный способ включает стадию введения человеку или высшему млекопитающему эффективного количества композиции, включающей одно или несколько соединений настоящего изобретения.
Эти и другие цели, отличительные признаки и преимущества станут очевидны специалисту в данной области после прочтения следующего подробного описания и прилагаемой формулы изобретения. Все проценты, соотношения и пропорции здесь являются массовыми, если не оговорено особо. Все температуры приводятся в градусах Цельсия (°C), если не оговорено особо. Все цитированные документы находятся в соответствующей части и включены здесь в качестве ссылки; цитирование любого документа не должно быть истолковано как допущение, что он является известным уровнем относительно настоящего изобретения.
Подробное описание изобретения
Настоящее изобретение относится к соединениям, которые способны опосредовать, регулировать или ингибировать иным путем внеклеточное высвобождение некоторых цитокинов, особенно воспалительных цитокинов, причем указанные цитокины играют роль в стимуляции, вызывании или проявлении большого числа заболеваний, патологических состояний или синдромов.
Для целей настоящего изобретения термин «гидрокарбил» определяют здесь как любое органическое звено или радикал, который состоит из атомов углерода и водорода. В термин гидрокарбил включены гетероциклы, которые описаны ниже. Примеры различных незамещенных негетероциклических гидрокарбильных звеньев включают пентил, 3-этилоктанил, 1,3-диметилфенил, циклогексил, цис-3-гексил, 7,7-диметилбицикло[2.2.1]гептан-1-ил и нафт-2-ил.
В определение «гидрокарбил» включены ароматические (арильные) и неароматические карбоциклические кольца, неограничивающие примеры которых включают циклопропил, циклобутанил, циклопентанил, циклогексан, циклогексенил, циклогептанил, бицикло[0.1.1]бутанил, бицикло[0.1.2]пентанил, бицикло[0.1.3]гексанил (туйанил), бицикло[0.2.2]гексанил, бицикло[0.1.4]гептанил (каранил), бицикло[2.2.1]гептанил (норборанил), бицикло[0.2.4]октанил (кариофилленил), спиропентанил, дициклопентанспиранил, декалинил, фенил, бензил, нафтил, инденил, 2Н-инденил, азуленил, фенантрил, антрил, флуоренил, аценафтиленил, 1,2,3,4-тетрагидронафталенил и тому подобное.
Термин «гетероцикл» включает как ароматические (гетероарильные), так и неароматические гетероциклические кольца, неограничивающие примеры которых включают: пирролил, 2Н-пирролил, 3Н-пирролил, пиразолил, 2Н-имидазолил, 1,2,3-триазолил, 1,2,4-триазолил, изоксазолил, оксазолил, 1,2,4-оксадиазолил, 2Н-пиранил, 4Н-пиранил, 2Н-пиран-2-онил, пиридинил, пиридазинил, пиримидинил, пиразинил, пиперазинил, симм-триазинил, 4Н-1,2-оксазинил, 2Н-1,3-оксазинил, 1,4-оксазинил, морфолинил, азепинил, оксепинил, 4Н-1,2-диазепинил, инденил, 2Н-инденил, бензофуранил, изобензофуранил, индолил, 3Н-индолил, 1Н-индолил, бензоксазолил, 2Н-1-бензопиранил, хинолинил, изохинолинил, хиназолинил, 2Н-1,4-бензоксазинил, пирролидинил, пирролинил, хиноксалинил, фуранил, тиофенил, бензимидазолил и тому подобное, причем каждый из них может быть замещенным или незамещенным.
Примером звена, определяемого термином «алкиленарил», является бензильное звено, имеющее формулу:
тогда как примером звена, определяемого термином «алкиленгетероарил», является 2-пиколильное звено, имеющее формулу:
Термин «замещенный» используют на всем протяжении описания. Термин «замещенный» определяют здесь как «охватывающий радикалы или звенья, которые могут заменить атом водорода, два атома водорода или три атома водорода гидрокарбильного радикала. Термин «замещенный» может также включать замену атомов водорода у двух соседних атомов углерода с образованием нового радикала или звена». Например, замещенное звено, которое требует замены одного атома водорода, включает галоген, гидроксил и тому подобное. Замена двух атомов водорода включает карбонил, оксимино и тому подобное. Замена двух атомов водорода у соседних атомов углерода включает эпокси и тому подобное. Замена трех атомов водорода включает циано и тому подобное. Эпоксидное звено является примером замещенного звена, которое требует замены атома водорода у соседних атомов углерода. Термин «замещенный», используемый на всем протяжении настоящего описания, указывает на то, что гидрокарбильный радикал, среди прочего, ароматическое кольцо, алкильная цепь, может иметь один или несколько атомов водорода, замененных заместителем. Когда радикал описан как «замещенный», может быть заменено любое число атомов водорода. Например, 4-гидроксифенил представляет собой «замещенное ароматическое карбоциклическое кольцо», (N,N-диметил-5-амино)октанил представляет собой «замещенное С8алкильное звено, 3-гуанидинопропил представляет собой «замещенное С3алкильное звено» и 2-карбоксипиридинил представляет собой «замещенное гетероарильное звено». Следующие звенья представляют собой неограничивающие примеры звеньев, которые могут служить в качестве замены атомов водорода, когда гидрокарбильное звено описано как «замещенное».
i) -[C(R12)2]p(CH=CH)qR12, где р равно от 0 до 12; q равно от 0 до 12;
ii) -C(Z)R12;
iii) -C(Z)2R12;
iv) -C(Z)CH=CH2;
v) -C(Z)N(R12)2;
vi) -C(Z)NR12N(R12)2;
vii) -CN;
viii) -CNO;
ix) -CF3, -CCl3, -CBr3;
x) -N(R12)2;
xi) -NR12CN;
xii) -NR12C(Z)R12;
xiii) -NR12C(Z)N(R12)2;
xiv) -NHN(R12)2;
xv) -NHOR12;
xvi) -NCS;
xvii) -NO2;
xviii) -OR12;
xix) -OCN;
xx) -OCF3, -OCCl3, -OCBr3;
xxi) -F, -Cl, -Br, -I и их смеси;
xxii) -SCN;
xxiii) -SO3M;
xxiv) -OSO3M;
xxv) -SO2N(R12)2;
xxvi) -SO2R12;
xxvii) -P(O)H2;
xxviii) -PO2;
xxix) -P(O)(OH)2;
xxx) и их смеси,
где R12 представляет собой водород, замещенный или незамещенный неразветвленный, разветвленный или циклический С1-С20алкил, С6-С20арил, С7-С20алкиленарил и их смеси; М представляет собой водород или солеобразующий катион; Z представляет собой =О, =S, =NR12 и их смеси. Подходящие солеобразующие катионы включают натрий, литий, калий, кальций, магний, аммоний и тому подобное.
Первый аспект настоящего изобретения, в общем, относится к новым соединениям, подходящим для ингибирования высвобождения воспалительных цитокинов, причем указанные соединения имеют формулу:
R представляет собой заместитель в положении 2 пиримидин-4-ильной части общей основной структуры, указанное звено R представляет собой:
а) простой эфир, имеющий формулу -О[CH2]kR3 или
b) первичное или вторичное аминозвено, имеющее формулу -NR4aR4b;
где R3 представляет собой замещенный или незамещенный С1-С4алкил, замещенный или незамещенный циклический гидрокарбил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил, замещенный или незамещенный гетероарил, индекс k равен от 0 до 5.
Ниже указываются различные варианты звеньев R настоящего изобретения, где R представляет собой простой эфир, имеющий формулу -О[CH2]kR3. Однако специалист в данной области не ограничивается иллюстративными вариантами и примерами данного описания.
А) Звенья R включают простые эфиры формулы -OR3 (индекс k равен 0), где R3 представляет собой замещенный или незамещенный арил.
i) Один вариант данного аспекта R включает простые эфиры, имеющие формулу -OR3, где R3 представляет собой замещенный или незамещенный арил. Данный вариант включает следующие неограничивающие примеры R: фенокси, 2-фторфенокси, 3-фторфенокси, 4-фторфенокси, 2,4-дифторфенокси, 3-трифторметилфенокси, 4-трифторметилфенокси, 2,4-дифторметилфенокси и тому подобное.
ii) Другой вариант данного аспекта R включает простые эфиры, имеющие формулу -OR3, где R3 представляет собой замещенный или незамещенный арил. Данный вариант включает следующие неограничивающие примеры: 2-метилфенокси, 3-метилфенокси, 4-метилфенокси, 2,4-диметилфенокси, 2-цианофенокси, 3-цианофенокси, 4-цианофенокси, 4-этилфенокси и тому подобное.
iii) Следующий вариант данного аспекта R включает простые эфиры, имеющие формулу -OR3, где R3 представляет собой замещенный или незамещенный арил. Данный вариант включает следующие неограничивающие примеры: (2-метокси)фенокси, (3-метокси)фенокси, (4-метокси)фенокси, 3-[(N-ацетил)амино]фенокси, 3-бензо[1,3]диоксол-5-ил и тому подобное.
В) Звенья R, включающие простые эфиры, имеющие формулу -OR3 (индекс k равен 0), где R3 представляет собой замещенный или незамещенный гетероарил.
i) Первый вариант данного аспекта R включает простые эфиры, имеющие формулу -OR3, где R3 представляет собой незамещенный гетероарил. Данный вариант включает следующие неограничивающие примеры: пиримидин-2-ил, пиримидин-4-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил и тому подобное.
ii) Второй вариант данного аспекта R включает простые эфиры, имеющие формулу -OR3, где R3 представляет собой замещенный гетероарил. Данный вариант включает следующие неограничивающие примеры: 2-аминопиримидин-4-ил и тому подобное.
С) Звенья R, включающие простые эфиры, имеющие формулу -OCH2R3 (индекс k равен 1), где R3 представляет собой замещенный или незамещенный арил.
i) Первый вариант данного аспекта R включает простые эфиры, имеющие формулу -OCH2R3, где R3 представляет собой замещенный или незамещенный гетероарил. Данный вариант включает следующие неограничивающие примеры: пиримидин-2-ил, пиримидин-4-ил, 2-аминопиримидин-4-ил, 4-аминопиримидин-6-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил и тому подобное.
ii) Второй вариант данного аспекта R включает простой эфир, имеющий формулу -OCH2R3, где R3 представляет собой замещенный или незамещенный алкиленгетероарил. Данный вариант включает следующие неограничивающие примеры: пиридин-3-илэтил, (2-метил-2-пиридин-3-ил)этил и тому подобное.
D) Звенья R, включающие простые эфиры, имеющие формулу -OR3 (индекс k равен 1), где R3 представляет собой замещенный или незамещенный С1-С4алкил.
i) Первый вариант данного аспекта R представляет собой простой эфир, имеющий формулу -OR3, где R3 представляет собой незамещенный неразветвленный, разветвленный или циклический С1-С4алкил. Данный вариант включает следующие неограничивающие примеры: метил, этил, изопропил, (S)-1-метилпропил и тому подобное.
ii) Второй вариант данного аспекта R представляет собой простой эфир, имеющий формулу -OR3, где R3 представляет собой замещенный неразветвленный, разветвленный или циклический С1-С4алкил. Данный вариант включает следующие неограничивающие примеры: 2-метоксиэтил, (S)-1-метил-3-метилоксипропил и тому подобное.
Ниже указываются различные аспекты звеньев R настоящего изобретения, где R представляет собой амин, имеющий формулу -NR4aR4b, R4a и R4b представляют собой, каждый независимо:
а) водород или
b) -[C(R5aR5b)]xR6;
каждый из R5a и R5b представляет собой, независимо, водород, -OR7, -N(R7)2, -CO2R7; -CON(R7)2; неразветвленный, разветвленный или циклический С1-С4алкил и их смеси; R6 представляет собой водород, -OR7, -N(R7)2, -CO2R7, -CON(R7)2; замещенный или незамещенный С1-С4алкил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил; R7 представляет собой водород, водорастворимый катион, С1-С4алкил или замещенный или незамещенный арил; индекс х равен от 0 до 5. Однако специалист в данной области не ограничивается иллюстративными вариантами и примерами данного описания.
А) Звенья R включают хиральные аминогруппы, где R4a представляет собой водород, R5a представляет собой водород и R5b представляет собой метил, причем указанные звенья имеют формулу:
и указанную стереохимию.
i) Первым вариантом данного аспекта R является амин, включающий R6, который представляет собой замещенный или незамещенный фенил. Данный вариант включает следующие неограничивающие примеры: (S)-1-метил-1-фенилметиламино, (S)-1-метил-1-(4-фторфенил)метиламино, (S)-1-метил-1-(4-метилфенил)метиламино, (S)-1-метил-1-(4-метоксифенил)метиламино, (S)-1-метил-1-(2-аминофенил)метиламино, (S)-1-метил-1-(4-аминофенил)метиламино и тому подобное.
ii) Вторым вариантом данного аспекта R является амин, включающий R6, который представляет собой замещенный или незамещенный гетероарил. Данный вариант включает следующие неограничивающие примеры: (S)-1-метил-1-(пиридин-2-ил)метиламино, (S)-1-метил-1-(пиридин-3-ил)метиламино, (S)-1-метил-1-(пиридин-4-ил)метиламино, (S)-1-метил-1-(фуран-2-ил)метиламино, (S)-1-метил-1-(3-бензо[1,3]диоксол-5-ил)метиламино и тому подобное.
iii) Третьим вариантом данного аспекта R является амин, включающий R6, который представляет собой замещенный или незамещенный С1-С4алкил. Данный вариант включает следующие неограничивающие примеры: (S)-1-метилпропиламино, (S)-1-метил-2-(метокси)этиламино.
В) Звенья R включают хиральные аминогруппы, где R4a представляет собой водород, R5a и R5b представляют собой, каждый, С1-С4алкил, причем указанные звенья имеют формулу:
и указанную стереохимию, когда R5a, R5b и R6 не являются одинаковыми.
i) Первым вариантом данного аспекта R является амин, который не имеет хирального центра и неограничивающие примеры которого включают 1,1-диметилэтиламин, 1,1-диметилбензиламин и тому подобное.
ii) Вторым вариантом данного аспекта R является амин, включающий R6, который представляет собой замещенный или незамещенный С1-С4алкил. Данный вариант включает следующие неограничивающие примеры: (S)-1-метил-2-гидрокси-2-метилпропиламин, (S)-1-метил-2-гидрокси-2-метилбутиламин и тому подобное.
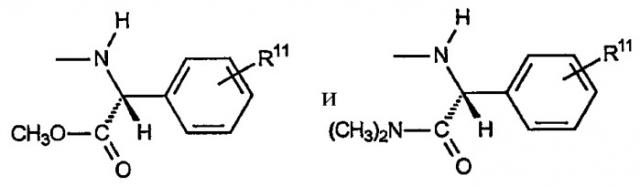
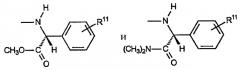
С) Звенья R, включающие алкиленариламины, где R4a представляет собой водород, оба R5a и R5b радикала R4b представляют собой водород, R6 представляет собой замещенный или незамещенный арил, причем указанное звено имеет формулу:
где R11 представляет собой водород или «замещенное звено», как указано выше.
i) Первый вариант данного аспекта включает следующие неограничивающие примеры звеньев R: бензиламино, (2-аминофенил)метиламино; (4-фторфенил)метиламино, (4-метоксифенил)метиламино; (4-пропансульфонилфенил)метиламино и тому подобное.
i) Второй вариант данного аспекта включает следующие неограничивающие примеры звеньев R: (2-метилфенил)метиламино; (3-метилфенил)метиламино, (4-метилфенил)метиламино и тому подобное.
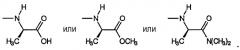
D) Звенья R, включающие амины, где R4a представляет собой водород, R4b включает R5b, равный водороду, и R5b, равный -СО2R7 или -CON(R7)2; причем указанное звено имеет формулу:
i) Первым вариантом данного аспекта R является амин, включающий R6, который представляет собой замещенный или незамещенный фенил. Данный вариант включает следующие неограничивающие примеры:
где R11 представляет собой водород или «заместитель», как указано выше.
ii) Вторым вариантом данного аспекта R является амин, включающий R6, который представляет собой замещенный или незамещенный алкил. Данный вариант включает следующие неограничивающие примеры:
Звенья R1 выбраны из:
а) замещенного или незамещенного арила или
b) замещенного или незамещенного гетероарила.
Первый аспект звеньев R1 охватывает галогензамещенные фенильные звенья, неограничивающие примеры которых включают 4-фторфенил, 2,4-дифторфенил, 4-хлорфенил и тому подобное. Звенья R2a и R2b выбраны, каждый независимо, из группы, состоящей из:
а) водорода;
b) -O(CH2)jR8;
c) -(CH2)jN9aR9b;
d) -(CH2)jCO2R10;
e) -(CH2)jOCO2R10;
f) -(CH2)jCON(R10)2;
g) карбонильного звена, когда два R2a или два R2b у одного и того же атома углерода могут быть взяты вместе с образованием карбонильного звена;
h) двойной связи, когда один R2a и один R2b взяты вместе с образованием двойной связи;
i) кольца, когда один R2a и один R2b взяты вместе с образованием замещенного или незамещенного кольца, включающего от 4 до 8 атомов, причем указанное кольцо выбрано из группы, состоящей из:
i) карбоциклического;
ii) гетероциклического;
iii) арильного;
iv) гетероарильного;
v) бициклического и
vi) гетеробициклического кольца;
l) и их смесей;
R8, R9a, R9b и R10 представляют собой, каждый независимо, водород, С1-С4алкил и их смеси; R9a и R9b могут быть взяты вместе с образованием карбоциклического или гетероциклического кольца, включающего от 3 до 7 атомов; два звена R10 могут быть взяты вместе с образованием карбоциклического или гетероциклического кольца, включающего от 3 до 7 атомов; j представляет индекс от 0 до 5.
Системы [5,6]-конденсированных колец
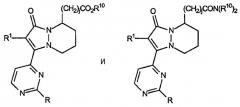
Первый аспект настоящего изобретения относится к циклическим основным структурам, в которых индексы m и n, каждый, равны 2, тем самым включая остовы 2-(R1-замещенный)-3-(2-R-замещенный-пиримидин-4-ил)-5,6,7,8-тетрагидропиразоло[1,2-a]пиридазин-1-она, имеющим формулу:
где звенья R2a и R2b представляют собой, каждый независимо, водород, -(CH2)jCO2R10, -(CH2)jCON(R10)2 и их смеси.
Варианты данной основной структуры включают циклический остов, имеющий формулу:
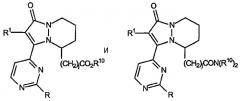
находящиеся в положении 8 сложные эфиры и амиды 5,6,7,8-тетрагидропиразоло[1,2-a]пиридазин-1-она, имеющие формулу:
а также находящиеся в положении 5 сложные эфиры и амиды 5,6,7,8-тетрагидропиразоло[1,2-a]пиридазин-1-она, имеющие формулу:
Второй аспект настоящего изобретения, когда он относится к звеньям R2a и R2b, включает остовы 2-(R1-замещенный)-3-(2-R-замещенный-пиримидин-4-ил)-5,6,7,8-тетрагидропиразоло[1,2-a]пиридазин-1-она, имеющие формулу:
где каждое из звеньев R2a и R2b независимо выбрано из группы, состоящей из:
а) водорода;
b) -O(CH2)jR8 и
с) -(CH2)jNR9aR9b.
Варианты данного аспекта включают 6-гидрокси-2-(R1-замещенный)-3-(2-R-замещенный-пиримидин-4-ил)-5,6,7,8-тетрагидропиразоло[1,2-a]пиридазин-1-оны, 7-гидрокси-2-(R1-замещенный)-3-(2-R-замещенный-пиримидин-4-ил)-5,6,7,8-тетрагидропиразоло[1,2-a]пиридазин-1-оны, 6-(диметиламино)-2-(R1-замещенный)-3-(2-R-замещенный-пиримидин-4-ил)-5,6,7,8-тетрагидропиразоло[1,2-a]пиридазин-1-оны, 6-морфолино-2-(R1-замещенный)-3-(2-R-замещенный-пиримидин-4-ил)-5,6,7,8-тетрагидропиразоло[1,2-a]пиридазин-1-оны.
Третий аспект настоящего изобретения, когда он относится к звеньям R2a и R2b, включает основные структуры, в которых два соседних звена R2a и R2b взяты вместе с образованием двойной связи, например остовы 2-(R1-замещенный)-3-(2-R-замещенный-пиримидин-4-ил)-5,8-дигидропиразоло[1,2-a]пиридазин-1-она, имеющие формулу:
Системы [5,6,X]-конденсированных колец
Настоящее изобретение относится также к [5,6,X]-конденсированным кольцевым системам, где Х представляет собой кольцо, образованное, когда один R2a и один R2b взяты вместе с образованием замещенного или незамещенного кольца, включающего от 4 до 8 атомов. Образованные кольца выбраны из группы, состоящей из:
i) карбоциклического;
ii) гетероциклического;
iii) арильного;
iv) гетероарильного;
v) бициклического и
vi) гетеробициклического кольца.
Первый вариант осуществления данного аспекта относится к кольцевым системам, в которых один R2a и один R2b взяты вместе с образованием 6-членного арильного кольца, среди прочего, системе [5,6,6]-конденсированных колец; 2-(R1-замещенный)-3-(2-R-замещенный-пиримидин-4-ил)-5,10-дигидропиразоло[1,2-b]фталазин-1-ону, имеющему формулу:
Варианты данного аспекта включают аналоги, которые замещены в С-кольце, например соединения, имеющие формулу:
где R12 представляет собой заместитель, как указано выше. Неограничивающими примерами [5,6,6]-циклических основных структур настоящего изобретения являются циклические остовы 2-(R1-замещенный)-3-(2-R-замещенный-пиримидин-4-ил)-5,10-дигидропиразоло[1,2-b]фталазин-1-она, например, соединение, имеющее формулу:
Первый аспект аналогов категории 1, способных ингибировать высвобождение воспалительных цитокинов настоящего изобретения, относится к соединениям, включающим остов 5,10-дигидропиразоло[1,2-b]фталазин-1-она, имеющим формулу:
где звенья R представляют собой амины, имеющие формулу -NH[CHR5]R6, и R1, R4a, R5 и R6 имеют значения, указанные ниже в таблице I. Стереохимия R5b является конфигурацией, показанной, когда R5b не является водородом.
| ТАБЛИЦА I | ||||
| № | R1 | R4a | R5b | R6 |
| 1 | 4-фторфенил | Н | Н | фенил |
| 2 | 4-фторфенил | Н | Н | 4-фторфенил |
| 3 | 4-фторфенил | Н | Н | 2-аминофенил |
| 4 | 4-фторфенил | Н | Н | 2-метилфенил |
| 5 | 4-фторфенил | Н | Н | 4-метилфенил |
| 6 | 4-фторфенил | Н | Н | 4-метоксифенил |
| 7 | 4-фторфенил | Н | Н | 4-(пропансульфонил)фенил |
| 8 | 4-фторфенил | Н | Н | 3-бензо[1,3]диоксол-5-ил |
| 9 | 4-фторфенил | Н | Н | пиридин-2-ил |
| 10 | 4-фторфенил | Н | Н | пиридин-3-ил |
| 11 | 4-фторфенил | Н | Н | Н |
| 12 | 4-фторфенил | Н | Н | метил |
| 13 | 4-фторфенил | Н | Н | этил |
| 14 | 4-фторфенил | Н | Н | винил |
| 15 | 4-фторфенил | Н | Н | циклопропил |
| 16 | 4-фторфенил | Н | Н | циклогексил |
| 17 | 4-фторфенил | Н | Н | метоксиметил |
| 18 | 4-фторфенил | Н | Н | метоксиэтил |
| 19 | 4-фторфенил | Н | Н | 1-гидрокси-1-метилэтил |
| 20 | 4-фторфенил | Н | Н | -СО2Н |
| 21 | 4-фторфенил | Н | метил | фенил |
| 22 | 4-фторфенил | Н | метил | 4-фторфенил |
| 23 | 4-фторфенил | Н | метил | 2-аминофенил |
| 24 | 4-фторфенил | Н | метил | 2-метилфенил |
| 25 | 4-фторфенил | Н | метил | 4-метилфенил |
| 26 | 4-фторфенил | Н | метил | 4-метоксифенил |
| 27 | 4-фторфенил | Н | метил | 4-(пропансульфонил)фенил |
| 28 | 4-фторфенил | Н | метил | 3-бензо[1,3]диоксол-5-ил |
| 29 | 4-фторфенил | Н | метил | пиридин-2-ил |
| 30 | 4-фторфенил | Н | метил | пиридин-3-ил |
| 31 | 4-фторфенил | Н | метил | Н |
| 32 | 4-фторфенил | Н | метил | метил |
| 33 | 4-фторфенил | Н | метил | этил |
| 34 | 4-фторфенил | Н | метил | винил |
| 35 | 4-фторфенил | Н | метил | циклопропил |
| 36 | 4-фторфенил | Н | метил | циклогексил |
| 37 | 4-фторфенил | Н | метил | метоксиметил |
| 38 | 4-фторфенил | Н | метил | метоксиэтил |
| 39 | 4-фторфенил | Н | метил | 1-гидрокси-1-метилэтил |
| 40 | 4-фторфенил | Н | метил | -СО2Н |
| 41 | 3-трифторметилфенил | Н | метил | фенил |
| 42 | 3-трифторметилфенил | Н | метил | 4-фторфенил |
| 43 | 3-трифторметилфенил | Н | метил | 2-аминофенил |
| 44 | 3-трифторметилфенил | Н | метил | 2-метилфенил |
| 45 | 3-трифторметилфенил | Н | метил | 4-метилфенил |
| 46 | 3-трифторметилфенил | Н | метил | 4-метоксифенил |
| 47 | 3-трифторметилфенил | Н | метил | 4-(пропансульфонил)фенил |
| 48 | 3-трифторметилфенил | Н | метил | 3-бензо[1,3]диоксол-5-ил |
| 49 | 3-трифторметилфенил | Н | метил | пиридин-2-ил |
| 50 | 3-трифторметилфенил | Н | метил | пиридин-3-ил |
| 51 | 3-трифторметилфенил | Н | метил | Н |
| 52 | 3-трифторметилфенил | Н | метил | метил |
| 53 | 3-трифторметилфенил | Н | метил | этил |
| 54 | 3-трифторметилфенил | Н | метил | винил |
| 55 | 3-трифторметилфенил | Н | метил | циклопропил |
| 56 | 3-трифторметилфенил | Н | метил | циклогексил |
| 57 | 3-трифторметилфенил | Н | метил | метоксиметил |
| 58 | 3-трифторметилфенил | Н | метил | метоксиэтил |
| 59 | 3-трифторметилфенил | Н | метил | 1-гидрокси-1-метилэтил |
| 60 | 3-трифторметилфенил | Н | метил | -СО2Н |
Ниже представлена схема получения соединений, относящихся к первому аспекту категории I настоящего изобретения. Первая стадия включает использование промежуточных соединений типа I, например промежуточного соединения 3 для введения выбранного звена R1, в соединяющуюся основную структуру.
Общая схема для получения промежуточного соединения типа I
Реагенты и условия: (а) LDA, ТГФ, -78°C, 45 мин.
Реагенты и условия: (b) CrO3, CH2Cl2, комнатная температура, 16 час.
ПРИМЕР 1
Метиловый эфир 2-(4-фторфенил)-3-(2-метилсульфанилпиримидин-4-ил)-3-оксопропионовой кислоты (3)
Ниже представлена методика получения 2-метилсульфанилпиримидин-4-карбальдегида, 1, адаптированная из методики H.Bredereck et al., Chem. Ber., 97, pp 3407-3417 (1964), включенной в данное описание в качестве ссылки.
В 3-горлую колбу объемом 12 л в инертной атмосфере загружают диметилацетил-N,N-диметилформамид (801 г) и диметилацеталь пировиноградного альдегида (779 г). Смесь нагревают при кипячении с обратным холодильником в течение 18 часов, в течение этого времени температура понижается приблизительно от 109°C до приблизительно 80°C. Раствор охлаждают и добавляют метанол (4 л) для растворения неочищенного остатка. Раствор затем охлаждают до 20°C и добавляют тиомочевину (892 г, 11,7 моль). После перемешивания смеси в течение приблизительно 15 минут добавляют метоксид натрия (741 г, 13,7 моль) 4 равными порциями на протяжении 1 часа, поддерживая температуру раствора в диапазоне 18-28°C. Смесь перемешивают в течение 5 часов при комнатной температуре, охлаждают до 20°C, затем на протяжении 1,25 часа добавляют метилиодид (2 кг), поддерживая температуру реакции в диапазоне 17-29°C. Перемешивание продолжают в течение 18 часов при комнатной температуре. Метанол и непрореагировавший метилиодид удаляют нагреванием раствора при 35°C и 40 мм рт. ст., получая приблизительно 4,46 кг темного остатка, который распределяют между 14 л воды и 5 л этилацетата. Водную фракцию экстрагируют второй раз этилацетатом, органические слои объединяют и концентрируют в вакууме с получением 685 г масла, которое очищают на диоксиде кремния, получая 522 г 4-диметоксиметил-2-метилсульфанилпиримидина.
Полученный выше диметилацеталь затем гидролизуют в свободный альдегид нагреванием до 60°C в течение 3 часов в 1М HCl. Нейтрализация и экстракция продукта с использованием этилацетата дает 347 г неочищенного продукта, который очищают на диоксиде кремния, получая 401 г 2-метилсульфанилпиримидин-4-карбальдегида, 1.
Получение метилового эфира 2-(4-фторфенил)-3-(2-метилсульфанилпиримидин-4-ил)-3-гидроксипропионовой кислоты (2): К холодному (-78°C) раствору диизопропиламида лития (21,4 мл 2М раствора в ТГФ, 42,8 ммоль) в ТГФ (70 мл) по каплям добавляют раствор метил 4-фторфенилацетата (6,0 г, 35,7 ммоль) в ТГФ (30 мл). Раствор перемешивают в течение 1 часа при -78°C, после чего к реакционной смеси по каплям добавляют раствор 2-метилсульфанилпиримидин-4-карбальдегида, 1 (6,0 г, 39,3 ммоль) в ТГФ (30 мл). Перемешивание продолжают в течение 45 минут при -78°C, затем реакционную смесь гасят, выливая реакционный раствор в водный насыщенный NH4Cl. Водную фазу экстрагируют этилацетатом. Органические фазы объединяют, сушат (MgSO4), фильтруют и концентрируют в вакууме. Неочищенный остаток очищают на диоксиде кремния (33% EtOAc/гексаны), получая 8,7 г (76%) требуемого продукта в виде смеси (1:1) диастереомеров.
Получение метилового эфира 2-(4-фторфенил)-3-(2-метилсульфанилпиримидин-4-ил)-3-оксопропионовой кислоты (3): К суспензии CrO3 в CH2Cl2 (300 мл) добавляют пиридин. Смесь энергично перемешивают в течение 1 часа при комнатной температуре. К хромсодержащей суспензии по каплям добавляют раствор неочищенного метилового эфира 2-(4-фторфенил)-3-(2-метилсульфанилпиримидин-4-ил)-3-гидроксипропионовой кислоты, 2, полученного выше, в CH2Cl2 (50 мл). Реакционную смесь перемешивают при комнатной температуре в течение 16 часов, разбавляют эфиром (1 л) и фильтруют через слой целита. Фильтрат концентрируют в вакууме и образовавшийся остаток очищают на диоксиде кремния (25% EtOAc/гексаны), получая 3,7 г (выход 43%) требуемого продукта в виде желтого твердого вещества.
Следующий пример относится к образованию 6,7-дигидро-5Н-пиразоло[1,2-a]пиразол-1-оновых кольцевых систем с использованием пиразолидина, однако специалист в данной области может заменить его другими циклическими гидразиновыми реагентами для получения других циклических систем настоящего изобретения, среди прочего, указывается использование гексагидропиридазина для получения 5,6,7,8-тетрагидропиразоло[1,2-a]пиридазин-1-онов. В примере, приведенном ниже, промежуточное соединение 3, полученное способом, описанным выше, используют для введения в качестве R1 4-фторфенильного звена, однако замещение для такого звена може