Способ получения синтетических процианидиновых олигомеров
Иллюстрации
Показать всеИзобретение относится к способу получения синтетических процианидиновых олигомеров, в частности к способу получения процианидинового димера, который включает стадии: (а) защиты каждой фенольной гидроксильной группы процианидинового мономера общей формулы 1: с помощью удаляемой защитной группы, которая не дезактивирует кольцо А мономера, причем стадия защиты проводится в апротонном растворителе; (b) необязательно блокирования С-8 положения мономера со стадии (а) галоидной группой; (c) активирования для сочетания С-4-положения соединения со стадии (а) или стадии (b) введением ацилоксильной группы с использованием соли свинца (IV) органической кислоты с получением активированного соединения; и (d) сочетания активированного соединения со стадии (с) с незащищенным процианидиновым мономером в присутствии катализатора сочетания с получением димера. В определенных условиях на стадии (b) получат кристаллический 8-бром-тетра-О-бензил(-)-эпикатехин в качестве промежуточного продукта. Технический результат - разработан универсальный способ получения олигомеров сложной конфигурации. 2 н. и 13 з.п. ф-лы., 1 табл., 8 ил.
Реферат
Область изобретения
Изобретение относится к синтетическим процианидиновым олигомерам и способам получения и применения олигомеров.
Предпосылки изобретения
Полифенолы являются очень разнообразной группой соединений (Ferreira D., Steynberg J.P., Roux D.G. и Brandt E.V., Tetrahedron, 48 (10), 1743-1803 (1992)), которые широко распространены в различных растениях, некоторые из которых входят в пищевые продукты. В некоторых случаях они представляют важную группу соединений для питания человека. Несмотря на то, что считается, что некоторые полифенолы не имеют пищевого значения, интерес к данным соединениям возрос в результате их возможных полезных эффектов на здоровье.
Например, было показано, что кверцетин обладает противоопухолевой активностью в опытах на экспериментальных животных (Decschner E.E., Ruperto J., Wong G. и Newmark H.L., Carcinogenesis, 7, 1193-1196 (1991) и Kato R., Nakadate Т., Yamamoto S. и Sugimura Т., Carcinogenesis, 4, 1301-1305 (1983)). Было показано, что (+)-катехин и (-)-эпикатехин ингибируют активность обратной транскриптазы вируса лейкемии (Chu S.-C., Hsieh Y.-S. и Lim J.-Y., J. of Natural Products, 55 (2), 179-183 (1992)). Также было показано, что нобатанин (олигомерный гидролизуемый таннин) обладает противоопухолевой активностью (Okuda Т., Yoshida Т. и Hatano Т., Molecular Structures and Pharmacological Activities of Polyphenols - Oligomeric Hydrolyzable Tannins and Others - Presented at the XVIth International Conference of the Group Polyphenols, Лиссабон, Португалия, 13-16 июля 1992). Статистические отчеты также показывали, что смертность в результате рака желудка значительно ниже в районах Японии, где производится чай. Сообщалось, что эпигаллокатехингаллат является фармакологически активным соединением в зеленом чае, которое ингибирует развитие рака кожи у мышей (Okuda et al., Ibid.). Было показано, что эллаговая кислота обладает противоопухолевой активностью на различных опухолевых моделях у животных (Boukharta M., Jalbert G. и Castonguay A., Efficacy of Ellagitannins and Ellagic Acid as Cancer Chemopreventic Agents - Presented at the XVIth International Conference of the Group Polyphenols, Лиссабон, Португалия, 13-16 июля 1992). Проантоцианидиновые олигомеры запатентованы Kikkoman Corporation для применения в качестве антимутагенов. Применение фенольных соединений в продуктах питания и модуляция под их воздействием развития опухолей на моделях экспериментальных животных недавно было представлено на 202-м Национальном собрании Американского химического общества (Phenolic Compounds in Foods and Their Effects on Health I, Analysis, Occurrence & Chemistry, Ho, C.-T., Lee C.Y. и Huang M.-T. editors, ACS Symposium Series 506, American Chemical Society, Вашингтон, D.C. (1992); Phenolic Compounds in Foods and Their Effects on Health II. Antioxidants & Cancer prevention, Huang M.-T., Ho С.-Т. и Lee C.Y. editors, ACS Symposium Series 506, American Chemical Society, Вашингтон, D.C. (1992)).
Однако данные ссылки не относятся к экстрактам какао или соединениям, входящим в их состав, или к каким-нибудь способам получения таких экстрактов или соединений из них, или к каким-нибудь из применений, описанных в патенте США 5554645 от 10 сентября 1996 года, Romanczyk et al., патенте США 5712305 от 27 января 1998 года, Romanczyk et al. и патенте США 5650432 от 22 июля 1997 года, Walker et al.
Были разработаны способы выделения, разделения, очистки и идентификации для извлечения ряда процианидиновых олигомеров в целях сравнительной оценки биологической активности в условиях in vitro и in vivo. Например, показана противоопухолевая активность для пентамерных-декамерных процианидинов, но не для мономерных-тетрамерных соединений. В настоящее время быстрыми способами получают граммовые количества чистого пентамера (>95%). Данные способы не подходят для получения значительных количеств пентамера для широкомасштабных фармакологических исследований и исследований биодоступности. Еще большие усилия необходимы для получения многограммовых количеств высших олигомеров (гексамеров-декамеров) для подобных исследований, поскольку их концентрация в натуральном продукте значительно ниже, чем для пентамера. Кроме того, увеличение размера олигомера увеличивает структурную сложность. Такие факторы, как хиральность мономерных единиц, составляющих олигомер, в различных местах межфлавановых связей, динамическая поворотная изомеризация межфлавановых связей, конформационные состояния пиранового кольца и многочисленные точки связывания в нуклеофильных центрах создают затруднения в отношении эффективности современных аналитических способов разделения и очистки для последующей идентификации.
Например, предыдущие попытки сочетать мономерные единицы в свободной фенольной форме с использованием минеральной кислоты в качестве катализатора в водной среде имели ограниченный успех. Выходы были низкими, реакции протекали с низкой селективностью, и олигомеры было трудно выделить (Stynberg P.J., Nel R.J. и Ferreira D., Tetrahedron, 54, 8153-8158 (1998); Botha J.J., Young D.A., Ferreira F. и Roux D.J.J., J.Chem.Soc., Perkins Trans. I, 1213-1219 (1981)).
Бензилированные мономеры получили способами, описанными Kawamoto H., Nakatsubo F. и Murkami К., Mokuzai Gakkashi, 37, 741-747 (1991), где использовали бензилбромид в сочетании с карбонатом калия (К2СО3) и диметилформамид (ДМФА). Однако выход составил только примерно 40%. Кроме того, конкурентное С-бензилирование приводит к образованию смеси продуктов, что затрудняет выделение целевого мономера. Кроме того, наблюдали частичную рацемизацию (+)-катехина в С-2- и С-3-положениях (Pierre M.-C. et al., Tetrahedron Letters, 38: 32, 5639-5642 (1997)).
В литературе описаны два основных способа окислительной функционализации (Betts M.J., Brown B.R. и Shaw M.R., J.Chem.Soc., C. 1178 (1969); Steenkamp J.A., Ferreira D. и Roux D.J., Tetrahedron Lett., 26, 3045-3048 (1985)). В более старом способе защищенный (+)-катехин обрабатывали тетраацетатом свинца (LTA) в бензоле с получением 4β-ацетокси-производного, которое затем успешно гидролизовали до 3,4-диола. Флаван-3,4-диолы представляют начальные электрофилы в биомимметическом синтезе процианидинов. Однако флаван-3,4-диолы, которые имеют кислородную функциональную группу в С-5-положении, недоступны из естественных источников, и их следует синтезировать. Таким образом окислительная функционализация прохирального бензильного положения с образованием 3,4-диолов предлагает значительную потенциальную возможность для синтеза процианидинов. Наибольшим недостатком данной реакции был низкий выход (30-36%) ацетата во время окисления с помощью LTA. Более поздний способ окислительной функционализации С-4-положения основан на использовании 2,3-дихлор-5,6-дициано-1,4-бензохинона (DDQ). В данном способе защищенный мономер обрабатывали DDQ в метаноле. Это позволяет ввести метоксильную группу в С-4-положение стереоспецифичным образом. Выход составляет примерно 40-50%.
Имеется ряд сообщений по реакции сочетания мономеров и их 3,4-диолов в водной кислоте. Данные способы являются неудовлетворительными за счет низких выходов, отсутствия специфичности и трудностей при выделении из водной среды. Kawamoto H., Nakatsubo F. и Murakami К., J. of Wood Chem. Tech., 9, 35-52 (1989) сообщили, что тетрахлорид титана (TiCl4) опосредует сочетание между 4-гидроксил тетра-O-бензил(+)-катехином и 5 эквивалентами (экв) тетра-O-бензил(+)-катехина с получением смеси 4α→8 и 4β→8 димеров 3:2.
Следовательно, имеется потребность в способах синтеза, которые обеспечивают большие количества структурно определенных олигомеров для оценки in vitro и in vivo. Подобные способы синтеза могут привести к получению олигомеров сложной конфигурации, некоторые из которых идентичны таковым, найденным в природе, а также редких или «неестественных» типов. Следовательно, будет полезным разработать универсальный способ синтеза, способный обеспечить большие количества любого желаемого процианидинового олигомера.
Краткое описание изобретения
Описан способ получения частично защищенного процианидинового димера. Он включает стадии:
(a) защиты каждой фенольной гидроксильной группы процианидинового мономера с помощью удаляемой защитной группы, которая не дезактивирует кольцо А мономера, где стадия защиты проводится в апротонном растворителе;
(b) активирования для сочетания С-4-положения соединения со стадии (а) путем введения ацилоксильной группы с использованием соли свинца (IV) органической кислоты с получением активированного соединения; и
(c) сочетания активированного соединения со стадии (b) с незащищенным процианидиновым мономером в присутствии катализатора сочетания с получением димера.
Также описан способ получения линейного процианидинового олигомера. Он включает стадии:
(a) получения частично защищенного процианидинового димера, в котором фенольные гидроксильные группы верхнего мера защищены удаляемой защитной группой, которая не дезактивирует кольцо А защищенного мера;
(b) маскирования незащищенных фенольных гидроксильных групп нижнего мера со стадии (а) и гидроксильных групп в С-3-положениях мера с помощью удаляемой маскирующей группы, которая дезактивирует нижний мер маскированного, защищенного димера;
(с) снятия защиты с верхнего мера димера со стадии (b) с получением маскированного димера со снятой защитой;
(d) сочетания димера со стадии (с) с неблокированным или блокированным, защищенным, активированным мономером с образованием тримера, в котором верхний мер тримера является защищенным, блокированным мером или защищенным, неблокированным мером, и где сочетание имеет место в С-8-положении;
(e) маскирования неблокированного или блокированного тримера со стадии (d);
(f) снятия защиты с неблокированного или блокированного, защищенного, маскированного тримера со стадии (е) с образованием неблокированного или блокированного маскированного тримера;
и
(g) необязательно повторяют или чередуют стадии (a)-(f) с получением высших олигомеров, в которых число мер составляет от 4 до 18.
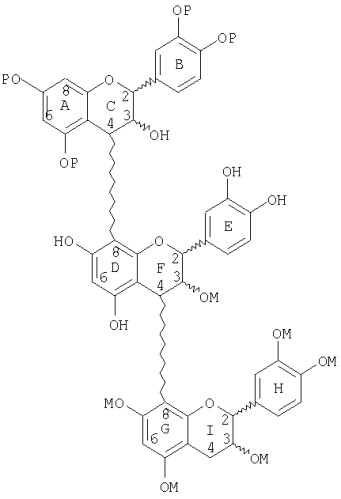
В следующих иллюстративных соединениях Р представляет защитную группу, В представляет блокирующую группу, и М представляет маскирующую группу. Следующее соединение является иллюстрацией частично защищенного процианидинового димера, такого, как получено на стадии (а) выше:
Следующее соединение является иллюстрацией защищенного, маскированного димера такого, как получено на стадии (b) выше:
Следующее соединение является иллюстрацией маскированного димера со снятой защитой такого, как получено на стадии (с) выше:
Следующие соединения являются иллюстрацией защищенного, маскированного, блокированного линейного триммера:
или
Следующие соединения являются иллюстрацией неблокированного и блокированного, защищенного, маскированного линейного тримера со стадии (d):
или
Следующие соединения являются иллюстрацией неблокированного и/или блокированного, маскированного линейного тримера со снятой защитой со стадии (е):
или
Следующие соединения являются иллюстрацией соединений, которые получают в результате необязательного повторения или чередования стадий (a)-(f) с получением высших олигомеров, в которых число меров равно 4:
или
или
Также описан способ получения разветвленных процианидиновых олигомеров. Он включает стадии:
(a) получения неблокированного или блокированного, частично защищенного процианидинового димера, в котором фенольные гидроксильные группы верхнего мера защищены удаляемой защитной группой, которая не дезактивирует кольцо А защищенного мера, в то время как нижний мер имеет свободные фенольные гидроксильные группы;
(b) сочетания димера со стадии (а) с неблокированным или блокированным, защищенным, активированным процианидиновым мономером с образованием разветвленного тримера;
(c) снятия защиты с тримера со стадии (b); и
(d) необязательно проведения одной из следующих стадий в последовательном, чередующемся или комбинационном порядке с получением процианидиновых олигомеров, имеющих 4-18 меров,
включающих связи (4→8), (4→6), (6→4) и/или (8→4);
(i) сочетания олигомера со стадии (с) с неблокированным или блокированным, защищенным процианидиновым мономером;
(ii) маскирования олигомера со стадии (с), снятия защиты с маскированного олигомера и сочетания маскированного олигомера с незащищенным или защищенным, блокированным, активированным процианидиновым мономером.
Свободные фенольные формы процианидинового димера, линейного процианидинового олигомера или разветвленного процианидинового олигомера получают снятием защиты с димера или олигомера и, если необходимо, демаскированием и/или деблокированием димера или олигомера. Димеры или олигомеры могут включать одинаковые или различные эпикатехиновые или катехиновые меры. Предпочтительно n равно 5-12, более предпочтительно n равно 5. В линейных олигомерах связи представляют (4→6), (4→8) и/или (4→6). В разветвленных олигомерах связи представляют (4→6), (4→8), (6→4) и/или (8→4).
Защитные группы могут быть бензилом, п-метоксибензилом, трет-бутилом или тритилом; бензил является предпочтительным. На стадии защиты используется апротонный растворитель, например диметилформамид, диметилацетамид или диметилсульфоксид; диметилацетамид является предпочтительным. Ацилоксильные активирующие группы обычно представляют ацетокси, формилокси или пропионилокси; ацетокси является предпочтительным. Активирование проводят с использованием соли свинца (IV), например тетраацетата свинца, тетраформиата свинца или тетрапропионата свинца. Предпочтительно стадию архивирования проводят также с использованием органической кислоты, которая является такой же, как при получении соли свинца. Пригодные органические кислоты включают муравьиную кислоту, уксусную кислоту и пропионовую кислоту. Предпочтительным растворителем для стадии активирования является бензол. Блокирующая группа представляет галоген, предпочтительно бром или йод. Стадию деблокирования проводят с алкиллитием, например трет-бутиллитием или н-бутиллитием. Стадию демаскирования проводят основным гидролизом. Стадию снятия защиты проводят гидрогенолизом.
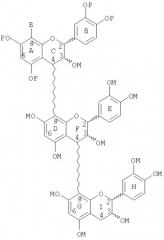
Дважды разветвленный олигомер, имеющий структуру:
можно получить способом, который включает стадии:
(a) защиты каждой фенольной гидроксильной группы первого процианидинового мономера с помощью первой удаляемой защитной группы, которая не дезактивирует кольцо А мономера, где стадию защиты проводят в апротонном растворителе с получением защищенного мономера;
(b) активирования для сочетания С-4-положения соединения со стадии (а) введением ацилоксильной группы с использованием соли свинца органической кислоты с получением активированного, защищенного мономера;
(c) сочетания соединения со стадии (b) с незащищенным процианидиновым мономером в присутствии катализатора сочетания с получением частично защищенного димера;
(d) маскирования димера со стадии (с) с получением маскированного, частично защищенного димера;
(e) снятия защиты с маскированного, частично защищенного димера со стадии (d) с получением маскированного димера;
(f) сочетания маскированного димера со стадии (е) с 4β-ацетокси-защищенным процианидиновым мономером с получением тримера;
(g) сочетания тримера со стадии (f) с 4β-ацетокси-процианидиновым мономером с получением процианидинового тетрамера;
(h) демаскирования тетрамера со стадии (g); и
(i) сочетания тетрамера со стадии (h) с 4β-ацетокси-процианидиновым мономером с получением процианидинового пентамера.
Стадии до (i) можно повторить с получением множественно разветвленного процианидинового олигомера, включающего n меров, где n равно целому числу от 6 до 18.
Описан способ получения процианидинового димера, имеющего связь (8↔8). Он включает стадии:
(a) взаимодействия первого 8-бром-защищенного мономера с гексаалкилдистаннаном в присутствии палладия(0) с получением защищенного мономер-8-триалкилстаннана;
(b) сочетания соединения со стадии (а) со вторым 8-бром-защищенным мономером в присутствии тетракис(трифенилфосфин)-палладия(0) в бензоле с получением (8↔8) связанного димера; и
(с) снятия защиты с соединения со стадии (b) с получением (8↔8) димера.
Также описан способ получения процианидинового димера, имеющего связь (6↔6). Способ включает стадии:
(a) взаимодействия первого 6-бром-защищенного мономера с гексаалкилдистаннаном в присутствии палладия(0) с получением мономер-6-триалкилстаннана;
(b) сочетания соединения со стадии (а) со вторым 6-бром-защищенным мономером в присутствии тетракис(трифенилфосфин)-палладия(0) в бензоле с получением (6↔6) связанного димера; и
(c) снятия защиты с соединения со стадии (b) с получением (6↔6) димера.
Также описан способ получения процианидинового димера, имеющего связь (6↔8). Способ включает стадии:
(a) взаимодействия первого 6-бром-защищенного мономера с гексаалкилдистаннаном в присутствии палладия(0) с получением защищенного мономер-6-триалкилстаннана;
(b) сочетания соединения со стадии (а) со вторым 8-бром-защищенным мономером в присутствии тетракис(трифенилфосфин)-палладия(0) в бензоле с получением (6↔8) связанного димера; и
(c) снятия защиты с соединения со стадии (b) с получением (6↔8) димера.
Также описан способ получения процианидинового димера, имеющего связь (8↔6). Способ включает стадии:
(a) взаимодействия первого 8-бром-защищенного мономера с гексаалкилдистаннаном в присутствии палладия(0) с получением защищенного мономер-8-триалкилстаннана;
(b) сочетания соединения со стадии (а) со вторым 6-бром-защищенным мономером в присутствии тетракис(трифенилфосфин)-палладия(0) в бензоле с получением (8↔6) связанного димера; и
(c) снятия защиты с соединения со стадии (b) с получением (8↔6) димера.
Настоящий способ имеет важные преимущества и эффективность по сравнению с более ранними способами получения процианидиновых олигомеров, они включают лучший выход, лучшую селективность и более легкое выделение продукта. При проведении стадии защиты в диметилацетамиде вместо диметилформамида легче контролировать частичную и полную защиту фенольных гидроксильных групп.
Настоящее изобретение также относится к кристаллическому 8-бром-тетра-О-бензил(-)-эпикатехину, когда используется диметилацетамид в качестве растворителя на стадии защиты.
Подробное описание изобретения
Мономеры, входящие в состав процианидинов, имеют структуру
Процианидины включают таковые, обнаруженные в какао-бобах, полученных из Theobroma cacao и различных родственных видов какао, а также рода Herrania и их внутри- и межродовых гибридов.
Мономеры, входящие в состав процианидинов, включают (+)катехин, (-)-эпикатехин и их соответствующие эпимеры (например, (-)-катехин и (+)-эпикатехин).
Синтетические линейные и/или разветвленные олигомеры, имеющие следующие структуры, показаны в качестве таковых, которые можно получить вышеуказанным способом.
Линейные олигомеры, где n равно целому числу от 0 до 16
разветвленные олигомеры, где А и В независимо представляют олигомеры от 1 до 15, в целом 3-18 в конечном олигомере.
В олигомерах n равно целому числу от 2 до 18, предпочтительно от 3 до 12, более предпочтительно от 5 до 12 и наиболее предпочтительно равно 5. Олигомеры имеют межфлавановые связи (4→6) и/или (4→8). Олигомеры, полученные способом по изобретению, могут быть представлены вышеуказанными структурами. В отношении линейного олигомера, то, когда n равно 0, олигомер называют «димером»; когда n равно 1, олигомер называют «тримером»; когда n равно 2, олигомер называют «тетрамером»; когда п равно 3, олигомер называют «пентамером»; и аналогичными перечислениями можно обозначить олигомеры, имеющие n до и включая 16 и выше, так, например, когда n равно 16, олигомер называют «октадекамером». В отношении разветвленного олигомера, то, когда А или В равно 1, олигомер называют «тримером»; с аналогичными перечислениями, описанными для линейных олигомеров.
Стереоизомеры олигомеров включены в объем изобретения. Стереохимию мономеров, входящих в состав олигомера, можно описать терминами их относительной стереохимии, т.е. «альфа/бета» или «цис/транс» или терминами их абсолютной стереохимии, т.е. «R/S». Термин «альфа» (α) указывает, что заместитель ориентирован ниже плоскости флаванового кольца, в то время как термин «бета» (β) означает, что заместитель ориентирован выше плоскости кольца. Термин «цис» указывает, что два заместителя ориентированы на одной стороне кольца, в то время как «транс» указывает, что два заместителя ориентированы с противоположных сторон кольца. Термины «R» и «S» используются для обозначения расположения заместителей около стереогенного центра, основываясь на расположении групп соответственно атомному номеру атомов, непосредственно связанных со стереогенным центром (система КИП).
Имеются многочисленные стереохимические связи между С-4-положением флаван-3-ол-мономера и С-6- и С-8-положениями смежного мономера. Стереохимические связи между мономерными единицами обозначены здесь как (4α→6), или (4β→6), или (4α→8), или (4β→8) для линейных олигомеров. Для связей с разветвленным или соединительным мономером стереохимическими связями являются (6→4α), или (6→4β), или (8→4α), или (8→4β). Когда (+)-катехин, обозначенный здесь как С, связан с другим С или (-)-эпикатехином, обозначенным здесь как ЕС, связи предпочтительно представляют (4α→6) или (4α→8). Когда ЕС связан с С или другим ЕС, связи предпочтительно представляют (4β→6) или (4β→8).
Линейные или разветвленные олигомеры можно получить способами по настоящему изобретению с использованием стадий защиты, активирования, сочетания, маскирования, блокирования, снятия защиты, демаскирования и деблокирования. В каждой последовательности реакций мономеры можно использовать для получения линейных или разветвленных олигомеров, включающих одинаковые или различные мономеры. Высшие олигомеры можно получить повторением сочетания димера, тримера и т.п. с дополнительным мономером, используя вышеуказанные стадии.
Примеры соединений, которые можно синтезировать способом по изобретению, включают димеры;
ЕС-(4β→8)-ЕС и ЕС-(4β→6)-ЕС, где ЕС-(4β→8) -ЕС является предпочтительным; тримеры [ЕС-(4β→8)]2-ЕС, [ЕС-(4β→8)]2-С и [ЕС-(4β→6)]2-EC, где [ЕС-(4β→8)]2-EC является предпочтительным; тетрамеры [ЕС- (4β→8)]3-ЕС, [ЕС-(4β→8)]3-С и [ЕС-(4β→8)]2-ЕС-(4β→6)-С, где [ЕС-(4β→8)]3-ЕС является предпочтительным; и пентамеры [ЕС-(4β→8)]4-ЕС, [ЕС-(4β→8)]3-ЕС-(4β→6)-ЕС, [ЕС-(4β→8)]3-ЕС-(4β→8)-С и [ЕС-(4β→8)]3-ЕС-(4β→6)-С, где [ЕС-(4β→8)]4-ЕС является предпочтительным. Примером разветвленного тримера является
примером разветвленного тетрамера является
примером разветвленного пентамера является
Дополнительные соединения, которые можно синтезировать, включают следующие:
(i) гексамер, в котором один мономер (С или ЕС) связан с пентамером соединения, входящим в перечень выше, например [ЕС-(4β→8)]5-EC, [ЕС-(4β→8)]4-ЕС-(4β→6)-ЕС, [ЕС-(4β→8)]4-ЕС-(4β→6)-С и [ЕС-(4β→8)]4-ЕС-(4β→6)-С, где [ЕС-(4β→8)]5-EC является предпочтительным, с примером разветвленного гексамера
(ii) гептамер, в котором любая комбинация двух мономеров (С и/или ЕС) связана с одним из вышеуказанных пентамеров, например [ЕС-(4β→8)]6-ЕС, [ЕС-(4β→8)]5-ЕС-(4β→6)-ЕС, [ЕС-(4β→8)]5-ЕС-(4β→8)-С и [ЕС-(4β→8)]5-ЕС-(4β→6)-С, где [ЕС-(4β→8)]6-ЕС является предпочтительным, с примером разветвленного гептамера
(iii) октамер, в котором любая комбинация трех мономеров (С и/или ЕС) связана с одним из вышеуказанных пентамеров, например [ЕС-(4β→8)]7-ЕС, [ЕС-(4β→8)]6-EC-(4β→6)-EC, [ЕС-(4β→8)]6-ЕС-(4β→8)-С, [ЕС-(4β→8)]6-ЕС-(4β→6)-С, где [ЕС-(4β→8)]7-ЕС является предпочтительным, с примером разветвленного октамера
(iv) нонамер, в котором любая комбинация четырех мономеров (С и/или ЕС) связана с одним из вышеуказанных пентамеров, например [ЕС-(4β→8)]8-ЕС, [ЕС-(4β→8)]7-ЕС-(4β→6)-ЕС, [ЕС-(4β→8)]7-ЕС-(4β→8)-С, [ЕС-(4β→8)]7-ЕС-(4β→6)-С, где [ЕС-(4β→8)]8-ЕС является предпочтительным, с примером разветвленного нонамера
(v) декамер, в котором любая комбинация пяти мономеров (С и/или ЕС) связана с одним из вышеуказанных пентамеров, например [ЕС-(4β→8)]9-ЕС, [ЕС-(4β→8)]8-ЕС-(4β→6)-ЕС, [ЕС-(4β→8)]8-ЕС-(4β→8)-С, [ЕС-(4β→8)]8-ЕС-(4β→6)-С, где [ЕС-(4β→8)]9-ЕС является предпочтительным, с примером разветвленного декамера
(vi) ундекамер, в котором любая комбинация шести мономеров (С и/или ЕС) связана с одним из вышеуказанных пентамеров, например [EC-(4β→8)]10-EC, [EC-(4β→8)]9-ЕС-(4β→6)-ЕС, [ЕС-(4β→8)]9-ЕС-(4β→8)-С, [ЕС-(4β→8)]9-ЕС-(4β→6)-С, где [ЕС-(4β→8)]10-ЕС является предпочтительным, с примером разветвленного ундекамера
(vii) додекамер, в котором любая комбинация семи мономеров (С и/или ЕС) связана с одним из вышеуказанных пентамеров, например [ЕС-(4β→8)]11-ЕС, [ЕС-(4β→8)]10-ЕС-(4β→6)-ЕС, [ЕС-(4β→8)]10-ЕС-(4β→8)-С, [ЕС-(4β→8)]10-ЕС-(4β→6)-С, где [ЕС-(4β→8)]11-ЕС является предпочтительным, с примером разветвленного додекамера
Вышеуказанный перечень олигомеров является иллюстративным и приводится для демонстрации типов соединений, которые можно получить способами по изобретению, и не представляет исчерпывающий перечень соединений, входящих в изобретение. Олигомеры можно разделить и очистить способами, раскрытыми в патенте США 5554645 от 10 сентября 1976, Romanczyk et al. и патенте США 5712305 от 27 января 1998, Romanczyk et al.
Специалистам в данной области очевидно понятно, что вращение ряда связей внутри олигомера может быть ограниченным за счет стерического препятствия особенно, если олигомер является замещенным, например, бензильными группами. Следовательно, все возможные региоизомеры и стереоизмеры соединений, полученных по изобретению, включены в объем изобретения.
Определения
Как здесь использовано, «защитная группа» является удаляемой группой, которая замещает водород фенольных гидроксильных групп в процианидиновых мономерах или олигомерах. Группу следует удалить в условиях, которые не влияют отрицательно на процианидиновые олигомеры.
Как здесь использовано, «блокирующая группа» является удаляемой группой, которая направляет сочетание блокированием С-8-положения кольца А процианидинового олигомера, направляя таким образом сочетание с другим процианидиновым мономером по С-6-положению кольца А. Группу следует удалить в условиях, которые не влияют отрицательно на процианидиновый олигомер.
Как здесь использовано, «маскирующая группа» является удаляемой группой в С-4-положении, которая маскирует незащищенную фенольную гидроксильную и С-3-гидроксильную группу(ы) процианидинового мономера или высшего олигомера во время сочетания димера высшего олигомера с другим процианидиновым мономером. Группу следует удалить в условиях, которые не влияют отрицательно на процианидиновый олигомер.
Как здесь использовано, «активирующая группа» является ацилоксильной группой, которая активирует С-4-положение С-кольца процианидинового димера или олигомера и приводит к сочетанию с другим процианидиновым мономером или олигомером в этом положении.
Термин «комбинационный», используемый здесь, относится к вероятным возможностям региохимических связей для получения любого данного процианидинового олигомера. Например, линейный процианидиновый тетрамер может включать связи (4→8) и (4→6) между мономерами, входящими в состав тетрамера. Для целей синтеза данные связи приводят к получению отдельных соединений, которые могут обладать различной биологической активностью. Для исследования зависимости структура-активность будет полезным обеспечить ряд таких олигомеров с целью определения важности региохимических связей в отношении биологической активности. Для линейного тетрамера возможные связи являются следующими:
| Тетрамер1 | Тетрамер 2 | Тетрамер 3 | Тетрамер 4 | Тетрамер 5 | Тетрамер 6 | Тетрамер 7 | Тетрамер 8 |
| 4→8 | 4→6 | 4→8 | 4→8 | 4→6 | 4→6 | 4→6 | 4→8 |
| 4→8 | 4→6 | 4→8 | 4→6 | 4→8 | 4→6 | 4→8 | 4→6 |
| 4→8 | 4→6 | 4→6 | 4→8 | 4→8 | 4→8 | 4→6 | 4→6 |
что делает необходимым потребность в способе синтеза для получения 8 различных тетрамеров, для каждого из которых требуются различные стадии получения.
Защитные группы
Защитные группы, пригодные для данного изобретения, представляют электронодонорные группы, функция которых заключается в активировании процианидиновых мономеров в реакциях С-4-активирования и сочетания, описанных ниже. В реакции С-4-активирования электронодонорные фенольные защитные группы функционируют для стабилизации и таким образом они способствуют образованию промежуточного С-4-бензильного катиона, образующегося при окислении защищенного мономера солью свинца (IV). В реакции сочетания, реакции электрофильного ароматического замещения электронодонорные фенольные защитные группы также функционируют для стабилизации и таким образом способствуют образованию С-4-бензильного катиона, образующегося при обработке С-4-ацилокси-замещенного процианидинового мономера (активированного мономера) кислотой Льюиса в качестве катализатора. В реакции сочетания электронодонорные фенольные защитные группы также функционируют для того, чтобы увеличить различия в реакционной способности у различных арильных групп, которые могут находиться в реакции. Как описано ниже, незащищенные процианидиновые мономеры или выбранные незащищенные (со снятой защитой) мономерные единицы процианидинового олигомера используются в качестве нуклеофилов в реакции сочетания; С-4-ацилокси-замещенный, защищенный процианидиновый мономер при обработке кислотой Льюиса функционирует в качестве электрофила. Незащищенные процианидины функционируют в качестве нуклеофилов, поскольку они обладают более высокой электронной плотностью, которая выше нуклеофильности, чем у защищенных процианидиновых мономеров. Любое самосочетание между защищенными процианидиновыми мономерами ограничивается за счет сравнительно более высокой нуклеофильности у незащищенных процианидинов.
Среди различных защитных групп бензильные группы являются предпочтительными, поскольку они легче удаляются в мягких условиях, таких как гидрогенолиз. Другим преимуществом бензилирования (за исключением, например, п-нитробензилирования) является то, что оно не дезактивирует ароматическое кольцо перед сочетанием, когда процианидиновые мономеры или олигомеры действуют в качестве нуклеофилов. Является удивительным и совершенно неожиданным, что замена апротонного органического растворителя, используемого на стадии защиты с диметилформамида (ДМФА) на диметилацетамид (ДМА), приводила к повышенному выходу защищенного олигомера, возможно за счет того факта, что незначительно более высокая диэлектрическая константа ДМА может способствовать О-алкилированию. Выход составил по меньшей мере примерно 50%, обычно примерно от 60% до примерно 70%. Кроме того, при этом не требовалось дополнительной очистки, и продукты легко кристаллизовались. В примерах 1 и 2 описываются конкретные условия получения тетра-O-бензил-(+)-катехина и тетра-O-бензил-(-)-эпикатехина. Дальнейшее исследование системы растворителей показало, что карбонат калия (К2СО3) был предпочтителен по сравнению с карбонатом натрия (Na2СО3) в результате его растворимости в предпочтительной системе растворителей. Было установлено, что йодид калия можно применять в каталитических количествах в сочетании с бензилбромидом.
Другой пригодной защитной группой для (-)-эпикатехина является п-метоксибензильная группа (РМВ). Если выбрана РМВ в качестве защитной группы при получении частично защищенного процианидинового димера, тогда стадия защиты дополнительно включает ацетилирование процианидинового мономера с последующей обработкой гидридом натрия, РМВ-хлоридом и ДМФА в воде для удаления фенольных ацетатных групп, приводя к алкилированию феноксидных ионов с помощью РМВ. При использовании ДМА в качестве растворителя на стадии защиты РМВ-группы использовать не следует. Тетра-O-РМВ-(-)-эпикатехин можно получить с использованием способа Kawamoto H., Nakatsubo F. и Murakami К., Synth. Commun., 26, 531-534 (1996). Вначале получают пентаацетил (-)-эпикатехин (как описано в примере 3 ниже) обработкой гидридом натрия (NaH), п-метоксибензилхлоридом (PMBCl), диметилформамидом (ДМФА) и водой в количестве, достаточном (4 экв) для получения эквивалентного количества основания для последовательного удаления четырех фенольных ацетатных групп. Полученные феноксидные ионы подвергаются быстрому алкилированию с помощью PMBCl. В примерах 4 и 5 описаны конкретные условия, при которых получали пентаацетил(+)-катехин и тетра-О-п-метоксибензил-3-ацетил-(-)-эпикатехин.
Очевидно специалистам в данной области понятно, что можно использовать другие защитные группы, такие как трет-бутил, тритил и 2,4-диметоксибензил.
С-4-активирование
Изменение условий реакции при участии LTA на смесь бензол: уксусная кислота 1:1 в конечном итоге давало наиболее высокий выход (60-70%) и стереоспецифичный 4β-продукт. Другие пригодные смеси растворителей включают бензол, толуол, хлорбензол, циклогексан, гептан, четыреххлористый углерод или их смеси, смешанные с органической кислотой, которая является такой же, какая была использована для получения соли свинца (IV), примененного в реакции активирования.
На стадии активирования применяют соли свинца органических кислот, например тетраформиат свинца, тетрапропионат свинца и тому подобное. Предпочтительно использовать для улучшения выхода соответствующие органические кислоты, например муравьиную и пропионовую кислоты в сочетании с солью свинца. Предпочтительной солью является ацетат свинца и предпочтительную комбинацию представляют тетраацетат свинца и уксусная кислота.
В примерах 6-9 описаны конкретные условия получения 4β-ацетокси тетра-O-бензил-(-)-эпикатехина, 4β-гидроксил тетра-O-бензил-(+)-катехина, 4β-гидроксил тетра-O-бензил-(-)-эпикатехина и 4β-ацетокси тетра-O-бензил-(+)-катехина.
Маскирующие группы
Маскирующие группы, пригодные для данного изобретения, представляют электроноакцепторные группы, функция которых заключается в дезактивировании выбранных мономерных единиц процианидиновых олигомеров в реакции электрофильного ароматического заместительного сочетания, описанной ниже. Когда в реакции сочетания используются процианидиновые олигомеры, требуется, чтобы активированный мономер не взаимодействовал произвольно с