Способ регистрации макромолекул при проведении протеомных исследований и биочип, используемый при их регистрации
Иллюстрации
Показать всеИзобретение относится к протеомике и медицинской диагностике. Регистрация макромолекул и их комплексов осуществляется с использованием сканирующей зондовой микроскопии и биочипа, представляющего иммобилизованное поле молекул, способных ковалентно или нековалентно взаимодействовать с исследуемыми макромолекулами и/или их комплексами, на подложке из слюды, с поверхностью, обработанной в плазме электрического разряда посредством прикладывания постоянного или низкочастотного напряжения к разрядному промежутку подложки с образцом и химически модифицированной силаном, при котором биочип помещают в раствор, содержащий исследуемые макромолекулы и/или их комплексы, и за счет ковалентного или нековалентного взаимодействия с иммобилизованными на подложке молекулами исследуемые макромолекулы и их комплексы вылавливают и после отмывки поля от неспецифических комплексов регистрируют. Использование способа позволяет повысить чувствительность метода сканирующей зондовой микроскопии при проведении протеомных исследований и медицинской диагностики. 2 н. и 2 з.п. ф-лы, 3 ил.
Реферат
Изобретение относится к протеомике и медицинской диагностике и касается применения методов зондовой микроскопии для регистрации макромолекул при протеомных исследованиях и диагностики, а также к технологии изготовления биочипов, используемых в зондовой микроскопии.
Основной проблемой в протеомике является отсутствие возможности применения для белков реакции, подобной полимеразной цепной реакции (ПЦР), которая бы позволила производить копии белковых молекул и, как следствие, повышать их концентрацию.
Отсутствие амплификации белков и их фрагментов ограничивает предельно допустимую чувствительность современных протеомных технологий на уровне 10-15 М, что не позволяет регистрировать при исследовании многие маркеры заболеваний.
Известен ряд методов идентификации единичных молекул с использованием сканирующей зондовой микроскопии, основанных не на измерении концентрации молекул, а на подсчете их числа. Одним из таких методов, широко использующихся в настоящее время в биохимии, является зондовая микроскопия с использованием атомно-силового микроскопа (АСМ). По методу зондовой микроскопии для обнаружения в пробе белков используется биочип, на подложку которого наносится капля аналита.
Однако ограничение объема пробы каплей предопределяет низкий концентрационный предел обнаружения молекул этим методом на уровне (10-15 М), что является недостаточным для регистрации многих маркеров, используемых в медицинской диагностике и протеомных исследованиях.
Кроме того, одной из основных проблем применения для регистрации макромолекул зондовой микроскопии с использованием, например, атомно-силового микроскопа (АСМ), является слабая адгезия макромолекул к подложке биочипа. При слабой адгезии макромолекулы под действием движения измерительного зонда относительно биочипа могут смещаться. Так, например, установлено, что антиген HBsAg вируса гепатита В имеет слабую адгезию к подложке и смещается зондом микроскопа при его движении относительно подложки биочипа. Из-за смещения пространственное разрешение снижается, а в ряде случаев объекты вообще невозможно регистрировать с применением зондовой микроскопии при использовании АСМ.
Наиболее близким к предлагаемому способу является способ идентификации единичных молекул - аптамеров (олигонуклеотидов) с использованием атомно-силового микроскопа, в соответствии с которым для выявления олигонуклеотидов, способных специфически связываться с молекулами-мишенями (на примере аптамеров, связывающихся с тромбином), указанные молекулы-мишени иммобилизуют на подложке. При контактировании различных олигонуклеитидов с указанными молекулами-мишениями происходит выбор из смеси олигонуклеитидов тех атпамеров, которые имеют высокое сродство к молекулам-мишениям. Регистрацию указанных аптамеров осуществляют с помощью атомно-силового микроскопа после отмывки поля от несвязанных молекул (Guthold M et al. "Novel methodology to detect, isolate, amplify and characterize single aptamer molecules with desirable target-binding properties" (Biophysical Journal, 2002, 82 (1).
При создании способа регистрации макромолекул для протеомных исследований ставилась задача повышения чувствительности метода зондовой микроскопии за счет увеличения количества вылавливаемых из биологической жидкости макромолекул.
В соответствии с поставленной задачей предлагается способ регистрации макромолекул и/или их комплексов с использованием сканирующей зондовой микроскопии и биочипа, представляющего иммобилизованное поле молекул, способных ковалентно или нековалентно взаимодействовать с исследуемыми макромолекулами и/или их комплексами на подложке из слюды с поверхностью, обработанной в плазме электрического разряда посредством прикладывания постоянного или низкочастотного напряжения к разрядному промежутку подложки с образцом и химически модифицированной силаном, при котором биочип помещают в раствор, содержащий исследуемые макромолекулы и/или их комплексы, и за счет ковалентного или нековалентного взаимодействия с иммобилизованными на подложке молекулами исследуемые макромолекулы и их комплексы вылавливают и после отмывки поля от неспецифических комплексов регистрируют.
Применение термина "вылавливают" (на английском языке "Fishing"), используемого в международных научных изданиях, в данном контексте означает захват молекулой, иммобилизованной на поверхности чипа, макромолекулы-партнера из раствора и концентрирование захваченных макромолекул на поверхности биочипа (см. review: Nelson R.W and Krone J.R. J. of Molecular recognition, 1999, 12, 77-93. Natsume Т., Nakayama H., Isobe Т. Trends in Biotechnology, 2001, 19, S28-S33).
Так как макромолекулы, например функционально-важные белки, могут существовать в растворе в аггрегированном состоянии либо в комплексе с другими белками, как например, в случае цитохром Р450-содержащих систем, то иммобилизованная на поверхности биочипа молекула может захватывать из раствора и формировать на поверхности биочипа комплекс не только с отдельной макромолекулой, а и захватывать из раствора сразу комплекс молекул и формировать более сложный комплекс, например захватывать бинарный комплекс, состоящий из двух молекул и соответственно формировать тройной комплекс (Kiselyova O.I., Yaminsky I.V., Ivanov Yu. D., Kanaeva I.P., Kuznetsov V.Yu., Archakov A.I. AFM study of membrane proteins, cytochrome P450 2B4 and NADPH-cytochrome P450 reductase, and of their complex formation. Archives of Biochemistry and Biophysics, 1999, v.371, N 1, 1-7, Atomic force microscopy revelation of molecular complexes in the multiprotein cytochrome P450 2B4-containing system. Proteomics. 2004 Aug; 4(8):2390-2396).
Повышение чувствительности метода зондовой микроскопии для протеомных исследований обеспечивается одновременным действием трех существенных признаков предлагаемого способа:
1) Обработкой подложки из слюды в плазме электрического разряда, что обеспечивает: увеличение прочности иммобилизации молекул-зондов на положке биочипа.
2) Прочностью связывания регистрируемых макромолекул маркерных белков с молекулами-партнерами, иммобилизованными на поверхности подложки биочипа за счет их ковалентного связывания между собой.
3) Повышением возможного объема биологической жидкости, используемой для анализа, приводит к повышению количества макромолекул, используемых для их регистрации
Известны биочипы, в которых макромолекулы, играющие роль молекулярных зондов, иммобилизированы в ячейки гидрогеля, закрепленные на общей подложке и образующие регулярную структуру (матрицу) (пат. США 5552270 и 5552271).
Известны композиции для иммобилизации олигонуклеотидов и белков в полиакриламидном геле при изготовлении биочипов методом сополимеризации (F.N.Rehman. M.Audeh, E.S.Abrams, P.W.Hammond, M.Kenney and T.C.Boles, Nucleic Acids Research, 1999, v.27, 15, p.649-655 [1]. A.V.Vasiliskov, E.N.Timofeev, S.A.Surzhikov, A.L.Drobyshev, V.V.Shick and A.D.Mirzabekov, BioTechniques, 1999, v.27, p.592-606 [2]).
В состав таких композиций, используемых для изготовления указанных биочипов, входят:
- подложка, составляющая основу поля иммобилизованных макромолекул;
- модифицированные олигонуклеотиды и белки, высаживаемые на подложку.
В известных способах изготовления биочипов на основе гидрогелей технологический цикл включает: (1) подготовку подложки, (2) формирование на ней матрицы ячеек геля, (3) нанесение на ячейки растворов биологических макромолекул в соответствии с заранее составленной схемой биочипа, (4) химическую обработку ячеек с целью иммобилизации молекул-зондов, (5) отмывку и просушку полученных биочипов.
Известен способ приготовления биочипов, согласно которому ячейки биочипа получают полимеризацией композиций в каплях, нанесенных на подложку с помощью микропипетки (F.N.Rehman, M.Audeh, E.S.Abrams, P.W.Hammond, M.Kenney and T.C.Boles, Nucleic Acids Research, 1999, v.27, 15, p.649-655).
К недостаткам применительно к сканирующей зондовой микроскопии известных способов и используемых биочипов относятся:
1. Низкая воспроизводимость свойств ячеек и неоднородность распределения в объеме ячейки иммобилизуемого соединения.
2. Технически сложная технология изготовления биочипов, не обеспечивающая необходимой однородности и воспроизводимости свойств молекул аналита и плохо подающаяся автоматизации.
3. Образование полимерными материалами типа гелей, адсорбированных на поверхности биочипов, структур с размерами, превышающими размеры анализируемых макромолекул.
Известно использование в биочипе подложки из слюды для иммобилизации биологических макромолекул при исследованиях с помощью сканирующей зондовой микроскопии (Muller DJ et al. Adsorption of biological molecules to a solid support for scanning probe microscopy. J.Struct Biol., 1997, Jui, 119(2), p.172-188).
Слюда является одной из наиболее подходящих подложек при изготовлении биочипов для зондовой микроскопии с применением, в частности, атомно-силового микроскопа при визуальной регистрации макромолекул с размерами порядка нанометров (к ним относятся белки, белковые комплексы, олигонуклеотиды и т.д.), поскольку при скалывании на ее поверхности образуются протяженные атомно-гладкие подплощадки, на которых для анализа с помощью сканирующей зондовой микроскопии можно иммобилизовывать макромолекулы.
Однако слюда, как таковая, химически слабо активна, в связи с чем ковалентная пришивка макромолекул к ее поверхности без дополнительной обработки ее поверхности проблематична.
Для модификации поверхности слюды и обеспечения необратимости реакции комплексообразования с иммобилизованным партнером поверхность слюды подвергают модификации в плазме, создаваемой высокочастотным разрядом. При этом для получения такого разряда используется среда, содержащая 0.03 Торр аргона и 0.02 Торр водяного пара (T.J.Senden and W.A.Ducker - Surface roughness of plasma-treated mica. Langmuir, 8, 733-735, 1992 г.).
Для создания таких условий откачка плазменного реактора, содержащего подложку из слюды, должна быть доостаточного давления (Р), не менее 0.0001 Торр [Parker J.L, Choa D.J., Claesson P.M. «Plasma modification on mica: Forces between fluorocarbon surface in water and nonpolar liquid». - J. Phys. Chem. 1989, 93, 6121-6125].
Недостатком данного способа модификации поверхности слюды является необходимость создания высокого вакуума Р, порядка 0.0001 Торр, и распространение высокочастотного поля, создаваемого источником мощностью 25 Вт, 18 МГц, во внешнюю среду из разрядной трубки, что вредно для оператора.
Наиболее близким к предлагаемому биочипу является протеиновый биочип, представляющий собой расположенные на твердой подложке макромолекулы (антитела, антигены или их фрагменты), с помощью которого осуществляют диагностику путем идентификации биологических макромолекул, специфичных для инфекционного заболевания (гепатит В, С, сифилиса и др. (CN 1373365, кл. G 01 N 33/68, опубл. 09.10.2002).
Недостатком данного биочипа является использование для диагностики только белков или их фрагментов, то есть только биомолекул, количество которых ограничено и производство которых требует больших финансовых затрат.
Задачей создания биочипа для регистрации макромолекул при протеомных исследованиях является устранение перечисленных выше недостатков с одновременным повышением чувствительности метода сканирующей зондовой микроскопии и диагностики за счет закрепления полученных комплексов (макромолекул/иммобилизованных молекул на подложке) с помощью ковалентной сшивки образованных комплексов на поверхности биочипа, что включает в себя ковалентную иммобилизацию молекул-зондов на подложке и ковалентное связывание иммобилизованных молекул с макромолекулами-партнерами в образованных комплексах. Молекулами-зондами могут быть не только биомолекулы, но синтетические молекулы, то есть искусственно синтезированные молекулы.
В качестве иммобилизованных молекул могут быть антитела, антигены, аптамеры, фотоаптамеры, олигонуклеотиды или их фрагменты, как в виде отдельного биочипа, так и любые комбинации этих молекул в виде поля.
В соответствии с поставленной задачей создан биочип для идентификации макромолекул с использованием сканирующей зондовой микроскопии, состоящий из поля иммобилизованных молекул, способных ковалентно и нековалентно взаимодействовать с исследуемыми макромолекулами и/или их комплексами, расположенными на подложке, в котором в качестве подложки использована слюда, поверхность которой обработана в плазме электрического разряда и химически модифицирована силаном.
В соответствии с настоящим изобретением подложка из слюды модифицируется без применения высокого вакуума, что значительно уменьшает затраты на создание Р вакуума и рабочей среды плазмы и минимизирует или совсем исключает негативное воздействие на оператора излучения в высокочастотом диапазоне.
С этой целью подложка из свежесколотой слюды помещается в плазму тлеющего электрического разряда и посредством прикладывания постоянного, либо низкочастотного напряжения к разрядному промежутку подложки с образцом модифицируется, после чего подвергается химической модификации в парах силана, при которой происходит ковалентная иммобилизация силана на поверхности слюды. На силанизированной таким образом поверхности слюды белок ковалентно иммобилизуется.
Установлено, что неровность рельефа поверхности силанизированной подложки не превышает 1 нм.
Присутствие на модифицированной поверхности слюды силана повышает адгезию молекул, пришиваемых к подложке, и позволяет проводить ковалентную пришивку молекул к подложке за счет ковалентной пришивки их к силанизированной предлагаемым способом поверхности подложки
Сущность изобретения поясняется фиг.1, на которой представлена схема осуществления способа регистрации макромолекул, фиг.2, на которой представлены с помощью атомно-силового микроскопа изображения биочипа, на подложке которого иммобилизованы макромолекулы, и фиг.3, на которой показан пример использования аптамеров, иммобилизованных на подложке биочипа для выявления макромолекулярных партнеров к аптамерам, и регистрация этих комплексов на подложке биочипа с помощью атомно-силового микроскопа
При реализации схемы, представленной на фиг.1, поле иммобилизованных на подложке молекул (в частности, антител, аптамеров (синтезируемых олигонуклеотидов по методу, изложенному, например в Comb. Chem. Heigh Throughput Screen, 1999, 2, 271-278, Tasset DM, Kubik MF, Steiner W. J Mol Biol. 1997, Oct 10; 272(5):688-698), антигенов, олигонуклеотидных зондов) помещается в объем раствора, содержащий исследуемые макромолекулы, с последующим вылавливанием маркерных белков-партнеров (в частности, антигенов, антител или олигонуклеотидов, в частности, нуклеиновых кислот вирусов) за счет их взаимодействия на этом поле с иммобилизованными молекулами. После чего поле молекул отмывается от неспецифических комплексов и анализируется. Объем раствора может варьироваться от одной капли до одного литра и более.
Расчеты показывают, что если используется в качестве исходного материала 1 мл биологической жидкости с концентрацией белка 10-15 М, то предлагаемый способ позволяет на подложке площадью 20×20 мкм2 обнаружить порядка 36 молекул белков, образующих комплексы с иммобилизованным партнером, имеющим Kd=10-12 М.
Антитела, антигены, их фрагменты, аптамеры, фотоаптамеры, олигонуклеотидные зонды могут быть ковалентно иммобилизованы на силанизированной поверхности слюды с помощью химических методов (в том числе фотохимических, электрохимических, радиохимических и т.д.). Ниже приводится пример необратимой ковалентной иммобилизации таких молекул на подложке из слюды на примере антител к вирусу гепатита В (фиг.2) и аптамеров, иммобилизованных на подложке биочипа (фиг.3).
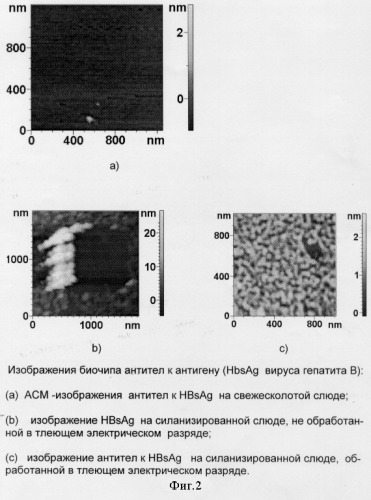
На фиг.2 в качестве примера осуществления предлагаемого изобретения представлены полученные с помощью атомно-силового микроскопа изображения биочипа (для примера антител к антигену HBsAg вируса гепатита В), где в позиции (а) изображены макромолекулы, адсорбированные на подложке из свежесколотой слюды, поверхность которой не обработана, в позиции (в) - изображения макромолекул (в примере HBsAg вируса гепатита В) на модифицированной силаном подложке свежесколотой слюды без предварительной обработки ее поверхности перед силанизацией в тлеющем электрическом разряде; в позиции (с) - макромолекулы, ковалентно пришитые к подложке из свежесколотой слюды, поверхность которой предварительно перед силанизацией обработана в электрическом разряде.
Как видно на фиг.2 из сравнения позиций (а) и (с), количество иммобилизованных объектов на модифицированной силаном подложке с предварительной перед силанизацией обработкой подложки в электрическом разряде по сравнению с немодифицированной силаном поверхностью увеличивается. Изображения получены в полуконтактной моде измерения. Причем при увеличенном воздействии зонда атомно-силового микроскопа в квадрате (позиция (с) на фиг.2) отрыва молекул белка (антител) от поверхности подложки не наблюдалось, в то время как в позиции (в), когда перед силанизацией подложки не проводилась обработка подложки в электрическом разряде, наблюдается отрыв и смещение молекул белка.
В случае, когда слюда была обработана в электрическом разряде перед силанизацией, при сканировании поверхности биочипа с ковалентно иммобилизованными антигенами к силанизированной поверхности в режиме контактной моды в квадрате (позиция (с) на фиг.2) не наблюдается сдвигание молекул белка к краям квадрата в направлении сканирования зонда микроскопа.
Электрический разряд осуществлялся посредством прикладывания постоянного напряжения к разрядному промежутку, содержащему образец. Таким образом, изображения, представленные на фиг.2, показывают, что молекулы белка более прочно иммобилизованы на поверхности силанизированной слюды, обработанной перед силанизацией электрическим разрядом.
Аналогичные результаты были получены, когда в качестве иммобилизированных на подложке макромолекул использовались фотореактивный белок, антитела, антигены, аптамеры, фотоаптамеры, олигонуклеотиды или их фрагменты, способные образовывать ковалентный комплекс со специфическим компонентом биологической пробы, как в виде отдельного биочипа, так и любые комбинации этих молекул в виде поля.
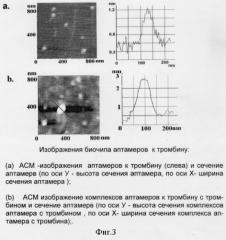
Пример использования аптамеров, иммобилизованных на подложке биочипа для выявления макромолекулярных партнеров к аптамерам, и регистрация этих комплексов на подложке биочипа с помощью атомно-силового микроскопа представлены на фиг.3. Как видно из фиг.3, высота аптамера тромбина порядка 1 нм. При формировании комплексов аптамера с тромбином высота комплекса изображения увеличивается и становится около 3 нм, то есть биочип с иммобилизованным аптамером можно использовать для выявления их комплексов с белками-партнерами.
При иммобилизации на биочипе олигонуклеотидных зондов, например олигонуклеотидного зонда 5' GACCTTGAGG-САТАСТТС с участком, идентичным участку ДНК вируса гепатита В, он образует комплекс с комплементарным участком другого олигонуклеотида 3' CTGGAACTCCGTAT-GAAGTTTCTGACACACAAATGACTCA, при этом регистрируется увеличение линейного размера примерно с 10 до 15 нм.
Обработанная в электрическом разряде силанизированная поверхность подложки биочипа из слюды, обеспечивающая ковалентную сшивку молекул, позволяет вылавливать даже низкоафинные макромолекулы.
Осуществление необратимой реакции комплексообразования за счет фотореактивного белка или фотоаптамера, иммобилизованного на поверхности, позволяет увеличить концентрационную чувствительность метода зондовой микроскопии до уровня 10-19 M; расчеты показывают, что при такой концентрации можно обнаружить порядка 60 молекул.
Чувствительность метода зондовой микроскопии при использовании предлагаемого биочипа для протеомных исследований повышается за счет: а) необратимости иммобилизации молекулы к поверхности подложки, которая обеспечивается ковалентным связыванием молекул за счет обработки поверхности слюды, модифицированной силаном и используемой в качестве подложки биочипа в плазме электрического разряда; б) ковалентной связи между иммобилизованными молекулами и исследуемыми позволяет выловить даже низкоафинные макромолекулы и повысить чувствительность регистрации макромолекул с использованием атомно-силового микроскопа по проведенным расчетам с 10-12 М (для обратимой реакции комплексообразования при афинности, характеризуемой константой Kd=10-12 M) до 10-19 M (для необратимой реакции при Kd=0, достигаемой за счет их ковалентного связывания); в) увеличения объема раствора инкубации.
При использовании нанополя - подложки к сканирующим зондовым микроскопам с иммобилизованными молекулами разных типов - с разными типами иммобилизованных зондов - предлагаемый способ позволяет проводить регистрацию различных типов заболеваний по регистрации комплексов зонд/мишень одновременно.
Применение вместо одноканального многоканального, например 24-50 канального, атомно-силового микроскопа (АСМ) позволяет поднять производительность метода зондовой микроскопии в соответствующее число раз, например 24-50 раз, а при использовании АСМ в режиме одновременного измерения во многих точках, например 24-50 точках, нанополя увеличить чувствительность до зептомолярного уровня в режиме измерения, при котором в этих точках, например в 24-50 точках, иммобилизован один и тот же тип молекул.
В качестве сканирующих зондовых микроскопов в данном способе регистрации макромолекул и биочипов к ним могут быть использованы, кроме сканирующих атомно-силовых, также и сканирующие туннельные микроскопы.
При использовании флуоресцирующих иммобилизованных молекул и/или макромолекул или введении специальных флуоресцирующих меток в иммобилизованные молекулы макромолекулы для получения флуоресценции в выбранном спектральном диапазоне вместо атомно-силового микроскопа могут быть использованы ближнепольные сканирующие оптические микроскопы.
1. Способ регистрации макромолекул и/или их комплексов с использованием сканирующей зондовой микроскопии и биочипа, представляющего иммобилизованное поле молекул, способных ковалентно или нековалентно взаимодействовать с исследуемыми макромолекулами и/или их комплексами, на подложке из слюды, с поверхностью, обработанной в плазме электрического разряда посредством прикладывания постоянного или низкочастотного напряжения к разрядному промежутку подложки с образцом и химически модифицированной силаном, при котором биочип помещают в раствор, содержащий исследуемые макромолекулы и/или их комплексы, и за счет ковалентного или нековалентного взаимодействия с иммобилизованными на подложке молекулами исследуемые макромолекулы и их комплексы вылавливают и после отмывки поля от неспецифических комплексов регистрируют.
2. Способ по п.1, при котором в качестве сканирующего зондового микроскопа используется атомно-силовой микроскоп или сканирующий туннельный микроскоп или оптический ближнепольный микроскоп в одноканальном или в многоканальном исполнении.
3. Биочип для индентификации макромолекул с использованием сканирующей зондовой микроскопии, состоящий из поля иммобилизованных молекул, способных ковалентно или нековалентно взаимодействовать с исследуемыми макромолекулами и/или их комплексами, расположенных на подложке, в котором в качестве подложки используется слюда, поверхность которой обработана в плазме электрического разряда посредством прикладывания постоянного или низкочастотного напряжения к разрядному промежутку подложки с образцом и химически модифицирована силаном.
4. Биочип по п.2, в котором в качестве иммобилизованных молекул могут быть антитела, антигены, аптамеры, фотоаптамеры, олигонуклеотиды или их фрагменты, как в виде отдельного биочипа, так и любые комбинации этих молекул в виде поля.