Ингибиторы металлопротеиназ, их применение и фармацевтические композиции на их основе
Иллюстрации
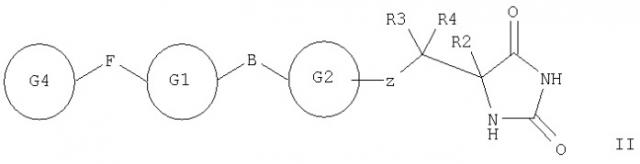
Показать всеОписываются соединение общей формулы (I)
где Х обозначает NR1, Y1 и Y2 представляют О, Z выбран из SO, SO2, m=1, A представляет собой прямую связь, R1 обозначает Н, R2 и R3 независимо выбраны из Н, (С1-6)алкила, гетероциклоалкила, фенила, гетероарила, фенил-алкила, фенил-гетероалкила, гетероарил-алкила, гетероциклоалкил-алкила, R4 представляет собой H, R5 представляет собой моноциклическую, бициклическую или трициклическую группу. Описывается также фармацевтическая композиция и применение соединений в изготовлении лекарства для использования в лечении заболеваний или состояний, опосредованных одним или более чем одним ферментом, представляющим собой металлопротеиназу. Соединения формулы (I) полезны в качестве ингибиторов металлопротеиназ, особенно в качестве ингибиторов ММР12. 3 н. и 11 з.п. ф-лы, 12 табл.
Реферат
Настоящее изобретение относится к соединениям, пригодным для ингибирования металлопротеиназ и, в частности, к фармацевтическим композициям, содержащим их, а также к их применению.
Соединения по данному изобретению являются ингибиторами одного или более чем одного фермента, представляющего собой металлопротеиназу. Металлопротеиназы представляют собой надсемейство протеиназ (ферментов), число которых в последние годы резко возросло. По структурным и функциональным соображениям эти ферменты разделены на семейства и подсемейства, как описано в N. М. Hooper (1994) FEBS Letters 354: 1-6. Примерами металлопротеиназ являются матриксные металлопротеиназы (MMPs), такие как коллагеназы (ММР1, ММР8, ММР13), желатиназы (ММР2, ММР9), стромелизины (ММР3, ММР10, ММР11), матрилизин (ММР7), металлоэластаза (ММР12), энамелизин (ММР19), МТ-ММР (ММР14, ММР15, ММР16, ММР17); репролизин или адамализин или семейство MDC, которое включает в себя секретазы и шеддазы, такие как TNF-конвертирующие ферменты (ADAM10 и ТАСЕ); семейство астацинов, которое включает в себя такие ферменты, как протеиназа процессинга проколлагена (РСР), а также другие металлопротеиназы, такие как аггреканаза, семейство эндотелин-конвертирующих ферментов и семейство ангиотензин-конвертирующих ферментов.
Считается, что металлопротеиназы имеют важное значение при многих физиологических болезненных процессах, в которые вовлечено ремоделирование тканей, такое как развитие эмбриона, костеобразование и маточное ремоделирование во время менструации. В основе этого лежит способность металлопротеиназ расщеплять целый ряд матриксных субстратов, таких как коллаген, протеогликан и фибронектин. Считается также, что металлопротеиназы играют важную роль в процессинге, или секреции, биологически значимых клеточных медиаторов, таких как фактор некроза опухоли (TNF), и в посттрансляционном протеолитическом процессинге, или шеддинге, биологически значимых мембранных белков, таких как IgE рецептор CD23 низкой аффинности (более полный перечень смотри в N. М. Hooper et al., (1997) Biochem. J. 321: 265-279).
Металлопротеиназы связаны со многими заболеваниями или состояниями. Ингибирование активности одной или более чем одной металлопротеиназы может принести большую пользу при этих заболеваниях или состояниях, например при различных воспалительных и аллергических заболеваниях, таких как воспаление сустава (особенно ревматоидный артрит, остеоартрит и подагра), воспаление желудочно-кишечного тракта (особенно воспалительное кишечное заболевание, неспецифический язвенный колит и гастрит), воспаление кожи (особенно псориаз, экзема, дерматит); при метастазировании опухоли или инвазии; при заболевании, связанном с неконтролируемым разрушением внеклеточного матрикса, таком как остеоартрит; при заболевании, связанном с резорбцией кости (таком как остеопороз и болезнь Педжета); при заболеваниях, связанных с аберрантным ангиогенезом; при усиленном ремоделировании коллагена, связанном с диабетом, заболеванием периодонта (таким как гингивит), изъязвлением роговицы, изъязвлением кожи, послеоперационными состояниями (такими как кишечный анастомоз) и заживлением кожных ран; при заболеваниях, связанных с демиелинизацией центральной и периферической нервных систем (таких как рассеянный склероз); при болезни Альцгеймера; при ремоделировании внеклеточного матрикса, которое наблюдается при сердечно-сосудистых заболеваниях, таких как рестеноз и атеросклероз; при астме; при рините и при хронических обструктивных болезнях легких (ХОБЛ).
ММР12, известная также как макрофагальная эластаза или металлоэластаза, первоначально была клонирована в мыши исследователями Shapiro et al. [1992, Journal of Biological Chemistry 267: 4664] и в человеке той же группой ислледователей в 1995 году. ММР-12 преимущественно экспрессируется в активированных макрофагах, и было показано, что она секретируется из альвеолярных макрофагов курящих людей [Shapiro et al., 1993, Journal of Biological Chemistry 268: 23824], а также в пенистых клетках в атеросклеротических повреждениях [Matsumoto et al., 1998, Am. J. Pathol. 153: 109]. Мышиная модель ХОБЛ основана на провокации мышей сигаретным дымом в течение шести месяцев, две сигареты в сутки шесть суток в неделю. После такой обработки у мышей дикого типа развивалась легочная эмфизема. Когда в данной модели тестировали мышей, которым вводили ударную дозу ММР12, у них не развивалась значительная эмфизема, что четко указывает на то, что ММР12 является ключевым ферментом в патогенезе ХОБЛ. Роль ММР, таких как ММР12, при ХОБЛ (эмфиземе и бронхите) обсуждалась в Anderson and Shinagawa, 1999, Current Opinion in Anti-inflammatory and Immunomodulatory Investigational Drugs 1(1): 29-38. Недавно было обнаружено, что курение усиливает инфильтрацию макрофагов и экспрессию ММР-12 макрофагального происхождения в бляшках Кангавари сонной артерии человека [Matetzky S., Fishbein MC et al., Circulation 102(18), 36-39 Suppl. S, Oct 31, 2000].
ММР13, или коллагеназа 3, первоначально была клонирована из библиотеки кДНК, полученной из опухоли молочной железы [J. M. P. Freije et al. (1994) Journal of Biological Chemistry 269 (24): 16766-16773]. ПЦР-РНК анализ РНК из различных тканей показал, что экспрессия ММР13 ограничивается карциномами молочной железы, так как она не была обнаружена в фиброаденомах молочной железы, в нормальной или покоящейся молочной железе, в плаценте, печени, яичнике, матке, простате или околоушной железе, или в клеточных линиях рака молочной железы (T47-D, MCF-7 и ZR75-1). После этого наблюдения ММР13 была обнаружена в трансформированных эпидермальных кератиноцитах [N. Johansson et al. (1997) Cell Growth Differ. 8(2): 243-250], плоскоклеточных карциномах [N. Johansson et al. (1997) Am. J. Pathol. 151(2):499-508] и эпидермальных опухолях [К. Airola et al. (1997) J. Invest. Dermatol. 109(2): 225-231]. Эти результаты говорят о том, что ММР13 секретируется трансформированными эпителиальными клетками и может быть вовлечена в разрушение внеклеточного матрикса и во взаимодействие клетка-матрикс, связанное с метастазированием, в частности, как это было обнаружено при инвазивных повреждениях раковой опухоли молочной железы и при злокачественном эпителиальном росте при онкогенезе кожи.
Из недавно опубликованных данных вытекает, что ММР13 играет роль в обновлении других соединительных тканей. Например, была выдвинута гипотеза, согласующаяся с субстратной специфичностью ММР13 и предпочтительным разрушением коллагена типа II [Р. G. Mitchell et at. (1996) J. Clin. Invest. 97(3): 761-768; V. Knauper et al., (1996) The Biochemical Journal 271: 1544-1550], о том, что ММР13 выполняет определенную роль в процессе первичного окостенения и скелетного ремоделирования [М. Stahle-Backdahl et al. (1997) Lab. Invest. 76(5): 717-728; N. Johansson et al., (1997) Dev. Dyn. 208(3): 387-397], в деструктивных заболеваниях суставов, таких как ревматоидный артрит и остеоартрит [D. Wernicke et al. (1996) J. Pheumatol. 23: 590-595; P. G. Mitchell et al., (1996) J. Clin. Invest. 97(3): 761-768; O. Lindy et al., (1997) Arthritis Rheum 40(8): 1391-1399], и при асептическом ослаблении заменителей тазобедренного сустава [S. Imai et al. (1998) J. Bone Joint Surg. Br. 80(4): 701-710]. MMP13 также вовлечена в хронический периодонтит взрослых, так как она локализуется в эпителии хронически воспаленной слизистой оболочки ткани десен человека [V. J. Uitto et al. (1998) Am. J. Pathol. 152(6): 1489-1499], и в ремоделирование коллагенового матрикса в застарелых ранах [М. Vaalamo et al. (1997) J. Invest. Dermatol. 109(1): 96-101].
MMP9 (желатиназа В; коллагеназа типа IV 92 кДа; желатиназа 92 кДа) представляет собой секретируемый белок, который впервые был очищен, затем клонирован и секвенирован в 1989 году [S. М. Wilhelm et al. (1989) J. Biol. Chem. 264(29): 17213-17221; опечатки опубликованы в J. Biol. Chem. (1990) 265(36): 22570]. Недавно опубликованный обзор по MMP9 [Т.Н. Vu & Z. Werb (1998) (In: Matrix Metalloproteases, 1998. Edited by W. C. Parks & R. P. Mecnam. pp 115-148. Academic Press. ISBN 0-12-545090-7] является отличным источником подробной информации и ссылок по этой протеазе. Из этого обзора Т.Н. Vu & Z. Werb (1998) вытекает следующее.
Экспрессия MMP9 в норме ограничена несколькими типами клеток, в том числе трофобластами, остеокластами, нейтрофилами и макрофагами. Однако ее экспрессия может быть индуцирована в этих клетках и в клетках других типов несколькими медиаторами, включая воздействие на эти клетки факторов роста или цитокинов. Они представляют собой те самые медиаторы, которые, как правило, вовлечены в инициирование воспалительной реакции. Как и другие секретируемые ММР, MMP9 высвобождается в виде неактивного профермента (Pro-), который впоследствии расщепляется с образованием ферментативно активного фермента. Протеазы, необходимые для этой активации in vivo, не известны. Баланс активной ММР9 в сравнении с неактивным ферментом дополнительно регулируется in vivo взаимодействием с природным белком TIMP-1 (тканевый ингибитор металлопротеаз-1). TIMP-1 связывается с С-концевым участком ММР9, что приводит к ингибированию каталитического домена ММР9. Сочетание баланса индуцированной экспрессии ProMMP9, расщепления Pro- до активной ММР9 и присутствия TIMP-1 определяет количество каталитически активной ММР9, присутствующей в сайте локализации. Протеолитически активная ММР9 атакует субстраты, которые включают в себя желатин, эластин и природные коллагены типа IV и типа V; она не обладает активностью против нативного коллагена типа I, протеогликанов или ламининов.
Существует все возрастающая масса сведений о роли ММР9 в различных физиологических и патологических процессах. Физиологические роли включают в себя инвазию эмбриональных трофобластов через эпителий матки на ранних стадиях эмбриональной имплантации, определенное участие в росте и развитии костей и миграцию воспалительных клеток из сосудистой сети в ткани.
Высвобождение ММР-9, измеренное с применением иммуноферментного анализа, было значительно более высоким в жидкостях и в AM супернатантах от не подвергавшихся лечению астматиков по сравнению с другими популяциями [Am. J. Resp. Cell & Mol. Biol., Nov 1997, 17(5): 583-591]. Повышенную экспрессию ММР9 наблюдали также при некоторых других патологических состояниях, и эти наблюдения свидетельствуют о том, что ММР9 вовлечена в такие болезненные процессы, как ХОБЛ, артрит, метастазирование опухолей, болезнь Альцгеймера, рассеянный склероз и перфорация бляшек при атеросклерозе, приводящая к острым коронарным состояниям, таким как инфаркт миокарда.
ММР-8 (коллагеназа-2, нейтрофильная коллагеназа) представляет собой фермент 53 кД семейства матриксных металлопротеаз, которые преимущественно экспрессируются в нейтрофилах. Последние исследования указывают на то, что ММР-8 экспрессируется также в других клетках, таких как остеоартритные хондроциты [Shlopov et al., 1997, Arthritis Rheum, 40: 2065]. ММР, продуцируемые нейтрофилами, могут вызывать ремоделирование тканей. Следовательно, блокирование ММР-8 может оказывать положительный эффект при фиброзных заболеваниях, например, легкого и при дегенеративных заболеваниях, подобных эмфиземе легких. Обнаружена также положительная регуляция ММР-8 при остеоартрите, указывающая на то, что блокирование ММР-8 также может быть полезным при этом заболевании.
ММР-3 (стромелизин-1) представляет собой фермент 53 кД семейства матриксных металлопротеаз. Активность ММР-3 была продемонстрирована в фибробластах, выделенных из воспаленной десны [Uitto V. J. et al., 1981, J. Periodontal Res., 16: 417-424], и было показано, что уровни фермента коррелируют с тяжестью заболевания десны [Overall С. М. et al., 1987, J. Periodontal Res., 22: 81-88]. ММР-3 продуцируется также базальными кератиноцитами при различных хронических язвах [Saarialho-Kere U. К. et al., 1994, J. Clin. Invest. 94: 79-88]. мРНК и белок ММР-3 были обнаружены в базальных кератиноцитах рядом с краем раны, но дистально от него, где вероятно имеются сайты пролиферирующего эпидермиса. Таким образом, ММР-3 может препятствовать заживлению эпидермиса. Несколько исследователей продемонстрировали стойкое повышение ММР-3 в синовиальных жидкостях пациентов с ревматоидным и остеоартритом по сравнению с контролями [Walakovits L. А. et al., 1992, Arthritis Rheum., 35: 35-42; Zafarullah M. et al., 1993, J. Rheumatol. 20: 693-697]. Эти исследования дают основание полагать, что ингибитор ММР-3 будет лечить заболевания, в которые вовлечено разрушение внеклеточного матрикса, приводящее к воспалению вследствие инфильтрации лимфоцитов или к потере структурной целостности, необходимой для функционирования органа.
Известно множество ингибиторов металлопротеиназ (см., например, обзор по ингибиторам ММР Beckett R. P. and Whittaker M., 1998, Exp. Opin. Ther. Patents, 8(3): 259-282). Разные классы соединений могут иметь разные степени эффективности и избирательности в отношении ингибирования различных металлопротеиназ.
Whittaker M. et al. [1999, Chemical Reviews 99(9): 2735-2776] рассматривают целый ряд известных соединений-ингибиторов ММР. Они утверждают, что эффективному ингибитору ММР необходима связывающая цинк группа (ZBG) (функциональная группа, способная хелатировать ион цинка(II) в активном сайте), по меньшей мере одна функциональная группа, которая обеспечивает взаимодействие водородной связи с основной цепью фермента, и одна или более чем одна боковая цепь, которая подвергается эффективным Ван-дер-Ваальсовым взаимодействиям с подсайтами фермента. В известных ингибиторах ММР связывающие цинк группы включают карбоновокислотные группы, гидроксамовокислотные группы, сульфгидрильные или меркаптогруппы и т.д. Например, Whittaker M. et al. обсуждают следующие ингибиторы ММР.
Приведенное выше соединение вошло в стадию клинической разработки. Оно имеет меркаптоацильную связывающую цинк группу, триметилгидантоинилэтильную группу в положении Р1 и лейцинил-трет-бутилглициниловую основную цепь.
Приведенное выше соединение имеет меркаптоацильную связывающую цинк группу и имидную группу в положении Р1.
Приведенное выше соединение разработано для лечения артрита. Оно имеет непептидную сукцинилгидроксаматную связывающую цинк группу и триметилгидантоинилэтильную группу в положении Р1.
Приведенное выше соединение представляет собой фталимидопроизводное, которое ингибирует коллагеназы. Оно имеет непептидную сукцинилгидроксаматную связывающую цинк группу и циклическую имидную группу в положении Р1.
Whittaker M. et al. также обсуждают другие ингибиторы ММР, имеющие Р1 циклическую имидогруппу и различные связывающие цинк группы (сукцинилгидроксаматную, карбоновокислотную, тиоловую группу, группу на основе фосфора).
Приведенные выше соединения представляются хорошими ингибиторами ММР8 и ММР9 (РСТ заявки WO 9858925, WO 9858915). Они имеют пиримидин-2,3,4-трионовую связывающую цинк группу.
Указанные ниже соединения не известны как ингибиторы ММР.
Lora-Tamayo M. et al. (1968, An. Quim 64(6): 591-606) описывают синтез указанных ниже соединений как потенциальных противораковых агентов:
В патентах Чехии №№151744 (19731119) и 152617 (1974022) описаны синтез и противосудорожная активность следующих соединений:
R=4-NO2, 4-OMe, 2-NO2.
В патенте США №3529019 (19700915) описаны указанные ниже соединения, используемые в качестве промежуточных соединений:
В РСТ заявке WO 00/09103 описаны соединения, полезные для лечения расстройства зрения, в том числе следующие (соединения 81 и 83, таблица А, с.47):
Теперь авторы изобретения открыли новый класс соединений, которые являются ингибиторами металлопротеиназ и представляют особый интерес при ингибировании таких ММР, как ММР-12. Эти соединения являются ингибиторами металлопротеиназ, имеющими связывающую металл группу, которая не обнаружена в известных ингибиторах металлопротеиназ. В частности, авторы изобретения открыли соединения, которые являются эффективными ингибиторами ММР-12 и обладают желательными профилями активности. Соединения по данному изобретению обладают благоприятными эффективностью, избирательностью и/или фармакокинетическими свойствами.
Соединения по данному изобретению, представляющие собой ингибиторы металлопротеиназ, содержат связывающую металл группу и одну или более чем одну функциональную группу или боковую цепь, отличаются тем, что связывающая металл группа имеет формулу (k)
где Х выбран из NR1, О, S;
Y1 и Y2 независимо выбраны из О, S;
R1 выбран из Н, алкила, галогеноалкила;
любые алкильные группы, упомянутые выше, могут быть прямоцепочечными или разветвленными; любая алкильная группа, упомянутая выше, предпочтительно представляет собой (С1-7)алкил и наиболее предпочтительно (С1-6) алкил.
Соединение, представляющее собой ингибитор металлопротеиназ, является соединением, которое ингибирует активность фермента, представляющего собой металлопротеиназу (например ММР). В качестве не ограничивающего примера соединение-ингибитор может показывать IC50 in vitro в диапазоне 0,1-10000 наномоль, предпочтительно 0,1-1000 наномоль.
Связывающая металл группа представляет собой функциональную группу, способную связывать ион металла в активном сайте фермента. Например, связывающая металл группа будет представлять собой связывающую цинк группу в ингибиторах ММР, связывающую ион цинка(II) в активном сайте. Связывающая металл группа формулы (k) основана на пятичленной кольцевой структуре и предпочтительно представляет собой гидантоиновую группу, наиболее предпочтительно 5-замещенный 1-Н,3-Н-имидазолидин-2,4-дион.
Таким образом, в первом аспекте изобретения предложены соединения формулы I
где X выбран из NR1, О, S;
Y1 и Y2 независимо выбраны из О, S;
Z выбран из SO, SO2;
m равно 1 или 2;
А выбран из прямой связи, (С1-6)алкила, (С1-6)галогеноалкила или (С1-6)гетероалкила, содержащего гетерогруппу, выбранную из N, О, S, SO, SO2, или содержащего две гетерогруппы, выбранные из N, О, S, SO, SO2 и разделенные по меньшей мере двумя атомами углерода;
R1 выбран из Н, (С1-3)алкила, галогеноалкила;
R2 и R3 каждый независимо выбран из Н, галогена (предпочтительно фтора), алкила, гетероалкила, циклоалкила, гетероциклоалкила, арила, гетероарила, алкиларила, алкилгетеро-арила, гетероалкил-арила, гетероалкил-гетероарила, арил-алкила, арил-гетероалкила, гетероарил-алкила, гетероарил-гетероалкила, арил-арила, арил-гетероарила, гетероарил-арила, гетероарил-гетероарила, циклоалкил-алкила, гетероциклоалкил-алкила, алкил-циклоалкила, алкил-гетероциклоалкила;
каждый R4 независимо выбран из Н, галогена (предпочтительно фтора), (С1-3)алкила или галогеноалкила;
каждый из радикалов R2 и R3 независимо возможно может быть замещен одной или более чем одной (предпочтительно одной) группой, выбранной из алкила, гетероалкила, арила, гетероарила, галогено, галогеноалкила, гидрокси, алкокси, галогеноалкокси, тиола, алкилтиола, арилтиола, алкилсульфона, галогеноалкилсульфона, арилсульфона, аминосульфона, N-алкиламиносульфона, N,N-диалкиламиносульфона, ариламиносульфона, амино, N-алкиламино, N,N-диалкиламино, амидо, N-алкиламидо, N,N-диалкиламидо, циано, сульфонамино, алкилсульфонамино, арилсульфонамино, амидино, N-аминосульфон-амидино, гуанидино, N-циано-гуанидино, тиогуанидино, 2-нитро-этен-1,1-диамина, карбокси, алкил-карбокси, нитро, карбамата;
R2 и R3 возможно могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R2 и R4 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R3 и R4 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов;
R5 представляет собой моноциклическую, бициклическую или трициклическую группу, содержащую одну, две или три кольцевые структуры, каждая из которых содержит вплоть до 7 кольцевых атомов, независимо выбранных из циклоалкила, арила, гетероциклоалкила или гетероарила, причем каждая кольцевая структура независимо возможно замещена одним или более чем одним заместителем, независимо выбранным из галогена, гидрокси, алкила, алкокси, галогеноалкокси, амино, N-алкиламино, N,N-диалкиламино, алкилсульфонамино, алкилкарбоксиамино, циано, нитро, тиола, алкилтиола, алкилсульфонила, галогеноалкилсульфонила, алкиламиносульфонила, карбоксилата, алкилкарбоксилата, аминокарбокси, N-алкиламино-карбокси, N,N-диалкиламино-карбокси, где любой алкильный радикал в пределах любого заместителя сам возможно может быть замещен одной или более чем одной группой, выбранной из галогена, гидрокси, алкокси, галогеноалкокси, амино, N-алкиламино, N,N-диалкиламино, N-алкилсульфонамино, N-алкилкарбоксиамино, циано, нитро, тиола, алкилтиола, алкилсульфонила, N-алкиламиносульфонила, карбоксилата, алкилкарбокси, аминокарбокси, N-алкиламинокарбокси, N,N-диалкиламинокарбокси, карбамата;
когда R5 представляет собой бициклическую или трициклическую группу, тогда каждая кольцевая структура соединена со следующей кольцевой структурой через прямую связь, через -О-, через (С1-6)алкил, через (С1-6)галогеноалкил, через (С1-6)гетероалкил, через (С1-6)алкенил, через (С1-6)алкинил, через сульфон, через СО, через NCO, через CON, через NH, через S, через С(ОН) или конденсирована со следующей кольцевой структурой;
любая гетероалкильная группа, упомянутая выше, представляет собой замещенный гетероатомом алкил, содержащий одну или более чем одну гетерогруппу, независимо выбранную из N, О, S, SO, SO2 (причем гетерогруппа представляет собой гетероатом или группу атомов);
любая гетероциклоалкильная или гетероарильная группа, упомянутая выше, содержит одну или более чем одну гетерогруппу, независимо выбранную из N, О, S, SO, SO2;
любая алкильная, алкенильная или алкинильная группа, упомянутая выше, может быть прямоцепочечной или разветвленной, если не указано иное, любая алкильная группа, упомянутая выше, предпочтительно представляет собой (С1-7)алкил и наиболее предпочтительно (С1-6)алкил.
Предпочтительными соединениями формулы I являются те, к которым применимо одно или более чем одно из указанных ниже условий:
Х представляет собой NR1;
Z представляет собой SO2 или SO, предпочтительно Z представляет собой SO2;
по меньшей мере один из Y1 и Y2 представляет собой О, особенно предпочтительно когда и Y1 и Y2 представляют собой О;
m равно 1;
R1 представляет собой Н, (С1-3)алкил, (С1-3)галогеноалкил; особенно предпочтительно R1 представляет собой Н, (С1-3)алкил; наиболее предпочтительно R1 представляет собой Н;
R2 представляет собой Н, алкил, гидроксиалкил, алкоксиалкил, арилоксиалкил, аминоалкил, циклоалкил-алкил, алкил-циклоалкил, арилалкил, алкиларил, алкил-гетероарил, гетероалкил, гетероциклоалкил-алкил, алкил-гетероциклоалкил, гетероарил-алкил, гетероалкил-арил; особенно предпочтительно R2 представляет собой алкил, аминоалкил, алкил-гетероарил, алкил-гетероциклоалкил или гетероарил-алкил;
R3 и/или R4 представляют собой Н;
R3 и/или R4 представляют собой метил;
R5 содержит одно, два или три возможно замещенных арильных или гетероарильных 5- или 6-членных кольца;
R5 представляет собой бициклическую или трициклическую группу, содержащую две или три возможно замещенные кольцевые структуры.
Особенно предпочтительными соединениями формулы I являются те, где R5 представляет собой бициклическую или трициклическую группу, содержащую две или три возможно замещенные кольцевые структуры.
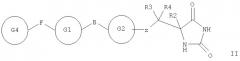
Далее в изобретении предложены соединения формулы II
где каждый из G1, G2 и G4 представляет собой моноциклическую кольцевую структуру, каждая из которых содержит вплоть до 7 кольцевых атомов, независимо выбранную из циклоалкила, арила, гетероарила, гетероциклоалкила или гетероарила, причем каждая кольцевая структура независимо возможно замещена одним заместителем или двумя заместителями, независимо выбранными из галогена, гидрокси, галогеноалкокси, амино, N-алкиламино, N,N-диалкиламино, циано, нитро, алкила, алкокси, алкилсульфона, галогеноалкилсульфона, алкилкарбамата, алкиламида, где любой алкильный радикал в пределах любого заместителя может сам быть возможно замещен одной или более чем одной группой, выбранной из галогена, гидрокси, амино, N-алкиламино, N,N-диалкиламино, циано, нитро, алкокси, галогеноалкокси, арилокси, гетероарилокси, карбамата;
Z представляет собой SO2;
каждый из В и F независимо выбран из прямой связи, О, (С1-6)алкила, (С1-6)гетероалкила, алкинила, СО, NCO, CON, NH, S;
R2 выбран из Н, алкила, гидроксиалкила, алкоксиалкила, арилоксиалкила, аминоалкила, (N-алкиламино)алкила, (N,N-диалкиламино)алкила, амидоалкила, тиоалкилциклоалкил-алкила, алкил-циклоалкила, арилалкила, алкиларила, алкил-гетероарила, гетероалкила, гетероциклоалкил-алкила, алкил-гетероциклоалкила, гетероарил-алкила, гетероалкил-арила;
R3 и R4 независимо выбраны из Н или (С1-3)алкила;
R2 и R3 возможно могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R2 и R4 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R3 и R4 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов;
любая гетероалкильная группа, упомянутая выше, представляет собой замещенный гетероатомом алкил, содержащий одну или более чем одну гетерогруппу, независимо выбранную из N, О, S, SO, SO2 (причем гетерогруппа представляет собой гетероатом или группу атомов);
любая гетероциклоалкильная или гетероарильная группа, упомянутая выше, содержит одну или более чем одну гетерогруппу, независимо выбранную из N, О, S, SO, SO2;
любая алкильная, алкенильная или алкинильная группа, упомянутая выше, может быть прямоцепочечной или разветвленной, если не указано иное, любая алкильная группа, упомянутая выше, предпочтительно представляет собой (С1-7)алкил и наиболее предпочтительно (С1-6)алкил.
Предпочтительные соединения формулы II включают в себя те, где R2 представляет собой алкил, аминоалкил, алкил-гетероарил, алкил-гетероциклоалкил или гетероарил-алкил.
Далее в изобретении предложены соединения формулы IIa
где каждый из G1 и G2 представляет собой моноциклическую кольцевую структуру, каждая из которых содержит вплоть до 7 кольцевых атомов, независимо выбранную из циклоалкила, арила, гетероарила, гетероциклоалкила или гетероарила, причем каждая кольцевая структура независимо возможно замещена одним или двумя заместителями, независимо выбранными из галогена, гидрокси, галогеноалкокси, амино, N-алкиламино, N,N-диалкиламино, циано, нитро, алкила, алкокси, алкилсульфона, галогеноалкилсульфона, алкилкарбамата, аллиламида, где любой алкильный радикал в пределах любого заместителя может сам быть возможно замещен одной или более чем одной группой, выбранной из галогена, гидрокси, амино, N-алкиламино, N,N-диалкиламино, циано, нитро, алкокси, галогеноалкокси, арилокси, гетероарилокси, карбамата;
Z представляет собой SO2;
В выбран из прямой связи, О, (С1-6)алкила, (С1-6)гетероалкила, СО, NCO, CON, NH, S, алкинила;
R2 выбран из Н, (С1-6)алкила, галогеноалкила, гидроксиалкила, алкоксиалкила, аминоалкила, (N-алкиламино)алкила, (N,N-диалкиламино)алкила, амидоалкила, тиоалкила, либо R2 представляет собой группу формулы III
С и D независимо выбраны из прямой связи, Н, (С1-6)алкила, (С1-6)галогеноалкила или (С1-6)гетероалкила, содержащего один или два гетероатома, независимо выбранных из N, О или S так, что когда присутствуют два гетероатома, они разделены по меньшей мере двумя атомами углерода;
G3 представляет собой моноциклическую кольцевую структуру, содержащую вплоть до 7 кольцевых атомов, независимо выбранную из циклоалкила, арила, гетероциклоалкила или гетероарила, возможно замещенную одним или двумя заместителями, независимо выбранными из галогена, гидрокси, амино, N-алкиламино, N,N-диалкиламино, циано, нитро, алкила, алкокси, алкилсульфона, галогеноалкилсульфона или алкила, замещенного одной или более чем одной группой, выбранной из галогена, гидрокси, амино, N-алкиламино, N,N-диалкиламино, циано, нитро, алкокси, галогеноалкокси;
возможно R2 замещен галогено, галогеноалкилом, гидрокси, алкокси, галогеноалкокси, амино, аминоалкилом, N-алкиламино, N,N-диалкиламино, (N-алкиламино)алкилом, (N,N-диалкиламино)алкилом, алкилсульфоном, аминосульфоном, N-алкиламино-сульфоном, N,N-диалкиламино-сульфоном, амидо, N-алкиламидо, N,N-диалкиламидо, циано, сульфонамино, алкил-сульфонамино, амидино, N-аминосульфон-амидино, гуанидино, N-циано-гуанидино, тиогуанидино, 2-нитрогуанидино, карбокси, алкилкарбокси, карбаматом;
R3 и R4 независимо выбраны из Н или (С1-3)алкила;
возможно R2 и R3 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R2 и R4 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R3 и R4 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов;
любая гетероалкильная группа, упомянутая выше, представляет собой замещенный гетероатомом алкил, содержащий одну или более чем одну гетерогруппу, независимо выбранную из N, О, S, SO, SO2 (причем гетерогруппа представляет собой гетероатом или группу атомов);
любая гетероциклоалкильная или гетероарильная группа, упомянутая выше, содержит одну или более чем одну гетерогруппу, независимо выбранную из N, О, S, SO, SO2;
любая алкильная, алкенильная или алкинильная группа, упомянутая выше, может быть прямоцепочечной или разветвленной, если не указано иное, любая алкильная группа, упомянутая выше, предпочтительно представляет собой (С1-7)алкил и наиболее предпочтительно (С1-6)алкил.
Предпочтительными соединениями формулы IIa являются те, к которым применимо одно или более чем одно из указанных ниже условий:
В выбран из прямой связи, О, СО, S, алкинила; особенно предпочтительно В представляет собой прямую связь, О, S или алкинил;
R2 выбран из Н, (С1-6)алкила, арил-(С1-6)алкила или гетероарил-(С1-6)алкила, возможно замещенных галогено, галогеноалкилом, гидрокси, алкокси, галогеноалкокси, амино, аминоалкилом, N-алкиламино, N,N-диалкиламино, (N-алкиламино)алкилом, (N,N-диалкиламино)алкилом, алкилсульфоном, аминосульфоном, N-алкиламино-сульфоном, N,N-диалкиламино-сульфоном, амидо, N-алкиламидо, N,N-диалкиламидо, карбаматом, циано, сульфонамино, алкил-сульфонамино, амидино, N-аминосульфон-амидино, гуанидино, N-циано-гуанидино, тиогуанидино, 2-нитрогуанидино, 2-нитро-этен-1,1-диамино, карбокси, алкилкарбокси, карбаматом;
каждый из R3 и R4 представляет собой Н;
G2 представляет собой азотсодержащее шестичленное кольцо;
G1 является пара-замещенным.
Особенно предпочтительными соединениями формулы IIa являются те, где каждый из R3 и R4 представляет собой Н.
Например, конкретные соединения по изобретению включают в себя соединения формулы IIa, где В представляет собой прямую связь, О, S или алкинил, и R2 выбран из Н, (С1-6)алкила, арил-(С1-6)алкила или гетероарил-(С1-6)алкила, возможно замещенных циклоалкилом, гетероциклоалкилом, галогено, галогеноалкилом, гидрокси, алкокси, арилокси, галогеноалкокси, амино, аминоалкилом, N-алкиламино, N,N-диалкиламино, (N-алкиламино)алкилом, (N,N-диалкиламино)алкилом, алкилсульфонилом, аминосульфонилом, N-алкиламино-сульфонилом, N,N-диалкиламино-сульфонилом, амидо, N-алкиламидо, N,N-диалкиламидо, циано, сульфонамино, алкил-сульфонамино, амидино, N-аминосульфон-амидино, гуанидино, N-циано-гуанидино, тиогуанидино, 2-нитрогуанидино, карбаматом, карбокси, алкилкарбокси, и каждый из R3 и R4 представляет собой Н.
Особенно предпочтительными соединениями по изобретению являются соединения формулы IIb:
где G2 представляет собой возможно замещенный пиперидин или пиперазин, a G1, В и R2 являются такими, как описано для формулы IIa.
В соединении формулы IIb предпочтительно G2 не замещен, a G1 возможно замещен, предпочтительно G1 является пара-замещенным.
Подходящие значения для R2 включают указанные ниже:
Подходящие значения для R5 включают указанные ниже:
X'=связь, О, СН2, CHF, CF2, S, SO2, СО;
X"=связь, СН2, CHF, CF2, SO2, СО;
R=F, Cl, Br, CF3, CF3O, СН3О, ОН, CF3CH2.
Должно быть понятно, что конкретные заместители и количество заместителей в соединениях по изобретению выбраны таким образом, чтобы избежать стерически нежелательных комбинаций.
Каждое проиллюстрированное примером соединение представляет собой конкретный и независимый аспект изобретения.
Если в соединениях по изобретению имеются оптически активные центры, авторы изобретения раскрывают все индивидуальные оптически активные формы и их комбинации как индивидуальные конкретные воплощения изобретения, также как и их соответствующие рацематы. Рацематы могут быть разделены на индивидуальные оптически активные формы с использованием известных методик (см. Advanced Organic Chemistry: 3rd Edition: author J March, p104-107), включая, например, образование диастереомерных производных, имеющих подходящие оптически активные вспомогательные группы, с последующим разделением, а затем отщеплением этих вспомогательных групп.
Должно быть поня