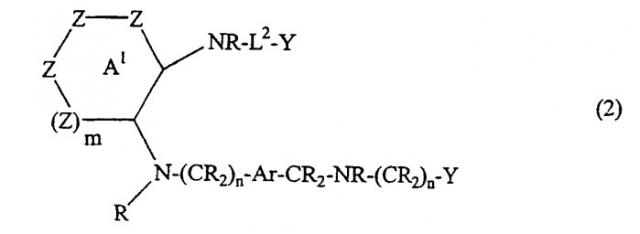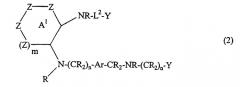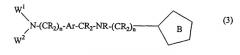Гетероциклические соединения, содержащая их фармацевтическая композиция и их применение
Иллюстрации
Показать всеИзобретение относится к соединениям формулы
и их солям, где кольцо А необязательно содержит гетероатом О; пунктирные линии представляют необязательную ненасыщенность; R1 представляет С1-4 алкокси; R2 и R3 независимо представляют Н, необязательно галогенированный C1-C4 алкил, необязательно замещенную ароматическую группу или R2 и R3 вместе могут образовывать замещенное или незамещенное 5-7-членное кольцо, конденсированное с кольцом Е; k равно 0-4; L1 представляет ковалентную связь или C1-С6 алкил, необязательно содержащий N; Х представляет незамещенный или замещенный С или N или представляет О или S; Ar представляет фенилен; каждый n независимо равен 0-2; каждый R независимо представляет Н или алкил (1-6С) и Y представляет необязательно замещенную ароматическую или гетероароматическую группу или 5-11-членную гетероциклическую группу, содержащую 1-4 гетероатома, выбранных из N, О и S, которые связываются с хемокиновыми рецепторами, включающими CXCR4 и CCR5, и проявляют защитное действие против поражения клеток-мишеней вирусом иммунодефицита человека (ВИЧ, HIV). 3 н. и 15 з.п. ф-лы, 1 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к новым соединениям, фармацевтическим композициям и их применению. В частности, настоящее изобретение касается новых гетероциклических соединений, которые связываются с хемокиновыми рецепторами, включающими CXCR4 и CCR5, и проявляют защитное действие против поражения клеток-мишеней вирусом иммунодефицита человека (ВИЧ, HIV).
Предпосылки создания изобретения
Известно примерно 40 хемокинов человека, которые действуют, по крайней мере частично модулируя сложный перекрывающийся набор биологических активностей, важных для передвижения лимфоидных клеток и экстравазации и тканевой инфильтрации лейкоцитов в ответ на действие стимулирующих веществ (см., например, Р.Ponath, Exp. Opin. Invest. Drugs, 7:1-18, 1998; Baggiolini M. Nature 392, 565-568 (1998); Locati et al. Annu. Rev. Med. 50, 425-40 (1999)). Указанные хемотаксические цитокины, или хемокины, образуют семейство белков размером приблизительно 8-10 кДа. Хемокины, видимо, составляют часть общей структурной цепи, состоящей из 4 сохраненных цистеинов, участвующих в поддержании третичной структуры. Существуют два основных подсемейства хемокинов: «СС», или β-хемокины, и «СХС», или α-хемокины. Рецепторы указанных хемокинов классифицируют по хемокину, составляющему естественный лиганд рецептора. Рецепторы β-хемокинов имеют обозначение «CCR», а рецепторы α-хемокинов «CXCR».
Считается, что хемокины являются основными медиаторами в инициировании и поддержании воспаления (см. Chemokines in Disease published by Humana Press (1999), Edited by C. Herbert; Murdoch et al. Blood 95, 3032-3043 (2000)). В частности, обнаружено, что хемокины играют важную роль в регуляции функции эндотелиальных клеток, включая пролиферацию, миграцию и дифференцировку при ангиогенезе и повторной эндотелиализации после повреждения (Gupta et al. J. Biol. Chem., 7:4282-4287 (1998); Volin et al. Biochem. Biophys Res. Commun. 242, 46-53 (1998)). Два специфических хемокина причастны к этиологии заражения вирусом иммунодефицита человека (ВИЧ).
В большинстве случаев ВИЧ сначала связывается через белок своей оболочки gp120 с CD4 рецептором клетки-мишени. По-видимому, в gp120 происходит конформационное изменение, которое приводит к последующему связыванию оболочки с хемокиновым рецептором, таким как CCR5 (Wyatt et al. Science, 280:1884-1888 (1998); Rizzuto et al. Science, 280:1949-1953 (1998); Berger et al. Annu. Rev. Immunol. 17: 657-700 (1999)). Изоляты ВИЧ-1, появляющиеся при последующем инфицировании, связываются с хемокиновым рецептором CXCR4.
После начального связывания ВИЧ с CD4 происходит слияние вируса с клеткой, опосредованное членами семейства хемокиновых рецепторов, причем в качестве кофакторов связывания для тропных к макрофагу (М-тропных) и тропных к Т-клеточной линии (Т-тропных) изолятов ВИЧ-1 служат разные члены (Carroll et al. Science, 276: 273-276 1997; Feng et al. Science 272, 872-877 (1996); Bleul et al. Nature 382, 829-833 (1996); Oberlin et al. Nature 382, 833-835 (1996); Cocchi et al. Science 270, 1811-1815 (1995); Dragic et al. Nature 381, 667-673 (1996); Deng et al. Nature 381, 661-666 (1996); Alkhatib et al. Science 272, 1955-1958, 1996). В ходе инфицирования организма больного, по-видимому, происходит сдвиг большинства ВИЧ-частиц от М-тропного до более патогенного, Т-тропного, вирусного фенотипа (Blaak et al. Proc. Natl. Acad. Sci. 97, 1269-1274 (2000); Miedema et al. Immune. Rev., 140:35 (1994); Simmonds et al. J. Virol. 70, 8355-8360 (1996); Tersmette et al. J. Virol. 62, 2026-2032 (1988); Connor R. I., Ho D. D. J. Virol. 68, 4400-4408 (1994); Schuitemaker et al. J. Virol. 66, 1354-1360 (1992)). М-тропный вирусный фенотип находится в соответствии со способностью вируса проникать в клетку после связывания с CCR5 рецептором, а Т-тропный вирусный фенотип находится в соответствии с проникновением вируса в клетку после связывания и мембранного слияния с CХCR5 рецептором. Клинические наблюдения заставляют думать, что пациенты, обладающие генетическими мутациями в CCR5, являются стойкими к ВИЧ-инфекции и менее подвержены ей (Liu et al. Cell 86, 367-377 (1996); Samson et al. Nature 382, 722-725 (1996); Michael et al. Nature Med. 3, 338-340 (1997); Michael et al. J. Virol. 72, 6040-6047 (1998); Obrien et al. Lancet 349, 1219 (1997); Zhang et al. AIDS Res. Hum. Retroviruses 13, 1357-1366 (1997); Rana et al. J. Virol. 71, 3219-3227 (1997); Theodorou et al. Lancet 349, 1219-1220 (1997). Несмотря на большое число хемокиновых рецепторов, которые уже описаны как посредники проникновения ВИЧ в клетки, CCR5 и CXCR4, по-видимому, являются лишь физиологически приемлемыми корецепторами, используемыми в самых разнообразных первичных клинических штаммах ВИЧ-1 (Zhang et al. J. Virol. 72, 9307-9312 (1998); Zhang et al. J. Virol. 73, 3443-3448 (1999); Simmonds et al. J. Virol. 72, 8453-8457 (1988)). Слияние и проникновение Т-тропных вирусов, которые используют CXCR4, ингибирует натуральный СХС-хемокиновый фактор-1, произведенный от стромальной клетки, а слияние и проникновение М-тропных вирусов, которые используют CCR5, ингибируют естественные СС-хемокины, а именно белки, отрегулированные при активации естественной Т-клетки, экспрессированные и секретированные (Regulated on Activation Normal T-cell Expressed and Secreted (RANTES)), и белки макрофага воспалительного (Macrophage Inflammatory proteins) (MIP-1 альфа и бета).
Кроме действия как кофактора для проникновения ВИЧ, уже было описано недавно непосредственное взаимодействие gp120 вируса с CXCR4 как возможной причины апоптоза Т-клеток CD8+ и связанной со СПИД деменции вследствие индукции апоптоза нервных клеток (Hesselgesser et al. Curr. Biol. 8, 595-598 (1998); Hesselgesser et al. Curr. Biol. 7, 112-121 (1997); Hesselgesser et al. "Chemokines and Chemokine receptors in the Brain" in Cheniokines in Disease published by Humana Press (1999), Edited by C. Herbert; Herbein et al. Nature 395, 189-194 (1998); Buttini et al. Nature Med. 4, 441-446 (1998); Ohagen et al. J. Virol. 73, 897-906 (1999); Biard-Piechaczyk et al. Virology 268, 329-344 (2000); Sanders et al. J. Neuroscience Res. 59, 671-679 (2000); Bajetto et al. J. Neurochem. 73, 2348-2357 (1999); Zheng et al. J. Virol. 73, 8256-8267 (1999)).
Однако связывание хемокиновых рецепторов с их естественными лигандами, по-видимому, играет более эволюционную и важную роль, чем опосредование ВИЧ-инфекции. Связывание естественного лиганда, пре-В-клетки ростстимулирующий фактор/стромальной клетки производный фактор (PBSF/SDF-1), с CXCR4 хемокиновым рецептором создает важный сигнальный механизм: мыши, лишенные CXCR4 или SDF-1, имеют нарушения в головном мозге, сердце и желудочно-кишечном тракте и умирают in utero (Zou et al. Nature, 393:591-594 (1998); Tachibana et al. Nature, 393:591-594 (1998); Nagasawa et al. Nature 382, 635-638 (1996)). У мышей, лишенных CXCR4, проявляются также гемопоэтические дефекты (Nagasawa et al. Nature 382, 635-638 (1996)); миграция CXCR4 экспрессирующих лейкоцитов и гемопоэтических прародителей к SDF-1, по-видимому, является важной для поддержания последовательности поколений В-клеток и локализации CD34+ прародительских клеток в костном мозге (Bleul et al. J. Exp. Med. 187, 753-762 (1998); Viardot et al. Ann. Hematol. 77, 195-197 (1998); Auiti et al. J. Exp. Med. 185, 111-120 (1997); Peled et al. Science 283, 845-848 (1999); Qing et al. Immunity 10, 463-471 (1999); Lataillade et al. Blood 95, 756-768 (1999); Ishii et al. J. Immunol 163, 3612-3620 (1999); Maekawa et al. Internal Medicine 39, 90-100 (2000); Fedyk et al. J. Leukocyte Biol. 66, 667-673 (1999); Peled et al. Blood 95, 3289-3296 (2000)).
Сигнал, вырабатываемый SDF-1 при связывании с CXCR4, может также играть важную роль в пролиферации опухолевых клеток и регуляции ангиогенеза, связанного с ростом опухоли (см. "Chemokines and Cancer" published by Humana Press (1999); Edited by B. J. Rollins; Arenburg et al. J. Leukocyte Biol. 62, 554-562 (1997); Moore et al. J. Invest. Med. 46, 113-120 (1998); Moore et al. Trends cardiovasc. Med. 8, 51-58 (1998); Seghal et al. J. Surg. Oncol. 69, 99-104 (1998)); известные ангиогенные факторы роста VEG-F и bFGF регулируют вверхние уровни CXCR4 в эндотелиальных клетках, и SDF-1 может вызывать реваскуляризацию in vivo (Salcedo et al. Am. J. Pathol. 154, 1125-1135 (1999)); лейкозные клетки, которые экспрессируют CXCR4, мигрируют и прикрепляются к стромальным клеткам лимфатических узлов и костного мозга, экспрессирующим SDF-1 (Burger et al. Blood 94, 3658-3667 (1999); Arai et al. Eur. J. Haematol. 64, 323-332 (2000); Bradstock et al. Leukemia 14, 882-888 (2000)).
Связывание SDF-1 с CXCR4 причастно также к патогенезу атеросклероза (Abi-Younes et al. Circ. Res. 86, 131-138 (2000)), отторжению почечного аллотрансплантата (Eitner et al. Transplantation 66, 1551-1557 (1998)), астме и аллергическому воспалению дыхательных путей (Yssel et al. Clinical and Experimental Allergy 28, 104-109 (1998); J. Immunol. 164, 5935-5943 (2000); Gonzalo et al. J. Immunol. 165, 499-508 (2000)), болезни Альцгеймера (Xia et al. J. Neurovirology 5, 32-41 (1999)) и артриту (Nanki et al. J. Immunol. 164, 5010-5014 (2000)).
В попытке лучше понять взаимозависимость между хемокинами и их рецепторами недавно были проведены эксперименты по блокированию слияния, проникновения и репликации ВИЧ через CXCR4 хемокиновый рецептор путем применения моноклональных антител или малых молекул, что, видимо, считается обычной терапевтической стратегией (Schols et al. J. Exp. Med. 186: 1383-1388 (1997); Schols et al. Antiviral Research 35:147-156 (1997); Bridger et al. J. Med. Chem. 42, 3971-3981 (1999); Bridger et al. "Bicyclam Derivatives as HIV Inhibitors" in Advances in Antiviral Drug Design Volume 3, p161-229; Published by JAI press (1999); Edited by E. De Clercq). Малые молекулы, такие как бицикламы, по-видимому, специфически связываются с CXCR4 и не связываются с CCR5 (Donzella et al. Nature Medicine, 4:72-77 (1998)). Указанные эксперименты показали наличие препятствия мембранному слиянию и проникновению ВИЧ в клетку-мишень in vitro. Позже было также показано, что бицикламы ингибируют слияние и репликацию вируса иммунодефицита кошки (ВИК, FIV), который использует для проникновения CXCR4 (Egberink et al. J. Virol. 73, 6346-6352 (1999)).
Дополнительные эксперименты показали, что бициклам в зависимости от дозы ингибирует связывание 125I-меченого SDF-1 c CXCR4 и передачу сигнала (на что показывает увеличение содержания внутриклеточного кальция) в ответ на SDF-1. Таким образом, бициклам также действует как антагонист передачи сигнала, происходящей в результате связывания естественного хемокина в виде стромального производного фактора, SDF-1α, с CXCR4. Бицикламы ингибируют также апоптоз, вызванный ВИЧ gp120 (оболочка) в не-ВИЧ-инфицированных клетках (Blanco et al. Antimicrobial Agents and Chemother. 44, 51-56 (2000)).
В патентах США №№ 5583131, 5698546, 5817807, 5021409 и 6001826, которые полностью включены в данное описание путем ссылки, раскрыты циклические соединения, которые проявили активность против ВИЧ-1 и ВИЧ-2 при испытаниях in vitro. Затем было открыто и дополнительно описано в одновременно рассматриваемых заявках №09/111895 и №60/172153 на патент США, что указанные соединения проявляют активность против ВИЧ, связываясь с хемокиновым рецептором CXCR4, выявленном на поверхности некоторых клеток иммунной системы. Таким образом, данное конкурентное связывание защищает указанные клетки-мишени от поражения ВИЧ, который использует для проникновения рецептор CXCR4. Кроме того, указанные соединения являются антагонистами связывания, сигнализации и хемотаксических эффектов естественного лиганда для CXCR4, производного от стромальных клеток хемокинового фактора 1α (SDF-1). Создатели настоящего изобретения дополнительно раскрыли, что указанные новые соединения проявляют защитные эффекты против ВИЧ-заражения клеток-мишеней, связываясь in vitro с рецептором CCR5.
Кроме того, данными заявителями в заявке №09/495298 на патент США было раскрыто, что указанные циклические полиаминные противовирусные средства, описанные в указанных выше патентах, обладают эффектом повышения продуцирования лейкоцитов, а также противовирусными свойствами. Поэтому указанные средства полезны для борьбы с побочными эффектами химиотерапии, повышения возможности удачной трансплантации костного мозга, повышения возможности излечения ран и лечения ожогов и борьбы с бактериальными инфекциями при лейкозе.
Позже данными заявителями был раскрыт в заявке № 09/535314 на патент США ряд гетероциклических соединений, которые проявляют активность против ВИЧ, связываясь с хемокиновыми рецепторами CXCR4 и CCR5, выявленными на поверхности некоторых клеток иммунной системы. Таким образом, данное конкурентное связывание защищает указанные клетки-мишени от заражения ВИЧ, который использует для проникновения рецепторы CXCR4 или CCR5. Кроме того, указанные соединения являются антагонистами связывания, сигнализации и хемотаксических эффектов естественного лиганда для CXCR4, производного от стромальных клеток хемокинового фактора 1α (SDF-1), и/или естественного лиганда для CCR5, хемокина RANTES.
В настоящем изобретении заявителями раскрыты новые соединения, которые проявляют защитные эффекты против ВИЧ-инфекции клеток-мишеней, связываясь с хемокиновым рецептором CXCR4 или CCR5 подобно ранее описанным макроциклическим соединениям. Кроме того, указанные соединения являются антагонистами связывания, сигнализации и хемотаксических эффектов естественного лиганда для CXCR4, производного от стромальных клеток хемокинового фактора 1α (SDF-1), и/или естественного лиганда для CCR5, хемокина RANTES.
Цитирование указанных выше документов не следует считать как признание, что любой из них является относящимся к предмету заявки. Все указания, касающиеся даты или представления указанных документов, основаны на информации, доступной заявителям, и не являются признанием, касающимся правильности дат или содержания указанных документов. Кроме того, все приведенные публикации включены в данное описание в качестве ссылки во всей своей полноте.
Краткое изложение сущности изобретения
В соответствии с настоящим изобретением предлагаются новые соединения, которые связываются с хемокиновыми рецепторами и препятствуют связыванию с указанными рецепторами естественного лиганда. Соединения по настоящему изобретению полезны как средства защиты клеток-мишеней от ВИЧ-инфекции. Другими вариантами настоящего изобретения являются соединения, действующие как антагонисты или агонисты хемокиновых рецепторов, а также обладающие другими биологическими активностями, связанными со способностью указанных соединений ингибировать связывание хемокинов с их рецепторами.
Соединения по настоящему изобретению представляют собой соединения формул 1-4, включая их фармацевтически приемлемые соли и пролекарства. Соединения формулы (1) являются соединениями формулы
где кольцо А необязательно содержит гетероатом, выбранный из N, O или S;
пунктирные линии представляют необязательную ненасыщенность;
R1, R2 и R3 представляют заместители, не создающие препятствий;
k равно 0-4;
m равно 0-2;
L1 представляет связующее звено 1,5-10 Å;
Х представляет незамещенный или замещенный С или N или представляет О или S;
Ar представляет остаток ароматического фрагмента;
каждый n независимо равен 0-2;
каждый R независимо представляет Н или алкил (1-6С) и
Y представляет ароматическую или гетероароматическую или другую гетероциклическую группу.
Предпочтительно набор соединений формулы 1 исключает следующие соединения:
AMD7186: N-(5-этилтиофен-2-илметил)-N'-(2-пиридинилметил)-N-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD7208: N-(1-метилпиррол-2-илметил)-N'-(2-пиридинилметил)-N-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD7222: N-(1-метилбензимидазол-2-илметил)-N'-(2-пиридинилметил)-N-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8780: N-(2-пиридинилметил)-N'-(транс-2-аминоциклогексил)-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин (гидробромидная соль),
AMD8931: N-(2-пиридинилметил)-N-(4-фенил-1Н-имидазол-2-илметил)-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8821: N-(2-пиридинилметил)-N'-[2-фуранилметил]-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8828: N-(2-пиридинилметил)-N'-[2-[(2-фуранилметил)амино]этил]-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8835: N-(2-пиридинилметил)-N'-[2-[(1Н-имидазол-2-илметил)амино]этил]-N'-(1,2,3,4-тетрагидро-1-нафталинил)-1,4-бензолдиметанамин,
AMD8836: N-(2-пиридинилметил)-N'-[2-тиофенилметил]-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8839: N-(2-пиридинилметил)-N'-(транс-2-аминоциклопентил)-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8841: N-(2-пиридинилметил)-N'-[2-тиазолилметил]-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8751: N-(2-пиридинилметил)-N'-(1Н-имидазол-2-илметил)-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8887: N-(2-пиридинилметил)-N'-[2-[(1Н-имидазол-2-илметил)амино]этил]-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8728: N-(2-пиридинилметил)-N'-[2-пирролилметил]-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8907: N-(2-пиридинилметил)-N'-(1Н-бензимидазол-2-илметил]-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8926: N-(2-пиридинилметил)-N'-(5-нитро-1Н-бензимидазол-2-илметил]-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8927: N-(2-пиридинилметил)-N'-(5,6-диметил-1Н-бензимидазол-2-илметил]-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
AMD8929: N-(2-пиридинилметил)-N'-[(1Н)-5-азабензимидазол-2-илметил]-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин и
AMD8764: N-(2-пиридинилметил)-N'-(2-бензоксазолил)-N'-(5,6,7,8-тетрагидро-8-хинолинил)-1,4-бензолдиметанамин,
которые раскрыты в первичной заявке РСТ/СА00/00321.
Соединения формулы 2 являются соединениями формулы
где R, m, n, Ar и каждый Y, такой, как определено для формулы 1;
каждый Z независимо представляет CR2, NR, О или S, при условии, что только два Z могут быть отличными от CR2, и
L2 представляет связующее звено 1,5-8 Å.
Соединения формулы 3 являются соединениями формулы
где W1 представляет моноциклическую (5-6-членную) или конденсированную бициклическую (8-12-членную) незамещенную или замещенную кольцевую систему, содержащую по крайней мере один гетероатом, выбранный из N, O и S;
W2 представляет Н или выбран из группы, состоящей из необязательно замещенной С1-6 алкильной группы; С0-6 алкильной группы, замещенной необязательно замещенной ароматической или гетероциклической группы; необязательно замещенной С0-6 алкиламино- или С3-7 циклоалкиламиногруппы и необязательно замещенной карбонильной или сульфонильной группы;
Ar, R и n, такие, как определено для формулы 1, и
представляет насыщенное или ненасыщенное 5-членное кольцо, содержащее 1-2 гетероатома, выбранных из N, O или S.
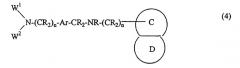
Соединения формулы 4 являются соединениями формулы
где W1 и W2, такие, как определено для формулы 3,
Ar, R и n, такие, как определенные для формулы 1, и
представляет конденсированную кольцевую систему из 10 членов, необязательно содержащую 1 или 2 гетероатома, выбранных из N, O и S.
Необязательные заместители определены ниже.
Одним из объектов настоящего изобретения является фармацевтическая композиция, содержащая терапевтически эффективное количество соединения формул 1-4. Другим его объектом является способ лечения человека или других млекопитающих, включающий введение указанной фармацевтической композиции. Еще одним объектом является способ воспрепятствования связыванию хемокинового рецептора с его естественным лигандом, включающий осуществление контактирования указанного хемокинового рецептора с эффективным количеством соединения формул 1-4.
И еще одним объектом является применение соединения формул 1-4 для изготовления лекарственного средства для лечения заболевания, при котором целесообразно воспрепятствование связыванию хемокинового рецептора с его естественным лигандом, включающее, например, составление композиции, содержащей терапевтически эффективное количество соединения формул 1-4. Настоящее изобретение охватывает способ защиты клеток-мишеней, обладающих хемокиновыми рецепторами, связывание с которыми патогенного агента приводит к заболеванию или патологии, включающий введение млекопитающему фармацевтической композиции, содержащей терапевтически эффективное количество соединения формул 1-4.
Настоящее изобретение включает также «пролекарственные» формы, то есть защищенные формы соединений, которые высвобождают соединение после введения пациенту. Например, соединение может иметь защитные группы, которые отщепляются в результате гидролиза в жидкостях организма, например в кровотоке, высвобождая тем самым активное соединение, или окисляются или восстанавливаются в жидкостях организма с высвобождением соединения. Описание пролекарств можно найти в «Smith and Williams` Introduction to the Principles of Drug Design», H. J. Smith, Wright, Second Edition, London 1988.
Настоящее изобретение охватывает также фармацевтически приемлемые кислотно-аддитивные соли, такие как соль с неорганическим основанием, соль с органическим основанием, соль с неорганической кислотой, соль с органической кислотой, соль с основной или кислотной аминокислотой и т.д. Примеры соли с неорганическим основанием включают соль с щелочным металлом (например, натрием, калием и т.д.), щелочноземельным металлом (например, кальцием, магнием и т.д.), алюминием, аммонием и т.д. Примеры соли с органическим основанием включают соль с триметиламином, триэтиламином, пиридином, пиколином, этаноламином, диэтаноламином, триэтаноламином, дициклогексиламином, N,N'-дибензилэтилендиамином и т.д. Примеры соли с неорганической кислотой включают соль с хлористоводородной кислотой, бромистоводородной кислотой, азотной кислотой, серной кислотой, фосфорной кислотой и т.д. Примеры соли с органической кислотой включают соль с муравьиной кислотой, щавелевой кислотой, уксусной кислотой, винной кислотой, яблочной кислотой, метансульфоновой кислотой, бензолсульфоновой кислотой, п-толуолсульфоновой кислотой и т.д. Примеры солей с основными аминокислотами включают соль с аргинином, лизином, орнитином и т.д. Примеры солей с кислотной аминокислотой включают соль с аспарагиновой кислотой, глутаминовой кислотой и т.д. Нетоксичность в данном контексте следует рассматривать по отношению к прогнозу для инфицированного пациента без лечения.
Способы осуществления изобретения
Настоящее изобретение касается соединений формул 1-4, которые могут действовать как средства, модулирующие активность хемокиновых рецепторов. Такие хемокиновые рецепторы включают (но не ограничиваются ими) CCR1, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8 и CXCR1, CXCR2, CXCR3, CXCR4 и CXCR5.
В соответствии с настоящим изобретением предлагаются новые соединения формул 1-4, которые обеспечивают защиту клеток-мишеней от ВИЧ-инфекции, специфически связываясь с хемокиновым рецептором, и влияют на связывание естественного лиганда или хемокина с рецептором клетки-мишени, таким как CXCR4 и/или CCR5.
В другом варианте соединения формул 1-4 могут быть полезны как средства, которые влияют на хемокиновые рецепторы, такие как CCR1, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8 и CXCR1, CXCR2, CXCR3, CXCR4 и CXCR5, когда такие хемокиновые рецепторы являются важными медиаторами многих воспалительных заболеваний человека, а также иммунорегуляторных заболеваний и рака, и соединение, модулирующее активность таких хемокиновых рецепторов, было бы полезным для лечения или профилактики таких заболеваний.
Термин «модуляторы» при использовании в данном описании охватывает антагонисты, агонисты, частичные антагонисты и/или частичные агонисты, ингибиторы и активаторы. В предпочтительном варианте осуществления настоящего изобретения соединения формул 1-4 проявляют защитные эффекты против ВИЧ-инфекции, ингибируя связывание ВИЧ с хемокиновым рецептором, таким как CXCR4 и/или CCR5, клетки-мишени, при контактировании клетки-мишени с количеством соединения, эффективным в ингибировании связывания вируса с хемокиновым рецептором.
Термин «терапевтически эффективное количество» означает количество предлагаемого соединения, которое вызывает биологический или медицинский ответ в клетке, ткани, органе, системе, животном или человеке при обследовании исследователем, ветеринаром, врачом или другим клиницистом. Ответ может быть профилактическим и/или терапевтическим.
Термин «введение» предлагаемого соединения следует понимать как означающий доставку соединения по настоящему изобретению или лекарства-предшественника соединения по настоящему изобретению в организм субъекта, нуждающегося в лечении.
Соединения, ингибирующие хемокиновые рецепторы, можно применять для лечения заболеваний, связанных с кроветворением, включая, но не ограничиваясь этим, борьбу с побочными эффектами химиотерапии, повышение возможности удачной трансплантации костного мозга, повышение возможности излечения ран и успешного лечения ожогов, а также борьбу с бактериальными инфекциями при лейкозе.
Соединения, ингибирующие активность и функцию хемокиновых рецепторов, можно применять для лечения заболеваний, связанных с воспалением, включая, но не ограничиваясь этим, воспалительные или аллергические заболевания, такие как астма, аллергический ринит, аллергические заболевания легких, аллергическая пневмония, эозинофильные пневмонии, аллергическая реакция замедленного типа, интерстициальная болезнь легких (ILD) (например, идиопатический фиброз легких или ILD, связанная с ревматоидным артритом, системной красной волчанкой, анкилозирующим спонидитом, системным склерозом, синдромом Шегрена, полимиозитом или дерматомиозитом); системную анафилаксию или аллергические реакции, лекарственные аллергии, аллергические реакции на укус насекомых; аутоиммунные заболевания, такие как ревматоидный артрит, псориатический артрит, системная красная волчанка, миастения тяжелая, ювенильный диабет; гломерулонефрит, аутоиммунный троидит, отторжение трансплантата, включая отторжение аллотрансплантата или болезнь «трансплантат против хозяина»; воспалительные болезни кишечника, такие как болезнь Крона и язвенный колит; спондилоартропатии; склеродермию; псориаз (включая псориаз, опосредованный Т-клетками) и воспалительные дерматозы, такие как дерматит, экзема, атопический дерматит, аллергический контактный дерматит, крапивница, васкулит (например, некротизирующий, кожный и аллергический васкулиты); эозинофильный миотит; эозинофильный фасцит и рак.
Соединения, которые активируют функцию хемокиновых рецепторов или способствуют ей, можно применять для лечения заболеваний, связанных с иммуносупрессией, например, у больных, подвергающихся химиотерапии, радиационной терапии, усиленному лечению ран и ожогов, терапии аутоиммунного заболевания или другой лекарственной терапии (например, лечению кортикостероидами) или при сочетании традиционных лекарств, применяемых для лечения аутоиммунных заболеваний и отторжения трансплантата, которое вызывает иммуносупрессию, лечения иммуносупрессии, обусловленной врожденной недостаточностью рецепторной функции или другими причинами, и лечения инфекционных заболеваний, таких как паразитарные болезни, включающие, но не ограничиваемые этим, гельминтные инвазии, такие как нематоды (круглые черви); трихиуриаз, энтеробиоз, аскаридоз, анкилостомоз, стронгилоидоз, трихинеллез, филяриоз; трематоды; висцеральные черви, висцеральный синдром «блуждающей личинки» (например, Toxocara), эозинофильный гастроэнтерит (например, Anisaki spp., Phocanema ssp.), кожный синдром «блуждающей личинки» (Ancylostoma braziliense, Ancylostoma caninum); вызывающее малярию простейшее Plasmodium vivax, цитомегаловирус человека, Herpesvirus saimiri и герпесвирус саркомы Капоши, известный также как герпесвирус 8 человека, и поксвирус Moluscum contagiosum.
Соединения формул 1-4 можно применять в комбинации с любой другой фармацевтической композицией, когда такая комбинированная терапия может быть полезной для модулирования активности хемокиновых рецепторов и тем самым предупреждения и терапевтического лечения заболеваний, связанных с кроветворением, воспаления, аутоиммунных заболеваний, воспалительных дерматозов, рака, воспалительных болезней кишечника и иммунорегуляторных нарушений.
Предполагается также, что настоящее изобретение можно применять в комбинациях с одним или несколькими средствами, пригодными для профилактики или лечения ВИЧ-инфекции. Примеры таких средств включают:
(1) нуклеотидный ингибитор обратной транскриптазы, такой как зидовудин, диданозин, ламивудин, залцитабин, абакавир, ставудин, адефовир, дипивоксил, фозивудин, тодоксил и т.д.;
(2) ненуклеотидный ингибитор обратной транскриптазы (включая средство, обладающее противоокислительной активностью, такое как иммунокал, олтипраз и т.д.), такой как невирапин, делавирдин, эфавиренз, ловиридин, иммунокал, олтипраз и т.д., и
(3) ингибиторы протеазы, такие как саквинавир, ритонавир, индинавир, нелфинавир, ампренавир, палинавир, лазинавир и т.д.
Объем комбинаций соединений формул 1-4 по настоящему изобретению со средствами против ВИЧ не ограничивается (1), (2) и/или (3), а включает в принципе любую комбинацию с любой фармацевтической композицией, полезной для лечения ВИЧ-инфекции. Кроме того, в таких комбинациях соединения по настоящему изобретению и другие средства против ВИЧ могут быть введены раздельно или в сочетании. Причем введение одного элемента может быть осуществлено до, во время или после введения другого средства или средств.
Соединения формул 1-4 по настоящему изобретению могут быть введены перорально, парентерально (например, внутримышечно, внутрибрюшинно, внутривенно, внутрицистернальной инъекцией или вливанием, подкожной инъекцией или с помощью имплантата), путем аэрозольной ингаляции, назально, вагинально, ректально, подъязычно или местно и могут быть изготовлены, отдельно или вместе, в виде дозированных лекарственных форм, содержащих традиционные нетоксические фармацевтически приемлемые носители, вспомогательные вещества и наполнители, соответствующие каждому способу введения.
Все соединения формул 1-4 активны и применяются для лечения животных, включая, но, не ограничиваясь ими, мышей, крыс, лошадей, крупного рогатого скота, овец, собак, кошек и обезьян. Соединения по настоящему изобретению эффективны также в применении к людям.
Соединения формул 1-4 по настоящему изобретению могут образовывать гидраты или сольваты, которые включены в объем формулы изобретения. Когда соединения формул 1-4 по настоящему изобретению существуют в виде региоизомеров, геометрических изомеров, конформеров или диастереоизомеров, все такие формы и различные их смеси включены в общие формулы. При необходимости можно выделить отдельные изомеры, пользуясь известными методами разделения и очистки. Например, когда соединение формул 1-4 по настоящему изобретению представляет собой рацемат, он может быть разделен на (S)-соединение и (R)-соединение путем оптического разделения. Отдельные оптические изомеры и их смеси включены в объем общей формулы.
Настоящее изобретение относится также к фармацевтической композиции, содержащей фармацевтически приемлемый носитель или разбавитель и эффективное количество соединения формул 1-4. Соединение формул 1-4 может быть введено отдельно или в смеси с фармацевтически приемлемым носителем (например, в виде твердых лекарственных форм, таких как таблетки, капсулы, гранулы, порошки и т.д., или жидких лекарственных форм, таких как сиропы, инъекционные растворы и т.д.) перорально или неперорально. Примеры непероральных лекарственных средств включают инъекционные растворы, капли, суппозитории, вагинальные суппозитории.
При лечении или профилактике состояний, требующих модулирования хемокиновых рецепторов, подходящая доза обычно составляет примерно 0,01-500 мг на 1 кг массы тела пациента в сутки и может быть введена за один или несколько раз. Предпочтительно доза составляет примерно 0,1-250 мг/кг в сутки. Понятно, что конкретную дозу и частоту приема для каждого конкретного пациента можно изменять в зависимости от разных факторов, включающих активность конкретно применяемого соединения, метаболическую стабильность и продолжительность действия указанного соединения, возраст, массу тела, общее состояние здоровья, пол, диету, способ и время введения, скорость выведения, комбинацию лекарств, тяжесть состояния пациента и проводимое лечение пациента.
В соответствии с настоящим изобретением предлагаются новые соединения, связывающиеся с хемокиновыми рецепторами и препятствующие связыванию с ними естественного лиганда. Соединения по настоящему изобретению полезны как средства, оказывающие защитные эффекты на клетки-мишени от ВИЧ-инфекции. Соединения по настоящему изобретению полезны также в качестве антагонистов или агонистов хемокиновых рецепторов с другими биологическими активностями, связанными со способностью данных соединений ингибировать связывание хемокинов с их рецепторами.
В соединениях формул 1-4 алкил, представленный символом R, может быть неразветвленным или разветвленным, или циклическим и может быть необязательно замещенным 1-2 заместителями, выбранными из галогена, гидрокси и алкокси. Предпочтительно каждый R представляет Н или низший неразветвленный алкил, предпочтительно метил.
Ar представляет ароматический или гетероароматический фрагмент в виде одного кольца или конденсированной кольцевой системы с 5-12 кольцевыми членами. Примеры Ar включают бензол, нафталин, дигидронафталин, тетрагидронафталин, пиридин, хинолин, изохинолин, имидазол, бензимидазол, азабензимидазол, бензотриазол, фуран, бензофуран, тиазол, бензотиазол, оксазол, бензоксазол, пиррол и индол. Предпочтительные примеры включают фенилен, пиридилен или пиридинилен, более предпочтительно п-формы и предпочтительно фенилен.
Когда соединения формул 1-4 содержат элементы, являющиеся «необязательно замещенными», то используют следующие заместители.
Необязательные заместители могут представлять собой галоген, нитро, циано, карбоновую кислоту, необязательно замещенную алкильную, алкенильную или циклоалкильную группу, необязательно замещенную гидроксильную группу, необязательно замещенную тиольную группу, необязательно замещенную амино- или ацильную группу, необязательно замещенную карбоксилатную, карбаматную, карбоксамидную или сульфонамидную группу, необязательно замещенную ароматическую или гетероциклическую группу.
Примеры галогена включают фтор, хлор, бром, иод и т.д., причем предпочтительными являются фтор и хлор.
Примеры алкила, который может быть необязательно замещенным, включают С1-10 алкил, включающий метил, этил, пропил и т.д., примеры алкенильных групп, которые могут быть необязательно замещенными, включают С2-10 алкенил, такой как аллил, кротил, 2-пентенил, 3-гексенил и т.д., и примеры циклоалкильных групп, которые могут быть необязательно замещенными, включают С3-10 циклоалкил, такой как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и т.д. В указанных случаях предпочтительными являются С1-6 алкил, алкенил и циклоалкил. Необязательный заместитель может также представлять собой необязательно замещенный аралкил (например, фенил-С1-4 алкил) или гетероалкил, например фенилметил (бензил), фенилэтил, пиридинилметил, пиридинилэтил и т.д. Гетероциклическая группа может представлять собой 5- или 6-членное кольцо, содержащее 1-4 гетероатома.
Примеры необязательно замещенных гидроксильных и тиольных групп включают группы, в которых заместитель представляет собой необязательно замещенный алкил (например, С1-10 алкил), такой как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил и т.д., предпочтительно С1-6 алкил; необязательно замещенный циклоалкил (например, С3-7 циклоалкил и т.д., такой как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и т.д.); необязательно замещенный аралкил (например, фенил-С1-4 алкил, например бензил, фенетил и т.д.). Когда имеются два соседних гидроксильных или тиольных заместителя, гетероатомы могут быть соединены через алкиленовую группу, такую как O(CH2)nО и S(CH2)nS (где n=1-5). Примеры включают метилендиокси, этилендиокси и т.д. Примеры охватывают также оксиды тиоэфирных групп, такие как сульфоксиды и сульфоны.
Другие примеры необязательно замещенной гидроксильной группы включают необязательно замещенный С2-4 алканоил (например, ацетил, пропионил, бутирил, изобутирил и т.д.), С1-4 алкилсульфонил (например, метансульфонил, этансульфонил и т.д.) и необязательно замещенные ароматические и гетероциклические карбонильные группы, включающие бензоил, пиридинкарбонил и т.д.
Заместители необязательно замещенной аминогруппы могут быть связаны друг с другом с образованием циклической аминогруппы (например, 5-6-членный циклический амино и т.д., такой как тетрагидропиррол, пиперазин, пиперидин, пирролидин, морфолин, тиоморфолин, пиррол, имидазол и т.д.). Указанная циклическая аминогруппа может иметь заместитель, и примеры заместителей включают галоген (например, фтор, хлор, бром, иод и т.д.), нитро, циано, гидроксигруппу, тиольную группу, аминогруппу, карбоксильную группу, необязательно галогенированный С1-4 алкил (например, трифторметил, метил, этил и т.д.), необязательно галогенированный С1-4 алкокси (например, метокси, этокси, трифторметокси, трифторэтокси и т.д.), С2-4 алканоил (например, ацетил, пропионил и т.д.), С1-4 алкилсульфонил (например, метансульфонил, этансульфонил и т.д.), причем число предпочтительных заместителей составляет 1-3.
Аминогруппа может быть та