Способ определения энергии связи влаги с веществом
Иллюстрации
Показать всеИзобретение относится к измерительной технике. В способе определения энергии связи влаги с веществом путем помещения образцов влажного вещества в газообразную среду и выдерживания образцов в этой среде до наступления состояния равновесия, новым является то, что берут два влажных образца и поочередно подвергают обезвоживанию в дериватографе при различных скоростях нагрева печи с фиксацией во времени убыли влаги, температуры образцов, скорости их обезвоживания с последующим расчетом величины энергии связи влаги с веществом с учетом указанных параметров. Техническим результатом изобретения является сокращение длительности и повышение надежности определения энергии связи влаги с веществом при фиксированном влагосодержании вещества. 2 ил., 1 табл.
Реферат
Изобретение относится к способам определения энергии связи влаги с веществом и может быть использовано в научных исследованиях сушки веществ, а также в пищевой, химической и других отраслях промышленности.
Ближайшим аналогом изобретения является способ расчета энергии связи влаги с материалом по известному уравнению Ребиндера, основанный на снятии кривых сорбции и десорбции (Гинзбург А.С., Савина И.М. Массовлагообменные характеристики пищевых продуктов. - М.: Легкая и пищевая промышленность, 1982, с.280).
Данный способ имеет существенные недостатки, обусловленные длительностью экспериментов. Кроме того, при снятии кривых сорбции и десорбции процесс является изохорно-изотермическим и равновесным, что существенно отличает его от условий реального процесса сушки.
Технической задачей изобретения является сокращение длительности и повышение надежности определения энергии связи влаги с веществом при фиксированном влагосодержании вещества.
Поставленная задача достигается тем, что в способе определения энергии связи влаги с веществом путем помещения образцов влажного вещества в газообразную среду с заданной относительной влажностью и температурой и выдерживания образцов в этой среде до наступления состояния равновесия с последующим расчетом величины энергии связи влаги с веществом по формуле:
где Е(u,Т) - энергия связи влаги с веществом при температуре Т и влагосодержании u, Дж/кг;
Т - абсолютная температура влажного вещества и газообразной среды, находящихся в состоянии равновесия, °К;
ϕ(u,Т) - относительная влажность газообразной среды, находящейся в состоянии равновесия с влажным веществом,
новым является то, что берут два влажных образца и поочередно подвергают обезвоживанию в дериватографе при различных скоростях нагрева печи с фиксацией во времени убыли влаги, температуры образцов и скорости их обезвоживания с последующим расчетом величины энергии связи влаги с веществом по формуле:
где T1, T2 - значения абсолютной температуры в образцах при влагосодержании образцов, равном u;
υ1, υ2 - скорости обезвоживания образцов при влагосодержании образцов, равном u;
r(Tcp) - удельная теплота парообразования воды при температуре, равной среднеарифметической температуре образцов;
Тср - среднеарифметическая температура образцов, °К.
Рассмотрим процесс удаления влаги из образцов в печи дериватографа как физико-химический процесс, при котором влажное вещество под воздействием теплоты разделяется на парообразную влагу и сухой остаток. Для расчета скорости процесса применим законы кинетики химических реакций. При этом исходим из следующих положений:
1. Переход влаги в парообразное состояние связан с преодолением энергетического барьера Е, наличие которого обусловлено энергией связи воды с сухой частью вещества Есв и теплотой парообразования r, Дж/кг.
2. В парообразное состояние переходят молекулы воды, энергия которых больше или равна Е.
3. Доля молекул с энергией больше или равной Е во влажном веществе определятся законом распределения Больцмана.
4. Вещество, из которого удаляется влага, является мелкодисперсным, т.е. наибольший поперечный размер частиц вещества не превышает двух зон испарения, это позволяет рассматривать процесс обезвоживания как процесс, происходящий в кинетической области.
Воспользуемся теорией Аррениуса о химических превращениях и выразим скорость процесса удаления влаги уравнением:
где f(α) - функция степени превращения вещества;
K0 - коэффициент, с-1;
- скорость превращения,
Е=Eсв+r - энергия активации молекул воды, Дж/моль.
Под α понимается отношение количества распавшегося вещества (в данном случае удаленной влаги) за рассматриваемый промежуток времени к количеству распавшегося вещества в конце опыта.
При проведении двух испытаний образцов в печи дериватографа, отличающихся различными скоростями нагрева, равное влагосодержание в образцах и соответствующие влагосодержанию одинаковые степени распада достигаются при температурах образцов соответственно T1 и T2.
Для двух экспериментов при неизменном виде функции степени превращения можно записать:
Таким образом, энергия связи влаги с веществом в интервале температур Т1 и T2 определяется по формуле:
Значения ν1 и ν2 принимаются при равном αi и им соответствуют T1 и T2. Температуру материала Тср при данном αi определяют как среднеарифметическое значение температур T1 и T2.
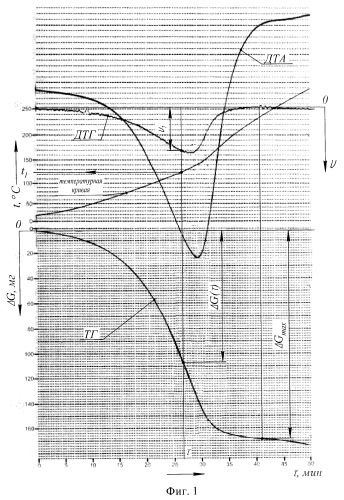
"На фиг.1 приведена дериватограмма казеина и схематично показано определение в момент времени τ температуры образца t1, скорости обезвоживания υ1, количество испарившейся влаги ΔG(τ), а также максимальное количество удаленной из образца влаги ΔGmax".
Расчетные параметры определяются следующим образом с использованием данных дериватограммы.
Влагосодержание определяется по количеству испарившейся влаги в данный момент времени:
где ΔGmax - максимальное количество испарившейся влаги из навески;
ΔG(r) - количество вещества, испарившегося в момент времени τ;
G - масса навески.
Начальное влагосодержание uн рассчитывается по формуле:
Величину αi рассчитывают по формуле:
При проектировании промышленных сушильных аппаратов возникает проблема правильного выбора способа сушки и типа сушильного аппарата. Одна из методик по выбору рационального способа сушки и сушильных установок основана на анализе вещества как объекта сушки и установлении его принадлежности к той или иной группе влажных веществ, после чего выбирается тип аппарата из числа выпускаемых промышленностью (Сажин Б.С. Основы техники сушки. М.: Химия, 1984. с.253).
Для пищевых продуктов важнейшими характеристиками является влага и ее энергия связи с твердым скелетом материала (Гинзбург А.С. Сушка пищевых продуктов. М.: Пищевая промышленность, 1973). Поэтому эти характеристики учитываются при выборе способа сушки вещества и сушильной установки.
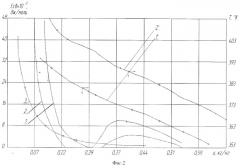
На фиг.2 представлены кривые изменения энергии связи влаги с казеином Есв и температуры материала Т при высушивании в печи дериватографа при параметрах, указанных в таблице.
| Таблица | ||||
| Обозначение кривых | Скорость нагрева печи, °С/мин. | Начальная влажность казеина, % | Срок хранения казеина, час | |
| 1 и 1' | Скорость нагрева в первом испытании | 1,25 | 55,1 | 20 |
| Скорость нагрева во втором испытании | 5 | |||
| 2 и 2' | Скорость нагрева в первом испытании | 2,5 | 53,5 | 0 |
| Скорость нагрева во втором испытании | 5 |
3 - кривая, рассчитанная по уравнению: Есв=-RT·lnϕ.
На фиг.2 (изменение энергии связи влаги с казеином и температуры материала, кривые 1 и 2) видно, что на графике зависимости Есв=f(W) можно выделить четыре характерных участка. Первый участок, который наблюдается при снижении влагосодержания до 0,53 кг/кг, характеризуется удалением свободной влаги, поэтому величина Есв равна нулю. На участке снижения влагосодержания в казеине от 0,53 кг/кг до 0,33÷0,37 кг/кг (второй участок) происходит небольшое возрастание энергии связи с молочным белком, после чего происходит резкое падение Есв до нуля (третий участок). Снижение Есв влаги на этом участке объясняется денатурацией молочного белка - изменением его структуры, в результате чего происходит высвобождение связанной «иммобилизационной» воды и переход ее в свободное состояние с меньшей Есв. Начиная с влагосодержания 0,19÷0,235 кг/кг, обезвоживание казеина сопровождается резким повышением энергии связи, достигая в конце процесса сушки (U=0,05 кг/кг) значения 40÷35 кДж/моль, что сопоставимо с удельной теплотой парообразования свободной влаги. Причем началу повышения Eсв на четвертом участке соответствует точка перегиба на температурной кривой: это свидетельствует об удалении наиболее прочной влаги казеина.
Кривая 3 на фиг.2 построена по известному уравнению Ребиндера Есв=-RT·lnϕ. При этом использована зависимость Wp=ƒ(ϕ), полученная Г.Р.Цыдендоржиевой при температуре 60°С. Отклонения теоретической кривой 3 от кривых 1 и 2 объясняется прежде всего тем, что процесс сушки в печи дериватографа не является изотермическим и неравновесным, как это предусматривается формулой Ребиндера.
Преимущества способа заключаются в том, что условия эксперимента приближены к реальным процессам сушки; поочередное обезвоживание в печи дериватографа двух влажных образцов позволяет сократить длительность эксперимента; получение комплексного характера информации в одном эксперименте с небольшим количеством вещества путем совмещения четырех методов термического анализа: термографического (Т), термогравиметрического (ТГ), дифференциального термического (ДТА), деривативного термогравиметрического (ДТГ) позволяет повысить точность и надежность измерений.
Способ определения энергии связи влаги с веществом, включающий помещение образцов влажного вещества в газообразную среду с заданными относительной влажностью и температурой, выдерживание образцов в этой среде до наступления состояния равновесия и последующий расчет величины энергии связи влаги с веществом, отличающийся тем, что берут два влажных образца и поочередно подвергают обезвоживанию в дериватографе при различных скоростях нагрева печи с фиксацией во времени убыли влаги, температуры образцов и скорости их обезвоживания, при этом для различных скоростей нагрева достигаются одинаковые степени распада при температурах соответственно T1, T2, а последующий расчет величины энергии связи влаги с веществом проводят по формуле:
где Т1, Т2 - значения абсолютной температуры в образцах при влагосодержании образцов, равном u;
υ1, υ2 - скорости обезвоживания образцов при влагосодержании образцов, равном u;
r(Tcp) - удельная теплота парообразования воды при температуре, равной среднеарифметической температуре образцов;
Тср - среднеарифметическая температура образцов, К.