Бензотиазолы
Иллюстрации
Показать всеИзобретение относится к соединениям общей формулы
в которой R1 представляет собой 3,6-дигидро-2Н-пиран-4-ил, 5,6-дигидро-4Н-пиран-3-ил, 5,6-дигидро-4Н-пиран-2-ил, тетрагидропиран-2,3- или 4-ил, циклогекс-1-енил, циклогексил или представляет собой 1,2,3,6-тетрагидропиридин-4-ил или пиперидин-4-ил, которые необязательно замещены -С(O)СН3 или -С(O)ОСН3 в 1 положении атома N; R2 представляет собой низший алкил, пиперидин-1-ил, необязательно замещенный гидрокси, или представляет собой фенил, необязательно замещенный -(CH2)n-N(R')-C(O)-(CH2)n-NR'2, -(CH2)n-галогеном, низшим алкилом или -(CH2)n-N(R')-(СН2)n-O-низшим алкилом, или представляет собой морфолинил или пиридинил, который необязательно замещен галогеном, -N(R')-(CH2)n-O-низшим алкилом, низшим алкилом, низшим алкокси, морфолинилом или -(СН2)n-пирролидинилом; n обозначает 0, 1 или 2; R' представляет собой водород или низший алкил; и их фармацевтически приемлемым кислотно-аддитивным солям. Также изобретение относится к лекарственному средству, обладающему сродством к аденозиновому рецептору A2A, содержащему одно или несколько соединений общей формулы (I) и фармацевтически приемлемые эксципиенты. 2 н. и 15 з.п. ф-лы.
Реферат
Настоящее изобретение относится к соединениям общей формулы
в которой
R1 представляет собой 3,6-дигидро-2H-пиран-4-ил, 5,6-дигидро-4H-пиран-3-ил, 5,6-дигидро-4H-пиран-2-ил, тетрагидропиран-2,3- или 4-ил, циклогекс-1-енил, циклогексил или представляет собой 1,2,3,6-тетрагидропиридин-4-ил или пиперидин-4-ил, которые необязательно замещены -С(O)СН3 или -С(O)ОСН3 в 1 положении атома N;
R2 представляет собой низший алкил, пиперидин-1-ил, необязательно замещенный гидрокси, или представляет собой фенил, необязательно замещенный -(CH2)n-N(R')-C(O)-(CH2)n-NR'2, -(СН2)n-галогеном, низшим алкилом или -(СН2)n-N(R')-(СН2)n-O-низшим алкилом, или представляет собой морфолинил или пиридинил, который необязательно замещен галогеном, -N(R')-(СН2)n-O-низшим алкилом, низшим алкилом, низшим алкокси, морфолинилом или -(CH2)n-пирролидинилом;
n обозначает 0, 1 или 2;
R' представляет собой водород или низший алкил;
и к их фармацевтически приемлемым кислотно-аддитивным солям.
Неожиданно было обнаружено, что соединения общей формулы I являются лигандами аденозинового рецептора. Конкретно, соединения настоящего изобретения имеют высокое сродство с А2А-рецептором и высокую селективность к рецепторам A1 и A3.
Аденозин модулирует множество физиологических функций взаимодействием со специфическими рецепторами клеточной поверхности. Активность аденозиновых рецепторов в качестве лекарственного средства была впервые открыта в 1982 году. Аденозин связан структурно и метаболически с биоактивными нуклеотидами аденозинтрифосфатов (АТФ), аденозиндифосфатов (АДФ), аденозинмонофосфатов (АМФ) и циклических аденозинмонофосфатов (цАМФ); с биохимическим метилированным агентом S-аденосил-L-метионом (SAM) и структурно с коэнзимами NAD, FAD и коэнзимом А; и с РНК. Аденозин и эти связанные с ним соединения вместе важны для регулирования многих аспектов клеточного метаболизма и для модуляции различных действий центральной нервной системы.
Рецепторы для аденозина классифицируются как рецепторы A1, A2A, А2В и A3, относясь к семейству рецепторов, связанных с G-белком. Активация аденозиновых рецепторов аденозином запускает механизм передачи сигнала. Эти механизмы зависят от G-белка, связанного с рецептором. Каждый из подтипов аденозиновых рецепторов обычно характеризуют по эффекторной системе аденилатциклазы, которая использует цАМФ в качестве вторичного мессенжера. Рецепторы A1 и A3, связанные с Gi белками, ингибируют аденилатциклазу, что приводит к уменьшению клеточных уровней цАМФ, в то время как рецепторы А2A и А2B связываются с Gs белками и активизируют аденилатциклазу, приводя к увеличению клеточных уровней цАМФ. Известно, что система рецептора A1 включает активацию фосфолипазы С и модуляцию ионных каналов калия и кальция. Подтип А3, в дополнение к его связыванию с аденилатциклазой, также стимулирует фосфолипазу С и, следовательно, активирует ионные каналы кальция.
Рецептор A1 (326-328 аминокислот) был клонирован из различных видов (псовый, человеческий, крысиный, собачий, куриный, бычий, морской свинки) с 90-95% идентичностью последовательностей среди млекопитающих. Рецептор А2А (409-412 аминокислот) был клонирован из собаки, крысы, человека, морской свинки и мыши. Рецептор А2B (332 аминокислоты) был клонирован из человека и мыши с 45% гомологичностью рецепторов А2B человека с рецепторами A1 и A2A человека. Рецептор А3 (317-320 аминокислот) был клонирован из человека, крысы, собаки, кролика и овцы.
Предполагается, что подтипы рецепторов A1 и A2A играют дополнительные роли в регулировании аденозином поставки энергии. Аденозин, который является метаболическим продуктом АТФ, диффундирует от клетки и действует местно, активируя аденозиновые рецепторы для уменьшения потребности кислорода (A1) или увеличения доставки кислорода (А2A), и таким образом восстанавливая баланс поставки энергии: потребность в пределах ткани. Действия обоих подтипов должны увеличить количество доступного кислорода в тканях и защищать клетки от повреждения, вызванного краткосрочной нестабильностью кислорода. Одной из важных функций эндогенного аденозина является предотвращение повреждения во время травм, таких как гипоксия, ишемия, гипотензия и эпилептический припадок.
Кроме того, известно, что связывание агониста аденозинового рецептора с тучными клетками, экспрессирующими рецептор А3 крысы, приводит к увеличению концентраций инозитолтрифосфата и внутриклеточного кальция, что вызывает индуцированную антигеном секрецию воспалительных медиаторов. Поэтому рецептор А3 играет роль в медиировании приступов астмы и других аллергических реакциях.
Аденозин является нейромодулятором, способным модулировать множество аспектов физиологической функции мозга. Эндогенный аденозин, центральное связующее звено между метаболизмом энергии и деятельностью нейронов, изменяется в соответствии с поведением и (пато)физиологическими состояниями. В условиях повышенной потребности и пониженной доступности энергии (таких как гипоксия, гипогликемия и/или избыточная деятельность нейронов) аденозин обеспечивает мощный защитный механизм отдачи. Взаимодействие с аденозиновыми рецепторами представляет собой многообещающую цель для терапевтического применения в многочисленных неврологических и психических болезнях, таких как эпилепсия, нарушения сна и движения (болезнь Паркинсона или Хантингтона), болезнь Альцгеймера, депрессия, шизофрения или наркомания. Повышение высвобождения нейротрансмиттеров приводит к травмам, таким как гипоксия, ишемия и эпилептические припадки. Эти нейротрансмиттеры в конечном счете отвечают за разрушение и гибель нервных клеток, что вызывает повреждение мозга или гибель индивидуума. Агонисты аденозина A1, которые имитируют центральные ингибирующие действия аденозина, могут поэтому быть полезны в качестве нейрозащитных агентов. Аденозин был предложен в качестве эндогенного антиконвульсионного агента, ингибирующего высвобождение глутамата из стимулирующих нейронов и ингибирующего нейронное сгорание. Агонисты аденозина поэтому могут использоваться в качестве противоэпилептических агентов. Антагонисты аденозина стимулируют деятельность ЦНС и, как оказывается, являются эффективными в качестве энхансеров распознавания. Селективные антагонисты A2a обладают терапевтической активностью при лечении различных форм слабоумия, например, болезни Альцгеймера и нейродегенеративных нарушений, например, припадка. Антагонисты аденозинового рецептора А2а модулируют деятельность стриарных GABA нейронов и регулируют плавные и хорошо скоординированные движения, таким образом обеспечивая возможное лечение симптомов болезни Паркинсона. Аденозин также вовлечен в многочисленное физиологические процессы, включая успокаивающее действие, гипноз, шизофрению, беспокойство, боль, дыхание, депрессию и наркоманию (амфетамин, кокаин, опиоиды, этанол, никотин, каннабиноиды). Поэтому лекарственные средства, выступающие в качестве аденозиновых рецепторов, обладают терапевтической активностью в качестве успокоительных средств, мышечных релаксантов, антипсихотических средств, транквилизаторов, анальгетиков, дыхательных стимуляторов, антидепрессантов и средств для лечения злоупотребления наркотиками. Они могут также использоваться для лечения ADHD (заболевание гиперактивности дефицита внимания).
Важная роль аденозина в сердечно-сосудистой системе заключается в использовании его в качестве кардиозащитного агента. Уровни эндогенного аденозина увеличиваются в ответ на ишемию и гипоксию и защищают сердечную ткань во время травмы и после нее (предварительное состояние). Действуя на рецепторе A1, агонисты аденозина A1 могут защищать от повреждений, вызываемых миокардиальной ишемией и реперфузией. Модулирующее влияние рецепторов А2а на адренергическую функцию может иметь значение для различных заболеваний, таких как коронарная артериальная болезнь и сердечная недостаточность. Антагонисты A2a могут терапевтически применяться в ситуациях, в которых необходим повышенный антиадренергический отклик, таких как острая миокардиальная ишемия. Селективные антагонисты рецепторов А2а могут также увеличивать эффективность аденозина в устранении суправентрикулярных аритмий.
Аденозин модулирует множество аспектов функции почек, включая высвобождение ренина, скорость гломерулярной фильтрации и поток крови через почки. Соединения, которые являются антагонистами почечных функций аденозина, активны в качестве почечных защитных агентов. Кроме того, антагонисты аденозина A3 и/или А2B могут быть полезны для лечения астмы и других аллергических ответов или для лечения сахарного диабета и ожирения.
Многочисленные документы описывают общий уровень техники относительно аденозиновых рецепторов, например, следующие публикации:
Bioorganic & Medicinal Chemistry, 6, (1998), 619-641,
Bioorganic & Medicinal Chemistry, 6, (1998), 707-719,
J.Med.Chem., (1998), 41, 2835-2845,
J.Med.Chem., (1998), 41, 3186-3201,
J.Med.Chem., (1998), 41, 2126-2133,
J.Med.Chem., (1999), 42, 706-721,
J.Med.Chem., (1996), 39, 1164-1171,
Arch.Pharm.Med.Chem., 332, 39-41, (1999),
Am.J.Physiol, 276, H1113-1116, (1999) или
Naunyn Schmied, Arch.Pharmacol. 362, 375-381, (2000).
Объектами настоящего изобретения являются соединения формулы I, применение соединений формулы I и их фармацевтически приемлемых солей для изготовления лекарственных средств для лечения заболеваний, связанных с аденозиновым рецептором A2, их получение, лекарственные средства, основанные на соединении в соответствии с изобретением и их получение, а также применение соединений формулы I для контроля или предотвращения заболеваний, основанных на модуляции системы аденозина, таких как болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, нейпротективное действие, шизофрения, беспокойство, боль, дефицит дыхания, депрессия, наркомания, такая как зависимость от амфетамина, кокаина, опиоидов, этанола, никотина, каннабиноидов, или для лечения астмы, аллергических реакций, гипоксии, ишемии, эпилептического припадка и токсикомании. Кроме того, соединения настоящего изобретения могут быть полезны в качестве успокоительных средств, мышечных релаксантов, антипсихотических веществ, противоэпилептических средств, антиконвульсантов и кардиозащитных агентов для заболеваний, таких как коронарная артериальная болезнь и сердечная недостаточность. Наиболее предпочтительные показания в соответствии с настоящим изобретением включают показания, которые основываются на антагонистической активности рецептора A2A и которые включают нарушения центральной нервной системы, например лечение или предотвращение болезни Альцгеймера, некоторых депрессивных нарушений, наркомании, защиты нервных клеток и болезни Паркинсона, а также ADHD.
Используемый здесь термин "низший алкил" обозначает алкильную группу с насыщенной линейной или разветвленной цепью, содержащей от 1 до 6 атомов углерода, например метил, этил, пропил, изопропил, н-бутил, изо-бутил, 2-бутил, трет-бутил и т.п. Предпочтительными низшими алкильными группами являются группы с 1-4 атомами углерода.
Термин "галоген" обозначает хлор, иод, фтор и бром.
Термин "низший алкокси" обозначает группу, в которой алкильные остатки являются такими, как определено выше, и которая присоединена через атом кислорода.
Термин "фармацевтически приемлемые кислотно-аддитивные соли" охватывает соли с неорганическими и органическими кислотами, такими как соляная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, сукциновая кислота, винная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и т.п.
Предпочтительными соединениями настоящего изобретения являются соединения формулы I, в которой R1 представляет собой 3,6-дигидро-2H-пиран-4-ил, например, следующее соединение: метиловый эфир [7-(3,6-дигидро-2H-пиран-4-ил)-4-метоксибензотиазол-2-ил]карбаминовой кислоты.
Также предпочтительными являются соединения, в которых R1 представляет собой тетрагидропиран-4-ил, например, следующие соединения:
4-фтор-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]бензамид,
N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-6-метилникотинамид,
2-метокси-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]изоникотинамид,
2-этокси-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]изоникотинамид,
2-этил-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]изоникотинамид,
N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-пропилизоникотинамид,
2-изопропокси-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]изоникотинамид,
2-изопропил-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]изоникотинамид,
N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-2-пирролидин-1-илметилизоникотинамид,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]-амид морфолин-4-карбоновой кислоты,
[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]амид 4-гидроксипиперидин-1-карбоновой кислоты,
2-(2-метоксиэтиламино)-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]изоникотинамид или
2-[(2-метоксиэтил)метиламино]-N-[4-метокси-7-(тетрагидропиран-4-ил)бензотиазол-2-ил]изоникотинамид.
Также предпочтительными являются соединения, в которых R1 представляет собой тетрагидропиран-2-ил, например, следующие соединения:
2-бром-N-[4-метокси-7-(тетрагидропиран-2-ил)бензотиазол-2-ил]изоникотинамид,
4-фтор-N-[4-метокси-7-(тетрагидропиран-2-ил)бензотиазол-2-ил]бензамид,
N-[4-метокси-7-(тетрагидропиран-2-ил)бензотиазол-2-ил]-2-метилизоникотинамид или
N-[4-метокси-7-(тетрагидропиран-2-ил)бензотиазол-2-ил]-2-морфолин-4-илизоникотинамид.
Дальнейшей предпочтительной группой соединений являются соединения, в которых R1 представляет собой 1,2,3,6-тетрагидропиридин-4-ил, замещенный -С(O)СН3, например, следующее соединение:
N-[7-(1-ацетил-1,2,3,6-тетрагидропиридин-4-ил)-4-метоксибензотиазол-2-ил]-4-фторбензамид.
Предпочтительными соединениями настоящего изобретения являются соединения формулы I, в которой R1 представляет собой пиперидин-4-ил, замещенный на атоме N -С(O)СН3, например, следующие соединения:
N-[7-(1-ацетилпиперидин-4-ил)-4-метоксибензотиазол-2-ил]-4-фторбензамид,
[7-(1-ацетилпиперидин-4-ил)-4-метоксибензотиазол-2-ил]амид морфолин-4-карбоновой кислоты,
N-[7-(1-ацетилпиперидин-4-ил)-4-метоксибензотиазол-2-ил]-2-метилизоникотинамид,
N-[7-(1-ацетилпиперидин-4-ил)-4-метоксибензотиазол-2-ил]-4-{[(2-метоксиэтил)метиламино]метил}бензамид,
N-[7-(1-ацетилпиперидин-4-ил)-4-метоксибензотиазол-2-ил]-4-метилбензамид,
N-[7-(1-ацетилпиперидин-4-ил)-4-метоксибензотиазол-2-ил]-2-морфолин-4-ил-изоникотинамид или
N-[7-(1-ацетилпиперидин-4-ил)-4-метоксибензотиазол-2-ил]-2-метоксиизоникотинамид.
Предпочтительной группой соединений формулы I являются также соединения, в которых R1 представляет собой циклогекс-1-енил, например, следующее соединение:
метиловый эфир (7-циклогекс-1-енил-4-метоксибензотиазол-2-ил)карбаминовой кислоты.
Предпочтительными соединениями настоящего изобретения являются соединения формулы I, в которых R1 представляет собой циклогексил, например, следующие соединения:
N-(7-циклогексил-4-метоксибензотиазол-2-ил)-4-фторбензамид,
N-(7-циклогексил-4-метоксибензотиазол-2-ил)-4-{[(2-метоксиэтил)метиламино]метил}бензамид или
N-(7-циклогексил-4-метоксибензотиазол-2-ил)-2-пирролидин-1-илметилизоникотинамид.
Соединения формулы I согласно настоящему изобретению и их фармацевтически приемлемые соли могут быть получены способами, известными из уровня техники, например, способами, описанными ниже, где способ включает
а) взаимодействие соединения формулы
с соединением формулы
или с соединением формулы
с получением соединения формулы
где R1 и R2 имеют определенные выше значения, или
б) гидрирование соединения формулы
с получением соединения формулы
где Х представляет собой кольцевой атом, выбранный из группы, включающей О, N или С, который может находиться в различных положениях кольца, и где атом кольцевой N может быть замещен -С(O)СН3 или -С(O)ОСН3, или
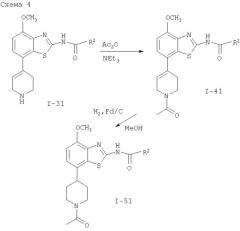
в) взаимодействие соединения формулы
с Ас2О
с получением соединения формулы
где пунктирная линия может обозначать связь, и R2 имеет определенные выше значения, и
при необходимости, преобразование полученных соединений в фармацевтически приемлемые кислотно-аддитивные соли.
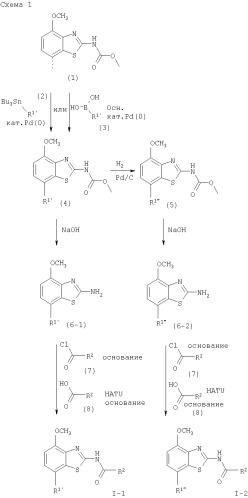
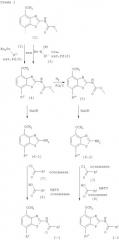
Соединения формулы I могут быть получены в соответствии с вариантами способа а)-в) и в соответствии со следующими схемами 1-5.
где R1' представляет собой 3,6-дигидро-2H-пиран-4-ил, 5,6-дигидро-4H-пиран-3-ил,
5,6-дигидро-4Н-пиран-2-ил, циклогекс-1-енил или 1,2,3,6-тетрагидропиридин-4-ил и R" представляет собой тетрагидропиран-2,3- или 4-ил, циклогексил или пиперидин-4-ил.
Получение соединений формулы (4)
Исходные 7-йодобензотиазольные производные формулы (1) могут быть получены способами, раскрытыми в ЕР 00113219,0. Исходные соединения трибутилстаннана формулы (2) могут быть коммерчески доступны, например, от Fluka, или могут быть получены способами, известными из уровня техники.
7-Йодобензотиазольное производное формулы (1) реагирует с избытком соединения трибутилстаннана формулы (2) в органическом растворителе, предпочтительно диоксане, содержащем палладиевый катализатор, предпочтительно бис(дибензилиденацетон)палладия (0), и каталитическое количество фосфинового лиганда, предпочтительно трифурилфосфина. Реакцию проводят при повышенной температуре, предпочтительно около 100°С, в течение около 2-24 часов, предпочтительно около 16 часов. Продукт формулы (4) выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
Альтернативное получение соединений формулы (4)
Исходные соединения бороновой кислоты формулы (3) могут быть коммерчески доступны, например, от Fluka, или могут быть получены способами, известными из уровня техники.
Соединения формулы (4) альтернативно могут быть получены обработкой 7-йодобензотиазольных производных формулы (1) избытком соединения бороновой кислоты формулы (3). Реакцию проводят в водном растворителе, предпочтительно в смеси воды и диоксана, содержащей палладиевый катализатор, предпочтительно бис(дибензилиденацетон)палладия (0), и каталитическое количество фосфинового лиганда, предпочтительно трифурилфосфина, и неорганического основания, предпочтительно карбоната натрия. Реакцию предпочтительно проводят при температуре кипения растворителя, предпочтительно около 100°С, в течение около 2-24 часов, предпочтительно около 16 часов. Продукт формулы (4) выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
Получение соединений формулы (5)
Соединения формулы (5) могут быть получены гидрированием соединений формулы (4) в присутствии катализатора гидрирования, предпочтительно 10% палладия на угле. Эти реакции могут проводиться в различных органических растворителях, таких как метанол, этанол или тетрагидрофуран, предпочтительно метанол, при комнатной температуре и при давлении одна атмосфера или выше, предпочтительно при одной атмосфере, в течение 16-72 часов, предпочтительно около 72 часов. Продукт формулы (5) выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
Получение соединений формулы (6-1) или (6-2)
Один способ получения соединений формулы (6-1) или (6-2) заключается в обработке соединения формулы (4) или (5) избытком гидроксида натрия или гидроксида калия в водном растворителе, предпочтительно водном этиленгликоле. Реакцию проводят при повышенной температуре, предпочтительно около 100°С, в течение около 1-16 часов, предпочтительно около 3 часов. Продукт формулы (6-1) или (6-2) выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
Получение соединений формулы I-1 или I-2
Один способ получения соединений формулы I-1 или I-2 заключается в обработке соединения формулы (6-1) или (6-2) небольшим избытком соответствующего ацилхлорида формулы (7), который может быть коммерчески доступным или может быть получен способами, известными из уровня техники. Реакцию проводят в апротонном органическом растворителе, предпочтительно в смеси дихлорметана и тетрагидрофурана, содержащей основание, предпочтительно N-этилдиизопропиламин или триэтиламин, при комнатной температуре в течение 2-24 часов, предпочтительно 24 часов. Продукт формулы I выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
Альтернативное получение соединений формулы I-1 или I-2
Альтернативный способ получения соединений формулы I включает обработку соответствующей карбоновой кислоты формулы (8) стехиометрическим эквивалентом реагента, связывающего пептид, предпочтительно гексафторфосфатом O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония (HATU), в эфирном растворителе, предпочтительно тетрагидрофуране, содержащем основание, предпочтительно N-этилдиизопропиламин, при комнатной температуре в течение 30-90 минут, предпочтительно 1 часа. Эту смесь затем обрабатывают соединением формулы (6) в смеси растворителей, предпочтительно в смеси тетрагидрофурана, диоксана и N,N-диметилформамида, при комнатной температуре в течение 16-24 часов, предпочтительно в течение 16 часов. Продукт формулы I выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
Альтернативное получение соединений формулы (6-2)
Альтернативным способом получения соединений формулы (6-2) является получение из промежуточных соединений формулы (13), получение которых показано ниже на схеме реакции 2.
где R1' и R1" определены в схеме 1.
Получение соединений формулы (10)
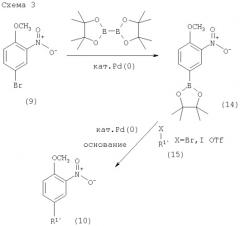
Исходные арилбромидные соединения формулы (9) могут быть коммерчески доступны, например от Fluka, или могут быть получены способами, известными из уровня техники. Исходные соединения трибутилстаннана формулы (2) могут быть коммерчески доступны, например от Fluka, или могут быть получены способами, известными из уровня техники.
Арилбромидное соединение формулы (9) реагирует с избытком соединения трибутилстаннана формулы (2) в органическом растворителе, предпочтительно диоксане, содержащем палладиевый катализатор, предпочтительно бис(дибензилиденацетон)палладий (0), и каталитическое количество фосфинового лиганда, предпочтительно трифурилфосфина. Реакцию проводят при повышенной температуре, предпочтительно около 100°С, в течение приблизительно 2-24 часов, предпочтительно около 16 часов. Продукт формулы (10) выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
Альтернативное получение соединений формулы (10)
Исходные соединения бороновой кислоты формулы (3) могут быть получены коммерчески, например от Fluka, или могут быть получены способами, известными из уровня техники.
Соединения формулы (10) альтернативно могут быть получены обработкой арилбромидных соединений формулы (9) избытком соединения бороновой кислоты формулы (3). Реакцию проводят в водном растворителе, предпочтительно в смеси воды и диоксана, содержащей палладиевый катализатор, предпочтительно бис(дибензилиденацетон)палладий (0), и каталитическое количество фосфинового лиганда, предпочтительно трифурилфосфина, и неорганическое основание, предпочтительно карбонат натрия. Реакцию предпочтительно проводят при температуре кипения растворителя, предпочтительно около 100°С, в течение около 2-24 часов, предпочтительно около 16 часов. Продукт формулы (10) выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
Получение соединений формулы (11)
Соединения формулы (11) могут быть получены гидрированием соединений формулы (10) в присутствии катализатора гидрирования, предпочтительно 10% палладия на угле. Эти реакции могут проводиться в различных органических растворителях, таких как метанол, этанол, тетрагидрофуран или дихлорметан, предпочтительно в смеси метанола и дихлорметана, при комнатной температуре и при давлении одна атмосфера или выше, предпочтительно при одной атмосфере, в течение 0,5-16 часов, предпочтительно около 1 часа. Продукт формулы (11) выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
Получение соединений формулы (12)
Один способ получения соединений формулы (12) включает обработку соединения формулы (11) небольшим избытком бензоилизотиоцианата в ацетоне при температуре между комнатной температурой и температурой кипения, предпочтительно при комнатной температуре, в течение 10-30 минут, предпочтительно 30 минут. Продукт формулы (12) выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
Получение соединений формулы (13)
Соединение формулы (12) обрабатывают стехиометрическим количеством алкоголята щелочного металла в соответствующем спиртовом растворителе, предпочтительно метилатом натрия в метаноле. Реакцию проводят при комнатной температуре в течение около 0,5-2 часов, предпочтительно около 1 часа. Продукт формулы (13) выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
Получение соединений формулы (6-2)
Один способ получения соединений формулы (6-2) заключается в обработке соединения формулы (13) стехиометрическим эквивалентом брома в галогенированном органическом растворителе, предпочтительно хлороформе. Реакцию проводят при повышенной температуре, предпочтительно при температуре кипения растворителя, в течение около 12-18 часов, предпочтительно около 16 часов. Продукт формулы (6) выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
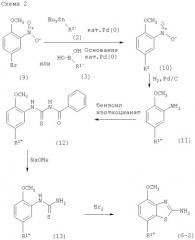
Альтернативное получение соединений формулы (10)
Альтернативным способом получения соединений формулы (10) является получение из промежуточного соединения формулы (14), получение которого показано ниже на схеме реакции 3.
где R1' описан на схеме 1.
Получение соединений формулы (14)
Арилбромидное соединение формулы (9) реагирует с небольшим избытком бис(пинаколято)дибора в органическом растворителе, предпочтительно диметил сульфоксиде, содержащем палладиевый катализатор, предпочтительно дихлорметановый аддукт дихлор(1,1'-бис(дифенилфосфино)ферроцен)палладия (II), и избыток ацетата калия. Реакцию проводят при повышенной температуре, предпочтительно около 80°С, в течение около 2-24 часов, предпочтительно около 2 часов. Продукт формулы (14) выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
Получение соединений Формулы (10)
Исходные винилбромидные, винилйодидные или винилтрифлатные соединения формулы (15) могут быть коммерчески доступны, например от Fluka, или могут быть получены способами, известными из уровня техники.
Один способ получения соединений формулы (10) заключается в обработке соединения формулы (14) соединением формулы (15) в присутствии палладиевого катализатора, предпочтительно дихлорметанового аддукта дихлор(1,1'-бис(дифенилфосфино)ферроцен)палладия (II), и неорганического основания, предпочтительно карбоната натрия. Реакцию проводят в смеси растворителей, предпочтительно в смеси этанола, толуола и воды, реакцию проводят при повышенной температуре, предпочтительно около 80°С, в течение около 0,1-2 часов, предпочтительно около 20 минут. Продукт формулы (10) выделяют обычными методами и предпочтительно очищают с помощью хроматографии или перекристаллизации.
где R2 имеет значения, описанные выше.
Получение соединений, описанных в вышеупомянутых схемах, проводят обычными способами.
Использовались следующие сокращения:
| HATU | гексафторфосфат O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония |
| ДМСО | диметилсульфоксид |
| ДМАП | 4-диметиламинопиридин |
| ТГФ | тетрагидрофуран |
Выделение и очистка соединений
Выделение и очистка описанных здесь соединений и промежуточных соединений могут производиться, при необходимости, любой подходящей процедурой разделения или очистки, такими как, например, фильтрация, экстракция, кристаллизация, колоночная хроматография, тонкослойная хроматография, толстослойная хроматография, препаративная жидкостная хроматография низкого или высокого давления или комбинацией этих процедур. Конкретные примеры подходящих процедур разделения и выделения можно обнаружить ниже в разделе Получение и Примеры. Однако, конечно, могут также использоваться другие эквивалентные процедуры разделения или выделения.
Соли соединений Формулы I
Соединения формулы I могут являться основаниями, например, когда остаток R содержит основную группу, такую как алифатическая или ароматическая аминогруппа. В таких случаях соединения формулы I могут быть преобразованы в соответствующую кислотную аддитивную соль.
Преобразование проводят обработкой по крайней мере стехиометрическим количеством соответствующей кислоты, такой как соляная кислота, бромоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п., и органических кислот, таких как уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, яблочная кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, манделиновая кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота и т.п. Обычно свободное основание растворяют в инертном органическом растворителе, таком как диэтиловый эфир, этилацетат, хлороформ, этанол или метанол и т.п., и добавляют кислоту в подобном растворителе. Температуру поддерживают между 0°С и 50°С. Полученную соль осаждают самостоятельно или могут перенести в раствор менее полярного растворителя.
Кислотно-аддитивные соли основных соединений формулы I могут быть преобразованы в соответствующие свободные основания обработкой по крайней мере стехиометрическим эквивалентом подходящего основания, такого как гидроксид натрия или калия, карбонат калия, бикарбонат натрия, аммиак и т.п.
Соединения формулы I и их фармацевтически приемлемые аддитивные соли обладают ценными фармакологическими свойствами. Конкретно, было обнаружено, что соединения согласно настоящему изобретению являются лигандами аденозинового рецептора и обладают высоким сродством к аденозиновому рецептору A2A.
Соединения были исследованы в соответствии с испытанием, приведенным далее.
Аденозиновый рецептор А2A человека
Аденозиновый рецептор А2A человека рекомбинантно экспрессировали в клетках яичников китайского хомячка (СНО), используя систему экспрессии вируса semliki forest. Клетки собирали, промывали дважды центрифугированием, гомогенизировали и снова промывали центрифугированием. Полученный промытый мембранный остаток суспендировали в буфере Tris (50 мМ), содержащем 120 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2 и 10 мМ MgCl2 (pH 7,4) (буфер А). Испытание связывания с [3H]-SCH-58261 (Dionisotti и др., 1997, Br J Pharmacol 121, 353; 1 нМ) проводили в 96-ячеечных планшетах в присутствии 2,5 мкг мембранного белка, 0,5 мг шариков Ysi-поли-1-лизина SPA и 0,1 U аденозиндеаминазы в конечном объеме буфера А 200 мкл. Неспецифическое связывание определяли с помощью представителей ксантинамина (ХАС; 2 мкМ). Соединения проверяли при 10 концентрациях от 10 мкМ до 0,3 нМ. Все испытания проводили дважды и повторяли по крайней мере два раза. Испытательные планшеты инкубировали в течение 1 часа при комнатной температуре перед центрифугированием и затем определяли связавшийся лиганд, используя сцинтилляционный счетчик Packard Topcount. Значения IC50 рассчитывали с помощью программы подгонки нелинейной кривой и значения Ki рассчитывали с помощью уравнения Cheng-Prussoff.
Предпочтительные соединения показывают pKi>8,0.
| № Примера | hA2 (pKi) | № Примера | hA2 (pKi) |
| 1 | 8,31 | 25 | 8,80 |
| 2 | 7,94 | 28 | 8,97 |
| 3 | 8,85 | 31 | 8,84 |
| 4 | 8,76 | 32 | 8,56 |
| 5 | 8,55 | 33 | 8,78 |
| 6 | 9,12 | 34 | 8,74 |
| 7 | 8,96 | 35 | 8,67 |
| № Примера | hA2 (pKi) | № Примера | hA2 (pKi) |
| 8 | 8,62 | 36 | 8,93 |
| 11 | 8,30 | 39 | 8,42 |
| 12 | 8,50 | 40 | 8,47 |
| 17 | 8,20 | 41 | 8,47 |
| 18 | 8,10 | 42 | 8,69 |
| 19 | 8,40 | 43 | 8,91 |
| 20 | 8,60 | 44 | 8,82 |
| 21 | 8,40 | 45 | 8,79 |
| 22 | 8,00 | 46 | 9,06 |
| 23 | 9,70 | 47 | 8,82 |
| 24 | 8,80 |
Соединения формулы I и фармацевтически приемлемые соли соединений формулы I могут использоваться в качестве лекарственных средств, например, в форме фармацевтических составов. Фармацевтические составы могут вводиться перорально, например, в форме таблеток, покрытых таблеток, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Введение, однако, может также осуществляться ректально, например, в форме свечей, парентерально, например, в форме инъекционных растворов.
Соединения формулы I могут быть обработаны фармацевтически инертными, неорганическими или органическими носителями для получения фармацевтических составов. Например, в качестве носителей для таблеток, покрытых таблеток, драже и твердых желатиновых капсул могут использоваться лактоза, кукурузный крахмал или его производные, тальк, стеариновые кислоты или их соли и т.п. Подходящими носителями для мягких желатиновых капсул являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п. В зависимости от природы активного вещества, однако, обычно не требуется никаких носителей для мягких желатиновых капсул. Подходящими носителями для получения растворов и сиропов являются, например, вода, полиолы, глицерин, растительное масло и т.п. Подходящими носителями для свечей являются, например, природные или закрепляющие масла, воски, жиры, полужидкие или жидкие полиолы и т.п.
Фармацевтические составы, кроме того, могут содержать консерванты, солюбилизаторы, стабилизаторы, увлажняющие агенты, эмульсификаторы, подслащивающие вещества, красители, отдушки, соли для изменения осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они также могут содержать другие терапевтически полезные вещества.
Лекарственные средства, содержащие соединение формулы I или его фармацевтически приемлемую соль и терапевтически инертный носитель, являются также объектом настоящего изобретения, а также способ их получения, который включает введение одного или нескольких соединений формулы I и/или фармацевтически приемлемых кислотных аддитивных солей и, при необходимости, одного или нескольких других терапевтически полезных веществ в галеновую форму введения вместе с одним или несколькими терапевтически инертными носителями.
В соответствии с изобретением соединения формулы I, а также их фармацевтически приемлемые соли, полезны для контролирования или предотвращени