Гетероциклические дигидропиримидиновые соединения
Иллюстрации
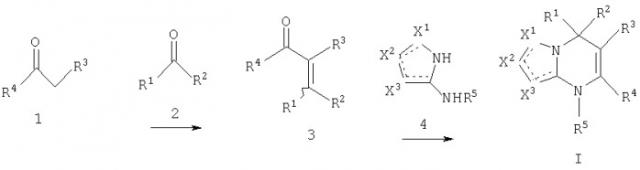
Показать всеНастоящее изобретение относится к дигидропиримидиновым соединениям формулы I*
их энантиомерам, диастереоизомерам и фармацевтически приемлемым солям, где Х1, X2 и X3 вместе с атомами, к которым они присоединены, образуют кольцо
R1 представляет собой водород; R2, R3*, R4, R5, R6 и R7 имеют значения, указанные в п.1 формулы изобретения. Кроме того, объектами изобретения являются отдельные дигидропиримидиновые соединения. Предложенные соединения являются ингибиторами функции кальциевого канала, особенно ингибиторами Кv1 подсемейства потенциал-перекрывающих K+ каналов, особенно ингибиторами Кv1.5, которые связаны со сверхбыстрым активирующим замедленным очистительным K+ потоком Ikur и могут быть использованы для лечения аритмии и Ikur связанных заболеваний. 4 н. и 11 з.п. ф-лы.
Реферат
Область изобретения
Настоящее изобретение относится к гетероциклическим дигидропиримидиновым соединениям, пригодным в качестве ингибиторов функции калиевого канала (особенно ингибиторов КV1 подсемейства потенциал-перекрывающих К+ каналов, более конкретно ингибиторов КV1.5, которые были связаны со сверхбыстро активирующим замедленным очистительным K+ потоком IKUR) и к фармацевтическим композициям, содержащим такие соединения. Настоящее изобретение далее относится к способам применения таких соединений для лечения аритмии, IKUR-связанных заболеваний и других заболеваний, опосредованных функцией ионного канала.
Предпосылки изобретения
Важность калиевых каналов была впервые исследована приблизительно пятьдесят лет назад, когда Hodgkin и Huxley обнаружили, что ионы калия вливаются в поток, который возбуждает головной гигантский аксон. Исследование в этой области, однако, затруднялось отсутствием селективных, высоко специфичных лигандов для калиевых каналов. Но с приходом технологий рекомбинантной ДНК и технологий сжатого напряжения отдельной клетки, а также всей клетки медленный темп развития в этой области изменился. Действительно, калиевые каналы, которые проявляют функциональные, фармакологические характеристики и характеристики распределения ткани, были клонированы. Указанные клонированные калиевые каналы являются полезными мишенями в испытаниях на идентификацию соединений-кандидатов для лечения различных заболеваний. Калиевые каналы, как оказалось, являются наиболее разнообразным семейством ионных каналов, открытых в настоящее время. Они модулируют ряд клеточных взаимодействий, таких, как сокращение мышц, нейроэндокринную секрецию, частоту и продолжительность действующих потенциалов, электролитный гомеостаз и остаточный мембранный потенциал.
Калиевые каналы экспрессируются в эукариотических и прокариотических клетках и являются элементами контроля электрических и неэлектрических клеточных функций. Калиевые каналы классифицируются в соответствии с их биофизическими и фармакологическими характеристиками. Подклассы указанных каналов называются на основании аминокислотной последовательности и функциональных свойств. Выдающимися среди них являются потенциал-зависимые калиевые каналы, например потенциал-перекрывающие калиевые каналы (например, Kv1, КV2, КV3, Кv4). Подтипы в этих подклассах характеризуются по их предполагаемой функции, фармакологии и распределению в клетках и тканях (Chandy и Gutman, "Voltage-gated potassium channel genes" in Handbook of Receptors и Channels - Ligand и Voltage-gated Ion Channels, ed. R.A. North, 1995; Doupnik и др., Curr. Opin. Neurobiol. 5:268, 1995). Например, Kv1 класс калиевых каналов далее подразделяется в зависимости от молекулярной последовательности канала, например KV1.1, KV1.2, KV1.3, KV1.4, K.V1.5, КV1.6 и КV1.7. Функциональные потенциал-перекрывающие К+ каналы могут существовать в качестве мультимерных структур, образованных при взаимодействии идентичных или различных субъединиц. Этот феномен, как считается, объясняет широкое разнообразие К+ каналов. Однако субъединичные составы природных К+ каналов и физиологическая роль, которую выполняют отдельные каналы, в большинстве случаев, все еще неясна.
Мембранная деполяризация K.V1.3 ингибиторами, как было показано, является эффективным способом предотвращения Т-клеточной пролиферации, и, следовательно, используется во многих аутоиммунных условиях. Ингибирование К+ каналов в плазматической мембране человеческих Т-лимфоцитов, как было установлено, играет роль при вызове иммуносупрессорных ответов при регулировании внутриклеточного Са++ гомеостаза, который, как было обнаружено, является важным в Т-клеточной активации.
KV1.3 перекрывающий напряжение калиевый канал обнаружен в нейронах, клетках крови, остеокластах и Т-лимфоцитах. Chandy и Cahalan лаборатории выдвинули гипотизу, что блокирование KV1.3 канала вызывает иммуносупрессорный ответ (Chandy и др., J. Exp. Med. 160, 369, 1984; Decoursey и др., Nature, 307, 465, 1984). Однако блокаторы K+ канала, применяемые на этих стадиях, были неселективными. До испытаний с пептидом маргатоксином, пептидом, обнаруженном в яде скорпиона, не существовало специфического ингибитора KV1.3 канала для тестирования этой гипотезы. Хотя лаборатория (Price и др., Proc.Natl, Acad, Sci. USA, 86, 10171, 1989) показала, что харибдотоксин блокирует KV1.3 в человеческих Т-клетках, харибдотоксин, как было позже показано, ингибирует четыре различных К+ канала (KV1.3 и три других малой проводимости Ca+ активированных K+ канала) в человеческих Т-лимфоцитах, ограничивая применение этого токсина в качестве пробы для определения физиологической роли KV1.3 (Leonard и др., Ргос. Natl, Acad. Sci, USA, 89, 10094, 1992). Маргатоксин, с другой стороны, блокирует только КV1.3 в Т-клетках и имеет иммуносупрессорную активность как в in vitro, так и in vivo моделях (Lin и др., J. exp. Med, 177,637, 1993). Терапевтическая пригодность этих соединений, однако, ограничена их сильной токсичностью. Недавно сообщалось о классе соединений, который может быть хорошей альтернативой вышеуказанным лекарственным средствам, смотри, например, US 5670504; 5631282; 5696156; 5679705 и 5696156. Хотя решены некоторые проблемы активности/токсичности указанных выше лекарственных средств, эти соединения имеют большой молекулярный вес и обычно получаются синтетическим способом из природного продукта, выделение которых является обременительным и трудоемким.
Иммунорегуляторные нарушения, как было показано, присутствуют в широком ряду аутоиммунных и хронических воспалительных заболеваний, включая системную красную волчанку, хронический ревматоидный артрит, сахарный диабет I и II типа, воспалительные кишечные заболевания, цирроз печени, увеит, рассеянный склероз и другие заболевания, такие как болезнь Крона, язвенный колит, пузырьковый амфигоид, саркоидоз, псориаз, ихтиоз, офтальмопатия Грейвза и астма.
Хотя базовый патогенез каждого из этих состояний может быть различным, в них во всех появляются различные аутоантитела и полуреактивные лимфоциты. Такая полуреактивность может быть обусловлена, частично, отсутствием контроля гомеостаза, при котором функционирует нормальная иммунная система. Также, используя трансплантацию костного мозга или органа, лимфоциты хозяина распознают чужеродные тканевые антигены и начинают производить антитела, которые приводят к отторжению пересаживаемого органа.
С одной стороны, результатом аутоиммунного процесса или процесса отторжения является отторжение ткани, вызванное воспалением клеток и освобождаемых медиаторов. Антивоспалительные агенты, такие как NSAID's, действуют принципиально, блокируя действия или секрецию указанных медиаторов, но не изменяют иммунологическую основу заболевания. С другой стороны, цитотоксические агенты, такие, как циклофосфамид, действуют таким неспецифическим образом, что изолируют нормальный и аутоиммунный ответы. Наконец, пациенты, которых лечат такими неспецифическими иммуносуппрессорными агентами, вероятно, подвергаются инфекции во время их аутоиммунных заболеваний.
Циклоспорин A (CsA), который был утвержден US FDA в 1983, в настоящее время является лидирующим лекарственным средством, использующимся для предотвращения отторжения трансплантируемых органов. В 1993, FK-506 (Prograf) был утвержден US FDA для предотвращения отторжения при трансплантации печени. CsA и FK-506 ингибируют иммунную систему организма от мобилизации его громадного запаса природных защитных агентов до отторжения чужеродного протеина трансплантата. В 1994 CsA утвержден US FDA для лечения тяжелого псориаза и утвержден European regulatory agencies для лечения поверхностного дерматита. Хотя они являются эффективными для борьбы с отторжением трансплантанта, CsA и FK-506, как известно, вызывают некоторые нежелательные побочные эффекты, включая нефротоксичность, нейротоксичность и гастрокишечное расстройство. Следовательно, все еще остается потребность в получении селективного иммуносупрессанта без этих побочных эффектов. Ингибиторы калиевого канала обещают решить эту проблему.
Фибрилляция предсердия (AF) и колебание предсердия являются наиболее распространенными сердечными аритмиями в клинической практике и увеличиваются в соответствии с возрастом населения. В настоящее время AF поражает более 1 миллиона американцев ежегодно, что составляет более 5% от всех кардиососудистых заболеваний и вызывает более чем 80000 случаев паралича в США. В то время, как AF редко является летальной аритмией, она ответственна за высокую заболеваемость и может приводить к осложнениям, таким, как развитие закупорочной сердечной недостаточности или тромбоэмболизма. В настоящее время доступные антиаритмические лекарственные средства класса I и класса III снижают скорость повторения AF, но они имеют ограниченное применение из-за различных потенциально вредных эффектов, включая проаритмию желудочка. Так как настоящая терапия является неадекватной и чревата побочными эффектами, существует определенная потребность в развитии новых терапевтических подходов.
Антиаритмические агенты класса III являются лекарственными средствами, которые вызывают селективную пролонгированность продолжительности действия потенциала без значительной сердечной депрессии. Доступные лекарственные средства этого класса ограничены. Примеры, такие как соталол и амиодарон, как было показано, обладают интересными свойствами класса III (Singh B.N., Vaughan Williams E.M. "A Third Class of Anti-Arrhythmic Action: Effects On Atrial And Ventricular Intracellular Potentials And Other Pharmacological Actions On Cardiac Muscle, of MJ 1999 And AH 3747" Br. J. Pharmacol 1970; 39:675-689, и Singh B.N., Vaughan Williams E.M, "The Effect of Amiodarone, A New Anti-Anginal Dru г, On Cardiac Muscle", Br J. Pharmacol 1970; 39:657-667), но они не являются селективными агентами класса III.
Соталол также обладает действиями класса II, которые могут вызывать сердечную депрессию и противопоказаны определенным восприимчивым пациентам. Амиодарон также не является селективным антиаритмическим агентом класса III, так как он обладает накапливающимся электрофизиологическим действием и строго ограничен из-за побочных эффектов (Nademanee, К. "The Amiodarone Odessey". J. Am. Coll. Cardiol. 1992;20:1063-1065.) Лекарственные средства этого класса, как ожидается, являются эффективными для предотвращения фибрилляции желудочка. Селективные агенты класса III, при определении, как считается, не вызывают миокардиологическую депрессию или индукцию аритмии, обусловленную ингибированием проводимости действующего потенциала, как показано для антиаритмических агентов класса I.
Агенты класса III повышают миокардиологическую устойчивость посредством пролонгирования потенциала продолжительности сердечного действия. Теоретически, пролонгация потенциала сердечного действия может быть достигнута увеличением внутренних потоков (то есть Na+ или Са2+ потоков; здесь и далее INa и ICa соответственно) или снижением внешних реполяризационных калиевых (К+)потоков. Препятствующая очистка (IK) К+ потока является основным внешним потоком, включенным в общий реполяризационный процесс во время действия потенциального плато, тогда как временный внешний (Ito) и внутренний очистительный (IKI)K+ потоки являются ответственными за быструю начальную и конечную фазы реполяризации соответственно. Изучение клеточной электрофизиологии показало, что IK состоит из двух фармакологически и кинетически различных К+ подтипов потока, Ikr (быстрая активация и дезактивация) и Iks (медленная активация и дезактивация) (Sanguinetti и Jurkiewicz, Two Components Of Cardiac Delayed Rectifier K+ Current: Differential Sensitivity To Block Class III Antiarrhythmic Agents, J Gen Physiol 1990, 96:195-215). Антиаритмические агенты класса III, разрабатываемые в настоящее время, включая d-соталол, дофетилид (UK-68798), алмокалант (Н234/09), Е-4031 и метансульфонамид-N-[1'-6-циано-1,2,3,4-тетрагидро-2-нафталенил)-3,4-дигидро-4-гидроксиспиро[2Н-1-бензопиран-2,4'-пиперидин]-6-ил]монохлорид, в основном, если не полностью, блокируют Ikr. Хотя амиодарон является блокатором Iks (Balser J.R, Bennett, P.B., Hondeghem, L.M. и Roden, D.M. "Suppression Of Time-Dependent Outward Current In Guinea Pig Ventricular Myocytes: Actions Of Quinidine And Amiodarone. Circ. Res. 1991, 69:519-529), он также блокирует INa и ICa, выполняя тироидную функцию, в качестве неспецифического адренергического блокатора и действует в качестве ингибитора фермента фосфолипазы (Nademanee, К. "The Amiodarone Odessey" J. Am. Coll.Cardiol. 1992;20:1063-10б5). Следовательно, этот способ лечения аритмии является неопределенным. Большинство агентов класса III, которые, как известно, находятся в разработке, в основном блокируют Ikr.
Входящее возбуждение (вход), как было показано, является значительным механизмом, лежащим в основе аритмий желудочка у человека. Входящее возбуждение требует критического баланса между медленной скоростью проводимости и достаточно короткими устойчивыми периодами, позволяющим инициацию и поддержку складываемых входящих кругооборотов для сосуществования одновременно и поддержки AF. Увеличение сердечной устойчивости при пролонгировании потенциала продолжительности действия (APD), предотвращает и/или завершает входящую аритмию. Большинство селективных антиаритмических агентов класса III, разрабатываемых в настоящее время, таких, как d-соталол и дофетилид, в основном, если не полностью, блокируют Ikr, быстро активируя компонент IK, обнаруженный в предсердии и желудочке человека.
Так как эти Ikr блокаторы повышают APD и устойчивость как в предсердии, так и в желудочке, без осуществления проводимости как таковой, теоретически они представляют собой потенциально пригодные агенты для лечения аритмии, такой как AF. Эти агенты имеют склонность к тому, что они повышают риск проаритмий при медленных скоростях работы сердца. Например, трепетание-мерцание желудочков наблюдалась при использовании указанных соединений (Roden, D.M. "Current Status of Class m Antiarrhythmic Drug Therapy", Am J. Cardiol., 1993; 72:44B-49В). Этот завышенный эффект при медленных скоростях работы сердца называется "обратная частотная зависимость", и она противоположна частотно-независимому или частотно-зависимому действиям (Hondeghem, L.M. "Development of Class III Antiarrhythmic Agents". J.Cadiovasc.Cardiol. 20 (Suppl.2):S17-S22).
Медленно активирующий компонент, препятствующий очистке (Ikc), потенциально превосходит некоторые ограничения Ikr блокаторов, связанные с аритмией желудочка. Из-за их медленной кинетики активации, однако, роль Iks в реполяризации предсердия может быть ограничена благодаря относительно короткому APD предсердия. Следовательно, хотя Iks блокаторы могут обеспечить особое преимущество в случае аритмии желудочка, их способность воздействия на SVT, как считается, является минимальной.
Ультрабыстрая активация препятствующего очистительного К+ потока (Ikur), как полагают, представляет собой природный двойник клонированного калиевого канала, обозначенного Kv1.5 и, когда присутствует в предсердии человека, оказывается, отсутствует в желудочке человека. Более того, из-за быстроты активации и ограниченной медленной инактивации, Ikur, как полагают, делает значительный вклад в реполяризацию предсердия человека. Следовательно, специфический блокатор Ikur, который является соединением, которое блокирует Kv1.5, превосходит ненадолго пришедшие другие соединения по пролонгированию устойчивости при замедлении реполяризации в предсердии человека без образования препятствий в реполяризации желудочка, которая становится аритмогенной после деполяризаций и приобретает продолжительный QT синдром, наблюдаемый при лечении настоящими лекарственными средствами класса III.
В неповрежденных миоцитах предсердия человека ультрабыстрая активация препятствующего очистительного К+ потока Ikur, которая также известна как непрерывный внешний поток, Isus или Iso, идентифицируется и этот поток имеет свойства и кинетику, идентичные свойствам и кинетике, экспрессируемым клоном К+ канала человека (hKv1.5, HK2) при выделении из сердца человека и стабильно экспрессируется в человеческих (НЕК-293) клеточных линиях (Wang и др., 1993, Circ Res 73:1061-1076; Fedida и др., 1993, Circ Res 73:210-216; Snyders и др., 1993, J Gen Physiol 101:513-543) и обычно клонируется из мозга крысы (Swanson и др., 10, Neuron 4:929-939). Хотя различные антиаритмические агенты являются сейчас доступными на рынке, не были получены агенты, имеющие удовлетворительную эффективность и высокую надежность. Например, антиаритмические агенты класса I в соответствии с классификационной схемой Vaughan-Williams ("Classification Of Antiarrhythmic Drugs: In: Cardiac Arrhythmias, edited: E. Sandoe, E. Flensted-Jensen, K. Olesen; Sweden, Astra, Sodertalje, pp449-472, 1981), которые вызывают селективное ингибирование максимальной скорости движения вверх действующего потенциала (max), являются неподходящими для предотвращения фибрилляции желудочка. К тому же, они проблематичны в отношении безопасности, а именно, они вызывают депрессию сокращения миокарда и имеют тенденцию вызывать аритмию, вызванную ингибированием проводимости импульса. Бета-адренорецепторные блокаторы и кальциевые антагонисты, относящиеся к классу II и IV соответственно, имеют недостатки в том, что их действия являются либо ограниченными для конкретного типа аритмии или имеют противопоказания из-за их сердечных депрессивных свойств у определенных пациентов с кардиососудистым заболеванием. Их безопасность, однако, является более высокой, чем безопасность антиаритмических агентов класса I.
Сущность изобретения
Настоящее изобретение относится к гетероциклическим дигидропиримидиновым соединениям следующей формулы I, включая энантиомеры, диастареоизомеры и их соли, полезные в качестве ингибиторов функции калиевого канала (особенно ингибиторов Кv1 подсемейства потенциал-перекрывающих К+ каналов, более конкретно ингибиторов КV1.5, которые связаны со сверхбыстрым активирующим замедленным очистительным K+ потоком IKUR) для лечения заболеваний, таких, как аритмия и IKUR-связанных заболеваний:
где X1, X2 и X3 независимо выбирают из N, NR6, (CR7)q (CHR7)q или С=O, где связи, соединяющие Х1, X2 и Х3 с соседними атомами могут быть простыми или двойными связями, образующими от 5 до 7-членное насыщенное, частично ненасыщенное или ароматическое кольцо;
R1, R2, R3, R4, R5, R6 и R7 являются одинаковыми или различными и независимо выбираются из групп формулы -(CR2)n-(Z1)m-(CH2)p-Z2 или
R1, R2, R3, R4 и R5 могут, в одной или более парах двух (таких, как R1 и R2, R1 и R3, R2 и R3, R3 и R4 или R4 и R5), вместе с атомами, к которым они присоединены, образовывать карбоциклическую, замещенную карбоциклическую, гетероциклическую или замещенную гетероциклическую группу или
R6 и R7 могут, в одной или более парах двух (таких, как R6 и R7, R6 и R6 или R7 и R7), вместе с атомами, к которым они присоединены, образовывать карбоциклическую, замещенную карбоциклическую, гетероциклическую или замещенную гетероциклическую группу;
Z1 представляет собой -CZ3Z4-, -О-, -NZ3-, -S-, -SO-, -SO2-, -C(O)-, -C(O)Z3-, -C(O)NZ4, -C(S)-, -C(=NOZ3)-, алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, карбоцикло, замещенный карбоцикло, арил, замещенный арил, гетероцикло или замещенный гетероцикло;
Z2 представляет собой водород, -OZ5, -OC(O)Z5, -NZ5-C(O)-Z6, -NZ5-CO2-Z6, -NZ5(C=O)-NZ6Z7, -NZ5Z6, -NO2, галоген, -CN, -C(O)Z5, -CO2Z5, -C(S)Z5, -(C=NOZ5)Z6, -C(O)NZ5Z6, -C(S)NZ5Zб, -SZ5, -SOZ5, -SO2Z5, -SO2NZ5Z6, алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, карбоцикло, замещенный карбоцикло, арил, замещенный арил, гетероцикло (такой, как гетероарил), или замещенный гетероцикло;
Z3, Z4, Z5, Z6 и Z7 независимо представляют собой водород, галоген, алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, карбоцикло, замещенный карбоцикло, арил, замещенный арил, гетероцикло или замещенный гетероцикло или
Z3, Z4, Z5, Z6 и Z7 могут, в одной или более парах двух (таких, как Z3 и Z4, Z5 и Z6 или Z6 и Z7), вместе с атомом, к которому они присоединены, образовывать карбоциклическую, замещенную карбоциклическую, гетероциклическую или замещенную гетероциклическую группу;
n и р независимо выбирают из целых чисел от 0 до 10 при этом, когда m является 0, р является также 0;
m является целым числом, выбранным из 0 или 1 и
q является целым числом, выбранным от 1 до 3.
Настоящее изобретение относится к новым способам профилактики и лечения аритмии и IKur-связанных заболеваний, при использовании одного или более соединений формулы I, энантиомеров, диастареоизомеров или их фармацевтически приемлемых солей. Особенно настоящее изобретение относится к новому способу селективного предотвращения и лечения аритмии желудочка.
Кроме того, соединения, входящие в формулу I, так же как энантиомеры, диастареоизомеры и их соли, являются новыми соединениями, включая соединения формулы I* и их соли:
где X1, X2, X3, R1, R2, R4 и R5 являются такими, как определено выше;
R3* представляет собой -OZ5, -OC(O)-Z5, -NZ5-C(O)2-Z6, -NZ5(C=O)-NZ6Z7, -NZ5Z6, -(C=NOZ5)Z6, -C(O)NZ5*Z6*, -C(S)NZ5*Z6*, -SZ5, -SOZ5, -SO2Z5, -SO2NZ5Z6, -C(O)Z3*-Z2*, галоген, алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, карбоцикло, замещенный карбоцикло, арил, замещенный арил, гетероцикло или замещенный гетероцикло;
Z2* не является водородом, когда Z3* представляет собой гетероцикло; Z3* представляет собой гетероцикло или замещенный гетероцикло;
Z5* представляет собой замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, карбоцикло, замещенный карбоцикло, арил, замещенный арил, гетероцикло или замещенный гетероцикло и
Z6* представляет собой водород, алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, карбоцикло, замещенный карбоцикло, арил, замещенный арил, гетероцикло или замещенный гетероцикло, при условии, что Z6* не является водородом, когда Z5* представляет собой незамещенный циклоалкил, незамещенный арил или незамещенный бензил,
или Z5* и Z6* вместе с атомом азота, к которому они присоединены, могут образовывать гетероциклическую группу или замещенную гетероциклическую группу при условии, что Z5* и Z6* не образуют вместе незамещенный пиперидинил, незамещенный пирролидинил или незамещенный морфолинил и далее при условии, что когда
(i) R1 и R5 каждый представляет собой водород и
(ii) R2 представляет собой арил или замещенный арил и
(iii) R4 представляет собой гетероциклозамещенный арил и
(iv) X1, X2 и X3 образуют кольцо
где R7* представляет собой Н или алкил,
Z5* и Z6* вместе не образуют незамещенный пиперазинил или N-алкилзамещенный пиперазинил.
Предпочтительные соединения
Соединения формулы I и их соли, где один или более, и особенно все, из X1, X2, X3, R1, R2, R3, R4 и R5 выбираются из следующих значений, являются предпочтительными соединениями настоящего изобретения:
R1 представляет собой водород;
R2 представляет собой водород, алкил, замещенный алкил, арил, замещенный арил, гетероцикло, замещенный гетероцикло, карбоцикло или замещенный карбоцикло;
R3 представляет собой -(CH2)n-Z2, -(CH2)n-C(O)Z3-(CH2)p-Z2 или -(СН2)n-С(O)NZ4-(СН2)р-Z2;
R4 представляет собой алкил или замещенный алкил;
R5 представляет собой водород или -(СН2)n-Z2 и
X1, X2 и X3 вместе с атомами, к которым они присоединены, образуют кольцо, выбранное из
где R6 и/или R7 являются одинаковыми или различными, как определено выше.
Соединения формулы I и их соли, где один или более, и особенно все, из X1, X2, X3, R1, R2, R3, R4 и R5 выбирают из следующих значений, являются более предпочтительными соединениями настоящего изобретения:
R1 представляет собой водород;
R2 представляет собой арил (особенно, если арил представляет собой фенил), замещенный арил, гетероцикло, замещенный гетероцикло, карбоцикло или замещенный карбоцикло;
R3 представляет собой -(CH2)n-Z2, -(СН2)n-С(О)Z3-(CH2)р-Z2 или -(СН2)n-С(O)NZ4-(CH2)p-Z2, где
Z2 выбирают из -C(O)NZ5Z6, -CO2Z5, -SO2Z5, -NZ5Z6, -NZ5CO2Z6, -NZ5C(O)Z6, -OZ5, арил, замещенный арил, гетероцикло, замещенный гетероцикло, алкил или замещенный алкил;
Z3 представляет собой гетероцикло или замещенный гетероцикло и n и p независимо выбирают из целых чисел от 0 до 3;
R4 представляет собой алкил или замещенный алкил;
R5 представляет собой водород или -(CH2)n-Z2, где Z2 выбирают из-C(O)NZ5Z6, -СО2Z5, -NZ5Z6, арила, замещенного арила, алкила или замещенного алкила и
X1, X2 и X3, вместе с атомами, к которым они присоединены, образуют кольцо, выбранное из
Соединения формулы I и их соли, где один или более, и особенно все, из X1, X2, X3, R1, R2, R3, R4 и R5 выбирают из следующих значений, являются наиболее предпочтительными соединениями настоящего изобретения:
R1 представляет собой водород;
R2 представляет собой арил (особенно, если арил представляет собой фенил), замещенный арил, гетероцикло, замещенный гетероцикло, карбоцикло или замещенный карбоцикло;
R3 представляет собой гетероцикло или замещенный гетероцикло, -C(O)NZ5Z6, -C(O)Z3-CONZ5Z6, -C(O)Z3-Z2 или -C(O)Z3-CO2Z5, где Z3 представляет собой гетероцикло или замещенный гетероцикло и Z2 представляет собой арил или замещенный арил;
R4 представляет собой алкил (особенно низший алкил) или замещенный алкил (особенно галогензамещенный алкил или алкоксизамещенный алкил);
R5 представляет собой водород, алкил или замещенный алкил и
X1, X2 и X3, вместе с атомами, к которым они присоединены, образуют кольцо, выбранное из
где R6 представляет собой Н или C(O)Z5, где Z5 представляет собой алкил или карбоцикло, и
R7 независимо выбирают из Н, алкила, замещенного алкила (особенно галогенамещенного), галогена или CN.
Подробное описание изобретения
Далее приводятся определения терминов, использующихся в этом описании. Начальное определение, относящееся здесь к группе или термину, применимо к такой группе или термину в настоящем описании, отдельно или в виде части другой группы, если не указано иначе.
Термины "алк" или "алкил" относятся к линейным или разветвленным цепочечным углеводородным группам, имеющим от 1 до 12 атомов углерода, предпочтительно от 1 до 8 атомов углерода, таким как метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, пентил, гексил, гептил, октил и т.д. Низшие алкильные группы, такие как алкильные группы с 1 - 6 атомами углерода, являются обычно наиболее предпочтительными. Термин "замещенный алкил" относится к алкильным группам, замещенным одной или более группами (такими, как группы, указанные выше при определении R1), которые предпочтительно выбирают из арила, замещенного арила, гетероцикло, замещенного гетероцикло, карбоцикло, замещенного карбоцикло, галогена, гидрокси, алкокси (необязательно замещенного), арилокси (необязательно замещенного), алкилэфира (необязательно замещенного), арилэфира (необязательно замещенного), алканоила (необязательно замещенного), арила (необязательно замещенного), циано, нитро, амино, замещенного амино, амидо, лактама, мочевины, уретана, сульфонила и т.д.
Термин "алкенил" относится к линейным или разветвленным цепочечным углеводородным группам, имеющим от 2 до 12 атомов углерода, предпочтительно от 2 до 4 атомов углерода, и по крайней мере одну двойную углерод-углеродную связь (цис или транс), таким как этенил. Термин "замещенный алкенил" относится к алкенильным группам, замещенным одной или более группами (такими, как группы, описанные выше при определении R1), предпочтительно выбираемыми из арила, замещенного арила, гетероцикло, замещенного гетероцикло, карбоцикло, замещенного карбоцикло, галогена, гидрокси, алкокси (необязательно замещенного), арилокси (необязательно замещенного), алкилэфира (необязательно замещенного), арилэфира (необязательно замещенного), алканоила (необязательно замещенного), ариола (необязательно замещенного), циано, нитро, амино, замещенного амино, амидо, лактама, мочевины, уретана, сульфонила и т.д.
Термин "алкинил" относится к линейным или разветвленным цепочечным углеводородным группам, имеющим от 2 до 12 атомов углерода, предпочтительно от 2 до 4 атомов углерода, и по крайней мере одну тройную углерод-углеродную связь, таким как этинил. Термин "замещенный алкинил" относится к алкинильным группам, замещенным одной или более группами (такими, как группы, описанные выше при определении R1), предпочтительно выбираемыми из арила, замещенного арила, гетероцикло, замещенного гетероцикло, карбоцикло, замещенного карбоцикло, галогена, гидрокси, алкокси (необязательно замещенного), арилокси (необязательно замещенного), алкилэфира (необязательно замещенного), арилэфира (необязательно замещенного), алканоила (необязательно замещенного), ариола (необязательно замещенного), циано, нитро, амино, замещенного амино, амидо, лактама, мочевины, уретана, сульфонила и т.д.
Термины "ар" или "арил" относятся к ароматическим гомоциклическим (т.е. углеводородным) моно-, би- или трициклическим кольцевым группам, предпочтительно имеющим от 6 до 12 членов, таким как фенил, нафтил и бифенил. Фенил является предпочтительной арильной группой. Термин "замещенный арил" относится к арильным группам, замещенным одной или более группами (такими, как группы, описанные выше при определении R1), предпочтительно выбираемые из алкила, замещенного алкила, алкенила (необязательно замещенного), арила (необязательно замещенного), гетероцикло (необязательно замещенного), галогена, гидрокси, алкокси (необязательно замещенного), арилокси (необязательно замещенного), алканоила (необязательно замещенного), ароила (необязательно замещенного), алкилэфира (необязательно замещенного), арилэфира (необязательно замещенного), циано, нитро, амино, замещенного амино, амидо, лактама, мочевины, уретана, сульфонила и т.д., где необязательно одна или более пар заместителей вместе с атомами, к которым они присоединены, образуют 3-7 членное кольцо.
Термины "циклоалкил" и "циклоалкенил" относятся к моно-, би- или три гомоциклическим кольцевым группам с 3 - 15 атомами углерода, которые являются соответственно полностью насыщенными и частично ненасыщенными. Термин "циклоалкенил" включает би- и трициклические кольцевые системы, которые не являются ароматическими, но содержат ароматические части (например, флуорен, тетрагидронафтален, дигидроинден и им подобные). Кольца поликольцевых циклоалкильных групп могут быть конденсированными, мостиковыми и/или соединенньми через одну или более спироединиц. Термины "замещенный циклоалкил" и "замещенный циклоалкенил" относятся соответственно к циклоалкильным и циклоалкенильным группам, замещенным одной или более группами (такими, как группы, описанные выше при определении R1), предпочтительно выбранным из арила, замещенного арила, гетероцикло, замещенного гетероцикло, карбоцикло, замещенного карбоцикло, галогена, гидрокси, алкокси (необязательно замещенного), арилокси (необязательно замещенного), алкилэфира (необязательно замещенного), арилэфира (необязательно замещенного), алканоила (необязательно замещенного), ариола (необязательно замещенного), циано, нитро, амино, замещенного амино, амидо, лактама, мочевины, уретана, сульфонила и т.д.
Термины "карбоцикло", "карбоциклическая" или "карбоциклическая группа" относятся к циклоалкильным и циклоалкенильным группам. Термины "замещенный карбоцикло", "замещенная карбоциклическая" или "замещенная карбоциклическая группа" относятся к карбоцикло или карбоциклическим группам, замещенным одной или более группами, как определено при определении циклоалкила и циклоалкенила.
Термины "галоген" и "гало" относятся к фтору, хлору, брому и йоду.
Термины "гетероцикл", "гетероциклический", "гетероциклическая группа" или "гетероцикло" относятся к полностью насыщенным или частично или полностью ненасыщенным, включая ароматические ("гетероарил"), или неароматические циклические группы (например, 3 - 13 членную моноциклическую, 7 - 17 членную бициклическую или 10 - 20 членную трициклическую кольцевую систему, предпочтительно содержащую всего от 3 до 10 кольцевых атома), которые имеют по крайней мере один гетероатом в по крайней мере одном кольце, содержащем атом углерода. Каждое кольцо гетероциклической группы, содержащее гетероатом, может иметь 1, 2, 3 или 4 гетероатома, выбираемых из атомов азота, атомов кислорода и/или атомов серы, где гетероатомы азота и серы могут быть необязательно окислены и гетероатомы азота могут быть необязательно кватернизированы. Гетероциклическая группа может присоединяться по любому гетероатому или атому углерода кольца или кольцевой системы. Кольца поликольцевых гетероциклов могут быть конденсированными, мостиковыми и/или соединенными через одну или более спироединиц.
Примеры моноциклических гетероциклических групп включают азетидин, пирролидинил, пирролил, пиразолил, оксетанил, пиразолинил, имидазолил, имидазолинил, имидазолидинил, оксазолил, оксазолидинил, изоксазолинил, изоксазолил, тиазолил, тиадиазолил, тиазолидинил, изотиазолил, изотиазолидинил, фурил, тетрагидрофурил, тиенил, оксадиазолил, пиперидинил, пиперазинил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролодинил, 2-оксоазепинил, азепинил, 4-пиперидонил, пиридил, пиразинил, пиримидинил, пиридазинил, триазинил, тетрагидропиранил, тетразоил, триазолил, морфолинил, тиаморфолинил, тиаморфолинилсульфоксид, тиаморфолинилсульфон, 1,3-диоксолан и тетрагидро-1, 1-диоксотиенил,
и им подобные.
Примеры бициклических гетероциклических групп включают индолил, бензотиазолил, бензоксазолил, бензотиенил, хинуклидинил, хинолинил, тетрагидроизохинолинил, изохинолинил, бензимидазолил, бензопиранил, индолизинил, бензофурил, бензофуранил, дигидробензофуранил, хромонил, кумаринил, бензодиоксолил, дигидробензодиоксолил, бензодиоксинил, циннолинил, хиноксалинил, индазолил, пирролопиридил, фуропиридинил (такой, как фуро[2,3-c]пиридинил, фуро[3,2-b]пиридинил] или фуро[2,3-b]пиридинил), дигидроизоиндолил, дигидрохиназолинил (такой, как 3,4-дигидро-4-оксохиназолинил), тетрагидрохинолинил, азабициклоалкилы (такие, как 6-азабицикло[3.2.1]октан), азаспироалкилы (такие, как 1,4-диокса-8-азаспиро[4.5]декан), имидазопиридинил (такой, как имидазо[1,5-а]пиридин-3-ил), триазолопиридинил (такой, как 1,2,4-триазол[4,3-а]пиридин-3-ил) и гексагидроимидазопиридинил (такой, как 1,5,6,7,8,8а-гексагидроимидазо[1,5-а] пиридин-3-ил),
и им подобные.
Примеры трициклических гетероциклических групп включают карбазолил, бензидолил, фенантролинил, акридинил, фенантридинил, ксантенил и им подобные.
Термины "замещенный гетероцикл", "замещенный гетероциклический", "замещенная гетероциклическая группа" и "замещенный гетероцикло" относятся к