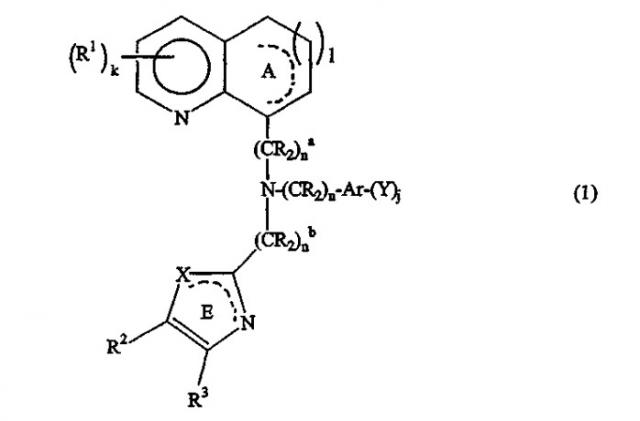
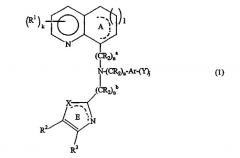
Гетероциклические соединения, моделирующие активность хемокинового рецептора, их применение и содержащая их фармацевтическая композиция
Иллюстрации
Показать всеИзобретение относится к новым соединениям формулы
и их солям,
в которой значения для R1, k, Ar, n, j, Y, R, R2 определены в формуле изобретения. Новые соединения модулируют активность хемокинового рецептора. Изобретение также относится к применению указанных соединений для лечения вируса иммунодефицита человека или вируса иммунодефицита кошачьих и к фармацевтической композиции на их основе. 10 н. и 6 з.п. ф-лы.
Реферат
По данной заявке испрашивается приоритет на основании 35 U.S.C. 119(e) по предварительной заявке 60/232891, поданной 15 сентября 2000; 60/234510, поданной 22 сентября 2000; заявке 0/233087, поданной 15 сентября 2000; и заявке 60/234816, поданной 22 сентября 2000. Содержание данных заявок включено в настоящее описание в качестве ссылок.
Область техники
Данное изобретение относится к новым соединениям, фармацевтическим композициям и их применению. Более конкретно данное изобретение относится к новым гетероциклическим соединениям, которые связываются с хемокиновыми рецепторами, включая CXCR4 и CCR5, и демонстрируют защитное действие против инфицирования клеток-мишеней вирусом иммунодефицита человека (ВИЧ).
Предпосылки создания изобретения
Описано примерно 40 хемокинов человека, которые функционируют, по крайней мере частично, путем модулирования комплекса и перекрывания последовательности биологических активностей, важных для движения лимфоидных клеток и транссудации и тканевой инфильтрации лейкоцитов в ответ на возбуждающие агенты (см., например, P.Ponath, Exp.Opin.Invest. Drugs, 7:1-18, 1998; Baggiolini M., Nature 393, 565-568 (1998); Locati et al., Annu. Rev. Med. 50, 425-40 (1999)). Такие хемотактические цитокины, или хемокины, составляют семейство белков размером приблизительно 8-10 кДа. Хемокины, очевидно, имеют часть общего структурного мотива, который составляет 4 сохраненных цистеина, включенных в поддержание третичной структуры. Имеется два основных подсемейства хемокинов: «СС», или β-хемокины, и «СХС», или α-хемокины. Рецепторы данных хемокинов классифицируют на основе хемокина, который создает природный лиганд рецептора. Рецепторы β-хемокинов обозначают «CCR», тогда как рецепторы α-хемокинов обозначают «CXCR».
Хемокины рассматриваются как основные медиаторы в инициировании и поддержании воспаления (см., «Chemokines in Disease», опубликованной Humana Press (1999), под редакцией C.Herbert; Murdoch et al., Blood 95, 3032-3042 (2000)). Более конкретно, установлено, что хемокины играют важную роль в регулировании функции эндотелиальной клетки, включая пролиферацию, миграцию и дифференцировку во время ангиогенеза и повторную эндотелиализацию после повреждения (Gupta et al., J. Biol. Chem., 7:4282-4287 (1998); Volin et al., Biochem. Biophys. Res. Commun., 242, 46-53 (1998)). Два конкретных хемокина вовлечены в этиологию инфицирования вирусом иммунодефицита человека (ВИЧ).
В большинстве случаев ВИЧ первоначально связывается через свой gp120 оболочечный белок с CD4 рецептором клетки-мишени. По-видимому, в gp120 происходит конформационное изменение, которое приводит к последующему связыванию с хемокиновым рецептором, таким как CCR5 (Wyatt et al., Science, 280:1884-1888 (1998); Rizzuto et al., Science, 280: 1949-1953 (1998); Berger et al. Annu.Rev.Immunol. 17:657-700 (1999)). ВИЧ-1 изолят (штамм) возникает впоследствии в инфекционном связывании с CXCR4 хемокиновым рецептором.
После первоначального связывания ВИЧ с CD4 происходит слияние вирус-клетка, которое опосредовано членами семейства хемокиновых рецепторов, где различные члены служат кофакторами слияния для магрофаг-тропных (М-тропных) и Т-клеточная линия-тропных (Т-тропных) штаммов ВИЧ-1 (Carroll et al., Science, 276: 273-276, 1997; Feng et al., Science 272, 872-877 (1996); Bleul et al., Nature 382, 829-833 (1996); Oberlin et al. Nature 382, 833-835 (1996); Cocchi et al., Science 270, 1811-1815 (1995); Dragic et al., Nature 381, 667-673 (1996); Deng et al., Nature 381, 661-666 (1996); Alkhatib et al., Science 272, 1955-1958 (1996)). Во время процесса инфицирования внутри организма пациента оказывается, что большинство ВИЧ-частиц переходят из М-тропного в более патогенный Т-тропный вирусный фенотип (Blaak et al., Proc. Natl. Acad. Sci. 97, 1269-1274 (2000); Miedema et al., Immune Rev., 140:35 (1994); Simmonds et al., J.Virol. 70, 8355-8360 (1996); Tersmette et al., J.Virol., 62, 2022-2032, (1988); Connor R.I., Ho.D.D., J.Virol., 68, 4400-4408 (1994); Schuitemaker et al., J.Virol. 66, 1354-1360 (1992)). М-тропный вирусный фенотип соотносится со способностью вируса проникать в клетку после связывания с CCR5 рецептором, тогда как Т-тропный вирусный фенотип соотносится со способностью проникновения вируса в клетку после связывания и мембранного слияния с CXCR4 рецептором. На основании клинических наблюдений предполагают, что пациенты, обладающие генетическими мутациями в CCR5, оказываются устойчивыми или менее подверженными ВИЧ инфицированию (Liu et al, Cell, 86, 367-377 (1996); Samson et al., Nature 382, 722-725 (1996); Michael et al., Nature Med. 3, 338-340(1997); Michael et al., J.Virol., 72, 6040-6047 (1998); Obrien et al., Lancet 349, 1219 (1997); Zhang et al., AIDS Res.Hum.Retroviruses, 13, 1357-1366 (1997); Rana et al., J.Virol., 71, 3219-3227 (1997); Theodorou et al., Lancet 349, 1219-1220 (1997)). Несмотря на то что сообщалось о ряде хемокиновых рецепторов, опосредующих проникновение ВИЧ в клетки, CCR5 и CXCR4 оказываются единственными физиологически значимыми сорецепторами, используемыми широким рядом первичных клинических ВИЧ-1 штаммов (Zhang et al., J.Virol., 72, 9307-9312 (1998); Zhang et al., J.Virol., 73, 3443-3448 (1999); Simmonds et al., J.Virol., 72, 8453-8457 (1988)). Слияние и проникновение Т-тропных вирусов, которые используют CXCR4, ингибируется природным СЧС-хемокиновым стромальным клеточно-производным фактором-1, тогда как слияние и проникновение М-тропных вирусов, использующих CCR5, ингибируется природными СС-хемокинами, а именно регулируемым при экспрессировании и секретировании нормально активированной Т-клеткой (RANTES) и макрофагвоспалительными белками (MIP-1 альфа и бета).
Недавно было высказано предположение, что, в дополнение к тому, что он служит кофактором для проникновения ВИЧ, непосредственное взаимодействие вирус-ассоциированного gp-120 с CXCR4 служит возможной причиной CD8+T-клеточного апоптоза и относящегося к СПИД слабоумия за счет индуцирования апоптоза нейронных клеток (Hesselgesser et al., Curr.Biol., 8, 595-598 (1998); Hesselgesser et al., Curr.Biol., 7, 112-121 (1997); Heddelgesser et al., "Chemokines and Chemokine receptors in the Brain" в «Chemokines in Disease», опубликованной Humana Press (1999), под редакцией C.Herbert; Herbein et al., Nature 395, 189-194 (1998); Buttini et al., Nature Med., 4, 441-446 (1998); Ohagen et al., J.Virol., 73, 897-906 (1999); Biard-Piechaczyk et al., Virology 268, 329-344 (2000); Sanders et al., J.Neuroscience Res., 59, 671-679 (2000); Bajetto et al., J.Neurochem., 73, 2348-2357 (1999); Zheng et al., J.Virol., 73, 8256-8267 (1999)).
Однако связывание хемокиновых рецепторов с их природными лигандами, оказывается, играет более эволюционную и центральную роль, чем только в качестве медиаторов ВИЧ инфицирования. Связывание природного лиганда, пред-В-клеточного стимулирующего фактора роста/фактора производного стромальных клеток (PBSF/SDF-1), с CXCR4 - хемокиновым рецептором обеспечивает важный сигнальный механизм: мыши с повреждением CXCR4 или SDF-1 проявляют церебральные, сердечные аномалии и аномалии желудочно-кишечного тракта и умирают in utero (Zou et al., Nature, 393: 591-594 (1998); Tachibana et al., Nature, 393: 591-594 (1998); Nagasawa et al., Nature 382, 635-638 (1996)). CXCR4-недостаточные мыши также проявляют гематопоэтические дефекты (Nagasawa et al., Nature 382, 635-638 (1996)); миграция CXCR4-экспрессирующих лейкоцитов и гематопоэтических предшественников к SDF-1 оказалась важной для поддержания В-клеточной линии и локализации CD34+ клеток-предшественников в костном мозге (Bleul et al., J.Exp.Med., 187, 753-762 (1998); Viardot et al., Ann.Hematol., 77, 195-197 (1998); Auiti et al., J.Exp.Med. 185, 111-120 (1997); Peled et al., Science 283, 845-848 (1999); Qing et al., Immunity 10, 463-471 (1999); Lataillade et al., Blood 95, 756-768 (1999); Ishii et al., J.Immunol., 163, 3612-3620 (1999); Maekawa et al., Internal Medicine 39, 90-100 (2000); Fedyk et al., J.Leukocyte Biol., 66, 667-673 (1999); Peled et al., Blood 95, 3289-3296 (2000)).
Сигнал, обеспечиваемый SDF-1 при связывании с CXCR4, также может играть важную роль в пролиферации опухолевых клеток и регуляции ангиогенеза, связанного с ростом опухоли (см., "Chemokines and Cancer", опубликованной Humana press (1999); под редакцией B.J.Rollins; Arenburg et al., J.Leucocyte Biol., 62, 554-562 (1997); Moore et al., J.Invest. Med., 46, 113-120 (1998); Moore et al., Trends cardiovasc. Med., 8, 51-58 (1998); Seghal et al., J.Surg.Oncol., 69, 99-104 (1998)); известные ангиогенные факторы роста VEG-F и bFGF регулируют с повышением уровня CXCR4 в эндотелиальных клетках, и SDF-1 может индуцировать неоваскуляризацию in vivo (Salcedo et al., Am.J.Pathol. 154, 1125-1135 (1999)); лейкозные клетки, которые экспрессируют CXCR4, мигрируют и слипаются с лимфатическими узлами и стромальными клетками костного мозга, которые экспрессируют SDF-1 (Burger et al., Blood 94, 3658-3667 (1999); Arai et al., Eur.J.Haematol., 64, 323-332 (2000); Bradstock et al., Leukemia 14, 882-888 (2000)).
Связывание SDF-1 с CXCR4 также вовлечено в патогенез атеросклероза (Abi-Yones et al., Circ. Res., 86, 131-138 (2000)), отторжение почечного аллотрансплантата (Eitner et al., Transplantation 66, 1551-1557 (1998)), астматическое и аллергическое воспаление дыхательных путей (Yssel et al., Clinical and Experimental Allergy 28, 104-109 (1998); J.Immunol., 164, 5935-5943 (2000); Gonzalo et al., J.Immunol., 165, 499-508 (2000)), болезнь Альцгеймера (Xia et al., J.Neurovirology 5, 32-41 (1999)) и артрит (Nanki et al., J.Immunl., 164, 5010-5014 (2000)).
Для лучшего понимания взаимоотношения между хемокинами и их рецепторами недавно были выполнены эксперименты по блокированию слияния, проникновения и репликации ВИЧ через CXCR4 хемокиновый рецептор посредством применения моноклональных антител или малых молекул, которые, как предполагается, предлагают полезную терапевтическую стратегию (Schols et al., J.Exp. Med., 186: 1383-1388 (1997); Schols et al., Antiviral Research 35:147-156 (1997); Bridger et al., J.Med. Chem.., 42, 3971-3981 (1999); Bridger et al., "Bicyclam Derivatives as HIV Inhibitors" в Advances in Antiviral Drug Design, Volume 3, 161-229; опубликовано JAI press (1999); под редакцией E.De.Clereq). Малые молекулы, такие как бицикламы, проявляют специфическое связывание с CXCR4, а не с CCR5 (Donzella et al., Nature Medicine, 4: 72-77 (1998)). Данные эксперименты продемонстрировали вмешательство ВИЧ-проникновения и мембранного слияния в клетку-мишень in vitro. Позднее также было показано, что бицикламы ингибируют слияние и репликацию Вируса Иммунодефицита Кошачьих (ВИК), который использует CXCR4 для проникновения (Egberink et al., J.Virol., 73, 6346-6352 (1999)).
Дополнительные эксперименты показали, что бициклам доза-зависимым образом ингибирует связывание 121I-меченного SDF-1 с CXCR4 и сигнальную трансдукцию (выявленную по увеличению внутриклеточного кальция) в ответ на SDF-1. Таким образом, бициклам также функционирует как антагонист сигнальной трансдукции, являющейся результатом связывания стромального производного фактора или SDF-1α, природного хемокина, с CXCR4. Бицикламы также ингибируют ВИЧ gp120 (оболочка)-индуцированный апоптоз в не-ВИЧ инфицированных клетках (Blanco et al., Antimicrobial Agents and Chemother., 44, 51-56 (2000)).
В патентах США №№ 5583131, 5698546, 5817807, 5021409 и 6001826, которые включены в данное описание во всей своей полноте в качестве ссылки, описаны циклические соединения, которые проявляют активность против ВИЧ-1 и ВИЧ-2 в тестах in vitro. Впоследствии было установлено и дополнительно описано в находящихся одновременно на рассмотрении заявках на патент США номер 09/111895 и 60/172153, что такие соединения проявляют анти-ВИЧ активность за счет связывания хемокинового рецептора CXCR4, экспрессируемого на поверхности некоторых клеток иммунной системы. Такое конкурентное связывание таким образом защищает такие клетки-мишени от инфицирования ВИЧ, который использует рецептор CXCR4 для вторжения. В дополнение данные соединения антагонизируют связывающее, сигнальное и хемотактическое действие природного лиганда для СXCR4, хемокинового фактора 1α, являющегося производным стромальных клеток (SDF-1). В дальнейшем авторами данного изобретения было установлено, что такие новые соединения проявляют защитное действие против ВИЧ инфицирования клеток-мишеней путем связывания in vitro с CCR5 рецептором.
Кроме того, авторами данного изобретения в заявке на патент США номер 09/495298 было раскрыто, что такие циклические полиаминные противовирусные агенты, описанные в указанных выше патентах, обладают действием, усиливающим продуцирование белых кровяных клеток, а также проявляют противовирусные свойства. Таким образом, данные агенты можно использовать для контролирования побочного действия химиотерапии, усиления успеха трансплантации костного мозга, усиления заживления ран и лечения ожогов, а также борьбы с бактериальными инфекциями при лейкемии.
Позднее авторами данного изобретения в заявке на патент США номер 09/535314 был раскрыт ряд гетероциклических соединений, которые обладают анти-ВИЧ активностью за счет связывания с хемокиновыми рецепторами СXCR4 и CCR5, экспрессируемыми на поверхности некоторых клеток иммунной системы. Такое конкурентное связывание таким образом защищает указанные клетки-мишени от инфицирования ВИЧ, который использует CXCR4 или CCR5 рецепторы для вторжения. В дополнение данные соединения антагонизируют связывающее, сигнальное и хемотактическое действие природного лиганда для СXCR4, хемокинового фактора 1α, являющегося производным стромальных клеток (SDF-1), и/или природного лиганда для CCR5, хемокина RANTES.
В данном изобретении описаны новые соединения, обладающие защитным действием против ВИЧ инфицирования клеток-мишеней за счет связывания с хемокиновым рецептором CXCR4 или CCR5 аналогичным образом, что и ранее описанные макроциклические соединения. Кроме того, данные соединения антагонизируют связывающее, сигнальное и хемотактическое действие природного лиганда для СXCR4, хемокинового фактора 1α, являющегося производным стромальных клеток (SDF-1), и/или природного лиганда для CCR5, хемокина RANTES.
Цитирование указанных выше публикаций не следует рассматривать как признание того, что любое из изложенного выше представляет собой относящийся к делу предшествующий уровень развития данной области. Все положения в отношении даты или утверждения, касающиеся содержания данных публикаций, основаны на информации, доступной заявителю, и не составляют любое допущение в отношении правильности дат или содержания данных публикаций. Кроме того, все публикации, приведенные в тексте заявки, включены в данное описание во всей своей полноте в качестве ссылки.
Краткое изложение сущности изобретения
Настоящее изобретение относится к новым соединениям, которые связывают хемокиновые рецепторы и мешают их связыванию с природными лигандами. Соединения настоящего изобретения могут использоваться в качестве агентов, демонстрирующих защитное действие для клеток-мишеней против ВИЧ инфицирования. Другими вариантами осуществления настоящего изобретения являются соединения, которые действуют как антагонисты или агонисты хемокиновых рецепторов, а также проявляют другие виды биологической активности, относящиеся к способности данных соединений ингибировать связывание хемокинов с их рецепторами.
Соединения по изобретению имеют формулу (1), включая их фармацевтически приемлемые соли и пролекарственные формы. Соединения формулы (1) имеют формулу:
где
кольцо А необязательно включает гетероатом, выбранный из N, О и S;
пунктирные линии представляют необязательную ненасыщенность;
R1, R2 и R3 представляют заместители, не создающие препятствий;
k равно 0-4;
l равно 0, 1 или 2;
Х является незамещенным или замещенным С или N, или представляет О или S;
Ar представляет остаток ароматического или гетероароматического фрагмента;
каждый n независимо равен 0-2;
каждый R независимо представляет Н или алкил(1-6С);
j равен 0-3; и
каждый Y независимо является необязательным заместителем, не создающим препятствий, как определено в данном описании, отличающимся от CR2NR(CR2)nB, где В является ароматическим, или гетероароматическим, или другим гетероциклом.
Предпочтительно каждый Y независимо представляет галоген, ОН, SH, SO, SO2 или органический фрагмент из 1-20С атомов, который не содержит N, где два таких Y могут быть связаны с образованием конденсированного кольца с Ar, или выбран из группы, состоящей из
и те, где Y включает гуанидино или NHNHR, или амидино;
где Z представляет необязательно замещенный ароматический или гетероароматический фрагмент, содержащий 5-12 кольцевых членов; и
где R является таким, как определено выше, каждый m независимо равен 0-4, и R4 и каждый R5 независимо представляет Н, алкил (1-6С), алкенил (1-6С), алкинил (1-6С) или ацил (1-6С), каждый из которых необязательно замещен одним или более неароматическим(и), негетероциклическим(и) заместителем(ями), и где два R5 могут быть связаны с образованием циклического амина, необязательно содержащего один или более дополнительных гетероатомов, выбранных из N, O и S.
Соединения изобретения специально исключают варианты осуществления, где Y представляет CR2NR(CR2)nB, где В является ароматическим, или гетероароматическим, или другим гетероциклом.
Необязательные заместители определены ниже.
Изобретение охватывает фармацевтические композиции, включающие терапевтически эффективное количество соединения формулы (1); способы лечения заболеваний организма человека или организмов других млекопитающих, включающие введение таких фармацевтических композиций; и способ блокирования или предотвращения связывания хемокинового рецептора с его природным лигандом, включающий контактирование указанного хемокинового рецептора с эффективным количеством соединения формулы (1).
Данное изобретение также относится к применению соединения формулы (1) для получения лекарственного средства для лечения заболевания, при котором блокирование или предотвращение связывания хемокинового рецептора с его природным лигандом является благоприятным, причем данный способ может включать составление(получение) композиции, включающей терапевтически эффективное количество соединения формулы (1). В изобретении также разработан способ защиты клеток-мишеней, обладающих хемокиновыми рецепторами, связывание с которыми патогенного агента приводит к заболеванию или патологии, включающий введение млекопитающему фармацевтической композиции, включающей терапевтически эффективное количество соединения формулы (1).
Соединениям по изобретению может быть придана форма пролекарства, то есть защищенных форм соединений, которые высвобождают соединение после введения пациенту. Например, соединение может обладать защитными группами, которые отщепляются при гидролизе в жидкостях организма, например в круге кровообращения, высвобождая таким образом активное соединение, или окисляются, или восстанавливаются в жидкостях организма, высвобождая соединение. Обсуждение пролекарств можно найти у "Smith and Williams' Introduction to the Principles of Drug Design", H.J.Smith, Wright, Second Edition, London, 1988.
Кислотно-аддитивные соли, которые являются фармацевтически приемлемыми, такие как соль с неорганическим основанием, соль с органическим основанием, соль с неорганической кислотой, соль с органической кислотой, соль с основной или кислотной аминокислотой и т.д., также охватываются настоящим изобретением. Примеры соли с неорганическим основанием включают соль с щелочным металлом (например, натрием, калием и т.д.), щелочноземельным металлом (например, кальцием, магнием и т.д.), алюминием, аммонием и т.д. Примеры соли с органическим основанием включают соль с триметиламином, триэтиламином, пиридином, пиколином, этаноламином, диэтаноламином, триэтаноламином, дициклогексиламином, N,N'-дибензилэтилендиамином и т.д. Примеры соли с неорганической кислотой включают соль с хлористоводородной кислотой, бромистоводородной кислотой, азотной кислотой, серной кислотой, фосфорной кислотой и т.д. Примеры соли с органической кислотой включают соль с муравьиной кислотой, щавелевой кислотой, уксусной кислотой, винной кислотой, метансульфоновой кислотой, бензолсульфоновой кислотой, яблочной кислотой, п-толуолсульфоновой кислотой и т.д. Примеры солей с основными аминокислотами включают соль с аргинином, лизином, орнитином и т.д. Примеры солей с кислотными аминокислотами включают соль с аспартамовой кислотой, глутаминовой кислотой и т.д. Термин «нетоксичные» в настоящем контексте следует рассматривать с учетом прогноза для инфицированного пациента, не подвергающегося лечению.
Способы осуществления изобретения
Настоящее изобретение относится к соединениям формулы (1), которые могут действовать в качестве агентов, модулирующих активность хемокинового рецептора. Такие хемокиновые рецепторы включают, но не ограничиваются ими, CCR1, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8 и CXCR1, CXCR2, CXCR3, CXCR4 и CXCR5, предпочтительно CXR4 и/или CCR5.
Соединения воздействуют на связывание природного лиганда или хемокина с рецептором клетки-мишени, таким как CXR4 и/или CCR5.
Таким образом, соединения оказывают влияние на хемокиновые рецепторы, такие как CCR1, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8 и CXCR1, CXCR2, CXCR3, CXCR4 и CXCR5, где такие хемокиновые рецепторы являются важными медиаторами многих воспалительных процессов у человека, а также иммунорегулируемых заболеваний и рака, и модулируют активность таких хемокиновых рецепторов таким образом, чтобы оказаться полезными для лечения или профилактики подобных заболеваний.
В частности, соединения формулы (1) оказывают защитное действие на клетки-мишени против ВИЧ инфицирования способом, включающим специфическое связывание с хемокиновым рецептором.
Подразумевается, что термин «модуляторы», как он использован в настоящем описании, включает в себя антагонист, агонист, частичный антагонист и/или частичный агонист, ингибиторы и активаторы. В предпочтительном варианте осуществления настоящего изобретения соединения формулы (1) демонстрируют защитное действие против ВИЧ инфицирования путем ингибирования связывания ВИЧ с хемокиновым рецептором клетки-мишени, таким как CXR4 и/или CCR5. Изобретение включает способ, который включает контактирование клетки-мишени с количеством соединения, эффективным для ингибирования связывания с хемокиновым рецептором.
Термин «терапевтически эффективное количество» означает количество представленного соединения, с помощью которого достигается биологическая или медицинская ответная реакция в клетке, ткани, органе, системе, животном или человеке, которая является искомой для исследователя, ветеринара, лечащего врача или другого клинического врача.
Термин «введение» и/или «применение по назначению» представленного соединения следует понимать как означающий обеспечение соединением по изобретению, включая пролекарство соединения по изобретению, индивидуума, нуждающегося в лечении.
Соединения по изобретению, которые ингибируют хемокиновые рецепторы, могут использоваться для лечения как профилактического, так и терапевтического заболеваний, связанных с гемопоэзом (кроветворением), включая, но не ограничиваясь этим, контролирование побочного действия химиотерапии, увеличение успеха при трансплантации костного мозга, улучшение заживления ран и лечения ожогов, а также для борьбы с бактериальными инфекциями при лейкемии.
Соединения по изобретению, которые ингибируют активность и функцию хемокинового рецептора, могут использоваться для лечения заболеваний, связанных с воспалением, включая, но не ограничиваясь этим, воспалительные или аллергические заболевания, такие как астма, аллергический ринит, аллергические заболевания легких, аллергическая пневмония, эозинофильная пневмония, аллергия отсроченного типа, внутритканевое заболевание легких (ILD) (например, идиопатический фиброз легких или ILD, связанное с ревматоидным артритом, системной красной волчанкой, анкилозирующим спондилитом, рассеянным склерозом, синдромом Шегрена (ксеродерматоз), полимиозитом или дерматомиозитом); системную анафилаксию или аллергические реакции, аллергию к лекарственным средствам, аллергию к укусам насекомых, аутоиммунные заболевания, такие как ревматоидный артрит, псориазный артрит, системная красная волчанка, астенический бульбарный паралич, юношеский диабет, гломелуронефрит, аутоиммунный троидит, отторжение трансплантата, включая отторжение аллотрансплантата или заболевание трансплантат-против-хозяина; воспалительные заболевания кишечника, такие как болезнь Крона и язвенный колит; спондилоартропатии; склеродерму; псориаз (включая опосредованный Т-клетками псориаз) и воспалительные кожные заболевания, такие как дерматит, экзема, атопический дерматит, аллергический контактный дерматит, крапивная лихорадка, васкулит (например, некротизированный, кожный и аллергический васкулит); эозинофильный миотит, эозинофильный фасцит; и раковые заболевания.
Соединения по изобретению, которые активируют или поддерживают функцию хемокинового рецептора, могут использоваться для лечения заболеваний, которые связаны с подавлением иммунитета, как, например, у индивидуумов, подвергающихся химиотерапии, лучевой терапии, для усиления заживления ран и лечения ожогов, терапии при аутоиммунных заболеваниях или при другой лекарственной терапии (кортикостероидная терапия) или при сочетании обычных лекарственных средств, используемых при лечении аутоиммунных заболеваний и отторжении трансплантата/трансплантации, которые вызывают подавление иммунитета; c подавлением иммунитета вследствие врожденного недостатка функций рецепторов или в других случаях; при инфекционных заболеваниях, таких как заболевания, вызываемые паразитами, включая, но не ограничиваясь этим, заражение организма гельминтами, такими как нематоды (круглые черви); трихоцефалез, энтеробиоз, аскаридоз, анкилостомоз, стронгилоидоз, трихинеллез, филяриотоз; трематодами, висцеральными червями, висцеральными личинками (например, Toxocara), эозинофильный гастроэнтерит (например, Anisaki spp., Phocanema ssp.), кожными личинками (Ancylostona brazilliense, Acylostoma caninum); вызывающими малярию простейшими Plasmodium vivax, цитомегаловирусом человека, вирусом герпеса herpersvirus saimiri и вирусом герпеса, вызывающим саркому Капоши, также известным как вирус герпеса человека 8, и кожным вирусом Moluscum contagiosum.
Одно или более соединений формулы (1) можно использовать в сочетании с любой другой фармацевтической композицией, где такая комбинированная терапия модулирует активность хемокинового рецептора и таким образом предотвращает и лечит заболевания, связанные с гемопоэзом, воспалением, аутоиммунные заболевания, воспалительные кожные заболевания, раковые заболевания, воспалительные заболевания кишечника и нарушения иммунорегуляции.
Также предполагается, что настоящее изобретение можно использовать в сочетании с одним или несколькими агентами, полезными для профилактики или лечения ВИЧ. Примеры таких агентов включают:
(1) нуклеотидный ингибитор ревертазы (обратной транскриптазы), такой как зидовудин, диданозин, ламивудин, зальцитабин, абакавир, ставудин, адефовир, адефовир дипивоксил, фозивудин тодоксил и т.д.;
(2) не-нуклеотидный ингибитор ревертазы (обратной транскриптазы) (включая агент, обладающий антиоксидантной активностью, такой как иммунокал, олтипраз и т.д.), такой как невирапин, делавирдин, эфавиренц, ловирид, иммунокал, олтипраз и т.д.; и
(3) ингибиторы протеазы, такие как саквинавир, ритонавир, индинавир, нельфинавир, ампренавир, палинавир, лазинавир и т.д.
Объем комбинаций соединений формулы (1) с ВИЧ-агентами не ограничен пунктами (1), (2) и (3), но включает, в принципе, любую комбинацию с любой фармацевтической композицией, полезной для лечения ВИЧ. Кроме того, в таких комбинациях соединения настоящего изобретения и другие ВИЧ-агенты можно вводить по отдельности или вместе. Дополнительно, введение одного элемента можно проводить перед, совместно или после введения другого агента(ов).
Соединения формулы (1) можно вводить перорально, парентерально (например, внутримышечно, внутрибрюшинно, внутривенно, путем интрацистернальной инъекции или инфузии, подкожной инъекции или в виде имплантата), ингаляционным распылением, назально, вагинально, ректально, сублингвально или с помощью местных путей введения, и их можно использовать в получении лекарственного средства, по отдельности или вместе, в виде подходящих стандартных препаративных лекарственных форм, содержащих обычные нетоксичные фармацевтически приемлемые носители, адьюванты и средства распространения, подходящие для каждого пути введения.
Все соединения формулы (1) являются активными и используются для лечения животных, включая, но не ограничиваясь этим, мышей, крыс, лошадей, крупный рогатый скот, овец, собак, кошек и обезьян. Соединения по изобретению также эффективны для применения у людей.
Соединения формулы (1) могут образовывать гидраты или сольваты. Те соединения формулы (1), которые могут существовать в виде региоизомеров, конфигурационных изомеров, конформеров или диастреоизомерных форм, могут встречаться в виде смесей таких форм. При желании, смеси могут быть обработаны таким образом, чтобы выделить индивидуальные изомеры с использованием известных способов разделения и очистки. Например, когда соединение формулы (1) представляет собой рацемат, он может быть разделен на (S)-соединение и (R)-соединение путем оптического разделения. Индивидуальные оптические изомеры и их смеси также включены в объем настоящего изобретения.
Данное изобретение также относится к фармацевтической композиции, включающей фармацевтически приемлемый носитель или разбавитель и эффективное количество соединения формулы (1). Соединение формулы (1) можно вводить само по себе или их можно вводить перорально или не-перорально в виде смеси с фармацевтически приемлемым носителем (например, твердые препаративные лекарственные формы, такие как таблетки, капсулы, гранулы, порошки и т.д.; жидкие препаративные лекарственные формы, такие как сиропы, инъекции и т.д.). Примеры не-пероральных препаративных лекарственных форм включают инъекции, капли, суппозитории, пессарии.
При лечении или профилактике болезненных состояний, при которых требуется модуляция хемокинового рецептора, подходящий уровень дозировки обычно будет составлять от примерно 0,01 до 500 мг на кг массы тела пациента в сутки, которую можно вводить в виде единичной дозы или многократных доз. Предпочтительно, уровень дозировки будет составлять от примерно 0,1 до примерно 250 мг/кг в сутки. Следует понимать, что конкретный уровень дозировки и частота дозировки для каждого конкретного пациента могут изменяться и будут зависеть от множества факторов, включая активность конкретного используемого соединения, метаболическую стабильность и продолжительность действия соединения, возраст, массу тела, общее состояние здоровья, пол, режим питания, способ и время введения, скорость выделения, комбинацию лекарственных средств, серьезность конкретного заболевания и пациента, подвергающегося лечению.
Настоящее изобретение дополнительно относится к новым соединениям, которые связывают хемокиновые рецепторы и мешают их связыванию с природным лигандом. Соединения настоящего изобретения могут использоваться в качестве агентов, проявляющих защитное действие для клеток-мишеней от ВИЧ-инфекции. Соединения настоящего изобретения также могут использоваться в качестве антагонистов или агонистов хемокиновых рецепторов, а также в другой биологической деятельности, относящейся к способности таких соединений ингибировать связывание хемокинов с их рецепторами.
Дополнительное определение заместителей
В соединениях формулы (1) R может представлять линейный или разветвленный алкил или может быть циклическим и необязательно может быть замещен 1-2 заместителями, выбранными из галогена, гидрокси и алкокси. Предпочтительно каждый R представляет Н или низший линейный алкил (1-4С), предпочтительно метил.
Ar представляет остаток ароматического или гетероароматического фрагмента, который содержит отдельную или конденсированную кольцевую систему и содержит 5-6 кольцевых членов в моноциклической системе и 9-12 членов в конденсированной кольцевой системе. Остаток необязательно может быть замещенным. Примеры необязательно замещенных ароматических и гетероароматических групп включают бензол, нафталин, дигидронафталин, тетрагидронафталин, пиридин, хинолин, изохинолин, имидазол, бензимидазол, азабензимидазол, бензотриазол, фуран, бензофуран, тиазол, бензотиазол, оксазол, бензоксазол, пиррол, индол, имидазол, тетрагидрохинолин, тетрагидроизохинолин, пиразол, тиофен, изоксазол, изотиазол, триазол, тетразол, оксадиазол, тиадиазол, имидазолин и бензопиран. Настоящее изобретение также включает гетероароматические кольца, содержащие оксиды азота и серы. Особенно предпочтительными формами Ar являются фенилен, пиридилен или пиридинилен.
Когда соединения формулы (1) содержат элементы, которые являются «необязательно замещенными», такие заместители предпочтительно представляют собой галоген, нитро, циано, карбоновую кислоту, необязательно замещенные алкильные, алкенильные или циклоалкильные группы, необязательно замещенную гидроксильную группу, необязательно замещенную тиольную группу, необязательно замещенную аминогруппу, необязательно замещенную ацильную группу, необязательно замещенную карбоксилатную, карбаматную, карбоксамидную или сульфонамидную группу или необязательно замещенную ароматическую или гетероциклическую группу.
Примеры галогена включают фтор, хлор, бром, иод и т.д., при этом фтор и хлор являются предпочтительными.
Примеры необязательно замещенного алкила включают С1-10 алкил, включая метил, этил, пропил и т.д.; примеры необязательно замещенных алкенильных групп включают С2-10 алкенил, такой как аллил, кротил, 2-пентенил, 3-гексенил и т.д.; и примеры необязательно замещенных циклоалкильных групп включают С3-10 циклоалкил, такой как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и т.д. В данных случаях С1-6 алкил, алкенил и циклоалкил являются предпочтительными. Необязательный заместитель также может представлять собой необязательно замещенный аралкил (например, фенил С1-4 алкил) или гетероалкил, например, фенилметил (бензил), фенилэтил, пиридинилметил, пиридинилэтил и т.д. Гетероциклическая группа может представлять собой 5- или 6-членное кольцо, содержащее 1-4 гетероатома.
Примеры необязательно замещенной гидроксильной и тиольной групп включают такие, в которых заместитель представляет собой необязательно замещенный алкил (например, С1-10 алкил), такой как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил и т.д., предпочтительно (С1-6) алкил; необязательно замещенный циклоалкил (например, С3-7 циклоалкил и т.д., такой как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и т.д.); необязательно замещенный аралкил (например, фенил С1-4 алкил, например, бензил, фенетил и т.д.). Когда имеется два смежных гидроксильных или тиольных заместителя, гетероатомы могут быть связаны алкиленовой группой, как, например, О(СН2)nO и S(СН2)nS (где n=1-5). Примеры включают метилендиокси, этилендиокси и т.д. Также охвачены оксиды простой тиоэфирной группы, такие как сульфоксиды и сульфоны.
Дополнительные примеры необязательно замещенной гидроксильной группы включают необязательно замещенный С2-4 алканоил (например, ацетил, пропиноил, бутирил, изобутирил и т.д.), С1-4 алкилсульфонил (например, метансульфонил, этансульфонил и т.д.) и необязательно замещенную ароматическую и гетероциклическую карбонильную группу, включая бензоил, пиридинкарбонил и т.д.
Заместители при необязательно замещенной аминогруппе могут быть связаны друг с другом с образованием циклической аминогруппы (например, 5-6-членный циклический амино и т.д., такой как тетрагидропиррол, пиперазин, пиперидин, пирролидин, морфолин, тиоморфолин, пиррол, имидазол и т.д.). Указанные циклические аминогруппы могут иметь заместитель, и примеры заместителей включают галоген (например, фтор, хлор, бром, иод и т.д.), нитро, циано, гидроксильную группу, тиольную группу, аминогруппу, карбоксильную группу, необязательно галогенированный С1-4 алкил (например, трифторметил, метил, этил и т.д.), необязательно галогенированный С1-4 алкокси (например, метокси, этокси, трифторметокси, трифторэтокси и т.д.), С2-4 алканоил (например, ацетил, пропионил и т.д.), С1-4 алкилсульфонил (например, метансульфонил, этансульфонил и т.д.), число предпочтительных заместителей составляет от 1 до 3.
Аминогруппа также может быть замещена один или два раза (с образованием вторичного или третичного амина) такой группой, как необязательно замещенная алкильная группа, включая С1-10 алкил (например, метил, этил, пропил и т.д.); необязательно замещенная аленильная группа, такая как аллил, кротил, 2-пентенил, 3-гексенил и т.д., или необязательно замещенная циклоалкильная группа, такая как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и т.д. В таких случаях С1-6 алкил, алкенил и циклоалкил являются предпочтительными. Аминная группа также может быть необязательно замещена ароматической или гетероциклической группой, аралкилом (например, фенилС1-4алкилом) или гетероалкилом, например, фенилом, пиридином, фенилметилом (бензил), фенетилом, пиридинилметилом, пиридинилэтилом и т.д. Гетероциклическая группа может представлять собой 5- или 6-членное кольцо, содержащее 1-4 гетероатома. Необязательные заместители в «необязательно замещенных аминогруппах» являются такими же, как определено в