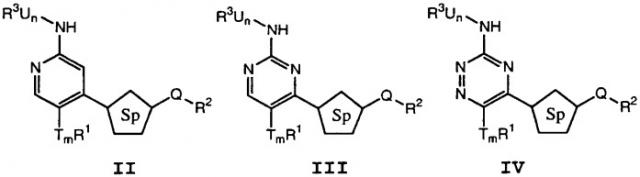
Гетероциклические ингибиторы erk2 и их использование
Иллюстрации
Показать всеИзобретение относится к области медицины, фармакологии и органической химии и касается способа ингибирования ERK2 у пациента с помощью соединений формулы 111-а, новых соединений, композиции для ингибирования действия ERK2, способа ингибирования действия ERK2, GSK-3, Aurora, CDK2 или Lck у пациента, способов лечения опосредованных ERK2, или GSK-3, или Aurora, или CDK2, или Lck заболеваний, способа ускорения синтеза гликогена, способа снижения уровня глюкозы в крови, способа ингибирования образования гиперфосфорилированного Tau белка у пациента, способа ингибирования фосфорилирования β-катенина у пациента, способа ингибирования действия ERK2, GSK-3, Aurora, CDK2 или Lck в биологическом образце. Изобретение обеспечивает повышенную эффективность ингибирования. 16 н. и 15 з.п. ф-лы, 2 табл.
Реферат
Перекрестная ссылка на родственные заявки
По настоящей заявке испрашивается приоритет в соответствии с предварительной патентной заявкой США 60/267818, поданной 9 февраля 2001, и предварительной патентной заявкой США 60/328768, поданной 12 октября 2001, содержание которых включено в данное описание в качестве ссылок.
Область техники, к которой относится изобретение
Настоящее изобретение относится к области медицинской химии и касается соединений пиразола, которые являются ингибиторами протеинкиназы, особенно ингибиторами ERK, композиций, содержащих такие соединения, и способов их использования. Соединения могут быть использованы для лечения рака и других заболеваний, облегчаемых ингибиторами протеинкиназы.
Предпосылки создания изобретения
Активированные митогеном протеинкиназы млекопитающих (MAP)1 представляют собой серин/треонин киназы, которые являются промежуточным звеном во внутриклеточной трансдукции сигнала при метаболизме (Cobb and Goldsmith, 1995, J. Biol. Chem., 270, 14843; Davis, 1995, Mol. Reprod. Dev. 42, 459). Члены семейства МАР киназы разделяют сходство последовательности и консервативные структурные домены и включают ERK2 (киназу межклеточного регулированного сигнала - extracellular signal regulated kinase), JNK (Jun N-концевую киназу - Jun N-terminal kinase) и р38 киназы. JNK и р38 киназы активируются в ответ на провоспалительные TNF-альфа и интерлейкин-1 цитокиназы и на клеточный стресс, такой как острая сердечная слабость, гиперосмолярность, ультрафиолетовое излучение, липополисахариды и ингибиторы синтеза протеина (Derijard et al., 1994, Cell 76, 1025; Han et al., 1994, Science 265, 808; Raingeaud et al., 1995, J. Biol. Chem. 270, 7420; Shapiro and Dinarello, 1995, Proc. Natl. Acad. Sci, USA 92, 12230). В отличие от этого ERK активируются митогенами и факторами роста (Bokemeyer et al., 1996, Kidney Int. 49, 1187).
ERK2 представляет собой широко распространенную протеинкиназу, которая достигает максимальной активности при фосфорилировании обоих Thr183 и Tyr185 противоположно направленной МАРкиназе киназой, МEK1 (Anderson et al., 1990, Nature 343, 651; Crews et al., 1992, Science 258, 478). При активировании ERK2 фосфорилирует многие регуляторные протеины, включая протеинкиназы Rsk90 (Bjorbaek et al., 1995, J. Biol. Chem. 270, 18848) и MAPKAP2 (Rouse et al., 1994, Cell 78, 1027) и фактор транскрипции, такой как ATF2 (Raingeaud et al., 1996, Mol. Cell Biol. 16, 1247), Elk-1 (Raingeaud et al. 1996), c-Fos (Chen et al., 1993, Proc. Natl. Acad. Sci. USA 90, 10952), и c-Myc (Oliver et al., 1995, Proc. Soc. Exp. Biol. Med. 210, 162). ERK2 также представляет нижнюю мишень Ras/Raf зависимых путей метаболизма (Moodie et al., 1993, Science 260, 1658) и может помочь передавать сигналы от этих потенциально онкогенных протеинов. Показано, что ЕRK2 играет роль в негативном контроле роста клеток рака груди (Frey and Mulder, 1997, Cancer Res. 57, 628) и опубликованы данные о гиперэкспрессии ERK2 при раке груди человека (Sivaraman et al., 1997, J. Clin. Invest. 99, 1478). Активированная ERK2 также вовлекается в пролиферацию клеток гладкой мускулатуры стимулированных эндотелином дыхательных путей, что позволяет предположить участие этой киназы в развитии астмы (Whelchel et al., 1997, Am. J. Respir. Cell Mol. Biol. 16, 589).
Aurora-2 представляет собой серин/треонин протеинкиназу, которая вовлекается в развитие рака человека, такого как рак толстой кишки, груди и других твердых опухолей. Полагают, что эта киназа участвует в событии фосфорилирования протеина, которое регулирует клеточный цикл. В частности, Aurora-2 может играть роль в регулировании точного расщепления хромосом в процессе митоза. Неправильное регулирование клеточного цикла может привести к клеточной пролиферации и другим отклонениям. Установлено, что в ткани рака толстой кишки человека для aurora-2 протеина характерна избыточная экспрессия. См. Bischoff et al., EMBO J., 1998, 17, 3052-3065; Schumacher et al., J. Cell Biol., 1998, 143, 1635-1646; Kimura et al.,J. Biol. Chem., 1997, 272, 13766-13771.
Гликоген-синтаза-киназа-3 (GSK-3) представляет собой серин/треонин протеинкиназу, состоящую из α и β изоформ, каждая из которых кодируется характеристическим геном [Coghlan et al., Chemistry & Biology, 7, 793-803 (2000); Kim and Kimmel, Curr. Opinion Genetics Dev., 10, 508-514 (20000]. GSK-3 вовлекается в различные заболевания, включая диабет, болезнь Альцгеймера, такие заболевания ЦНС, как маниакально-депрессивное расстройство и нейродегенеративные заболевания, и гипертрофию миокарда [WO 99/65897; WO 00/38675; и Hag et al., J. Cell Biol., (2000) 151, 117]. Эти заболевания могут быть вызваны или быть результатом ненормального действия некоторых клеточных сигнальных путей метаболизма, в которых GSK-3 играет роль. Установлено, что GSK-3 фосфорилирует и модулирует активность ряда регуляторных протеинов. Эти протеины включают гликоген-синтазу, которая представляет собой ограничивающий скорость энзим, необходимый для синтеза гликогена, микротрубчатая связанная протеин Tau, фактор транскрипции гена β-катенин, фактор трансляции инициации elF2B, а также АТР цитрат-лиаза, аксин, фактор-1 теплового удара, с-Jun, c-Myc, c-Myb, CREB и CEPBα. Эти разнообразные протеин-мишени вовлекают GSK-3 во многие аспекты клеточного метаболизма, пролиферации, дифференциации и развития.
В опосредованном GSK-3 пути метаболизма, который относится к лечению диабетов типа II, индуцированное инсулином возникновение сигналов приводит к захвату клеточной глюкозы и синтезу гликогена. При таком пути метаболизма GSK-3 является отрицательным регулятором индуцированного инсулином сигнала. Обычно присутствие инсулина вызывает ингибирование опосредованного GSK-3 фосфорилирования и дезактивацию гликоген-синтазы. Ингибирование GSK-3 приводит к увеличению синтеза гликогена и расходу глюкозы [Klein et al., PNAS, 93, 8455-9 (1996); Cross et al., Biochem. J., 303, 21-26 (1994); Cohen, Biochem. Soc. Trans., 21, 555-567 (1993); Massillon et al., Biochem J., 299, 129-128 (1994)]. Однако у больных диабетом, когда отклик инсулина нарушен, синтез гликогена и захват глюкозы не могут увеличиться несмотря на присутствие относительно высокого содержания инсулина в крови. Это приводит к ненормально высокому содержанию глюкозы, сопровождающемуся острыми и долговременными эффектами, которые неизбежно приводят к сердечно-сосудистому заболеванию, почечной недостаточности и слепоте. У таких пациентов нормального индуцированного инсулином ингибирования GSK-3 не происходит. Сообщается также, что у больных диабетами типа II GSK-3 является сверхвыраженной [WO 00/38675]. Поэтому считают, что терапевтическое ингибирование GSK-3 является подходящим для лечения больных диабетом, страдающих нарушенным откликом на инсулин.
Активность GSK-3 также связывают с болезнью Альцгеймера. Эта болезнь характеризуется хорошо известным β-амилоид-пептидом и образованием внутриклеточных нейрофибриллярных зацеплений. Нейрофибриллярные зацепления содержат гиперфосфорилированный Tau-протеин, где Tau фосфорилирован по аномальным центрам. Экспериментами в клетке и на модельных животных показано, что GSK-3 фосфорилирует эти аномальные центры. Кроме того, показано, что ингибирование GSK-3 предотвращает гиперфосфорилирование Tau в клетках [Lovestone et al., Current Biology 4, 1077-86 (1994); Brownlees et al., Neuroreport 8, 3251-55 (1997)]. Поэтому полагают, что активность GSK-3 может ускорять образование нейрофибриллярных зацеплений и способствовать развитию болезни Альцгеймера.
Другим субстратом GSK-3 является β-катенин, который разрушается после фосфорилирования GSK-3. Сообщается, что у больных шизофренией наблюдаются пониженные уровни содержания β-катенина и это также связывают с другими заболеваниями, характеризующимися увеличением омертвления нейронных клеток [Zong et al., Nature, 395, 698-702 (1998); Takashima et al., PNAS, 90, 7789-93 (1993); Pei et al., J. Neuropathol. Exp., 56, 70-78 (1997)].
Вследствие биологической значимости GSK-3 в настоящее время возрос интерес к терапевтически эффективным ингибиторам GSK-3. Недавно появились данные о небольших молекулах, которые ингибируют GSK-3 [WO 99/65897 (Chiron) и WO 00/38675 (SmithKline Beecham)].
Из публикаций известны арилзамещенные пирролы. В частности, описаны триарилпирролы (патент США 5837719) как обладающие действием глюкагон-антагониста. 1,5-Диарилпиразолы описаны как ингибиторы р38 (WO 9958523).
Существует высокая медицинская потребность в разработке новых терапевтических методов лечения, которые могут быть использованы при лечении различных состояний, связанных с активацией ERK2. Для многих из этих состояний доступные в настоящее время различные методы лечения являются недостаточными.
Поэтому существует большая заинтересованность в новых и эффективных ингибиторах протеинкиназы, включая ингибиторы ERK2, которые могут быть использованы при лечении различных состояний, связанных с активацией протеинкиназы.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторами изобретения установлено, что соединения по настоящему изобретению и композиции на их основе являются эффективными ингибиторами протеинкиназы, особенно ингибиторами ERK2. Эти соединения имеют общую формулу I:
или их фармацевтически приемлемые производные, в которых
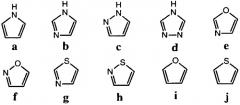
Sp означает объемную группу, включающую 5-членное гетероароматическое кольцо, где кольцо А и QR2 присоединены к Sp в положениях, не являющихся соседними; и где Sp имеет до двух R6 заместителей, при условии, что два замещенных атома углерода кольца в Sp не замещены одновременно R6;
каждый из Z1 и Z2 независимо выбран из N или CH;
каждый из T и Q представляет собой независимо выбранную связующую группу;
U выбран из -NR7-, -NR7CO-, -NR7CONR7-, -NR7CO2-, -O-, -CONR7-, -CO-, -CO2-, -OC(O)-, -NR7SO2-, -SO2NR7-, -NR7SO2NR7- или -SO2-;
каждый из m и n независимо выбран из нуля или единицы;
R1 выбран из водорода, CN, галогена, R, N(R7)2, OR или ОН;
R2 выбран из -(CH2)yR5, -(CH2)yCH(R5)2, -(CH2)yCH(R8)CH(R5)2, -N(R4)2 или -NR4(CH2)yN(R4)2;
y равно 0-6;
R3 выбран из R7, R, -(CH2)yCH(R8)R, CN, -(CH2)YCH(R8)CH(R5)2 или -(CH2)yCH(R8)N(R4)2;
каждый R независимо выбран из необязательно замещенной группы, выбранной из С1-6алифатической группы, С6-10арила, гетероарильного кольца, содержащего в кольце 5-10 атомов, или гетероциклильного кольца, содержащего 3-10 атомов в кольце;
каждый R4 независимо выбран из R, R7, -COR7, -CO2R, -CON(R7)2, -SO2R7, -(CH2)yR5 или -(CH2)yCH(R5)2;
каждый R5 независимо выбран из R, OR, CO2R, (CH2)YN(R7)2, N(R7)2, OR7, SR7, NR7COR7, NR7CON(R7)2, CON(R7)2, SO2R7, NR7SO2R7, COR7, CN или SO2N(R7)2;
каждый R6 независимо выбран из R7, F, Cl, (CH2)yN(R7)2, N(R7)2, OR7, SR7, NR7COR7, NR7CON(R7)2, CON(R7)2, SO2R7, NR7SO2R7, COR7, CN или SO2N(R7)2;
каждый R7 независимо выбран из водорода или необязательно замещенной С1-6алифатической группы, или два R7 при одном и том же атоме азота вместе с азотом образуют 5-8-членное гетероциклильное или гетероарильное кольцо;
R8 выбран из R, (CH2)wOR7, (CH2)wN(R4)2 или (CH2)wSR7; и
каждый w независимо выбран из 0-4.
Как здесь используется, применяются следующие определения, если не указано иного. Фраза "необязательно замещенный" использована взаимозаменяемо с фразой "замещенный или незамещенный" или с термином "(не)замещенный". Если не указано иного, необязательно замещенная группа может иметь заместитель в каждом положении замещения группы и каждое замещение не зависит от другого.
Термин "алифатический" или "алифатическая группа", использованный в данном описании, означает линейную или разветвленную С1-С12 углеводородную цепь, которая является полностью насыщенной или которая содержит одно или более звеньев ненасыщенности, или моноциклический С3-С8 углеводород или бициклический С8-С12 углеводород, который является полностью насыщенным или который содержит одно или более звеньев ненасыщенности, но который не является ароматическим (также называемый в данном тексте "карбоцикл" или "циклоалкил"), который имеет единственную точку присоединения к остальной молекуле, причем любое отдельное кольцо в указанной бициклической кольцевой системе содержит 3-7 членов. Например, подходящие алифатические группы включают, но не ограничивают объема притязаний, линейные или разветвленные алкильные, алкенильные, алкинильные группы и их гибриды, такие как (циклоалкил)алкил, (циклоалкенил)алкил или (циклоалкил)алкенил.
Термины "алкил", "алкокси", "гидроксиалкил", "алкоксиалкил" и "алкоксикарбонил", использованные по отдельности или как часть более крупного фрагмента, включают и прямые, и разветвленные цепи, содержащие от одного до двенадцати атомов углерода. Термины "алкенил" и "алкинил", использованные отдельно или как часть более крупного фрагмента, должны включать и прямые, и разветвленные цепи, содержащие от двух до двенадцати атомов углерода.
Термины "галогеналкил", "галогеналкенил и "галогеналкокси" означают алкил, алкенил или алкоксигруппы, замещенные одним или более атомами галогена, как может быть в одном из случаев. Термин "галоген" означает F, Cl, Br или I.
Термин "гетероатом" означает азот, кислород или серу и включает любую окисленную форму азота и серы и кватернизированную форму любого основного азота.
Также термин "азот" включает способный к замещению азот гетероциклического кольца. Например, в насыщенном или частично ненасыщенном кольце, содержащем 0-3 гетероатома, выбранных из кислорода, серы или азота, азот может быть представлен в виде N (как в случае 3,4-дигидро-2Н-пирролила), NH (как в случае пирролидинила) или NR+ (как в случае N-замещенного пирролидинила).
Термин "арил", использованный отдельно или как часть более крупного фрагмента, как "аралкил", "аралкокси" или "арилоксиалкил", относится к моноциклической, бициклической и трициклической кольцевым системам, содержащим суммарно от пяти до четырнадцати кольцевых членов, причем, по меньшей мере, одно кольцо в системе является ароматическим и при этом каждое кольцо в системе содержит от 3 до 7 кольцевых членов. Термин "арил" может быть использован взаимозаменяемо с термином "арильное кольцо".
Термин "гетероцикл", "гетероциклил" или "гетероциклический", использованный в данном тексте, означает неароматическую, моноциклическую, бициклическую или трициклическую кольцевые системы, содержащие от пяти до четырнадцати кольцевых членов, в которых один или более кольцевых членов представляет собой гетероатом, причем каждое кольцо в системе содержит от 3 до 7 кольцевых членов.
Термин "гетероарил", использованный самостоятельно или как часть более крупного фрагмента, как в термине "гетероаралкил" или "гетероарилалкокси", относится к моноциклической, бициклической или трициклической кольцевой системе, содержащей суммарно от пяти до четырнадцати кольцевых членов, причем, по меньшей мере, одно кольцо в системе является ароматическим, по меньшей мере, одно кольцо в системе содержит один или более гетероатомов, при этом каждое кольцо в системе содержит от 3 до 7 кольцевых членов. Термин "гетероарил" может быть использован взаимозаменяемо с термином "гетероарильное кольцо" или термином "гетероароматический".
Арильная (включая аралкил, аралкокси, арилоксиалкил и т.п.) или гетероарильная (включая гетероаралкил и гетероарилалкокси и т.п.) группа может содержать один или более заместителей. Подходящие заместители при ненасыщенном атоме углерода арильной, гетероарильной, аралкильной или гетероаралкильной группы выбраны из галогена, -R°, -OR°, -SR°, 1,2-метилендиокси, 1,2-этилендиокси, защищенного ОН (такой как ацилокси), фенила (Ph), Ph, замещенного группой R°, -O(Ph), O-(Ph), замещенного группой R°, -CH2(Ph), -CH2(Ph), замещенного группой R°, -CH2CH2(Ph), -CH2CH2(Ph), замещенного группой R°, -NO2, -CN, -N(R°)2, -NR°C(O)R°, -NR°C(O)N(R°)2, -NR°CO2R°, -NR°NR°C(O)R°, -NRoNRoC(O)N(Ro)2, -NRoNRoCO2Ro, -C(O)C(O)Ro, -C(O)CH2C(O)Ro, -CO2Ro, -C(O)Ro, -C(O)N(Ro)2, -OC(O)N(Ro)2, -S(O)2Ro, -SO2N(Ro)2, -S(O)Ro, -NRoSO2N(Ro)2, -NRoSO2Ro, -C(=S)N(Ro)2, -C(=NH)-N(Ro)2, -(CH2)yNHC(O)Ro или -(CH2)yNHC(O)CH(V-Ro)(Ro), причем каждый Ro независимо выбран из водорода, необязательно замещенной С1-6алифатической группы, незамещенного 5-6-членного гетероарильного или гетероциклического кольца, фенила (Ph), -O(Ph) или -CH2(Ph)-CH2(Ph), причем y равен 0-6 и V означает связующую группу. Заместители алифатической группы Ro выбраны из групп NH2, NH(C1-4алифатической), N(C1-4алифатической), галогена, С1-4алифатической, ОН, О-(С1-4алифатической), NO2, CN, CO2H, CO2(C1-4алифатической), О(галогенС1-4алифатической) или галогенС1-4алифатической.
Алифатическая группа или неароматическое гетероциклическое кольцо могут содержать один или более заместителей. Подходящие заместители у насыщенного атома углерода алифатической группы или неароматического гетероциклического кольца выбраны из тех, что перечислены выше для ненасыщенного углерода арильной или гетероарильной группы, и из следующих: =O, =S, =NNHR*, =NN(R*)2, =N-, =NNHC(O)R*, =NNHCO2(алкил), =NNHSO2(алкил) или =NR*, где каждый R* независимо выбран из водорода или необязательно замещенной С1-6алифатической группы. Заместители алифатической группы R* выбраны из групп NH2, NH(C1-4алифатической), N(C1-4алифатической)2, галогена, С1-4алифатической, ОН, О-(С1-4алифатической), NO2, CN, CO2H, CO2(C1-4алифатической), -O(галогенС1-4алифатической) или галогенС1-4алифатической.
Заместители азота неароматического гетероциклического кольца выбраны из -R+, -N(R+)2, -C(O)R+, -CO2R+, -C(O)C(O)R+, -C(O)CH2C(O)R+, -SO2R+, -SO2N(R+)2, -C(=S)N(R+)2, -C(=NH)-N(R+)2 или -NR+SO2R+; где R+ означает водород, необязательно замещенную С1-6алифатическую группу, необязательно замещенный фенил (Ph), необязательно замещенный -O(Ph), необязательно замещенный -CH2(Ph), необязательно замещенный -CH2CH2(Ph) или незамещенное 5-6-членное гетероарильное или гетероциклическое кольцо. Заместители алифатической группы или фенильного кольца R+ выбраны из групп NH2, NH(C1-4алифатической), N(C1-4алифатической)2, галогена, С1-4алифатической, ОН, О-(С1-4алифатической), NO2, CN, CO2H, CO2(C1-4алифатической), -О(галогенС1-4алифатической) или галогенС1-4алифатической.
Термин "алкилиденовая цепь" относится к необязательно замещенной, прямой или разветвленной углеродной цепи, которая может быть полностью насыщенной или содержать одно или более звеньев ненасыщенности. Необязательные заместители те, что описаны выше для алифатической группы.
Термин "объемная группа" относится к группе, которая разделяет и ориентирует другие части молекулы, присоединенные к ней, таким образом, что соединение легко взаимодействует с функциональными группами в активном месте энзима. Указанная в данном тексте объемная группа разделяет и ориентирует кольцо А и QR2 внутри активного места так, что они могут реализовать благоприятные взаимодействия с функциональными группами, которые существуют внутри активного места энзима ERK2. Когда объемной группой является 5-членное гетероароматическое кольцо, кольцо А и группа QR2 присоединены в несопряженных положениях "В" и "С", а 5-членное кольцо присоединено к кольцу А в точке "D", а к QR2 в точке "Е", как показано ниже.
Предпочтительно расстояние между "D" и "C" составляет 3,7Å, расстояние между "D" и "Е" составляет 5,0Å, расстояние между "В" и "С" составляет 2,2Å, и расстояние между "В" и "Е" составляет 3,5Å, причем точность каждого из описанных выше расстояний составляет плюс/минус 0,2Å.
Сама объемная группа также может дополнительно взаимодействовать внутри активного места с дополнительным увеличением ингибирующего действия соединений. Например, когда Sp представляет пиррол, то пиррол-NH может образовать дополнительную водородную связь внутри активного места энзима ERK2.
Термин "связующая группа" означает органическую группу, которая соединяет две части соединения. Связующие группы обычно включают такой атом, как атом кислорода или серы, такую группу, как -NH-, -CH2-, -CO-, или цепь атомов, такую как алкилиденовая цепь. Молекулярная масса связующей группы обычно лежит в интервале примерно от 14 до 200. Примеры связующих групп включают насыщенную или ненасыщенную С1-6алкилиденовую цепь, которая необязательно замещена, и при этом до двух насыщенных атомов углерода цепи необязательно замещены такими группами, как -C(O)-, -C(O)C(O)-, -CONR7-, -CONR7NR7-, -CO2-, -OC(O)-, -NR7CO2-, -O-, -NR7CONR7-, -OC(O)NR7-, -NR7NR7-, -NR7CO-, -S-, -SO-, -SO2-, -NR7-, -SO2NR7- или -NR7SO2-.
Как использовано в настоящем тексте, связующая группа Q соединяет Sp с R2. Q также может давать дополнительные взаимодействия внутри места связывания ERK2 с дополнительным увеличением ингибирующего действия соединения. Когда Q представляет карбонилсодержащий остаток, такой как -C(O)-, -CO2- -OC(O)-, -C(O)C(O)-, -CONH-, -CO2NH-, -CONHNH-, -NHCO-, -OC(O)NH- или -NHCO2, или такой сульфонилсодержащий остаток, как -SO2-, -SO2NH- или -NHSO2-, кислород карбонила или сульфонила образует водородную связь с лизином 54 в месте связывания ERK2. Когда Q представляет собой NH-содержащий остаток, такой как -CH2NH- или NHNH-, NH-группа образует водородную связь с остатком аспарагиновой кислоты 167 в месте связывания ERK2. Когда Q представляет собой гидрофобную группу, такую как алкильная цепь, -О- или -S-, Q дает дополнительные гидрофобные взаимодействия с местом связывания ERK2.
R2 дает гидрофобные взаимодействия внутри места связывания ERK2, особенно с атомами углерода боковой цепи лизина 54 и аспарагиновой кислоты 167. R2 также может давать гидрофобные взаимодействия с обогащенной глицином петлей, которая состоит из аминокислотных остатков 33-38. Когда R2 является замещенным, заместители могут обеспечивать дополнительные взаимодействия внутри места связывания с увеличением ингибирующего действия соединения. Например, когда заместителем R2 является донор водородной связи или акцептор водородной связи, указанный заместитель образует водородную связь с молекулами энзим-связанная вода, которые существуют в месте связывания.
Используемая в данном тексте связующая группа Т, когда она присутствует, соединяет Sp с R1. Т также может дополнительно взаимодействовать внутри места связывания ERK2 c дополнительным увеличением ингибирующего действия соединения. Когда Т представляет собой карбонилсодержащую группу, такую как -CO-, -CO2-, -OCO-, -COCO-, -CONH-, -CO2NH-, -CONHNH-, -NHCO- или -NHCO2-, или такую сульфонилсодержащую группу, как -SO2-, -SO2NH- или -NHSO2-, кислород карбонила или сульфонила образует водородную связь с NH глутамина 105 в месте связывания ERK2. Когда Т означает такую NH-содержащую группу, как -CH2NH- или -NHNH-, NH-группа образует водородную связь с карбонилом глутамина 105. Когда Т означает такую гидрофобную группу, как алкильная цепь, -О- или -S-, Т дает дополнительные гидрофобные взаимодействия с атомами углерода боковой цепи глутамина 105, а также изолейкина 84.
Описанные здесь связывающие взаимодействия между соединениями по настоящему изобретению и местом связывания ERK2 определены с помощью программ молекулярного моделирования, которые известны специалистам в данной области. Эти программы молекулярного моделирования включают QUANTA [Molecular Simulations, Inc., Burlington, Mass., 1992] и SYBYL [Molecular Modeling Software, Tripos Associates, Inc., St. Louis, Mo., 1992]. Использованное в настоящем описании численное обозначение аминокислот для фермента ERK2 соответствует входу в Swiss-Prot базу данных для оценки #P28482. Swiss-Prot база данных является международной базой данных по последовательности белка, распространяемой Европейским институтом биоинформатики (European Bioinformatics Institute (EBI)) в Женеве, Швейцария. Базу данных можно найти на сайте www.ebi.ac.uk/swissprot.
Соединения по настоящему изобретению ограничиваются теми, которые являются химически доступными и стабильными.
Поэтому комбинация заместителей или изменения в описанных выше соединениях допустимы только тогда, когда такая комбинация приводит к получению стабильного или химически доступного соединения. Стабильное соединение или химически доступное соединение представляет собой соединение, в котором химическая структура по существу не меняется при сохранении температуры 40°С или меньше, в отсутствие влаги или других химически реакционноактивных условий, по меньшей мере, в течение недели.
Если не указано иного, изображенные в настоящем описании структуры также подразумевают включение всех стереохимических форм структуры; т.е. R и S конфигураций для каждого центра асимметрии. Поэтому единственные стереохимические изомеры, а также смеси энантиомеров и диастереомеров по настоящему изобретению входят в объем притязаний изобретения. Если не указано иного, то подразумевается, что изображенные в настоящем тексте структуры включают соединения, которые различаются только наличием одного или более обогащенных изотопом атомов. Например, соединения, имеющие настоящие структуры, но в которых водород заменен дейтерием или тритием, или в которых углерод заменен на 13С- или 14С-обогащенный углерод, также входят в объем притязаний настоящего изобретения.
Соединения формулы I или их соли могут быть представлены в виде композиций. В предпочтительном варианте осуществления композицией является фармацевтически приемлемая композиция. В одном варианте осуществления композиция включает такое количество ингибитора протеинкиназы, которое эффективно для ингибирования протеинкиназы, особенно ERK2, в биологическом образце или у пациента. В другом варианте осуществления соединения настоящего изобретения и их фармацевтически приемлемые композиции, которые включают такое количество ингибитора протеинкиназы, которое эффективно для лечения или предупреждения опосредованных действием ERK-2 состояний, и фармацевтически приемлемый носитель, добавку или разбавитель, могут быть составлены для введения пациенту.
Термин "пациент" включает людей и ветеринарные объекты.
Термин "биологический образец", использованный в настоящем описании, включает, без ограничения объема притязаний, клеточные культуры или их экстракты; препараты энзима, пригодные для оценки in vitro; материал биопсии, полученный от млекопитающего, или его экстракты; и кровь, слюну, мочу, кал, семенную жидкость, слезы или другие жидкости тела или их экстракты.
Другие аспекты настоящего изобретения относятся к способу лечения или предупреждения опосредованного действием ERK-2 заболевания, причем этот способ включает введение пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы I или фармацевтически приемлемой композиции, содержащей указанное соединение.
Термин "опосредованное действием ERK-2 состояние" или "заболевание", использованный в настоящем описании, означает любое заболевание или другое неблагоприятное состояние, при котором, как известно, ERK-2 играет определенную роль. Термин "опосредованное действием ERK-2 состояние" или "заболевание" также означает те заболевания или состояния, которые облегчаются при лечении ингибитором ERK-2. Такие состояния включают, без ограничения объема притязаний, рак, удар, диабет, гепатомегалию, заболевания сердечно-сосудистой системы, включая кардиомегалию, болезнь Альцгеймера, муковисцидоз, вирусные заболевания, аутоиммунные заболевания, атеросклероз, рестеноз, псориаз, аллергические заболевания, включая астму, воспаление, нейрологические заболевания и гормоно-обусловленные заболевания. Термин "рак" включает, но не ограничивает объема притязаний, следующие виды рака: груди, яичников, шейки матки, простаты, яичек, мочеполовых путей, пищевода, гортани, глиобластома, нейробластома, рак желудка, кожи, кератоакантома, рак легких, плоскоклеточный рак, крупноклеточный рак, мелкоклеточный рак, легочная аденокарционома, рак костей, толстой кишки, аденома, рак поджелудочной железы, аденокарцинома, рак щитовидной железы, фолликулярная карцинома, недифференцированная карцинома, папиллокарцинома, семинома, меланома, саркома, рак мочевого пузыря, рак печени и желчных протоков, рак почек, болезни спинного мозга, болезни лимфоидные, болезнь Ходжкина, "волосатые" клетки, рак преддверия рта и глотки (ротовой), рак губы, рак языка, рта, глотки, тонкой кишки, рак ободной-прямой кишки, рак толстой кишки, прямой кишки, рак мозга и центральной нервной системы и лейкемия.
Настоящий способ особенно применим для лечения заболеваний, которые облегчаются при использовании ингибитора ERK2 или других протеинкиназ. Хотя настоящие соединения были разработаны как ингибиторы ERK2, было установлено, что некоторые соединения по настоящему изобретению также ингибируют другие протеинкиназы, такие как GSK3, Aurora2, Lck, CDK2 и AKT3.
Другой аспект настоящего изобретения относится к способу ингибирования активности ERK-2 в биологическом образце, причем этот способ включает контактирование биологического образца с соединением формулы I или фармацевтически приемлемой композицией, включающей указанное соединение.
Другой аспект настоящего изобретения относится к способу ингибирования активности ERK-2 у пациента, причем этот способ включает введение пациенту соединения формулы I или фармацевтически приемлемой композиции, включающей указанное соединение.
Другой аспект настоящего изобретения относится к способу лечения или предупреждения Aurora-2 опосредованных заболеваний, при этом способ включает введение пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы I или фармацевтически приемлемой (композиции), включающей указанное соединение.
Термин "Aurora-2 опосредованное состояние" или "заболевание", использованный в данном описании, подразумевает любое заболевание или другое неблагоприятное состояние, при котором, как известно, Aurora играет определенную роль. Термин "Aurora-2 опосредованное состояние" или "заболевание" также подразумевает заболевания или состояния, которые облегчаются лечением ингибитором Aurora-2. Такие состояния включают, без ограничения объема притязаний, рак. Термин "рак" включает, но не ограничивает объема притязаний, следующие виды рака: толстой кишки, груди, желудка и яичников.
Другой аспект настоящего изобретения относится к ингибированию активности Aurora-2 в биологическом образце, причем этот способ включает контактирование биологического образца с соединением формулы I или фармацевтически приемлемой композицией, включающей указанное соединение.
Другой аспект настоящего изобретения относится к способу ингибирования активности Aurora-2 у пациента, при этом способ включает введение пациенту соединения формулы I или фармацевтически приемлемой композиции, включающей указанное соединение.
Другой аспект настоящего изобретения относится к способу лечения или предупреждения GSK-3-опосредованных заболеваний, причем способ включает введение пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы I или фармацевтически приемлемой композиции, включающей указанное соединение.
Термин "GSK-3-опосредованное состояние" или "заболевание", использованный в настоящем описании, означает любое заболевание или другое неблагоприятное состояние, в котором, как известно, GSK-3 играет роль. Такие заболевания и состояния включают, без ограничения объема притязаний, диабет, болезнь Альцгеймера, болезнь Хантингтона, болезнь Паркинсона, слабоумие, связанное со СПИДом, боковой амиотрофический склероз (AML), рассеянный склероз (MS), шизофрению, гипертрофию миокарда, реперфузию/ишемию и алопецию.
Один из аспектов настоящего изобретения относится к способу ускорения синтеза гликогена и/или снижению уровня глюкозы в крови пациента, нуждающегося в этом, причем способ включает введение пациенту терапевтически эффективного количества соединения формулы I или его фармацевтически приемлемой соли. Этот способ особенно применим для больных диабетом. Другой способ относится к ингибированию образования гиперфосфорилированного Tau протеина, который используют для прекращения или замедления развития болезни Альцгеймера. Другой способ относится к ингибированию фосфорилирования β-катенина, который используют для лечения шизофрении.
Другой аспект настоящего изобретения относится к ингибированию GSK-3 активности в биологическом образце, причем способ включает контактирование биологического образца с соединением формулы I.
Другой аспект настоящего изобретения относится к способу ингибирования GSK-3 активности у пациента, причем способ включает введение пациенту соединения формулы I или фармацевтически приемлемой композиции, включающей указанное соединение.
Ингибирование активности ERK2, Aurora2, CDK2, GSK-3, Lck или AKT3 киназ в биологическом образце может быть использовано для различных целей, которые известны специалистам в данной области, примеры таких целей включают, но не ограничивают объема притязаний, переливание крови, трансплантацию органов, хранение биологических образцов и биологические пробы.
Термин "фармацевтически приемлемый носитель, добавка или разбавитель" относится к нетоксичному носителю, добавке или растворителю, который может быть введен пациенту вместе с соединением настоящего изобретения и который не разрушает его фармакологической активности.
Количество, эффективное для ингибирования протеинкиназы, например, Aurora2 и GSK-3, составляет количество, заметно ингибирующее активность киназы при сравнении с активностью фермента в отсутствие ингибитора. Для определения степени ингибирования может быть использован любой метод, такой как, например, описанные ниже примеры биологического тестирования.
Фармацевтически приемлемые носители, которые могут быть использованы в таких фармацевтических композициях, включают, но не ограничивают объема притязаний, ионообменные смолы, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как альбумин человеческой сыворотки, буферные вещества, такие как фосфаты, глицин, сорбиновая кислота, сорбат калия, смеси частичных глицеридов насыщенных растительных жирных кислот, вода, соли или электролиты, такие как сульфат протамина, гидрофосфат динатрия, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный диоксид кремния, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, карбоксиметилцеллюлоза натрия, полиакрилаты, воски, блок-полимеры типа полиэтилен-полиоксипропилен, полиэтиленгликоль и линолин.
Композиции по настоящему изобретению могут быть введены перорально, парентерально, ингаляцией спрея, локально, ректально, назально, трансбуккально, вагинально или через имплантированный резервуар. Термин "парентерально", использованный в настоящем описании, включает введение подкожно, внутривенно, внутримышечно, интраартикуллярно, внутрисуставно, внутригрудинно, внутриоболочечно, внутрипеченочно, внутрь патологического изменения и интракраниальной инъекцией или методами вливания. Предпочтительно композиции вводят перорально, внутрибрюшинно или внутривенно.
Стерильные формы для вливаний композиций по настоящему изобретению могут представлять собой водные или маслянистые суспензии. Эти суспензии могут быть составлены согласно известным в данной области техники методам с использованием подходящих диспергирующих или смачивающих агентов и суспендирующих агентов. Стерильным препаратом для вливаний также может быть стерильный раствор или суспензия для вливаний в нетоксичном, парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Среди подходящих разбавителей и растворителей, которые могут быть использованы, можно указать воду, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды обычно исполь