Гликопептид глицирризиновой кислоты с l-пролином, стимулирующий гуморальный иммунный ответ
Иллюстрации
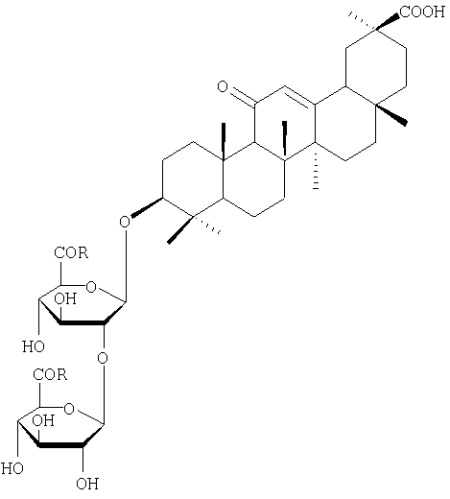
Показать всеОписывается новое химическое соединение - производное глицирризиновой кислоты, а именно гликопептид глицирризиновой кислоты с L-пролином: 3-О-{2-О-[N-(β-O-глюкопиранозилуроноил)-L-пролин-N-(β-D-глюкопиранозилуроноил)-L-пролин]}-(3β, 20β)-11-оксо-олеан-12-ен-30-оевая кислота, стимулирующий гуморальный иммунный ответ. Соединение является малотоксичным и повышает уровень агглютининов (в 3,7 раз) и гемолизинов (в 3 раза) в крови у мышей по сравнению с контролем, превосходя препарат сравнения - гликопептид ГК с (S-бензил)-L-цистеином, являющийся его структурным и фармакологическим аналогом, по стимулирующей активности на выработку агглютининов при введении в дозе 2 мг/кг. 1 табл.
Реферат
Изобретение относится к новым биологически активным соединениям, конкретно к гликопептиду глицирризиновой кислоты с L-пролином (Pro): 3-O-{2-O-[N-(β-D-глюкопиранозилуроноил)-L-пролин-N-(β-D-глюкопиранозилуроноил)-L-пролин]}-(3β, 20β)-11-оксо-олеан-12-ен-30-оевая кислота, формулы (Iб), стимулирующему первичный иммунный ответ. Указанное соединение и его свойства в литературе не описаны.
Известно, что глицирризиновая кислота (ГК) и ее производные, содержащие фрагменты аминокислот и их алкиловых эфиров, проявляют иммуномодулирующую активность (Г.А.Толстиков, Л.А.Балтина, Э.Э.Шульц, А.Г.Покровский. Глицирризиновая кислота. // Биоорган, химия, 1997, т.23, №9, с.691-709; Р.М.Кондратенко, Л.А.Балтина, С.Р.Мустафина, Н.В.Макарова, Х.М.Насыров, Г.А.Толстиков. Способ получения кристаллической глицирризиновой кислоты из промышленного глицирама. Иммуномодулирующие свойства. // Хим.-фарм. жур., 2001, т.35, №2, с.39-42; Л.А.Балтина, Г.М.Сахаутдинова, Ф.С.Зарудий, Д.Н.Лазарева, Г.А.Толстиков, В.А.Давыдова. Синтез гликопептидов глицирризиновой кислоты и их Иммуномодулирующие свойства. // Хим.-фарм. жур., 1990, №2, с.119-121; Л.А.Балтина, С.А.Рыжова, Е.В.Васильева, Г.А.Толстиков, Г.М.Сахаутдинова, Ф.С.Зарудий. Трансформации глицирризиновой кислоты. VIII. Синтез иммуномодулирующих гликопептидов с использованием трет-бутиловых эфиров аминокислот. // Биоорган. химия, 1994, т.20, №12, с.1365-1374).
(1a) R=L-Pro-OBut
(Iб) R=L-Pro-OH
(II) R=L-Cys (SBzl)-ОН
Задача, на решение которой направлено заявленное техническое решение, заключается в поиске нового малотоксичного соединения в ряду гликопептидов ГК, обладающего иммуностимулирующей активностью. В заявленном техническом решении синтезировано новое химическое соединение - гликопептид ГК, содержащий остатки L-пролина формулы (Iб), стимулирующий выработку агглютининов и гемолизинов в сыворотке крови мышей.
Способ получения предлагаемого соединения заключается в том, что ГК обрабатывают N-гидроксисукцинимидом (HOSu) и N,N'-дициклогексилкарбодиимидом (DCC) в среде тетрагидрофурана (ТГФ), при 0-+5°С в течение 2 ч при соотношении реагентов ГК: HOSu: DCC=1:4:2,5 ммоль, отфильтровывают осадок N,N'-дициклогексилмочевины, к фильтрату при 0-+5°С прибавляют 2,5 ммоля гидрохлорида трет-бутилового эфира L-пролина и 3 ммоль триэтиламина, перемешивают смесь при этой температуре 1 ч и выдерживают при комнатной температуре 20 ч.
Реакционную смесь разбавляют холодной водой, подкисляют лимонной кислотой до рН˜4, осадок отфильтровывают, промывают водой, сушат и хроматографируют на колонке с силикагелем (СГ). Гомогенные фракции объединяют и упаривают. Выход защищенного гликопептида (Iа) 49,5%.
Защищенный гликопептид (Iа) обрабатывают трифторуксусной кислотой в хлористом метилене при комнатной температуре 1 ч, упаривают растворители и остаток хроматографируют на колонке с СГ и получают 0,29 г (64,4%) гомогенного по ТСХ целевого гликопептида (Iб), структура которого подтверждена спектральными методами и данными элементного анализа.
Острая токсичность соединения (Iб) изучена на белых беспородных мышах массой 15-20 г при внутрибрюшинном введении по методу Кербера (Елизарова О.Н. Определение пороговых доз промышленных ядов при пероральном введении. М.: Медицина, 1971. С.47-48.). Данное соединение в дозе до 950 мг/кг токсических явлений не вызывало и может быть отнесено к III классу малоопасных веществ.
Влияние гликопептида (Iб) на гуморальные звенья иммунного ответа изучено на белых беспородных мышах массой 18-20 г при сенсибилизации 3% взвесью эритроцитов барана (ЭБ). С первого дня сенсибилизации животные получали соединение (1б) внутрь в дозах 10 мг/кг (7-дневное введение) и 2 мг/кг (10-дневное введение). Контрольным животным вводили физиологический раствор или структурный аналог, обладающий высокой иммуностимулирующей активностью, гликопептид ГК с S-бензил-L-цистеином (II), полученный ранее и описанный в работе (Р.М.Кондратенко, Л.А.Балтина, Е.В.Васильева, Л.А.Балтина (мл.), А.Ф.Исмагилова, Х.М.Насыров, Н.Ж.Басченко, Р.М.Киреева. Синтез и иммуностимулирующая активность цистеинсодержащих гликопептидных производных глицирризиновой кислоты. // Биоорган, химия, 2004, т.30, №1, с.61-67).
Через сутки у животных путем декапитации собирали кровь, в сыворотке которой определяли содержание агглютининов и гемолизинов согласно работе (В.В.Сперанский. Роль хронического гонадотропина, аутоантител к нему и его аналогов в системе иммунитета в норме и патологии. Дисс. д-ра мед. наук, Казань, 1990. С.346). Реакцию оценивали при помощи Log2 титров антител - гемагглютининов и гемолизинов. Результаты опытов приведены в таблице.
Как видно из таблицы, соединение (Iб) через 7 суток в дозе 10 мг/кг статистически значимо повышает уровень агглютининов и гемолизинов по сравнению с контролем (в 3,7 раза и 3 раза соответственно). К 14-му дню титр агглютининов в группе животных, получивших соединение (Iб) в дозе 2 мг/кг, был выше в 4 раза, а титр гемолизинов в 2,5 раза по сравнению с контрольными животными, получившими внутрь физиологический раствор. Соединение (Iб) по стимулирующей активности на выработку агглютининов превосходит препарат сравнения (II) ˜ в 2 раза в дозе 2 мг/кг при 14-ти дневном введении и не уступает ему по стимулирующему действию на выработку гемолизинов в обеих исследованных дозах.
Таким образом, соединение (Iб) является малотоксичным соединением, которое обладает выраженным стимулирующим действием на гуморальные звенья иммунного ответа и превосходит по иммуностимулирующей активности структурный и фармакологический аналог - гликопептид ГК (II) (референс-препарат).
Сущность изобретения иллюстрируется следующими примерами.
Пример 1. Влияние гликопептида (Iб) на гуморальные звенья иммунного ответа.
Влияние гликопептида (Iб) на гуморальные звенья иммунного ответа изучено на белых беспородных мышах массой 18-20 г. Опыты проведены на 3-х группах животных (по 14 мышей в каждой группе, разделенных на 2 подгруппы по 7 мышей) при сенсибилизации мышей 3% взвесью эритроцитов барина (ЭБ) по 0,5 мл на мышь (внутрибрюшинно). С первого дня сенсибилизации животные получали исследуемое соединение внутрь в дозах 10 мг/кг (7-ми дневное введение) и 2 мг/кг (14-ти дневное введение). Контрольным животным вводили внутрь физиологический раствор. В качестве препарата сравнения использовали гликопептид ГК с S-бензил-L-цистеином (II) в дозах 10 и 2 мг/кг, описанный в работе (Р.М.Кондратенко, Л.А.Балтина, Е.В.Васильева, Л.А.Балтина (мл.), А.Ф.Исмагилова, Х.М.Насыров, Н.Ж.Басченко, Р.М.Киреева, Г.А.Толстиков. Синтез и иммуностимулирующая активность цистеинсодержащих гликопептидных производных глицирризиновой кислоты. // Биоорган, химия, 2004, т.30, №1, с.61-67).
На 7-й и 14-й день сенсибилизации мышам каждой подгруппы субплантарно в правую лапку вводили разрешающую дозу ЭБ в концентрации 108; другая лапка оставалась интактной. Через сутки у животных путем декапитации собирали кровь, в сыворотке которой определяли содержание агглютининов и гемолизинов по методике (В.В.Сперанский. Роль хронического гонадотропина, аутоантител к нему и его аналогов в системе иммунитета в норме и патологии. Дисс. д-ра мед. наук, Казань, 1990. С.346). Реакцию оценивали при помощи Log2 титра антител - гемагглютининов и гемолизинов. Результаты опытов приведены в таблице.
Соединение (Iб) в дозе 10 мг/кг при 7-ми дневном введении статистически значимо повышает титр агглютининов и гемолизинов соответственно в 3,7 и 3 раза по сравнению с контролем. При 14-ти дневном введении в дозе 2 мг/кг титр агглютининов в группе животных, получивших соединение (Iб) был в 4 раза выше, а титр гемолизинов в 2,5 раза по сравнению с контролем. Таким образом, гликопептид (Iб) ˜ в 2 раза превосходит референс-препарат - гликопептид (II) по стимулированию агглютининов в дозе 2 мг/кг и не уступает последнему по стимулирующей активности на выработку гемолизинов.
Пример 2. Синтез 3-O-{2-O-[N-(β-D-глюкопиранозилуроноил)-L-пролин-N-(β-D-глюкопиранозилуроноил)-L-пролин]}-(3β, 20β)-11-оксо-олеан-12-ен-30-оевой кислоты (Iб).
1. К раствору 0,82 г (1 ммоль) глицирризиновой кислоты в 20 мл сухого ТГФ при 0-+5°С прибавили 0,46 г (4 ммоль) N-гидроксисукциниимида, 0,5 г (2,4 ммоль) N,N'-дициклогексилкарбодиимида и перемешивали при этой температуре 2 ч. Осадок N,N'-дициклогексилмочевины отфильтровали, к фильтрату при 0-+5°С прибавляли 0,58 г (2,5 ммоль) гидрохлорида трет-бутилового эфира L-пролина и 0,5 мл (3,6 ммоль) триэтиламина, перемешивали смесь при этой температуре 1 ч и выдерживали 20 ч при комнатной температуре с периодическим перемешиванием. Реакционную смесь разбавляли водой, подкисляли лимонной кислотой до рН˜4, осадок отфильтровывали, промывали водой и сушили. Продукт (1,0 г) хроматографировали на колонке с силикагелем L (40/100 мкм), элюируя смесью хлороформа-метанола-воды, 300:10:1, 200:10:1 и 100:10:1 (V%). Смесью 200:10:1 вымывали 0,55 г (49,5%) защищенного гликопептида (Ia), гомогенного по ТСХ. Rf=0,54 (хлороформ-метанол-вода, 45:10:1). ИК-спектр, ν, см-1: 3600-3200 (ОН, NH); 1730 (COOR); 1710 (COOH); 1660 (С=O); 1540 (CONH). УФ-спектр, λmax (MeOH) (lg ε): 250 нм (4,1). Найдено, %: N 2,58. C60H91N2O17. Вычислено, %: N 2,52. Мr=1112,34.
2. 0,5 г (0,45 ммоль) защищенного гликопептида (Iа) выдержали в течение 1 ч в смеси 10 мл трифторуксусной кислоты и 10 мл хлористого метилена. Остаток после упаривания растворителей хроматографировали на колонке с силикагелем, элюируя смесью хлороформа-метанола-воды, 100:10:1, 50:10:1 (V%). Выход гликопептида (Iб) 0,29 г (64,4%). Rf=0,48 (хлороформ-метанол-вода, 45:10:1), [α]D 20+45°С (с 0,02; MeOH). ИК-спектр, ν, см-1: 3600-3200 (ОН, NH); 1710-1720 (COOH); 1660 (C=O). УФ-спектр, λmax (MeOH) (lg ε): 250,5 нм (4,05). Найдено, %: N 2,82. C52H75N2O17. Вычислено, %: N 2,80. Mr=1000,13. Спектр ЯМР 13С (CD3OD, δ, м.д.): 40,3 (C1); 90,9 (С3); 56,5 (С5); 33,8 (С7); 63,2 (С9); 202,5 (С11); 128,9 (С12); 168,9 (С13); 27,4 (С15); 32,9 (С17); 42.5 (С19); 32,0 (С21); 180,5 (С30); 105,4 (С1'); 83,8 (С2'); 75,7 (С3'); 72,4 (С4'); 77,3 (С5'); 172,7 (С6'); 106,1 (C1"); 74,8 (С2"); 75,1 (С3"); 72,2 (С4"); 77,6 (С5"); 172,9 (С6"). Остатки L-пролина: 175,0; 173,2; 61,7; 61,3; 30,2; 30,1; 25,8; 25,6; 44,9; 44,6.
| Таблица | ||
| Влияние гликопептида (Iб) на уровень агглютининов и гемолизинов у сенсибилизированных мышей | ||
| Соединения | Через 7 дней (10 мг/кг) | Через 14 дней (2 мг/кг) |
| Агглютинины (Log2) | ||
| (Iб) | 1,50±0,22* | 3,40±0,10* |
| (II) | 1,00±0,20* | 1,75±0,10* |
| Контроль | 0,40±0,24 | 0,80±0,20 |
| Гемолизины (Log2) | ||
| (Iб) | 1,20±0,20* | 1,90±0,10* |
| (II) | 1,00±0,10* | 1,30±0,10* |
| Контроль | 0,40±0,30 | 0,75±0,30 |
| *р<0,05 (достоверно относительно контроля) |
Гликопептид глицирризиновой кислоты с L-пролином формулы
R=L-Pro-OH,
стимулирующий гуморальный иммунный ответ.