Производные пропионовых кислот и их применение в качестве активаторов hppars.
Иллюстрации
Показать всеСоединение формулы (I) или его фармацевтически приемлемая соль, сольват или гидролизуемый сложный эфир, где R1 и R2 независимо представляют собой водород или С1-3алкил; Х представляет собой О; один из R3 и R4 независимо представляет собой водород, а другой представляет собой C1-3алкил; X1 представляет собой CH2 или SO2; R5 представляет собой -C1-6алкил (возможно замещенный С1-6алкокси или C1-6алкилтио), -С2-6алкенил, -С0-6алкилфенил (где фенил возможно замещен одним или более чем одним CF3, галогеном, C1-3алкилом, С1-3алкокси), -COC1-6алкил, SO2С1-6алкил; R6 представляет собой фенил или 6-членную гетероарильную группу, содержащую 1 или 2 атома N, причем фенил или гетероарильная группа возможно замещена 1, 2 или 3 группировками, выбранными из группы, состоящей из C1-6алкила, фенила (возможно замещенного одной или более чем одной группой, выбранной из галогена, CF3, С1-3алкила, OC1-3алкила, CN). Соединение формулы (I) предназначено для применения в качестве активатора рецепторов человека, активируемых пероксисомными пролифераторами (hPPAR). Технический результат - производные пропионовых кислот, активирующие рецепторы человека, активируемые пероксисомными пролифераторами (hPPAR). 2 н. и 12 з.п. ф-лы.
Реферат
Химические соединения
Настоящее изобретение относится к некоторым новым соединениям. В частности, настоящее изобретение относится к соединениям, которые активируют рецепторы человека, активируемые пероксисомными пролифераторами (hPPARs). Настоящее изобретение также относится к способу получения соединений, их применению в медицине, фармацевтическим композициям, содержащим их, и к способам предупреждения или лечения PPAR-опосредованных заболеваний или состояний.
С сердечно-сосудистым заболеванием связывают несколько независимых факторов риска. Они включают гипертензию, повышенные уровни фибриногена, высокие уровни триглицеридов, повышенный LDL-холестерин (холестерин липопротеинов низкой плотности), повышенный общий холестерин и низкие уровни HDL-холестерина (холестерина липопротеинов высокой плотности). Ингибиторы HMG-CoA-редуктазы (3-гидрокси-3-метилглютарил-коэнзим А-редуктазы) ("статины") полезны для лечения состояний, характеризующихся высокими уровнями LDL-c (холестерина липопротеинов низкой плотности). Было показано, что уменьшение LDL-c не является достаточным для снижения риска сердечно-сосудистого заболевания у некоторых пациентов, в частности у пациентов с нормальными уровнями LDL-c. Эту популяцию определяют по независимому фактору риска - низкому HDLc (холестерину липопротеинов высокой плотности). Лекарственная терапия до сих пор была недостаточно успешно направлена на повышенный риск сердечно-сосудистого заболевания, связанного с низкими уровнями HDL-c (Bisgaier, C.L; Pape, M.E. Curr. Pharm. Des. 1998, 4, 53-70).
Синдром X (включая метаболический синдром) широко определяется как совокупность отклонений от нормы, включая гиперинсулинемию, ожирение, повышенные уровни следующих соединений: триглицеридов, мочевой кислоты, фибриногена, LDL-частиц небольшой плотности и ингибитора активатора плазминогена-1 (PAI-1), и пониженные уровни HDL-c.
NIDDM (инсулиннезависимый сахарный диабет) описывают как резистентность к инсулину, которая в свою очередь является причиной аномального продуцирования глюкозы и снижения потребления глюкозы скелетной мышцей. Эти факторы в итоге приводят к ухудшенной толерантности к глюкозе (IGT) и гиперинсулинемии.
Рецепторы, активируемые пероксисомными пролифераторами (PPARs), являются рецепторами-сиротами, принадлежащими к суперсемейству стероидных/ретиноидных рецепторов лигандактивируемых факторов транскрипции. Смотри, например, Willson T.M. and Wahli, W., Curr. Opin. Chem. Biol., 1, pp.235-241 (1997), и Willson T.M. et al., J. Med. Chem., 43, p.527-549 (2000). Связывание агонистов-лигандов с рецептором приводит к изменениям в уровне экспрессии мРНК, кодируемых генами-мишенями PPAR.
У млекопитающих были выделены три типа рецепторов, активируемых пероксисомными пролифераторами, и обозначены как PPAR-альфа, PPAR-гамма и PPAR-дельта (также известен как NUC1 или PPAR-бета). Эти PPARs регулируют экспрессию генов-мишеней посредством связывания с элементами последовательности ДНК, называемыми PPAR-отвечающими элементами (PPRE). До настоящего времени PPREs были идентифицированы в энхансерах ряда генов, кодирующих белки, которые регулируют метаболизм липидов, что позволяет предположить, что PPAR играют центральную роль в адипогенном сигнальном каскаде и липидном гомеостазе (Н.Keller and W.Wahli, Trends Endocrinol. Metab., 291-296, 4 (1993)).
В настоящее время сообщается о том, что лекарственные средства из класса тиазолидиндионов являются сильнодействующими и селективными активаторами PPAR-гамма и связываются непосредственно с PPAR-гамма рецептором (J.M.Lehmann et al., J.Biol. Chem., 12953-12956, 270 (1995)), что свидетельствует о том, что PPAR-гамма является возможной мишенью для терапевтических воздействий тиазолидиндионов.
В условиях клиники показано, что активаторы ядерного рецептора PPARγ, например розиглитазон, усиливают действие инсулина, понижают содержание глюкозы в сыворотке и оказывают небольшие, но значимые воздействия на снижение уровней триглицеридов в сыворотке у пациентов с диабетом 2 типа. Смотри, например, D.Е.Kelly et. al., Curr. Opin. Endocrinol. Diabetes., 90-96, 5 (2), (1998); M.D.Johnson et. al., Ann. Pharmacother., 337-348, 32 (3), (1997), и M.Leutenegger et al., Curr. Ther. Res., 403-416, 58 (7), (1997).
По-видимому, механизм этого понижающего уровень триглицеридов действия преимущественно заключается в повышенном клиренсе липопротеинов очень низкой плотности (VLDL) через индукцию экспрессии гена липопротеинлипазы (LPL). Смотри, например, В.Staels et al., Arterioscler. Thromb., Vasc., Biol., 1756-1764, 17 (9), (1997).
Фибраты представляют собой класс лекарственных средств, которые могут снижать триглицериды в сыворотке на 20-50%, снижать LDL-c на 10-15%, сдвигать размер LDL-частиц от более атерогенной малой плотности к LDL нормальной плотности и увеличивать HDLc на 10-15%. Экспериментальные данные указывают на то, что действия фибратов на липиды сыворотки опосредованы активацией PPARα. Смотри, например, В.Staels et al., Curr. Pharm. Des., 1-14, 3 (1), (1997). Активация PPARα вызывает транскрипцию ферментов, усиливающих катаболизм жирных кислот и уменьшающих синтез жирных кислот в печени de-novo, что ведет к уменьшению синтеза триглицеридов и к уменьшению продуцирования/секреции VLDL. Кроме того, активация PPARα уменьшает продуцирование ароС-III. Снижение уровня ароС-III, ингибитора активности LPL, повышает кпиренс VLDL. Смотри, например, J.Auwerx et al., Atherosclerosis (Shannon, Irel), S29-S37,124 (Suppl), (1996).
Некоторые соединения, которые активируют или иным образом взаимодействуют с одним или более PPARs, были вовлечены в регуляцию уровней триглицеридов или холестерина в моделях на животных. Смотри, например, патенты США 5847008 (Doebber et al.) и 5859051 (Adams et al.) и публикации PCT WO 97/28149 (Leibowitz et al.), WO 99/04815 (Shimokawa et al.) и WO 01/00603 (Glaxo Group Ltd.). В Oliver et al., Proc. Natl. Acad. Sci., 98, 5306-5311 (2001), сообщается об увеличении HDLc и понижении триглицеридов сыворотки у страдающей ожирением макаки-резус после введения агониста PPAR-дельта.
Согласно данному изобретению предложено соединение формулы (I) и его фармацевтически приемлемые соли и сольваты и гидролизуемые сложные эфиры
где R1 и R2 независимо представляют собой водород или С1-3алкил;
X представляет собой связь, СН2 или О;
R3 и R4 независимо представляют собой водород, C1-6алкил, ОСН3, CF3, аллил или галоген;
X1 представляет собой СН2, SO2 или СО;
R5 представляет собой -С1-6алкил (возможно замещенный С1-6алкокси или С1-6алкилтио), -С2-6алкенил, -С0-6алкилфенил (где фенил возможно замещен одним или более чем одним CF3, галогеном, C1-3алкилом, С1-3алкокси), -СОС1-6алкил, -SO2С1-6алкил;
R6 представляет собой фенил или 6-членную гетероарильную группу, содержащую 1, 2 или 3 атома N, при этом фенил или гетероарильная группа возможно замещена 1, 2 или 3 группировками, выбранными из группы, состоящей из С1-6алкила, галогена, -ОС1-6алкила, -SO2С1-3алкила, фенила (возможно замещенного одной или более группами, выбранными из галогена, CF3, C1-3алкила, ОС1-3алкила, ацетила, CN).
В другом аспекте настоящего изобретения описан способ предупреждения или лечения заболевания или состояния, опосредованного одним или более PPAR-альфа, -гамма или -дельта человека (DPPARs), включающий введение терапевтически эффективного количества соединения по данному изобретению. hPPAR-опосредованные заболевания или состояния включают дислипидемию, в том числе дислипидемию, связанную с диабетом, и смешанную дислипидемию, синдром Х (как определено в данной заявке, он включает метаболический синдром), сердечную недостаточность, гиперхолестеринемию, сердечно-сосудистое заболевание, включая атеросклероз, артериосклероз и гипертриглицеридемию, сахарный диабет II типа, диабет I типа, резистентность к инсулину, гиперлипидемию, воспаление, эпителиальные гиперпролиферативные заболевания, включая экзему и псориаз, и состояния, связанные с легким и кишечником и регуляцией аппетита и потребления пищи у субъектов, страдающих такими расстройствами, как ожирение, булимическая анорексия и нервная анорексия, рак, болезнь Альцгеймера и другие когнитивные нарушения. В частности, соединения по данному изобретению полезны в лечении и предупреждении диабета, ожирения и сердечно-сосудистых заболеваний и состояний, включая атеросклероз, артериосклероз, гипертриглицеридемию и смешанную дислипидемию.
В другом аспекте настоящего изобретения предложены фармацевтические композиции, содержащие соединение по изобретению, предпочтительно объединенное с фармацевтически приемлемым разбавителем или носителем.
В другом аспекте настоящего изобретения предложено соединение по изобретению для применения в терапии и, в частности, в терапии людей.
В другом аспекте настоящего изобретения предложено применение соединения по изобретению для изготовления лекарства для лечения hPPAR-опосредованного заболевания или состояния.
При использованиии в данном описании, "соединение по изобретению" означает соединение формулы (I) или его фармацевтически приемлемую соль, или сольват, или гидролизуемый сложный эфир.
Хотя гидролизуемые сложные эфиры включены в объем данного изобретения, предпочтительными являются кислоты, так как определенные данные позволяют предположить, что хотя сложные эфиры являются полезными соединениями, в действительности активными соединениями могут быть кислоты, до которых они гидролизуются. Из сложных эфиров, которые легко гидролизуются, в условиях анализа или in vivo может получаться карбоновая кислота. Как правило, карбоновая кислота активна как в анализах связывания, так и в анализах с временной трансфекцией, тогда как сложный эфир обычно не очень хорошо связывается, но активен в анализе с временной трансфекцией, предположительно вследствие гидролиза. Предпочтительными гидролизуемыми сложными эфирами являются С1-6алкильные сложные эфиры, в которых алкильная группа может быть прямой или разветвленной. Более предпочтительными являются метиловые или этиловые сложные эфиры.
Предпочтительно каждый R1 и R2 независимо представляет собой Н или метил. Более предпочтительно R1 и R2 оба представляют собой Н или оба представляют собой Me. Еще более предпочтительно R1 и R2 оба представляют собой Н.
Предпочтительно Х представляет собой О.
Предпочтительно R3 и R4 независимо представляют собой Н или C1-3алкил. Более предпочтительно по меньшей мере один из R3 и R4 представляет собой водород и, когда один из R4 и R3 представляет собой водород, а другой не является водородом, тогда тот радикал, который не является водородом, предпочтительно находится в орто-положении к изображенной группировке X. Более предпочтительно радикал, который не является водородом, представляет собой метил.
Предпочтительно X1 представляет собой СН2.
Предпочтительно R5 представляет собой бутил или метоксиэтил.
Предпочтительно R6 представляет собой фенил или 6-членный гетероцикл, выбранный из пиримидина, пиридина, пиридазина, пиразина, каждый из которых замещен фенилом (возможно замещенным одним или более чем одним CF3, C1-3алкилом, галогеном, CN) и возможно дополнительным C1-3алкильным заместителем. Предпочтительно этот фенильный заместитель находится в мета-положении к изображенной группе N. Более предпочтительно заместитель на фениле или 6-членном гетероцикле представляет собой пара-С6H4C3, C6H4Me или С6Н4Cl.
Предпочтительными соединениями по изобретению являются следующие:
2-метил-2-{2-метил-4-[([4-(трифторметил)бензил]{6-[4-(трифторметил)фенил]пиридин-2-ил}амино)метил]фенокси}пропановая кислота;
2-{4-[(бутил{6-[4-(трифторметил)фенил]пиридин-2-ил}амино)метил]-2-метилфенокси}-2-метилпропановая кислота;
{4-[(бутил{6-[4-(трифторметил)фенил]пиридин-2-ил}амино)метил]-2-метилфенокси}уксусная кислота;
[4-({бутил[4′-(трифторметил)-1,1′-бифенил-3-ил]амино}метил)-2-метилфенокси]-уксусная кислота;
[4-({(2-метоксиэтил)[4′-(трифторметил)-1,1′-бифенил-3-ил]амино}метил)-2-метилфенокси]уксусная кислота;
[2-метил-4-({пентил[4′-(трифторметил)-1,1′-бифенил-3-ил]амино}метил)-фенокси]уксусная кислота;
[4-({(2-циклопропилэтил)[4′-(трифторметил)-1,1′-бифенил-3-ил]амино}метил)-2-метилфенокси]уксусная кислота;
[2-метил-4-({пропил[4′-(трифторметил)-1,1′-бифенил-3-ил]амино}метил)-фенокси]уксусная кислота;
[2-метил-4-({[2-(метилтио)этил][4′-(трифторметил)-1,1′-бифенил-3-ил]амино}-метил)фенокси]уксусная кислота;
[4-({бутил[2-метил-4′-(трифторметил)-1,1′-бифенил-3-ил]амино}метил)-2-метилфенокси]уксусная кислота;
[4-({(2-метоксиэтил)[2-метил-4′-(трифторметил)-1,1′-бифенил-3-ил]амино}-метил)-2-метилфенокси]уксусная кислота;
[4-({бутирил[4′-(трифторметил)-1,1′-бифенил-3-ил]амино}метил)-2-метилфенокси]уксусная кислота;
[2-метил-4-({(пропилсульфонил)[4′-(трифторметил)-1,1′-бифенил-3-ил]амино}-метил)фенокси]уксусная кислота;
[4-({бутил[4′-(трифторметил)-1,1′-бифенил-3-ил]амино}сульфонил)-2-метилфенокси]уксусная кислота;
[2-метил-4-({пентил[4′-(трифторметил)-1,1′-бифенил-3-ил]амино}сульфонил)-фенокси]уксусная кислота;
[4-({(2-циклопропилэтил)[4′-(трифторметил)-1,1′-бифенил-3-ил]амино}-сульфонил)-2-метилфенокси]уксусная кислота;
{4-[(бутил{4-[4-(трифторметил)фенил]пиримидин-2-ил}амино)метил]-2-метилфенокси}уксусная кислота;
[4-({бутил[4-(4-хлорфенил)пиримидин-2-ил]амино}метил)-2-метилфенокси]-уксусная кислота;
{4-[((2-метоксиэтил){4-[4-(трифторметил)фенил]пиримидин-2-ил}амино)метил]-2-метилфенокси}уксусная кислота;
(4-{[[4-(4-хлорфенил)пиримидин-2-ил](2-метоксиэтил)амино]метил}-2-метилфенокси)уксусная кислота;
{2-метил-4-[(пропил{4-[4-(трифторметил)фенил]пиримидин-2-ил}амино)метил]-фенокси}уксусная кислота;
{4-[(бутил{6-[4-(трифторметил)фенил]пиразин-2-ил}амино)метил]-2-метилфенокси}уксусная кислота;
[4-({бутил[6-(4-метилфенил)пиразин-2-ил]амино}метил)-2-метилфенокси]-уксусная кислота;
{4-[{(2-метоксиэтил){6-[4-(трифторметил)фенил]пиразин-2-ил}амино)метил]-2-метилфенокси}уксусная кислота;
(4-{[бутил(2,4′-диметил-1,1′-бифенил-3-ил)амино]метил}-2-метилфенокси)-уксусная кислота;
(4-{[бутил(4′-фтор-2-метил-1,1′-бифенил-3-ил)амино]метил}-2-метилфенокси)-уксусная кислота;
(4-{[бутил(4′-циано-2-метил-1,1′-бифенил-3-ил)амино]метил}-2-метилфенокси)-уксусная кислота;
(4-{[бутил(4′-метокси-2-метил-1,1′-бифенил-3-ил)амино]метил}-2-метилфенокси)уксусная кислота;
(4-{[бутил(4′-хлор-2-метил-1,1′-бифенил-3-ил)амино]метил}-2-метилфенокси)-уксусная кислота;
(4-{[(4′-хлор-2-метил-1,1′-бифенил-3-ил)(2-метоксиэтил)амино]метил}-2-метилфенокси)уксусная кислота;
(4-{[(2,4′-диметил-1,1′-бифенил-3-ил)(2-метоксиэтил)амино]метил}-2-метилфенокси)уксусная кислота;
(4-{[(2-метоксиэтил)(4′-метокси-2-метил-1,1′-бифенил-3-ил)амино]метил}-2-метилфенокси)уксусная кислота;
(2-метил-4-{[[2-метил-4′-(трифторметил)-1,1′-бифенил-3-ил](пропил)амино]-метил}фенокси)уксусная кислота;
(4-{[(4′-хлор-2-метил-1,1′-бифенил-3-ил)(пропил)амино]метил}-2-метилфенокси)-уксусная кислота;
(4-{[(2,4′-диметил-1,1′-бифенил-3-ил)(пропил)амино]метил}-2-метилфенокси)-уксусная кислота;
(4-{[(4′-фтор-2-метил-1,1′-бифенил-3-ил)(пропил)амино]метил}-2-метилфенокси)уксусная кислота;
(4-{[(4′-циано-2-метил-1,1′-бифенил-3-ил)(пропил)амино]метил}-2-метилфенокси)уксусная кислота;
(4-{[(4′-метокси-2-метил-1,1′-бифенил-3-ил)(пропил)амино]метил}-2-метилфенокси)уксусная кислота;
{4-[(бутил{5-метило-6-[4-(трифторметил)фенил]пиримидин-4-ил}амино)метил]-2-метилфенокси}уксусная кислота;
[4-({бутил[6-(4-метоксифенил)-5-метилпиримидин-4-ил]амино}метил)-2-метилфенокси]уксусная кислота;
[4-({бутил[5-метил-6-(4-метилфенил)пиримидин-4-ил]амино}метил)-2-метилфенокси]уксусная кислота;
[4-({бутил[6-(4-хлорфенил)-5-метилпиримидин-4-ил]амино}метил)-2-метилфенокси]уксусная кислота;
[4-({бутил[6-(4-хлорфенил)-2-пиразин-2-ил]амино}метил)-2-метилфенокси]-уксусная кислота;
[4-({[6-(4-хлорфенил)пиразин-2-ил][2-(метилокси)этил]амино}метил)-2-метилфенокси]уксусная кислота;
{2-метил-4-[(пропил{6-[4-(трифторметил)фенил]пиразин-2-ил}амино)метил]-фенокси}уксусная кислота;
(2-метил-4-{[{5-метил-6-[4-(трифторметил)фенил]пиримидин-4-ил}(пропил)-амино]метил}фенокси)уксусная кислота;
(4-{[[6-(4-хлорфенил)-5-метилпиримидин-4-ил](пропил)амино]метил}-2-метилфенокси)уксусная кислота;
(2-метил-4-{[[5-метил-6-(4-метилфенил)пиримидин-4-ил](пропил)амино]метил}-фенокси)уксусная кислота;
(2-метил-4-{[{5-метил-6-[4-(метилокси)фенил]пиримидин-4-ил}(пропил)амино]-метил}фенокси)уксусная кислота;
{4-[(бутил{6-[4-(трифторметил)фенил]пиразин-2-ил}амино)метил]-2-этилфенокси}уксусная кислота;
{2-этил-4-[(2-метилоксиэтил){6-[4-(трифторметил)фенил]пиразин-2-ил}амино)-метил]фенокси}уксусная кислота;
[4-({бутил[5-метил-6-(4-метилфенил)пиримидин-4-ил]амино}метил)-2-этилфенокси]уксусная кислота;
[4-({бутил[2-метил-4′-(трифторметил)-1,1′-бифенил-3-ил]амино}сульфонил)-2-метилфенокси]уксусная кислота;
[2-метил-4-({(пропилсульфонил)[4′-(трифторметил)-1,1′-бифенил-3-ил]амино}-метил)фенокси]уксусная кислота;
[4-({бутил[6-(4-хлорфенил)-5-метилпиримидин-4-ил]амино}метил)-2-этилфенокси]уксусная кислота;
{4-[(бутил{5-метил-6-[4-(трифторметил)фенил]пиримидин-4-ил}амино)метил]-2-этилфенокси}уксусная кислота;
{2-этил-4-[([2-(метилокси)этил]{4-[4-(трифторметил)фенил]пиримидин-2-ил}амино)метил]фенокси}уксусная кислота;
{2-метил-4-[(2-пропен-1-ил{6-[4-(трифторметил)фенил]пиридин-2-ил}амино)-метил]фенокси}уксусная кислота.
Хотя предпочтительные группы для каждой переменной в общем виде перечислены выше отдельно для каждой переменной, предпочтительные соединения по данному изобретению включают такие соединения, в которых несколько или каждая переменная в Формуле (I) выбрана из групп предпочтительных, более предпочтительных или наиболее предпочтительных для каждой переменной. Следовательно, подразумевается, что данное изобретение включает все комбинации предпочтительных и наиболее предпочтительных групп.
Специалистам в данной области техники очевидно, что в соединениях формулы (I) имеются стереоцентры. Соответственно, настоящее изобретение включает все возможные стереоизомеры и геометрические изомеры формулы (I) и включает не только рацемические соединения, но также подразумевается, что данное изобретение охватывает каждый из этих изомеров в их рацемической, обогащенной или очищенной формах. Если желательно иметь соединение формулы (I) в виде единственного энантиомера, его можно получить либо путем разделения конечного продукта, либо путем стереоспецифического синтеза, используя оптически активный катализатор или каталитическую систему с оптически активными лигандами, или изомерно чистое исходное вещество, или любое подходящее промежуточное соединение. Разделение конечного продукта, промежуточного соединения или исходного вещества может быть осуществлено любым подходящим способом, известным в данной области техники. Смотри, например, "Stereochemistry of Carbon Compounds" (E.L.Eliel; Mcgraw Hill, 1962) и "Tables of Resolving Agents" (S.H.Wilen). Кроме того, в ситуациях, когда возможны таутомеры соединений формулы (I), подразумевается, что настоящее изобретение охватывает все таутомерные формы соединений. У некоторых из этих хиральных соединений активности S- или R-изомеров в отношении различных PPAR-рецепторов различаются. Какой из этих изомеров является предпочтительным, зависит от конкретной целевой применимости соединения. Другими словами, даже для одного и того же соединения возможно, что для одних применений будет предпочтителен S-изомер, в то время как для других будет предпочтителен R-изомер.
hPPAR-агонисты формулы (I) могут быть агонистами только одного типа ("селективные агонисты"), агонистами двух подтипов PPAR ("двойные агонисты") или агонистами всех трех подтипов ("пан-агонисты"). При использовании здесь, под "агонистом" или "активирующим соединением" или "активатором" или подобным понимают такие соединения, которые имеют pKi по меньшей мере 6,0, предпочтительно по меньшей мере 7,0 в отношении релевантного PPAR, например hPPARδ, в анализе связывания, описанном ниже, и с помощью которых добиваются по меньшей мере 50%-ной активации релевантного PPAR относительно соответствующего указанного положительного контроля в описанном ниже трансфекционном анализе при концентрациях 10-5 М или ниже. Более предпочтительно, когда с помощью агонистов до данному изобретению добиваются 50%-ной активации по меньшей мере одного PPAR человека в релевантном трансфекционном анализе при концентрациях 10-6 М или ниже. Предпочтительно соединения формулы (I) являются агонистами hPPAR. Более предпочтительно данные соединения являются агонистами hPPARδ. Более предпочтительно они являются селективными агонистами hPPARδ.
Кроме того, специалистам в данной области техники очевидно, что соединения по настоящему изобретению также можно использовать в форме их фармацевтически приемлемой соли или сольвата. Физиологически приемлемые соли соединений формулы (I) включают традиционные соли, образованные фармацевтически приемлемыми неорганическими или органическими кислотами или основаниями, а также соли присоединения кислот и четвертичного аммония. Более конкретные примеры подходящих солей кислот включают соли соляной, бромистоводородной, серной, фосфорной, азотной, перхлорной, фумаровой, уксусной, пропионовой, янтарной, гликолевой, муравьиной, молочной, малеиновой, винной, лимонной, пальмовой, малоновой, оксималеиновой, фенилуксусной, глутаминовой, бензойной, салициловой, толуолсульфоновой, метансульфоновой, нафталин-2-сульфоновой, бензолсульфоновой, оксинафтойной, иодистоводородной, яблочной, стеариновой, дубильной кислоты и подобных. Другие кислоты, как, например, щавелевая кислота, несмотря на то, что сами по себе не являются фармацевтически приемлемыми, могут быть использованы в получении солей, полезных в качестве промежуточных соединений при получении соединений по изобретению и их фармацевтически приемлемых солей. Более конкретные примеры подходящих солей оснований включают соли натрия, лития, калия, магния, алюминия, кальция, цинка, N,N′-дибензилэтилендиамина, хлорпрокаина, холина, диэтаноламина, этилендиамина, N-метилглюкамина и прокаина. Специалистам в области органической химии очевидно, что многие органические соединения могут образовывать комплексы с растворителями, в которых они взаимодействуют или из которых они осаждаются или кристаллизуются. Эти комплексы известны как "сольваты". Например, комплекс с водой известен как "гидрат". Сольваты соединения формулы (I) входят в объем данного изобретения. Ниже приведенные ссылки на соединение по изобретению включают как соединения формулы (I), так и их фармацевтически приемлемые соли и сольваты.
Соединения по изобретению и их фармацевтически приемлемые производные удобно вводить в форме фармацевтических композиций. Такие композиции удобно могут быть представлены для использования традиционным образом в смеси с одним или более физиологически приемлемыми носителемями или эксципиентами.
Хотя возможно, что соединения по настоящему изобретению могут быть терапевтическим образом введены в виде неочищенного химического средства, предпочтительно представить активный ингредиент в виде фармацевтического препарата. Носитель(и) должен быть "приемлемым(и)" в смысле совместимости с другими ингредиентами препарата и не оказывать вредного воздействия на их реципиента.
Таким образом, в настоящем изобретении также предложен фармацевтический препарат, содержащий соединение формулы (I) или его фармацевтически приемлемую соль или сольват вместе с одним или более фармацевтически приемлемыми носителями и, возможно, другими терапевтическими и/или профилактическими ингредиентами.
Данные препараты включают препараты, подходящие для перорального, парентерального (в том числе подкожного, например путем инъекции или посредством депо-таблетки, интрадермального, интратекального, внутримышечного, например путем депо, или внутривенного), ректального или местного (в том числе дермального, трансбуккального и сублингвального) введения, хотя наиболее подходящий путь может зависеть, например, от состояния и нарушения у реципиента. Данные препараты удобным образом могут быть представлены в стандартной лекарственной форме и могут быть изготовлены любым способом, хорошо известным специалистам в области фармацевтики. Все способы включают стадию объединения соединений ("активного ингредиента") с носителем, который образуется одним или более вспомогательными ингредиентами. Обычно препараты изготовляют путем равномерного и близкого объединения активного ингредиента с жидкими носителями или тонко измельченными твердыми носителями, или с обоими, и затем, если необходимо, придания продукту формы желаемого препарата.
Препараты, подходящие для перорального введения, могут быть представлены в виде отдельных единиц, таких как капсулы, облатки или таблетки (например жевательные таблетки, в частности для педиатрического введения), каждая из которых содержит предварительно определенное количество активного ингредиента; в виде порошка или гранул; в виде раствора или суспензии в водной жидкости или неводной жидкости; или в виде жидкой эмульсии масло-в-воде, или жидкой эмульсии вода-в-масле. Активный ингредиент также может быть представлен в виде болюса, электуария или пасты.
Таблетка может быть изготовлена путем прессования или формования, возможно с одним или более вспомогательными ингредиентами. Прессованные таблетки могут быть изготовлены путем прессования в подходящей машине активного ингредиента в свободно текучей форме, такой как порошок или гранулы, возможно смешанного с другими традиционными эксципиентами, такими как связывающие агенты (например сироп, аравийская камедь, желатин, сорбит, трагакант, крахмальный клейстер или поливинилпирролидон), наполнители (например, лактоза, сахар, микрокристаллическая целлюлоза, кукурузный крахмал, фосфат кальция или сорбит), смазывающие вещества (например, стеарат магния, стеариновая кислота, тальк, полиэтиленгликоль или диоксид кремния), разрыхлители (например картофельный крахмал или натрия крахмала гликолят) или увлажняющие агенты, такие как лаурилсульфат натрия. Формованные таблетки могут быть изготовлены путем формования в подходящей машине смеси порошкообразного соединения, увлажненного инертным жидким разбавителем. Таблетки возможно могут иметь покрытие или насечки и могут быть изготовлены в виде препарата, обеспечивающего медленное или регулируемое высвобождение активного ингредиента. Таблетки могут быть покрыты оболочкой способами, хорошо известными в данной области техники.
Альтернативно, соединения по настоящему изобретению могут входить в состав пероральных жидких препаратов, таких как, например, водные или масляные суспензии, растворы, эмульсии, сиропы или эликсиры. Кроме того, препараты, содержащие эти соединения, могут быть представлены в виде сухого продукта для разбавления водой или другим подходящим растворителем перед использованием. Такие жидкие препараты могут содержать традиционные добавки, такие как суспендирующие агенты, например сироп сорбита, метилцеллюлозу, глюкозный/сахарный сироп, желатин, гидроксиэтилцеллюлозу, карбоксиметилцеллюлозу, гель стеарата алюминия или гидрированные пищевые жиры; эмульгирующие агенты, такие как лецитин, сорбитанмоноолеат или аравийская камедь; неводные наполнители (которые могут включать пищевые масла), такие как миндальное масло, ректифицированное кокосовое масло, сложные эфиры масел, пропиленгликоль или этиловый спирт; и консерванты, такие как метил- или пропил-пара-гидроксибензоаты или сорбиновая кислота. Такие препараты также могут быть изготовлены в виде суппозиториев, например, содержащих традиционные основы для суппозиториев, такие как какао-масло или другие глицериды.
Препараты для парентерального введения включают водные и неводные стерильные инъекционные растворы, которые могут содержать антиоксиданты, буферы, бактериостатические средства и растворенные вещества, делающие препарат изотоничным крови предполагаемого реципиента; и водные и неводные стерильные суспензии, которые могут включать суспендирующие агенты и загущающие агенты.
Препараты могут быть представлены в однодозовых и многодозовых контейнерах, например герметично закрытых ампулах и флаконах, и могут храниться в высушенном вымораживанием (лиофилизованном) состоянии, нуждаясь только в добавлении стерильного жидкого носителя, например воды для инъекций, непосредственно перед использованием. Инъекционные растворы и суспензии для применения в нужный момент могут быть приготовлены из ранее описанных стерильных порошков, гранул и таблеток.
Препараты для ректального введения могут быть представлены в виде суппозитория с обычными носителями, такими как какао-масло, твердый жир или полиэтиленгликоль.
Препараты для местного введения в полость рта, например трансбуккально или сублингвально, включают таблетки, содержащие активный ингредиент в основе с добавлением корригентов, такой как сахароза и аравийская камедь или трагакант, и пастилки, содержащие активный ингредиент в такой основе, как желатин и глицерин или сахароза и аравийская камедь.
Кроме того, соединения могут быть изготовлены в виде депо-препаратов. Такие препараты с продолжительным действием могут быть введены путем имплантации (например, подкожно или внутримышечно) или путем внутримышечной инъекции. Так, например, соединения могут быть изготовлены в виде препаратов с подходящими полимерными или гидрофобными веществами (например, в виде эмульсии в подходящем масле) или ионообменными смолами, или в виде умеренно растворимых производных, например в виде умеренно растворимой соли.
В дополнение к ингредиентам, отдельно упомянутым выше, данные препараты могут включать другие традиционно используемые в данной области техники агенты, имеющие отношение к рассматриваемому типу препарата, например препарат, подходящий для перорального введения, может включать корригирующие агенты.
Специалистам в данной области техники очевидно, что ссылка в данном описании на лечение распространяется на профилактику, а также на лечение установленных заболеваний или симптомов. Более того, очевидно, что количество соединения по изобретению, необходимое для применения в лечении, будет меняться в зависимости от природы состояния, которое лечат, и возраста и состояния пациента, и в конечном счете будет находиться на усмотрении лечащего врача или ветеринара. В общем случае, однако, дозы, используемые для лечения взрослого человека, в типичном случае будут находиться в интервале 0,02-5000 мг в сутки, предпочтительно 1-1500 мг в сутки. Требуемая доза удобным образом может быть представлена в виде разовой дозы или разделенных доз, вводимых через подходящие интервалы, например в виде двух, трех, четырех или более субдоз в сутки. Препараты согласно изобретению могут содержать 0,1-99% активного ингредиента; для таблеток и капсул подходит 30-95% и для жидких препаратов подходит 3-50%.
Соединение формулы (I) для применения в настоящем изобретении могут быть использованы в комбинации с другими терапевтическими агентами, например статинами и/или другими снижающими содержание липидов лекарственными средствами, например ингибиторами МТР (микросомального переносящего белка) и позитивными регуляторами LDLR. Соединения по изобретению также могут быть использованы в комбинации с антидиабетическими агентами, например метформином, сульфонилмочевинами и/или агонистами PPAR-гамма, PPAR-альфа или PPAR-альфа/гамма (например, с тиазолидиндионами, такими как, например, пиоглитазон и розиглитазон). Эти соединения также можно использовать в комбинации с антигипертензивными агентами, такими как антагонисты ангиотензина, например телмисартаном, с антагонистами кальциевых каналов, например лацидипином, и с ингибиторами АСЕ, например эналаприлом. Таким образом, в следующем аспекте данного изобретения предложено применение комбинации, содержащей соединение формулы (I) с еще одним терапевтическим агентом, в лечении hPPAR-опосредованного заболевания.
Когда соединения формулы (I) используют в комбинации с другими терапевтическими агентами, эти соединения могут быть введены либо последовательно, либо одновременно любым удобным путем.
Указанные выше комбинации удобным образом могут быть представлены для применения в форме фармацевтического препарата, и таким образом фармацевтические препараты, содержащие комбинацию, как она определена выше, оптимально вместе с фармацевтически приемлемым носителем или эксципиентом, составляют еще один аспект данного изобретения. Индивидуальные компоненты таких комбинаций могут быть введены либо последовательно, либо одновременно в виде отдельных или объединенных фармацевтических препаратов.
Очевидно, что при объединении в одном и том же препарате два соединения должны быть стабильны и совместимы друг с другом и другими компонентами этого препарата и могут быть приготовлены в виде препарата для введения. В случае раздельных препаратов они могут быть представлены в виде любого подходящего препарата, подходящего так, как подходят для таких соединений известные в данной области техники препараты.
Если соединение формулы (I) используют в комбинации со вторым терапевтическим агентом, активным в отношении того же hPPAR-опосредованного заболевания, доза каждого соединения может отличаться от дозы, когда соединение используют само по себе. Соответствующие дозы очевидны специалистам в данной области техники.
Соединения по данному изобретению могут быть получены удобным образом согласно общим способам, представленным ниже на схемах.
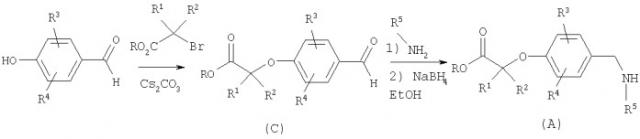
Схема 1
Промежуточные соединения (А) могут быть получены алкилированием подходящего 4-гидроксибензальдегида, с получаем бензальдегидов (промежуточное соединение С), с последующим восстановительным аминированием альдегидной группировки.
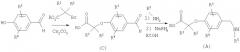
Схема 2
Промежуточные соединения (В) могут быть получены путем восстановления подходящего 4-гидроксибензальдегида до спирта. В результате алкилирования фенольной группировки подходящим бромацетатом с последующим галогенированием бензилового спирта получают промежуточные соединения (В).
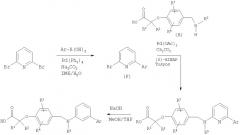
Схема 3
Имеющийся в продаже 2,6-дибромпиридин можно подвергнуть реакции сочетания с бороновыми кислотами в условиях сочетания Сузуки. Полученные монобромиды затем можно обработать амином (промежуточное соединение А) в реакции Бухвальда (Buchwald) с получением продуктов сочетания. Эфирную группу затем можно гидролизовать до соответствующих карбоновых кислот в стандартных условиях.
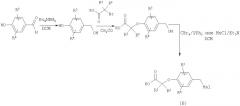
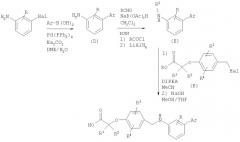
Схема 4
Подходящие галогенированные анилины можно подвергнуть реакции сочетания с бороновыми кислотами в условиях сочетания Сузуки с получением продуктов сочетания (промежуточное соединение D). В результате восстановительного аминирования или ацилирования и восстановления полученных соединений получают вторичные анилины (промежуточное соединение Е), которые алкилируют галогенидами (промежуточное соединение В). В результате гидролиза сложных эфиров карбоновых кислот в стандартных условиях получают карбоновые кислоты.
Схема 5
В результате восстановительного аминирования анилина (промежуточное соединение D) альдегидом (промежуточное соединение С) получают вторичный анилин (промежуточное соединение F), который может быть превращен в амид путем сочетания с подходящей карбоновой кислотой, а в сульфонамид путем взаимодействия с соответствующим алкилсульфонилхлоридом. Полученные сложные эфиры гидролизуют в стандартных условиях с получением карбоновых кислот.
Схема 6
В результате взаимодействия вторичного анилина (промежуточное соединение Е) с сульфонилхлоридом (промежуточное соединение G) получают связанные через сульфонамид соединения. В результате гидролиза сложных эфиров в стандартных условиях получают карбоновые кислоты.
Схема 7