Фторированные производные 4-азастероида в качестве модуляторов рецептора андрогена
Иллюстрации
Показать всеОписывается соединение формулы I или его фармацевтически приемлемая соль или его энантиомер, где n равно 0 или 1; a-b означает CF=CH или CHFCH2; R1 представляет C1-3алкил, где алкил является незамещенным; R2 представляет собой водород; R3 выбран из С1-4алкила, (СН2)n-циклогетероалкила и (СН2)n-арила; или R2 и R3 вместе образуют 6-членное насыщенное кольцо, конденсированное с 5-членной ароматической кольцевой системой, имеющей 2 гетероатома, выбранных из N, фармацевтические композиции. Соединения формулы I представляют собой модуляторы рецептора андрогена (AR), при этом обладающие тканеселективным действием. Указанные соединения полезны в качестве агонистов рецептора андрогена в костной и/или мышечной ткани при антагонизировании AR в простате пациента мужского пола или в матке пациента женского пола. 18 н. и 18 з.п. ф-лы, 2 табл.
Реферат
Область техники
Настоящее изобретение относится к фторированным производным 4-азастероида, их синтезу и их применению в качестве модуляторов рецептора андрогена. В частности, соединения настоящего изобретения представляют собой тканеселективные модуляторы рецептора андрогена и, в связи с этим, являются полезными для лечения состояний, вызванных недостаточностью андрогенов или интенсивность симптомов которых может быть уменьшена введением андрогена, таких как остеопороз, периодонтальная болезнь, перелом (трещина)кости, хрупкостьи саркопения.
Предшествующий уровень техники
Рецептор андрогена (AR) относится к надсемейству ядерных рецепторов стероидных/тиреоидных гормонов, другие представители которого включают рецептор эстрогена (ER), рецептор прогестерона (PR), рецептор глюкокортикоида (GR) и рецептор минералокортикоида (MR). AR экспрессируется во многих тканях тела и представляет собой рецептор, посредством которого экспрессируются физиологические, а также патофизиологические действия эндогенных лигандов андрогена, таких как тестостерон (Т) и дигидротестостерон (DHT). Структурно AR состоит из трех основных функциональных доменов: домена, связывающего лиганд (LBD); ДНК-связывающего домена и аминоконцевого домена. Соединение, которое связывается с AR и имитирует действия эндогенного лиганда AR, называют агонистом AR, в то время как соединение, которое ингибирует действия эндогенного лиганда AR, называют антагонистом AR.
Связывание лиганда андрогена с AR дает комплекс лиганд/рецептор, который после транслокации внутри ядра клетки связывается со специфическими регуляторными последовательностями ДНК (называемыми элементами ответа андрогена или ARE) в пределах областей промотора или энхансера гена или генов мишени, присутствующих в ядре клетки. Затем наращиваются другие белки, называемые кофакторами, которые связываются с аминоконцевым доменом или лигандсвязывающим доменом (LBD) рецептора, что приводит к транскрипции и последующей трансляции гена с получением белка(ов), кодируемого указанным геном или генами.
Андрогенотерапию использовали в клинике для лечения целого ряда нарушений у мужчин, таких как репродуктивные нарушения и первичный или вторичный мужской гипогонадизм. Кроме того, различные природные или синтетические агонисты AR были клинически исследованы при лечении мышечно-скелетных нарушений, таких как болезнь костной ткани, гемопоэтические расстройства, нервно-мышечная болезнь, ревматическая болезнь, кахексия, а также при заместительной гормональной терапии (HRT), как, например, в случае недостаточности андрогенов у женщин. Кроме того, антагонисты AR, такие как флутамид и бикалутамид, были использованы для лечения рака предстательной железы. Поэтому было бы полезно иметь доступные соединения, которые могут активировать («агонизировать») функцию AR тканеселективным способом, что обеспечило бы проявление желательных благотворных остео- и миоанаболических действий андрогенов, но без проявления негативных андрогенных свойств, таких как вирилизация и индуцирование атерогенного (способствующего развитию атеросклероза) профиля липида, которые могут привести к развитию сердечно-сосудистого заболевания.
Роль андрогенов в остеогенезе подтверждается документами. Например, анаболические стероиды, такие как нандролон деканоат или станозолол, как было показано, увеличивают костную массу у женщин в постменопаузальном периоде. Благотворные воздействия андрогенов на костную ткань при постменопаузальном остеопорозе были зарегистрированы в последних исследованиях, использующих комбинированное введение тестостерона и эстрогена [Hofbauer, et al., "Androgen effects on bone metabolism: recent progress and controversies," Eur. J. Endocrinol.140: 271-286 (1999)]. Комбинированное лечение значительно увеличивало скорость повышения плотности минеральных компонентов кости (BMD) и ее величину в поясничной области и области бедра, по сравнению с лечением только одним эстрогеном. Кроме того, комбинации эстроген-прогестин, которые содержали андрогенный прогестин (такой как норетиндрон), а не медроксипрогестерон ацетат, давали лучшую положительную динамику для BMD тазобедренного сустава. Эти результаты недавно были подтверждены при сравнительном исследовании двойным слепым методом на протяжении более 2 лет, в котором, как было показано, пероральные комбинации сопряженных эстрогенов (СЕЕ) и метилтестостерона оказываются эффективными в стимуляции наращивания костной массы в позвоночнике и тазобедренном суставе, в то время как лечение только сопряженными эстрогенами предотвращало разрежение кости (остеопороз) ["A two-year, double-blind comparison of estrogen-androgen and conjugated estrogens in surgically menopausal women: Effects on bone mineral density, symptoms and lipid profiles," J. Reprod. Med., 44: 1012-1020 (1999)]. Несмотря на благоприятные воздействия андрогенов на женщин в постменопаузальном периоде, использование андрогенов было ограничено из-за нежелательного вирилизирующего и метаболического действия андрогенов. Данные Watts и коллег демонстрируют, что «приливы» уменьшаются у женщин, подвергнутых лечению CEE и метилтестостероном; однако 30% из вышеуказанных женщин страдали от существенного увеличения (появления) угрей и волос на лице, осложнение всех современных методов фармакотерапии с использованием андрогена [Watts, et al., "Comparison of oral estrogens and estrogens plus androgen on bone mineral density, menopausal symptoms, and lipid-lipoprotein profiles in surgical menopause," Obstet. Gynecol., 85: 529-537 (1995)]. Кроме того, как видно из других исследований, добавление метилтестостерона к СЕЕ заметно снижало уровни HDL. Поэтому не селективные к ткани агонисты AR могут увеличить риск возникновения сердечно-сосудистого заболевания. Таким образом, возможность вирилизации и негативные воздействия на липидный профиль современных методов андрогенотерапии предоставляют существенное логическое обоснование для разработки тканеселективных агонистов рецептора андрогена для кости. Делается ссылка на J. A. Kanis, "Other agents for generalized osteoporosis," in Osteoporosis, Blackwell Science, Ch. 8, pp 196-227 (1994), где обсуждаются неселективные анаболические стероиды для лечения остеопороза.
Также было установлено, что андрогены играют важную роль в костном метаболизме у мужчин, которая соответствует роли эстрогенов у женщин [Anderson, et al., "Androgen supplementation in eugonadal men with osteoporosis - effects of six months of treatment on bone mineral density and cardiovascular risk factors," Bone, 18: 171-177 (1996)]. Даже у эугонадных мужчин с установленным остеопорозом терапевтическая реакция на лечение тестостероном предоставляла дополнительное доказательство того, что андрогены оказывают важные остеоанаболические воздействия. Средняя BMD в поясничной области возрастает от 0,799 до 0,839 г/см2, за период от 5 до 6 месяцев в ответ на лечение 250 мг сложного эфира тестостерона, вводимого внутримышечно каждые две недели. Обычный сценарий для проявления андрогенной недостаточности имеет место у мужчин с раком простаты стадии D (метастатический), которые подвергаются терапии, направленной на подавление выработки андрогена (ADT). Эндокринная орхиэктомия (удаление яичек) достигается длительным воздействием агонистов GnRH, тогда как блокада рецептора андрогена осуществляется действием флутамида, нилутамида, бикалутамида или RU 58841 (антагонисты AR). В ответ на выключение эндокринной функции вышеуказанные мужчины страдают от «приливов», существенного остеопороза (разрежение кости), слабости и утомления. В последнем экспериментальном исследовании мужчин с раком простаты стадии D нарушение остеогенеза (50% против 38%) и остеопороз (38% против 25%) встречались более часто у мужчин, которые подвергались ADT на протяжении более чем одного года, чем у пациентов, которые не подвергались лечению ADT [Wei, et al., "Androgen deprivation therapy for prostate cancer results in significant loss of bone density," Urology, 54: 607-611 (1999)]. BMD поясничной области позвоночника оказалась значительно ниже у мужчин, которые подверглись ADT. Таким образом, помимо использования тканеселективных агонистов AR для лечения остеопороза, тканеселективные антагонисты AR в простате, которые не обладают антагостическим действием на костную и мышечную ткань, могут быть полезными средствами для лечения рака простаты, либо сами по себе, либо в качестве вспомогательного лечебного средства при традиционной ADT, как, например, комбинация агонист/антагонист GnRH[См. также A. Stoch, et al., J. Clin. Endocrin. Metab., 86: 2787-2791 (2001)]. Тканеселективные антагонисты AR могут также быть полезными для лечения синдрома поликистоза яичников у женщин в постменопаузальном периоде [см. С.A. Eagleson, et al., "Polycystic ovarian syndrome: evidence that flutamide restores sensitivity of the gonadotropin-releasing hormone pulse generator to inhibition by estradiol and progesterone," J. Clin. Endocrinol. Metab,, 85: 4047-4052 (2000) и E. Diamanti-Kandarakis, "The Effect of a Pure Antiandrogen Receptor Blocker, Flutamide, on the Lipid Profile in the Polycystic Ovary Syndrome," Int. J. Endocrinol. Metab., 83: 2699-2705 (1998)].
Существует потребность в более эффективных средствах для лечения нарушения остеогенеза и остеопороза как для мужчин, так и для женщин. Остеопороз характеризуется разрежением костной ткани вследствие нарушения равновесия между резорбцией (разрушением) и образованием костной ткани, которое начинается в четвертом десятилетии и продолжается на всем протяжении жизни со скоростью около 1-4% в год [Eastell, "Treatment of postmenopausal osteoporosis," New Engl. J. Med., 338: 736 (1998)]. В Соединенных Штатах в настоящее время имеется приблизительно 20 миллионов человек с выявленными трещинами и переломами позвонков вследствие остеопороза. Кроме того, имеет место около 250000 трещин (переломов) тазобедренного сустава (бедра) в год вследствие остеопороза, ассоциируемых с 12-20% коэффициентом смертности в пределах первых двух лет, тогда как 30% из вышеуказанных пациентов требуют помощи медсестер на дому после перелома, и многие из указанных пациентов никогда не станут полностью амбулаторными больными снова. У женщин в постменопаузальном периоде дефицит эстрогена ведет к повышенной резорбции кости, приводящей к потере костной ткани в позвонках около 5% в год, сразу после менопаузы. Поэтому первым направлением лечения и профилактики указанного выше состояния является ингибирование резорбции кости бисфосфонатами, эстрогенами, селективными модуляторами рецептора эстрогена (SERM) и кальцитонином. Однако ингибиторов резорбции кости недостаточно для восстановления костной массы у пациентов, которые уже потеряли значительную часть костной массы. Увеличение BMD позвоночника, достигнутое лечением бисфосфонатами, может достигнуть 11% после лечения алендронатом в течение 7 лет. Кроме того, поскольку скорость обновления костной ткани различна в зависимости от места поражения костной ткани, более высокая в трабекулярной кости позвонков, чем в корковом слое длинных костей, то ингибиторы резорбции кости менее эффективны в повышении BMD тазобедренного сустава и предотвращении перелома бедра. Поэтому остеоанаболические средства, которые увеличивают кортикальный остеогенез и костную массу длинных костей, стимулируя периостальный остеогенез, вероятно, можно направить на решение неудовлетворенной потребности в лечении остеопороза, особенно для пациентов с высоким риском перелома бедра. Остеоанаболические средства также дополняют ингибиторы резорбции кости, которые атакуют трабекулярную оболочку, приводя к образованию биомеханически благоприятной костной структуры(Schmidt, et al., "Anabolic steroid: Steroid effects on bone in women," In: J. P. Bilezikian, et al., Ed., Principles of Bone Biology, San Diego: Academic Press, 1996). Тканеселективные агонисты AR с уменьшенными вредными воздействиями на сердечно-сосудистую систему и ограниченным вирилизирующим потенциалом могут быть использованы в качестве монотерапии для профилактики и/или лечения остеопороза у женщин. Кроме того, соединение с остеоанаболическими свойствами по отношению к костной и мышечной ткани, но с пониженной активностью в простате и придаточных тканях половых органов, может быть использовано для профилактики и/или лечения остеопороза у мужчин и нарушения остеогенеза (остеопении) у мужчин, особенно пожилых мужчин.
Кроме того, селективные модуляторы рецептора андрогена могут быть использованы для лечения некоторых гемопоэтических нарушений. Известно, что андрогены стимулируют почечную гипертрофию и продуцирование эритропоэтина (EPO). До введения рекомбинантного человеческого EPO андрогены использовали для лечения анемии, вызванной хронической почечной недостаточностью. Кроме того, было установлено, что андрогены при фармакологических дозах повышают сывороточные уровни EPO у пациентов с нетяжелой апластической анемией и миелодиспластическими синдромами, но не у пациентов без анемии. Лечебное воздействие на анемию нуждается в избирательном действии, таком которое может быть обеспечено селективными модуляторами рецептора андрогена.
Кроме того, селективные модуляторы рецептора андрогена могут также иметь клиническое значение как вспомогательное средство при лечении ожирения. Указанный подход к снижению жира в теле подтверждается опубликованными наблюдениями, согласно которым введение андрогена уменьшало подкожный и висцеральный абдоминальный жир у тучных людей [J.C. Lovejoy, et al., "Oral anabolic steroid treatment, but not parenteral androgen treatment, decreases abdominal fat in obese, older men," Int. J. Obesity, 19: 614-624 (1995)]. Поэтому SARM, лишенные андрогенных воздействий на простату, могут быть полезными для лечения тучных мужчин. В отдельном исследовании введение андрогена привело к потере подкожного абдоминального жира у тучных женщин в постменопаузальном периоде[J.C. Lovejoy, et al., "Exogenous Androgens Influence Body Composition and Regional Body Fat Distribution in Obese Postmenopausal Women - A Clinical Research Center Study," J. Clin. Endocrinol. Metab., 81: 2198-2203 (1996)]. В последнем исследовании было установлено, что нандролон деканоат, слабое андрогенное и анаболическое средство, повышает массу тела у тощих людей и интенсивность обмена веществ в покое у тучных женщин в постменопаузальном периоде, соблюдающих диету, способствующую снижению массы тела.
Нестероидные соединения, обладающие свойством модуляциирецептора андрогена, были раскрыты в патентах США №№ 5688808; 5696130; 6017924; 6093821; WO 01/16139 (опубликованной 8 марта 2001); и WO 01/16108 (опубликованной 8 марта 2001), все переуступлены Ligand Pharmaceuticals, и в WO 01/27086, переуступленной Kaken Pharm. Co. Дополнительная характеристика известного уровня техники, имеющего отношение к развитию селективных модуляторов рецептора андрогена, имеется в L. Zhi and E. Martinborough in Ann. Rep. Med. Chem. 36: 169-180 (2001). Нестероидные SARM были раскрыты в J.P. Edwards, "New Nonsteroidal Androgen Receptor Modulators Based on 4-(Trifluoromethyl)-2(1H)-Pyrrolidino[3,2-g]quinolinone," Bioorg. Med. Chem. Lett., 8: 745-750 (1998) и в L. Zhi et al., "Switching Androgen Receptor Antagonists to Agonists by Modifying C-ring Substituents on Piperidino[3,4-g]quinolinone," Bioorg. Med. Chem. Lett., 9: 1009-1012 (1999).
В клинической области существует потребность в более эффективных средствах, которые могут выявлять положительные реакции заместительной андрогенной терапии, но без нежелательных побочных действий, присущих неселективным к ткани агонистам AR. Требуются именно такие соединения, которые могут обеспечивать такие же положительные реакции, как заместительная андрогенная терапия, но без нежелательных побочных действий. Также требуются андрогенные соединения, которые проявляют селективные действия на различные ткани тела. В данном изобретении идентифицированы соединения, которые функционируют как селективные модуляторы рецептора андрогена (SARM), с использованием ряда in vitro клеточных проб, которые профилируют опосредованную лигандом активацию AR, а именно (i) N-C взаимодействие, (ii) подавление транскрипции и (iii) активацию транскрипции. Соединения-SARM в настоящем изобретении, идентифицированные перечисленными выше методами, демонстрируют тканеселективный агонизм AR in vivo, т.е. агонизм в кости (стимуляция остеогенеза на модели остеопороза у грызунов) и антагонизм в простате (минимальные воздействия на рост простаты у кастрированных грызунов и антагонизм роста простаты, индуцированного агонистами AR).
Соединения настоящего изобретения, идентифицированные как SARM, используют для лечения заболеваний или состояний, вызванных недостаточностью андрогена, интенсивность симптомов которых может быть уменьшена введением андрогена. Такие соединения являются идеальными для лечения остеопороза у женщин и мужчин в качестве монотерапии или в комбинации с ингибиторами резорбции кости, такими как бисфосфонаты, эстрогены, SERM, ингибиторы катепсина К, антагонисты рецептора интегрина αvβ3, кальцитонин и ингибиторы протонного насоса. Они могут быть также использованы со средствами, которые стимулируют остеогенез, такими как паратиреоидный гормон или его аналоги. Соединения-SARM по данному изобретению могут также быть использованы для лечения заболеваний простаты, таких как рак простаты и доброкачественная гиперплазия простаты (BPH). Кроме того, соединения данного изобретения демонстрируют минимальные воздействия на кожу (прыщи и рост волос на лице) и могут быть полезны для лечения гирсутизма. Дополнительно, соединения данного изобретения могут стимулироватьрост мышечной ткани и могут быть полезны для лечения саркопении и хрупкости. Вышеуказанные соединения можно использовать для уменьшения подкожного и висцерального абдоминального жира при лечении ожирения. Кроме того, соединения данного изобретения могут проявлять андрогенный агонизм в центральной нервной системе и могут быть использованы для лечения вазомоторных симптомов («приливы») и для повышения энергии и либидо, особенно у женщин в период менопаузы. Соединения настоящего изобретения могут быть использованы для лечения рака простаты, либо как таковые, либо как вспомогательное лечебное средство при традиционной терапии с использованием агониста/антагониста GnRH, из-за их способности восстанавливать кость, либо как замена при антиандрогенной терапиииз-за их способности антагонизировать андроген в простате и свести к минимуму истощение костной ткани в скелетной системе. Далее, соединения настоящего изобретения могут быть использованы, из-за их способности восстанавливать кость, при лечении рака поджелудочной железы в качестве вспомогательного средства для лечения антиандрогеном, или как монотерапия из-за их антиандрогенных свойств, при этом демонстрируя преимущество перед традиционными антиандрогенами, заключающееся в способности восстанавливать кость. Дополнительно, соединения данного изобретения могут увеличивать количество клеток крови, таких как эритроциты и тромбоциты, и могут быть полезны для лечении гемопоэтических расстройств, таких как апластическая анемия. Наконец, соединения данного изобретения оказывают минимальные воздействия на липидный метаболизм. Таким образом, вследствие своего тканеселективного агонизмак рецептору андрогена, изложенного выше, соединения данного изобретения являются идеальными для заместительной гормональной терапии для мужчин, страдающих от гипогонадизма (недостаточности секреции андрогена).
Поэтому целью настоящего изобретения является разработка фторированных производных 4-азастероида, которые используют в качестве селективных модуляторов рецептора андрогена.
Другой целью настоящего изобретения является разработка фармацевтических композиций, содержащих фторированные производные 4-азастероида по данному изобретению в сочетании с фармацевтически приемлемым носителем.
Другой целью настоящего изобретения является разработка фармацевтических композиций, содержащих фторированные производные 4-азастероида, для использования в качестве селективных модуляторов рецептора андрогена.
Другой целью настоящего изобретения является разработка способов лечения заболеваний или состояний, вызванных недостаточностью андрогена, интенсивность симптомов которых может быть уменьшена введением андрогена.
Другой целью настоящего изобретения является разработка способов лечения заболеваний или состояний, вызванных недостаточностью андрогена, интенсивность симптомов которых может быть уменьшена введением андрогена в комбинации с другими средствами.
Другой целью настоящего изобретения является разработка фторированных производных 4-азастероида и их фармацевтических композиций для использования в качестве лекарственного средства при лечении заболеваний или состояний, вызванных недостаточностью андрогена, интенсивность симптомов которых может быть уменьшена введением андрогена.
Другой целью настоящего изобретения является разработка фторированных производных 4-азастероида и их фармацевтических композиций для получения лекарственного средства для лечения заболеваний или состояний, вызванных недостаточностью андрогена, интенсивность симптомов которых может быть уменьшена введением андрогена.
Эти и другие цели настоящего изобретения становятся очевидными из подробного описания, которое следует ниже.
Краткое описание изобретения
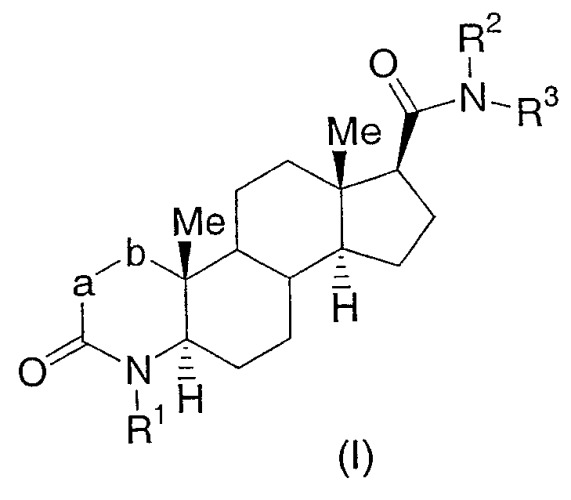
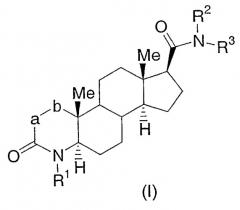
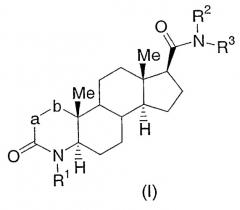
Настоящее изобретение относится к соединениям структурной формулы I:
или их фармацевтически приемлемой соли или их энантиомеру; где
n равно 0, 1 или 2;
a-b означает CF=CH, CHFCH2 или CF2CH2;
R1 представляет собой водород, гидроксиметил или C1-3алкил, где алкил является незамещенным или замещен одним-семью атомами фтора;
R2 представляет собой водород или C1-4алкил;
R3 выбран из
C1-4алкила,
(CH2)n-циклогетероалкила и
(CH2)n-арила, где арил выбран из
(1) фенила,
(2) нафтила,
(3) бензимидазолила,
(4) бензофуранила,
(5) бензотиофенила,
(6) бензоксазолила,
(7) бензотиазолила,
(8) бензодигидрофуранила,
(9) 1,3-бензодиоксолила,
(10) 2,3-дигидро-1,4-бензодиоксинила,
(11) индолила,
(12) хинолила,
(13) изохинолила,
(14) фуранила,
(15) тиенила,
(16) имидазолила,
(17) оксазолила,
(18) тиазолила,
(19) изоксазолила,
(20) изотиазолила,
(21) пиразолила,
(22) пирролила,
(23) пиридила,
(24) пиримидила,
(25) пиразинила,
(26) тиадиазолила,
(27) оксадиазолила,
(28) триазолила,
(29) тетразолила и
(30) инданила;
где алкильная группа или циклогетероалкильная группа является незамещенной или замещена одним-тремя заместителями, независимо выбранными из галогена, гидрокси и С1-4алкокси; арильная группа, определенная в пунктах (1)-(30), является незамещенной или замещена одной-тремя группами, независимо выбранными из галогена, фенила, С1-8алкила, С3-8циклоалкила, С3-8циклогетероалкила, фенил-С1-6алкила, амино-С0-6алкила, С1-6алкиламино-С0-6алкила, (C1-6алкил)2амино-C0-6алкила, фенил-C0-6алкиламино-С0-6алкила, (фенил-C0-6алкил)2амино-C0-6алкила, C1-6алкилтио, фенил-C0-6алкилтио, C1-6алкилсульфинила, фенил-C0-6алкилсульфинила, C1-6алкилсульфонила, фенил-C0-6алкилсульфонила, C1-6алкокси-C0-6алкила, фенил-C0-6алкокси-C0-6алкила, гидроксикарбонил-C0-6алкила, C1-6алкоксикарбонил-C0-6алкила, фенил-C0-6алкоксикарбонил-C0-6алкила, гидроксикарбонил-C1-6алкилокси, гидрокси-C0-6алкила, циано, нитро, перфтор-C1-4алкила, перфтор-C1-4алкокси, оксо, C1-6алкилкарбонилокси, фенил-C0-6алкилкарбонилокси, С1-6алкилкарбониламино, фенил-C0-6алкилкарбониламино, С1-6алкилсульфониламино, фенил-C0-6алкилсульфониламино, C1-6алкоксикарбониламино, фенил-C0-6алкоксикарбониламино, C1-6алкиламинокарбониламино, фенил-C0-6алкиламинокарбониламино, (C1-6алкил)2аминокарбониламино, (фенил-C0-6алкил)2аминокарбониламино, (C1-6алкил)2аминокарбонилокси и (фенил-C0-6алкил)2аминокарбонилокси; и где углеродный атом любого метилена (СН2) в (CH2)n является незамещенным или замещен одной-двумя группами, независимо выбранными из галогена, гидрокси и С1-4алкила; или два заместителя, когда они принадлежат одной и той же метиленовой (СН2) группе, взятые вместе с атомом углерода, к которому они присоединены, образуют циклопропильную группу;
или R2 и R3 вместе образуют 5- или 6-членное насыщенное кольцо, конденсированное с 5- или 6-членной ароматической кольцевой системой, имеющей 0, 1 или 2 гетероатома, выбранных из N, O и S.
Вышеуказанные соединения эффективны в качестве агонистов рецептора андрогена и, в частности, эффективны в качестве селективных агонистов рецептора андрогена (SARM). Поэтому указанные соединения используют для лечения состояний, вызванных недостаточностью андрогена или интенсивность симптомов которых может быть уменьшена введением андрогена.
Настоящее изобретение также относится к фармацевтическим композициям, содержащим соединения настоящего изобретения и фармацевтически приемлемый носитель.
Настоящее изобретение также относится к способам лечения состояний, вызванных недостаточностью андрогена или интенсивность симптомов которых может быть уменьшена введением андрогена, у млекопитающего, нуждающегося в таком лечении, путем введения соединений и фармацевтических композиций по данному изобретению.
Настоящее изобретение также относится к способам лечения остеопороза, нарушения остеогенеза, глюкокортикоид-индуцированного остеопороза, периодонтальной болезни, перелома кости, повреждения кости после реконструктивной костной хирургии, саркопении, хрупкости, старения кожи, мужского гипогонадизма, постменопаузальных симптомов у женщин, атеросклероза, гиперхолестеринемии, гиперлипидемии, ожирения, апластической анемии и других гемопоэтических нарушений, артритных состояний, таких как, например, воспалительный артрит и восстановление поврежденного сустава, ВИЧ-истощения, рака простаты, раковой кахексии, мышечной дистрофии, преждевременного угасания функции яичников и аутоиммунного заболевания, путем введения соединений и фармацевтических композиций настоящего изобретения как таковых или в комбинации с терапевтически эффективным количеством другого средства, которое, как известно, используют для лечения таких состояний.
Подробное описание изобретения
Настоящее изобретение относится к соединениям, которые используют в качестве агонистов рецептора андрогена, в частности в качестве селективных агонистов рецептора андрогена. Соединения настоящего изобретения представляют собой соединения, описываемые структурной формулой I:
или их фармацевтически приемлемую соль или их энантиомер; где
n равно 0, 1 или 2;
a-b означает CF=CH, CHFCH2 или CF2CH2;
R1 представляет собой водород, гидроксиметил или C1-3алкил, где алкил является незамещенным или замещен одним-семью атомами фтора;
R2 представляет собой водород или C1-4алкил;
R3 выбран из
C1-4алкила,
(CH2)n-циклогетероалкила и
(CH2)n-арила, где арил выбран из
(1) фенила,
(2) нафтила,
(3) бензимидазолила,
(4) бензофуранила,
(5) бензотиофенила,
(6) бензоксазолила,
(7) бензотиазолила,
(8) бензодигидрофуранила,
(9) 1,3-бензодиоксолила,
(10) 2,3-дигидро-1,4-бензодиоксинила,
(11) индолила,
(12) хинолила,
(13) изохинолила,
(14) фуранила,
(15) тиенила,
(16) имидазолила,
(17) оксазолила,
(18) тиазолила,
(19) изоксазолила,
(20) изотиазолила,
(21) пиразолила,
(22) пирролила,
(23) пиридила,
(24) пиримидила,
(25) пиразинила,
(26) тиадиазолила,
(27) оксадиазолила,
(28) триазолила,
(29) тетразолила и
(30) инданила;
где алкильная группа или циклогетероалкильная группа является незамещенной или замещена одним-тремя заместителями, независимо выбранными из галогена, гидрокси и С1-4алкокси; арильная группа, определенная в пунктах (1)-(30), является незамещенной или замещена одной-тремя группами, независимо выбранными из галогена, фенила, С1-8алкила, С3-8циклоалкила, С3-8циклогетероалкила, фенил-С1-6алкила, амино-С0-6алкила, С1-6алкиламино-С0-6алкила, (C1-6алкил)2амино-C0-6алкила, фенил-C0-6алкиламино-С0-6алкила, (фенил-C0-6алкил)2амино-C0-6алкила, C1-6алкилтио, фенил-C0-6алкилтио, C1-6алкилсульфинила, фенил-C0-6алкилсульфинила, C1-6алкилсульфонила, фенил-C0-6алкилсульфонила, C1-6алкокси-C0-6алкила, фенил-C0-6алкокси-C0-6алкила, гидроксикарбонил-C0-6алкила, C1-6алкоксикарбонил-C0-6алкила, фенил-C0-6алкоксикарбонил-C0-6алкила, гидроксикарбонил-C1-6алкилокси, гидрокси-C0-6алкила, циано, нитро, перфтор-C1-4алкила, перфтор-C1-4алкокси, оксо, C1-6алкилкарбонилокси, фенил-C0-6алкилкарбонилокси, С1-6алкилкарбониламино, фенил-C0-6алкилкарбониламино, С1-6алкилсульфониламино, фенил-C0-6алкилсульфониламино, C1-6алкоксикарбониламино, фенил-C0-6алкоксикарбониламино, C1-6алкиламинокарбониламино, фенил-C0-6алкиламинокарбониламино, (C1-6алкил)2аминокарбониламино, (фенил-C0-6алкил)2аминокарбониламино, (C1-6алкил)2аминокарбонилокси и (фенил-C0-6алкил)2аминокарбонилокси; и где углеродный атом любого метилена (СН2) в (CH2)n является незамещенным или замещен одной-двумя группами, независимо выбранными из галогена, гидрокси и С1-4алкила; или два заместителя, когда они принадлежат одной и той же метиленовой (СН2) группе, взятые вместе с атомом углерода, к которому они присоединены, образуют циклопропильную группу;
или R2 и R3 вместе образуют 5- или 6-членное насыщенное кольцо, конденсированное с 5- или 6-членной ароматической кольцевой системой, имеющей 0, 1 или 2 гетероатома, выбранных из N, O и S.
В одном варианте соединений настоящего изобретения R1 представляет собой водород или метил. В классе указанного выше варианта R1 представляет собой метил.
Во втором варианте соединений настоящего изобретения a-b означает CF=CH.
В третьем варианте соединений настоящего изобретения a-b означает CHFCH2.
В четвертом варианте соединений настоящего изобретения R2 представляет собой водород и R3 представляет собой (CH2)n-арил. В классе указанного выше варианта n равно 0 или 1.
В пятом варианте соединений настоящего изобретения R1 представляет собой метил, a-b означает CF=CH, R2 представляет собой водород и R3 представляет собой (CH2)n-арил. В классе указанного выше варианта n равно 0 или 1.
В шестом варианте соединений настоящего изобретения R1 представляет собой метил, a-b означает CHFCH2, R2 представляет собой водород и R3 представляет собой (CH2)n-арил. В классе указанного выше варианта n равно 0 или 1.
В другом варианте R1 выбран из водорода и метила, a-b выбран из CHFCH2, R2 представляет собой водород и R3 представляет собой (CH2)n-циклогетероалкил. В классе указанного выше варианта R1 представляет собой метил и a-b означает CF=CH.
В еще одном варианте осуществления данного изобретения R3 выбран из:
C1-4алкила и
(CH2)n-арила, где арил выбран из
(1) фенила,
(2) нафтила,
(3) бензимидазолила,
(4) бензофуранила,
(5) бензотиофенила,
(6) бензоксазолила,
(7) бензотиазолила,
(8) бензодигидрофуранила,
(9) 1,3-бензодиоксолила,
(10) 2,3-дигидро-1,4-бензодиоксинила,
(11) индолила,
(12) хинолила,
(13) изохинолила,
(14) фуранила,
(15) тиенила,
(16) имидазолила,
(17) оксазолила,
(18) тиазолила,
(19) изоксазолила,
(20) изотиазолила,
(21) пиразолила,
(22) пирролила,
(23) пиридила,
(24) пиримидила,
(25) пиразинила,
(26) тиадиазолила,
(27) оксадиазолила,
(28) триазолила,
(29) тетразолила и
(30) инданила;
где алкильная группа или циклогетероалкильная группа является незамещенной или замещена одним-тремя заместителями, независимо выбранными из галогена, гидрокси и С1-4алкокси; арильная группа, определенная в пунктах (1)-(30), является незамещенной или замещена одной-тремя группами, независимо выбранными из галогена, фенила, С1-8алкила, С3-8циклоалкила, С3-8циклогетероалкила, фенил-С1-6алкила, амино-С0-6алкила, С1-6алкиламино-С0-6алкила, (C1-6алкил)2амино-C0-6алкила, фенил-C0-6алкиламино-С0-6алкила, (фенил-C0-6алкил)2амино-C0-6алкила, C1-6алкилтио, фенил-C0-6алкилтио, C1-6алкилсульфинила, фенил-C0-6алкилсульфинила, C1-6алкилсульфонила, фенил-C0-6алкилсульфонила, C1-6алкокси-C0-6алкила, фенил-C0-6алкокси-C0-6алкила, гидроксикарбонил-C0-6алкила, C1-6алкоксикарбонил-C0-6алкила, фенил-C0-6алкоксикарбонил-C0-6алкила, гидроксикарбонил-C1-6алкилокси, гидрокси-C0-6алкила, циано, нитро, перфтор-C1-4алкила, перфтор-C1-4алкокси, оксо, C1-6алкилкарбонилокси, фенил-C0-6алкилкарбонилокси, С1-6алкилкарбониламино, фенил-C0-6алкилкарбониламино, С1-6алкилсульфониламино, фенил-C0-6алкилсульфониламино, C1-6алкоксикарбониламино, фенил-C0-6алкоксикарбониламино, C1-6алкиламинокарбониламино, фенил-C0-6алкиламинокарбониламино, (C1-6алкил)2аминокарбониламино, (фенил-C0-6алкил)2аминокарбониламино, (C1-6алкил)2аминокарбонилокси и (фенил-C0-6алкил)2аминокарбонилокси; и где углеродный атом любого метилена (СН2) в (CH2)n является незамещенным или замещен одной-двумя группами, независимо выбранными из галогена, гидрокси и С1-4алкила; или два заместителя, когда они принадлежат одной и той же метиленовой (СН2) группе, взятые вместе с атомом углерода, к которому они присоединены, образуют циклопропильную группу.
Иллюстративными, но неограничивающими примерами соединений настоящего изобретения, которые полезны в качестве модуляторов рецептора андрогена, являются следующие:
N-(2,2,2-трифторэтил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(2-фторфенилметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(3-фторфенилметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(2-трифторметилфенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(2-хлорфенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(4-метоксифенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(3-метоксифенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(2-метилфенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(3-метилфенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(2-фторфенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(3-фторфенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(4-фторфенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(4-хлор-2-фторфенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(2,4-дифторфенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(α-метилфенилметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(фенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(4-хлор-2-трифторметилфенил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(5-метилпиридин-2-ил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(тиофен-2-илметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(тиофен-3-илметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(2-трифторметилфенилметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(бензимидазол-2-илметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(1-метилбензимидазол-2-илметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(1-метил-5-трифторметилбензимидазол-2-илметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(5-хлорбензимидазол-2-илметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(5-метоксибензимидазол-2-илметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(бензтиазол-2-илметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(2,3-дигидро-1,4-бензодиоксин-2-илметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(тиазол-2-илметил)-2-фтор-4-метил-3-оксо-4-аза-5α-андрост-1-ен-17β-карбоксамид;
N-(4-метилтиазол-2-илметил)-2-фтор