Способ получения no-донорных соединений, таких как no-донорный диклофенак
Иллюстрации
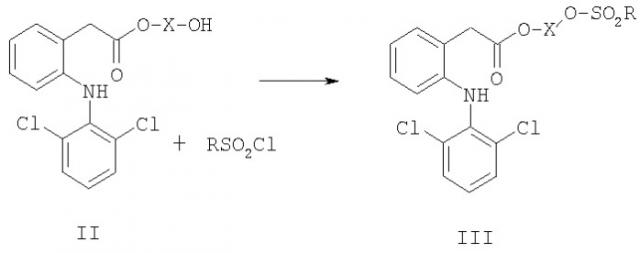
Показать всеНастоящее изобретение относится к новому способу получения NO-донорных соединений формулы (IV), включающему: стадию 1) реакцию соединения формулы (I)
с соединением формулы НО-Х-ОН с помощью кислотного или дегидрирующего агента и первого растворителя, необязательно с последующей очисткой экстракцией или кристаллизацией, чтобы получить соединение формулы (II)
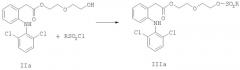
стадию 2) реакцию соединения формулы (II) с соединением формулы RSO2Cl, с помощью второго растворителя, основания и, необязательно, катализатора, с последующей очисткой экстракцией и кристаллизацией, чтобы получить соединение формулы III,
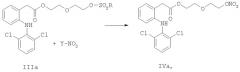
стадию 3) реакцию соединения формулы (III) с соединением формулы Y-NO3 с помощью третьего растворителя и, необязательно, катализатора, необязательно с последующей кристаллизацией для получения соединения формулы IV
в котором MLT1AT2 выбран из группы, состоящей из
и
в котором X выбран из группы, состоящей из линейного -(CH2)w1-, где w1 имеет значение от 2 до 10; -(СН2-СН2-О)2-СН2-СН2- и -СН2-С6H4-CH2-. R выбран из группы, состоящей из С1-С8алкила, фенила, фенилметила, С1-С4алкилфенила, галогенфенила, нитрофенила, ацетиламинофенила, галогена, CF3 и n-C4F9; Y-NO3 представляет собой нитрат лития, нитрат натрия, нитрат калия, нитрат магния, нитрат кальция, нитрат железа, нитрат цинка и нитрат тетраалкиламмония, где алкил представляет собой C1-C18-алкил, который может быть линейным или разветвленным и их смесью; m имеет значение 2; и при условии, что когда MLT1AT2-COOH представляет собой напроксен, X не является (СН2)4. Изобретение также относится к применению способа для получения соединений формул IVa, IVb, IVc и IVd, к новым промежуточным соединениям формул IIIa, IIIb, IIIc и IIId, к кристаллической форме 2-[2-(нитроокси)этокси]этил{2-[(2,6-дихлорфенил)амино]фенил}ацетата и способу ее получения, и к ее применению для получения лекарственного средства для лечения боли и/или воспаления, к применению соединений формулы III, в качестве промежуточных соединений. А также к применению промежуточных соединений формул IIIa, IIIb, IIIc и IIId для получения соединений формулы IVa, IVb, IVc и IVd. Технический результат - новый способ получения соединений формулы (IV). 8 н. и 24 з.п. ф-лы, 1 ил., 1 табл.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новому способу получения NO-донорных соединений, то есть соединений, высвобождающих оксид азота, с помощью сульфонированного промежуточного соединения. Изобретение относится к полученным таким образом новым промежуточным соединениям, пригодным для получения большого числа NO-донорных соединений. Изобретение далее относится к применению новых промежуточных соединений для получения фармацевтически активных NO-донорных соединений.
Изобретение далее относится по существу к кристаллической форме NO-донорных NSAID, особенно 2-[2-(нитроокси)этокси]этил{2-[(2,6-дихлорфенил)амино]фенил} ацетата, способам их получения и к фармацевтическим составам, содержащим указанную кристаллическую форму, и к применению указанной кристаллической формы для получения лекарственного средства.
УРОВЕНЬ ТЕХНИКИ
NO-донорные соединения являются соединениями, имеющими NO или NO2 группу, связанную с фармацевтически активным соединением. Между фармацевтически активным соединением и NO или NO2 группой может использоваться линкер.
Преимуществом NO-донорных соединений по сравнению с близким соединением является, среди прочего, хорошая толерантность и снижение желудочно-кишечных побочных эффектов. Это является особенно очевидным для NO-донорных аналогов NSAID, таких как диклофенак и кетопрофен. NO-донорные аналоги NSAID известны благодаря их фармацевтической активности в качестве противовоспалительных и/или анальгетических агентов.
В уровне техники описаны различные способы получения NO-донорных соединений.
Cainelli и др. (Tetrahedron Lett., 1985, 28, 3369-3372) и Cainelli и др. (Tetrahedron 1985, 41, 1385-1392) описывают замещение сульфонатных эфиров нитратом тетрабутиламмония или ионообменную реакцию с нитратными ионами в растворителе, таком как пентан, толуол или бензол. В этом способе применяются высокие температуры, что делает способ небезопасным для широкомасштабного применения.
Cainelli и др. (J. Chem. Soc. Perkin Trans. I, 1987, 2637-2642) описывает нитратное замещение сульфонатных эфиров реакцией алкилметансульфонатов с нитратом тетрабутиламмония в толуоле.
Kawamura и др. (Chem. Parm. Bull, 1990, 38, 2092-2096) описывает реакцию, в которой алкилфенилсульфонат реагирует с нитратом тетрабутиламмония в толуоле.
Стоимость исходного нитрата тетраалкиламмония, применяемого в стехиометрических количествах, как описано в документах предшествующего уровня техники, является высокой для широкомасштабного получения NO-донорных соединений. По экономически причинам предпочтительными являются способы, в которых могут использоваться более дешевые нитраты и нитраты щелочного металла с низким молекулярным весом. Однако нитраты тетраалкиламмония могут использоваться в качестве катализаторов фазового переноса в количествах, ниже стехиометрических.
У Hwu и др. (Synthesis, 1994, 471-474) описано получение нитратных эфиров из эфиров сульфоновой кислоты. Слишком высокие температуры и долгая продолжительность реакции в сочетании с низкой стабильностью полученных конечных продуктов делает этот способ менее пригодным для широкомасштабного производства. Кроме того, молярный избыток нитрата натрия почти вдвое больше по сравнению с настоящим изобретением, что повышает стоимость и может обеспечить проблемы с отходами. Кроме того, сырой продукт, полученный способом согласно Hwu и др., требует очистки либо хроматографией, либо перегонкой для обеспечения фармацевтически приемлемой чистоты. Никакой из этих двух способов очистки не подходит для широкомасштабного получения соединений.
ES 2073995 описывает синтезы алкилнитратных эфиров из алкилсульфонатов или 4-толуолсульфонатов и нитратов металла с помощью растворителей, таких как диметилформамид, диметилацетамид, ацетонитрил или диметилсульфоксид. Используя диметилацетамид или диметилсульфоксид в качестве растворителя в синтезе NO-донорных соединений исходя из сульфонированных промежуточный соединений, получают сырой продукт, который нуждается в очистке либо хроматографией, либо перегонкой для достижения фармацевтически приемлемой чистоты.
Примерами NSAID является диклофенак (соединение формулы Ia) и кетопрофен (соединение формулы Id):
WO 94/04484 и WO 94/12463 описывают способы получения NO-донорных аналогов диклофенака и кетопрофена соответственно. В указанных способах дигалогенидные производные подвергают реакции с солью карбоновой кислоты ДМФА. Продукты реакции превращают в конечные продукты реакцией с AgNO3 в ацетонитриле способом, известным из уровня техники.
Способ настоящего изобретения включает использование сульфонированного промежуточного соединения. Это промежуточное соединение может быть легко получено и является высокореакционным в реакциях с нитратными ионами для получения соответствующего нитрооксиалкильного эфира.
Таким образом, существует потребность в более удобном и экономически выгодном широкомасштабном способе получения фармацевтически чистых NO-донорных соединений, и их сульфонированных промежуточных соединений, где такие факторы, как стоимость, время получения, применение более безопасных для окружающей среды растворителей, являются важными для коммерческого использования. Настоящее изобретение обеспечивает такой способ.
В составе лекарственных композиций важно, чтобы соединение находилось в форме, в которой его можно легко обрабатывать и использовать. Это важно для обеспечения коммерчески приемлемого способа получения и для изготовления фармацевтических составов, включающих активное соединение.
Далее, при изготовлении лекарственных композиций важно, чтобы при введении пациенту обеспечивался надежный, воспроизводимый и постоянный профиль концентрации соединения в плазме.
Химическая стабильность и физическая стабильность соединений являются важными факторами. Соединение и содержащие его составы должны эффективно храниться в течение длительных периодов времени, без существенных изменений физико-химических характеристик активного соединения, таких как его химический состав, плотность, гигроскопичность и растворимость.
Кроме того, важно получить соединение в форме, которая является как можно более химически чистой.
Аморфные материалы могут создавать существенные проблемы в этом отношении. Такие материалы трудно обрабатывать и вводить в составы, они показывают плохую растворимость и часто оказывается, что они являются нестабильными и химически загрязненными.
Таким образом, при получении коммерчески выгодных и фармацевтически приемлемых составов важно, по возможности, получить лекарственное средство по существу в кристаллической и стабильной форме.
Следует отметить, однако, что эта цель не всегда достижима. Действительно, обычно только из молекулярной структуры невозможно предсказать, каким будет поведение соединения при кристаллизации. Обычно это может быть определено только экспериментально.
Неожиданно было обнаружено, что 2-[2-(нитроокси)этокси]этил{2-[(2,6-дихлорфенил)амино]фенил}-ацетат (соединение IVa) может быть получено в форме, которая является по существу кристаллической и стабильной.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новому способу получения NO-донорных соединений. Кроме того, оно относится к новым промежуточным соединениям и к способу получения указанных промежуточных соединений, особенно к широкомасштабному способу получения.
Новый способ получения NO-донорных соединений описан ниже.
Одно воплощение изобретения относится к способу получения NO-донорных соединений, включающему:
стадию 1
с помощью кислотного или дегидрирующего агента и растворителя, необязательно с последующей очисткой экстракцией или кристаллизацией, и
стадию 2
с помощью растворителя, основания и, необязательно, катализатора, с последующей очисткой экстракцией и кристаллизацией, и
стадию 3
с помощью растворителя и, необязательно, катализатора,
необязательно с последующей кристаллизацией для получения соединения формулы IV по существу в кристаллической форме, и
где:
М представляет собой радикал физиологически активного соединения;
L представляет собой О, S, (CO)O, (CO)NH, (CO)NR1, NH, NR1, где R1 представляет собой линейную или разветвленную алкильную группу, или
или
где Rb представляет собой Н, С1-12алкил или С2-12алкенил;
R2 представляет собой (CO)NH, (CO)NR1, (CO)O или CR1 и а и b независимо имеют значение 0 или 1;
А представляет собой замещенную или незамещенную линейную или разветвленную алкильную цепь;
Х представляет собой углеродный линкер;
R выбран из группы, состоящей из C1-C8алкила, фенила, фенилметила, C1-C4алкилфенила, галогенфенила, нитрофенила, ацетиламинофенила, галогена, CF3 и н-C4F9;
Y-NO3 представляет собой нитрат лития, нитрат натрия, нитрат калия, нитрат магния, нитрат кальция, нитрат железа, нитрат цинка или нитрат тетраалкиламмония (где алкил представляет собой C1-C18-алкил, который может быть линейным или разветвленным);
m имеет значение 1 или 2; и
Т1 и Т2 каждый независимо имеет значение 0, 1, 2 или 3;
при условии, что
когда MLT1АT2-СООН представляет собой напроксен, X не является (СН2)4.
Другое воплощение изобретения относится к способу получения промежуточных соединений формулы III, которые могут использоваться для получения NO-донорных соединений, включающему:
стадию 1,
с помощью кислотного или дегидрирующего агента и растворителя, необязательно с последующей очисткой экстракцией или кристаллизацией, и стадию 2,
с помощью растворителя, основания и, необязательно, катализатора, с последующей очисткой экстракцией и кристаллизацией, и где М, L, A, T1, T2, X и R имеют указанные выше значения.
Термин "C1-C8алкил" обозначает алкил с 1-8 атомами углерода и включает алкильные группы как с линейной, так и с разветвленной цепью, такие как метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил и т.д.
Термин "C1-C4алкилфенил" обозначает метилфенил, этилфенил, н-пропилфенил, изопропилфенил, н-бутилфенил, изобутилфенил и трет-бутилфенил.
Термин "фенилметил" обозначает бензил.
Термин "гало" и "галоген" обозначает фтор, хлор или бром.
Термины "галогенфенил", "нитрофенил" и "ацетиламинофенил" относятся к фенильным группам, замещенным одним или несколькими группами галогена, нитро или ацетиламино.
Термин "широкомасштабный" обозначает получение количества в области "от килограмма до мультитонны".
М может представлять собой любой радикал любого физиологически активного соединения.
MLT1АT2-СООН может быть любая физиологически активная карбоновая кислота.
В одном воплощении изобретения группа М является частью молекулы NSAID, ингибитора СОХ1 или СОХ2.
В другом воплощении изобретения группа М выбрана из группы, состоящей из
как описано в WO 00/51988, и
как описано в US 3641127, и
как описано в WO 96/32946, и
циклоалкилов, описанных в WO 98/25918, таких как 2,2-диметил-циклопропан-1-метанол, и
как описано в CN 1144092, и
как описано в WO 95/09831, и
как описано в WO 95/30641, и
как описано в WO 02/30866, и
как описано в US 6297260.
В одном воплощении изобретения L выбран из группы, состоящей из О, S, NH, NR1, где R1 представляет собой линейную или разветвленную алкильную группу, как описано в WO 95/09831, и (СО) или (CO)O, как описано в WO 95/30641, и
где Rb представляет собой Н, С1-12 алкил или C2-12 алкенил и а и b независимо имеют значения 0 или 1, как описано в WO 02/053188,
и
где Rb, а и b имеют указанные выше значения; и
R2 представляет собой (CO)NH, (CO)NR1, (CO)O или CR1.
В другом воплощения изобретения А выбран из группы, состоящей из -(CH2)n-, где n имеет значение 0, 1, 2, 3 или 4,
| И |
где d1 имеет значение 1, 2 или 3.
В другом воплощении изобретения А выбран из группы, состоящей из
| И |
где d1 имеет значение 1, 2 или 3.
Углеродный линкер X может быть выбран из группы, состоящей из
где А′ и В выбраны из водорода, линейной или разветвленной или циклической замещенной или незамещенной алкильной группы, и v1 имеет значение от 1 до 10 как описано в WO 95/09831, и
-(СН2-СН2-O)2-, или циклоалкил, имеющий 5-7 атомов углерода, необязательно замещенных, и
где m1 имеет значение от 0 до 3, и
и
где Rc представляет собой Н или метил, и р имеет значение от 0 до 6, как описано в WO 95/30641 и WO 02/92072, и
-(CH2)q-OCO-(CH2)r, где q и r каждый независимо имеет значение от 0 до 6, и
где Z представляет собой О, SO, S или насыщенное, ненасыщенное или ароматическое 5 или 6-членное кольцо или 5 или 6-членное гетероциклическое кольцо, содержащее один или несколько гетероатомов, независимо выбранных из N, О и S, где указанное кольцо необязательно может быть замещено, и v2 и v3 независимо имеют значения от 0 до 4.
В одном воплощении изобретения X выбран из группы, состоящей из линейной, разветвленной или циклической -(CH2)w1-, где w1 имеет значение от 2 до 10; -(CH2)w2-O-(CH2)w3-, где w2 и w3 имеют значения от 2 до 10; и -СН2-С6Н4-СН2-.
В другом воплощении изобретения X выбран из группы, состоящей из линейной -(CH2)w1-, где w1 имеет значение от 2 до 6; -(СН2)2-O-(СН2)2- и -СН2-C6H4-CH2-.
В другом воплощении изобретения R выбран из группы, состоящей из C1-C8алкила, фенила, фенилметила, C1-C4алкилфенила, галогенфенила, нитрофенила, ацетиламинофенила и галогена.
В одном воплощении изобретения группа MLT1АT2 выбрана из группы, состоящей из
| и |
В другом воплощении изобретения группа MLT1АT2 выбрана из группы, состоящей из
и
В конкретном воплощении группа MLT1АT2 представляет собой
или
Описание способа
Стадия 1
где М, L, A, T1, T2 и X имеют значения, указанные выше.
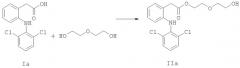
MLT1АT2-СООН может быть этерифицирован на стадии 1 реакции с помощью кислотной катализируемой этерификации в присутствии диэтиленгликоля, как описано в DE 88-3811118, при использовании п-толуолсульфоновой кислоты.
Стадия 1 этерификации может осуществляться способом, известным специалисту в данной области техники, например, обработкой соединения формулы I, например диклофенака и диэтиленгликоля, кислотным или дегидрирующим агентом.
Одно воплощение относится к способу по изобретению, в котором кислотный или дегидрирующий агент на стадии 1 выбирают из группы, состоящей из серной кислоты или ее солей, перхлорной кислоты (например, 70%) или других подходящих кислот, таких как полистиролсульфоновые кислоты, цеолиты, кислые глины, песок в комбинации с сильными гидрофильными кислотами, такими как перхлорная кислота или газообразный хлорид водорода, и монтмориллониты.
Соединения формулы II могут быть также получены тем же способом с помощью 1,4-бутандиола, 1,3-пропандиола и триэтиленгликоля, соответственно. В ES 85-548226 для катализирования этерификации используют тионилхлорид.
Кислоты могут использоваться в виде газа, жидкости или в твердой форме.
Гетерогенные кислоты могут быть относительно легко отфильтрованы из реакционного раствора и повторно использоваться в широкомасштабных способах получения.
Примерами других конденсирующих реагентов, используемых на стадии 1 этерификации, являются карбодиимиды, такие как N,N'-дициклогексилкарбодиимид (DCC), хлориды кислот, такие как оксалилхлорид, хлорформаты, такие как изобутилхлорформат, или другие реагенты, такие как цианурилхлорид, N,N'-карбонилдиимидазол, диэтилхлорфосфит, 2-хлор-1-метил-пиридинйодид и 2,2′-дипиридилдисульфид.
Одно воплощение относится к способу по изобретению, в котором растворитель на стадии 1 является неполярным и/или некислотным растворителем.
Стадия 1 реакции может проводиться в растворителе, выбранном из группы, включающей ароматические углеводороды, такие как бензол или толуол, алифатические углеводороды, такие как н-гептан, кетоны, такие как метилизобутилкетон, эфиры, такие как тетрагидрофуран или диметиловый эфир диэтиленгликоля и хлорированные углеводороды, такие как дихлорметан или хлорбензол, или их смеси.
Альтернативно, избыток соответствующего диола может использоваться в качестве растворителя, необязательно в смеси с любыми другими органическими растворителями, упомянутыми выше.
Соединения формулы II, полученные на стадии 1, могут быть очищены экстракцией, партиями или непрерывно, получая раствор, содержащий соединение формулы II, имеющий хроматографическую чистоту по крайней мере 92% и, предпочтительно, более 97% (после стадии i экстракции) и содержание алкилендиола или алкиленгликоля ниже 0.5% (вес.) (после на стадии ii экстракции).
Стадия i) экстракции
На этой стадии экстракции повышается хроматографическая чистота. Раствор, используемый на этой стадии экстракции, может включать смесь i) алкилендиола или алкиленгликоля, ii) воды и/или алифатического спирта с низким молекулярным весом и iii) углеводородный растворитель или их смеси или смеси органических растворителей с углеводородными растворителями.
Алифатические спирты с низким молекулярным весом могут быть выбраны из группы, состоящей из метанола, этанола и пропанола или их смеси.
Углеводородные растворители, используемые на стадии i) экстракции, могут быть выбраны из группы, включающей толуол, кумол, ксилол, лигроин, петролейный эфир, галогенбензолы, гептаны, гексаны, октаны, циклогексаны, циклогептаны и им подобные, или их смеси.
Подходящие органические растворители, используемые на стадии i) экстракции, могут быть выбраны из группы, включающей кетоны, такие как метилизобутилкетон, эфиры, такие как ди-н-бутиловый эфир или трет-бутилметиловый эфир, и алифатические эфиры, такие как этилацетат или н-бутилацетат, и галогеналканы, такие как дихлорметан, или их смеси.
Очищенное соединение формулы II получают в виде раствора в смеси с алкилендиолом или алкиленгликолем с водой и/или алифатическим спиртом с низким молекулярным весом.
Стадия ii) экстракции
Эта экстракция осуществляется для снижения содержания алкилендиола или алкиленгликоля и проводится после стадии i) экстракции, на которой повышается хроматографическая чистота, как описано выше. Раствор может включать i) смесь воды и/или алифатического спирта с низким молекулярным весом, ii) органический растворитель или смеси органических растворителей. Алифатические спирты с низким молекулярным весом могут быть выбраны из группы, состоящей из метанола, этанола и пропанола или их смесей.
Подходящие органические растворители, используемые на стадии ii) экстракции, могут быть выбраны из группы, включающей ароматические углеводороды, такие как толуол, кумол или ксилолы, кетоны, такие как метилизобутилкетон, эфиры, такие как ди-н-бутиловый эфир или трет-бутилметиловый эфир и алифатические эфиры, такие как этилацетат или н-бутилацетат и галогеналканы, такие как дихлорметан, или их смеси.
Общее количество растворителей, используемых на стадии 1 процесса этерификации, может изменяться от 0 до 100 частей по объему от веса исходного сырья.
Температура стадии 1 этерификации может изменяться от -100°С до +130°С, предпочтительно от 0°С до +120°С.
Стадия 2
где М, L, A, T1, T2, X и R имеют указанные выше значения.
Условия реакции стадии 2 включают избыток RSO2Cl в органическом растворителе или смеси органических растворителей.
Подходящие растворители на стадии 2 могут быть выбраны из группы, включающей ароматические углеводороды, такие как толуол, кумол или ксилолы, кетоны, такие как метилизобутилкетон, эфиры, такие как ди-н-бутиловый эфир или трет-бутилметиловый эфир или тетрагидрофуран, алифатические нитрилы, такие как ацетонитрил, и алифатические эфиры, такие как этилацетат или н-бутилацетат, и галогеналканы, такие как дихлорметан, или их смеси.
Одно воплощение относится к способу по изобретению, в котором растворители на стадии 2 выбраны из группы, состоящей из толуола, кумола, ксилолов, этилацетата, ацетонитрила, бутилацетата и изопропилацетата.
На стадии 2 может быть добавлено основание. В одном воплощении изобретения основание на стадии 2 может быть выбрано из группы, состоящей из триэтиламина, пиридина, N-метилморфолина, диизопропилэтиламина, трибутиламина и N-метилпиперидина.
Другое воплощение относится к способу изобретения, в котором основание на стадии 2 представляет собой триэтиламин или N-метилморфолин.
Другое воплощение относится к способу по изобретению, в котором на стадии 2 необязательно может использоваться катализатор, такой как 4-(диметиламино)пиридин.
Соединения формулы III, полученные на стадии 2, могут быть очищены кристаллизацией из органического растворителя для получения кристаллического твердого вещества, имеющего химическую чистоту около 95% и особенно около 98%.
Другое воплощение относится к способу по изобретению, в котором на стадии 2 для перекристаллизации соединения формулы III используется осаждающий растворитель.
В другом воплощении изобретения растворитель, используемый для кристаллизации, может быть выбран из группы, включающей ароматические углеводороды, такие как толуол, кумол или ксилолы, кетоны, такие как метилизобутилкетон, эфиры, такие как ди-н-бутиловый эфир, трет-бутилметиловый эфир или тетрагидрофуран, алифатические нитрилы, такие как ацетонитрил, и алифатические эфиры, такие как этилацетат или бутилацетат, или их смеси.
Другое воплощение относится к способу по изобретению, в котором растворитель, используемый для кристаллизации на стадии 2, выбран из группы, состоящей из толуола, кумола, ксилолов, этилацетата, ацетонитрила, бутилацетата и изопропилацетата, или их смесей.
Другое воплощение относится к способу по изобретению, в котором осаждающий растворитель, используемый для кристаллизации на стадии 2, выбран из группы, включающей лигроин, петролейный эфир, галогенбензолы, гептаны, гексаны, октаны, такие как изооктан, циклогексаны, циклогептаны и спирты, или их смеси.
Стадия 3
где M, L, A, T1, T2, X, R, m и Y являются такими, как определено выше.
На стадии 3 способа получения соединение формулы IV получают по реакции соединения формулы III с источником нитрата (Y-NO3), необязательно в присутствии растворителя.
Эта реакция может осуществляться с источником нитрата Y-NO3, выбранным из группы, состоящей из нитрата лития, нитрата натрия, нитрата калия, нитрата магния, нитрата кальция, нитрата железа, нитрата цинка и нитрата тетраалкиламмония (где алкил представляет собой C1-C18-алкил, который может быть линейным или разветвленным).
Одно воплощение относится к способу по изобретению, в котором источники нитрата Y-NO3 на стадии 3 выбраны из группы, состоящей из нитрата лития, нитрата натрия, нитрата калия, нитрата магния и нитрата кальция, или их смесей.
Другое воплощение относится к способу по изобретению, в котором органический растворитель на стадии 3 является полярным апротонным растворителем.
В другом воплощении по изобретению полярные апротонные растворители, используемые на стадии 3, могут быть выбраны из группы, включающей N-метилпирролидинон, N,N-диметилацетамид, сульфолан, тетраметилмочевину, 1,3-диметил-2-имидазолидинон и нитрилы, такие как ацетонитрил, или их смеси.
Другими растворителями могут быть ароматические углеводороды, такие как толуол, алифатические углеводороды, такие как н-гептан, кетоны, такие как метилэтилкетон, метилизобутилкетон, эфиры, такие как тетрагидрофуран или диметиловый эфир диэтиленгликоля, хлорированные углеводороды, такие как хлорбензол, алифатические эфиры, такие как этилацетат, бутилацетат или изопропилацетат, нитроуглеводороды, такие как нитрометан, этиленгликоли, такие как полиэтиленгликоль и их смеси, необязательно с дополнительными алифатическими спиртами, такими как метанол, этанол, н-пропанол, изопропанол, н-бутанол, изобутанол или трет-бутанол.
Одно воплощение изобретения относится к способу по изобретению, в котором органический растворитель на стадии 3 выбран из группы, состоящей из N-метилпирролидинона, сульфолана, тетраметилмочевины, 1,3-диметил-2-имидазолидинона, ацетонитрила, метилизобутилкетона, этилацетата, бутилацетата и изопропилацетата, или их смесей.
Стадия 3 нитрования может также осуществляться в воде, необязательно в комбинации с любыми указанными выше органическими растворителями.
Стадия 3 нитрования может необязательно проводиться в присутствии катализатора фазового переноса.
Одно воплощение относится к способу по изобретению, в котором катализатор фазового переноса на стадии 3 выбран из группы, состоящей из соли тетраалкиламмония, соли арилалкиламмония, соли тетраалкилфосфония, соли арилалкилфосфония, краунэфира, пентаэтиленгликоля, гексаэтиленгликоля и полиэтиленгликолей, или их смесей.
Кристаллизация соединений формулы IV
Соединения формулы IV, полученные на стадии 3, могут быть очищены кристаллизацией из органического растворителя, необязательно с помощью углеводородов, спиртов или воды в качестве осаждающего растворителя, для получения кристаллического твердого продукта химической чистоты 90% и особенно около 95%.
Одно воплощение относится к способу по изобретению, в котором соединение формулы IV на стадии 3 экстрагируют порциями или непрерывно и кристаллизуют из органического растворителя, необязательно с помощью осаждающего растворителя, для получения кристаллического твердого вещества, имеющего химическую чистоту по крайней мере 95%.
Предпочтительно кристаллизацию осуществляют в подходящей системе растворителя. Кристаллизация может также осуществляться без системы растворителя. Другие примеры перекристаллизации включают перекристаллизацию из расплава, в надкритических условиях или при сублимации.
Кристаллизация соединений формулы IV из подходящей системы растворителя может проводиться при достижении сверхнасыщения в системе растворителя, которая включает соединение формулы IV. Это может быть достигнуто охлаждением системы растворителя, упариванием растворителя, добавлением подходящего осаждающего растворителя или любой комбинацией этих методов. Кристаллизация может также достигаться при снижении растворимости соединения путем добавления соли, такой как, например, NaCl.
Способ кристаллизации может применяться к реакционному раствору, включающему соединение формулы IV, полученному после приготовления указанного соединения.
Способ кристаллизации также может применяться к сухому соединению формулы IV. Альтернативно способ кристаллизации может применяться после экстракции соединения формулы IV из реакционного раствора.
Одно воплощение настоящего изобретения относится к описанному выше способу, в котором способ кристаллизации соединения формулы IV включает следующие стадии:
a) i) растворение соединения в растворителе;
или
ii) экстракция соединения из реакционного раствора в растворитель;
или
iii) из реакционного раствора, включающего указанное соединение;
b) упаривание растворителя;
c) добавление осаждающего растворителя и/или охлаждение;
d) выделение полученных кристаллов, и необязательно:
e) перекристаллизация кристаллов, полученных на стадии с); или выделенных на стадии d).
Другое воплощение изобретения относится к описанному выше способу, в котором способ кристаллизации соединения 2-[2-(нитроокси)-этокси]этил{2-[(2,6-дихлорфенил)амино]фенил}ацетата (IVa) включает следующие стадии:
a) экстракция соединения из реакционного раствора в растворитель;
b) упаривание растворителя;
c) добавление осаждающего растворителя и/или охлаждение;
d) выделение полученных кристаллов и, необязательно:
e) перекристаллизация кристаллов, полученных на стадии с); или выделенных на стадии d).
По существу кристаллическая форма 2-[2-(нитроокси)-этокси]этил{2-[(2,6-дихлорфенил)амино] фенил} ацетата обозначена далее как "Форма А соединения IVa".
Другое воплощение изобретения включает способ получения Формы А соединения IVa, который включает кристаллизацию 2-[2-(нитроокси)-этокси]этил{2-[(2,6-дихлорфенил)амино]фенил} ацетата.
Подходящие растворители, используемые для способа перекристаллизации, могут