Высвобождаемые полимерные конъюгаты на основе алифатических биоразлагаемых сшивающих агентов
Иллюстрации
Показать всеОписаны активированные полимерные производные бицина, а также полученные с их помощью конъюгаты. Также описаны способы получения и применения производных бицина. 5 н. и 19 з.п. ф-лы, 11 ил., 2 табл.
Реферат
ОБЛАСТЬ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к разветвленным полимерам, применимым для увеличения времени циркуляции биологически активных веществ in vivo. Данное изобретение также относится к конъюгатам, изготовленным с этими полимерами.
ПРЕДПОСЫЛКИ К СОЗДАНИЮ ИЗОБРЕТЕНИЯ
Некоторые исходные концепции «прикрепления» пептидов или полипептидов к поли(этиленгликолю) ПЭГ и подобным водорастворимым поли(алкиленоксидам) раскрыты в патенте США № 4179337, описание которого включено здесь в качестве ссылки. Полипептиды, модифицированные этими полимерами, проявляют меньшую иммуногенность/антигенность и циркулируют в кровотоке в течение более длительного времени, чем немодифицированные варианты.
Для конъюгации поли(алкиленоксидов) одну из концевых гидроксильных групп превращают в реакционноспособную функциональную группу. Этот процесс зачастую называют «активацией», а продукт называют «активированным поли(алкиленоксидом)». Другие, по существу неантигенные полимеры, «активизируют» или функционализируют подобным образом.
Активированные полимеры подвергают взаимодействию с терапевтическими агентами, имеющими нуклеофильные функциональные группы, которые служат в качестве области присоединения. Одной нуклеофильной функциональной группой, обычно используемой как область присоединения, являются ε-аминогруппы лизинов. Свободные карбоксильные группы, соответствующим образом активированные карбонильные группы, окисленные углеводородные части молекулы и меркаптогруппы также могут быть использованы в качестве области присоединения.
Инсулин и гемоглобин находятся среди первых конъюгированных терапевтических агентов. Эти сравнительно крупные полипептиды содержат несколько свободных ε-амино областей присоединения. Могло быть присоединено достаточное число полимеров для снижения иммуногенности и увеличения времени циркулирования без значительной потери биологической активности.
Однако было обнаружено, что излишняя конъюгация полимеров и/или конъюгация, вовлекающая терапевтически активные части молекулы, в которых группы связаны с биологической активностью, часто приводит к потере активности и, следовательно, к потере терапевтической эффективности. Это зачастую происходит с пептидами низкой молекулярной массы, которые имеют незначительное число областей присоединения, не связанных с биологической активностью. Многим непептидным лекарственным средствам также не хватает достаточного количества областей присоединения для получения благоприятной модификации полимера.
Одним вариантом преодоления указанных выше проблем является применение более длинных полимеров с большей молекулярной массой. В зависимости от требуемой молекулярной массы, эти вещества могут быть трудными для получения и дорогими для использования. Кроме того, иногда они дают незначительное улучшение по сравнению с более легкодоступными полимерами.
Другим альтернативным предложением является присоединение двух цепей полимера через кольцо триазина к аминогруппам белка. Смотри, например, Enzyme, 26, 49-53 (1981) и Proc. Soc. Exper. Biol. Med., 188, 364-9 (1988). Триазин, однако, является токсичным веществом, содержание которого трудно снизить до приемлемых уровней после конъюгации. Кроме того, триазин представляет собой плоскостную группу и может быть замещен только двойным полимером. Плоская структура жестко фиксирует на месте две цепи полимера. Это ограничивает преимущества полимерной конъюгации примерно до такой же степени, которая достигается при увеличении длины полимерной цепи. Таким образом, полимеры, активированные без участия триазина, внесли бы существенный вклад в уровень техники.
В указанных выше случаях, однако, биологически активные полимерные конъюгаты были получены при наличии по существу устойчивых к гидролизу связей (мостиков) между полимером и исходной биологически активной частью молекулы. Таким образом, были получены долговечные конъюгаты, которые скорее являются постоянно связанными, чем пролекарствами как таковыми (где исходная молекула в конечном итоге высвобождается in vivo).
В общедоступных патентах США №№ 5643575, 5919455 и 6113906 описаны дополнительные усовершенствования, относящиеся к многоцепочечным ПЭГ, имеющим общую точку присоединения к нуклеофилу через алифатический линкер. В отличие от более ранних разветвленных полимерных конъюгатов на основе триазина, алифатические линкеры дают возможность избежать токсического действия триазина, а также дают другие преимущества. Кроме того, с годами также были предложены некоторые способы получения пролекарств. Пролекарства включают в себя химические производные биологически активного исходного соединения, которое, при введении, будет, в конечном счете, высвобождать активное исходное соединение in vivo. Применение пролекарств позволяет изменять начало и/или продолжительность действия биологически активного соединения in vivo. Пролекарства часто представляют собой биологически инертные или по существу неактивные формы исходного или активного соединения. На скорость высвобождения активного лекарственного средства влияет несколько факторов, в том числе скорость гидролиза линкера, который соединяет исходное биологически активное соединение с носителем пролекарства.
Были описаны некоторые пролекарства на основе сложноэфирных или фосфатных связей. В большинстве случаев главным образом сложноэфирный тип связи, используемый для получения пролекарств, обеспечивает t1/2 для гидролиза вплоть до нескольких дней в водном окружении. Хотя можно было ожидать, что было получено пролекарство, большинство конъюгатов выводится из организма до достижения достаточной степени гидролиза in vivo. Таким образом, было бы предпочтительным предоставить пролекарства, которые имеют связь, дающую возможность более быстрому гидролизу связи полимер-лекарственное средство in vivo с тем, чтобы исходное лекарственное соединение образовывалось быстрее.
Также были описаны пролекарства, основанные на амидных или карбаматных связях. В общем, известно, что амидные связи высокоустойчивы к гидролизу. Однако недавно было обнаружено, что C-концевые амиды ε-аминокислот легко подвергаются гидролизу при 25°C и pH 7,4, когда N-конец N-гидроксиэтилирован одной или двумя гидроксиэтильными группами. Бис N-2-гидроксиэтилглициновый (бициновый) тип молекул является ключом для таких реакций гидролиза. Такие группы бицинового типа недавно были использованы в синтезе пролекарств, смотри общедоступную заявку на выдачу патента США 10/218,167, содержание которой включено здесь в качестве ссылки.
Все еще существует свободное пространство для усовершенствования в области создания пролекарств. Настоящее изобретение относится к такому усовершенствованию.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
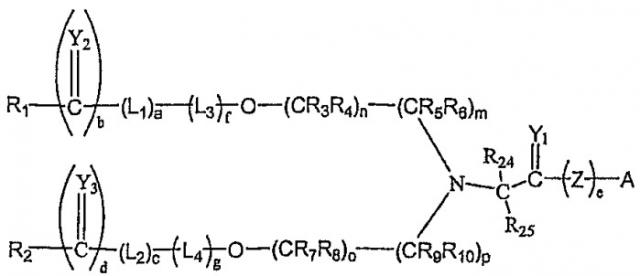
В одном аспекте данное изобретение относится к соединениям формулы (I):
где R1 и R2 независимо выбраны из группы, состоящей из по существу неантигенных полимерных остатков, H, C1-6 алкилов, C2-6 алкенила, C2-6 алкинила, аралкилов и концевых разветвленных групп, при условии, что R1 и R2 оба не являются H;
Z выбран из частей молекулы, активно транспортируемых в клетки-мишени, гидрофобных частей молекулы, бифункциональных связующих частей молекулы и их комбинаций;
Y1-3 могут быть одинаковыми или различными и выбраны из O, S или NR11;
L1 и L2 могут быть одинаковыми или различными бифункциональными линкерами;
R3-R11, R24 и R25 могут быть одинаковыми или различными и выбраны из группы, состоящей из водорода, C1-6 алкилов, C2-6 алкенила, C2-6 алкинила, C3-19 разветвленных алкилов, C3-8 циклоалкилов, C1-6 замещенных алкилов, C2-6 замещенных алкенилов, C2-6 замещенных алкинилов, C3-8 замещенных циклоалкилов, арилов, замещенных арилов, аралкилов, C1-6 гетероалкилов, замещенных C1-6 гетероалкилов, C1-6алкокси, фенокси и C1-6гетероалкокси;
L3 и L4 могут быть одинаковыми или различными и выбраны из:
-C(О)(CR30R31)Y15(CR32R33)C(О)- или
-C(O)(CR30R31)(CR32R33)C(O)-
где Y15 выбран из O, S, NR34 или CH2, и
R30-34 могут быть одинаковыми или различными и выбраны из H, алкила, алкенила, алкинила, гетероалкила или арила;
A выбрано из уходящих групп, функциональных групп, биологически активных частей молекулы и OH;
a, b, c, d и e независимо равны 0 или 1,
m, n, o и p независимо представляют собой положительные целые числа,
f и g равны 0 или 1, при условии, что
по меньшей мере одно из (f + a) или (g + c) равняется 2.
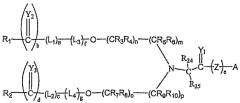
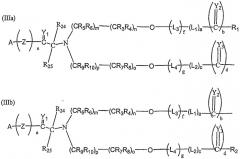
Другой аспект данного изобретения включает в себя бифункциональные соединения, образующиеся в тех случаях, когда, по меньшей мере один из (R1) и (R2) представляет собой полимерный остаток, включающий в себя как альфа, так и омега концевые связующие группы. В этом аспекте данного изобретения возможно присоединить два эквивалента биологически активного компонента лекарственного средства, белка, полипептида, олигонуклеотида и т.д. к полимерной (предпочтительно ПЭГ) бициновой системе. Пример такого бифункционального полимерного конъюгата проиллюстрирован ниже в виде формул (IIa) и (IIb):
где Z представляет собой где Y4 представляет собой O, S или NR11 и L5 представляет собой бифункциональный мостик, а все остальные варианты описаны выше.
Также описаны способы получения соединений по настоящему изобретению и способы лечения с их использованием.
Для целей настоящего изобретения, понятно, что термин «остаток» означает часть соединения, к которому он относится, которая остается после проведения реакции замещения, в которой присоединяется несущая часть полимерного пролекарства.
Для целей настоящего изобретения понятно, что каждый термин «полимерный остаток» или «ПЭГ остаток» означает часть полимера или ПЭГ, которая остается после его реакции с биологически активным соединением.
Для целей настоящего изобретения понятно, что термин «алкил» включает в себя прямые, разветвленные, замещенные, например, гало-, алкокси-, нитро-, C1-2алкилы, C3-8 циклоалкилы или замещенные циклоалкилы, и т.д.
Для целей настоящего изобретения, понятно, что «замещенный» включает в себя добавление или замещение одного или более атомов, находящихся в функциональной группе или соединении одним или более различными атомами.
Для целей настоящего изобретения замещенные алкилы включают в себя карбоксиалкилы, аминоалкилы, диалкиламины, гидроксиалкилы и меркаптоалкилы; замещенные алкенилы, в том числе карбоксиалкенилы, аминоалкенилы, диалкениламины, гидроксиалкенилы и меркаптоалкенилы; замещенные алкинилы, в том числе карбоксиалкинилы, аминоалкинилы, диалкиниламины, гидроксиалкинилы и меркаптоалкинилы; замещенные циклоалкилы, в том числе такие части молекулы, как 4-хлорциклогексил; арилы, в том числе такие части молекулы, как нафтил; замещенные арилы, в том числе такие части молекулы, как 3-бром-фенил; аралкилы, в том числе такие части, как толуил; гетероалкилы, в том числе такие части, как этилтиофен; замещенные гетероалкилы, в том числе такие части, как 3-метокси-тиофен; алкокси включает в себя такие части молекулы, как метокси; и фенокси включает в себя такие части молекулы, как 3-нитрофенокси. Понятно, что гало- включает в себя фтор, хлор, йод и бром.
Термин «достаточные количества» для целей настоящего изобретения будет означать количество, при котором достигается терапевтический эффект, в том смысле, как это понимает специалист в данной области.
Для целей настоящего изобретения будет понятно, что «по сути неантигенный» и «по существу неантигенный» включает в себя все полимерные материалы, которые в данной области подразумеваются нетоксичными и не вызывают заметный иммунный ответ у млекопитающих.
Для целей настоящего изобретения будет понятно, что «положительное целое число» будет означать положительное целое число, предпочтительно примерно от 1 до 6, и более предпочтительно 1 или 2.
Одно основное преимущество настоящего изобретения состоит в том, что бициновый линкер дает возможность управлять скоростью гидролиза пролекарства, предпочтительно высвобождая компоненты в чистом виде с различными скоростями in vivo, а также и in vitro. Например, различные бифункциональные части молекулы, в том числе остатки аминокислот или коротких пептидов, могут быть включены как часть любого из L1-3 для изменения скорости гидролиза пролекарства и/или поступления в клетку, и т.д. in vivo и in vitro.
Другое преимущество данного изобретения состоит в том, что эти целевые соединения, доставляемые посредством полимерной транспортной системы, зачастую демонстрируют заметное увеличение растворимости в воде и продолжительность циркулирования in vivo.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На Фиг.1-11 схематически представлены способы получения соединений по настоящему изобретению, которые подробно описаны в описании и примерах.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
A. ФОРМУЛА (I)
В одном варианте осуществления данное изобретение относится к соединениям формулы (I)
где R1 и R2 могут быть одинаковыми или различными и выбраны из группы, состоящей из по существу неантигенных полимерных остатков, H, C1-6 алкилов, C2-6 алкенила, C2-6 алкинила, аралкилов и концевых разветвленных групп, при условии, что R1 и R2 оба не являются H;
Z выбран из частей молекулы, активно транспортируемых в клетку-мишень, гидрофобных частей молекулы, бифункциональных связующих частей молекулы и их комбинаций;
Y1-3 могут быть одинаковыми или различными и выбраны из О, S или NR11;
L1 и L2 могут быть одинаковыми или различными бифункциональными линкерами; R3-R11, R24 и R25 могут быть одинаковыми или различными и выбраны из группы, состоящей из водорода, C1-6 алкилов, C2-6 алкенила, C2-6 алкинила, C3-19 разветвленных алкилов, C3-8 циклоалкилов, C1-6 замещенных алкилов, C2-6 замещенных алкенилов, C2-6 замещенных алкинилов, C3-8 замещенных циклоалкилов, арилов, замещенных арилов, аралкилов, C1-6 гетероалкилов, замещенных C1-6гетероалкилов, C1-6 алкокси, фенокси и C1-6 гетероалкокси;
L3 и L4 могут быть одинаковыми или различными и выбраны из: -C(O)(CR30R31)Y15(CR32R33)C(O)- или -C(О)(CR30R31)(CR32R33)C(О)-
где Y15 выбран из O, S, NR34 или CH2, и
R30-34 могут быть одинаковыми или различными и выбраны из H, алкила, алкенила, алкинила, гетероалкила или арила;
A выбрано из уходящих групп, функциональных групп, биологически активных частей молекулы и OH;
a, b, c, d, и e независимо равны 0 или 1,
m, n, o, и p независимо представляют собой положительные целые числа,
f и g равны 0 или 1, при условии, что
по меньшей мере один из (f + a) или (g + c) равняется 2.
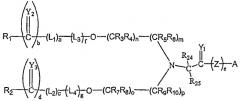
В некоторых предпочтительных аспектах данного изобретения один или более из R1 и R2 включает в себя неантигенный полимерный остаток, такой как группа полиэтиленгликоля (ПЭГ). Необязательно, R1-2 включает в себя кэп-группировку, обозначенную здесь как J. Предпочтительные J группы, используемые для кэппирования полимера, включают в себя такие части молекулы, как OH, NH2, SH, CO2H, части C1-6 алкила, такие как CH3, и соединения формул (IIIa) и (IIIb):
где все переменные определены ранее.
Другим вариантом осуществления изобретения являются соединения формул IV и V:
гдеа, b, c, d, f и gявляются положительными целыми числами, и все остальные переменные определены выше.
В другом аспекте данного изобретения R1 и R2 вместе с атомами, к которым они присоединены, могут образовывать мостиковую структуру, имеющую формулу:
где R70-80 могут быть одинаковыми или различными и выбраны из водорода, C1-6 алкилов, C2-6 алкенила, C2-6 алкинила, C3-19 разветвленных алкилов, C3-8 циклоалкилов, C1-6 замещенных алкилов, C2-6 замещенных алкенилов, C2-6 замещенных алкинилов, C3-8 замещенных циклоалкилов, арилов, замещенных арилов, аралкилов, C1-6 гетероалкилов, замещенных C1-6 гетероалкилов, C1-6 алкокси, фенокси и C1-6гетероалкокси;
n' представляет собой положительное целое число, предпочтительно от примерно 1 до примерно 7, а все остальные переменные определены ранее.
В отношении других переменных, которые составляют формулы настоящего изобретения, в некоторых аспектах данного изобретения предпочтительными являются следующие:
в некоторых аспектах, R1 и R2 представляют собой остатки полиалкиленоксида, и, более предпочтительно, остатки полиэтиленгликоля.
В других аспектах R1 и R2 представляют собой концевые разветвленные группы, на основе бицина, более подробно описанные ниже, дающие возможность многочисленным ветвлениям полимерных цепей; R3-R10, и R24-25 каждый представляет собой водород; a, b, c, d, f, m, n, o и p каждый предпочтительно равны 1;
e предпочтительно равно 0 или 1;
Z представляет собой , как определено выше, или, альтернативно, Z содержит аминокислотный остаток, пептидный остаток, группу, активно транспортируемую в клетку-мишень, гидрофобную или обладающую комбинацией таких свойств, так, что при объединении с биологически активными A группами, образуются пролекарства, которые высвобождаются из бициновой полимерной части формул (I), (II), и т.д. Также смотри общедоступный USSN 09/758,993, содержание которого включено здесь в качестве ссылки.
B. ПО СУЩЕСТВУ НЕАНТИГЕННЫЕ ПОЛИМЕРЫ
Как указано выше, R1 и R2 каждый предпочтительно является водорастворимым полимерным остатком, которые предпочтительно являются по существу неантигенными, такие как полиалкиленоксиды (ПАО) и, более предпочтительно, полиэтиленгликоли, такие как mПЭГ. С целью иллюстрации, а не для ограничения, остаточные части R1 и R2, содержащие полиэтиленгликоль, могут быть выбраны из:
J-О-(CH2CH2О)x-,
J-О-(CH2CH2О)x-CH2C(О)-О-,
J-O-(CH2CH2O)Х-CH2CH2NR12-,
J-O-(CH2CH2O)Х-CH2CH2SH-,
-OC(О)CH2-О-(CH2CH20)x-CH2C(О)-О-,
-NR12CH2CH2-О-(CH2CH2О)x-CH2CH2NR12- и
-SHCH2CH2-О-(CH2CH2О)x-CH2CH2SH-.
где x означает степень полимеризации;
R12 выбран из водорода, C1-6 алкилов, C2-6 алкенилов, C2-6 алкинилов, C3-12 разветвленных алкилов, C3-8 циклоалкилов, C1-6 замещенных алкилов, C2-6 замещенных алкенилов, C2-6 замещенных алкинилов, C3-8 замещенных циклоалкилов, арилов, замещенных арилов, аралкилов, C1-6 гетероалкилов, замещенных C1-6гетероалкилов, C1-6 алкокси, фенокси и C1-6гетероалкокси, и J представляет собой кэп-группировку, описанную выше в отношении формулы II.
В одном особенно предпочтительном варианте осуществления, R1-2 выбраны из CH3-О-(CH2CH2О)x-, CH3-О-(CH2CH2О)x-CH2C(О)-О-, CH3 О-(CH2CH2О)x-CH2CH2NH- и CH3-О-(CH2CH2О)x-CH2CH2SH-, где x представляет собой положительное целое число, предпочтительно выбранное таким образом, что средняя молекулярная масса составляет от примерно 2000 до примерно 25000 Да. В альтернативных аспектах данного изобретения, молекулярная масса полимера находится в пределах от нескольких сотен до 40000 или более, в зависимости от требований специалиста. ПЭГ главным образом представлен структурой: -О-(CH2CH2О)х-,
а R1 и R2 предпочтительно содержат остатки этой формулы.
Степень полимеризации для полимера (x) может составлять от примерно 10 до примерно 2300. Представляет число повторяющихся единиц в полимерной серии и зависит от молекулярной массы полимера. Часть молекулы (J) представляет собой кэпгруппировку, описанную выше, т.е. группу, которая находится на конце полимера, и, в некоторых аспектах, может быть выбрана любая из NH2, OH, SH, CO2H, C1-6 алкилов или других концевых активирующих групп ПЭГ, известных специалистам в данной области.
Также подходят полипропиленгликоли, разветвленные производные ПЭГ, описанные в общедоступном патенте США № 5643575 (патент '575), «звездчатые-ПЭГ» и многолучевые ПЭГ, описанные в каталоге «Polyethylene Glycol and Derivatives for Biomedical Application», Shearwater Corporation, 2001. Описание любого изложенного ниже включено здесь в качестве ссылки. Ветвление, представленное в патенте '575, дает вторичное или третичное ветвление от бициновой группы, как способ увеличения загрузки полимера биологически активной молекулой или ферментом из одной точки присоединения. Будет понятно, что водорастворимый полимер может быть функционально активирован для присоединения к бифункциональным связующим группам, если требуется, без лишних экспериментальных работ.
Хотя ПАО и ПЭГ могут существенно различаться по средней молекулярной массе, предпочтительно, R1 и R2 каждый имеет среднюю молекулярную массу от примерно 2000 до примерно 25000 Да в большинстве аспектов данного изобретения.
Включенные здесь полимерные вещества предпочтительно растворимы в воде при комнатной температуре. Не ограничивающий перечень таких полимеров включает в себя полиалкиленоксидные гомополимеры, такие как полиэтиленгликоль (ПЭГ), или полипропиленгликоли, полиоксиэтиленированные полиолы, их сополимеры и их блок-сополимеры, при условии, что сохраняется водорастворимость этих блок-сополимеров.
Еще в одном варианте осуществления и в качестве альтернативы полимерам, основанным на ПАО, R1 и R2 каждый необязательно выбран из одного или нескольких по сути неантигенных веществ, таких как декстран, поливиниловые спирты, полимеры на основе углеводов, гидроксипропилметакриламида (HPMA), полиалкиленоксидов, и/или их сополимеров. Смотри также общедоступный патент США № 6153655, содержание которого включено здесь в качестве ссылки. Специалистам в данной области будет понятно, что используют один и тот же тип активации, описанный здесь как для ПАО, так и для ПЭГ. Специалистам в данной области также понятно, что приведенный выше перечень является только иллюстрирующим, и что рассматриваются все полимерные вещества, обладающие описанными здесь свойствами, и что также рассматриваются другие производные полиалкиленоксида, такие как полипропиленгликоли, и т.д.
Полимеры по настоящему изобретению также могут быть сополимеризованы с бифункциональными веществами, такими как поли(алкиленгликоль)диамины, для получения взаимопроникающих полимерных сетей, подходящих для использования в проницаемых контактных линзах, раневых повязках, устройствах для доставки лекарственных средств и подобном. Пространственные ограничения и водорастворимость таких разветвлений могут быть легко определены специалистами в данной области. Предпочтительно, однако, чтобы молекулярная масса полимеров с множественным ветвлением не превышала 80000 дальтон.
C. БИФУНКЦИОНАЛЬНЫЕ МОСТИКОВЫЕ ГРУППЫ: L1, L2, L3 и L4
Во многих аспектах данного изобретения и, в частности, в формуле (I), L1, L2, L3 и/или L4 представляют собой мостиковые группы, которые облегчают присоединение бицинового производного к полимерным цепям, например, R1 и/или R2. Получаемое соединение может быть либо прямым, либо осуществляться через дополнительные соединяющие группы, известные специалистам в данной области. В описании упомянуты другие Lх группы, и понятно, что они могут быть выбраны из тех же групп, что и L1. В этом аспекте данного изобретения, L1 и L2 могут быть одинаковыми или различными, и выбраны из:
-NR19(CR14R15)tO-
-NR19(CR14R15)t(CR16CR17О)qNR19-
-О(CR14R15)tNR19-
-О(CR14R15)tO-
-NR19(CR14R15)tNR19-
-NR19(CR14R15)t(CR16CR17О)q-
-NR19(CR16CR17O)t-
-NR19(CR16CR17О)t(CR14R15)qNR19-
-NR19(CR16CR17О)t-
-O(CR14R15)t-NR19-
-O(CR14R15)tNR19-
-O(CR14R15)tO-
-O(CR16CR17O)tNR19-
где R14-R17 и R19 независимо выбраны из группы, состоящей из водорода, C1-6 алкилов, C2-6 алкенилов, C2-6 алкинилов, C3-19 разветвленных алкилов, C3-8 циклоалкилов, C1-6 замещенных алкилов, C2-6 замещенных алкенилов, C2-6 замещенных алкинилов, C3-8 замещенных циклоалкилов, арилов, замещенных арилов, аралкилов, C1 6гетероалкилов, замещенных C1-6гетероалкилов, C1-6алкокси, фенокси и C1-6гетероалкокси; и
R18 выбран из группы, состоящей из водорода, C1-6 алкилов, C2-6 алкенилов, C2-6 алкинилов, C3-19 разветвленных алкилов, C3-8 циклоалкилов, C1-6 замещенных алкилов, C2-6 замещенных алкенилов, C2-6 замещенных алкинилов, C3-8 замещенных циклоалкилов, арилов, замещенных арилов, аралкилов, C1-6 гетероалкилов, замещенных C1-6 гетероалкилов, C1-6алкокси, фенокси и C1-6 гетероалкокси, NO2, галоалкила и галогена; и
t и q каждые представляют отдельно выбранные положительные целые числа, предпочтительно от примерно 1 до примерно 4.
В других аспектах данного изобретения L1 и/или L2 могут включать в себя аминокислотный остаток. Аминокислота может быть выбрана из любых известных природных L-аминокислот, например, аланина, валина, лейцина, изолейцина, глицина, серина, треонина, метионина, цистеина, фенилаланина, тирозина, триптофана, аспарагиновой кислоты, глутаминовой кислоты, лизина, аргинина, гистидина, пролина и/или их комбинаций, нескольких, без конкретного указания. В тех случаях, когда L1 и/или L2 включают в себя пептид, размеры данного пептида находятся в пределах от примерно 2 до примерно 10 аминокислотных остатков. В другом предпочтительном варианте осуществления данным пептидом является Gly-Phe-Leu-Gly.
Аминокислотные остатки предпочтительно имеют формулу
где X' представляет собой O, S или NR26, Y5 представляет собой О, S или NR27, а R26, R27 и R28 независимо выбраны из той же группы, которая определяет R3, но каждый предпочтительно представляет собой H или низший алкил (т.е. C1-6 алкил); и f представляет собой положительное целое число от примерно 1 до примерно 10, предпочтительно 1.
Производные и аналоги природных аминокислот, а также различные известные в данной области неприродные аминокислоты (D или L), гидрофобные или не гидрофобные, также входят в объем данного изобретения. Только для примера, аналоги аминокислот и производные включают в себя: 2-амино-адипиновую кислоту, 3-аминоадипиновую кислоту, бета-аланин, бета-аминопропионовую кислоту, 2-аминомасляную кислоту, 4-аминомасляную кислоту, пиперидиновую кислоту, 6-аминокапроновую кислоту, 2-аминогептановую кислоту, 2-аминоизомасляную кислоту, 3-аминоизомасляную кислоту, 2-аминопимелиновую кислоту, 2,4-аминомасляную кислоту, десмозин, 2,2-диаминопимелиновую кислоту, 2,3-диаминопропионовую кислоту, н-этилглицин, N-этиласпарагин, 3-гидроксипролин, 4-гидроксипролин, изодесмозин, алло-изолейцин, N-метилглицин, саркозин, N-метилизолейцин, 6-N-метил-лизин, N-метилвалин, норвалин, норлейцин, орнитин и другие, которых слишком много, чтобы упоминать, перечисленные в 63 Федеральном регистре (Fed. Reg.), 29620, 29622, включенные здесь в качестве ссылки.
Например, короткими пептидами являются пептиды, в диапазоне от 2 до примерно 10 или более аминокислотных остатков, упомянутых выше.
Более предпочтительно, L1 и L2 могут быть одинаковыми или различными и выбраны из:
-NH(CH2CH2)2О-
-NH(CH2CH2)(CH2CH2O)NH-
-O(CH2CH2)NH-
-O(CH2CH2)O-
-NH(CH2CH2)NH-
-NH(CH2CH2)(CH2CH2O)-
-NH(CH2CH2O)-
-NH(CH2CH2O)(CH2)NH-
-NH(CH2CH2O)2-
-O(CH2)3NH-
-O(CH2)3O-
-O(CH2CH2O)2NH-
В другом варианте осуществления данного изобретения L3 и L4 могут быть одинаковыми или различными, и выбраны из:
-C(О)CR30R31OCR32R33C(О)-;
-C(О)CR30R31NR34CR32R33C(О)-;
-C(O)CR30R31SCR32R33C(O)-, или
-C(О)(CR30R31)nC(О)-;
где R30-34 независимо выбраны из H, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C1-6 гетероалкила или арила, и
n представляет собой положительное целое число, предпочтительно примерно от 2 до 3.
Предпочтительно, L3 и L4 выбраны из
-C(О)CH2OCH2C(О)-;
-C(О)CH2NHCH2C(О)-;
-C(О)CH2SCH2C(О)-;
-C(О)CH2CH2CH2C(О)-, или
-C(О)CH2CH2C(О)-.
Основным преимуществом данного изобретения является то, что специалист может контролировать скорость гидролиза или высвобождения биологически активной части молекулы или лекарственного средства из полимерной бициновой платформы. В зависимости от выбранных специфических линкеров, специалист в данной области может модифицировать соединения для управления скоростью гидролиза. Этот предпочтительный аспект изобретения позволяет специалисту регулировать скорость, с которой биологически активная часть молекулы доставляется в намеченную мишень. В тех ситуациях, в которых было бы желательно быстрое высвобождение биологической части молекулы или лекарственного средства, включение линкеров L3 и L4 обеспечивает более высокую скорость гидролиза. Напротив, для прежних полимерных платформ на основе бицина, описанных в общедоступной патентной заявке США 10/218,167, где высвобождение данной части молекулы или лекарственного средства из указанной платформы зачастую зависит от условий, таких как pH, или присутствия ферментов, линкеры L3 и L4 благодаря нехимерному взаимодействию, способны значительно увеличить скорость, при которой биологически активная часть молекулы или лекарственное средство высвобождается из полимерной платформы независимо от условий рН или присутствия или отсутствия ферментов. В присутствии ферментов, однако, скорость гидролиза будет контролироваться либо нехимерным взаимодействием, когда возможно, либо ферментативными реакциями, которые в любом случае протекают быстрее. Таким образом, скорость гидролиза в высокой степени зависит от типа линкеров, используемых между самой бициновой частью молекулы и ПЭГ-частью. Таким образом, данное изобретение позволяет использовать и постоянные, и высвобождаемые линкеры на любой ветви бициновой части молекулы, при условии, что, по меньшей мере, одна из ветвей включает в себя высвобождаемые части линкеров L1-L3 или L2-L4.
D. Z ЧАСТИ МОЛЕКУЛЫ И ИХ ФУНКЦИЯ
В одном аспекте данного изобретения Z представляет собой L5-C(=Y4), где L5 представляет собой бифункциональный линкер, выбранный из группы, которая характеризует L1 и L2, и Y4 выбран из тех же групп, которые характеризуют Y1-3. В этом аспекте данного изобретения группа Z служит в качестве мостика между группой А и остатком бициновой транспортной формы.
В других аспектах данного изобретения Z представляет собой часть молекулы, которая активно транспортируется в клетку-мишень, гидрофобную часть молекулы и их комбинации. Хотя Z предпочтительно является моновалентным, необязательно Z может быть бивалентным или мультивалентным, так, что дает возможность присоединения более чем одной А группы к полимеру на основе бицина. Для достижения активного переноса Z может включать в себя аминокислоту, пептидный остаток или остаток полиамина, например, любой из описанных выше в отношении L1 и L2, остаток сахара, остаток жирной кислоты, C6-18 алкил, замещенный арил, гетероарил, -C(=О), -C(=S) или -C(=NR29), где R29 представляет собой H, низший алкил, и т.д.
Этот аспект данного изобретения в широком смысле основан на том принципе, что биологически активные вещества, подходящие для включения в конъюгаты лекарственного средства с полимером на основе бицина, сами могут быть веществами/соединениями, которые не являются активными после гидролитического высвобождения из композиции, соединенной с бицином, но которые станут активными после прохождения дальнейшего химического процесса/реакции. В этом варианте осуществления терапевтический или диагностический агент, пептид, полипептид и т.д., который доставляется в кровоток посредством полимерной системы на основе бицина, будет оставаться неактивным до проникновения или до активного переноса в интересующую клетку-мишень, где он активируется химическими процессами, протекающими внутри клетки, например ферментом или ферментативной системой, присутствующей в этой ткани или клетке.
Пролекарства по данному аспекту изобретения изготовляют таким образом, что гидролиз полимерного конъюгата на основе бицина, протекающий in vivo, расщепляет конъюгат с высвобождением активного биологического вещества (здесь обозначенного «А») во внеклеточную жидкость, оставаясь связанным с Z-частью. Биологически активные вещества в данном аспекте изобретения предпочтительно, но не исключительно, представляют собой терапевтические и/или диагностические агенты с небольшой молекулярной массой. Например, одна возможная комбинация Z-A представляет собой лейцин-доксорубацин, другая комбинация представляет собой связанный с аминокислотой камптотецин или паклитаксел, а ткань, подвергаемая лечению, представляет собой опухолевую ткань.
Не привязываясь к какой-либо теории или гипотезе, как может работать данное изобретение, считается, что в зависимости от дополнительной части молекулы, выбранной в качестве усилителя переноса, скорость транспорта биологически активного вещества в опухолевые клетки представляется доставкой биологически активного вещества во внеклеточное пространство ткани, например ткани, демонстрирующей эффект EPR, в защищенной форме и/или в форме ускоренного переноса.
Еще в одном варианте усилитель переноса (Z) выбран из известных веществ для транспортной системы клеточных мембран. Только для примера, известно, что клетки активно переносят некоторые питательные вещества и эндокринные факторы, и подобное, и такие питательные вещества, или их аналоги, охотно используют для усиления активного транспорта биологически эффективных веществ в клетки-мишени. Примеры таких питательных веществ включают в себя аминокислотные остатки, пептиды, например короткие пептиды, размер которых находится в пределе от примерно 2 до примерно 10 остатков, или более, простые сахара и жирные кислоты, эндокринные факторы и подобное.
Короткими пептидами, например, являются пептиды в диапазоне от 2 до примерно 10, или более, аминокислотных остатков, как упомянуто выше.В данном варианте осуществления изобретения считается, что таким пептидным ускорителям переноса не нужно быть гидрофобными, но полагают, что они действуют другими путями для усиления захвата и/или защиты соединенных агентов небольшой молекулярной массой от преждевременного гидролиза в системном кровотоке. Например, полагают, что пептидные ускорители переноса, например, такие как, полиаргинин, и другие ускорители переноса сходной молекулярной массы, пространственно препятствуют отщеплению биологически активного агента гидролитическими ферментами п