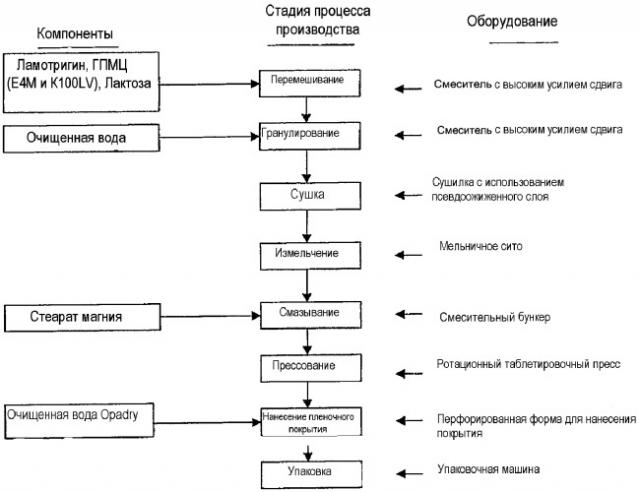
Композиции с пролонгированным высвобождением, включающие ламотригин
Иллюстрации
Показать всеИзобретение относится к медицине и касается композиции ламотригина или его фармацевтически приемлемого производного с пролонгированным высвобождением. Композиция включает: 1) ядро, содержащее ламотригин или его фармацевтически приемлемое производное; 2) окружающее ядро наружное покрытие, толщина которого подобрана так, что оно по существу непроницаемо для поступления через него жидкости из окружающей среды и по существу непроницаемо для выхода ламотригина или его фармацевтически приемлемого производного, и 3) указанное наружное покрытие имеет одно или несколько отверстий, простирающихся от внешней стороны покрытия по существу через все покрытие, но не проникающих в указанное ядро, что позволяет осуществлять высвобождение ламотригина или его фармацевтически приемлемого производного из ядра в жидкость окружающей среды. Указанные отверстия имеют площадь или объединенную площадь от примерно 10 до примерно 60% от площади лицевой поверхности формы указанной композиции. При этом высвобождение ламотригина или его фармацевтически приемлемого производного осуществляется по существу через указанное отверстие. Причем наружное покрытие растворяется в том случае, когда рН окружающей среды превышает 5. Композиция обеспечивает пролонгированное высвобождение ламотригина посредством двух механизмов: более медленное за счет начального высвобождения ламотригина через отверстие и более быстрое - в последующей фазе за счет растворения наружного покрытия. Это позволяет устранить побочные эффекты терапии ламотригином или его фармацевтически приемлемыми производными. 4 з.п. ф-лы, 7 ил., 9 табл.
Реферат
Настоящее изобретение относится к новому способу лечения с использованием ламотригина и к новым композициям, в частности, к таблеточным композициям, используемым в рамках таких способов.
Ламотригин, или 3,5-диамино-6-(2,3-дихлорфенил)-1,2,4-триазин, описан в патентах US 4602017 и ЕР 0021121. Продукты, содержащие ламотригин, продаются под торговой маркой ЛамикталТМ (LamictalTM) (группа компаний ГлаксоСмитКляйн (GlaxoSmithKline)). Такие продукты особенно эффективны при лечении расстройств ЦНС, в частности, эпилепсии, болевого синдрома, отеков, рассеянного склероза, а также в случае их применения по психиатрическим показаниям, включая биполярное расстройство.
На фармацевтическом рынке имеются различные таблеточные композиции ламотригина, разрешенные для применения, например, обычные прессованные таблетки с немедленным высвобождением (НВ), включающие 25 мг, 50 мг, 100 мг, 150 мг или 200 мг активного ингредиента. Указанные формы вводятся один, два или три раза в день. В том случае, когда ламотригин добавляют к курсу лечения противоэпилептическими препаратами, включающими вальпроевую кислоту, титрование дозы начинают с дозы 25 мг, принимаемой через день в течение 1 и 2 недель, и затем повышают дозу до приема по 25 мг каждый день в течение 3 и 4 недели. После завершения указанного начального периода может быть достигнута поддерживающая доза от 100 до 400 мг путем повышения принимаемой дозы на 25-50 мг/день. Если ламотригин добавляют к противоэпилептическим препаратам, индуцирующим ферментативную активность (EIAEDS), без вальпроевой кислоты, указанная доза составляет 50 мг/день в течение 1 и 2 недели и далее по 100 мг/день при разделении дозы на два приема. Для достижения поддерживающей дозы 300-500 мг/день при разделении ее на два приема указанные дозы можно повышать по 100 мг/день каждые 1-2 недели. Указанный режим приема обеспечивает терапевтическое количество ламотригина.
Дополнительно, в WO 92/13527 (The Wellcome Foundation Limited) описываются таблеточные композиции, включающие диспергируемые в воде таблетки, включающие ламотригин и диспергирующее средство, где указанное диспергирующее средство представляет собой способную к набуханию глину, такую как смектит, которая в основном присутствует внутри гранул таблетки для придания таблетке способности диспергироваться в воде в течение 3 минут, что обеспечивает дисперсию, которая будет проходить через сито с порами размером 710 мкм. Данная таблетка может необязательно иметь пленочную оболочку, и в этом случае время диспергирования будет составлять менее чем 5 минут. На фармацевтическом рынке имеются также жевательные таблетки, которые могут быть проглочены полностью, разжеваны или диспергированы в небольшом количестве воды, включающие 2 мг, 5 мг, 25 мг или 100 мг активного ингредиента. Указанные формы обычно вводят пациентам детского возраста.
В WO 96/17611 (The Wellcome Foundation Limited) описываются фармацевтические композиции, включающие:
а) от 0,5 до 50 мас.% ламотригина;
b) от 15 до 50 мас.% лактозы;
с) от 15 до 50 мас.% крахмала;
d) от 0,5 до 50 мас.% кристаллической целлюлозы и
е) от 5 до 15 мас.% поливинилпирролидона;
и которые имеют вид свободно текучего порошка, обладающего следующими свойствами:
(i) отсутствуют гранулы с размером частиц более чем 850 мкм,
(ii) по меньшей мере 90 мас.% имеют размер частиц от 75 до 850 мкм,
(iii) гранулы дезинтегрируются в течение 30 минут при анализе в рамках теста на дезинтеграцию Японской Фармакопеи, 12 издание и
(iv) по меньшей мере 90 мас.% ламотригина растворяется в течение 30 минут при анализе в рамках теста на растворение Японской Фармакопеи, методика 2 (методика с использованием лопастной мешалки), 12 издание 1991 года.
Ламотригин быстро и полностью всасывается после перорального приема при незначительном пресистемном метаболизме. Абсолютная биодоступность составляет примерно 98%, на которую не оказывает воздействие прием пищи.
Было показано, что жевательные диспергируемые таблетки эквивалентны в отношении скорости и уровня всасывания прессованным НВ таблеткам ламотригина, независимо от того, как они вводятся: в диспергированном в воде состоянии, разжевываются с последующим проглатыванием, или проглатываются целиком.
Другие доступные на фармацевтическом рынке лекарственные препараты, применяемые для лечения эпилепсии, включают, но не ограничиваются только ими, карбамазепин (ТегретолТМ (TegretolTM)), вальпроат (ДепакотТМ (DepakoteTM)), тиагабин (ГабитрилТМ (GabitrilTM)), леветирацетам (КеппраТМ (KeppraTM)), габапентин (НейронтинTM (NeurontinTM)) и фенитоин (ДилантинТМ (DilantinTM)). Карбамазепин доступен в виде таблеток с немедленным высвобождением, жевательных таблеток с пролонгированным высвобождением (Карбатрол (Carbatrol), шарики с длительным высвобождением) или таблеток Тегретол-XR в виде таблетки-осмотического насоса и жидкости для приема через рот. Вальпроат доступен в виде таблеток и суспензии с немедленным высвобождением. В США вальпроат доступен также в виде таблеток (с покрытием) Депакот с замедленным высвобождением, которые содержат композицию вальпроата натрия и вальпроата в соотношении 1:1, и Депакот ER в форме пролонгированного действия. Габапентин, тиагабин и леветирацетам доступны в виде таблеток с немедленным высвобождением. Дилантин доступен в форме капсул «капсил» ("kapseal"), которые модифицируют высвобождение.
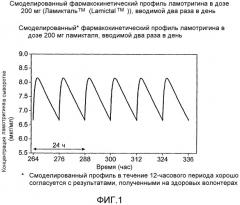
Имеющиеся на фармацевтическом рынке таблеточные композиции ламотригина обеспечивают немедленное высвобождение активных ингредиентов при поступлении таблетки в желудок. Пиковые концентрации в плазме достигаются в период времени от 1,4 до 4,8 часов после введения лекарственного средства. Недостаток заключается в том, что достигаемая при использовании таких традиционных таблеток создаваемая в плазме концентрация (фармакокинетический профиль (ФК)) характеризуется цикличностью, в соответствии с которой за пиками, достигаемыми после введения, следуют спады, предшествующие следующему введению лекарственного средства (см. фиг.1).
В частности, высказывалось предположение, что при лечении эпилепсии указанные спады в концентрации могут приводить к развитию некоторых побочных реакций (ПР), отмечаемых у некоторых пациентов, или, альтернативно, скорость повышения концентрации в плазме на начальных стадиях перед достижением пиковой концентрации в плазме может также воздействовать на ФК профиль.
До последнего времени не было известно, на каком участке желудочно-кишечного тракта происходит всасывание ламотригина. Недавно в результате изучения регионарного всасывания было обнаружено, что уровень всасывания ламотригина является одинаковым при доставке данного лекарственного средства в любую точку желудочно-кишечного тракта на участке между желудком и восходящей ободочной кишкой. В том случае, когда лекарственное средство доставляется в виде твердого вещества или раствора, всасывание происходит также на эквивалентном уровне.
Соответственно, в первом аспекте настоящее изобретение относится к композиции ламотригина с пролонгированным высвобождением или его фармацевтически приемлемого производного.
Другой аспект настоящего изобретения относится к способу лечения расстройств ЦНС, который включает пероральное введение пациенту терапевтически эффективного количества ламотригина или его фармацевтически приемлемого производного в форме композиции с пролонгированным высвобождением.
Другой аспект настоящего изобретения относится к способу лечения расстройств ЦНС, который включает пероральное введение пациенту терапевтически эффективного количества ламотригина или его фармацевтически приемлемого производного в форме композиции с пролонгированным высвобождением, в соответствии с которым ламотригин или его фармацевтически приемлемое производное высвобождается в течение примерно 2-20 часов после введения, предпочтительно, в течение 6-16 часов после введения, более предпочтительно, в течение 10-15 часов и, альтернативно, в течение 10-14 часов после введения.
Термин «расстройство ЦНС» в контексте настоящего описания включает эпилепсию, болевой синдром, отек, рассеянный склероз, шизофрению и психиатрические состояния, включающие биполярное расстройство, предпочтительно, эпилепсию, болевой синдром, отек, рассеянный склероз, шизофрению и психиатрические состояния, включающие биполярное расстройство, в особенности, эпилепсию, болевой синдром и биполярное расстройство.
Термин «болевой синдром» в контексте настоящего описания включает острую боль, такую как скелетно-мышечная боль, послеоперационную боль и хирургическую боль, хроническую боль, такую как боль при хроническом воспалении (например, боль при ревматоидном артрите и остеоартрите), невропатическую боль (например, постгерпетическую невралгию, тригеминальную невралгию, симпатически поддерживаемую боль и боль, связанную с диабетической невропатией) и боль, связанную с раком и фибромиалгией, или боль, связанную с мигренью.
Шизофрения представляет собой серьезное психическое заболевание, которое поражает 1% населения мира. Начало заболевания приходится в типичном случае на позднюю фазу возраста тинейджеров или на раннюю фазу третьего десятилетия жизни и примерно в 80% случаев становится состоянием, охватывающим всю жизнь. Кроме того, шизофрения связана со значительным уровнем смертности, поскольку 40% пациентов предпринимают попытки суицида в первые 10 лет развития заболевания. Указанное нарушение считается 5-й ведущей причиной потери трудоспособности в США, как следует из результатов совместного исследования Всемирной Организации Здравоохранения - Всемирного Банка, проведенного в 1996 г. (Murray and Lopez, 1996).
Клиническое проявление шизофрении может включать позитивные симптомы, такие как галлюцинации, бред или нарушение мышления, а также негативные симптомы, такие как апатия, безволие или бедность речи.
Лечение шизофрении основывается на использовании антидопаминергических лекарственных средств, которое последовало за открытием в 1950-х годах эффективности и механизма действия хлорпромазина. Хлорпромазин и другие так называемые "типичные" антипсихотические средства все еще широко используются в настоящее время, хотя из-за их связи с моторно-двигательными побочными реакциями, они все больше заменяются новыми "атипичными" антипсихотическими средствами, таким как клозапин (КлозарилТМ (ClozarilTM)), оланзапин (ЗипрексаTM (ZiprexaTM)) или рисперидон (РиспердалТМ (RisperdalTM)). Указанные новые лекарственные средства имеют смешанную фармакологию, которая включает антагонизм в отношении D2 допаминового рецептора и антагонизм в отношении 5-НТ2а рецептора. Несмотря на эффективность и относительную безопасность указанных новых лекарственных средств, значительная часть пациентов не реагирует на лечение, а среди тех, кто реагирует, у многих не удается достичь клинически значимого улучшения в плане общего функционирования и качества жизни.
У некоторых пациентов приступы большой депрессии, маний или смешанных маний могут иметь место параллельно с симптомами шизофрении. В этой связи, различие между шизофренией и расстройством настроения несколько расплывчаты и обычно для диагноза используют термин шизоаффективное расстройство. Для лечения шизоаффективного расстройства в типичном случае требуется сочетание антипсихотических средств, антидепрессантов, стабилизаторов настроения и анксиолитиков. В то время как позитивные психотические симптомы обычно могут контролироваться, негативные симптомы и аффективные симптомы с трудом поддаются контролю имеющимися лекарственными средствами.
Несмотря на 40-летний период развития препаратов соответствующего действия, все еще имеется неудовлетворенная потребность в лечении пациентов с хронической шизофренией по типу истощающего расстройства.
Рассеянный склероз (РС) относится к аутоиммунному заболеванию, представляющему собой прогрессирующее заболевание центральной нервной системы (ЦНС), при котором отложения миелина (представляющие защитное покрытие нервных волокон) в головном мозге и позвоночнике разрушаются под действием собственной иммунной системы организма. Указанное разрушение ведет к рубцеванию и поражению лежащих ниже нервных волокон, что может проявляться в виде множества симптомов, в зависимости от того, какие части головного мозга или позвоночника поражены. Поражение позвоночника может приводить к покалыванию или онемению, а также к чувству тяжести и/или слабости в конечностях. Повреждение в области головного мозга может приводить к мышечной слабости, утомляемости, изменениям веса, онемению, невнятности речи, нарушению зрения, головокружению и т.п. Линдри с соавт. (Leandri et al., J Neurool (2000) 247:556-558)) сообщили об использовании ламотригина при лечении тригеминальной невралгии, вторичной по отношению к рассеянному склерозу.
Другой аспект настоящего изобретения относится к применению ламотригина или его фармацевтически приемлемого производного при лечении рассеянного склероза.
Еще один аспект настоящего изобретения относится к способу лечения рассеянного склероза, который включает пероральное введение пациенту терапевтически эффективного количества ламотригина или его фармацевтически приемлемого производного.
Другой аспект настоящего изобретения относится к применению ламотригина или его фармацевтически приемлемого производного в производстве лекарственного средства, пригодного для лечения рассеянного склероза.
Термин "фармацевтически приемлемое производное" в контексте настоящего описания обозначает соль, сложный эфир или соль такого сложного эфира, которые при введении в организм реципиента, такого как человек, способны обеспечивать (прямо или опосредованно) ламотригин или его активный метаболит. Предпочтительными солями являются соли неорганической кислоты, такие как гидрохлорид, гидробромид, фосфат, или соли органической кислоты, такие как ацетат, фумарат, ксинафоат, тартрат, сукцинат или глютарат.
Термин "лечение" в контексте настоящего описания включает лечение установленных расстройств, а также включает их профилактику. Указанное особенно справедливо в отношении эпилепсии, когда лекарственный препарат может использоваться как для лечения эпилептических припадков, так и для предупреждения развития таких припадков в будущем.
В контексте настоящего описания термин "пролонгированное высвобождение" относится к постепенному, но непрерывному высвобождению в течение какого-то длительного периода времени ламотригина после перорального проглатывания, например, через 2-20 часов, предпочтительно, в период времени от 6 до 16 часов, и, более предпочтительно, в период времени от 10 до 15 часов, альтернативно, от 10 до 14 часов, и которое начинается, как только композиция попадает в желудок и начинает дезинтегрироваться/растворяться/разрушаться. Высвобождение будет продолжаться в течение некоторого периода времени и может продолжаться в тонком кишечнике и после того, как композиция поступит в толстую кишку.
Другой аспект настоящего изобретения относится к способу лечения расстройств ЦНС, который включает пероральное введение пациенту терапевтически эффективного количества ламотригина в форме композиции с пролонгированным высвобождением, в соответствии с которым по существу весь ламотригин высвобождается из композиции в течение 2-20 часов после введения, предпочтительно, в течение 6-16 часов после введения и, более предпочтительно, в течение 10-15 часов, альтернативно, в течение 10-14 часов после введения.
Другой аспект настоящего изобретения относится к композиции с пролонгированным высвобождением ламотригина или его фармацевтически приемлемого производного, где по существу весь ламотригин или его фармацевтически приемлемое производное высвобождается из композиции в течение 2-20 часов после введения, предпочтительно, в течение 6-16 часов после введения и, более предпочтительно, в течение 10-15 часов, альтернативно, в течение 10-14 часов после введения.
В контексте настоящего описания фраза "по существу весь" означает более 85%, предпочтительно, более 90%.
Введение ламотригина в течение указанного периода времени приводит к его постепенной доставке в сайты, где ламотригин быстро всасывается при медленном повышении концентраций в сыворотке и снижении пиков, возникающих после введения дозы, для ослабления связанных с приемом дозы побочных реакций (ПР), но обеспечения при этом достижения достаточных минимальных концентраций в плазме/сыворотке (Cmin) для поддержания эффективности. Композицию, которая достигает величины площади под кривой (AUC), эквивалентной величины для традиционной таблетки с быстрым/немедленным высвобождением (НВ) (90% доверительный интервал (ДИ), определяемый по методу наименьших квадратов среднегеометрических значений коэффициента (GLC), должен попадать в диапазон 80-125% относительно эталонного НВ продукта), обозначают термином "биоэквивалентная".
Альтернативно, композиция пролонгированного высвобождения не будет рассматриваться Управлением США по контролю за пищевыми продуктами и лекарственными препаратами (FDA) как биоэквивалентная НВ таблеткам, если оцениваемые точки и соответствующий им 90% доверительный интервал для Cmax не будут укладываться в диапазон 80-125% относительно НВ продукта, при том, что показатель AUC будет оставаться в пределах 80-125% сравнительно с эталонным НВ продуктом.
Композиции изготавливают соответствующим образом, так что они высвобождают активное вещество преимущественно в желудке, тонком кишечнике и в ободочной кишке.
Другой аспект настоящего изобретения относится к способу лечения расстройств ЦНС, который включает пероральное введение пациенту терапевтически эффективного количества ламотригина или его фармацевтически приемлемого производного в форме композиции с пролонгированным высвобождением, в которой ламотригин или его фармацевтически приемлемое производное присутствует в диапазоне от 1 до 500 мг, предпочтительно, от 25 до 400 мг.
Предпочтительно, композиция с пролонгированным высвобождением включает количество ламотригина или его фармацевтически приемлемого производного, выбранное из 25 мг, 50 мг, 100 мг, 200 мг или 400 мг.
Предпочтительно, композицию с пролонгированным высвобождением вводят в таком режиме дозирования, который достаточен для обеспечения контроля расстройства.
Предпочтительно, режим дозирования представляет собой ежедневное однократное введение.
Преимуществом композиций с пролонгированным высвобождением является их лучшее соблюдение пациентом режима и схемы лечения.
Социально-экономические факторы не влияют на соблюдение режима и схемы лечения: невыполнение этих условий относится как к благополучному, хорошо образованному и здоровому пациенту, так и к пациенту, который не попадает в рамки таких категорий. В большинстве случаев эпилепсия представляет собой заболевание, захватывающее длительный период жизни, которое требует поддержания непрерывных и адекватных уровней в крови антиэпилептических средств (АЭС) для достижения максимального контроля эпилептических припадков. Кроме того, в целом признано, что каждый дополнительный эпилептический припадок повышает риск рецидива и ухудшает общий прогноз. В этой связи, главной целью лечения пациентов с эпилепсией является поддержание адекватных уровней АЭС и предупреждение последующих эпилептических припадков. Соблюдение предписанного режима дозирования является обязательным условием для поддержания терапевтических уровней в крови.
Пациенты с эпилепсией часто подвергаются одновременному лечению несколькими лекарственными средствами. В случае пациентов с эпилептическими припадками или с трудно поддающейся лечению эпилепсией часто требуется совместное введение двух или более АЭС для достижения адекватного контроля эпилептических припадков. Для данных пациентов также не является необычным наличие других сопутствующих хронических медицинских показаний, таких как депрессия, проблемы с сердцем или диабет, которые также требуют соблюдения режима ежедневного введения доз лекарственных средств.
При лечении биполярного расстройства в настоящее время рекомендуется введение в режиме один раз в день, однако настоящая композиция обеспечивает замедленное повышение концентрации лекарственного средства в плазме, что, как ожидается, будет сопряжено с благоприятными эффектами для пациента.
Доступность режима однократного введения в день таблетки для лечения болевого синдрома будет существенным преимуществом, так как боль является непрерывным проявлением болезненного состояния и композиция с пролонгированным высвобождением будет обеспечивать облегчение боли за счет достижения Cmax в соответствующей точке дня или ночи, в зависимости от того, когда пациент наиболее ослаблен.
Предпочтительно, указанная композиция обеспечивает примерно от 10 до 40%, альтернативно, от 10 до 20% снижение Cmax относительно Cmax у того же пациента в случае приема им дозы НВ, вводимой один раз в день.
Предпочтительно, указанная композиция обеспечивает время достижения Cmax (tmax), составляющее от 8 до 24 часов после введения дозы, альтернативно, 10-16 часов после введения дозы.
Предпочтительно, указанная композиция обеспечивает повышение до tmax на уровне менее 50% от индивидуальной НВ дозы.
Через 24 часа после введения дозы композиция может обеспечивать достижение среднего значения минимальной концентрации в сыворотке (Cmin) на уровне, по меньшей мере равном от 80 до 125% в сравнении с той же дозой НВ композиции у того же пациента, или значения Cmin, выше, чем при введении НВ дозы, и/или значения, выходящего за пределы диапазона 80-125%, в сравнении с той же дозой НВ композиции.
Предпочтительно, композиция обеспечивает достижение показателя флуктуации (Cmax-Cmin/Cave) в диапазоне значений от 0,15 до 0,45.
В настоящее время у некоторых пациентов, при приеме традиционных НВ таблеток, отмечается развитие побочных реакций (ПР) со стороны ЦНС, таких как головокружение, атаксия, диплопия и сыпь.
При приеме НВ композиции уровень ПР составляет, например, в случае головокружения 31-38%, в случае атаксии 10-22% и в случае диплопии 24-28%. Не ограничиваясь какой-либо теорией, следует отметить, что авторы полагают, что некоторые из указанных побочных реакций имеют отношение к пиковым уровням в плазме или к скорости повышения концентрации в плазме после введения дозы и перед достижением пиковой концентрации в плазме. Риск развития сыпи, и в том числе серьезной сыпи, может определяться исходной дозой или скоростью повышения дозы ламотригина, и разработка композиции, которая бы снижала пиковый уровень в ходе титрования дозы, могла бы уменьшить риск развития указанных побочных реакций.
Другой аспект настоящего изобретения относится к способу лечения расстройств ЦНС, который включает пероральное введение пациенту терапевтически эффективного количества ламотригина или его фармацевтически приемлемого производного в форме композиции с пролонгированным высвобождением, при котором достигается снижение профиля ПР.
Предпочтительно, снижение профиля ПР представляет собой снижение уровня развития побочных реакций, по меньшей мере, одного неблагоприятного эффекта, выбранного из головокружения, атаксии, диплопии или сыпи.
Предпочтительно, снижение профиля ПР представляет собой снижение уровня развития побочных реакций, по меньшей мере, одного неблагоприятного эффекта на 10%, предпочтительно, на 20% и, более предпочтительно, на 30%.
Другой аспект настоящего изобретения относится к способу снижения частоты развития, по меньшей мере, одной побочной реакции, связанной с введением ламотригина или его фармацевтически приемлемого производного, где указанный способ включает пероральное введение пациенту терапевтически эффективного количества ламотригина или его фармацевтически приемлемого производного в форме композиции с пролонгированным высвобождением.
Предпочтительно, побочная реакция представляет собой, по меньшей мере, одну реакцию, выбранную из головокружения, атаксии, диплопии или сыпи.
Другой аспект настоящего изобретения относится к способу лечения эпилепсии, который включает пероральное введение пациенту терапевтически эффективного количества ламотригина или его фармацевтически приемлемого производного в форме композиции с пролонгированным высвобождением.
Другой аспект настоящего изобретения относится к использованию ламотригина или его фармацевтически приемлемого производного для лечения расстройств ЦНС при производстве композиции с пролонгированным высвобождением, как средства лечения эпилепсии и снижения уровня развития побочных реакций.
Другой аспект настоящего изобретения относится к применению ламотригина или его фармацевтически приемлемого производного при производстве композиции с пролонгированным высвобождением для лечения расстройств ЦНС.
Другой аспект настоящего изобретения относится к применению ламотригина или его фармацевтически приемлемого производного при производстве композиции с пролонгированным высвобождением для лечения расстройств ЦНС в соответствии с любым из приведенных в настоящем описании способов.
Другой аспект настоящего изобретения относится к применению ламотригина или его фармацевтически приемлемого производного при лечении расстройств ЦНС.
Дозировка композиции с пролонгированным высвобождением, рассчитанная для проглатывания ее целиком, где целостность дозированной формы существенна для контролирования скорости высвобождения, может быть соответствующим образом обеспечена за счет множества принимаемых внутрь таблеток или капсул, например, в количестве двух, трех или четырех. В тех случаях, когда происходит высвобождение из множества дискретных частиц, шариков или гранул, дозированную форму необязательно проглатывать в интактном виде, главное, чтобы оставались интактными сами шарики или другие такие частицы.
Дозировка композиции с пролонгированным высвобождением может быть также обеспечена за счет одной таблетки.
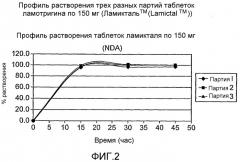
Предпочтительно, композиция с пролонгированным высвобождением по настоящему изобретению имеет профиль растворения in vitro, в соответствии с которым от 40 до 65%, предпочтительно, от 45 до 65%, более предпочтительно, от 45 до 55% от всего содержания ламотригина растворяется в течение периода времени от 3 до 8 часов, более предпочтительно, от 4 до 6 часов, и 90% ламотригина растворяется в течение периода времени от 6 до 16 часов, предпочтительно, от 10 до 15 часов, альтернативно, от 10 до 14 часов. Для сравнения можно указать, что традиционная таблетка ламотригина с немедленным высвобождением растворяется на 80% в течение 30 минут. Профиль растворения может быть измерен в рамках стандартного теста на растворение, например, Теста на растворение <724>, с использованием приборов 1 или 2 или 3, приведенного в руководстве Американской Фармакопеи USP 24, 2000 c последующими добавлениями, внесенными в текст обновленной редакции, при температуре 37,0±0,5°С с использованием разбавленной хлористоводородной кислоты или других подходящих сред (500-3000 мл) и со скоростью вращения 50-100 об/мин.
Дозировка композиции с пролонгированным высвобождением может обеспечивать in vivo достижение величины "площади под кривой" (AUC), которая эквивалентна данному параметру для имеющейся в настоящее время традиционной таблетки с немедленным высвобождением НВ, составляя, например, по меньшей мере, 80%, предпочтительно, по меньшей мере, 90%-110%, более предпочтительно, примерно 100%, но не превышая 125% от данного параметра для соответствующей дозировки ламотригина в форме традиционной (с немедленным высвобождением) композиции в течение того же периода времени, за счет чего максимизируется всасывание ламотригина из композиции с пролонгированным высвобождением.
Фармакокинетический профиль для дозировки по настоящему изобретению может быть легко определен на основе изучения биологической доступности однократной дозировки у волонтеров. Далее в образцах крови, взятых у пациентов в соответствии с известными процедурами, которые описаны в соответствующих источниках, могут быть без труда определены концентрации ламотригина в плазме.
Специалист в данной области понимает, что терапевтически эффективное количество зависит от возраста пациента, его размеров, тяжести заболевания и других медицинских показателей.
Предпочтительные композиции с пролонгированным высвобождением представляют собой функциональные таблетки или каплеты с пленочным покрытием, или матрицы таблеток или каплет с задержанным высвобождением, содержащие воск или полимер, или устройства осмотических насосов, или их сочетания. Контролируемое высвобождение может быть также достигнуто с помощью шариков, гранул, сфероидов, которые содержатся внутри капсулы или вводятся из саше или другой стандартной дозированной формы порошка.
Репрезентативные примеры композиций с пролонгированным высвобождением включают таблетки, в том числе проглатываемые таблетки, капсулы, гранулы или саше, в типичном случае проглатываемую таблетку, которая может иметь или не иметь пленочное покрытие.
Другой аспект настоящего изобретения относится к композиции, включающей ламотригин или его фармацевтически приемлемое производное и наполнитель для задержки высвобождения, который позволяет обеспечить длительное высвобождение ламотригина или его фармацевтически приемлемого производного. Подходящие наполнители для задержки высвобождения включают задерживающие высвобождение полимеры, которые могут как набухать, так и не набухать при контакте с водой или водными средами, такими как содержимое желудка; полимерные материалы, которые образуют гель при контакте с водой или водными средами; полимерные материалы, которые обладают как способностью к набуханию, так и к гелеобразованию при контакте с водой или водными средами, и полимеры, чувствительные к величине рН, например, полимеры, построенные на основе сополимеров метакриловой кислоты, такие как полимеры Эудрагит (Eudragit) (торговая марка), например, Эудрагит L (Eudragit L) (торговая марка), который может использоваться либо сам по себе, либо вместе с пластификатором.
Указанные композиции с пролонгированным высвобождением в данной области техники часто называют «матричными композициями», которые характеризуются тем, что лекарственное средство встроено в гидратированную полимерную матричную систему и которое высвобождается в процессе диффузии или разрушения, как описано, например, в WO 98/47491 и US 5242627.
Задерживающие высвобождение полимеры, которые могут или не могут набухать, включают, в том числе, сшитую натрий-карбоксиметилцеллюлозу, сшитую гидроксипропилцеллюлозу, гидроксиэтилцеллюлозу, высокомолекулярную гидроксипропилметилцеллюлозу, карбоксиметиламид, сополимер калия-метакрилатдивинилбензола, полиметилметакрилат, сшитый поливинилпирролидон, высокомолекулярные поливиниловые спирты гидроксиэтилцеллюлозы и т.п.
Гелеобразующие полимеры, задерживающие высвобождение, включают метилцеллюлозу, карбоксиметилцеллюлозу, низкомолекулярную гидроксипропилметилцеллюлозу, гидроксиэтилцеллюлозу, низкомолекулярные поливиниловые спирты, полиоксиэтиленгликоли, несшитый поливинилпирролидон, ксантановую камедь и т.п.
Задерживающие высвобождение полимеры, которые обладают одновременно способностью и к набуханию, и к гелеобразованию, включают гидроксипропилметилцеллюлозу умеренной вязкости и поливиниловые спирты умеренной вязкости.
Предпочтительно, используемый полимер, задерживающий высвобождение, имеет молекулярную массу в диапазоне от 5 до 95 тысяч, более предпочтительно, в диапазоне от 10 до 50 тысяч.
Предпочтительный полимер, задерживающий высвобождение, относится к одной из доступных марок гидроксипропилметилцеллюлозы или гидроксиэтилцеллюлозы.
Примеры полимеров, которые могут использоваться, включают Метоцель К4М (Methocel К4М) (торговая марка), Метоцель Е5М (торговая марка), Метоцель Е50 (торговая марка), Метоцель Е4М (торговая марка), Метоцель Е100М (торговая марка), Метоцель К15М (торговая марка), Метоцель К100М (торговая марка) и Метоцель К100LV (торговая марка), Полиокс WSR N-80 (POLYOX WSR N-80) или их смеси. Альтернативно, примеры полимеров, которые могут использоваться, включают Метоцель К4М (торговая марка), Метоцель Е5 (торговая марка), Метоцель Е50 (торговая марка), Метоцель Е4М (торговая марка), Метоцель К15М (торговая марка), Метоцель К100LV (торговая марка), Полиокс WSR N-80 (POLYOX WSR N-80) или их смеси.
Другие известные полимеры, задерживающие высвобождение, которые могут использоваться, включают гидроколлоиды, такие как природные или синтетические камеди, производные целлюлозы, отличные от перечисленных выше, вещества углеводной природы, такие как аравийская камедь, трагакант, камедь робинии, гуаровая камедь, агар, пектин, карагенан, растворимые и нерастворимые альгинаты, карбоксиполиметилен, казеин, зеин и т.п., а также протеионоподобные вещества, такие как желатин.
Предпочтительно, задерживающий высвобождение полимер представляет собой Метоцель Е4М, Полиокс WSR N-80 и Метоцель К100LV.
Композиция с пролонгированным высвобождением может также включать разбавители/средства, способствующие прессованию, такие как лактоза, микрокристаллическая целлюлоза, дикальцийфосфат, сахарозу, маннит, ксилит, крахмалы и замасливатели, такие как стеарат магния, стеарилфумарат натрия и стеариновая кислота. Композиция с пролонгированным высвобождением может также включать дезинтегранты такие, как сшитый поливинилпирролидон (СПВП) и натрий-крахмал-гликолят, связующие вещества, такие как повидон (поливинилпирролидон), средства, способствующие текучести, такие как диоксид кремния или тальк. В типичном случае композиция с пролонгированным высвобождением включает примерно от 2,5 до 80 мас.% ламотригина, от 0 до 70 мас.% разбавителя/средства, способствующего прессованию, и от 0,1 до 2,5 мас.% замасливателя. Предпочтительно, задерживающий высвобождение наполнитель представляет собой полимер, задерживающий высвобождение.
Предпочтительно, задерживающий высвобождение полимер присутствует в диапазоне от 10 до 70 мас.% полимера.
Предпочтительно, композиция с пролонгированным высвобождением включает от 2,5 до 80 мас.% ламотригина или его фармацевтически приемлемого производного.
Предпочтительно, композиция с пролонгированным высвобождением включает:
а) от 2,5 до 80 мас.% ламотригина или его фармацевтически приемлемого производного;
b) от 10 до 70 мас.% полимера, задерживающего высвобождение;
c) от 0 до 70 мас.% разбавителя;
d) от 0 до 20 мас.% средства, способствующего прессованию, и
e) от 0,1 до 2,5 мас.% замасливателя.
В предпочтительном варианте воплощения композиция с пролонгированным высвобождением включает:
а) от 2,5 до 80 мас.% ламотригина или его фармацевтически приемлемого производного;
b) от 17,5 до 70 мас.% полимера, задерживающего высвобождение;
c) от 0 до 60 мас.% разбавителя;
d) от 0 до 20 мас.% средства, способствующего прессованию, и
e) от 0,1 до 2,5 мас.% замасливателя.
В предпочтительном варианте воплощения композиция с пролонгированным высвобождением не содержит средства, способствующего прессованию.
Предпочтительно, композиция с пролонгированным высвобождением включает:
а) от 8,3 до 50 мас.% ламотригина или его фармацевтически приемлемого производного;
b) от 17,5 до 66,3 мас.% полимера, задерживающего высвобождение;
c) от 25 до 60 мас.% разбавителя;
d) от 0,1 до 0,4 мас.% замасливателя.
Более предпочтительно, композиция с пролонгированным высвобождением включает:
а) от 8,3 до 50 мас.% ламотригина или его фармацевтически приемлемого производного;
b) от 17,5 до 66,3 мас.% Метоцеля Е4МР, категории CR, Полиокса WSRN-80 или Метоцеля K100LV или их смеси;
c) от 25 до 60 мас.% лактозы и
d) от 0,1 до 0,4 мас.% стеарата магния.
Другой аспект настоящего изобретения относится к средству, включающему ламотригин или его фармацевтически приемлемое производное и задерживающее высвобождение покрытие, нанесенное на одну или большее число наружных поверхностей такого средства, например, таблетки или шарика. Традиционная прессова