Антагонисты соматостатина
Иллюстрации
Показать всеНастоящее изобретение относится к антагонистам соматостатина, которые используют в способе связывания одного или нескольких подтипов рецепторов соматостатина -1, -2, -3, -4 и -5 у человека или животного, способе выявления эффекта антагониста соматостатина у человека или животного, способе стимуляции высвобождения гормона роста у человека или животного, способе стимуляции высвобождения инсулина у человека или животного, способе усиления ранозаживления у человека или животного, способе стимуляции ангиогенеза у человека или животного, способе лечения заболевания или состояния у нуждающегося в этом человека или животного, где указанное заболевание или состояние выбрано из группы, состоящей из низкорослости, кахексии, истощения и диабета типа 2. 7 н.п. ф-лы, 1 ил., 3 табл.
Реферат
Предпосылки создания изобретения
Показано, что соматостатин (SRIF), тетрадекапептид, открытый Brazeau et al., обладает мощными ингибиторными эффектами в отношении различных секреторных процессов в тканях, таких как гипофиз, поджелудочная железа и желудочно-кишечный тракт. SRIF также действует как нейромодулятор в центральной нервной системе. Данные биологические эффекты SRIF, все из которых являются ингибирующими по своей природе, выявляются через ряд рецепторов, связанных с белком G, из которых охарактеризованы пять различных подтипов (sstr1-sstr5). Данные пять подтипов имеют близкие значения сродства к эндогенным лигандам SRIF, но отличаются различным распределением в разных тканях. Соматостатин связывается с пятью различными подтипами рецептора (SSTR) с относительно высоким и одинаковым сродством к каждому подтипу. Связывание с различными видами подтипов рецептора к соматостатину было соотнесено с лечением различных состояний и/или заболеваний ("sstr2") (Raynor, et al., Molecular Pharmacol. 43: 838 (1993); Lloyd, et al., Am. J.Physiol. 268:G102 (1995), в то время как ингибирование инсулина было приписано типу-5 рецептора к соматостатину ("sstr5") (Coy, et al. 197:366-371 (1993)). Активация типов 2 и 5 была соотнесена с подавлением гормона роста и, более конкретно, GH-секретирующими аденомами (Акромегалия) и TSH-секретирующими аденомами. Активация типа 2, но не типа 5 была связана с лечением пролактин-секретирующих аденом. Другими показаниями, связанными с активацией подтипов рецепторов к соматостатину, являются ингибирование инсулина и/или глюкагона для лечения сахарного диабета, ангиопатии, пролиферативной ретинопатии, феномена дауна и нефропатии; ингибирование секреции желудочной кислоты и более конкретно пептических язв, кишечно-кожного и поджелудочно-кожного свищей, синдрома раздраженной кишки, демпинг-синдрома, синдрома водянистого стула, диареи, вызываемой СПИДом, диареи, индуцированной химиотерапией, острых или хронических панкреатитов и опухолей, секретирующих желудочно-кишечный гормон; лечение рака, такого как гепатома; ингибирование ангиогенеза, лечение воспалительных расстройств, таких как артрит; ретинопатии; хроническое отторжение трансплантата; ангиопластика; профилактика пересадки сосуда и желудочно-кишечное кровотечение. Предпочтительно иметь аналог, который является селективным по отношению к специфическому подтипу или подтипам рецептора к соматостатину, отвечающим за требуемый биологический ответ, таким образом уменьшая взаимодействие с другими подтипами рецептора, которое может приводить к нежелательным побочным эффектам.
Разработка высокоактивных, меньших по размеру агонистов SRIF привела к обнаружению отличающихся значений сродства различных процессированных лигандов к различным подтипам. Является очевидным, что последовательность Trp8-Lys9 часто присутствует в лигандах, которые распознаются рецептором. Последовательность Trp8-Lys9 образует часть β-изгиба, который обычно стабилизирован посредством замены D- на L-Trp, циклизации остова, дисульфидного мостика или совокупностью ограничивающих факторов. Одним непредусмотренным последствием такого структурного упрощения, проведенного перед обнаружением множественных подтипов рецептора, была утрата широкого спектра сродства связывания. Типичным примером служит высокое сродство к типу 2, но низкое к типам 1, 3, 4 и 5 у пептидов в ряду OCTREOTIDER. Таким образом, многие фундаментальные биологические исследования с этим типом аналога для обнаружения эффектов, опосредованных всеми, но не одним, типами рецептора к соматостатину закончились неудачей. С тех пор была проведена большая работа по повторному приданию широкого спектра связывания небольшим биологически стабильным пептидам, с одной стороны, и разработке пептидов и пептидомиметиков с дискретной селективностью по отношению к конкретному рецептору.
Авторы данного изобретения обнаружили, что ограничение пептидного остова может быть введено посредством N-алкилирования индивидуальных аминокислот. Такая модификация значительно ограничивает затронутый остаток и аминокислоту, предшествующую ему, для принятия вытянутой конформации. Таким образом, дополнительно происходит блокирование потенциальных внутримолекулярных участков образования водородных связей и также участков расщепления протеолитическими ферментами, значительно улучшая фармакокинетические свойства пептида. Лишь несколько N-метиламинокислот коммерчески доступны, и их синтез является трудоемким. Однако в другом аспекте настоящего изобретения авторы обнаружили методику получения N-метилатных процессированных аналогов соматостатина по каждому аминокислотному остатку, с применением твердофазного метода, заимствованную из недавней публикации, доложенной Miller и Scanlan.
Краткое содержание изобретения
В одном аспекте настоящее изобретение направлено на пептид формулы (I),
A1-цикло{D-Cys-A2-D-Trp-A3-A4-Cys}-A5-Y1,
(I)
где
А1 представляет собой необязательно замещенную ароматическую α-аминокислоту;
А2 представляет собой необязательно замещенную ароматическую α-аминокислоту;
А3 представляет собой Dab, Dap, Lys или Orn;
А4 представляет собой β-гидроксивалин, Ser, Hser или Thr;
А5 представляет собой необязательно замещенную D- или L-ароматическую α-аминокислоту; и
Y1 представляет собой OH, NH2 или NHR1, где R1 представляет собой (С1-6)алкил;
где каждая упомянутая необязательно замещенная ароматическая α-аминокислота необязательно замещена одним или несколькими заместителями, каждый из которых независимо выбран из группы состоящей из галогена, NO2, OH, CN, (С1-6)алкила,
(C2-6)алкенила, (C2-6)алкинила, (С1-6)алкокси, Bzl, O-Bzl, и NR9R10, где каждый из R9 и R10 независимо представляет собой Н, O или
(С1-6)алкил; и
где аминный азот каждой амидной пептидной связи и аминогруппа А1 из формулы (I) необязательно замещены метильной группой, при условии, что присутствует по меньшей мере одна упомянутая метильная группа;
или его фармацевтически приемлемая соль.
В одном воплощении изобретение связано с пептидами формулы (I), где
A1 представляет собой Cpa, 1-Nal, 2-Nal, 2-Pal, 3-Pal, 4-Pal, Phe, Tfm, Tyr или Tyr (I);
A2 представляет собой 2-Pal, 3-Pal, 4-Pal, Phe, Tyr или Tyr(I); и
A5 представляет собой Dip, 1-Nal, 2-Nal, 2-Pal, 3-Pal, 4-Pal, Phe или D-Trp;
или их фармацевтически приемлемой солью.
В другом воплощении изобретение связано с пептидом из последней вышеприведенной группы пептидов, где A1 представляет собой Cpa.
В дальнейшем воплощении изобретение связано с пептидом из последней вышеприведенной группы пептидов, где А3 представляет собой NMeLys.
В дальнейшем воплощении изобретение связано с пептидом формулы (I), где упомянутый пептид представляет собой
NmeCpa-цикло(DCys-3-Pal-DTrp-Lys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(NMeDCys-3-Pal-DTrp-Lys-Thr-Cys)-2-Nal-NHMe;
Cpa-цикло(DCys-NMe3-Pal-DTrp-Lys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-3-Pal-NMeDTrp-Lys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-3-Pal-DTrp-Lys-NMeThr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-3-Pal-DTrp-Lys-Thr-NMeCys)-2-Nal-NH2;
Cpa-цикло(DCys-3-Pal-DTrp-Lys-Thr-Cys)-Nme2-Nal-NH2;
Cpa-цикло(NMeDCys-3-Pal-DTrp-Lys-Thr-Cys)-Dip-NHMe;
Cpa-цикло(DCys-3-Pal-NMeDTrp-NMeLys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-Tyr-DTrp-NMeLys-Thr-Cys)-2-Nal-NH2;
Tfm-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-DTrp-NH2;
Nal-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-DTrp-NH2; или
3-Pal-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-DTrp-NH2; или его фармацевтически приемлемой солью.
Еще в дальнейшем воплощении изобретение связано с пептидом формулы (I), где упомянутый пептид представляет собой
NmeCpa-цикло(DCys-3-Pal-DTrp-Lys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-3-Pal-NMeDTrp-NMeLys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-Tyr-DTrp-NMeLys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-DTrp-NH2;
Nal-цикло(DCys-Pal-DTrp-NMeLys-Thr-Cys)-DTrp-NH2; или
3-Pal-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-DTrp-NH2; или его фармацевтически приемлемой солью.
Еще в одном воплощении изобретение связано с пептидом формулы (I), где упомянутый пептид представляет собой
NmeCpa-цикло(DCys-3-Pal-DTrp-Lys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-3-Pal-NMeDTrp-NMeLys-Thr-Cys)-2-Nal-NH2;
Cpa-цикло(DCys-Tyr-DTrp-NMeLys-Thr-Cys)-2-Nal-NH2; или
Cpa-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-DTrp-NH2; или его фармацевтически приемлемой солью.
Еще в одном воплощении изобретение связано с пептидом формулы (I), где упомянутый пептид представляет собой:
Cpa-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-2-Nal-NH2; или
Cpa-цикло(DCys-Tyr-DTrp-NMeLys-Thr-Cys)-2-Nal-NH2;. или его фармацевтически приемлемой солью.
В другом аспекте настоящего изобретения описан способ связывания одного или нескольких подтипов рецептора к соматостатину -1, -2, -3, -4 и -5, который включает в себя стадию контакта соединения по пункту 1 или его фармацевтически приемлемой соли с одним или несколькими упомянутыми подтипами рецептора к соматостатину.
В одном воплощении вышеприведенного аспекта настоящего изобретения подразумевается способ связывания одного или нескольких подтипов рецептора к соматостатину -1, -2, -3, -4 и
-5 у человека или другого животного, который включает в себя стадию введения эффективного количества соединения по пункту 1 или его фармацевтически приемлемой соли пациенту, нуждающемуся в этом.
В другом воплощении аспекта настоящего изобретения описан способ выявления эффекта антагониста у клетки, где упомянутая клетка содержит один или несколько рецепторов к соматостатину, причем упомянутый способ включает в себя контакт упомянутой клетки с эффективным количеством соединения по пункту 1 или его фармацевтически приемлемой соли.
В другом воплощении настоящее изобретение предоставляет способ выявления эффекта антагониста соматостатина у человека или животного, который включает в себя стадию введения эффективного количества соединения по пункту 1 или его фармацевтически приемлемой соли пациенту, нуждающемуся в этом.
В дальнейшем воплощении настоящего изобретения описан способ стимулирования высвобождения гормона роста у человека или животного, который включает в себя введение упомянутому пациенту эффективного количества соединения по пункту 1 или его фармацевтически приемлемой соли.
В другом воплощении аспекта настоящего изобретения описан способ стимулирования высвобождения инсулина у человека или животного, нуждающегося в этом, который включает в себя введение упомянутому пациенту эффективного количества соединения по пункту 1 или его фармацевтически приемлемой соли.
В другом воплощении настоящего изобретения описан способ улучшения заживления ран у человека или животного, нуждающегося в этом, который включает в себя введение упомянутому пациенту эффективного количества соединения по пункту 1 или его фармацевтически приемлемой соли.
В другом воплощении настоящего изобретения описан способ стимулирования ангиогенеза у человека или животного, нуждающегося в этом, который включает в себя введение упомянутому пациенту эффективного количества соединения по пункту 1 или его фармацевтически приемлемой соли.
В другом воплощении настоящего изобретения описан способ лечения заболевания или состояния у человека или другого животного, нуждающегося в этом, который включает в себя стадию введения эффективного количества соединения по пункту 1 или его фармацевтически приемлемой соли упомянутому пациенту, где упомянутое заболевание или состояние выбирают из группы, состоящей из низкорослости, кахексии, истощения, диабетов типа 2, пониженной циркуляции и т.п.
В другом аспекте настоящего изобретения описан способ визуализации клеток, имеющих рецепторы к соматостатину, который включает в себя контакт упомянутой клетки с эффективным количеством соединения по пункту 1 или его фармацевтически приемлемой соли, которое содержит Tyr (I).
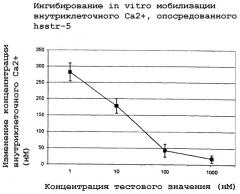
Краткое описание чертежа
Чертеж представляет собой график, показывающий ингибирование in vitro мобилизации внутриклеточного Сa2+, опосредованной hsstr-5.
Подробное описание
Специалист в данной области может на основании данного описания применять настоящее изобретение в наибольшей его полноте. Нижеследующие конкретные воплощения, следовательно, рассматриваются как простые иллюстрации изобретения, и не следует считать их ограничивающими полный объем изобретения.
Как хорошо известно специалистам в данной области, известные и потенциальные применения соматостатина разнообразны и многочисленны. Известно, что соматостатин и его аналоги применяются в лечении заболеваний и/или состояний, перечисленных ниже в настоящем документе. Разнообразные применения соматостатина могут быть обобщены следующим образом: синдром Кушинга (см. Clark, R. V. et al., Clin. Res. 38, p. 943A, 1990); гонадотропинома (см. Ambrosi B., et al., Acta Endocr. (Copenh.) 122, 569-576, 1990); гиперпаратиреоидизм (см. Miller, D., et al., Canad. Med. Ass. J., vol. 145, pp. 227-228, 1991); болезнь Пэджета (см. Palmieri, G. M. A., et al., J. of Bone and Mineral Research, 7, (Suppl. 1), p.S240 (Abs. 591), 1992); VIPома (см. Koberstein, B., et al., Z.Gastroenterology, 28, 295-301,1990 and Christensen, C., Acta Chir. Scand. 155, 541-543, 1989); незидиобластоз и гиперинсулинизм (см. Laron, Z., Israel J. Med. Sci., 26, № 1, 1-2, 1990, Wilson, D. C., Irish J. Med. Sci., 158, № 1, 31-32, 1989 и Micic, D., et al., Digestion, 16, Suppl. 1.70. Abs. 193, 1990); гастринома (см. Bauer, F. E., et al., Europ. J. Pharmacol, 183, 55 1990); синдром Золлингера-Эллисона (см. Mozell, E., et al., Surg. Gynec. Obstet., 170, 476-484, 1990); гиперсекреторная диарея, относящаяся к СПИДу и другие состояния (вследствие СПИДа, см. Cello, J. P., et al., Gastroenterology, 98, № 5, Part 2, Suppl., A163 1990; вследствие повышенного уровня гастрин-высвобождающего пептида, см. Alhindawi, R., et al., Can. J. Surg., 33, 139-142, 1990; вторичное последствие заболевания при реакции на кишечный трансплантат, см. Bianco J. A., et al., Transplantation, 49, 1194-1195, 1990; диарея, связанная с химиотерапией, см. Petrelli, N., et al., Proc. Amer. Soc. Clin. Oncol, vol. 10, p 138, Abstr. № 417 1991); синдром раздраженного кишечника (см. O'Donnell, L. J. D., et al., Aliment. Pharmacol. Therap., vol. 4, 177-181, 1990); панкреатит (см. Tulassay, Z., et al., Gastroenterology, 98, № 5, Part 2, Suppl., A238,1990); болезнь Крона (см. Fedorak, R. N., et al., Can. J. Gastroenterology, 3, № 2, 53-57,1989); системный склероз (см. Soudah, H., et al., Gastroenterology, 98, № 5, Part 2, Suppl., A129, 1990); рак щитовидной железы (см. Modigliani, E., et al., Ann., Endocr. (Paris), 50, 483-488, 1989); псориаз (см. Camisa, C., et al., Cleveland Clinic J. Med., 57 № 1,71-76, 1990); гипотензия (см. Hoeldtke, R. D., et al., Arch. Phys. Med. Rehabil., 69, 895-898, 1988 и Kooner, J. S., et al., Brit. J. Clin. Pharmacol., 28,735Р-736P, 1989); приступы паники (см. Abelson, J. L., et al., Clin. Psychopharmacol., 10, 128-132, 1990); склеродома (см. Soudah, H., et al., Clin. Res., Vol. 39, p. 303A, 1991); непроходимость тонкой кишки (см. Nott, D. M., et al., Brit. J. Surg., vol. 77, p. A691, 1990); гастроэзофагеальный рефлюкс (см. Branch, M. S., et al., Gastroenterology, vol. 100, №. 5, Part 2 Suppl., p. A425, 1991); дуоденогастральный рефлюкс (см. Hasler, W., et al., Gastroenterology, vol. 100, № 5, Part 2, Suppl., p. A448, 1991); болезнь Грэйвса (см. Chang, T. C., et al., Brit.Med. J., 304, p. 158, 1992); поликистоз яичника (см. Prelevic, G. M., et al., Metabolism Clinical and Experimental, 41, Suppl. 2, pp 76-79, 1992); верхнее желудочно-кишечное кровотечение (см. Jenkins, S. A., et al., Gut., 33, pp. 404-407, 1992 and Arrigoni, A., et al., American Journal of Gastroenterology, 87, p. 1311, (abs. 275), 1992); панкреатические псевдокисты и асциты (см. Hartley, J. E., et al., J. Roy. Soc. Med., 85, pp. 107-108, 1992); лейкемия (см. Santini, et al., 78, (Suppl. 1), p. 429A (Abs. 1708), 1991); менингиома (см. Koper, J. W., et al., J. Clin. Endocr. Metab., 74, pp. 543-547,1992); и раковая кахексия (см. Bartlett, D. L., et al., Surg. Forum., 42, pp. 14-16,1991). Содержание вышеприведенных ссылок включено в данное описание в качестве ссылки.
Пептиды согласно изобретению применимы в качестве антагонистов по отношению к активности или активностям соматостатина. Например, пептиды согласно изобретению можно применять для стимуляции высвобождения гормона роста или инсулина у пациента (например, млекопитающего, такого как пациент-человек). Таким образом, пептиды применимы для лечения физиологических состояний, при которых стимуляция высвобождения гормона роста или инсулина является благоприятным воздействием. Пептиды согласно изобретению могут также применяться для улучшения заживления ран или стимуляции ангиогенеза. Далее, пептиды согласно изобретению, имеющие остаток Tyr(I), могут применяться для визуализации клеток, содержащих рецепторы к соматостатину. Такие пептиды согласно изобретению могут применяться либо in vivo для детектирования клеток, имеющих рецепторы к соматостатину (например, раковых клеток), либо in vitro в качестве радиолиганда при определении связывания со соматостатиновым рецептором. Пептиды согласно изобретению могут также применяться в качестве векторов для мечения клеток радиоактивными изотопами.
Также в пределах объема данного изобретения рассматривают пептид, охватываемый вышеприведенной общей формулой как для лечения заболеваний или расстройств, связанных с необходимостью стимулировать высвобождение гормона роста или инсулина, так и для применения при детектировании рецепторов к соматостатину, например радиовизуализации.
Соединение формулы (I) или его фармацевтически приемлемая соль могут вводиться посредством перорального, парентерального (например, внутримышечного, внутриперитонеального, внутривенного, а также путем подкожной инъекции или имплантации), назального, вагинального, ректального, подъязычного или местного путей введения и могут быть получены вместе с фармацевтически приемлемыми носителями для обеспечения дозированных форм, пригодных для каждого пути введения.
Твердые дозированные формы для перорального введения включают в себя капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых дозированных формах активное соединение предварительно смешивают вместе по меньшей мере с одним инертным фармацевтически приемлемым носителем, таким как сахароза, лактоза или крахмал. В обычной практике такие дозированные формы могут также включать в себя дополнительные вещества, отличные от инертных разбавителей, например, смазывающие агенты, например стеарат магния. В случае капсул, таблеток и пилюль, дозированные формы могут также включать в себя забуферивающие агенты. Таблетки и пилюли могут быть дополнительно получены с энтеропокрытиями.
Жидкие дозированные формы для перорального введения включают в себя фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы, эликсиры, содержащие инертные разбавители, обычно применяемые в данной области, такие как вода. Кроме таких инертных разбавителей, композиции могут также включать в себя вспомогательные вещества, такие как увлажняющие агенты, эмульгирующие и суспендирующие агенты и подсластители, ароматизаторы и отдушки.
Препараты в соответствии с данным изобретением для парентерального введения включают в себя стерильные водные или неводные растворы, суспензии или эмульсии. Примерами неводных растворителей или сред являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло и кукурузное масло, желатин и органические сложные эфиры для инъекций, такие как этилолеат. Такие дозированные формы могут также содержать вспомогательные вещества, такие как консерванты, увлажняющие, эмульгирующие и диспергирующие агенты. Их можно стерилизовать посредством, например, фильтрации через фильтр, удерживающий бактерии, путем введения стерилизующих агентов в композиции, облучения композиций или нагревания композиций. Их можно также производить в виде стерильных твердых композиций, которые можно растворить в стерильной воде или некоторой другой стерильной среде для инъекций непосредственно перед применением.
Композиции для ректального или вагинального введения предпочтительно представляют собой суппозитории, которые могут содержать, в дополнение к активному веществу, эксципиенты, такие как кокосовое масло или суппозиторный воск.
Композиции для назального или подъязычного введения также получают вместе со стандартными эксципиентами, хорошо известными в области техники.
Доза активного ингредиента в композициях данного изобретения может варьировать; однако необходимо, чтобы количество активного ингредиента было таким, чтобы получить подходящую дозированную форму. Выбранная доза зависит от желаемого терапевтического эффекта, пути введения и продолжительности лечения. Обычно для достижения желаемого терапевтического эффекта при введении человеку или животным, например млекопитающим, вводят уровни дозы, составляющие от 25 мкг/кг/день до 100 мг/кг/день на массу тела в день в виде разовой дозы или с разделением на множественные дозы.
Предпочтительный общий диапазон дозы составляет от 250 мкг/кг/день до 5,0 мг/кг/день на массу тела в день, которую можно вводить в виде разовой дозы или с разделением на множественные дозы.
Далее, соединение формулы (I) можно вводить в составе композиции с замедленным высвобождением, такой, как описаны в нижеследующих патентах. Среди таких готовых форм предпочтительными будут 14-дневная или 28-дневная формы с медленным высвобождением. В патенте США № 5672659 описаны композиции с замедленным высвобождением, включающие в себя пептид и сложный полиэфир. В патенте США № 5595760 описаны композиции с замедленным высвобождением, включающие в себя пептид в желеобразной форме. В патенте США № 5821221 описаны полимерные композиции с замедленным высвобождением, включающие в себя пептид и хитозан. В патенте США № 5916883 описаны композиции с замедленным высвобождением, включающие в себя пептид и циклодекстрин. В международной патентной заявке №PCT/US99/01180, (номер публикации WO 99/38536, Август 5, 1999), описаны абсорбируемые композиции пептида с замедленным высвобождением. Содержание вышеприведенных патентов и заявок включено в данное описание в качестве ссылки.
Применение композиций с немедленным или замедленным высвобождением зависит от вида целевых показаний. Если показание состоит из острого или сверхострого расстройства, лечение формой с немедленным действием будет предпочтительней, чем лечение с помощью композиции с пролонгированным высвобождением. Наоборот, для профилактического или продолжительного курсов лечения композиция с пролонгированным высвобождением будет в целом предпочтительней.
Сокращения
Номенклатура подтипов рецептора к соматостатину соответствует рекомендациям IUPHAR, в которых sstr4 относится к рецептору, первоначально клонированному Bruno et al., а sstr5 относится к рецептору, клонированному O'Carroll et al.
Сокращения общеизвестных аминокислот соответствуют рекомендациям IUPAC-IUB. Далее, как использовано в настоящем документе, приведены следующие определения некоторых сокращений:
Abu = α-аминомасляная кислота;
Aib = α-аминоизомасляная кислота;
β-Ala = β-аланин;
Amp = 4-амино-фенилаланин;
Ava = 5-аминовалериановая кислота;
Cha = циклогексилаланин;
Cpa = 3-(4-хлорфенил)аланин;
Dab = 2,4-диаминомасляная кислота;
Dap = 2,3-диаминопропионовая кислота;
Dip = 3,3'-дифенилаланин;
Gaba = γ-аминомасляная кислота;
HSer = гомосерин;
1-Nal = 3-(1-нафтил)аланин;
2-Nal = 3-(2-нафтил)аланин;
Nle = норлейцин;
Nva = норвалин;
2-Pal = 3-(2-пиридил)аланин;
3-Pal = 3-(3-пиридил)аланин;
4-Pal = 3-(4-пиридил)аланин;
Tfm = Трифторметил; и
TfmA = 4-трифторметилфенил-аланин.
Tyr(I) = Йодированный остаток тирозина (например, 3-1-Tyr, 5-1-Tyr, 3,5-1-Tyr), в котором йод может быть радиоактивным изотопом, например, I125, I127, или I131.
В настоящем описании также используют следующие сокращения некоторых реагентов:
DBU = 1,8-диазабицикло[5.4.0]ундец-7-ен;
DCM = дихлорметан;
DIC = диизопропилкарбодиимид;
DIEA = диизопропилэтиламин;
DMF = диметилформамид;
MTBD = 1,3,4,6,7,8-гексагидро-1-метил-2H-пиримидо[1,2a]пиримидин;
o-NBS= 2-нитробензолсульфонил;
TBTU= O-Бензотриазол-1-ил-1-N,N,N',N'-тетраметилурония тетрафторборат;
и
TFA = трифторуксусная кислота.
За исключением N-концевой аминокислоты, все сокращения (например, Cpa для A1) аминокислот в данном описании обозначают структуру -NH-CH(R)-CO-, где R представляет собой боковую цепь аминокислоты (например, CH3 для Ala). Для N-концевой аминокислоты сокращение означает структуру (R1R2)-N-CH(R)-CO-, где R представляет собой боковую цепь аминокислоты, и каждый из R1 и R2 независимо представляет H или как в другом случае определено в данном документе.
Алифатическая аминокислота представляет собой α-аминокислоту, имеющую одну или две боковых цепи, которые независимо представляют собой углеводороды, например прямую или разветвленную цепь из 1-6 углеродов. Примеры алифатических аминокислот включают в себя Ala, Aib, Val, Leu, Tle, Ile, Nle, Nva, или Abu.
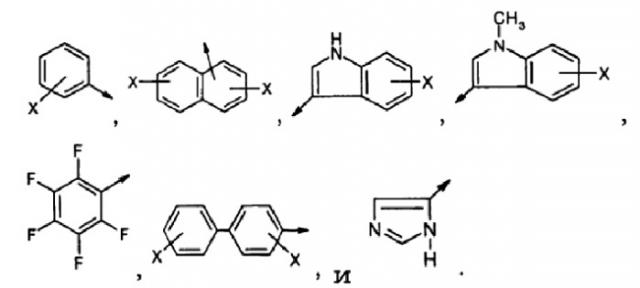
Под термином "ароматическая α-аминокислота" подразумевают аминокислотный остаток формулы, в которой Z1 представляет собой фрагмент, содержащий ароматическое кольцо, и Z2 представляет собой водород или фрагмент, содержащий ароматическое кольцо. Примеры таких фрагментов, содержащих ароматическое кольцо, включают в себя, не ограничиваясь ими, бензольное или пиридиновое кольцо и следующие структуры, содержащие или не содержащие один или несколько заместителей X в ароматическом кольце (где X, независимо для каждого случая, представляет собой, галоген, NO2, CH3, OCH3, CF3, или OH):
Другими примерами ароматических α-аминокислот согласно изобретению являются замещенные His, такие как MeHis, His(τ-Me), или His(π-Me).
При использовании в настоящем документе подразумевают, что термин "алкил" включает в себя алкильные группы означенной длины либо в прямой или разветвленной конфигурации. Примерами таких алкильных групп являются метил, этил, пропил, изопропил, бутил, втор-бутил, третичный бутил, пентил, изопентил, гексил, изогексил и т.п. Когда в определение включают термин C0-алкил, подразумевают, что он означает одинарную ковалентную связь.
Подразумевают, что термин "низший алкил" включает в себя одновременно разветвленные и прямоцепочечные алкильные группы, имеющие 1-6 углеродных атомов.
При использовании в настоящем документе подразумевают, что термин "арил" включает в себя любые стабильные моноциклические, бициклические или трициклические углеродные кольца до 7 звеньев в каждом кольце, в то время как по меньшей мере одно кольцо является ароматическим. Примеры арильных групп включают в себя фенил, нафтил, антраценил, бифенил, тетрагидронафтил, инданил, фенантренил и т.п.
Термин "гетероциклил", как использован в настоящем описании, представляет собой стабильное 5-7-членное моноциклическое или стабильное 8-11-членное бициклическое или стабильное 11-15-членное трициклическое гетероциклическое кольцо, которое является либо насыщенным, либо ненасыщенным и которое содержит углеродные атомы и от одного до четырех гетероатомов, выбранных из группы, состоящей из N, O и S, и включающее в себя любую бициклическую группу, в которой любое из вышеопределенных гетероциклических колец сопряжено с бензольным кольцом. Гетероциклическое кольцо может быть присоединено по любому гетероатому или углеродному атому, что приводит к созданию стабильной структуры. Примеры таких гетероциклических элементов включают в себя, не ограничиваясь ими, азепинил, бензимидазолил, бензизоксазолил, бензофуразанил, бензопиранил, бензотиопиранил, бензофурил, бензотиазолил, бензотиенил, бензоксазолил, хроманил, циннолинил, дигидробензофурил, дигидробензотиенил, дигидробензотиопиранил, дигидробензотиопиранилсульфон, фурил, имидазолидинил, имидазолинил, имидазолил, индолинил, индолил, изохроманил, изоиндолинил, изохинолинил, изотиазолидинил, изотиазолил, изотиазолидинил, морфолинил, нафтиридинил, оксадиазолил, 2-оксоазепинил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, пиперидил, пиперазинил, пиридил, пиридил N-оксид, хиноксалинил, тетрагидрофурил, тетрагидроизохинолинил, тетрагидрохинолинил, тиаморфолинил, тиаморфолинил сульфоксид, тиазолил, тиазолинил, тиенофурил, тиенотиенил, тиенил и т.п.
Считают, что термин "замещенный" включает в себя упомянутую химическую группу (например, низший алкил, арил, циклоалкил и т.д.), замещенную одним или несколькими упомянутыми заместителями (например, галогеном, гидрокси, низшим алкилом и т.д.). Заместитель может быть присоединен к любому атому в химической группе.
Сокращение "NMe" означает "N-метил-". Как использовано в настоящем описании, NMe указывает, что амидный азот ассоциированной аминокислоты является метилированным. Таким образом, "NmeCpa" означает -N(CH3)-CH(R)-CO-, где R представляет собой 4-хлорфенил, "Nme2-Nal" означает-N(CH3)-CH (R)-CO-, где R представляет собой 2-нафтил, и т.д.
Считают, что термин алкокси включает в себя алкокси-группы означенной длины либо прямой, либо разветвленной конфигурации. Примерами таких алкокси-групп являются метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, третичный бутокси, пентокси, изопентокси, гексокси, изогексокси и т.п.
Подразумевают, что термин галоген или гало включает в себя атомы галогена фтор, хлор, бром и йод.
Когда аминокислотный остаток является оптически активным, подразумевают, что он имеет L-форму, если D-форма отдельно не обозначена.
Материалы
4-метилбензгидриламиновая гидрохлоридная смола (0,25 или 0,5 мэквив g-1 был получен от Advanced ChemTech Inc., Louisville, KY. Nα трет-бутилоксикарбонил (Boc) защищенные аминокислоты были приобретены у Bachem Inc., Torrance, CA, Advanced ChemTech Inc., и Synthetech Inc., Albany, OR. Реакционноспособные боковые цепи аминокислот были защищены одной из следующих групп: Cys, 4-метилбензилоксикарбонил; Lys, 2-хлорбензилоксикарбонил; Thr, O-бензил; Tyr, О-2,6-дихлорбензил. Все реагенты и растворители имели степень чистоты ACS или выше и использованы без дальнейшей очистки.
Пептидный синтез
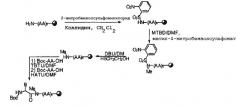
Пептидный синтез может быть обобщен следующей реакционной схемой:
Соединения формулы (I) могут быть и были синтезированы на функционализированной 4-метилбензгидриламиновой, 1% сшитой полистирольной смолы (0,25 или 0,5 мэквив g-1), на уровне 0,25 ммоль на синтезаторе Advanced ChemTech (модель 200), с использованием следующей методики: деблокирование, 40% TFA (2 мин, 20 мин); цикл промывки DCM (три промывки); нейтрализация, 10% DIEA (1 мин, 5 мин); цикл промывки DMF; цикл промывки DCM (две промывки); двойное связывание; первая, с помощью сложных эфиров 1,3-диизопропилкарбодиимида (3 эквив.), 30 мин в DCM; промывка DCM (три промывки); второе связывание с предварительно полученными сложными эфирами TBTU (3 эквив.), 90 мин в DMF, с каталитическим количеством DIEA; промывка DMF (одна промывка); промывка DCM (три промывки). Ход реакций связывания оценивали качественно.
N∝-защита
После деблокирования аминогруппы на требуемом участке метилирования, смола была суспендирована в DCM (20 мл). К этой суспензии были добавлены коллидин (3 эквив.) и o-нитробензолсульфонилхлорид (3 эквив.), и смесь встряхивали, используя синтезатор Advanced ChemTech (модель 200), в течение 2 час. Затем смолу промывали DCM (2 промывки) и DMF (3 промывки). Защиту оценивали качественно с помощью нингидринового теста.
Nα-метилирование
Защищенную о-нитробензолсульфонамидную смолу суспендировали в DMF (20 мл), к которому добавляли MTBD (3 эквив.) и метил-4-нитробензолсульфонат или диметилсульфат (для Cys11). Далее смесь встряхивали, используя синтезатор Advanced ChemTech (модель 200), в течение 0,5 час, и смолу промывали DMF (4 промывки).
Nα-Me снятие защиты
Как только целевой остаток был метилирован, смолу повторно суспендировали в DMF (20 мл). К суспензии добавляли DBU (3 эквив.), и 2-меркаптоэтанол (3 эквив.) и смесь встряхивали, используя синтезатор Advanced ChemTech (модель 200), в течение 0,5 час. Далее смолу тщательно промывали DMF (5 промывок).
Предшествующая методика метилирования была успешной для всех остатков, за исключением D-Cys6, что приводило к диметилированным производным (см., например, соединения 2 и 10.) Однако замена D-Cys6 на Cys6 приводила к монометилированным пептидам.
Отщепление пептидов
Пептиды отщепляли от смолы-подложки одновременным снятием защитных групп с боковых цепей посредством ацидолиза, используя безводный фторид водорода, содержащий анизольный акцептор (˜30% об./об.), в течение 45 мин при 0°C. Пептиды циклизовали в 90% уксусной кислоте (-600 мл) с небольшим избытком I2 (15 мин). Избыток I2 далее был удален добавлением аскорбиновой кислоты.
Очистка
Неочищенные пептиды очищали препаративной ОФ-ВЭЖХ на C-18-связанном силикагеле, используя колонки с аксиальной компрессией (Dynamax-300 Å, 5 или 8 мкм, 21,4 × 250 мм). Применяли систему элюирования с линейным градиентом со скоростью потока 20 мл мин-1: A; 0,1% TFA, B; 0,1% TFA в 80% MeCN, 20% B до 50% B при 1% мин-1. Разделение контролировали с помощью ОФ-ВЭЖХ при 215 нм. Фракции, содержащие продукт, объединяли, концентрировали в вакууме и лиофилизировали. Каждый пептид был получен в виде рыхлого белого порошка с постоянной массой путем лиофилизации из водной уксусной кислоты. Чистоту конечных пептидов оценивали при 215 нм с помощью аналитической ОФ-ВЭЖХ. Аналитическую ОФ-ВЭЖХ регистрировали, используя подложку Vydac C-18 (4,6 × 250 мм, 5 мкм, размер пор 300Å, Liquid Separations Group). Систему с линейным градиентом применяли при скорости потока 1,5 мл мин-1; ВЭЖХ -1, A, 0,1% TFA; B, 0,1% TFA в 80% MeCN; 20% B до 50% B при 1% мин-1; ВЭЖХ -2, C, 5% MeCN в TEAP (0,1 M, pH 3); D, 20% C в MeCN, 10% D до 70% D при 1% мин-1. Элюент с колонки контролировали при 215 нм. Время удерживания и чистоту каждого пептида оценивали с помощью Rainin Dynamax HPLC Method Manager. Было обнаружено, что каждый пептид имеет чистоту >98%. Результаты по временам удерживания ВЭЖХ приведены в Таблице 1.
| Таблица 1N-метильные аналоги и аналитические данные | |||||
| Пептид № | ПоследовательностьN-Me | Масс-спектр (М-Н+) | ВЭЖХс | ||
| Рассчит.а | Наблюд.b | (tR-1)d | (tR-2)e | ||
| 1 | NmeCpa-цикло(DCys-3-Pal-DTrp-Lys-Thr-Cys)-2-Nal-NH2 | 1178,7 | 1179,2 | 18,3 | 19,3 |
| 2 | Cpa-цикло(NMeDCys-3-Pal-DTrp-Lys-Thr-Cys)-2-Nal-NHMe | 1192,7 | 1193,4 | 19,6 | 19,3 |
| 3 | Cpa-цикло(DCys-NMe3-Pal-DTrp-Lys-Thr-Cys)-2-Nal-NH2 | 1178,7 | 1178,9 | 20,3 | 22,5 |
| 4 | Cpa-цикло(DCys-3-Pal-NMeDTrp-Lys-Thr-Cys)-2-Nal-NH2 | 1178,7 | 1179,2 | 17,9 | 17,2 |
| 5 | Cpa-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-2-Nal-NH2 | 1178,7 | 1178,9 | 19,2 | 18,7 |
| 6 | Cpa-цикло(DCys-3-Pal-DTrp-Lys-NMeThr-Cys)-2-Nal-NH2 | 1178,7 | 1179,3 | 17,4 | 15,1 |
| 7 | Cpa-цикло(DCys-3-Pal-DTrp-Lys-Thr-NMeCys)-2-Nal-NH2 | 1178,7 | 1179,0 | 18,5 | 16,7 |
| 8 | Cpa-цикло(DCys-3-Pal-DTrp-Lys-Thr-Cys)-(Nme)-2-Nal-NH2 | 1178,7 | 1179,0 | 20,3 | 19,0 |
| 9 | Cpa-цикло(DCys-3-Pal-DTrp-Lys-Thr-Cys)-Nal-NH2 | 1164,8 | 1164,7 | 17,2 | 17,2 |
| 10 | Cpa-цикло(NMeDCys-3-Pal-DTrp-Lys-Thr-Cys)-Dip-NHMe | 1218,9 | 1218,9 | 21,9 | 20,8 |
| 11 | Cpa-цикло(DCys-3-Pal-NMeDTrp-NMeLys-Thr-Cys)-2-Nal-NH2 | 1192,7 | 1192,3 | 19,9 | 19,7 |
| 12 | Cpa-цикло(DCys-Tyr-DTrp-NMeLys-Thr-Cys)-2-Nal-NH2 | 1193,8 | 1193,6 | 24,9 | 23,1 |
| 13 | Tfm-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-2-Nal-NH2 | 1212,2 | 1212,2 | 21,4 | 20,7 |
| 14 | Cpa-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-DTrp-NH2 | 1167,8 | 1168,0 | 16,6 | 14,9 |
| 15 | Nal-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-DTrp-NH2 | 1183,2 | 1183,5 | 18,0 | 16,4 |
| 16 | 3-Pal-цикло(DCys-3-Pal-DTrp-NMeLys-Thr-Cys)-DTrp-NH2 | 1135,0 | 1134,8 | 11,5 | 9,8 |
| аТеоретическая молекулярная масса (М-Н+, Да).bНаблюдаемая молекулярная масса (М-Н+, Да).сОбращенно-фазовая ВЭЖХ (С-18, 5 мкм, 4,6 × 250 мм, λ=215 нм) времена удерживания (мин). По данным ВЭЖХ было обнаружено, что каждое соединение имеет чистоту >98%.dСистема элюирования ВЭЖХ: A; 0,1% TFA, B; 0,1% TFA в 80% MeCN, 20% B до 50% B при 1% мин-1 и 1,5 мл мин-1.eСистема элюирования ВЭЖХ-2: C, 5% MeCN в TEAP (0,1 M, pH 3); D, 20% C в MeCN, 10% D до 50% D при 1% мин-1 и 1,5 мл мин-1. |
Аминокислотный анализ
Пептиды гидролизовали в вакууме 110°C; 20 час) в 4 М метансульфоновой кислоте, содержащей 0,2% 3-(2-аминоэтил) индола (Pierce). Аминокислотные анализы проводили на гидролизатах с последующей дериватизацией с помощью о-фталидальдегидного реагента (Sigma Chemical Co.), применяя автоматическую ВЭЖХ-систему (Rainin Instrument Co.), снабженную колонкой с аксиальной компрессией 100 × 4,6 мм, 3 мкм C18 с интегральной предколонкой (Microsorb AAAnalysisTM, Type O; Rainin Instrument Co.) Дериватизированные первичные аминокислоты элюировали, используя бинарный градиент буфера A; 0,10 M ацетат натрия, содержащий 4,5% об./об. метанол и 0,5% об./об. Тетрагидрофуран при pH 7,2 и буфер B; метанол. Градиентная последовательность; 0% A при 0 мин; 35% A при 16,5 мин; 90% A при 30 мин и 90% A при 33 мин. Применяли при скорости потока 1,0 мл мин-1 при температуре окружающей среды. Элюен