Производные пиперидинбензолсульфамида
Иллюстрации
Показать всеИзобретение относится к соединениям общей формулы
в которой R1 представляет собой низший алкил, -(СН2)n-арил, незамещенный или замещенный одним или двумя заместителями, выбранными из группы, состоящей из низшего алкила, низшего алкокси, галогена или трифторметила, или представляет собой пиридин; R2 представляет собой низший алкил, -(CH2)n-арил, незамещенный или замещенный одним или двумя заместителями, выбранными из группы, состоящей из низшего алкила, низшего алкокси, галогена, трифторметила, нитро, циано, -NR'R", гидрокси или гетероарильной группы, которая представляет собой моновалентный гетероциклический 5- или 6-членный ароматический радикал, содержащий атомы N, или R2 обозначает гетероарил, который представляет собой моновалентный гетероциклический 5- или 6-членный ароматический радикал, где гетероатомы выбирают из N, О или S, незамещенный или замещенный одним или двумя заместителями, выбранными из группы, состоящей из низшего алкила или галогена; R3 представляет собой пиридин или представляет собой арил, незамещенный или замещенный галогеном или низшим алкилом; R4 представляет собой водород или гидрокси; А представляет собой -S(O)2- или -С(O)-; X, Y независимо друг от друга представляют собой -СН2- или -О-, при условии, что Х и Y одновременно не представляют собой -О-; R'R" независимо друг от друга представляют собой водород или низший алкил; n означает 0, 1 или 2, и к их фармацевтически приемлемым аддитивным солям с кислотами. Изобретение также относится к лекарственному средству. Технический результат - получение новых биологически активных соединений, обладающих ингибирующим действием в отношении поглощения глицина. 2 н. и 19 з.п. ф-лы, 1 табл.
Реферат
Настоящее изобретение относится к соединениям общей формулы
в которой R1 представляет собой низший алкил, -(СН2)n-арил, незамещенный или замещенный одним или двумя заместителями, выбранными из группы, состоящей из низшего алкила, низшего алкокси, -OCF3, галоген, -NR'R'' или трифторметил, или представляет собой гетероарил;
R2 представляет собой низший алкил, -(СН2)n-арил, незамещенный или замещенный одним или двумя заместителями, выбранными из группы, состоящей из низшего алкила, низшего алкокси, галогена, трифторметила, нитро, циано, -NR'R'', гидрокси, или гетероарильной группой, или представляет собой гетероарил, незамещенный или замещенный одним или двумя заместителями, выбранными из группы, состоящей из низшего алкила или галогена;
R3 представляет собой гетероарил или представляет собой арил, незамещенный или замещенный галогеном или низшим алкилом;
R4 представляет собой водород или гидрокси;
А представляет собой -S(O)2- или -С(O)-;
X, Y независимо друг от друга представляют собой -СН2- или -O- при условии, что Х и Y одновременно не означают -О-;
R'R'' независимо друг от друга представляют собой водород, низший алкил или -С(O)-низший алкил;
n означает 0, 1 или 2,
и также относится к их фармацевтически приемлемым аддитивным солям с кислотой (солям - продуктам присоединения кислоты).
Кроме того, настоящее изобретение включает все их рацемические смеси, все их соответствующие энантиомеры и/или оптические изомеры.
Настоящее изобретение относится к соединениям общей формулы I, к содержащим их фармацевтическим композициям и к их применению при лечении неврологических или нейропсихиатрических нарушений и расстройств. Неожиданно было обнаружено, что соединения общей формулы I являются эффективными ингибиторами глицин-транспортера 1 (GlyT-1), переносчика глицина, и что эти соединения обладают хорошей селективностью в отношении ингибиторов глицин-транспортера 2 (GlyT-2).
Шизофрения представляет собой прогрессирующее и разрушительное неврологическое заболевание, характеризующееся эпизодическими позитивными симптомами, такими как мании, галлюцинации, нарушения мыслительной деятельности и психоз, и стойкими негативными симптомами, например, такими как вялый аффект, сниженное внимание и социальная самоизоляция, а также снижение когнитивной способности (Lewis D.A., Lieberman J.A., Neuron, 28: 325-33, 2000). В последнее десятилетие исследования сфокусировались на гипотезе так называемой "допаминовой гиперактивности", которая привела к терапевтической интервенции, связанной с блокированием допаминергической системы (Vandenberg R.J., Aubrey K.R., Exp. Opin. Ther. Targets, 5 (4): 507-518, 2001; Nakazato A., Okuyama S. et al., Exp. Opin. Ther. Patents, 10 (1): 75-98, 2000). Такой терапевтический подход незначительно воздействует на негативные и когнитивные симптомы, которые являются наиболее выраженными показателями прогноза функционального исхода (Sharma Т., Br. J. Psychiatry, 174 (suppl. 28): 44-51,1999).
Дополняющая модель шизофрении, предложенная в середине 1960-х, базируется на психотомиметическом действии, вызываемом посредством блокады глутаматной системы при воздействии таких соединений, как фенциклидин (РСР - сокр. от англ. phencyclidine) и родственных ему агентов (кетамин), которые являются неконкурентными антагонистами рецептора NMDA. Интересно, что у здоровых волонтеров РСР-индуцированные психотомиметическое действие включает позитивные и негативные симптомы, а также когнитивную дисфункцию, и таким образом, весьма схоже с шизофренией у пациентов (Javitt D.C. et al., Biol. Psychiatry, 45: 668-679, 1999). Кроме того, трансгенные мыши, экспрессирующие пониженное количество NMDAR1-субъединиц, проявляют поведенческие отклонения, сходные с отклонениями, наблюдающимися на фармакологически индуцированных моделях, что свидетельствуют в поддержку модели, в соответствии с которой пониженная активность NMDA-рецептора приводит к поведению, подобному шизофрении (Mohn A.R. et al., Cell, 98: 427-236, 1999).
Глутаматная нейротрансмиссия, в частности активность NMDA-рецептора, играет критическую роль в процессах синаптической пластичности, обучения и запоминания, так что, по-видимому, NMDA-рецептора служат в качестве сортирующего переключателя для прохождения порога синаптической пластичности и формирования памяти (Wiley NY; Bliss T.V., Collingridge G.L., Nature, 361: 31-39, 1993). Трансгенные мыши, чрезмерно экспрессирующие NMDA NR2B-субъединицы, проявляют повышенную синаптическую пластичность и лучшую способность к обучению и запоминанию (Tang J.P. et al., Natur, 401-63-69, 1999).
Таким образом, если дефицит глутамата связан с патофизиологией шизофрении, повышенная глутаматная трансмиссия, в частности, посредством активации NMDA-рецептора, могла бы привести к продуцированию как антипсихотических, так и усиливающих познавательные способности эффектов.
Аминокислота глицин, как известно, имеет по меньшей мере две важных функции в ЦНС (центральной нервной системе). Она действует как ингибирующая аминокислота, связываясь со стрихнин-чувствительными глициновыми рецепторами и также она влияет на возбуждающую активность, действуя как важнейший соагонист с глутаматом по отношению к функционированию N-метил-D-аспартат-рецепторов (NMDA - сокр. от англ. N-methyl-D-aspartate-N-метил-D-аспартат). Хотя глутамат высвобождается из синаптических терминалов зависящим от активности образом, глицин, по-видимому, присутствует в более постоянном количестве и, по-видимому, модулирует/контролирует рецепторы в отношении их отклика на глутамат.
Один из наиболее эффективных способов контролировать синаптическую концентрацию нейротрансмиттера заключается во влиянии на его повторное поглощение в синапсе. Нейротрансмиттер при транспортировании посредством удаления нейротрансмиттеров из внеклеточного пространства может контролировать время жизни вне клетки и таким образом модулировать величину синаптической трансмиссии (Gainetdinov R.R. et al, Trends in Pharm. Sci., 23 (8): 367-373, 2002).
Глицинтранспортеры (переносчики глицина), которые формируют часть натриевого и хлоридного семейства нейротрансмиттерных транспортеров, играют важную роль в терминировании постсинаптического глицинергического воздействия и поддержании низкой внеклеточной концентрации глицина посредством повторного поглощения глицина в пресинаптических терминалах нерва и при ближайших тонких глиальных процессах.
Были клонированы из мозга млекопитающих два различных гена-транспортера глицина (GlyT-1 и GlyT-2), которые приводят к двум транспортерам с ˜50%-ной гомологичностью аминокислотной последовательности. GlyT-1 представлен четырьмя изоформами, возникающими при альтернативном сплайсинге и альтернативном использовании промотора (1а, 1b, 1с и Id). Только две изоформ были обнаружены в мозге грызунов (GlyT-1а и GlyT-lb). GlyT-2 также имеет некоторую степень гетерогенности. Две изоформы GlyT-2 (2а и 2b) идентифицированы в мозге грызунов. GlyT-1, как известно, локализуется в центральной нервной системе (ЦНС) и в периферических тканях, в то время как GlyT-2 специфичен по отношению к ЦНС. GlyT-1 имеет преимущественно глиальное распределение и обнаружен не только в зонах, соответствующих стрихнин-чувствительным глициновым рецепторам, но и вне этих зон, где, как предполагают, он связан с модулированием функции NMDA рецептора (Lopez-Corcuera В. et al., Mol. Mem. Biol., 18: 13-20, 2001). Таким образом, одна из стратегий усиления активности NMDA рецептора заключается в том, чтобы повысить концентрацию глицина в локальном микроокружении синаптических NMDA рецепторов посредством ингибирования GlyT-1 транспортера (Bergereon R. et al., Proc. Natl. Acad. Sci. USA, 95: 15730-15734, 1998).
Ингибиторы транспортеров глицина подходят для лечения неврологических или нейропсихиатрических нарушений и расстройств. Большую часть соответствующих заболеваний представляют собой психические болезни, шизофрения (Armer R.E., Miller D.J., Exp. Opin. Ther. Patents, 11 (4): 563-572, 2001), психотические расстройства настроения, такие как выраженные депрессивные расстройства; расстройства настроения, связанные с психотическими нарушениями, такими как мания или депрессия, связанные с биполярными расстройствами, и расстройства настроения, связанные с шизофренией, (Pralong Е.Т. et al., Prog. Neurobiol, 67: 173-202, 2002), аутистические расстройства (Carlsson M.L., J. Neural Trans,. 105: 525-535, 1998), когнитивные нарушения или расстройства, например, такие как деменция (слабоумие), включая возрастную деменцию и старческое слабоумие типа болезни Альцгеймера, нарушения памяти у млекопитающих, включая человека, расстройства, связанные с дефицитом внимания и болью (Armer R.E., Miller D.J., Exp. Opin. Ther. Patents, 11 (4): 563-572, 2001).
Таким образом, усиление активации NMDA рецепторов посредством ингибирования GlyT-1 может привести к агентам, которые пригодны для лечения психоза, шизофрении, деменции (слабоумия) и других заболеваний, имеющих отношение к когнитивным процессам, например таким, как расстройства, связанные с дефицитом внимания или болезнь Альцгеймера.
Предметом настоящего изобретения являются соединения формулы I сами по себе, применение соединений формулы I и их фармацевтически приемлемых солей для получения лекарственных средств для лечения заболеваний, имеющих отношение к активации NMDA рецепторов посредством ингибирования Glyt-1, их получение, лекарственные средства на основе соединения согласно настоящему изобретению и их получение, а также применение соединений формулы I для контроля или профилактики заболеваний, таких как психические болезни, расстройства памяти и способности к обучению, шизофрения, деменция (слабоумие) и другие заболевания, связанные с когнитивными процессами, например заболевания, связанные с дефицитом внимания или болезнь Альцгеймера.
Предпочтительные показания для использования соединений согласно настоящему изобретению представляют собой шизофрению, когнитивные нарушения и расстройства и болезнь Альцгеймера.
При использовании в тексте настоящей заявки термин "низший алкил" означает насыщенную алкильную группу с линейной или разветвленной цепью, содержащую от 1 до 6 атомов углерода, например, такую как метил, этил, пропил, изопропил, н-бутил, изобутил, 2-бутил, трет-бутил и подобные им группы. Предпочтительные низшие алкильные группы представляют собой группы, содержащие 1-4 атома углерода.
Термин "галоген" обозначает хлор, иод, фтор и бром.
Термин "низший алкокси" обозначает группу, в которой алкильные остатки являются такими, как определено выше, и которая присоединена через атом кислорода.
Термин "арил" обозначает моновалентный циклический ароматический радикал, состоящий из одной или более конденсированных кольцевых систем, где по меньшей мере одна кольцевая система является ароматической по своей природе, например, такой радикал, как фенил или нафтил.
Термин "гетероарил" обозначает моновалентный гетероциклический 5- или 6-членный ароматический радикал, где гетероатомы выбирают из N, О или S, например, такой радикал, как тиофенил, пиридинил, пиримидинил, имидазолил, пиперидинил, фуранил, пирролил, изоксазолил, пиразолил, пиразинил, бензо[1,3]диоксолил, бензо{b}тиофенил или бензотриазолил.
Термин "фармацевтически приемлемые аддитивные соли с кислотами (соли - продукты присоединения кислоты)" включает соли, образованные как с неорганическими, так и с органическими кислотами, например, такими как хлороводородная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, n-толуолсульфоновая кислота и с подобными кислотами.
Предпочтительными являются соединения формулы
в которой R1 представляет собой низший алкил, бензил или представляет собой фенил, незамещенный или замещенный одним или двумя заместителями, выбранными из группы, состоящей из низшего алкила, низшего алкокси, галогена или трифторметила;
R2 представляет собой низший алкил, бензил, тиофенил или представляет собой фенил, незамещенный или замещенный одним или двумя заместителями, выбранными из группы, состоящей из низшего алкила, низшего алкокси, галогена или трифторметила, нитро, амино, гидрокси или группы -NHC(O)- низший алкил;
R3 представляет собой пиридин-3-ил, пиридин-4-ил или представляет собой фенил, незамещенный или замещенный галогеном или низшим алкилом;
R4 представляет собой водород или гидрокси;
А представляет собой -S(O)2- или -С(O)-;
X, Y независимо друг от друга представляют собой -СН2- или -О-, при условии, что Х и Y одновременно не означают -О-,
и их фармацевтически приемлемые аддитивные соли с кислотами (соли - продукты присоединения кислоты).
Особенно предпочтительными соединениями согласно настоящему изобретению являются такие соединения формулы I, в которой Х и Y оба представляют собой -СН2-, А представляет собой -S(O)2-, R3 представляет собой незамещенный фенил и R4 представляет собой водород, например, следующие соединения:
(+/-)-3,4-дихлор-N-фенил-N-[цис-1-(2-фенилциклогексил)пиперидин-4-ил]бензолсульфонамид,
(+/-)-4-метокси-N-(3-метоксифенил)-N-[цис-1-(2-фенилциклогексил)пиперидин-4-ил]бензолсульфонамид,
(+/-)-4-метокси-N-фенил-N-[цис-1-(2-фенилциклогексил)пиперидин-4-ил]бензолсульфонамид,
(+/-)-N-(4-фторфенил)-4-метил-N-[цис-1-(2-фенилциклогексил)пиперидин-4-ил]бензолсульфонамид,
(+/-)-N-(4-фторфенил)-4-метокси-N-[цис-1-(2-фенилциклогексил)пиперидин-4-ил]бензолсульфонамид,
(+/-)-4-метокси-N-[цис-1-(2-фенилциклогексил)пиперидин-4-ил]-N-(3-трифторметилфенил)бензолсульфонамид или
(+)-4-метокси-N-фенил-N-[цис-1-(2-фенилциклогексил)пиперидин-4-ил]бензолсульфонамид.
Кроме того, предпочтительными являются соединения, в которых Х и Y оба представляют собой -CH2-, А означает -С(O)-, R3 означает незамещенный фенил и R4 означает водород, например, следующие соединения:
(+/-)-3-метокси-N-[цис-1-(2-фенилциклогексил)пиперидин-4-ил]-N-n-толилбензамид,
(+/-)-4-фтор-N-[цис-1-(2-фенилциклогексил)пиперидин-4-ил]-N-n-толилбензамид,
(+/-)-N-(4-хлорфенил)-N-[цис-1-(2-фенилциклогексил)пиперидин-4-ил]-3-трифторметилбензамид или
(+/-)-N-(4-хлорфенил)-3-метокси-N-[цис-1-(2-фенилциклогексил)пиперидин-4-ил]бензамид.
Кроме того, еще одной предпочтительной группой соединений являются такие соединения, в которых Х и Y оба представляют собой -СН2-, А означает -С(O)-, R3 означает незамещенный фенил и R4 означает гидрокси, например, следующие соединения:
(+/-)-N-(4-фторфенил)-N-[цис-1-(2-гидрокси-2-фенилциклогексил)пиперидин-4-ил]-3-метоксибензамид,
(+/-)-N-(4-хлорфенил)-N-[цис-1-(2-гидрокси-2-фенилциклогексил)пиперидин-4-ил]-3-метоксибензамид,
(+/-)-4-фтор-N-[цис-1-(2-гидрокси-2-фенилциклогексил)пиперидин-4-ил]-N-n-толилбензамид,
(+/-)-N-[цис-1-(2-гидрокси-2-фенилциклогексил)пиперидин-4-ил]-N-(3-метоксифенил)бензамид или
(+/-)-N-[цис-1-(2-гидрокси-2-фенилциклогексил)пиперидин-4-ил]-3-метокси-N-n-толилбензамид.
Кроме того, предпочтительными являются соединения, в которых Х и Y оба представляют собой -СН2-, А означает -S(O)2-, R3 представляет собой незамещенный фенил или фенил, замещенный хлором, фтором или метилом, и R4 означает гидрокси, например, следующие соединения:
(+/-)-N-[цис-1-(2-гидрокси-2-фенилциклогексил)пиперидин-4-ил]-4-метокси-N-фенилбензолсульфонамид,
(+)-N-[цис-1-(2-гидрокси-2-фенилциклогексил)пиперидин-4-ил]-4-метокси-N- фенилбензолсульфонамид,
(+/-)-N-(4-хлорфенил)-N-[цис-1-(2-гидрокси-2-фенилциклогексил)пиперидин-4-ил]-4-метоксибензолсульфонамид,
(+/-)-N-{цис-1-[2-(4-хлорфенил)-2-гидроксициклогексил]пиперидин-4-ил}-4-метокси-N-фенилбензолсульфонамид,
(+/-)-N-{цис-1-[2-(4-фторфенил)-2-гидроксициклогексил]пиперидин-4-ил}-4-метокси-N-фенилбензолсульфонамид,
(+/-)-N-[цис-1-(2-гидрокси-2-о-толилциклогексил)пиперидин-4-ил]-4-метокси-N-фенилбензолсульфонамид,
(+/-)-N-(4-фторфенил)-N-[цис-1-(2-гидрокси-2-фенилциклогексил)пиперидин-4-ил]-4-метоксибензолсульфонамид,
(+/-)-N-(4-фторфенил)-N-{цис-1-[2-(4-фторфенил)-2-гидроксициклогексил]пиперидин-4-ил}-4-метоксибензолсульфонамид,
(+/-)-N-[цис-1-(2-гидрокси-2-фенилциклогексил)пиперидин-4-ил]-4-метокси-N-(3-метоксифенил)бензолсульфонамид,
(+/-)-N-{цис-1-[2-(4-фторфенил)-2-гидроксициклогексил]пиперидин-4-ил}-4-метокси-N-(3-метоксифенил)бензолсульфонамид или
(+/-)-N-[транс-1-(2-гидрокси-2-фенилциклогексил)пиперидин-4-ил]-4-метокси-N-фенилбензолсульфонамид.
Кроме того, предпочтительными являются соединения, в которых Х и Y оба представляют собой -СН2-, А означает -S(O)2-, R3 означает пиридин-3-ил или пиридин-4-ил и R4 означает гидрокси, например, следующие соединения:
(+/-)-N-(4-хлорфенил)-N-[цис-1-(2-гидрокси-2-пиридин-3-илциклогексил)пиперидин-4-ил]-4-метоксибензолсульфонамид,
(+/-)-N-[цис-1-(2-гидрокси-2-пиридин-4-илциклогексил)пиперидин-4-ил]-4-метокси-N-фенилбензолсульфонамид,
(+/-)-N-[цис-1-(2-гидрокси-2-пиридин-3-илциклогексил)пиперидин-4-ил]-4-метокси-N-фенилбензолсульфонамид,
(+/-)-N-(4-фторфенил)-N-[цис-1-(2-гидрокси-2-пиридин-4-илциклогексил)пиперидин-4-ил]-4-метоксибензолсульфонамид,
(+/-)-N-[цис-1-(2-гидрокси-2-пиридин-4-илциклогексил)пиперидин-4-ил]-4-метокси-N-(3-трифторметилфенил)бензолсульфонамид или
(+/-)-N-[цис-1-(2-гидрокси-2-пиридин-3-илциклогексил)пиперидин-4-ил]-4-метокси-N-(3-трифторметилфенил)бензолсульфонамид.
Кроме того, предпочтительными являются соединения, в которых Х означает -СН2-, Y означает -О-, А означает -S(O)2-, R3 означает незамещенный фенил и R4 означает гидрокси, например, следующее соединение:
(+/-)-N-(4-фторфенил)-N-[цис-1-(4-гидрокси-4-фенилтетрагидропиран-3-ил)пиперидин-4-ил]-4-метоксибензолсульфонамид.
Кроме того, предпочтительными являются соединения, в которых Х означает -СН2-, Y означает -О-, А означает -С(O)-, R3 означает незамещенный фенил и R4 означает гидрокси, например, следующее соединение:
(+/-)-N-(4-фторфенил)-N-[цис-1-(4-гидрокси-4-фенилтетрагидропиран-3-ил)пиперидин-4-ил]-3-метоксибензамид.
Также предпочтительными являются соединения, в которых Х и Y оба представляют собой -СН2-, А означает -С(О)- и R3 означает гетероарил, незамещенный или замещенный галогеном или низшим алкилом, или соединения, в которых Х и Y оба представляют собой -СН2-, А означает -С(O)-, R3 означает гетероарил, незамещенный или замещенный одним или двумя заместителями, выбранными из группы, состоящей из низшего алкила или галогена, и R4 означает водород.
Соединения формулы I и их фармацевтически приемлемые соли согласно настоящему изобретению могут быть получены с использованием способов, известных из предшествующего уровня техники, например, с использованием способа, описанного ниже, этот способ включает
а) взаимодействие соединения формулы
с соединением формулы
R2SO2Cl
в присутствии основания и/или акцептора протона с получением при этом соединения формулы
в которой X, Y, R1, R2 и R3 являются такими, как определено выше, или
б) взаимодействие соединения формулы
с соединением формулы
R2COCl
в присутствии основания и/или акцептора протона с получением при этом соединения формулы
в которой X, Y, R1, R2 и R3 являются такими, как определено выше, или
в) взаимодействие соединения формулы
с соединением формулы
R3Li
с получением при этом соединения формулы
в которой А, X, Y, R1, R2 и R3 являются такими, как определено выше, или
г) взаимодействие соединения формулы
с соединением формулы
с получением при этом соединения формулы
в которой А, X, Y, R1, R2 и R3 являются такими, как определено выше, и,
если необходимо, превращение полученных соединений в фармацевтически приемлемые аддитивные соли с кислотами (продукты присоединения кислоты).
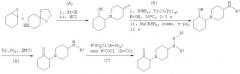
Соединения формулы I могут быть получены в соответствии с вариантами способа а)-г) и согласно приведенным ниже схемам 1-7.
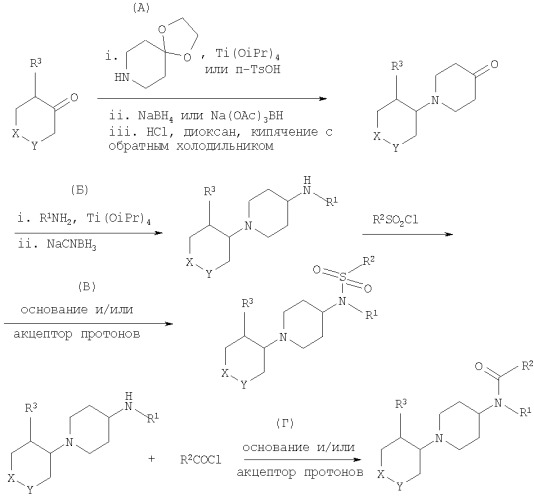
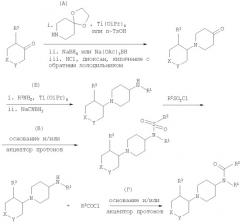
1. Получение соединений формулы I, в которой R4 означает водород (схема 1)
Соединения согласно настоящему изобретению могут быть получены способами, аналогичными способам, известным из предшествующего уровня техники.
Схема 1
Соединения формулы I, в которой R4 означает водород и А означает группу -S(O)2-, несложно получить посредством сульфонилирования соответствующих вторичных аминов с использованием методик, известных из предшествующего уровня техники, например, посредством обработки амина сульфонилхлоридом в присутствии подходящего основания или акцептора протонов (схема 1, стадия В). Подходящие амины включают диизопропилэтиламин, 4-диметиламинопиридин, пиридин, 1,8-диазабицикло[5.4.0]ундец-7-ен и другие амины. Акцепторы протонов включают, например, 1-метокси-2-метил-1-триметилсилилоксипропен.
Соединения формулы I, в которой R4 означает водород, и А означает группу -С(O)-, несложно получить посредством ацилирования соответствующих вторичных аминов с использованием методики, известной из предшествующего уровня техники, например, такой как обработка амина ацилхлоридом в присутствии подходящего основания или акцептора протонов (схема 1, стадия Г). Подходящие амины включают диизопропилэтиламин, диметиламинопиридин, триэтиламин и т.п. Акцепторы протонов включают, например, 1-метокси-2-метил-1-триметилсилилоксипропен.
Предшественники - вторичные амины получают посредством восстановительного аминирования кетона, взаимодействием полученного амина с соответствующим пиперидоном при 60°С в этаноле в присутствии стехиометрического количества тетраизопропоксида титана, с последующим взаимодействием с борогидридом натрия или цианоборогидридом натрия при комнатной температуре (схема 1, стадия Б), или взаимодействием полученного амина с соответствующим пиперидоном в присутствии кислоты, например, такой как уксусная кислота, и с триацетоксиборогидридом натрия. Также могут быть использованы другие методики восстановительного аминирования, известные из предшествующего уровня техники.
Предшественник - кетон - получают посредством восстановительного аминирования соответствующего циклоалканона с использованием 1,4-диокса-8-азаспиро[4.5]декана с последующим гидролизом ацеталя в кислотных условиях, как показано на схеме 1, стадия А. Может быть использовано как промотированное титаном, так и катализируемое кислотой восстановительное аминирование. Получают только цис-изомеры. Удаление защитной ацетальной группировки осуществляют, например, посредством обработки с использованием концентрированной хлороводородной кислоты в диоксане при кипячении смеси с обратным холодильником.
Соединения согласно настоящему изобретению также могут быть получены в соответствии с одним из описанных выше подходов с использованием методов и техники параллельного синтеза в растворе.
2. Получение соединений формулы I, в которой R4 означает гидроксигруппу (схемы 2-6)
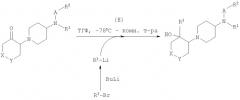
Схема 2
Соединения формулы I, в которой R4 означает гидроксигруппу и А означает -S(O)2- или -С(O)-, могут быть получены взаимодействием N-[1-(2-оксоциклоалкил)пиперидин-4-ил]-N-арил-арилсульфонамидов или N-[1-(2-оксоциклоалкил)пиперидин-4-ил]-N-арил-ариламидов при -78°С в ТГФ с одним из ариллитиевых реагентов R3-Li, которые либо являются коммерчески доступными, либо могут быть получены из соответствующих арилгалогенидов, согласно одной из множества методик, известных из предшествующего уровня техники (схема 2, стадия Е). По указанной методике получают только цис-форму.
Схема 3
Предшественники - N-[1-(2-оксоциклоалкил)пиперидин-4-ил]-N-арил-арилсульфонамиды - получают окислением N-[1-(2-гидроксициклоалкил)пиперидин-4-ил]-N-арил-арилсульфонамидов в соответствии с одной из множества методик, известных из предшествующего уровня техники, например, с использованием комплекса пиридин-триоксид серы в присутствии триэтиламина и диметилсульфоксида при комнатной температуре. Ту же самую методику используют для синтеза N-[1-(2-оксоциклоалкил)пиперидин-4-ил]-N-арил-ариламидов (схема 3, стадия Д).
Предшественник - циклический вторичный спирт - может быть получен взаимодействием подходящим образом функционализированного амина с циклическим эпоксидом (схема 3, стадия Г), например посредством смешения такого амина и эпоксида в этаноле при температуре образовании флегмы растворителем.
Подходящим образом функционализированные амины могут быть получены взаимодействием N-трет-бутоксикарбонил-4-пиперидона или N-бензил-4-пиперидинона с амином R1NH2 (схема 3, стадия А), с последующим сульфонилированием или ацилированием, как описано выше (схема 3, стадия Б). Защитную группу затем удаляют посредством кислотного гидролиза или гидрирования в соответствии с методиками, известными из предшествующего уровня техники (схема 3, стадия В).
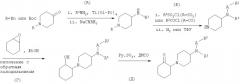
Схема 4
В качестве альтернативы для получения N-[1-(2-оксоциклоалкил)пиперидин-4-ил]-N-арил-арилсульфонамидов или N-[1-(2-оксоциклоалкил)пиперидин-4-ил]-N-арил-ариламидов может быть использован другой синтетический подход, как показано на схеме 4. 1-(2-Гидроксициклогексил)пиперидин-4-он обрабатывают амином R1NH2 в присутствии тетраизопропоксида титана и цианоборогидрида натрия (схема 4, стадия Б). Полученный 2-(4-ариламинопиперидин-1-ил)циклогексанол окисляют с использованием комплекса пиридин-триоксид серы, получая при этом соответствующий 2-(4-ариламинопиперидин-1-ил)циклогексанон (схема 4, стадия В). Это соединение либо сульфонилируют, либо ацилируют по вторичной аминогруппе, как описано выше, получая при этом N-[1-(2-оксоциклоалкил)пиперидин-4-ил]-N-арил-арилсульфонамиды или N-[1-(2-оксоциклоалкил)пиперидин-4-ил]-N-арил-ариламиды (схема 4, стадия Г).
1-(2-Гидроксициклогексил)пиперидин-4-он получают взаимодействием 1,4-диокса-8-азаспиро[4.5]декана с циклогексеноксидом с последующим гидролизом ацеталя в кислотных условиях, как показано на схеме 4, стадия А.
Схема 5
Подходящим образом функционализированные пиперидины, например, такие, как показано на схеме 3, также могут вступать во взаимодействие с 1-арилциклогексеноксидом, как показано на схеме 5, с получением при этом соединений согласно настоящему изобретению, в которых положение заместителей в циклоалкановом кольце является транс-положением.
Схема 6
Кроме того, подходящим образом функционализированные пиперидины например, такие, как показано на схеме 3, также могут вступать во взаимодействие с (+/-)-3,7-диоксабицикло[4.1.0]гептаном (получают, как описано в Tchelitcheff P.; C.R. Hebd. Seances Acad. Sci.; 224; 1947; 1722) (схема 6, стадия А), и затем полученные спирты окисляют до соответствующих кетонов, как описано выше (схема 6, стадия Б). Взаимодействие таких кетонов с ариллитиевыми реагентами (по аналогии со схемой 2, стадия Е), позволяет получить соединения согласно настоящему изобретению, в которых Х или Y представляет собой -О-.
3. Получение соединений, в которых R2-R4, Х и Y имеют такие значения, как описано выше, и R1 означает гетероарил
Соединения формулы I, в которой R1 означает гетероароматическую кольцевую систему, получают посредством ацилирования соответствующего гетероароматического амина подходящим ацилхлоридом в присутствии сильного апротонного основания, например, такого как 2-трет-бутилимино-2-диэтиламино-1,3-диметилпергидро-1,3,2-диазафосфорин (БЭМП). Для облегчения очистки реакционной смеси также можно использовать связанные со смолой апротонные основания, например полистирол-связанный БЭМП. Вторичные гетероароматические амины согласно настоящему изобретению, в которых R1 означает гетероароматическую кольцевую систему, в частности азиновую кольцевую систему, получают взаимодействием соответствующего первичного амина с гетероарилгалогенидом, предпочтительно с гетероарилиодидом или бромидом в присутствии основания и каталитического количества подходящего палладиевого комплекса. Предшественник - первичный амин - может быть получен посредством восстановительного аминирования соответствующего 4-пиперидона с источником NH3, например, посредством взаимодействия с формиатом аммония в присутствии Pd(0), или с использованием других методик, известных из предшествующего уровня техники (схема 7).
Схема 7
Превращение соединения формулы I в соль осуществляют посредством обработки по меньшей мере стехиометрическим количеством подходящей кислоты, например, такой как хлороводородная кислота, бромоводородная кислота, серная кислота, азотная кислота, фосфорная кислота или подобная кислота, и органической кислоты, например, такой как уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, яблочная кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, виннокаменная кислота, лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, n-толуолсульфоновая кислота, салициловая кислота и подобные им. Обычно свободное основание растворяют в инертном органическом растворителе, например, таком как диэтиловый эфир, этилацетат, хлороформ, этанол или метанол, или в подобном им растворителе, и добавляют кислоту в аналогичном растворителе. Температуру поддерживают между 0 и 50°С. Полученная соль выпадает в осадок самопроизвольно или может быть выделена из раствора при использовании менее полярного растворителя.
Аддитивные соли с кислотами (продукты присоединения кислоты) к основному соединению формулы I могут быть превращены в соответствующее свободное основание посредством обработки с использованием по меньшей мере стехиометрического эквивалента подходящего основания, например, такого как гидроксид натрия или гидроксид калия, карбонат калия, бикарбонат натрия, аммиак и подобного основания.
Соединения формулы I и их фармацевтически приемлемые аддитивные соли обладают ценными фармакологическими свойствами. В частности, было обнаружено, что соединения согласно настоящему изобретению являются эффективными ингибиторами глицинового транспортера I (GlyT-1).
Соединения исследовали с использованием тестов, приведенных ниже.
Растворы и вещества
Полная среда DMEM (модифицированная Иглом среда Дульбекко): DMEM ("Gibco Life-technologies"), глюкоза, фетальная бычья сыворотка (ФБС) 5%, ("Gibco life technologies"), пенициллин/стрептомицин 1% ("Gibco life technologies"), генетицин 1 мг/мл ("Gibco life technologies"), пролин 19,8 мг/0,5 л среды ("Sigma").
Буфер для поглощения (ПБ): 150 мМ NaCl, 10 мМ Гепес-Трис, рН 7,4, 1 мМ CaCl2, 2,5 мМ KCl, 2,5 мМ MgSO4, 10 мМ (+)D-глюкозы.
СНО-клетки (СНО сокр. от англ. Chinese Hamster Ovary - клетки яичников китайских хомячков) стабильно трансфектированные с hglyT1b cDNA, клон А467-47.
Исследование ингибирования процесса поглощения глицина (hGlyT-1b)
В день 1 клетки млекопитающего (СНО), трансфектированные с hGlyT-1b cDNA (клон А467-47), помещали при плотности, составляющей 50000 клеток/лунка, в полной среде DMEM в 96-луночные культуральные планшеты. В день 2 среду удаляют и клетки промывают дважды буфером для поглощения (ПБ). Затем клетки инкубируют в течение 30 мин при 22°С в соответствии с одним из следующих вариантов: (i) без потенциального конкурирующего соединения, (ii) с 10 мМ нерадиоактивного глицина, (iii) с потенциальным ингибитором в некоторой концентрации. Для получения данных, необходимых для вычисления концентрации ингибитора, приводящей к 50%-ному эффекту (например, IC50, для конкурентного ингибирования поглощения глицина) используют интервал концентраций потенциального ингибитора. Затем сразу же добавляют раствор, содержащий [3Н]-глицин 60 нМ (11-16 Кюри/ммоль) и 25 мкМ нерадиоактивного глицина. После этого клетки инкубируют при легком встряхивании в течение 30 мин при 22-24°С, после чего реакцию останавливают посредством удаления смеси и промывки (три раза) с использованием охлажденного на льду БП. Клетки лизируют, используя сцинтилляционную жидкость, встряхивают 3 часа и измеряют радиоактивность клеток с использованием сцинтилляционного счетчика.
Предпочтительные соединения характеризуются величиной IC50 (мкМ) в отношении GlyT-1 в интервале 0,015-0,100, как показано ниже в таблице.
| Пример | IC50 (мкМ) | Пример | IC50 (мкМ) |
| 1 | 0,048 | 108 | 0,04 |
| 3 | 0,094 | 109 | 0,073 |
| 11 | 0,056 | 110 | 0,076 |
| 17 | 0,049 | 111 | 0,068 |
| 22 | 0,083 | 112 | 0,061 |
| 34 | 0,098 | 114 | 0,066 |
| 35 | 0,066 | 115 | 0,071 |
| 67 | 0,099 | 120 | 0,091 |
| 69 | 0,029 | 121 | 0,071 |
| 75 | 0,068 | 123 | 0,095 |
| 96 | 0,049 | 125 | 0,096 |
| 98 | 0,033 | 139 | 0,044 |
| 99 | 0,028 | 141 | 0,1 |
| 100 | 0,015 | 142 | 0,063 |
| 102 | 0,092 | 144 | 0,082 |
| 105 | 0,084 | 159 | 0,068 |
| 107 | 0,083 | 163 | 0,085 |
Соединения формулы I и фармацевтически приемлемые соли соединений формулы I могут быть использованы в качестве лекарственных средств, например в виде фармацевтических препаратов. Фармацевтические препараты могут быть введены перорально, например, в виде таблеток, таблеток с покрытием, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Кроме того, введение эффективно может быть осуществлено ректально, например, в виде суппозиториев, парентерально, например, в виде растворов для инъекций.
Соединения формулы I могут быть использованы вместе с фармацевтически инертными, неорганическими или органическими носителями для получения фармацевтических композиций. В качестве носителей для таблеток, таблеток с покрытием, драже и твердых желатиновых капсул могут быть использованы, например, лактоза, кукурузный крахмал или его производные, тальк, стеариновые кислоты или их соли и тому подобные соединения. Подходящие носители для мягких желатиновых капсул представляют собой, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и тому подобные соединения. Однако в зависимости от природы активного соединения в случае мягких желатиновых капсул носитель может и не использоваться. Подходящие носители для получения растворов и сиропов представляют собой, например, воду, полиолы, глицерин, растительное масло и тому подобные соединения. Подходящие носители для суппозиториев представляют собой, например, природные или отвержденные масла, воски, жиры, полужидкие или жидкие полиолы и тому подобные соединения.
Фармацевтические композиции, кроме того, могут содержать консерванты, солюбилизаторы, стабилизаторы, улучшающие смачиваемость агенты, эмульгаторы, подсластители, подкрашивающие вещества, агенты, улучшающие вкус и запах, соли для регулирования осмотического давления, буферы, маскирующие агенты или антиоксиданты. Также они могут содержать и другие терапевтически значимые соединения.
Лекарственные средства, содержащие соединение формулы I или его фармацевтически приемлемую соль и терапевтически инертный носитель, также являются объектом настоящего изобретения, также как и способ их получения, который включает введение одного или более соединения формулы I и/или фармацевтически приемлемой аддитивной соли с кислотой и, если необходимо, одного или более терапевтически значимого вещества в состав лекарственного препарата, вместе с одним или более терапевтически инертным носителем.
Наиболее подходящие показания согласно настоящему изобретению - это показания, которые включают нарушения или расстройства центральной нервной системы, например, такие показания как лечение или профилактика шизофрении, когнитивные нарушения и болезнь Альцгеймера.
Дозировка может варьироваться в широких пределах и будет, безусловно, регулирова