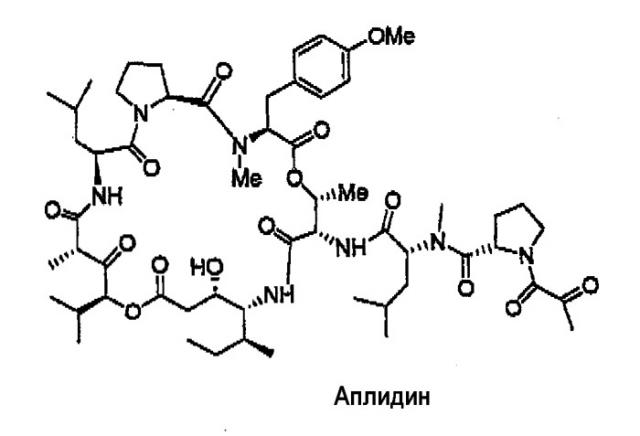
Аплидин для лечения множественной миеломы
Иллюстрации
Показать всеПредложено применение аплидина для получения медикамента для лечения множественной миеломы (ММ), соответствующие способ лечения ММ и фармацевтическая композиция того же назначения. Показано, что аплидин не только снижает жизнеспособность клеточных линий ММ, но и снижает секрецию факторов роста эпителия кровеносных сосудов, препятствуя распространению миеломы, повышает чувствиительность миеломных клеток к химиотерапии доксорубицином. 3 н.п. ф-лы, 7 ил.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к применению аплидина и аналогов для лечения рака, в особенности для лечения множественной миеломы.
Предпосылки создания изобретения
Множественная миелома представляет злокачественную пролиферацию плазмацитов, происходящих из единого клона. Термины множественная миелома и миелома могут использоваться взаимозаменяемо.
Плазмациты продуцируют антитела, белки, которые, передвигаясь в кровотоке, помогают организму избавиться от вредных веществ. Каждый тип плазмацитов реагирует только на одно конкретное вещество, вырабатывая большое количество одной разновидности антител. Данные антитела находят и действуют на одно вещество. Так как в организме присутствует большое разнообразие типов плазмацитов, он может реагировать на множество веществ. Если рак поражает плазмациты, то организм продолжает продуцировать все больше и больше этих клеток. Ненужные плазмациты - все ненормальные и все абсолютно одинаковые - называются миеломными клетками. Миеломные клетки предпочтительно накапливаются в костном мозге и в твердой внешней части костей. Иногда они накапливаются только в одной кости и образуют единую массу или опухоль, называемую плазмацитомой. В большинстве случаев, однако, миеломные клетки накапливаются во многих костях, часто образуя множество опухолей и вызывая другие поражения. Когда это происходит, заболевание называется множественной миеломой (ММ).
Поскольку люди, страдающие ММ, имеют паталогически высокое количество идентичных плазмацитов, то они также обладают очень большим количеством однотипных антител. Опухоль, ее продукты и ответ организма-хозяина на них приводят к ряду органных нарушений и к симптомам боли в костях или переломам, почечной недостаточности, восприимчивости к инфекции, анемии, гиперкальциемии и, иногда, патологическому свертыванию крови, неврологическим симптомам и сосудистым проявлениям гипервязкости.
ММ является вторым наиболее часто диагностируемым гематологическим злокачественным заболеванием на Западе с частотой ˜15000 новых случаев в год только в США. К сожалению, в настоящее время ММ считается неизлечимым заболеванием и суммарная продолжительность жизни пациентов с ММ остается, по существу, неизменной и в среднем составляет 3-4 года, несмотря на весьма интенсивные усилия в последние ˜3 десятилетия, направленные на улучшение цитотоксичной активности основного курса химиотерапии данного заболевания. Важно, что средний возраст пациентов, у которых диагностируется ММ, составляет менее 65 лет и у более 1/3 пациентов ММ диагностирована в возрасте менее 55 лет: для данной существенной доли относительно молодых пациентов, страдающих ММ, диагноз ММ означает, даже при отсутствии других сопутствующих заболеваний, высокую вероятность, что их общая продолжительность жизни будет значительно короче, чем средняя продолжительность жизни людей того же возраста, не страдающих ММ.
В последнее время были достигнуты успехи в лечении ММ, а именно сообщалось о противо-ММ активности 2 новых классов противораковых средств, талидомида (и его иммуномодуляторных производных) и ингибиторов протеасом. Несмотря на то, что данные классы средств показали активность в стабилизации пациентов с ММ, у которых отмечалось рецидивирование/резистентность при проведении обычных курсов или курсов с повышенной дозой химиотерапии, значительная часть пациентов с ММ проявляла denovo резистентность к этим новым средствам, а у первоначальных респондентов (даже достигшие длительных полных ремиссий) с течением времени мог возникнуть рецидив. Следовательно, разработка новых классов противо-ММ средств является крайне необходимым для дальнейшего улучшения результатов у пациентов с ММ и, надо надеяться, для достижения высокой вероятности выздоровления после неизлечимой на сегодня неоплазии.
Краткое изложение сущности изобретения
Авторы впервые установили, что аплидин обладает очень сильной активностью в отношении множеств миеломы.
Аплидин (дегидродидемнин В) представляет собой циклический депсипептид, выделенный из средиземноморских оболочечных Aplidium albicans.
Используемый в данном описании термин аплидин также относится к любой фармацевтически приемлемой соли, сложному эфиру, сольвату, гидрату или пролекарственному соединению, которые при введении реципиенту способны предоставить (непосредственно или опосредованно) соединение аплидин. Получение солей и других производных и пролекарств может осуществляться способами, известными в данной области.
Аналоги аплидина включают соединения, раскрытые в WO 02/2596.
Больше информации об аплидине, аналогах аплидина, их использовании, получении композиций на их основе и синтезе может быть найдено в патентных публикациях: WO 91/9485, WO 98/1352, WO 99/42125, WO 01 76616, WO 01/35974, WO 02/30441 и WO 02/2596. Авторы приводят в качестве конкретной ссылки содержание каждого из этих РСТ текстов.
Было показано, что как in vitro, так и в клинической фазе I и II испытаний аплидин может использоваться в качестве противоракового средства. Аплидин обладает несколькими механизмами действия, включая блокаду секреции VEGF, ингибирование синтеза белка и сигнальной трансдукции и индуцирование задержки G1 клеточного цикла. На фазе I/II испытаний ограничивающим дозу фактором является мышечная токсичность с выраженным недостатком в виде тяжелой миелосупрессии.
Было показано, что аплидин обладает высокой активностью in vitro в отношении клеточных линий твердых опухолей человека, особенно крупноклеточного рака легкого и опухолевых клеток рака прямой кишки со значениями IC50, равными 0,18 нМ и 0,45 нМ соответственно (Faircloth et al., 1995, Proceeding 8thECCO Congress,Paris,Abstract no. 122,529; Lobo et al., 1997, Anticancer Res, 17, 333-336). Список Национального института рака (NCI) клеточных линий человека in vitro подтверждает селективность в отношении крупноклеточного рака легкого (NSCLC), меланомы, клеточных линий рака яичника и колоректального рака (Faircloth et al., 1996, Ann Oncol.,7, 34).
На основании первоначальных исследований было сделано предположение, что этот морской депсипептид обладает активностью in vivoв отношениимышиных опухолей, таких как меланома В16 (Faircloth et al., 1995, Proceeding 8thECCO Congress, Paris,Abstract no. 122,529). Кроме того, дополнительные исследования in vivo, проводимые на мышах с трансплантированными опухолями человека, подтверждают активность в отношении рака молочной железы MX-1 и рака прямой кишки CX-1 (Faircloth et al., 1996, Ann Oncol,7, 34). Фаза I испытаний относительно лейкемии у детей находится в стадии осуществления (Jimeno J. et al., 2002, Ann Oncol., 13 (suppl. 5), Abst. 65P). Окончательно было продемонстрировано, что аплидин также проявляет противоопухолевую активность in vivo против подкожно имплантированных человеческих трансплантатов желудка, простаты и лимфомы Беркитта, а также карциномы мочевого пузыря с рецидивом в уретре (Faircloth et al., 1999, Proc.Am. Assoc. Cancer Res.,40, Abstract 2612; Faircloth et al., 1998, Proc. Am. Assoc.Cancer Res.,39, Abstract 227).
Настоящее изобретение относится к применению аплидина и аналогов для лечения множественной миеломы.
Настоящее изобретение также относится к фармацевтической композиции, содержащей аплидин или аналог и фармацевтически приемлемый носитель, среду или разбавитель для использования при лечении множественной миеломы.
Настоящее изобретение дополнительно относится к способу лечения любого млекопитающего, особенно человека, с множественной миеломой, который включает в себя введение пораженному индивиду терапевтически эффективного количества аплидина или аналога.
В еще одном аспекте настоящее изобретение относится к применению аплидина или аналога для получения лекарственного средства для лечения множественной миеломы.
Данное изобретение, кроме того, относится к наборам, содержащим раздельные контейнеры, содержащие фармацевтическую композицию, включающую в себя аплидин или аналог и восстанавливающее средство. Также представлены способы восстановления.
Краткое описание чертежей
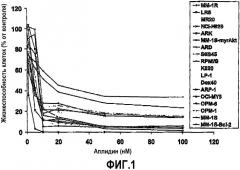
Фиг.1.Результаты МТТ - колориметрических анализов жизнеспособности из списка клеточных линий ММ, обработанных аплидином.
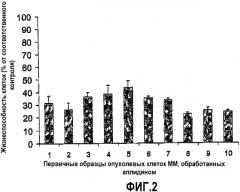
Фиг.2. Активность аплидина (20 нМ в течение 48 часов) in vitro в отношении образцов клеток первичной опухоли ММ, полученных у пациентов с резистентностью ко многим лекарствам.
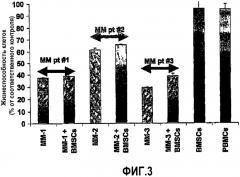
Фиг.3.Совместное культивирование клеток первичной опухоли ММ (выделенных у пациентов с резистентностью ко многим лекарствам) со стромальными клетками костного мозга (BMSC) значительно не усиливает восприимчивость клеток ММ к аплидину.
Фиг.4А.Обработка аплидином (20 нМ, 0-12 часов) клеток первичной опухоли ММ у пациентов с резистентностью ко многим лекарствам подавляет секрецию VEGF.
Фиг.4В. Аплидин (20 нМ, 12 часов) подавляет секрецию VEGF клетками первичной опухоли ММ, BMSC, а также совместно культивируемыми клетками ММ и BMSC.
Фиг.5.Аплидин сенсибилизирует клетки первичной опухоли ММ к доксорубиину.
Фиг.6. Аплидин ингибирует рост клеток множественной миеломы, резистентных к дексаметазону (MM1.R), в культуре также эффективно, как и клеток парентеральной линии (MM1.S).
Фиг.7. Аплидин ингибирует рост клеток ММ, сверхэкспрессирующих Bcl-2.
Подробное описание изобретения
Несмотря на последние достижения в терапии множественной миеломы (ММ) в настоящее время не существует способа лечения, полностью излечивающего данное заболевание, которое является вторым наиболее часто диагностируемым гематологическим злокачественным заболеванием на Западе. Идентификация новых терапевтических средств с противо-ММ активностью, особенно для пациентов с рецидивами или у пациентов с недостаточным ответом на обычные и/или новые схемы лечения, остается крайне желательной.
Авторы обнаружили, что аплидин (АПЛ), новый депсипептид из морских организмов, является очень активным в отношении клеток ММ in vitro. Конкретно, авторы обнаружили, что клинически допустимые концентрации АПЛ были эффективны в отношении большого списка клеточных линий ММ человека, который включал клеточные линии ММ, резистентные к общепринятым противо-ММ средствам (например, дексаметазону, алкилирующим агентам, антрациклинам) или новым (например, талидомиду, иммуномодуляторным производным талидомида, Apo2L/TRAIL), или клеток, сверхэкспрессирующих основные антиапоптозные регуляторы для клеток ММ. Колориметрические анализы жизнеспособности с МТТ показали, что аплидин обладает универсальной активностью в отношении клеточных линий этого списка с IC50 дозами (для подавляющего большинства данных клеточных линий ММ) в диапазоне 10 нМ или менее. Важно, что эта высокая противо-ММ активность наблюдается при концентрациях АПЛ, которые являются клинически достижимыми на фазе 1 клинического испытания данного средства на твердых опухолях. Кроме того, такие значения IC50 сравнимы с активностью in vitro данного средства в большинстве моделей твердых опухолей, чувствительных к АПЛ.
Для дальнейшего подтверждения того, что противо-ММ активность АПЛ in vitro не ограничена только моделями клеточных линий, авторы также тестировали эффект АПЛ против опухолевых клеток первичных ММ, выделенных у пациентов, резистентных к талидомиду или его аналогам и/или ингибированию протеасом. При предварительном тестировании 10 образцов первичных опухолей у пациентов с ММ (>90% чистоты для CD138+ CD38+ опухолевых клеток ММ) авторы наблюдали противо-ММ активность АПЛ in vitro, последовательно согласующуюся с результатами, полученными при тестировании авторского списка клеточных линий. Взятые вместе результаты исследований аплидина in vitro против образцов первичной опухоли ММ и клеточных линий ММ указывают, что данное средство может быть активным в отношении широкого спектра клеток ММ, включая клетки с de novo или приобретенной резистентностью к общепринятым терапиям или другим новым средствам с сильной противо-ММ активностью.
Несмотря на то, что опосредованные цитокинами или клеточной адгезией взаимодействия местного микроокружения костного мозга (КМ) (например, стромальных клеток КМ) защищают клетки ММ при обычных схемах лечения (например, дексаметазона или цитотоксичной химиотерапии) (ссылки), АПЛ способен компенсировать данный защитный эффект в моделях совместных культур клеток ММ со стромальными клетками КМ.
Кроме того, АПЛ, повышая чувствительность клеток ММ к цитотоксичной химиотерапии, индуцирующей клеточную гибель, блокировал секрецию проангиогенных цитокинов (например, VEGF) посредством клеток ММ или стромальных клеток КМ в моделях совместной культуры ex vivo. Это предполагает, что аплидин может сочетаться с общепринятыми методиками цитотоксичной химиотерапии для достижения повышенной противо-ММ активности. Сравнительные анализы схем чувствительности клеток ММ к АПЛ по сравнению с другими противораковыми лекарствами показали, что взаимодействие доза-ответ ММ, обработанных АПЛ, отличается от взаимодействий, связанных с введением лекарств. Это также еще раз доказывает, что противо-ММ свойства АПЛ опосредованы молекулярными механизмами, отличными от механизмов, доступных в настоящее время противо-ММ лекарств, и также позволяет предположить, что АПЛ может быть активен даже против подгрупп ММ, которые могут быть резистентными к другим новым подходам лечения, которые в настоящее время находятся в клинической разработке. Эти данные сочетаются с благоприятным профилем безопасности АПЛ в клинических испытаниях на твердых опухолях.
Для настоящего изобретения, вместо АПЛ, самого аплидина, могут применяться аналоги аплидина, обычно такие соединения как определено в WO 0202596. Примеры соединений по настоящему изобретению включают предпочтительные соединения, приведенные в WO 0202596, и, конкретно, авторы ссылаются на описание патента, где описаны предпочтительные соединения и родственные аспекты, приведенные в WO 0202596. Более предпочтительно эти аналоги являются структурно близкими аплидину и обычно отличаются от аплидина одной аминокислоты в концевой боковой цепи. Отличающаяся аминокислота может находиться в циклической части молекулы или в боковой цепи. Множество примеров таких соединений приведено в WO 0202596, и они являются возможными кандидатами для применения по настоящему изобретению.
Фармацевтические композиции аплидина или аналогов могут быть предназначены для введения любым подходящим путем, например пероральным (включая буккальный или подъязычный), ректальным, назальным, местным (включая буккальный, подъязычный или чрескожный), вагинальным или парентеральным (включая подкожный, внутримышечный, внутривенный или внутрикожный) путем. Такие композиции могут быть получены любым способом, известным в области фармацевтики, например путем объединения активного ингредиента с носителем (носителями) или эксципиентом (эксципиентами).
Примеры фармацевтических композиций, содержащих аплидин или аналоги, включают жидкости (растворы, суспензии или эмульсии) с подходящей композицией для внутривенного введения, и они могут содержать чистое соединение или его сочетание с любым носителем или другими фармакологически активными соединениями. Солюбилизированный аплидин значительно разлагается при нагревании или под действием света, и была разработана лиофилизированная дозированная форма, смотри WO 99/42125, приведенную здесь в качестве ссылки.
Введение аплидина и аналогов или композиций по настоящему изобретению может быть осуществлено посредством внутривенной инфузии. Время инфузии может составлять до 72 часов, более предпочтительно 1-24 часа, либо приблизительно 1, приблизительно 3 или приблизительно 24 часа, наиболее предпочтительно. Короткие периоды инфузии, которые позволяют проводить лечение без пребывания в стационаре ночью, являются особенно предпочтительными. Однако период инфузии может составлять приблизительно 24 часа и даже больше, если требуется. Инфузия может осуществляться в подходящих интервалах по различным схемам, например один раз в неделю, дважды в неделю или более часто в неделю, с повторением каждую неделю, необязательно с интервалами, типично равными 1 неделе.
В предпочтительном способе применения введение проводят циклами. Внутривенную инфузию соединения по данному изобретению осуществляют пациентам первую неделю каждого цикла, пациентам позволяют восстановиться для оставшейся части цикла. Предпочтительная продолжительность каждого цикла составляет 1, 3 или 4 недели; при необходимости можно проводить множественные циклы. В альтернативной методике введения доз соединение по данному изобретению вводят, например, приблизительно в течение 1 часа в течение 5 последовательных дней каждые 3 недели. В качестве альтернативы могут использоваться другие протоколы.
Задержки дозы и/или снижения дозы и регулирования режима проводят по необходимости в зависимости от индивидуальной переносимости пациента или лечений.
Хотя руководство по дозированию приведено выше, точная дозировка соединения может изменяться в соответствии с конкретной готовой формой, способом применения и конкретной областью, хозяином и опухолью, на которую направлено лечение. Следует учитывать другие факторы, такие как возраст, масса тела, пол, режим питания, время введения, скорость выведения, состояние пациента, сочетания с другими лекарствами, чувствительности реакций и тяжесть заболевания. Введение может осуществляться непрерывно или периодически с максимально переносимой дозой. Дополнительное руководство по введению аплидина приведено в WO 01/35974, которая включена здесь в качестве ссылки в полном объеме.
Аплидин и аналоги могут применяться с другими лекарствами в качестве комбинационной терапии для лечения множественной миеломы. Другие лекарства могут составлять часть той же композиции или вводиться в виде отдельной композиции для введения в то же время или в другое время.
Примеры
Статистический анализ
Статистическую значимость исследуют с помощью среднего отклонения в двухфакторном анализе с последующим тестом Дункана. Во всех анализах Р<0,05 считают статистически значимым.
Пример 1
Колориметрический анализ выживаемости с МТТ
Жизнеспособность клеток исследуют, используя колориметрический анализ с использованием бромида 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия (МТТ; Sigma Chemical, St Louis, MO), как описано ранее (Mitsiades C.S. et al. Blood, 2001, 98, 795-804; Mitsiades N. et al. Proc Natl Acad SciUSA, 2002, 99, 14374-14379; Mitsiades N. et al. Blood, 2003, 101, 2377-2380). Кратко, клетки помещают в 48-луночные планшеты при 70-80% слиянии в присутствии 2,5% фетальной сыворотки теленка (FBS) и в присутствии аплидина с конечной концентрацией, равной 0-100 нм, или в контрольной среде ДМСО. В конце каждой обработки клетки инкубируют с 1 мг/мл МТТ в течение 4 часов при 37°С; далее добавляют смесь изопропанола и 1N HCl (23:2, объем/объем) при энергичном пипетировании для растворения кристаллов формазана. Поглощение красителя (А) в жизнеспособных клетках измеряют при 570 нм, с 630 нм в качестве стандартной длины волны. Жизнеспособность клеток оценивают как процент от значения для необработанных контролей. Все эксперименты повторяют, по меньшей мере, 3 раза и каждый раз условия эксперимента повторяют, по меньшей мере, для трех лунок в каждом эксперименте. Приведенные данные представляют собой средние значения ± SD для представительных экспериментов.
Список клеточных линий ММ, резистентных к лекарствам, и первичных опухолевых клеток ММ
Авторы оценивали активность аплидина в списке клеточных линий ММ человека, чувствительных к лекарствам и резистентных к лекарствам, которые включают в себя: дексаметазон (Dex)-чувствительную MM-1S и Dex-резистентную ММ-1R клеточную линию (любезно предоставлены в виде подарка Dr. Steven Rosen, Northwestern University, Chicago, IL); химиочувствительная клеточная линия RPMI-8226/S и их доксорубицин- (Dox6, Dox40), мелфалан (LR5)- и митоксантрон (MR20)-резистентные сублинии (любезно предоставлены в виде академического дара Dr William Dalton, Lee Moffitt Cancer Center, Tampa, FL); клетки OCI-My-5 от Dr H. A. Messner (Ontario Cancer Institute, ON, Canada); клетки S6B45 от Dr T. Kishimoto (Osaka University, Osaka, Japan); клетки ARD, ARK и ARP-1 (любезно предоставлены Dr Nikhil Munshi, Dana-Farber Cancer Institute, Boston, MA); клетки OPM-1, OPM-6, K620 и LP-1 (любезно предоставлены в виде академического дара Dr Leif Bergsagel, Cornell University, New York, NY); а также клетки U226 и NCI-H929, полученные из Американской коллекции типовых культур (Rockville, MD).
Первичные опухолевые клетки ММ выделяют из аспиратов костного мозга (КМ) от 10 пациентов, которые были резистентными по отношению к общепринятым (стероидным и основанным на цитотоксичной химиотерапии) и совсем недавно разработанным противо-ММ средствам (например, талидомиду или ингибиторам протеасом). Аспираты КМ первоначально обрабатывают центрифугированием в градиенте плотности фикола, очищают посредством селекции CD138+ (либо сортировкой активированных клеток посредством проточной цитометрии (FACS) или посредством CD138+ положительной селекцией с иммуномагнитным разделением) с использованием ранее описанных методик (Mitsiades C.S. et al. Blood, 2001, 98, 795-804). Все сортированные образцы опухолевых клеток имеют чистоту >90% для клеток CD38+ CD138+ или CD38+CD45RA. Непосредственно перед обработкой аплидином подтверждают, что все образцы первичных опухолей имеют более чем 95% жизнеспособность с помощью эксклюзионного анализа с трипаном синим. Все клеточные линии ММ и клетки ММ пациентов культивируют в среде RPMI 1640 (Gibco Laboratories, Grand Island, NY), дополненной 10% фетальной сывороткой теленка, обработанной 10% декстрана с активированным углем (FBS; Hyclone, Logan, UT), а также L-глутамином, пенициллином и стрептомицином (Gibco Laboratories).
Результаты: активность аплидина против клеточных линий ММ, резистентных к лекарствам, и образцов первичных опухолей
Авторы настоящего изобретения тестировали активность аплидина in vitro против широкого списка клеточных линий ММ человека, который включал клетки ММ, чувствительные или резистентные к общепринятым (например, дексаметазону, алкилирующим агентам, антрациклинам) или новым (например, талидомиду, иммуномодуляторным производным талидомида, Apo2L/TRAIL) противо-ММ средствам. Колориметрические анализы выживаемости с МТТ (фиг.1) демонстрируют, что аплидин является универсально активным против клеточных линий данного списка с IC50 дозами (для подавляющего большинства данных клеточных линий ММ) в диапазоне 10 нМ или менее (которые соответствуют клинически достижимым концентрациям аплидина на основании фазы 1 опыта испытаний данного средства). Важным является то, что активность аплидина in vitro сравнима с его активностью in vitro в большинстве моделей солидных опухолей, чувствительных к аплидину. Применяя иерархический кластерный анализ и алгоритмы сетевой релевантности, авторы сравнили модели чувствительности клеток ММ к аплидину с другими противораковыми лекарствами и обнаружили, что модель взаимодействия доза-ответ для аплидина отчетливо различается от моделей для других лекарств.
Данное открытие не только дополнительно поддерживает представление о том, что противо-ММ свойства аплидина опосредованы молекулярными механизмами, отличными от механизмов для других лекарств, но также позволяет предположить, что АПЛ может быть активным против различных молекулярных подгрупп данного заболевания.
Результаты: активность аплидина против опухолевых клеток первичных ММ, резистентных к лекарствам
Для дальнейшего подтверждения того, что противо-ММ активность АПЛ in vitro не ограничена только моделями клеточных линий, авторы также тестировали эффект АПЛ в отношении опухолевых клеток первичных ММ, взятых у пациентов, резистентных к талидомиду или его аналогам и/или ингибированию протеасом. При предварительном тестировании 10 образцов первичных опухолей от пациентов с ММ (>90% чистоты для CD138+ CD38+ опухолевых клеток ММ) авторы наблюдают противо-ММ активность АПЛ in vitro, последовательно согласующуюся с результатами, полученными при тестировании авторского списка клеточных линий (фиг.2).
В итоге, результаты исследований аплидина in vitro в отношении образцов первичной опухоли ММ и клеточных линий ММ указывают, что данное средство может быть активным в отношении широкого спектра клеток ММ, включая клетки с de novo или приобретенной резистентностью к общепринятым терапиям или другим исследуемым средствам с сильной противо-ММ активностью.
Пример 2
Стабильные трансфекции Bcl-2 и конституитивно активный Akt
Клетки ММ-18 стабильно трансфицируют плазмидным вектором, кодирующим миристоилированный (конституитивно активный) Akt или Bcl-2 (Upstate Biotechnologies, Lake Placid, NY), или пустыми (нео) векторами и представляют, используя Lipofectamine 2000 (Life Technologies) c последующим культивированием в селекционной среде, содержащей G-418, как прежде описано (Mitsiades C.S. et al. Oncogene 2002, 21, 5673-5683; Mitsiades N. et al Proc Natl Acad Sci USA 2002, 99, 14374-14379).
Результаты: аплидин компенсирует антиапоптозный эффект Bcl-2 или конституитивно активный Akt
Благодаря роли Bcl-2 и каскада PI-3K/Akt в регуляции индуцированного лекарством апоптоза у ММ и других неоплазий авторы также характеризуют активность аплидина на клетках ММ-1S ММ человека, стабильно трансфицированных Bcl-2 или миристоилированного Akt в сравнении с контрольными ММ-1S клетками, трансфицированными пустым вектором. Авторы наблюдают, что клетки, трансфицированные Bcl-2 или myrAkt, не обладают более низкой чувствительностью к аплидину, чем клетки, трансфицированные пустым вектором (фиг.1), позволяя предположить, что сверхэкспрессия Bcl-2 или конституитивная активация Akt и их эффекторы ниже сайта считывания не являются достаточными для компенсации противо-ММ эффекта аплидина.
Пример 3
Анализы одновременного культивирования клеток ММ вместе со стромальными клетками костного мозга (BMSC)
Во время прилипания к BMSC клетки ММ обладают сниженной чувствительностью к обычным схемам лечения, направленным против ММ, таким как дексаметазон или цитотоксические химиотерапевтические средства (Chauhan D. et al. Blood. 1996, 87, 1104-1112). Эта форма лекарственной устойчивости считается основной причиной того, что у пациентов с ММ со временем возникает рецидив, когда они получают лечение, основанное на введении глюкокортикоидов и/или цитотоксической химиотерапии. Напротив, среди недавно разработанных методов лечения ММ противоопухолевая активность в случаях хеморезистентных ММ или резистентных к стероидным препаратам ММ достигается посредством классов лекарств, например ингибиторами протеасом (Hideshima T. et al. Cancer Res. 2001, 61, 3071-3076), которые могут компенсировать защитные эффекты BMSC на клетки ММ. Авторы, следовательно, исследовали может ли аплидин также компенсировать молекулярные последствия взаимодействия BMSC с клетками ММ и достичь противо-ММ активность в этом случае. Авторы, таким образом, осуществили исследования одновременного культивирования in vitro клеток ММ с BMSC, как описано выше: BMSC выращивают в 24-луночных планшетах до прилипания. Последующими промывками средой без сыворотки клетки первичной опухоли (>95% чистоты для CD138+ клеток) выделяют у 3 пациентов с ММ и добавляют к лункам, покрытым BMSC, или контрольным лункам, как описано ранее (Uchiyama H. et al. Blood 1993, 82, 3712-3720; Mitsiades N. et al. Blood 2003, 101, 4055-4062) и инкубируют в течение 48 часов в присутствии или отсутствии аплидина. Проводят поточный цитометрический анализ для обнаружения популяции CD138+ жизнеспособных клеток ММ и эффект аплидина на жизнеспособность клеток ММ выражают как % жизнеспособного количества клеток по сравнению с соответствующими культурами, обработанными средой.
Результаты: аплидин компенсирует защитный эффект стромальных клеток костного мозга (BMSC) на клетки ММ
Предыдущие исследования группы авторов настоящего изобретения и других исследователей показали, что опосредованные цитокинами или клеточной адгезией взаимодействия местного микроокружения костного мозга (КМ) (например, стромальными клетками КМ) могут защищать клетки ММ при общепринятых методах лечения (например, дексаметазоном или цитотоксической химиотерапией) (Chauhan D. et al. Blood, 1996, 87, 1104-1112). Авторы таким образом оценивали противо-ММ эффект аплидина в окружающей совместной культуре клеток ММ с BMSC и наблюдали, используя метод поточной цитометрии, гибель клеток в клеточном компартменте ММ (фиг.3), что взаимодействие ММ-BMSC не усиливает значительно противо-ММ активность аплидина in vitro (при дозах аплидина, которые не воздействуют значительно на выживаемость BMSC).
Пример 4
Количественная оценка секреции VEGF
Адгезия клеток ММ к BMSC индуцирует повышенную секрецию ангиогенных цитокинов, таких как фактор роста эпителия сосудов (VEGF), что, как считают, имеет основное значение для образования новых кровеносных сосудов на участках клеток ММ в среде КМ. Авторы, следовательно, оценивали, может ли аплидин подавлять секрецию VEGF ММ и/или BMSC, используя ранее описанные анализы совместных культур in vitro клеток ММ с BMSC: BMSC выращивают в 24-луночных планшетах до прилипания. Последующими промывками средой без сыворотки клетки первичной опухоли (>95% чистоты для CD138+ клеток) выделяют у 3 пациентов с ММ и добавляют к лункам, покрытым BMSC, или контрольным лункам, как описано ранее (Uchiyama H. et al. Blood 1993, 82, 3712-3720; Mitsiades N. et al. Blood 2003, 101, 4055-4062) и инкубируют в течение 12 часов в присутствии или отсутствии аплидина. Супернатанты собирают и анализируют концентрацию VEGF посредством ферментно-связанного иммуносорбентного анализа (ELISA) с использованием коммерчески доступного набора (набор VEGF ELISA; R&D Systems) в соответствии с инструкциями производителя.
Результаты: аплидин снижает секрецию VEGF ММ/BMSC
Предполагают, что VEGF является возможным медиатором пролиферативных ответов для клеток ММ в микроокружении КМ. VEGF также является ключевым медиатором индуцируемого опухолью образования новых кровеносных сосудов в областях роста опухолевых клеток. Учитывая предварительные сообщения, в которых предполагается, что обработка аплидином клеток острой лейкемии приводит к подавлению секреции VEGF, авторы исследовали, может ли аплидин также подавлять секрецию VEGF клетками ММ и/или BMSC. Действительно, 12-часовая обработка аплидином (20 нМ) способна подавить секрецию VEGF клетками ММ, а также противодействовать увеличению секреции VEGF, которая происходит, когда клетки ММ совместно культивируют с BMSC (фиг.4А и 4В).
Пример 5
Результаты: аплидин сенсибилизирует клетки ММ к цитотоксическим химиотерапевтическим средствам
Применяя колориметрический анализ выживаемости с МТТ, авторы обнаружили, что клетки ММ обладают повышенной чувствительностью к доксорубицину, когда данную обработку сочетают с аплидином. Фиг.5 иллюстрирует пример образца первичной опухоли ММ, сенсибилизированного к доксорубицину (10 нг/мл) посредством аплидина (2 нМ).
Пример 6
Аплидин тестируют против различных клеток, стабильных в культуре. Используемые клетки представляют собой:
- клетки множественной миеломы (ММ1.S);
- линии множественной миеломы, резистентной к дексаметазону (ММ1.R);
- линии множественной миеломы, сверхэкспрессирующие Bcl-2.
Для получения стабильных клеточных линий клетки помещают в 96-луночные планшеты и оставляют расти в течение 24 ч перед добавлением лекарственных средств. Клетки инкубируют с лекарственным средством в течение указанных периодов времени и жизнеспособность клеток измеряют посредством анализов ХТТ или MTS, используя автоматический планшет-ридер.
Результаты данных исследований приведены на фиг.6-7.
1. Применение аплидина для получения лекарственного средства для лечения множественной миеломы.
2. Способ лечения любого млекопитающего, в особенности человека, с множественной миеломой, который включает в себя введение пораженному млекопитающему терапевтически эффективного количества аплидина.
3. Фармацевтическая композиция, содержащая аплидин и фармацевтически приемлемые носитель, среду или разбавитель для использования при лечении множественной миеломы.