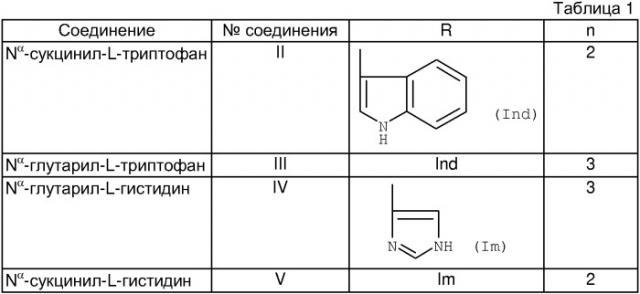
N-ацильные производные аминокислот, их фармацевтически приемлевые соли, фармацевтическая композиция и применение в качестве гиполипидемических средств
Иллюстрации
Показать всеНастоящее изобретение относится к области биоорганической химии и касается N-ацильных производных аминокислот общей формулы I, где n равно 2 или 3, и
R представляет
а также их фармацевтически приемлемых солей и их применения в качестве гиполипидемических средств. Кроме того, объектами изобретения являются фармацевтическая композиция, содержащая указанные соединения в эффективном количестве и способ лечения нарушений липидного обмена, атеросклероза, ишемической болезни сердца и головного мозга, инфаркта миокарда, инсульта. Технический результат - N-ацильные производные аминокислот, обладающие гиполипидемической активностью. 7 н. и 1 з.п. ф-лы, 28 табл., 1 ил.
Реферат
Настоящее изобретение относится к области биоорганической химии и касается N-ацильных производных аминокислот, их фармацевтически приемлемых солей, новых способов их синтеза, а также фармацевтических композиций на их основе и применения в медицине в качестве противоаллергических, противовоспалительных и гиполипидемических средств.
Предшествующий уровень техники
Как известно в настоящее время аллергические заболевания и нарушения липидного обмена весьма распространены вследствие плохой экологической обстановки, изменения структуры питания и образа жизни населения. Поэтому проблема создания лекарственных средств для борьбы с этими патологиями, а также с воспалительными процессами, как правило, сопровождающими аллергию, продолжает оставаться актуальной.
Наиболее распространенной группой противоаллергических препаратов являются блокаторы H1-гистаминовых рецепторов. В настоящее время выделяют 2 поколения антигистаминных препаратов [Машковский М.Д. Лекарственные средства. / Москва: Новая волна. 2005. с.285].
Антигистаминные препараты 1-го поколения проникают через гематоэнцефалический барьер и способны вызывать блокаду Н1-рецепторов клеток центральной нервной системы, что обусловливает их нежелательный седативный эффект. Для достижения выраженного антигистаминного действия необходимы высокие концентрации этих препаратов в крови, что требует назначения их в больших дозах. Отрицательной характеристикой этих препаратов является довольно частое развитие тахифилаксии, влияние на ЦНС, проявляющееся в нарушении координации, головокружении, чувстве вялости, снижении способности концентрировать внимание. Несмотря на вышеуказанное, антигистаминные средства первого поколения по-прежнему применяются, особенно в тех ситуациях, когда необходим очень быстрый эффект от лечения, например при анафилаксии. К антигистаминным препаратам первого поколения относятся димедрол, пипольфен, перитол, супрастин, клемастин, тавегил, фенкарол.
Антигистаминные препараты 2-го поколения получили в последние годы широкое применение в аллергологической практике, поскольку не обладают побочными эффектами, присущими препаратам 1-го поколения. В частности, препараты 2-го поколения не проникают через гематоэнцефалический барьер, не имеют седативного и снотворного эффектов. Для них характерно быстрое и продолжительное антигистаминное действие. К антигистаминным средствам второго поколения относятся кларитин (лоратадин), зиртек (цетиризин), кестин (эбастин). Однако проведенные клинические испытания выявили побочные действия и этих препаратов, обусловленные их взаимодействием с другими лекарственными средствами или нарушением их метаболизма цитохромом P 450. Таким образом, были выявлены потенциально седативные (цетиризин, лоратадин) и потенциально кардиотоксичные (терфенадин, астемизол, эбастин) эффекты у антигистаминных средств 2-го поколения.
В некоторых случаях, например при бронхиальной астме, применяют глюкокортикостероиды, оказывающие мощное антиаллергическое действие. Однако их применение сопровождается системными проявлениями в виде синдрома Иценко-Кушинга, гипертензии, гипергликемии, остеопороза и др. [Машковский М.Д. Лекарственные средства. / Медицина. Москва. 1993. т.1, с.565].
Особое значение в развитии аллергических заболеваний имеет патохимическая стадия аллергических реакций, которая в значительной степени определяется степенью активации клеток-мишеней аллергии 1-го порядка (базофилов и тучных клеток). Их важной особенностью является способность к накоплению и высвобождению под действием стимула (аллергена) биологически активных соединений, в первую очередь, гистамина. При IgE- и/или IgG-опосредованном ответе на антиген именно эти клетки определяют степень выраженности клинической картины немедленной аллергии [Паркер Ч.В. / Медиаторы: высвобождение и функции. // В кн.: Иммунология. Под редакцией У.Пола. - М. - Мир. - 1989. - т.3. - с.170-247; Chakravarty N.K. // In: The mast cell: Its role in health and disease, ed. J Pepys. - 1979. - p.38-46].
Существует группа препаратов (кромолин-натрия, кетотифен, оксатомид), применяемых при бронхиальной астме и бронхоспастических состояниях, в основе действия которых лежит способность тормозить дегрануляцию тучных клеток и задерживать высвобождение из них медиаторных веществ, способствующих развитию бронхоспазма, аллергии и воспаления (брадикинина, гистамина). В качестве побочных эффектов могут наблюдаться раздражение слизистых оболочек, головная боль, отек гортани, кашель, удушье [Машковский М.Д. Лекарственные средства./Москва: Новая волна. 2005. с.297].
Известно, что наиболее частым проявлением атеросклероза является ишемическая болезнь сердца, стоящая на первом месте в ряду причин смертности взрослого населения планеты. Одним из ведущих нарушений при данном заболевании признано нарушение липидного обмена, выражающееся в повышении содержания в плазме крови холестерина, в том числе в составе липопротеинов низкой (ЛПНП) и очень низкой плотности (ЛПОНП), получивших название "атерогенных", с одновременным снижением количества "антиатерогенных" липопротеинов высокой плотности (ЛПВП).
Показано, что изменение содержания и соотношения липидов в плазме отражает их изменение в мембранных структурах паренхиматозных органов. Состав мембран клетки, например микросомальных, прямо зависит от состава рациона экспериментальных животных [Wade A., Harred W. // Feder. Proct.- 1976.- vol. 55.- pp. 2475-2479]. Введение животным холестерина вызывает накопление его в мембранах клеток, уменьшая ее текучесть, что, в свою очередь, приводит к изменению функционального состояния ферментов [Buters J.T.M., Zysset T., Reichen J. // Biochem. Pharmacol.- 1993.- vol. 46.- Iss 6.- pp. 983-991.
Гиполипидемические средства, снижающие содержание холестерина и триглицеридов в крови, могут применяться для лечения и профилактики заболеваний, связанных с нарушениями липидного обмена. Последние характеризуются повышением содержания триглицеридов, общего холестерина (ХС), холестерина в составе липопротеинов низкой и очень низкой плотности (ЛПНП и ЛПОНП) и снижением содержания холестерина в составе липопротеинов высокой плотности при таких заболеваниях, как атеросклероз, ожирение, ишемическая болезнь сердца и головного мозга, инфаркт миокарда, инсульт, и которые служат фактором риска манифестации сахарного диабета и тромбообразования.
Известно клиническое применение так называемых статинов, ингибиторов биосинтеза холестерина. Препараты данной группы в дозах 80 мг/день достаточно эффективны главным образом в отношении понижения уровня общего холестерина в крови, при этом малодоступны, дороги и представляют собой чужеродные для организма химические соединения. Кроме того, их применение может сопровождаться побочными эффектами: изменением функций печени с повышением уровня трансаминаз в крови, диспепсией [Машковский М.Д. Лекарственные средства./Медицина. Москва. 1993. т.1, с.463].
В связи с указанным выше актуальным является поиск новых эффективных противоаллергических и гиполипидемических средств с альтернативными механизмами действия, способных проявлять активность в низких концентрациях и лишенных побочных эффектов. В этом отношении особый интерес представляют соединения, включающие остатки веществ природного происхождения, так как для них можно прогнозировать более низкую токсичность и частоту побочных эффектов.
В публикации международной заявки WO 99/01103 описано противоаллергическое и гиполипидемическое действие N-ацильных производных биогенных аминов, например γ-глутамилгистамина и его ближайшего аналога глутарилгистамина, которые наиболее близки по структуре и действию к заявляемым соединениям. В статье Кржечковская В.В., Желтухина Г.А., Небольсин В.Е. и др. Изучение антианафилактической активности и механизмов действия γ-L-глутамилгистамина. // Патогенез. 2003. Т.1. №2. С. 60-64 показано, что γ-глутамилгистамин обладает выраженной антианафилактической активностью при использовании различных видов животных и способов введения. Полученные результаты свидетельствуют о том, что в тучных клетках животных под действием γ-глутамилгистамина достоверно снижается содержание гистамина и его антиген-стимулированная секреция. В тесте по исследованию влияния глутарилгистамина на выраженность антиген-индуцированного бронхоспазма было показано снижение величины бронхоспазма более чем на 50% по сравнению с контролем. Данный эффект проявлялся как при пероральном, так и интратрахеальном способе его введения в низкой дозе - 50 мкг/кг. Глутарилгистамин обладает способностью снижать проявления пассивной кожной анафилаксии от 34 до 42% и таким образом превосходит по эффективности супрастин, но уступает кларитину. В WO 99/01103 показано, что при введении животным глутарилгистамина в дозах 50 и 500 мкг/кг было продемонстрировано достоверное снижение интенсивности гиперчувствительности замедленного типа. Кроме того, глутарилгистамин в дозах 50 и 500 мкг/кг обладал также некоторой антихолестеринмимической активностью, снижая содержание общего холестерина по сравнению с животными с атерогенной нагрузкой на 5-7%.
Недостатком глутарилгистамина является его сравнительно высокая стоимость и малая доступность исходного сырья для его получения - гистамина. Кроме того, указанное вещество недостаточно эффективно в вышеперечисленных тестах.
С целью расширения арсенала технических средств и создания более эффективного и доступного противоаллергического, противовоспалительного и гиполипидемического средства, авторами изобретения были выявлены некоторые специфические N-ацильные производные аминокислот общей формулы (I), раскрытой в публикации международной заявки WO 99/01103, но конкретно в ней не описанные, не полученные и не охарактеризованные.
Так, под общую формулу (I) вышеуказанной международной заявки подпадают соединения настоящего изобретения Nα-сукцинил-L-триптофан (II), Nα-глутарил-L-триптофан (III), Nα-глутарил-L-гистидин (IV) и Nα-сукцинил-L-гистидин (V). Однако в указанной публикации не приведены ни конкретные структурные формулы данных соединений, ни какие-либо физико-химические характеристики, а также не описаны способы их получения. В публикации международной заявки WO 03/072124 приведены формулы Nα-глутарил-L-триптофана (II), Nα-глутарил-L-гистидина (IV) и Nα-сукцинил-L-гистидина (V), но не описан способ их синтеза и не приведены их физико-химические константы.
Одно из соединений глутарилгистидин упоминается только в виде метилового эфира по С-концу His [Glt-His(OMe)] в патенте США 3963691, в качестве промежуточного соединения в синтезе пептида Glt-His-Trp-Ser-Tyr-Gly-Leu-Arg-Pro-Gly-poly-Lys.
Соединение сукцинилгистидин упоминается в публикации международной заявки WO 93/04690. В этой публикации указано, что добавление свободного имидазола или сукцинилгистидина ускоряет взаимодействие карнозина с дигидроксиацетоном. Методики синтеза сукцинилгистидина и его физико-химические константы не приведены.
Структурная формула сукцинилтриптофана упоминается в заявке США 2005079515. В указанной публикации ни методики синтеза сукцинилтриптофана, ни его физико-химические константы не приведены.
Получение Nα-глутарил-L-гистамина описано в публикации международной заявки WO 99/01103 и представляет собой N-ацилирование биогенного амина глутаровым ангидридом в среде безводного N,N-диметилформамида. Кроме того, в публикации Гершкович А.А., Киберев В.К. // Химический синтез пептидов / Киев, Наукова думка, 1992, 360 описан способ ацилирования аминокислот в водно-органической сильнощелочной среде.
В Sorm F., Pravda Z. Proteins and amino acids. X. Synthesis of two peptide analogs. // Chemicke Listy pro Vedu a Prumysl. 1951. V.45. P.423-425 описан способ синтеза сукцинилтирозина этилового эфира в смеси воды и этилацетата при соотношении (1:1) исходя из хлоргидрата этилового эфира тирозина и глутарового ангидрида в присутствии NaHCO3 для поддержания слабощелочного рН.
Однако ацилирование ангидридами дикарбоновых кислот свободного гистидина в литературе не описано.
Целью настоящего изобретения являются новые эффективные N-ацильные производные аминокислот, обладающие противоаллергическим и гиполипидемическим действием в низких дозах и не проявляющие побочных эффектов, фармацевтические композиции на их основе, их применение в качестве более эффективных противоаллергических, противовоспалительных и гиполипидемических средств, а также новые способы синтеза N-ацильных производных аминокислот.
Авторами изобретения разработан простой и препаративный способ синтеза соединений общей формулы (I), заключающийся в том, что ангидрид глутаровой или янтарной кислоты в виде твердого вещества прибавляют к водному раствору аминокислоты в отсутствие неорганического и органического основания с получением целевого продукта с достаточно высоким выходом 55-60%.
Авторами изобретения также разработан еще один способ синтеза соединений общей формулы (I), в том числе N-ацильных производных гистидина, включающий проведение реакции в двухфазной системе, состоящей из водного раствора гистидина и раствора ангидрида в подходящем органическом растворителе при использовании избытка ацилирующего агента.
Краткое описание изобретения
Настоящее изобретение относится к новым N-ацильным производным аминокислот общей формулы I:
где n равно 2 или 3; и
R представляет
и их фармацевтически приемлемым солям, обладающим противоаллергическим, противовоспалительным и гиполипидемическим действием.
Настоящее изобретение также относится к способу получения N-ацильных производных аминокислот общей формулы I и их солей, включающему прибавление ангидрида глутаровой или янтарной кислоты в виде твердого вещества к водному раствору аминокислоты общей формулы:
или ее соли, где
R представляет
и, необязательно, превращение целевого продукта в его соль.
Настоящее изобретение далее относится к способу получения N-ацильных производных аминокислот общей формулы I и их солей, включающему проведение реакции в двухфазной системе с ангидридом глутаровой или янтарной кислоты в несмешивающемся с водой органическом растворителе с водным раствором аминокислоты общей формулы:
или ее соли, где R представляет
и, необязательно, превращение целевого продукта в его соль.
Настоящее изобретение относится также к применению соединений общей формулы I и их фармацевтически приемлемых солей в качестве противоаллергических, противовоспалительных и гиполипидемических средств.
Далее, настоящее изобретение относится к фармацевтической композиции и средству, обладающим противоаллергическим, антианафилактическим и противовоспалительным и гиполипидемическим действием, содержащим эффективное количество соединения общей формулы I или его фармацевтически приемлемой соли, а также, если требуется фармацевтически приемлемый носитель.
Еще одним объектом изобретения является способ лечения аллергических заболеваний, включающих бронхиальную астму, аллергический ринит, поллинозы, сезонный ринит, круглогодичный ринит, атопический дерматит, псориаз, крапивницу, аллергические (в том числе анафилактические) реакции на укусы насекомых и лекарственные препараты, холодовую аллергию, аллергический конъюктивит, хронических обструктивных заболеваний легких, а именно хронического обструктивного бронхита, эмфиземы, облитерирующего бронхита, муковисцидоза, а также заболеваний, связанных с нарушениями липидного обмена: атеросклероз, ожирение, ишемическая болезнь сердца и головного мозга, инфаркт миокарда, инсульт, включающий введение эффективного количества соединения общей формулы I или его фармацевтически приемлемое соли.
Детальное описание изобретения
Предпочтительные соединения общей формулы I представлены в таблице 1.
Синтез соединений общей формулы I может быть осуществлен двумя способами. Первый способ заключается в постепенном добавлении к водному раствору аминокислоты общей формулы
или ее соли, где R представляет
глутарового или янтарного ангидрида в виде твердого вещества, с последующим выделением целевого продукта ионообменной хроматографией, предпочтительно пропусканием реакционной смеси через колонку с катионитом и последующей кристаллизацией из водного раствора. Полученные кристаллы целевого продукта промывают подходящим растворителем, предпочтительно метанолом. Главное преимущество заявляемого способа состоит в отсутствии щелочи в водном растворе аминокислоты, что препятствует инактивации ангидрида дикарбоновой кислоты в результате гидролиза. Кроме того, остаток имидазола в составе молекулы аминокислоты может осуществлять кислотно-основный аутокатализ реакции ацилирования аминогруппы аминокислоты. Достаточно высокие выходы (55-60%) при использовании заявляемого способа достигаются, в частности, благодаря постепенному прибавлению ангидрида дикарбоновой кислоты, взятого в избытке, и интенсивному перемешиванию реакционной массы.
Соединения общей формулы I также могут быть получены альтернативным способом в двухфазной системе, включающим добавление ангидрида глутаровой или янтарной кислоты в несмешивающемся с водой органическом растворителе к водному раствору аминокислоты общей формулы:
или ее соли, где
R представляет
Данный способ позволяет использовать избыток ацилирующего агента, достичь полного ацилирования α-аминогруппы аминокислоты и выхода целевого продукта около 70%. Для поддержания необходимого рН вместо неорганической щелочи используют органическое основание - пиридин, который не гидролизует ангидрид и, кроме того, как известно, является катализатором ацилирования. Использование пиридина позволяет избежать загрязнения конечного продукта неорганическими солями, которые вместе с продуктом реакции остаются в водном слое. Использованные подходы позволяют упростить отделение целевого продукта от непрореагировавших ангидрида и соответствующей аминокислоты и выделять целевой продукт простой кристаллизацией.
Предпочтительными несмешивающимися с водой органическими растворителями являются бутанол, этилацетат, хлороформ.
Предпочтительными растворителями, используемыми для кристаллизации целевого продукта, являются водно-спиртовые смеси, в частности вода-этанол.
Соединения общей формулы I могут быть также получены в виде фармацевтически приемлемых солей с гидроксидом натрия, гидроксидом калия, карбонатом магния, гидроксидом лития, карбонатом кальция рутинными способами, широко описанными в литературе.
Соединения общей формулы I обладают противоаллергической, противовоспалительной и гиполипидемической активностью и могут быть использованы для лечения аллергических, анафилактических, в том числе сопровождающихся воспалением заболеваний, а также нарушениями липидного обмена.
В частности, соединения настоящего изобретения могут быть использованы для лечения следующих аллергических заболеваний: бронхиальной астмы, аллергического ринита, поллинозов, сезонного ринита, круглогодичного ринита, атопического дерматита, псориаза, крапивницы, аллергических (в том числе анафилактических) реакций на укусы насекомых и лекарственные препараты, холодовой аллергии, аллергического конъюктивита, хронических обструктивных заболеваний легких, а именно хронического обструктивного бронхита, эмфиземы, облитерирующего бронхита, муковисцидоза, а также заболеваний, связанных с нарушениями липидного обмена, таких как атеросклероз, ожирение, ишемическая болезнь сердца и головного мозга, инфаркт миокарда, инсульт.
Соединения настоящего изобретения вводятся в эффективном количестве, которое обеспечивает желаемый терапевтический результат.
Для лечения аллергических заболеваний, включающих бронхиальную астму, аллергический ринит, поллинозы, сезонный ринит, круглогодичный ринит, атопический дерматит, псориаз, крапивницу, аллергические (в том числе анафилактические) реакции на укусы насекомых и лекарственные препараты, холодовую аллергию, аллергический конъюктивит, хронические обструктивные заболевания легких, а именно хронический обструктивный бронхит, эмфизему, облитерирующий бронхит, муковисцидоз, а также заболеваний, связанных с нарушениями липидного обмена, таких как атеросклероз, ожирение, ишемическая болезнь сердца и головного мозга, инфаркт миокарда, инсульт, соединения общей формулы I могут быть введены перорально, местно, парентерально, интраназально, ингаляционно и ректально в виде стандартных лекарственных форм, содержащих нетоксичные фармацевтически приемлемые носители. Используемый в настоящем описании термин «парентеральное введение» означает подкожные, внутривенные, внутримышечные или внутригрудные инъекции или вливания.
Соединения настоящего изобретения могут быть введены пациенту в дозах, составляющих от 0,01 до 10 мг/кг веса тела в день, предпочтительно в дозах от 0,05 до 5 мг/кг один или более раз в день.
При этом следует отметить, что конкретная доза для каждого конкретного пациента будет зависеть от многих факторов, включая активность данного используемого соединения, возраст, вес тела, пол, общее состояние здоровья, и режим питания пациента, время и способ введения лекарственного средства, скорость его выведения из организма, конкретно используемую комбинацию лекарственных средств, а также тяжесть заболевания у данного индивида, подвергаемого лечению.
Фармацевтические композиции по настоящему изобретению содержат соединение общей формулы (I) в количестве, эффективном для достижения желаемого результата, и могут быть введены в виде стандартных лекарственных форм (например, в твердой, полутвердой или жидкой формах), содержащих соединения настоящего изобретения в качестве активного ингредиента в смеси с носителем или наполнителем, пригодным для внутримышечного, внутривенного, перорального, сублингвального, ингаляционного, интраназального и интраректального введения. Активный ингредиент может быть включен в композицию вместе с обычно используемыми нетоксичными фармацевтически приемлемыми носителями, пригодными для изготовления растворов, таблеток, пилюль, капсул, драже, суппозиториев, эмульсий, суспензий, мазей, гелей и любых других лекарственных форм.
В качестве наполнителей могут быть использованы различные вещества, такие как сахариды, например глюкоза, лактоза или сахароза, манит или сорбит, производные целлюлозы и/или фосфаты кальция, например трикальций фосфат или кислый фосфат кальция, в качестве связующего компонента могут быть использованы такие, как крахмальная паста, например кукурузный, пшеничный, рисовый, картофельный крахмал, желатин, трагакант, метилцеллюлоза, гидроксипропилметилцеллюлоза, натрий карбоксиметилцеллюлоза и/или поливинилпирролидон. При необходимости могут быть использованы разрыхляющие агенты, такие как вышеупомянутые крахмалы и карбоксиметилкрахмал, поперечно сшитый поливинилпирролидон, агар или альгиновая кислота или ее соль, такая как альгинат натрия.
Могут быть использованы необязательные добавки, такие как агенты, регулирующие текучесть и смазывающие агенты, такие как диоксид кремния, тальк, стеариновая кислота и ее соли, такие как стеарат магния или стеарат кальция и/или пропиленгликоль.
Ядро драже обычно покрывают слоем, который устойчив к действию желудочного сока. Для этой цели могут быть использованы концентрированные растворы сахаридов, которые могут необязательно содержать аравийскую камедь, тальк, поливинилпирролидон, полиэтиленгликоль и/или диоксид титана, и подходящие органические растворители или их смеси.
В качестве добавок могут быть также использованы стабилизаторы, загустители, красители и отдушки.
В качестве мазевой основы могут быть использованы углеводородные мазевые основы, такие как вазелин белый и желтый (Vaselinum album, Vaselinum flavum), вазелиновое масло (Oleum Vaselini), мазь белая и жидкая (Unguentum album, Unguentum flavum), а в качестве добавок для придания более плотной консистенции, такие как твердый парафин и воск; абсорбтивные мазевые основы, такие как гидрофильный вазелин (Vaselinum hydrophylicum), ланолин (Lanolinum), кольдкрем (Unguentum leniens); мазевые основы, смываемые водой, такие как гидрофильная мазь (Unguentum hydrophylum); водорастворимые мазевые основы, такие как полиэтиленгликолевая мазь (Unguentum Glycolis Polyaethyleni), бентонитовые основы и другие.
В качестве основы для гелей могут быть использованы метилцеллюлоза, натриевая соль карбоксиметилцеллюлозы, оксипропилцеллюлоза, полиэтиленгликоль или полиэтиленоксид, карбопол.
В качестве основы для суппозитория могут быть использованы основы, нерастворимые в воде, такие как масло какао; основы, растворимые в воде или смешиваемые с водой, такие как желатино-глицериновые или полиэтиленоксидные; комбинированные основы - мыльно-глицериновые.
При приготовлении стандартной лекарственной формы количество активного ингредиента, используемого в комбинации с носителем, может варьироваться в зависимости от реципиента, подвергающегося лечению, от конкретного способа введения лекарственного средства.
Так, например, при использовании соединений настоящего изобретения в виде растворов для инъекций содержание активного агента в них составляет 0,01-5%. В качестве разбавителей могут быть использованы 0,9% раствор хлорида натрия, дистиллированная вода, раствор новокаина для инъекций, раствор Рингера, раствор глюкозы, специфические добавки для растворения. При введении в организм соединений настоящего изобретения в виде таблеток и суппозиториев их количество составляет 5,0-500 мг на стандартную лекарственную форму.
Лекарственные формы настоящего изобретения получают по стандартным методикам, таким как, например, процессы смешивания, гранулирования, формирование драже, растворение и лиофилизация.
Следует отметить, что соединения настоящего изобретения проявляют биологическую активность в дозах на два-три порядка ниже по сравнению с известными препаратами, использованными для сравнения, при практически одинаковой эффективности, и для них не выявлено отрицательных побочных действий и не обнаружено противопоказаний к применению. При этом при исследовании токсичности соединений настоящего изобретения в дозе 3000 мг/кг, перорально, не зарегистрировали гибели экспериментальных животных.
Детальное описание соединений настоящего изобретения, их получения и исследования фармакологической активности представлены в нижеследующих примерах, предназначенных для иллюстрации предпочтительных вариантов изобретения и не ограничивающих его объем.
Примеры синтеза N-ацильных производных аминокислот общей формулы (I)
Индивидуальность полученных соединений проверялась методом ТСХ на пластинках "Kieselgel 60 F254" "Merck" (Германия) в системах: метанол (1), хлороформ-метанол-аммиак (4:3:1) (2).
Хроматограммы проявляли хлортолидиновым реактивом, нингидрином, йодом по свечению в УФ-свете.
Углы оптического вращения измеряли на поляриметре "Perkin Elmer 341" (Швеция).
1Н-ЯМР регистрировали на приборе "AMX-400 Bruker" (Германия).
Температуру плавления определяли на приборе "Boetius" (Германия).
Аналитическую ВЭЖХ поводили на приборе "System Gold" ("Beckman", США), скорость элюции 0,25 мл/мин, детекция при 214 нм в условиях: колонка Ultrasphere ODS "Beckman", 2Ч250 мм, 5 мкм, элюция 0,1%-ной TFA, скорость элюирования 0,25 мл/мин (1).
Пример 1
Nα-Глутарил-L-гистидин (IV)
Методика А
К раствору 103,4 г (0,67 моль) гистидина в 400 мл воды добавляют 83,7 г (0,73 моль) глутарового ангидрида. Суспензию перемешивают 1 час, образующийся раствор упаривают до объема 150 мл, оставляют в холодильнике на 16 часов. Выпавший осадок отфильтровывают, промывают 150 мл метанола и сушат. Очистку проводят ионообменной хроматографией на смоле Пьюролайт в Н+ форме, элюируя водой. Фракции, содержащие целевой продукт, объединяют, упаривают до начала выпадения осадка и оставляют на 16 часов при +4°C. Выпавший осадок отфильтровывают, промывают 200 мл метанола и сушат до постоянного веса. Выход 98,8 г (55%). Rf 0,55 (1), 0,37 (2). Тпл = 222-224°С. [α]D 20+15, 95° (C 0,53, вода). [М+Н]+ 270,1. 1H-ЯМР спектр (D2O), δ, м.д.: 1,60-1,80 (м, 2Н, β-CH2-Glt), 2,10-2,25 (м, 4Н, α,γ-CH2-Glt), 2,90-3,25 (м, 2Н, β-CH2-His), 4,40-4,50 (м, 1Н, α-CH-His), 7,15 (с, 1Н, CH-4-Im), 8,50 (с, 1Н, CH-2-Im).
Найдено, %: C 49,18; H 5,91; N 15,42.
C11H15N3O5.
Вычислено, %: C 49,07; H 5,62; N 15,61.
Методика Б
К суспензии 0,3 г (1,93 ммоль) гистидина в 5 мл воды при интенсивном перемешивании добавляют 0,44 г (3,86 ммоль) глутарового ангидрида, растворенного в 2,5 мл этилацетата. Перемешивают 2 часа, пиридином доводят рН до 7 и перемешивают еще 1 час. Этилацетатный и водный слой разделяют. Водный слой дважды промывают эфиром, эфирный слой отбрасывают. Воду удаляют в вакууме, остаток растворяют в минимальном количестве воды и добавляют этанол до начала выпадения белого осадка, оставляют при +4°C на 20 ч. Осадок отделяют фильтрованием, сушат в вакууме. Выход 0,36 г (70%). Rf 0,56 (1), 0,35 (2). Тпл = 219-221°С. [α]D 20 = +15,71° (C 0,56, вода). [М+Н]+ 270,1. 1H-ЯМР спектр (D2O), δ, м.д.: 1,40-1,55 (м, 2Н, β-CH2-Glt), 1,90-2,0 (м, 4H, α, γ-CH2-Glt), 2,7-3,0 (м, 2H, β-CH2-His), 4,20-4,30 (м, 1H, α-CH-His), 6,95 (c, 1H, 4-CH-Im), 8,30 (c, 1H, 2-CH-Im). ВЭЖХ в условиях: (1) - индивидуальный пик, время удерживания 14,55 мин.
Найдено, %: C 49,07; H 5,65; N 15,65.
C11H15N3O5.
Вычислено, %: C 49,07; H 5,62; N 15,61.
Пример 2
Nα-Сукцинил-L-гистидин (V)
Синтез проводили в соответствии с методикой А, приведенной для соединения IV.
Выход 0,08 г (57%).
Rf 0,44 (1), 0,25 (2).
Тпл = 179-181°С
[α]D 20 = +30,71° (C 0,56, вода)
[М]+ 255,2
1H-ЯМР спектр (D2O), δ, м.д.: 2,15-2,30 (м, 4Н, (CH2)2-Suc), 2,75-2,95 (м, 2H, β-CH2-His), 4,25 (уш.с, 1H, α-CH-His), 6,95 (c, 1H, 4-CH-Jm), 8,25 (c, 1H, 2-CH-Jm).
Найдено, %: C 47,09; H 5,04; N 16,40.
C10H13N3O5.
Вычислено, %: C 47,06; H 5,13; N 16,46.
Синтез проводили в соответствии с методикой Б, приведенной для соединения IV.
Выход 0,101 г (67%).
Rf 0,45 (1), 0,27 (2).
Тпл = 178-180°С
[α]D 20 = +30,8° (C 0,57, вода)
ВЭЖХ в условиях (1) - индивидуальный пик, время удерживания 7,54 мин.
Найдено, %: C 47,15; H 5,2; N 16,50.
C10H13N3O5.
Вычислено, %: C 47,06; H 5,13; N 16,46.
Пример 3
Nα-Сукцинил-L-триптофан (II)
Синтез проводили в соответствии с методикой Б, приведенной для соединения IV.
Выход 100,5 мг (67%).
Rf 0,39 (1).
1H-ЯМР спектр (CD3OD), δ, м.д.: 1,87-1,93 (м, 2Н, β-CH2-Glt), 2,25-2,37 (м, 4Н, α,γ-CH2-Glt), 3,37-3,47 (м, 2Н, β-CH2-Trp), 3,81-3,94 (м, 1Н, α-CH-Trp), 6,99 (т, J 7 Гц, 1H, CH-6-Ind), 7,07 (т, J 7 Гц, 1Н, CH-7-Ind), 7,24 (д, J 7 Гц, 1H, CH-2-Ind), 7,35 (д, J 7 Гц, 1H, CH-5-Ind), 7,55 (д, J 7 Гц, 1Н, CH-8-Ind).
[М]+ 304,3
Найдено, %: С 59,07; H 5,65; N 9,35.
C15H16N2O5.
Вычислено, %: С 59,21; H 5,3; N 9,21.
Пример 4
Глутарилтриптофан (III)
Синтез проводили в соответствии с методикой Б, приведенной для соединения IV.
Выход 100,5 мг (67%).
Rf 0.63 (1).
=+21,05° (С 0,6, вода)
1Н-ЯМР спектр (DMSO-d6), δ, м.д.: 2,33-2,41 (м, 4Н, α,β-СН2-Suc), 2,93-3,01 (м, 1Н, β-СН2-Trp), 3.10-3.16 (м, 1Н, β-СН2-Trp), 4,39-4,47 (м, 1Н, α-СН-Trp), 6,93-7,06 (м, 2Н, СН-6,7-Ind), 7,11 (д, J 2,2 Гц, 1Н, CH-2-Ind), 7,30-7,32 (м, 1Н, CH-5-Ind), 7,44-7,47 (м, 1Н, CH-8-Ind). [М]+ 304,3.
ВЭЖХ в условиях: (2) - индивидуальный пик, время удерживания 6,35 мин.
Найдено, %: С 59,07; Н 5,65; N 9,35.
C15H16N2O5.
Вычислено, %: С 59,21; Н 5,3; N 9,21.
Пример 5
Мононатриевая соль Nα-глутарил-L-гистидина (IV)
К раствору 1,0 г (3,7 ммоль) Nα-глутарил-L-гистидина в 15 мл воды при перемешивании и охлаждении до +5°С прибавляют раствор 0,15 г (3,7 ммоль) NaOH в 20 мл воды. Раствор перемешивают 30 мин, растворитель удаляют в вакууме. К маслообразному остатку порциями добавляют бензол, растворитель удаляют в вакууме. Твердый остаток сушат над гранулированной щелочью.
Выход 1.07 г (99.7%).
Тпл=208-210°С
=+16.27° (С 0.58, вода)
Найдено, %: С 45,25; Н 5,51; N 14,52.
C11H15N3O5Na.
Вычислено, %: С 45,21; Н 5,17; N 14,38.
Пример 6
Мононатриевая соль Nα-сукцинил-L-гистидина (V)
Синтез проводили в соответствии с методикой, приведенной для мононатриевой соли Nα-глутарил-L-гистидина (IV) (пример 5).
Выход 1.06 г (97.0%).
=+40.21° (С 0.48, вода)
Найдено, %: С 43,25; Н 4,51; N 15,52.
C10H13N3O5Na.
Вычислено, %: С 43,17; Н 4,71; N 15,10.
Пример 7
Мононатриевая соль Nα-сукцинил-L-триптофана (II)
Синтез проводили в соответствии с методикой, приведенной для мононатриевой соли Nα-глутарил-L-гистидина (IV) (пример 5).
Выход 0.21 г (98.0%).
Тпл=147-150°С
=+22.02° (С 0.39, вода)
Найдено, %: С 55,25; Н 4,51; N 8,32.
C15H16N2O5Na.
Вычислено, %: С 55,05; Н 4,93; N 8,56.
ВЭЖХ в условиях: (2) - индивидуальный пик, время удерживания 6,56 мин.
Пример 8
Мононатриевая соль Nα-глутарил-L-триптофана (III)
Синтез проводили в соответствии с методикой, приведенной для мононатриевой соли Nα-глутарил-L-гистидина (IV) (пример 5).
Выход 0.11 г (99.0%).
Тпл=128-130°С
=+22.06° (С 0.34, метанол)
Найдено, %: С 56,15; Н 5,21; N 8,22.
C16H18N2O5Na.
Вычислено, %: С 56,30; Н 5,32; N 8,21.
ВЭЖХ в условиях: (2) - индивидуальный пик, время удерживания 6,96 мин.
Пример 9
Динатриевая соль Nα-глутарил-L-гистидина (IV)
К раствору 1,0 г (3,7 ммоль) Nα-глутарил-L-гистидина в 15 мл воды при перемешивании и охлаждении до +5°С прибавляют раствор 0,3 г (7,44 ммоль) NaOH в 15 мл воды. Раствор перемешивают 30 мин, растворитель удаляют в вакууме. К маслообразному остатку порциями добавляют бензол, растворитель удаляют в вакууме. Твердый остаток сушат над гранулированной щелочью.
Выход 1.15 г (99.0%).
=+11.92° (С 0.57, вода)
Найдено, %: С 41,25; Н 4,51; N 13,52.
C141H15N3O5Na2.
Вычислено, %: С 41,91; Н 4,80; N 13,3.
Пример 10
Динатриевая соль Nα-сукцинил-L-гистидина (V)
Синтез проводили в соответствии с методикой, приведенной для динатриевой соли Nα-глутарил-L-гистидина (IV) (пример 9).
Выход 1.16 г (99.0%).
Тпл=124-128°С
=+20.06° (С 0.67, вода)
Найдено, %: С 39,55; Н 4,31; N 13,52.
C10H13N3O5Na2.
Вычислено, %: С 39,88; Н 4,35; N 13,95.
Пример 11
Динатриевая соль Nα-сукцинил-L-триптофана (II)
Синтез проводили в соответствии с методикой, приведенной для динатриевой соли Nα-глутарил-L-гистидина (IV) (пример 9).
Выход 0.56 г (97.7%).
Найдено, %: С 51,35; Н 4,31; N 8,22.
C15H16N2O5Na2.
Вычислено, %: С 51,43; Н 4,60; N 8,0.
Пример 12
Ди-натриевая соль Nα-глутарил-L-триптофана (III)
Синтез проводили в соответствии с методикой, приведенной для ди-натриевой соли Nα-глутарил-L-гистидина (IV) (пример 9).
Выход 0.56 г (98.5%).
Найдено, %: С 52,55; Н 4,71; N 7,52.
C16H18N2O5Na2.
Вычислено, %: С 52,75; Н 4,98; N 7,69.
Тесты на биологическую активность
Пример 13
Влияние соединений общей формулы I на аллергические реакции немедленного типа (тест индуцированной овальбумином (ОА) дегрануляции базофилов крови иммунизированной морской свинки in vitro.
Выделение лейкоцитов из крови морской свинки осуществляли по методу Фримеля [Иммунологические методы / Под ред. Г.Фримеля /, М.: Медицина, 1987, стр.222 в нашей модификации].
Для постановки теста использовали морских свинок обоего пола массой 600-800 г. Животны