Способ с использованием выбранных углей для взаимодействия с парами al2o и al при карботермическом получении алюминия
Иллюстрации
Показать всеИзобретение относится к способу улавливания Al из отходящего газа, полученного во время карботермического восстановления алюминия по меньшей мере в одной плавильной печи. В способе отходящий газ направляют в закрытый реактор, в который подают древесный уголь, имеющий пористость от примерно 50 об.% до 85 об.% и средний диаметр пор от примерно 0,05 мкм до примерно 2,0 мкм, при этом древесный уголь контактирует с отходящим газом с образованием, по меньшей мере, Al4C3,который направляют обратно в плавильную печь. Обеспечивается снижение энергозатрат и потерь алюминия. 11 з.п. ф-лы, 4 ил., 2 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к способу получения дополнительного Al4C3, который требуется для выполнения реакций, задействованных при карботермическом получении алюминия, путем взаимодействия паров Al2O и Al в отходящих газах с выбранными углями с образованием Al4C3, который рециркулируют в плавильную печь, где он взаимодействует с образованием алюминия.
Уровень техники
Прямое карботермическое восстановление оксида алюминия было описано в патентах США №2974032 (Grunert et al.) и 6440193 B1 (Johansen et al.). Уже давно было установлено, что суммарная реакция
обычно протекает, или же ее можно заставить протекать, через такие стадии, как:
и
Реакция (2) протекает при температурах ниже 2000°C, а как правило - от 1900°C до 2000°C. Реакция (3), которая представляет собой реакцию получения алюминия, протекает при более высоких температурах, составляющих примерно 2050°C. Очень важно, что в дополнение к веществам, указанным в реакциях (2) и (3), по реакции (4) или (5) образуются летучие вещества, включая газообразный Al, реакция (6), и газообразный субоксид алюминия, т.е. Al2O, и уносятся с отходящим газом. Без улавливания эти летучие вещества будут представлять собой потери в выходе алюминия и потери большого количества энергии, связанной со стадиями восстановления и испарения.
В суммарном процессе карботермического восстановления газообразные Al2O и Al улавливают путем их взаимодействия с углеродом в отдельном реакторе, обычно называемом устройством улавливания паров или реактором улавливания паров, как это описано, например, в патенте США №6530970 B2 (Lindstad). Там углеводородный газ, такой как метан, бутан, ацетилен или т.п., подвергают крекингу, получая тонкодисперсный уголь, который может осаждаться на затравочные частицы угля. Это требует дополнительной стадии крекинга. В зависимости от состава газа и температуры реакции продукт реакции с углем может представлять собой Al4C3, жидкий шлак (Al4C3-Al2O3) или же газы могут просто конденсироваться в виде Al2O3. Желательно получить Al4C3, поскольку он требуется в плавильной печи, а энергия, связанная с Al и Al2O, извлекается (утилизируется) в виде полезной химической энергии и может быть возвращена в плавильную печь. Если в результате конденсации образуются Al2O3 и уголь, то эта энергия выделяется в реакторе улавливания паров в виде тепла и возвращается в процесс лишь в очень незначительном количестве. Если образуется шлак Al4C3-Al2O3, то улавливается весь Al и утилизируется некоторое количество энергии. Однако жидкий продукт может вызвать смыкание частиц в реакторе, затрудняя работу этого реактора улавливания паров.
Другие патенты, относящиеся к карботермическому восстановлению для получения алюминия, включают патенты США №4486229 и 4491472 (Troup et al. и Stevenson et al.). В патенте США №4099959 (Dewing et al.) описаны двойные реакционные зоны, где отходящие газы пропускают через гранулированный углеродный материал и противотоком через свежий уголь или не полностью закоксованный кокс в газоочистителе. В патенте США №4261736 (Dewing et al.) отходящий газ, содержащий пары Al и Al2O, приводят в контакт с порошкообразным углем в псевдоожиженном слое при температуре выше той температуры, при которой образуется липкий оксикарбид алюминия, и при этом нагретый уголь, обогащенный Al4C3, удаляют из псевдоожиженного слоя. При использовании частиц угля, как описано в данном патенте, поверхность каждой частицы угля может, в конечном итоге, стать покрытой продуктами реакции, и скорость реакции, таким образом, будет снижаться, поскольку для продолжения реакции газ должен проникать через слой продукта реакции на каждой частице угля. Таким образом, только часть углерода в частицах угля будет реагировать до Al4C3. Следовательно, эффективность реакции является низкой. Кроме того, пары Al и Al2O выходят вверх из реактора, образуя шлак или конденсируясь, а непрореагировавший углерод поступает в основную плавильную печь, что является нежелательным.
В патенте Канады №1185435 (Sood et al.) упакованный углеродный слой, состоящий из «активированного» угля, полностью или частично превращает возгоняющиеся газообразные Al и Al2O непосредственно в Al4C3. Там «активированным» углем считается любая форма углерода, обладающего большой удельной площадью поверхности и, следовательно, относительно небольшой прочностью, так что полученный в результате продукт реакции Al4C3 сильно не сцепляется с частицами угля и/или является очень пористым и открытым, так что осаждение продукта реакции не приводит к цементации частиц угля друг с другом.
Различные породы древесины, которые могут быть использованы для изготовления древесного угля, очень многообразны, как описано в FAO FORESTRY PAPER 41 (1987) ″Simple Technologies for Charcoal Making″, http://www.fao.org/docre/x5328e/x5328e00.htm, 8/19/2002 и включают в себя: Dakama, эперуа блестящую (Wallaba), Kautaballi, древесину тропических твердолиственных пород, дуб, кокосовый орех и эвкалипт Saligna. В патенте США №6124028 (Nagle) также обсуждаются активированные угли и древесный уголь, а также карбонизированные/углеродполимерные древесные продукты, причем упоминается использование железного дерева, клена, дуба, американской липы, сосны, красного дерева, бальзы и тополя. Эти древесные продукты описываются как пригодные для применения в фурнитуре, тормозных колодках, спортивном оборудовании, трубах, тормозных роторах и т.п.
В карботермическом способе тип используемого угля будет важным для улучшения образования Al4C3 и снижения образования Al2O3 в реакторе улавливания паров. Важными являются скорости реакций и термодинамические соображения. Необходим эффективный способ улавливания Al-содержащих летучих веществ и снижения 25%-ных потерь энергии и 25%-ных потерь алюминия, уносимого в виде газа. Поэтому одна из основных задач настоящего изобретения состоит в предложении более эффективного с точки зрения стоимости и затрат энергии усовершенствованного способа получения алюминия посредством использования нового или намного улучшенного материала в реакторе отходящего газа.
Сущность изобретения
Вышеуказанные потребности удовлетворяются, а вышеуказанные проблемы решаются посредством создания способа улавливания Al-содержащих парообразных веществ (Al и Al2O) из отходящего газа, полученного в по меньшей мере одной плавильной печи во время карботермического восстановления оксида алюминия (глинозема) с образованием алюминия, причем отходящий газ содержит CO, Al (пар) и Al2O (пар), то есть субоксид алюминия, включающий в себя: (a) направление упомянутого отходящего газа в закрытый реактор при повышенной температуре; (b) подачу в этот закрытый реактор древесного угля, имеющего пористость от примерно 50 об.% до 85 об.% и объемную плотность от примерно 0,4 г/см3 до 0,7 г/см3; и (c) контактирование древесного угля с отходящим газом с получением продукта, содержащего Al4C3. Предпочтительно, древесный уголь имеет средний диаметр пор от примерно 0,05 мкм до примерно 2,00 мкм. Используемый здесь термин «субоксид алюминия» предназначен охватывать Al2O и соединения, имеющие отношения алюминия к кислороду, отличные от 2:1. Одним из древесных углей, который особенно пригоден для применения в качестве слоя катализатора в этом реакторе, является эвкалиптовый древесный уголь. Термин «повышенная температура» означает температуру от примерно 1550°C до примерно 2050°C.
Пористость должна составлять, по меньшей мере, примерно 50 об.% для обеспечения возможности изменения объема при превращении угля в Al4C3. Если пористость является слишком низкой, кристаллы Al4C3 будут заполнять или блокировать поры, мешая реагирующему газу контактировать с непрореагировавшим углем. Например, когда используют низкопористый уголь, Al4C3 образуется на внешней поверхности угля, но не внутри. Пористость должна быть относительно однородной, с большинством пор среднего диаметра от примерно 0,05 мкм до примерно 2,00 мкм. Например, металлургический кокс имеет относительно высокую пористость, больше 50 об.%, но одни поры могут достигать 200 мкм или более, а другие - быть меньше чем 0,1 мкм. Поэтому данная пористость связана, прежде всего, с относительно небольшим числом крупных пор. В данном случае поверхности этих крупных пор участвуют в реакции, однако большая часть угля не реагирует, поскольку поры становятся заблокированными. С другой стороны, если пористость составляет более примерно 85 об.%, то слой катализатора не будет обладать достаточной прочностью для того, чтобы использоваться в противоточном реакторе.
Один тип древесного угля выделяется среди разнообразных углеродных продуктов, используемых в металлургических процессах, включая карботермическое улавливание паров при карботермическом восстановлении оксида алюминия, с точки зрения пористости и однородного диаметра пор, давая возможность Al4C3 образовываться глубоко внутри частиц угля, а не забивать поры. В случае данной формы углерода древесного угля реакции продолжаются, поскольку Al-содержащие пары (Al и Al2O) могут диффундировать через поры и взаимодействовать с образованием карбида алюминия, а не образовывать материал, который заполняет поры, вызывая остановку реакции. Такой древесный уголь, предпочтительно, получают из древесины эвкалипта, наиболее предпочтительно - из разновидностей бразильского Eucalyptus Camaldulensis. Данный материал имеет однородный размер пор, как видно на фигуре 4. Данный материал имеет пористость от примерно 55% до 65% и имеет относительно однородное распределение пор/диаметр, как показано в области A на фигуре 4. Он также имеет низкое содержание золы (зольность), составляющее от примерно 2% до 4%.
Использование эвкалипта, как описано выше, увеличивает скорость образования Al4C3 более чем на 100% по сравнению с другими формами угля. Это обеспечивает возможность полной или почти полной (по меньшей мере 85%) конверсии угля в карбид по сравнению с менее чем 30% для других форм угля. Кроме того, если пары Al и Al2O не образуют карбид, то они будут просто конденсироваться, так что большая часть энергии теряется, или образовывать шлак, который будет препятствовать протеканию газа через противоточный реактор, тем самым ухудшая его эксплуатационные характеристики.
Краткое описание чертежей
Изобретение далее описано со ссылкой на сопровождающие неограничивающие чертежи, на которых:
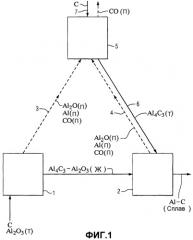
Фиг.1 представляет собой блок-схему, показывающую один пример полной системы способа карботермического восстановления для получения алюминия;
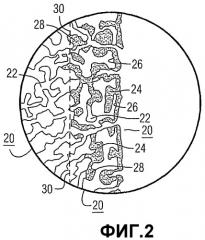
Фиг.2 представляет собой увеличенный идеализированный поперечный разрез с проникновением Al4C3 в поры частиц эвкалиптового древесного угля, используемых в реакторе отходящего газа, показывающий, что поры, по меньшей мере частично, остаются открытыми, обеспечивая возможность продолжения реакции с образованием Al4C3 при взаимодействии газообразного Al2O и угля;
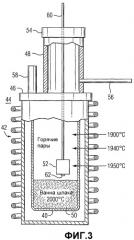
Фиг.3 представляет собой схематическое изображение экспериментального оборудования, используемого для реагирования образцов угля; и
Фиг.4 представляет собой график зависимости удельного объема пор эвкалиптового древесного угля от среднего диаметра пор с полезным диапазоном, показанным в виде области A в границах линий 100, 110, 120 и 130, при этом 80% объема пор имеет диаметры в диапазоне от 0,05 до 2,0 микрометров (мкм) между линиями 100 и 110.
Подробное описание предпочтительных вариантов осуществления
Фиг.1 иллюстрирует один вариант осуществления процесса карботермической реакции для получения металлов, таких как алюминий, улавливания (извлечения) Al и Al2O из отходящих газов в виде Al4C3 и перемещения Al4C3 в плавильную печь. На Фиг.1 потоки газа показаны пунктирными линиями, а потоки твердых веществ и расплавленных веществ показаны сплошными линиями.
На Фиг.1 отходящий газ из карботермической плавильной печи, включающей в себя первую ступень 1 и, возможно, вторую ступень 2, направляют через каналы 3 и 4 в закрытый реактор 5 отходящего газа, работающий при температуре примерно 2000°С. Данный реактор 5 может быть противоточным реактором с подвижным слоем, который способен работать при предельной температуре от примерно 1600°С до примерно 1800°С. Может быть предусмотрен больше чем один такой реактор, например, один - для плавильной печи 1 ступени один, и один - для плавильной печи 2 ступени два. Данный реактор 5 может также быть с псевдоожиженным (кипящим) слоем или рядом псевдоожиженных слоев. Al-содержащие компоненты отходящего газа, входя в реактор 5, реагируют с углем 7 с образованием Al4C3. Данный Al4C3 удаляют из реактора и направляют на ступень 2 карботермической печи через канал 6.
Газ из реактора 5 содержит главным образом СО, возможно - некоторое количество Н2 из летучей части древесного угля, и содержит немного или не содержит совсем Al или Al2O. Отходящий газ из реактора 5 имеет высокую энергетическую ценность (теплоту сгорания) из-за горячего СО и может быть использован для производства электрической энергии в газовой турбине или традиционном паровом котле. Парообразные алюминийсодержащие вещества будут реагировать с образованием карбида или конденсироваться в виде Al2O3 и С. Al4C3 и непрореагировавший уголь подают на вторую ступень карботермической плавильной печи через канал 6. Жидкий сплав Al-C выходит из ступени 2 плавильной печи, как показано на Фиг.1, где (Т) обозначает твердое, (П) обозначает пар и (Ж) обозначает жидкое.
В любом способе карботермического восстановления с целью получения алюминия требуются предельно высокие температуры (>2000°С). При таких температурах СО-содержащему отходящему газу сопутствует большое количество газообразных частиц Al и Al2O. В зависимости от температуры и состава расплава (Al2O3-Al4C3) давления Al2O-Al могут составлять 0,2 атм или выше. Это может составить более 25% произведенного металлического алюминия, выходящего из печи в виде газа. Для того чтобы способ был экономичным, алюминий в этом газе и энергия, израсходованная на получение парообразных частиц Al, должны улавливаться и возвращаться в процесс. Потенциально возможная потеря массы Al очевидна, но в равной степени важно, что большая часть подведенной в процесс энергии тратится на получение этих парообразных частиц. В зависимости от условий эксплуатации потери энергии могут составить 25% или выше.
Чтобы исследовать скорость реакции паров Al2O и Al с углем, необходимо получить данные вещества (частицы) и знать их давления. Одним из путей достижения этого является взаимодействие Al2O3 с углем с образованием карбида алюминия, как происходит в реальном процессе карботермического восстановления. По мере того, как расплав шлака Al2O3 нагревают в присутствии угля на первой стадии или ступени, Al2O3 восстанавливается с образованием Al4C3 при примерно 2000°C.
Al2O3+6C=Al4C3+3CO.
В течение данного процесса образуются пары Al и Al2O. Если предположить установление равновесия, то давление паров можно вычислить исходя из любой соответствующей реакции. Например, для Al2O:
Al2O3+2С=Al2O(г)+2CO.
По мере увеличения температуры выше примерно 2050°C-2080°C образуется металлический Al, содержащий углерод в растворенном виде, по следующей реакции:
Al4C3+Al2O3=6Al+3CO,
и образуются газы Al и Al2O с высокими парциальными давлениями. Затем пары Al и Al2O взаимодействуют с углем в устройстве улавливания паров, образуя Al4C3, шлак Al4C3-Al2O3, или конденсируются в виде C и Al2O3. Расчет давлений паров образовавшихся Al2O и Al, а также продукта их последующей реакции с углем требует знания свободных энергий образования и активностей соответствующих веществ. Al и Al2O взаимодействуют с углем в реакторе улавливания паров по следующим реакциям:
2Al2O+5С=Al4C3+2CO
4Al+3C=Al4C3.
Однако различные формы угля имеют весьма различные свойства, которые, как было обнаружено, содействуют или препятствуют образованию Al4C3. Было обнаружено, что в случае с таким углем, как графит, низкопористый металлургический кокс, нефтяной кокс и имеющий высокую общую, но неоднородную пористость металлургический кокс, Al4C3 не образуется в сколько-нибудь большой степени. Как только карбид начал образовываться, он заполняет поры на поверхности, препятствуя дальнейшей реакции, если пористость составляет менее примерно 50 об.%. Высокопористый металлургический кокс с примерно 51 об.% пор может иметь очень немного очень больших пор и множество более мелких пор. И снова реакция останавливается, когда эти мелкие поры заполнены. Поэтому, в дополнение к высокой пористости, поры должны быть однородными по размеру.
Очень важным является то, что, как было обнаружено, определенные виды древесного угля с пористостью, превышающей 50 об.%, экстенсивно взаимодействовали, образуя Al4C3, при воздействии СО-Al-Al2O газа, полученного в результате восстановления Al2O3 углем. Высокая пористость является существенной, поскольку скорость реакции лимитируется диффузией реакционного газа через поры слоя продукта Al4C3. Если эти поры заполнены или почти заполнены, реакция прекращается. Поскольку имеет место значительное изменение объема при переходе от угля к карбиду, поры, существующие в исходном угле, в качестве упомянутых пор становятся заполненными кристаллами карбида, как было подтверждено анализом с помощью СЭМ. Чтобы обеспечить пространство для этого увеличения объема и поддерживать приемлемую пористость в карбидном слое, пористость исходного угля должна быть очень высокой. Дополнительно, пористость должна быть однородной. Один из испытанных металлургических коксов имел высокую пористость, но экстенсивно (сильно) не реагировал. Этот кокс имел немного больших пор, но большая часть кокса не являлась очень пористой. Площадь, связанная с большими порами, была небольшой по сравнению с древесным углем.
Также очень важно отметить, что другое главное требование к углю, используемому при карботермическом восстановлении, является количество золы. Зола обычно состоит из SiO2, оксидов железа, других оксидов и сульфида железа. Эти оксиды и сульфиды будут восстанавливаться в данном процессе, и кремний, железо и т.д. будут присутствовать в конечном алюминии и их будет трудно удалить. Снова выбранный древесный уголь наилучшим образом соответствует этому требованию; он содержит наименьшее количество золы среди всех испытанных углей за исключением графита, который не взаимодействует и не является применимым на практике источником углерода.
Как показано на Фиг.2, выбранный, обладающий низким содержанием золы и высокой пористостью древесный уголь, предпочтительно - эвкалиптовый древесный уголь 20, показанный в увеличенной идеализированной форме, имеющий пористую матрицу с большим числом взаимосвязанных, относительно однородных пор 22, позволяет отходящим газам собираться и образовывать кристаллы Al4C3 24 не только на поверхности 26 частицы древесного угля, но и глубоко внутри внутренней пористой структуры, как показано в точках 28, вплоть до пограничной зоны 30, показанной пунктирной линией.
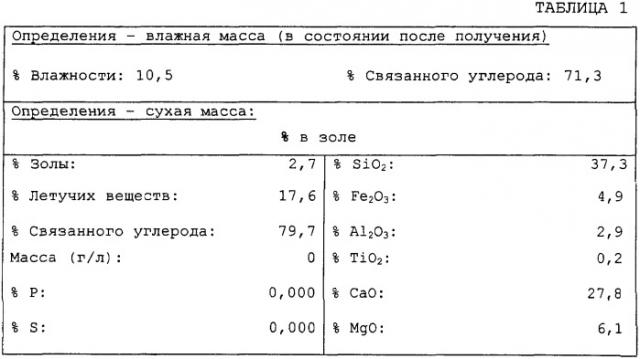
Было обнаружено, что эвкалиптовый древесный уголь, предпочтительно - древесный уголь из бразильского Eucalyptus Camaldulensis, имеет правильные свойства для использования в реакторе отходящего газа. Таблица 1 показывает свойства древесного угля из бразильского эвкалипта.
На Фиг.4 область А между линиями 100 и 110 также предусматривает полезный диапазон пористости для данного древесного угля, где по меньшей мере 80% пор имеют средний диаметр в диапазоне от примерно 0,05 микрометра до примерно 2,0 микрометра.
ПРИМЕРЫ
Одна из основных трудностей при изучении реакции газообразных веществ Al и Al2O с углями состоит в получении этих газов в достаточных количествах. Для достижения этого требуются температуры, превышающие 2000°С. Схематическое изображение специально сконструированного экспериментального оборудования показано на Фиг.3. Расплавы, используемые для получения паров, нагревали в графитовом тигле 40 (внутренний диаметр 17,5 см) в индукционной печи 42 мощностью 65 кВт. Реактор 44, имеющий оптическую смотровую трубу 58, был оборудован плотно прилегающей крышкой 46 и вытяжной трубой 48 также с крышкой 54. Примерно от 5 кг до 7 кг шлака 50 (Al2O3-Al4C3) использовали в качестве расплава для получения паров. Температуру этого расплава и в месте расположения образца 52 измеряли вольфрам-рениевой (5%W-Re)-(26%W-Re) термопарой, которая способна измерять температуры вплоть до 2200°С. Для измерения температуры также использовали два цветовых оптических пирометра. Два данных метода измерения температуры давали одинаковые значения в пределах 10°С. Печь непрерывно продували аргоном для предотвращения избыточного окисления. Состав отходящего газа, взятого через трубку 56 отбора образца отходящего газа, измеряли подключенным масс-спектрометром. Основными веществами были CO, Ar и N2; все Al-содержащие вещества либо прореагировали, либо сконденсировались до попадания в масс-спектрометр.
В качестве образца 52 использовали несколько различных видов углерода, включая древесный уголь, кокс, нефтяной («pet») кокс и графит. Перед реакцией используемые угли были исследованы в сканирующем электронном микроскопе (СЭМ). Дополнительно были измерены объемная плотность, пористость и средний размер пор. Образцы угля были в форме цилиндров, примерно 25 мм в диаметре на 25 мм в высоту. Образец угля прикрепляли к графитовому стержню 60, высверливая отверстие через образец 52 угля, через которое вводили этот стержень, и закрепляли графитовой гайкой 62.
Шлак содержал примерно 4 массовых процента углерода. Данный шлак не был насыщенным по Al4C3 при 2000°С, поэтому Al2O3 взаимодействовал с углеродом, давая Al4C3, CO, Al(г) и Al2O(г). Когда желаемая температура была достигнута и начали образовываться пары, образцы угля опускали в вытяжную трубу и подвергали взаимодействию в течение заданного периода времени, а затем извлекали. Образцы быстро переносили в охлаждающую камеру при комнатной температуре, которую непрерывно продували аргоном для предотвращения избыточного окисления продуктов реакции или угля. Образцы обычно укрепляли и изучали в СЭМ и анализировали фазовый состав. В нескольких случаях образцы подвергали химическому анализу.
В нескольких экспериментах образцы угля сначала выдерживали более высоко в вытяжной трубе, где температура составляла примерно 1930°С. Как будет обсуждаться в следующем разделе, при этой температуре должен образоваться шлак (Al2O3-Al4C3). В некоторых экспериментах образец выдерживали при температуре примерно 1930°С в течение от 10 до 20 минут и затем извлекали с тем, чтобы убедиться в образовании шлака на образце угля. В трех последующих экспериментах после выдерживания образца при температуре примерно 1930°С в течение 15 минут его опускали туда, где температура составляла 1950°С и где должен образовываться карбид. Эти эксперименты проводили для того, чтобы определить, будет ли образовавшийся шлак мешать диффузии Al2O и Al в уголь и, следовательно, препятствовать образованию карбида.
В данных экспериментах шлак (Al4C3-Al2O3), который не был насыщен карбидом, нагревали до температуры примерно 2000-2020°С. Поэтому имела место реакция восстановления. Для предотвращения окисления и для оценки скорости образования СО в экспериментах также использовалась продувка аргоном. Присутствие Ar влияет на реакции, давления Al2O и Al и их последующую реакцию с углем. Образовавшийся в результате газ, как было измерено масс-спектрометром, содержал 50-55% СО и 45-50% Ar. При 2000°С в присутствии Ar и СО в таком соотношении давление пара Al2O и Al составляет 0,12 и 0,042 атмосферы соответственно. Если данная газовая смесь CO-Ar-Al2O-Al затем взаимодействует с углем, Al4C3 будет образовываться в шлаке Al2O3-Al4C3 при 1930°С, а чистый карбид образуется при 1950°С. Равновесные давления Al2O и Al составляют 0,047 и 0,020 соответственно в присутствии карбида при 1950°С. Существуют неопределенности в термодинамике в отношении равновесных давлений и тех температур, при которых образуются фазы. Информация, приведенная выше, представляет собой наилучшие оценки, доступные в настоящее время.
Объемная плотность, пористость и средний размер пор нескольких видов использованных в экспериментах углей приведены ниже в таблице 2.
| ТАБЛИЦА 2 | ||||
| Объемная плотность, г/см3 (куб. см) | Средний диаметр пор, мкм | Открытая пористость, % | Общая пористость, % | |
| Мет.кокс А* | 1,0378 | 0,0205 | 24,15 | 50,5 |
| Нефт.кокс* | 1,6003 | 0,0302 | 24,71 | 23,8 |
| Мет.кокс В* | 0,919 | 0,0907 | 50,35 | 56,2 |
| Эвкалиптовый древесный уголь | 0,5165 | 0,0655 | 61,68 | 75,4 |
| *Сравнительные Примеры |
Приведены результаты двух измерений пористости. Общая пористость рассчитана из объемной плотности. На типичных изображениях в СЭМ древесный уголь имеет большую однородную пористость. И хотя использовали ряд видов угля, эвкалиптовый древесный уголь прореагировал намного лучше. Как будет описано, Al4C3 образовывался на и в древесном угле, в случае с нефтяным коксом имела место некоторая реакция, в то время как в случае с графитом протекали только реакции конденсации на внешней поверхности образца угля.
Присутствующие фазы определяли в первую очередь с использованием СЭМ и химического анализа. Как уже отмечалось, в случае с более плотными углями, такими как графит, возможна только конденсация Al2O3 и образование С по следующим реакциям:
Al2O(г)+2CО=Al2О3+2C
2Al(г)+3CО=Al2О3+3C
Следует отметить, что даже в случае эвкалиптового древесного угля, если образцы не были предварительно эффективно прогреты, происходила только конденсация Al2O3 и С на поверхностях. В случае эвкалиптового древесного угля и, в меньшей степени, в случае нефтяного кокса образовывался Al4C3 или шлак Al4C3-Al2O3 в зависимости от температуры образца. В общем, если температура образца превышала 1950°С, то имела место лишь незначительная реакция или реакция отсутствовала вообще, между 1940°С и 1960°С образовывался Al4C3, при 1910°С-1930°С образовывался шлак, в то время как ниже 1910°С происходила только конденсация. Эти результаты находятся в разумном согласии с термодинамическими предсказаниями.
Изображенные в СЭМ границы раздела карбид-уголь в случае образования карбида в порах и в случае образования шлака показали, что граница раздела между непрореагировавшим углем и фазой карбида хорошо различима и легко идентифицируется. Существовала небольшая область частично прореагировавшего угля. Кристаллы карбида начинают расти внутрь пор угля, и когда образуется первичный Al4C3, пористость значительно сокращается. Жидкий шлак является плотным и, наиболее вероятно, замедляет любую дальнейшую реакцию. Важным является скорость и механизм регулирования скорости образования Al4C3. Наблюдения в СЭМ указывают на то, что существует сокращающаяся непрореагировавшая сердцевина угля, и это предполагает, что скорость лимитируется диффузией Al(г) и Al2O(г) через слой продукта Al4C3.
При использовании графита, металлургического кокса, нефтяного кокса и металлургического кокса (В) Al4C3 не образовывался в какой-либо значительной степени. Как только карбид начинает образовываться, он заполняет поры на поверхности и затрудняет дальнейшую реакцию, если пористость низкая, менее примерно 50 об.%. Металлургический кокс (В) действительно имел высокую пористость. Однако он имел очень немного больших пор и многочисленные маленькие поры. Как только маленькие поры заполнились, реакция вновь останавливается. Поэтому, в дополнение к высокой пористости, сами поры должны быть однородными по размеру, как это имеет место в случае эвкалиптового древесного угля.
Некоторые виды угля, которые могут быть использованы в данном процессе, не могли быть получены в виде отдельных частиц. Поэтому куски угля просто помещали в контейнер. Информация, полученная в результате этих экспериментов, ограничена. Результаты действительно подтвердили, что древесный уголь взаимодействует с образованием карбида, а при более низких температурах происходило образование шлака или простая конденсация Al2О3. Нефтяной и металлургический кокс не взаимодействовали с образованием Al4C3, и по большей части образовывался только конденсат Al2O3.
Экспериментальные результаты показали, какой вид угля следует использовать в реакторе улавливания паров, используемом при карботермическом восстановлении. Древесный уголь, предпочтительно - эвкалиптовый древесный уголь с пористостью свыше 60 об.%, взаимодействовал экстенсивно, образуя Al4C3 при воздействии газа СО-Al-Al2O, полученного в результате восстановления Al2O3. Высокая пористость является существенной, поскольку скорость реакции лимитируется диффузией реакционного газа через поры слоя продукта (Al4C3). Поскольку существует значительное изменение объема при переходе от угля к карбиду поры, существующие в исходном угле, становятся заполненными кристаллами карбида. Это было подтверждено анализом в СЭМ. Чтобы обеспечить пространство для этого увеличения объема и поддерживать приемлемую пористость в карбидном слое, пористость исходного угля должна быть очень высокой, больше, чем 50 об.% или 60 об.%.
В дополнение к этому, пористость должна быть относительно однородной. Один из испытанных металлургических коксов имел высокую пористость, но экстенсивно не взаимодействовал. Этот кокс имел немного больших пор, но большая часть кокса не была очень пористой. Площадь, связанная с большими порами, была небольшой по сравнению с древесным углем.
Другое требование к углю, используемому при карботермическом восстановлении, заключается в количестве золы. Зола обычно состоит из SiO2, оксидов железа, других оксидов и сульфида железа. Эти оксиды и сульфиды будут восстанавливаться в ходе данного процесса, давая железо, которое трудно удалить из продукта. И вновь древесный уголь наилучшим образом соответствует этому требованию; он содержит наименьшее количество золы среди всех испытанных углей, за исключением графита, который не взаимодействует и не является применимым на практике источником углерода. Содержание золы должно составлять примерно 6 мас.% или менее, предпочтительно - примерно от 2 мас.% до 4 мас.%, из расчета на массу связанного углерода в древесном угле.
Описав предпочтительные в настоящее время варианты осуществления изобретения, должно быть понятно, что настоящее изобретение может быть осуществлено иным образом в пределах объема прилагаемой формулы изобретения.
1. Способ улавливания Al-содержащих парообразных веществ из отходящего газа, полученного в по меньшей мере одной плавильной печи во время карботермического восстановления оксида алюминия с образованием алюминия, отличающийся тем, что он включает в себя стадии а) направления отходящего газа, содержащего Al-содержащие парообразные вещества, в закрытый реактор, содержащий древесный уголь, и b) контактирования древесного угля с отходящим газом с получением продукта, содержащего Al4С3, при этом древесный уголь имеет пористость от примерно 50 до 85 об.% и объемную плотность от примерно 0,4 до 0,7 г/см3.
2. Способ по п.1, отличающийся тем, что древесный уголь имеет средний диаметр пор от примерно 0,05 до примерно 2,00 мкм.
3. Способ по п.1, отличающийся тем, что древесный уголь имеет пористость в единицах удельного объема пор в мм3/г в зависимости от диаметра пор в мкм, выбранную из области А на фиг.4.
4. Способ по п.1, отличающийся тем, что древесный уголь представляет собой эвкалиптовый древесный уголь.
5. Способ по п.1, отличающийся тем, что древесный уголь представляет собой Eucalyptus Camalduensis.
6. Способ по п.1, отличающийся тем, что на стадии контактирования имеет место диффузия части образовавшегося Al4C3 в микроструктуру, импрегнирование части пор без формирования плотного покрывающего верхнего слоя шлака.
7. Способ по п.1, отличающийся тем, что древесный уголь имеет содержание золы от примерно 2 до 4% из расчета на массу связанного углерода в этом древесном угле.
8. Способ по п.1, отличающийся тем, что древесный уголь имеет большое число взаимосвязанных пор.
9. Способ по п.1, отличающийся тем, что закрытый реактор представляет собой противоточный реактор с подвижным слоем.
10. Способ по п.1, отличающийся тем, что закрытый реактор представляет собой по меньшей мере один реактор с псевдоожиженным слоем.
11. Способ по п.1, отличающийся тем, что древесный уголь на стадии контактирования обеспечивает по меньшей мере 85%-ю конверсию углерода в карбид в виде Al4C3 в этом древесном угле.
12. Способ по п.1, отличающийся тем, что образовавшийся на стадии контактирования Al4C3 направляют обратно в упомянутую по меньшей мере одну плавильную печь для дальнейшего карботермического восстановления.