Ингибиторы цитозольной фосфолипазы а2
Иллюстрации
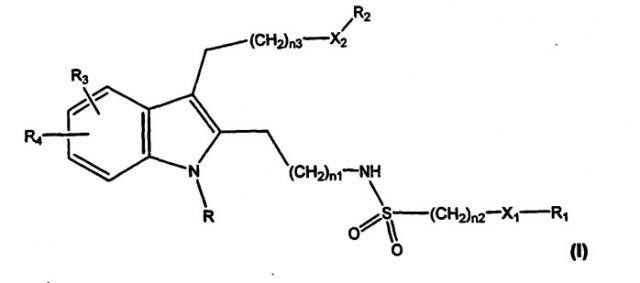
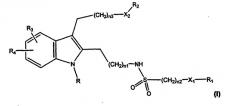
Показать всеИзобретение относится к новым соединениям формулы
где R является -(СН2)n-А, где А
где каждый из В и С независимо представляет собой фенил или фенил, замещенный 1-3 заместителями, независимо выбранными из галогена, -CN, -СНО, -CF3, -OCF3, -ОН, -C1-С6алкила, C1-С6алкокси, -NH2, -N(C1-С6алкил)2, -NH(C1-С6алкил), -NH-С(O)-(C1-С6алкил) и -NO2; или n равно целому числу от 0 до 3; n1 равно целому числу от 1 до 3; n2 равно целому числу от 0 до 4; n3 равно целому числу от 0 до 3; n4 равно целому числу от 0 до 2; X1 выбран из химической связи, -S-, -S(O)2-, -NH-, -NHC(O)- и -С=С-, R1 выбран из C1-С6алкила, C1-С6фторалкила, C3-С6циклоалкила, тетрагидропиранила, CN, -N(C1-С6алкил)2, фенила, пиридинила, пиримидинила, фурила, тиенила, нафтила, морфолинила, триазолила, пиразолила, пиперидинила, пирролидинила, имидазолила, пиперизинила, тиазолидинила, тиоморфолинила, тетразолила, бензоксазолила, имидазолидин-2-тионила, 7,7-диметилбицикло[2.2.1]гептан-2-онила, бензо[1.2.5]оксадиазолила, 2-окса-5-азабицикло[2.2.1]гептила и пирролила, каждый из которых необязательно замещен 1-3 заместителями, независимо выбранными из галогена, -CN, -СНО, -CF3, OCF3, -ОН, -C1-С6алкила, -C1-С6алкокси, -NH2, -N(C1-С6алкил)2, -NH(C1-С6алкил), -NO2, -SO2(C1-С3алкил), -SO2NH2, -SO2N(C1-С3алкил)2, -СООН, -СН2-СООН, пиридила, 2-метилтиазолила, морфолино, 1-хлор-2-метилпропила, фенила (дополнительно необязательно замещенного одним или более галогенами), бензилокси и
Х2 выбран из -O-, -СН2-, -S-, -SO-, -SO2-, -NH- и
R2 представляет собой кольцевую группу, выбранную из фенильной и тиенильной групп, причем кольцевая группа замещена группой формулы -(СН2)n4-CO2Н; и, кроме того, необязательно замещена 1 или 2 дополнительными заместителями, независимо выбранными из галогена, -C1-С6алкила и -C1-С6алкокси; R3 выбран из Н, галогена и -NO2; R4 выбран из Н, галогена и морфолино; или его фармацевтически приемлемая солевая форма. Изобретение также относится к фармацевтической композиции, к способам лечения и к соединениям формулы (А). Технический результат - получение новых биологически активных соединений и фармацевтических композиций на их основе, обладающих ингибирующей активностью по отношению к цитозольной фосфолипазе А2. 7 н. и 38 з.п. ф-лы.
Реферат
Настоящее изобретение относится к химическим ингибиторам активности различных ферментов фосфолипазы, особенно ферментов цитозольной фосфолипазы А2 (cPLA2), более конкретно к ингибиторам ферментов цитозольной фосфолипазы А2 альфа (cPLA2α), и к новым N-бензгидрилиндольным промежуточным соединениям для их получения. Изобретение также относится к способам лечения и облегчения астмы и симптомов астмы и/или симптомов артритических или ревматических расстройств у млекопитающих, включая людей, с использованием данных химических ингибиторов.
Предпосылки изобретения
Лейкотриены и простагландины являются важными медиаторами воспалительных процессов, каждый из которых различными путями вносит вклад в развитие воспалительной реакции. Лейкотриены пополняют клетки воспаления, такие как нейтрофилы, к участку воспаления, содействуют экстравазации данных клеток и стимулируют выделение супероксида и протеазы, которые повреждают ткань. Лейкотриены также играют патофизиологическую роль в гиперчувствительности, которую испытывают астматики [см., например, B. Samuelson et al., Science, 237:1171-76 (1987)]. Простагландины усиливают воспаление, увеличивая поток крови и, следовательно, инфильтрацию лейкоцитов к участкам воспаления. Простагландины также усиливают болевую реакцию, вызванную раздражителем.
Простагландины и лейкотриены являются нестабильными и не сохраняются в клетках, но взамен синтезируются [W.L. Smith, Biochem. J.,259:315-324 (1989)] из арахидоновой кислоты при отклике на воздействие раздражителя. Простагландины продуцируются из арахидоновой кислоты действием ферментов СОХ-1 и СОХ-2. Арахидоновая кислота также является субстратом для особого ферментного пути, ведущего к получению лейкотриенов.
Арахидоновая кислота, которая поступает в данные два различающиеся пути воспалительного процесса, выделяется из sn-2 положения мембранных фосфолипидов ферментами фосфолипазы А2 (в дальнейшем PLA2). Считается, что катализируемая PLA2 реакция представляет лимитирующую скорость стадию в процессе биосинтеза, медиаторами в котором являются липиды, и продукции воспалительных простагландинов и лейкотриенов. Когда фосфолипидный субстрат PLA2 принадлежит к фосфотидилхолиновому классу с эфирным мостиком в sn-1 положении, продуцируемый лизофосфолипид является непосредственным предшественником фактора, активирующего тромбоциты (в дальнейшем называемого PAF), другого мощного медиатора воспаления [S.I. Wasserman, Hospital Practice, 15:49-58 (1988)].
Большинство противовоспалительных терапий фокусируется на предотвращении продукции простагландинов либо лейкотриенов данными различными путями, но не на предотвращении продукции тех и других. Например, ибупрофен, аспирин и индометацин представляют собой нестероидные противовоспалительные препараты, которые подавляют продукцию простагландинов, ингибируя COX-1/COX-2, но не оказывают воздействия на воспалительную продукцию лейкотриенов из арахидоновой кислоты другими путями. Наоборот, зилеутон ингибирует только пути конверсии арахидоновой кислоты в лейкотриены, не оказывая воздействия на продукцию простагландинов. Ни один из данных, широко используемых противовоспалительных препаратов не оказывает воздействия на продукцию PAF.
Поэтому прямое ингибирование активности PLA2 было выдвинуто в качестве полезного механизма для лекарственного препарата, т.е. для того, чтобы препятствовать воспалительной реакции. [См., например, J. Chang et al., Biochem. Pharmacol.36: 2429-2436 (1987).]
Семейство PLA2 ферментов, характеризующееся присутствием сигнала секреции направляемым и, в конечном счете, секретированным из клеток, было упорядочено и структурно определено. Данные секретированные PLA2 имеют молекулярную массу примерно 14 кДа и содержат семь дисульфидных связей, которые необходимы для активности. Данные PLA2 обнаруживаются в огромных количествах в поджелудочной железе млекопитающих, яде пчелы и различных змеиных ядах. [См., например, ссылки 13-15 в цитируемой выше работе J. Chang et al. и E.A. Dennis, Drug Devel. Res., 10:205-220 (1987).] Однако ферменты поджелудочной железы, как считается, имеют пищеварительную функцию и сами по себе не должны играть важную роль в продукции медиаторов воспаления, чья продукция должна строго регулироваться.
Была определена первичная структура первого человеческого не панкреатического PLA2. Данный не панкреатический PLA2 обнаруживается в тромбоцитах, синовиальной жидкости и селезенке и также представляет собой секретируемый фермент. Данный фермент является членом вышеуказанного семейства. [См. J.J. Seilhamer et al., J. Biol.Chem.,264: 5335-5338 (1989), R.M. Kramer et al., J. Biol. Chem., 264:5768-5775 (1989) и A. Kando et al., Biochem. Biophys. Res. Comm.,163: 42-48 (1989).] Однако вызывает сомнение, что данный фермент является важным в синтезе простагландинов, лейкотриенов и PAF, поскольку не панкреатический PLA2 является внеклеточным белком, который было бы трудно регулировать, и следующие ферменты в пути биосинтеза для данных соединений являются внутриклеточными белками. Более того, есть доказательство, что PLA2 регулируется белками протеинкиназы С и G [R. Burch, J. Axelrod, Proc. Natl. Acad. Sci. U.S.A., 84: 6374-6378 (1989)], которые являются цитозольными белками, которые должны действовать на внутриклеточные белки. Было бы невозможно для не панкреатического PLA2 функционировать в цитозоле, поскольку высокий восстановительный потенциал восстановил бы дисульфидные связи и дезактивировал бы фермент.
Мышиный PLA2 был идентифицирован в макрофагной клеточной линии мышей, обозначенной RAW 264.7. Удельная активность, равная 2 моль/мин/мг, устойчивая к восстановительным условиям, как сообщалось, была связана с молекулой, имеющей молекулярную массу примерно 60 кДа. Однако данный белок не был очищен до гомогенности. [См. C.C. Leslie et al., Biochem. Biophys. Acta., 963:476-492 (1988).] Цитируемая выше ссылка включается здесь ссылкой для информации, имеющей отношение в функции ферментов фосфолипазы, в частности PLA2.
Цитозольная фосфолипаза А2 альфа (в дальнейшем ″cPLA2α″) также была идентифицирована и клонирована. [См. патенты США №5322776 и 5354677, которые включаются здесь ссылкой во всей полноте.] Ферменты данных патентов являются внутриклеточными PLA2 ферментами, выделенными из своего природного источника или полученными в очищенной форме иным способом, которые функционируют внутриклеточно, продуцируя арахидоновую кислоту в ответ на воспалительный стимул.
Теперь, когда были идентифицированы несколько ферментов фосфолипазы, было бы желательно идентифицировать химические ингибиторы действия конкретных ферментов фосфолипазы, причем данные ингибиторы можно было бы использовать для лечения воспалительных состояний, в частности, в случаях, когда является желательным подавить продукцию простагландинов, лейкотриенов и PAF. Остается необходимость в идентификации таких противовоспалительных агентов для терапевтического использования при различных болезненных состояниях и промежуточных соединений для их получения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Данное изобретение охватывает соединения формулы (I):
где
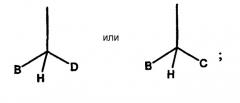
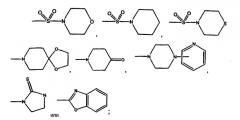
R выбран из формул -(CH2)n-A, -(CH2)n-S-A или -(CH2)n-O-A, где A выбран из групп:
где
D представляет собой С1-С6 низший алкил, С1-С6 низший алкокси, С3-С6циклоалкил, -CF3 или -(CH2)1-3-CF3;
B и C независимо выбраны из фенильной, пиридинильной, пиримидинильной, фуранильной, тиофенильной или пирролильной групп, каждая из которых необязательно замещена 1-3, предпочтительно 1-2 заместителями, независимо выбранными из H, галогена, -CN, -CHO, -CF3, -OCF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил), -NO2, или 5- или 6-членным гетероциклическим или гетероароматическим кольцом, содержащим 1 или 2 гетероатома, которые выбраны из O, N или S; или
n равно целому числу от 0 до 3;
n1 равно целому числу от 1 до 3;
n2 равно целому числу от 0 до 4;
n3 равно целому числу от 0 до 3;
n4 равно целому числу от 0 до 2;
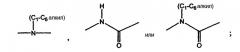
X1 выбран из химической связи, -S-, -O-, -S(O)-, -S(O)2-, -NH-, -NHC(O)-, -C=C-,
R1 является группой, выбранной из С1-С6алкильной, С1-С6фторированной алкильной, С3-С6циклоалкильной, тетрагидропиранильной, камфорильной, адамантильной, CN, -N(С1-С6алкил)2, фенильной, пиридинильной, пиримидинильной, фурильной, тиенильной, нафтильной, морфолинильной, триазолильной, пиразолильной, пиперидинильной, пирролидинильной, имидазолильной, пиперазинильной, тиазолидинильной, тиоморфолинильной, тетразольной, индольной, бензоксазольной, бензофурановой, имидазолидин-2-тионовой, 7,7-диметилбицикло[2.2.1]гептан-2-оновой, бензо[1.2.5]оксадиазольной, 2-окса-5-азабицикло[2.2.1]гептановой, пиперазин-2-оновой или пирролильной групп, каждая из которых необязательно замещена 1-3, предпочтительно 1-2 заместителями, независимо выбранными из H, галогена, -CN, -CHO, -CF3, -OCF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил), -NO2, -SO2(С1-С3алкил), -SO2NH2, -SO2NH(С1-С3алкил), -SO2N(С1-С3алкил)2, -COOH, -CH2-COOH, -CH2-N(С1-С6алкил), -CH2-N(С1-С6алкил)2, -CH2-NH2, пиридина, 2-метилтиазола, морфолино, 1-хлор-2-метилпропила, -С1-С6тиоалкила, фенила (дополнительно необязательно замещенного галогенами), бензилокси, -(С1-С3алкил)C(O)CH3, -(С1-С3алкил)OCH3, -C(O)NH2 или
или
X2 выбран из -O-, -CH2-, -S-, -SO-, -SO2-, -NH-, -C(O)-,
R2 представляет собой кольцевую группу, выбранную из фенильной, пиридинильной, пиримидинильной, фурильной, тиенильной или пирролильной групп, причем кольцевая группа замещена группой формулы -(CH2)n4-CO2H или фармацевтически приемлемым кислотным мимическим или миметическим соединением; и, кроме того, необязательно замещена 1 или 2 дополнительными заместителями, независимо выбранными из H, галогена, -CN, -CHO, -CF3, -OCF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2;
R3 выбран из H, галогена, -CN, -CHO, -CF3, -OCF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2;
R4 выбран из H, галогена, -CN, -CHO, -CF3, -OCF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил), -NO2, -N-C(O)-N(С1-С3алкил)2, -N-C(O)-NH(С1-С3алкил), -N-C(O)-O-(С1-С3алкил)2, -SO2-С1-С6алкила, -S-C3-C6циклоалкила, -S-CH2-C3-C6циклоалкила, -SO2-С3-С6циклоалкила, -SO2-CH2-C3-C6циклоалкила, -C3-C6циклоалкила, -CH2-C3-C6циклоалкила, -O-C3-C6циклоалкила, -O-CH2-C3-C6циклоалкила, фенила, бензила, бензилокси, морфолино или других гетероциклов, таких как пирролидино, пиперидин, пиперазин, фуран, тиофен, имидазол, тетразол, пиразин, пиразолон, пиразол, имидазол, оксазол или изоксазол, причем циклы каждой из данных R4 групп необязательно замещены 1-3 заместителями, выбранными из группы H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил), -NO2, -SO2(С1-С3алкил), -SO2NH(С1-С3алкил), -SO2N(С1-С3алкил)2 или -OCF3;
или их фармацевтически приемлемую солевую форму.
Необходимо понимать, что С1-С6фторированные алкильные группы в определении R1 могут представлять собой любую алкильную группу, содержащую от 1 до 6 атомов углерода с любым количеством заместителей, представляющих собой фтор, включая, но не ограничиваясь этим, -CF3, алкильные цепи, содержащие от 1 до 6 атомов углерода, с концевой трифторметильной группой, -CF2CF3 и т.д.
Сложноэфирные формы настоящих соединений включают фармацевтически приемлемые сложноэфирные формы, известные из уровня техники, включая формы, которые могут преобразоваться в теле животного в ходе обмена веществ в свободную кислотную форму, такую как свободная карбоксильная форма, например, по изобретению можно использовать соответствующие алкильные сложные эфиры, циклоалкильные сложные эфиры, арильные сложные эфиры и их гетероциклические аналоги, где алкильные сложные эфиры, циклоалкильные сложные эфиры и арильные сложные эфиры являются предпочтительными и спиртовые остатки могут иметь дополнительные заместители. Особенно предпочтительными являются C1-C8алкильные сложные эфиры, предпочтительно C1-C6алкильные сложные эфиры, такие как метиловый сложный эфир, этиловый сложный эфир, пропиловый сложный эфир, изопропиловый сложный эфир, бутиловый сложный эфир, изобутиловый сложный эфир, трет-бутиловый сложный эфир, пентиловый сложный эфир, изопентиловый сложный эфир, неопентиловый сложный эфир, гексиловый сложный эфир, циклопропиловый сложный эфир, циклопропилметиловый сложный эфир, циклобутиловый сложный эфир, циклопентиловый сложный эфир, циклогексиловый сложный эфир, или арильные сложные эфиры, такие как фениловый сложный эфир, бензиловый сложный эфир или толиловый сложный эфир.
В определении X1 имеется в виду, что алкенильная мостиковая группа -C=C- обозначает цис- либо транс-ориентацию показанного(ых) соединения(й).
Фармацевтически приемлемые кислотные мимические или миметические соединения, применимые в соединениях по настоящему изобретению, включают соединения, где R2 выбран из группы:
(кислотные мимические соединения показаны присоединенными к фенилу)
где Ra выбран из -CF3, -CH3, фенила или бензила, причем фенильная или бензильная группа необязательно замещена 1-3 группами, выбранными из -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -CF3, галогена, -OH или -COOH; Rb выбран из -CF3, -CH3, -NH2, фенила или бензила, причем фенильная или бензильная группа необязательно замещена 1-3 группами, выбранными из -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -CF3, галогена, -OH или -COOH; и Rc выбран из -CF3 или -С1-С6алкила.
В соединениях по настоящему изобретению, его подгруппах и промежуточных соединениях примерами переменных величин является нижеследующее:
Примером R является -(CH2)n-A, например, где n равно 0 и/или A представляет собой группу
где B и C являются такими, как определено в настоящем описании.
Примерами каждого из B и C независимо являются незамещенные фенильная, пиридинильная, пиримидинильная, фурильная, тиенильная или пирролильная группы, например, где A представляет собой группу:
Примеры R3 выбраны из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) и -NO2.
Примеры R4 выбраны из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил), -NO2, морфолино или других гетероциклов, таких как пирролидино, пиперидин, пиперазин, фуран, тиофен, имидазол, тетразол, пиразин, пиразолон, пиразол, имидазол, оксазол и изоксазол.
В некоторых вариантах осуществления на практике R3 и R4 присоединены к 5 и 6 положению индольного кольца.
Примером n3 является 1.
Примерами X2 являются -O-, -SO2-, -NH- и-CH2-.
Примерами R2 являются группы, выбранные из:
или фармацевтически приемлемые кислотные мимические или миметические соединения, где n4 равно 0-2 и
R8 и R9 независимо выбраны из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2.
Примером n4 является 0.
В некоторых вариантах осуществления на практике -(CH2)n4-CO2H группа, или фармацевтически приемлемые кислотные мимические или миметические соединения находятся в положении 4 фенильного кольца.
Примерами n1 являются целые числа 1 или 2. Примерами n2 являются 0, 1 или 2; например, n1 и n2 оба могут быть равны 1.
X1, например, может быть выбран из химической связи, -S-, -O-, -NH- или -N(C1-C3алкил)-.
Примерами R1 являются С1-С6алкил, С3-С6циклоалкил, фенил, пиридинил, нафтил, тетразол, каждый из которых необязательно замещен 1-3 заместителями, независимо выбранными из H, галогена, -CN, -CHO, -CF3, -OCF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил), -NO2, -SO2(С1-С3алкил), -SO2NH2, -SO2NH(С1-С3алкил), -SO2N(С1-С3алкил)2, -COOH, -CH2-COOH, -CH2-N(С1-С6алкил), -CH2-N(С1-С6алкил)2, -CH2-NH2, -С1-С6тиоалкила, фенила (дополнительно необязательно замещенного галогенами), бензилокси, -(С1-С3алкил)C(O)CH3, -(С1-С3алкил)OCH3 и -C(O)NH2.
В некоторых вариантах осуществления на практике R1 имеет формулу:
где R5, R6 и R6' независимо выбраны из H, галогена, -CN, -CHO, -CF3, -OCF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) и -NO2.
Первая подгруппа соединений по данному изобретению, или их фармацевтических солей, включает соединения вышеуказанной группы, где A представляет собой фрагмент:
и B, C, n, n1, n2, n3, n4, R, X1, X2, R1, R2, R3 и R4 являются такими, как определено выше.
Вторая подгруппа соединений по данному изобретению включает соединения вышеуказанной первой подгруппы, где B и C представляют собой незамещенную фенильную, пиридинильную, пиримидинильную, фурильную, тиенильную или пирролильную группы и R, n, n1, n2, n3, n4, R1, X1, X2, R2, R3 и R4 являются такими, как определено выше.
Третья подгруппа соединений и фармацевтически приемлемых солевых форм по данному изобретению включает соединения вышеуказанной второй подгруппы, где A представляет собой фрагмент:
и n, n1, n2, n3, n4, R, X1, X2, R1, R2, R3 и R4 являются такими, как определено выше.
Четвертая подгруппа соединений по данному изобретению включает соединения формул (II) или (III):
где n1, n2, n3, n4, X1, X2, R1, R2, R3 и R4 являются такими, как определено выше, или их фармацевтически приемлемые соли.
Пятая подгруппа соединений по данному изобретению включает соединения формулы (II) или (III), где n3=1 и n1, n2, n4, X1, X2, R1, R2, R3 и R4 являются такими, как определено выше, или их фармацевтически приемлемые соли.
Шестая подгруппа соединений по данному изобретению включает соединения вышеуказанной пятой подгруппы, где R2 представляет собой фенил, замещенный группой формулы -(CH2)n4-CO2H, и необязательно замещенный 1 или 2 дополнительными заместителями, независимо выбранными из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO; и n1, n2, n4, R1, X1, X2, R2, R3 и R4 являются такими, как определено выше, или их фармацевтически приемлемые соли.
Седьмая подгруппа соединений по данному изобретению включает соединения формул (IV) или (V):
где
n1 представляет собой целое число от 1 до 3;
n2 представляет собой целое число от 1 до 3;
R5, R6 и R6' независимо выбраны из H, галогена, -CN, -CHO, -CF3, -OCF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2;
X1 выбран из химической связи, -S-, -O-, -NH- или -N-(С1-С3алкил)-;
X2 выбран из -O-, SO2 или -CH2-;
R2 представляет собой фрагмент, выбранный из группы:
R8 и R9 независимо выбраны из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2;
n4 равно целому числу от 0 до 2;
R3 выбран из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2; и
R4 выбран из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил), -NO2, морфолино или других гетероциклов, таких как пирролидино, пиперидин, пиперазин, фуран, тиофен, имидазол, тетразол, пиразин, пиразолон, пиразол, имидазол, оксазол или изоксазол;
или их фармацевтически приемлемые солевые формы.
Восьмая подгруппа соединений по данному изобретению включает соединения формул (VI) или (VII):
где
X1 выбран из химической связи, -S-, -O-, -NH- или -N-(С1-С3алкил)-;
X2 выбран из -O-, -SO2- или -CH2-;
R3 выбран из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2; и
R4 выбран из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил), -NO2, морфолино или других гетероциклов, таких как пирролидино, пиперидин, пиперазин, фуран, тиофен, имидазол, тетразол, пиразин, пиразолон, пиразол, имидазол, оксазол или изоксазол;
n1 равно целому числу от 1 до 2;
n2 равно целому числу от 1 до 2;
R5, R6 и R6' независимо выбраны из H, галогена, -CN, -CHO, -CF3, -OCF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2;
R8 и R9 независимо выбраны из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2;
или их фармацевтически приемлемые солевые формы.
Девятая подгруппа соединений по данному изобретению включает соединения формул (VI) или (VII), где n1 равно 1; n2 равно 1 и X1, X2, R3, R4, R5, R6, R6', R8 и R9 являются такими, как определено в вышеуказанной восьмой подгруппе, или их фармацевтически приемлемые солевые формы.
Десятая подгруппа соединений по данному изобретению включает соединения вышеуказанной девятой подгруппы, где X1 представляет собой химическую связь, n1, n2, X2, R3, R4, R5, R6, R6', R8 и R9 являются такими, как определено в вышеуказанной девятой подгруппе, или их фармацевтически приемлемые солевые формы.
Одиннадцатая подгруппа соединений по данному изобретению включает соединения формул (VIII) или (IX)
или
где
n1 равно целому числу от 1 до 3;
n2 равно 0;
X1 представляет собой химическую связь;
n3, n4, X2, R1, R2, R3 и R4 являются такими, как определено выше, или их фармацевтически приемлемые соли.
Двенадцатая подгруппа соединений по данному изобретению включает соединения формул (X) или (XI)
где
n1 равно целому числу от 1 до 3;
n2 равно 0;
R5, R6 и R6' независимо выбраны из H, галогена, -CN, -CHO, -CF3, -OCF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2;
X1 представляет собой химическую связь;
X2 выбран из -O-, -SO2- или -CH2-;
R2 представляет собой фрагмент, выбранный из группы:
R8 и R9 независимо выбраны из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2;
n4 равно целому числу от 0 до 2;
R3 выбран из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2; и
R4 выбран из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил), -NO2, морфолино или других гетероциклов, таких как пирролидино, пиперидин, пиперазин, фуран, тиофен, имидазол, тетразол, пиразин, пиразолон, пиразол, имидазол, оксазол или изоксазол;
или их фармацевтически приемлемые солевые формы.
Тринадцатая подгруппа соединений по данному изобретению включает соединения формул (XII) или (XIII):
где
X1 представляет собой химическую связь;
X2 выбран из -O-, -SO2- или -CH2-;
R3 выбран из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2; и
R4 выбран из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -С1-С6тиоалкила, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил), -NO2, морфолино или других гетероциклов, таких как пирролидино, пиперидин, пиперазин, фуран, тиофен, имидазол, тетразол, пиразин, пиразолон, пиразол, имидазол, оксазол или изоксазол;
n1 равно целому числу от 1 до 2;
n2 равно 0;
R5, R6 и R6' независимо выбраны из H, галогена, -CN, -CHO, -CF3, -OCF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2;
R8 и R9 независимо выбраны из H, галогена, -CN, -CHO, -CF3, -OH, -С1-С6алкила, -С1-С6алкокси, -NH2, -N(С1-С6алкил)2, -NH(С1-С6алкил), -N-C(O)-(С1-С6алкил) или -NO2;
или их фармацевтически приемлемые солевые формы.
Соединения по изобретению можно использовать для лечения, подавления, облегчения или ослабления астмы и астматических состояний. Способы лечения, подавления, облегчения или ослабления астмы и астматических состояний по данному изобретению включают способы лечения приобретенной бронхиальной астмы (также известной как аллергическая астма или атопическая астма), наследственной бронхиальной астмы (также известной как неаллергическая астма или неатопическая бронхиальная астма) или их комбинаций, которые названы смешанной астмой. Состояния пациентов, испытывающих или подвергающихся воздействию приобретенной или аллергической бронхиальной астмы, включают случаи, вызванные или связанные со многими аллергенами, такими как пыльца, споры, трава или сорники, перхоть домашних животных, пыль, клещи и т.д. Ввиду того что аллергены и другие раздражающие вещества сами по себе присутствуют в различные моменты в течение года, эти типы случаев также называют сезонной астмой. В группу приобретенной астмы также входит бронхиальная астма и аллергический аспергиллёз бронхов и легких.
Наследственная бронхиальная астма, которую можно лечить или облегчить настоящими способами, включает случаи, вызванные инфекционными агентами, такими как возбудители простуды и гриппа у взрослых и респираторно-синцитиальный вирус (РСВ), риновирус и вирус гриппа, распространенные у детей. Также включаются астматические состояния, которые могут быть вызваны у некоторых астматиков физическими упражнениями и/или холодным воздухом. Способы являются применимыми для наследственной астмы, связанной с промышленными или профессиональными воздействиями, такими как смог, озон, вредные газы, диоксид серы, оксид азота, испарения, включающие изоцианаты, испарения краски, пластмассы, полиуретанов, лаков и т.д., древесная, растительная пыль или другая органическая пыль и т.д. Способы также применимы для астматических случаев, связанных с пищевыми добавками, консервантами и фармакологическими препаратами. Обычными веществами данных типов являются пищевые красители, такие как тартразин, консерванты, аналогичные бисульфитам и метабисульфитам, и фармакологические препараты, такие как аспирин и нестероидные противовоспалительные препараты (NSAID). Также включаются способы лечения, подавления или облегчения типов астмы, называемых скрытой астмой или кашлевым вариантом астмы.
Описываемые здесь способы также являются применимыми для лечения или облегчения наследственной бронхиальной астмы, связанной с желудочно-пищеводным рефлюксом (GERD), который может стимулировать бронхостеноз. GERD, вместе с удерживаемыми выделениями организма, подавляемым кашлем и воздействием аллергенов и раздражающих веществ в спальне, может внести вклад в астматические состояния и называется ночной астмой или Noctumal астмой. В способах лечения, подавления или облегчения астмы, связанной с GERD, фармацевтически эффективное количество соединений по данному изобретению можно использовать, как описывается здесь, в комбинации с фармацевтически эффективным количеством препарата для лечения GERD. Данные препараты включают, но не ограничиваются ими, ингибиторы протонового насоса, аналогичные таблеткам пантопразола натрия пролонгированного действия торговой марки PROTONIX®, капсулам омепразола пролонгированного действия торговой марки PRILOSEC®, таблеткам ребепразола натрия пролонгированного действия торговой марки ACIPHEX® или капсулам ланзопразола пролонгированного действия торговой марки PREVACID®. Понятно, что фармацевтически эффективные количества данных препаратов включают количества, описанные в обычной медицинской литературе, включая фармацевтически эффективные дозы и способы применения данных препаратов, описанные в 2001 Physicians' Desk Reference (55 Edition), Medical Economics Company, Montvale, New Jersey 07645-1742.
Соединения и способы по данному изобретению применимы для лечения, облегчения, подавления и ослабления артритических состояний у млекопитающих. Способы по данному изобретению включают облегчение, подавление, ослабление и лечение у млекопитающих артритических состояний, включающих, но не ограничивающихся ими, ревматоидный артрит, спондилоартропатию, подагрический артрит, инфекционный артрит, остеоартрит (который включает эрозивный остеоартрит и также известен как артрозоартрит, или дегенеративный артроз, или DJD), системную красную волчанку и болезнь Стилла. Каждый из данных способов включает введение млекопитающему при необходимости такого действия фармацевтически эффективного количества замещенного индола по изобретению, как описывается здесь, или его фармацевтически приемлемой солевой или сложноэфирной формы.
Способы по данному изобретению включают способы лечения артритических состояний, связанных со спондилитом, включая анкилозирующий спондилит, реактивным артритом (синдром Рейтера), псориатическим артритом, артритом, связанным с хроническим воспалительным заболеванием кишечника и связанной со СПИД серонегативной спондилоартропатией.
Данное изобретение также предлагает способы лечения, облегчения или подавления ревматических заболеваний и расстройств. Данные способы применимы для лечения системной красной волчанки, системного склероза и форм склеродермии, полимиозита, дерматомиозита, некротического васкулита и других васкулопатий, гиперчувствительного васкулита (включая болезнь Шенлейна-Геноха), гранулематоз Вегенера, артериита гигантских клеток, слизисто-кожного лимфатического синдрома (болезнь Кавасаки), синдрома Бехчета, криоглобулинемии, юношеского дерматомиозита, синдрома Шегрена, перекрывающихся синдромов (включая смешанную диффузную болезнь соединительной ткани), ревматической полимиалгии, узловатой эритемы, рецидивной полихондрии, тендонита (теносиновита), тенденита двухглавой мышцы, бурсита, бурсита локтевого отростка, адгезивного капсулита плеча (плечелопаточный периартрит), пружинящих пальцев и болезнь Уиппла.
Соединения по данному изобретению также применимы для лечения, облегчения или подавления болезней обмена веществ или эндокринных заболеваний с ревматическими состояниями, включая подагру, псевдоподагру, хондрокальциноз, амилоидоз, цингу, специфические состояния дефицита ферментов (включая болезнь Фабри, алкаптонурию, охроноз, синдром Леша-Нихана и болезнь Гоше), гиперлипопротеинемию (типы II, IIa, IV), синдром Эхлера-Данлоса, синдром Марфана, эластическую псевдоксантому, болезнь Вильсона. Кроме того, настоящими способами можно лечить ревматические состояния, связанные с эндокринными болезнями, такими как сахарный диабет, акромегалия, гиперпаратиреоз, оссифицирующий прогрессирующий миозит, синдром гиперподвижности, врожденный сложный артрогрипоз и заболевания щитовидной железы, такие как струмит, атиреоз и базедова болезнь. Данные способы также можно использовать при ревматических состояниях, связанных с новообразованиями, такими как первичная опухоль (синовиома), метастатические опухоли, множественная миелома, лейкемия и лимфома, пигментный виллонодулярный синовит, остеохондроматоз и другие. В качестве способов по настоящему изобретению также включается облегчение при ревматических состояниях, связанных с невропатическими расстройствами, включающими суставы Шарко, синдром дрожания рук (также известный как синдром побеления пальцев, вызываемого вибрацией, или синдром Рейно), синдромы повторяющегося стресса,