Соединения (2-карбоксиамидо)(3-амино)тиофена
Иллюстрации
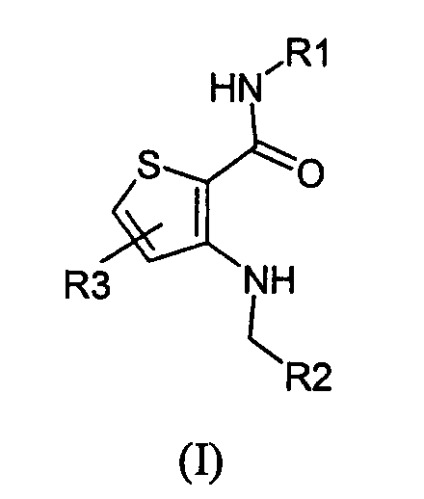
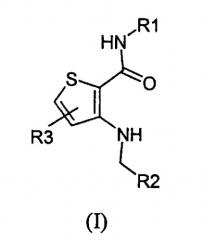
Показать всеНастоящее изобретение относится к соединению общей формулы I
или его фармацевтически приемлемым солям или N-оксидам, где R1 представляет собой R2 представляет собой R3 представляет собой С0-4алкил. Соединения могут быть использованы при разработке противораковых фармацевтических препаратов. 2 н. и 9 з.п. ф-лы, 1 табл.
Реферат
Настоящее изобретение направлено на 2,3-замещенные тиофены. Конкретно, настоящее изобретение направлено на (2-карбоксамидо)(3-амино)тиофены, являющиеся ингибиторами с-Kit протоонкогена (так же известного как Kit, CD-117, рецептор фактора стволовых клеток, рецептор фактора роста тучных клеток).
Полагают, что с-Kit протоонкоген имеет большое значение в эмбриогенезе, меланогенезе, гематопоэзе и патогенезе мастоцитоза, опухолей желудочно-кишечного тракта и других солидных опухолей, а также некоторых лейкемий, включая AML. Соответственно, является желательным разработать новые соединения, которые являются ингибиторами с-Kit рецептора.
Во многих современных способах лечения гиперпролиферативных нарушений (рак) используются соединения, ингибирующие синтез ДНК. По механизму действия такие соединения являются токсичными для клеток, в особенности, быстро делящихся опухолевых клеток. Таким образом, их обширная токсичность может представлять проблему для пациента. Однако были исследованы другие подходы к противораковым средствам, действующим образом отличным, чем ингибирование синтеза ДНК, в попытках усилить селективность противоракового действия и посредством чего снизить неблагоприятные побочные эффекты.
Известно, что клетки могут становиться раковыми вследствие трансформации части их ДНК в онкоген (т.е. ген, который при активации ведет к образованию злокачественных опухолевых клеток). Многие онкогены кодируют белки, являющиеся аберрантными протеин-тирозинкиназами, способными вызывать трансформацию клеток. При отличном пути сверхэкспрессия нормальной протоонкогенной тирозинкиназы может также приводить к пролиферативным нарушениям, иногда приводящим к злокачественному фенотипу. Альтернативно, ко-экспрессия рецептора тирозинкиназы и ее сходного лиганда в пределах такого же клеточного типа также может вести к злокачественной трансформации.
Рецепторные тирозинкиназы представляют собой крупные ферменты, которые встроены в клеточную мембрану и обладают i) внеклеточным доменом связывания для факторов роста, таких как KIT лиганд (так же известный как фактор стволовых клеток (SCF), фактор Стила (SLF) или фактор роста тучных клеток (MGF)), ii) трансмембранным доменом и iii) внутриклеточной частью, которая функционирует как киназа, фосфорилирующая специфичные остатки тирозина в белках. Связывание KIT лиганда с KIT тирозинкиназой приводит к гомодимеризации рецептора, активации активности KIT тирозинкиназы и последующему фосфорилированию различных белковых субстратов, многие из которых являются эффекторами передачи внутриклеточных сигналов. Данные явления могут приводить к увеличенной пролиферации клеток или стимулировать увеличение выживаемости клеток. С некоторыми рецепторными киназами может также происходить гетеродимеризация рецептора.
Известно, что такие киназы зачастую аберрантно экспрессируются при распространенных раковых заболеваниях человека, таких как рак молочной железы, раки головы и шеи, гастроинтестинальный рак, такой как рак толстой кишки, рак прямой кишки и желудка, лейкемия и рак яичника, бронхов, легкого или поджелудочной железы. Экспрессия Kit киназы была документирована при большом разнообразии злокачественных заболеваний человека, таких как мастоцитоз/тучноклеточная лейкемия, стромальные гастроинтестинальные опухоли (GIST), мелкоклеточная карцинома легкого (SCLC), синоназальная естественная Т-киллерклеточная лимфома, рак тестикул (семинома), карцинома щитовидной железы, злокачественная меланома, карцинома яичника, карцинома лимфатических пузырьков, острая миелогенная лейкемия (AML), карцинома молочной железы, детская острая Т-клеточная лимфобластная лейкемия, ангиосаркома, анапластическая крупноклеточная лимфома, карцинома эндометрия и карцинома предстательной железы. Активность киназы у KIT включена в патофизиологию многих из указанных и дополнительных опухолей, включая карциному молочной железы, SCLC, GIST, эмбриональноклеточные опухоли, тучноклеточную лейкемию, нейробластому, AML, меланому и карциному яичника.
Сообщается о некоторых механизмах KIT-активации в опухолевых клетках, включая активирующие мутации, аутокринную и паракринную активацию рецепторной киназы посредством ее лиганда, утрату активности протеин-тирозинфосфатазы и перекрестную активацию других киназ. Полагают, что механизмы трансформации, инициируемые активирующими мутациями, включают образование димера и повышение внутренней активности домена киназы, оба из которых приводят к сложной лиганд-независимой активации киназы и возможно измененной специфичности субстрата. Более тридцати активирующих мутаций Kit белка соотнесено со злокачественными опухолями с высокой степенью малигнизации у человека.
Соответственно, признают, что ингибиторы рецепторных тирозинкиназ пригодны в качестве селективных ингибиторов роста раковых клеток млекопитающих. Например, GleevecTM (так же известный как иматинибмезилат или STI571), 2-фенилпиримидиновый ингибитор тирозинкиназы, который ингибирует активность киназы BCR-ABL гибридного генного продукта, был недавно разрешен U.S. Food and Drug Administration для лечения CML. GleevecTM в дополнение к ингибированию BCR-ABL киназы также ингибирует KIT киназу и PDGF-рецепторную киназу, несмотря на то, что он неэффективен в отношении всех мутантных изоформ KIT киназы. Рост МО7е лейкемических клеток человека, стимулируемый Kit-лигандом, ингибируется GleevecTM, который также индуцирует апоптоз в данных условиях. Напротив, рост МО7е лейкемических клеток человека, стимулируемый GM-CSF, не подвергается влиянию GleevecTM. Далее, в недавних клинических исследованиях, c использованием GleevecTM для лечения пациентов с GIST, заболевания, при котором KIT киназа вовлечена в трансформацию клеток, у многих пациентов отмечают заметное улучшение.
Данные исследования показали, насколько ингибиторы KIT киназы могут лечить опухоли, чей рост зависит от активности KIT киназы. Другие ингибиторы киназ показали даже большую избирательную способность к киназам. Например, соединение 4-анилинохиназолина TarcevaTM с высокой эффективностью ингибирует только рецептор EGF киназы, несмотря на то, что оно может ингибировать передачу сигналов других рецепторных киназ, вероятно, вследствие того факта, что данные рецепторы гетеродимеризируются с EGF рецептором.
Хотя противораковые соединения, такие как описано выше, вносят заметный вклад в данную область, сохраняется потребность в усовершенствовании противораковых фармацевтических препаратов и является желательной разработка новых соединений с улучшенной селективностью и эффективностью или со сниженной токсичностью или побочными эффектами.
В опубликованной заявке № WO00/27820 описаны амидные производные N-арил(тио)антраниловой кислоты. В опубликованной заявке № WO99/32477 и патенте США № 6140351 описаны производные ортоантранилимида. В опубликованной заявке № WO00/27819 описаны амиды антраниловой кислоты. В опубликованных заявках №№ WO02/00651 и WO01/19798 описаны ингибиторы фактора Ха. В опубликованной заявке № WO01/07050 описаны агонисты рецептора ноцицептина ORL-1. В патенте США № 5968965 описаны ингибиторы фарнезил-белка. В опубликованной заявке № WO01/64642 и патенте США №6376515 описаны бензамиды. В опубликованной заявке № WO01/05763 и патенте США №6410561 описаны соединения, активные в отношении мускаринового рецептора. Патент США № 6410561 описывает амидные производные.
В опубликованной заявке № WO02/066470 описаны замещенные производные алкиламина. В опубликованной заявке № WO02/068406 описаны производные замещенных аминов. В опубликованной заявке № WO02/055501 описаны производные замещенных ариламинов.
В патентах США №№ 6207693 и 6316482 и Европейском патенте № ЕР0832061 описаны бензамидные производные, обладающие антагонистической активностью по отношению к вазопрессину.
Настоящее изобретение относится к соединениям, представленным формулой (I):
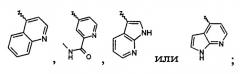
или его фармацевтически приемлемой соли или N-оксиду, где R1 представляет собой
R2 представляет собой
и R3 представляет собой С0-4алкил, полезные для лечения опухолей.
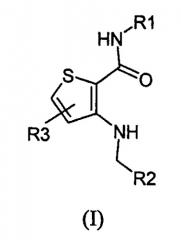
Настоящее изобретение относится к соединению, представленному формулой (I):
или его фармацевтически приемлемой соли или N-оксиду, где R1 представляет собой
R2 представляет собой
и R3 представляет собой С0-4алкил.
В одном варианте, настоящее изобретение направлено на соединение, представленное формулой (I), или его фармацевтически приемлемую соль или N-оксид, где R2 представляет собой ; и другие переменные являются такими, как описано выше для формулы (I).
В одной из форм выполнения данного варианта настоящее изобретение направлено на соединение, представленное формулой (I), или его фармацевтически приемлемую соль или N-оксид, где R2 представляет собой ; R3 представляет собой водород; и другие переменные являются такими, как описано выше для формулы (I).
Во втором варианте, настоящее изобретение направлено на соединение, представленное формулой (I), или его фармацевтически приемлемую соль или N-оксид, где R2 представляет собой ; R3 представляет собой С0-4алкил, и другие переменные являются такими, как описано для формулы (I).
В одной из форм воплощения второго варианта настоящее изобретение направлено на соединение, представленное формулой (I), или его фармацевтически приемлемую соль или N-оксид, где R2 представляет собой ; R3 представляет собой водород; и другие переменные являются такими, как описано выше для формулы (I).
В третьем варианте, настоящее изобретение направлено на соединение, представленное формулой (I), или его фармацевтически приемлемую соль или N-оксид, где R2 представляет собой ; R3 представляет собой С0-4алкил, и другие переменные являются такими, как описано выше для формулы (I).
В одной из форм воплощения третьего варианта настоящее изобретение направлено на соединение, представленное формулой (I), или его фармацевтически приемлемую соль или N-оксид, где R2 представляет собой ; R3 представляет собой водород; и другие переменные являются такими, как описано выше для формулы (I).
В четвертом варианте, настоящее изобретение направлено на соединение, представленное формулой (I), или его фармацевтически приемлемую соль или N-оксид, где R2 представляет собой ; R3 представляет собой С0-4алкил, и другие переменные являются такими, как описано выше для формулы (I).
Настоящее изобретение также направлено на способ лечения гиперпролиферативных нарушений, включающих рак молочной железы, рак головы или рак шеи, гастроинтестинальный рак, лейкемию, рак яичников, бронхов, легких и поджелудочной железы, синоназальную лимфому природных киллеров/Т-клеток, рак тестикул (семиному), карциному щитовидной железы, злокачественную меланому, карциному лимфатических желез, ангиосаркому, анапластическую крупноклеточную лимфому, карциному эндометрия или карциному предстательной железы, посредством введения эффективного количества соединения, представленного формулой (II) или его фармацевтически приемлемой соли:
где R11 представляет собой арил, С3-6циклоалкил или гетероциклил, каждый из которых необязательно замещен 1-6 независимыми атомами галогена; гидрокси; нитро; амино; ацил; замещенный ацил; ацилС1-6алкилсульфинил; ацилС1-6алкилсульфонил; ацилокси; С1-6алкиламиноС1-6алкилкарбамоилокси; арил; циано; гетероциклил; С2-6алкенил, необязательно замещенный ацилом, замещенным ацилом, арилом или ацилзамещенным арилом; С2-6алкинил, необязательно замещенный амино, ациламино или замещенной ациламино; С1-6алкил, необязательно замещенный атомом галогена, амино, С1-6алкиламино, ациламино, замещенной ациламино, гидрокси, ацилокси, ацилС1-6алканоилокси, ацилом, замещенным ацилом, ацилС1-6алкоксимино, арилом или ацилзамещенным арилом; С1-6алкилтио, необязательно замещенный ацилом или замещенным ацилом; алкокси, необязательно замещенный арилом, замещенным арилом, гидрокси, ацилокси, амино, низшим алкиламино, защищенной аминогруппой, гетероциклилом, ацилзамещенным пиридилом, замещенным ацилзамещенным пиридилом, атомом галогена, ацилС1-6алкиламино, N-защищенным ацилС1-6алкиламино, N-ацилС1-6алкил-N-низшим алкиламино, ацилом, замещенным ацилом, ациламино, замещенным ациламино, С1-6алкилгидразинокарбониламино, гидроксиимино, ацилС1-6алкоксиимино, замещенным ацилС1-6алкоксиимино, ацилС1-6алкокси, гуанидино или N-защищенным гуанидино; или С2-6алкенилокси, необязательно замещенный ацилом или замещенными ацилом заместителями;
R21 представляет собой водород; низший алкил, необязательно замещенный гидрокси, арилом или ацилом; или цикло(низший)алкил;
R31 представляет собой водород; галоген; гидрокси; ацилокси; замещенный ацилокси; С1-6алкил, необязательно замещенный гидрокси или С1-6алкокси; С1-6алкокси, необязательно замещенный арилом, амино, защищенной аминогруппой, ацилом, гидрокси, циано или С1-6алкилтио; нитро; амино; ацил; замещенный ацил; или С3-6циклоалкилокси;
R41 представляет собой гидрокси; галоген; нитро; амино; защищенный амино; С1-6алкиламино; ацилокси; аминоС1-6алкиламино; N-защищенный аминоС1-6алкиламино; С1-6алкокси, необязательно замещенный гидрокси, арилом, замещенным арилом, ацилом, замещенным ацилом, амино, С1-6алкиламино, ациламино, замещенным ациламино, защищенной аминогруппой, гетероциклилом или гуанидино; С1-6алкилтио, необязательно замещенный ацилом, замещенным ацилом, амино, С1-6алкиламино, ациламино, замещенным ациламино, защищенной аминогруппой, гетероциклилом, гидрокси, С1-6алкилсульфонилокси, арилсульфонилокси, арС1-6алкокси или замещенным арС1-6алкокси; С1-6алкил, замещенный ацилом, замещенным ацилом, амино, низшим алкиламино, ациламино, замещенным ациламино, защищенной аминогруппой, гетероциклилом, гидрокси, С1-6алкилсульфонилокси или арилсульфонилокси; С2-6алкенил, необязательно замещенный ацилом; С2-6алкинил, необязательно замещенный гидрокси, амино, защищенной аминогруппой, С1-6алкилсульфонилокси или арилсульфонилокси; аминоС1-6алкилсульфонил; N-защищенный аминоС1-6алкилсульфонил; С1-6алкиламиносульфонил; гетероциклилсульфонил; аминоС1-6алкилсульфинил; N-защищенный аминоС1-6алкилсульфинил; пиперидилокси; или N-защищенный пиперидилокси;
R51 представляет собой водород, С1-6алкил, С1-6алкокси или галоген;
А представляет собой простую связь, О или NH;
Е представляет собой С1-6алкилен, С2-6алкилен,
или Е представляет собой группу формулы -G-J-, в которой
G представляет собой С1-6алкилен и
J представляет собой О или , где R61 представляет собой водород или N-защитную группу;
X представляет собой -СН=СН-, -С=N- или S и
Y представляет собой СН или N.
Соединения формулы (II) описаны в патенте США № 6054457.
В одном варианте настоящее изобретение направлено на способ лечения гиперпролиферативных заболеваний, включающих рак молочной железы, рак головы или рак шеи, гастроинтестинальный рак, лейкемию, рак яичника, бронхов, легкого и поджелудочной железы, синоназальную лимфому природных киллеров/Т-клеток, рак тестикул (семиному), карциному щитовидной железы, злокачественную меланому, карциному лимфатических желез, ангиосаркому, анапластическую крупноклеточную лимфому, карциному эндометрия или карциному предстательной железы, посредством введения эффективного количества соединения, представленного формулой II, или его фармацевтически приемлемой соли, где Х представляет собой S, и другие переменные являются такими, как описано для формулы II.
В одной из форм воплощения данного варианта настоящее изобретение направлено на способ лечения гиперпролиферативных заболеваний, включающих рак молочной железы, рак головы или рак шеи, гастроинтестинальный рак, лейкемию, рак яичника, бронхов, легкого и поджелудочной железы, синоназальную лимфому природных киллеров/Т-клеток, рак тестикул (семиному), карциному щитовидной железы, злокачественную меланому, карциному лимфатических желез, ангиосаркому, анапластическую крупноклеточную лимфому, карциному эндометрия или карциному предстательной железы, посредством введения эффективного количества соединения, представленного формулой II, или его фармацевтически приемлемой соли, где Х представляет собой S; R11 представляет собой необязательно замещенный арил, и другие переменные являются такими, как описано для формулы II.
В еще одной из форм воплощения данного варианта настоящее изобретение направлено на способ лечения гиперпролиферативных заболеваний, включающих рак молочной железы, рак головы или рак шеи, гастроинтестинальный рак, лейкемию, рак яичника, бронхов, легкого и поджелудочной железы, синоназальную лимфому природных киллеров/Т-клеток, рак тестикул (семиному), карциному щитовидной железы, злокачественную меланому, карциному лимфатических желез, ангиосаркому, анапластическую крупноклеточную лимфому, карциному эндометрия или карциному предстательной железы, посредством введения эффективного количества соединения, представленного формулой II, или его фармацевтически приемлемой соли, где Х представляет собой S; R11 представляет собой необязательно замещенный гетероциклил, и другие переменные являются такими, как описано для формулы II.
В еще одной из форм воплощения данного варианта настоящее изобретение направлено на способ лечения гиперпролиферативных заболеваний, включающих рак молочной железы, рак головы или рак шеи, гастроинтестинальный рак, лейкемию, рак яичника, бронхов, легкого и поджелудочной железы, синоназальную лимфому природных киллеров/Т-клеток, рак тестикул (семиному), карциному щитовидной железы, злокачественную меланому, карциному лимфатических желез, ангиосаркому, анапластическую крупноклеточную лимфому, карциному эндометрия или карциному предстательной железы, посредством введения эффективного количества соединения, представленного формулой II, или его фармацевтически приемлемой соли, где Х представляет собой S, Y представляет собой N, и другие переменные являются такими, как описано для формулы II.
Настоящее изобретение также направлено на способ лечения гиперпролиферативных заболеваний, включающих рак молочной железы, рак головы или рак шеи, гастроинтестинальный рак, лейкемию, рак яичника, бронхов, легкого и поджелудочной железы, синоназальную лимфому природных киллеров/Т-клеток, рак тестикул (семиному), карциному щитовидной железы, злокачественную меланому, карциному лимфатических желез, ангиосаркому, анапластическую крупноклеточную лимфому, карциному эндометрия или карциному предстательной железы, посредством введения эффективного количества соединения, представленного формулой III:
где
R12 представляет собой арил, С3-6циклоалкил или гетероциклил, каждый из которых необязательно замещен 1-6 независимыми атомами галогена; гидрокси; нитро; защищенную аминогруппу, амино; ацил; замещенный ацил; ацилС1-6алкилсульфинил; ацилС1-6алкилсульфонил; ацилокси; С1-6алкиламиноС1-6алкилкарбамоилокси; арил; циано; гетероциклил; С2-6алкенил, необязательно замещенный ацилом, замещенным ацилом, арилом или ацилзамещенным арилом; С2-6алкинил, необязательно замещенный амино, ациламино или замещенным ациламино; С1-6алкил, необязательно замещенный галогеном, амино, С1-6алкиламино, ациламино, замещенной ациламино, гидрокси, ацилокси, ацилС1-6алканоилокси, ацилом, замещенным ацилом, ацилС1-6алкоксиимино, арилом или ацилзамещенным арилом; С1-6алкилтио, необязательно замещенный ацилом или замещенным ацилом; алкокси, необязательно замещенный арилом, замещенным арилом, гидрокси, алкокси, амино, низшей алкиламино, защищенной аминогруппой, гетероциклилом, ацилзамещенным пиридилом, замещенным ацилзамещенным пиридилом, галогеном, ацилС1-6алкиламино, N-защищенным ацилС1-6алкиламино, N-ацилС1-6алкил-N-низшим алкиламино, ацилом, замещенным ацилом, алкиламино, замещенным алкиламино, С1-6алкилгидразинкарбониламино, гидроксиимино, ацилС1-6алкоксиимино, замещенными ацилС1-6алкоксиимино, ацилС1-6алкокси, гуанидино или N-защищенным гуанидино; или С2-6алкенилокси, необязательно замещенный ацилом или замещенными ацилом заместителями;
R22 представляет собой водород; С1-6алкил, необязательно замещенный гидрокси, арилом или ацилом; или С3-6циклоалкил;
R32 представляет собой водород; галоген; гидрокси; ацилокси; замещенный ацилокси; С1-6алкил, необязательно замещенный гидрокси или С1-6алкокси; С1-6алкокси, необязательно замещенный арилом, амино, защищенной аминогруппой, ацилом, гидрокси, циано или С1-6алкилтио; нитро; амино; ацил; замещенный ацил; или С3-6циклоалкокси;
А1 представляет собой простую связь, О или NH;
Е1 представляет собой С1-6алкилен, С2-6алкенил,
или Е1 представляет собой группу формул, -G1-J1-, в которой
G1 представляет собой С1-6алкилен или и
J1 представляет собой О или , где R62 представляет собой водород или N-защитную группу;
X1 представляет собой -СН=СН-, -С=N- или S; и
Y1 представляет собой арил, необязательно замещенный 1-6 независимыми ацилами, замещенным аминоС1-6алканоилом, защищенными амино и нитрогруппами, амино и нитро или диамино заместителями; или Y1 представляет собой сопряженный гетероциклил, необязательно замещенный 1-6 галогенами, ацилом, С1-6алкокси, гидрокси, гуанидино, меркапто, ациламино, амино, гетероциклилом, цианамино, аминоС1-6алкил(С1-6алкил)амино, С1-6алкиламино, С1-6алкиламино(С1-6алкиламино), замещенным гетероциклилом, С1-6алкилгидразино, арилокси, С1-6алкилтио, арилом, защищенной аминогруппой, N-защищенным С1-6алкиламино(С1-6алкил)амино, N-защищенным аминоС1-6алкил(N'-С1-6алкил)амино, аминоС1-6алкил(N-С1-6алкил)амино, С1-6алкиламино(С1-6алкил)(N-С1-6алкил)амино или С1-6алкокси(С1-6алкил)амино заместителями, или С1-6алкильным заместителем, дополнительно необязательно замещенным арилом, арС1-6алкокси, циано, гидроксиимино, меркапто, С1-6алкиламино, ацилокси, галогеном, С1-6алкокси, защищенным гидрокси, гидрокси, С1-6алкоксиарилом, защищенной аминогруппой, амино, гетероциклилом или замещенными гетероциклилом заместителями;
при условии, если Y1 представляет собой фенил, необязательно замещенный С1-6алкилом или арилом,
А1 представляет собой простую связь и
Е1 представляет собой .
Соединения формулы (III) описаны в патенте США № 6316482.
В одном варианте настоящее изобретение направлено на способ лечения гиперпролиферативных заболеваний, включающих рак молочной железы, рак головы или рак шеи, гастроинтестинальный рак, лейкемию, рак яичника, бронхов, легкого и поджелудочной железы, синоназальную лимфому природных киллеров/Т-клеток, рак тестикул (семиному), карциному щитовидной железы, злокачественную меланому, карциному лимфатических желез, ангиосаркому, анапластическую крупноклеточную лимфому, карциному эндометрия или карциному предстательной железы, посредством введения эффективного количества соединения, представленного формулой III, или его фармацевтически приемлемой соли, где Х1 представляет собой S, и другие переменные являются такими, как описано для формулы III.
В настоящем изобретении "С0-4алкил" означает алкил, имеющий 0-4 углерода, то есть 0, 1, 2, 3 или 4 углерода, в неразветвленной или разветвленной структуре. Алкил, не имеющий углерода, представляет собой водород, если алкил представляет собой концевую группу. Алкил, не имеющий углерода, представляет собой прямую связь, если алкил представляет собой мостиковую (соединяющую) группу.
В настоящем изобретении, если не указано иначе, "алкил", "алкенил" и "алкинил" включают разветвленные и неразветвленные структуры. Низшие алкилы, алкенилы и алкинилы имеют 1-6 углеродов. Высшие алкилы, алкенилы и алкинилы имеют более чем 6 углеродов.
В настоящем изобретении, если не указано иначе, термины "арил" и "ар" хорошо известны химикам и включают, например, фенил и нафтил, а также фенил с одной или более короткими алкильными группами (толил, ксилил, мезитил, куменил, ди(трет-бутил)фенил). Фенил, нафтил, толил и ксилил являются предпочтительными. "Замещенный арил" представляет собой арил, замещенный подходящими заместителями, такими как, например, ацил, замещенный ацил, N-защищенный пиперазинилсульфонил, пиперазинилсульфонил, N-C1-6алкилпиперазинилсульфонил, гидроксиС1-6алкил, гетероциклил, галоген, нитро, амино, С1-6алкиламино, циано или С1-6алкокси.
В настоящем изобретении, если не указано иначе, "гетероциклил" является хорошо известным химикам и содержит, по меньшей мере, один N, S или О гетероциклический атом и включает насыщенные, ненасыщенные, частично насыщенные, моно- и полициклические гетероциклические группы, такие как, например, пирролил, пирролинил, имидазолил, пиразолил, пиридил, пиримидинил, пиразинил, пиридазинил, триазолил, тетразолил, пирролидинил, имидазолидинил, пиперидил, пиперазинил, гомопиперазинил, индолил, изоиндолил, индолизинил, бензимидазолил, хинолил, изохинолил, имидазопиридил, индазолил, бензотриазолил, тетразолопиридазинил, пиранил, фурил, 1Н-тетрагидропиранил, тетрагидрофуранил, тиенил, оксазолил, изоксазолил, оксадиазолил, оксазолинил, морфолинил, бензофуранил, бензоксазолил, бензоксадиазолил, тиазолил, тиадиазолил, тиазолидинил, бензотиазолил, бензотиадиазолил, бензофуранил или бензодиоксил и подобные. Такие гетероциклилы подходящим образом замещены низшими алкилами или оксо заместителями.
В настоящем изобретении, если не указано иначе, "ацил" включает, например, карбокси, этерифицированный карбокси, карбамоил, низший алкилкарбамоил, низший алканоил, ароил, гетероциклилкарбонил и подобные. Этерифицированный карбокси включает замещенный или незамещенный низший алкоксикарбонил, такой как метоксикарбонил, этоксикарбонил, пропоксикарбонил, бутоксикарбонил, трет-бутоксикарбонил, гексилоксикарбонил, 2-иодэтоксикарбонил, 2,2,2-трихлорэтоксикарбонил, диметиламинопропоксикарбонил, диметилэтоксиаминокарбонил; замещенный или незамещенный арилоксикарбонил, такой как феноксикарбонил, 4-нитрофеноксикарбонил, 2-нафтилоксикарбонил; замещенный или незамещенный ар(низший)алкоксикарбонил, такой как бензилоксикарбонил, фенетилоксикарбонил, бензгидрилоксикарбонил, 4-нитробензилоксикарбонил, 3-метокси-4-нитробензилоксикарбонил и N-содержащий гетероциклилкарбонил, такой как N-метилпиперидилоксикарбонил, и подобные.
В настоящем изобретении, если не указано иначе, "галоген" представляет собой фтор, хлор, бром или йод.
В настоящем изобретении, если не указано иначе, "С1-6алкилгидразино" может быть 2-моно- или 2,2-ди(С1-6алкил)гидразино, таким как 2-метилгидразино, 2,2-диметилгидразино, 2-этилгидразино, 2,2-диэтилгидразино или т.п.
В настоящем изобретении, если не указано иначе, "С1-6алкиламиноС1-6алкил" включает, например, метиламинометил, диметиламинометил, диметиламиноэтил или т.п.
"С1-6алканоил" включает замещенные или незамещенные алканоилы, такие как формил, ацетил, пропионил, бутирил, изобутирил, валерил, изовалерил, пивалоил, гексаноил, трифторацетил или т.п.
"Ароил" включает бензоил, нафтоил, толуоил, ди(трет-бутил)бензоил и т.п.
В настоящем изобретении, если не указано иначе, "N-защитная группа" в "защищенной аминогруппе" включает замещенный или незамещенный низший алканил (такой как, например, формил, ацетил, пропионил, трифторацетил), фталоил, низший алкоксикарбонил (такой как трет-бутоксикарбонил, трет-амилоксикарбонил), замещенный или незамещенный аралкилоксикарбонил (такой как бензилоксикарбонил, п-нитробензилоксикарбонил), 9-флуоренилметоксикарбонил, замещенный или незамещенный аренсульфонил (бензолсульфонил, тозил). Фталоил, трет-бутоксикарбонил или 9-флуоренилметоксикарбонил являются предпочтительными.
В настоящем изобретении, если не указано иначе, "N-защитная группа" в "защищенном гуанидино" включает низший алкоксикарбонил (такой как трет-бутоксикарбонил, трет-амилоксикарбонил).
В настоящем изобретении, если не указано иначе, "гидрокси-защитная группа" включает замещенный или незамещенный арилметил (например, бензил, низший алкоксибензил), ацил или замещенный силил (например, трет-бутилдифенилсилил).
Приведенные выше формулы I, II и III показаны без определенной стереохимии в некоторых положениях. Настоящее изобретение включает все стереоизомеры соединений, представленных формулами I, II, и III, и их фармацевтически приемлемых солей. Далее, также включены смеси стереоизомеров, равно как и выделенные специфические стереоизомеры. В ходе синтеза, применяемого для получения таких соединений, или при использовании рацемизации или эпимеризации, известных специалистам в данной области, результатом таких методик может быть смесь стереоизомеров.
Настоящее изобретение также охватывает фармацевтическую композицию, включающую соединение формулы I в комбинации с фармацевтически приемлемым носителем.
Предпочтительно, композиция включает фармацевтически приемлемый носитель и нетоксичное терапевтически эффективное количество соединения формулы I, как описано выше (или его фармацевтически приемлемой соли или N-оксида).
Вместе с тем, в пределах данного предпочтительного варианта, настоящее изобретение охватывает фармацевтическую композицию для лечения заболевания посредством ингибирования с-Kit киназы, которая может быть формой дикого типа или мутантной формой белка, включающую фармацевтически приемлемый носитель и нетоксичное терапевтически эффективное количество соединения, представленного формулой I, как описано выше (или его фармацевтически приемлемой соли или N-оксида).
Соединения и композиции настоящего изобретения эффективны для лечения млекопитающих, таких как, например, человек.
Термин "фармацевтически приемлемые соли" означает соли, полученные из фармацевтически приемлемых нетоксичных оснований или кислот. Если соединение настоящего изобретения является кислотным, его соответствующая соль может быть легко получена из фармацевтически приемлемых нетоксичных оснований, включающих неорганические основания и органические основания. Соли полученные из таких неорганических оснований, включают соли алюминия, аммония, кальция, меди (I и II), трехвалентного железа, двухвалентного железа, лития, магния, марганца (I и II), калия, натрия, цинка и подобные соли. Особенно предпочтительны соли аммония, кальция, магния, калия и натрия. Соли, полученные из фармацевтически приемлемых органических нетоксичных оснований, включают соли первичных, вторичных и третичных аминов, а также циклических аминов и замещенных аминов, таких как природные или синтезированные замещенные амины. Другие фармацевтически приемлемые органические нетоксичные основания, из которых могут образовываться соли, включают ионообменные смолы, такие как, например, аргинин, бетаин, кофеин, холин, N',N'-дибензилэтилендиамин, диэтиламин, 2-диэтиламиноэтанол, 2-диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лизин, метилглюкамин, морфолин, пиперазин, пиперидин, полиаминовые смолы, прокаин, пурины, теобромин, триэтиламин, триметиламин, трипропиламин, трометамин и подобные.
Если соединение настоящего изобретения является основным, его соответствующая соль может быть легко получена из фармацевтически приемлемых нетоксичных кислот, включающих неорганические и органические кислоты. Такие кислоты включают, например, уксусную, бензолсульфоновую, бензойную, камфорсульфоновую, лимонную, этансульфоновую, фумаровую, глюконовую, глутаминовую, бромистоводородную, хлористоводородную, изэтионовую, молочную, малеиновую, яблочную, миндальную, метансульфоновую, слизевую, азотную, памоевую, пантотеновую, фосфорную, янтарную, серную, винную, п-толуолсульфоновую кислоту и подобные. Особенно предпочтительными являются лимонная, бромистоводородная, хлористоводородная, малеиновая, фосфорная, серная, метансульфоновая и винная кислоты.
Фармацевтические композиции настоящего изобретения или используемые в способах настоящего изобретения включают соединение, представленное формулами I, II или III (или его фармацевтически приемлемую соль или N-оксид), в качестве активного ингредиента, фармацевтически приемлемый носитель и необязательно другие терапевтические ингредиенты или адъюванты. Композиции включают композиции, пригодные для перорального, ректального, местного и парентерального (включая подкожное, внутримышечное и внутривенное) введения, несмотря на то, что наиболее удобный путь введения в каждом случае будет зависеть от конкретного организма и природы и тяжести состояний, при которых применяются активные ингредиенты. Фармацевтические композиции могут быть представлены в виде подходящих единичных дозированных форм и приготовлены одним из способов, хорошо известных в области фармацевтики.
На практике, соединение, представленное формулой I, или его фармацевтически приемлемые соли, или N-оксиды данного изобретения могут быть комбинированы как активные ингредиенты в смеси с фармацевтическими носителями в соответствии с общепринятыми методами получения фармацевтических композиций. Носитель может принимать большое разнообразие форм в зависимости от приготовления форм, желаемых для введения. Например, пероральные или парентеральные (включая внутривенные). Таким образом, фармацевтические композиции настоящего изобретения могут быть представлены как дискретные единицы, подходящие для перорального введения, такие как капсулы, саше или таблетки, каждая из которых содержит заранее установленное количество активного ингредиента. Далее, композиции могут быть представлены в виде порошка, гранул, раствора, суспензии в водной жидкости, в неводной жидкости, эмульсии типа "масло в воде" или жидкой эмульсии типа "вода в масле". В дополнение к обычным дозированным формам, указанным выше, соединение, представленной формулой I, или его фармацевтически приемлемая соль или N-оксид, может также быть введено посредством средств управляемого высвобождения и/или устройств доставки. Композиции могут быть получены любым фармацевтическим способом. В общих чертах, такие способы включают стадию введения в состав активного ингредиента с носителем, который составляет один или более необходимых ингредиентов. В целом, композиции получают при равномерном и тщательном перемешивании активных ингредиентов с жидкими носителями или мелкодиспергированными твердыми носителями, или обоими. Затем продукту может быть легко придана подходящая для введения форма.
Таким образом, фармацевтические композиции данного изобретения могут включать фармацевтически приемлемый носитель и соединение или его фармацевтически приемлемую соль, или N-оксид, представленные фо