Производное пропан-1,3-диона или его соль
Иллюстрации
Показать всеОписывается производное пропан-1,3-диона общей формулы (I) или его фармацевтически приемлемая соль, в которой символы обозначают следующее: кольцо А: бензол, который может быть замещен, пиридин, который может быть замещен, или тиофеновое кольцо; кольцо В: бензольное или тиофеновое кольцо; R1: Н или -СО-низший алкил; R2: H, -O-R5, -N(R6)R7, -N3, -S(O)m-низший алкил, пиридил или имидазолил, которые могут быть замещены; R3: Н или низший алкил; X: связь, низший алкилен, который может быть замещен, или циклоалкандиил. Описываются также производные пропан-1,3-диона формул (Ia) и (Ib) и фармацевтическая композиция. Предложенные соединения полезны в качестве антагонистов рецептора GnRH и полезны при лечении заболеваний, зависящих от половых гормонов, таких как рак простаты, рак груди, эндометриоз, маточная лейомиома и доброкачественная гипертрофия предстательной железы. 4 н. и 6 з.п. ф-лы, 26 табл.
Реферат
Область техники
Настоящее изобретение относится к новому производному пропан-1,3-диона, которое полезно в качестве лекарственного средства, в частности в качестве терапевтического агента для заболеваний, зависящих от половых гормонов.
Уровень техники
Известно, что гормон гипоталамуса или гормон гипофиза связан с механизмом, контролирующим выделение периферических гормонов. В общем случае секреция гормонов передней доли гипофиза контролируется с помощью ускоряющего секрецию гормона или ингибирующего секрецию гормона, выделяемых из его дальнего центрального гипоталамуса, или с помощью периферического гормона, выделяемого из органа-мишени соответствующего гормона.
Гонадотропин - высвобождающий гормон (который обозначается далее как GnRH, и GnRH также называют фактором, высвобождающим лютеинизирующий гормон, LHRH) известен как гормон, который контролирует секрецию половых гормонов при наиболее высоком положении и контролирует секрецию гормонов передней доли гипофиза лютеинизирующего гормона (далее обозначаемый как LH) и фолликулостимулирующего гормона (далее обозначаемый FSH), а также половых гормонов в половых железах, посредством рецептора, который присутствует в передней доле гипофиза (далее называемый рецептором GnRH) (Hormone To Rinsho (Hormone and Clinics), специальный номер источника, 46, 46-57 (1998)). Так как антагонисты, специфические и селективные для такого рецептора GnRH, регулируют действие GnRH и контролируют секрецию подчиненных LH и FSH, а также половых гормонов, они рассматриваются как профилактические или терапевтические агенты для заболеваний, зависящих от половых гормонов (см. приведенный выше Hormone and Clinics, специальный номер источника (1998)).
На сегодняшний день в качестве антагонистов рецептора GnRH на рынке представлены пептидные соединения цетрореликс (непатентная ссылка 1) и абареликс (непатентная ссылка 2).
Альтернативно в качестве непептидных соединений, обладающих антагонизмом в отношении рецепторов GnRH, в настоящее время клинические испытания проходят производное тиенопиримидина ТАК-013 (непатентная ссылка 3) и производное урацила NBI-42902 (непатентная ссылка 4).
Кроме того, в патентной ссылке 1 раскрыто, что производное пропан-1,3-диона обладает антагонистическим действием в отношении рецептора GnRH.
(В формуле А и В могут быть одинаковыми или отличаются друг от друга и каждый представляет собой арил, который может быть замещен, или гетероарил, который может быть замещен. Подробнее см. приведенный выше официальный орган печати).
Несмотря на то, что соединение, содержащее 1-гидроксиалкильную группу в качестве замещающей группы в кольце А или в кольце В, включено в объем типичного концептуального производного пропан-1,3-диона, содержащего группу d в качестве замещающей группы в кольцах, в патентной ссылке 1 отсутствует иллюстративное описание для указанного соединения.
[Непатентная ссылка 1] Proc. Natl. Acad. Sci., USA, 85, 1637-1641, 1988.
[Непатентная ссылка 2] J. Urol., 167, 1670-1674, 2002.
[Непатентная ссылка 3] J. Clin. Endocrinol. Metab., 88, 1697-1704, 2003.
[Непатентная ссылка 4] J. Med. Chem., 2005, 48, 1169-1178.
[Патентная ссылка 1] International Piblication WO 02/02533.
Описание изобретения
Проблемы, которые решает настоящее изобретение
Целью настоящего изобретения является разработка лекарственного средства, которая проявляет прекрасное антагонистическое действие в отношении рецептора GnRH в живом организме, в особенности разработка нового соединения, которое полезно в качестве терапевтического агента при раке простаты, доброкачественной предстательной гипертрофии и т.д.
Способы решения проблемы
Авторами исследованы производные пропан-1,3-диона, и в результате подтверждено, что соединение, которое содержит бензольное или тиофеновое кольцо, замещенное группой, являющейся производной 1-гидроксиалкила, в структуре пропан-1,3-диона, содержащем 2-(1,3-дигидро-2Н-бензимидазол-2-илиден), неожиданно проявляет превосходную доступность при пероральном введении в дополнение к прекрасному антагонистическому действию в отношении рецепторов GnRH, за счет чего реализуется настоящее изобретение.
То есть, изобретение относится к производному пропан-1,3-диона, представленному общей формулой (I), или к его соли. Изобретение также относится к лекарственному средству, в особенности к антагонисту рецептора GnRH, в котором указанное производное используется в качестве активного ингредиента.
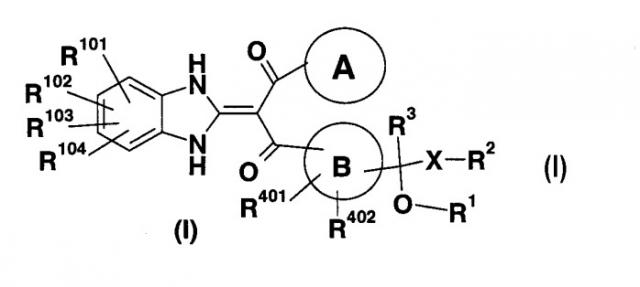
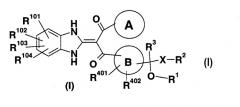
[Символы в формуле означают следующее:
кольцо А: бензол, который может быть замещен, пиридин, который может быть замещен, или тиофеновое кольцо;
кольцо В: бензольное или тиофеновое кольцо;
R1: Н или -СО-низший алкил;
R2: Н, -O-R5, -N(R6)R7, -N3, -S(O)m-низший алкил, -S(O)m-N(R6)R7, атом галогена, пиридил или имидазолил, которые могут быть замещены;
R5: Н, низший алкил, -СО-низший алкил, который может быть замещен, или -СО-О-низший алкил, который может быть замещен;
R6 и R7: могут быть одинаковыми или отличаются друг от друга и каждый из них представляет собой Н, низший алкил или -СО-низший алкил при условии, что R1 и R2 вместе могут образовывать диоксолан, который может быть замещен;
m: 0, 1 или 2;
R3: Н или низший алкил;
R401 и R402: могут быть одинаковыми или отличаются друг от друга и каждый из них представляет собой Н, атом галогена, ОН, -О-низший алкил или низший алкил;
Х: связь, низший алкилен, который может быть замещен, или циклоалкандиил;
R101, R102, R103 и R104: могут быть одинаковыми или отличаются друг от друга и каждый из них представляет собой Н, атом галогена, ОН или -О-низший алкил, который может быть замещен (арилом или гетероарилом). Такие же значения будут использоваться в данном описании и далее].
Кроме того, настоящее изобретение представляет собой фармацевтическую композицию, содержащую в качестве активного ингредиента пропан-1,3-дионовое соединение, представленное приведенной выше общей формулой (I), или его фармацевтически приемлемую соль, и фармацевтически приемлемый носитель, предпочтительно фармацевтическую композицию, которая является антагонистом рецептора GnRH; и более предпочтительно фармацевтическую композицию, где антагонист рецептора GnRH представляет собой агент для лечения связанных с GnRH заболеваний, таких как рак простаты, рак груди, эндометриоз, маточная лейомиома и доброкачественная гипертрофия предстательной железы.
Более того, настоящее изобретение предлагает способ лечения пациента, страдающего от связанных с GnRH заболеваний, который включает введение пациенту эффективного количества пропан-1,3-дионового соединения, представленного приведенной выше формулой (I), или его фармацевтически приемлемой соли, предпочтительно способ лечения связанных с GnRH заболеваний, где связанные с GnRH заболевания представляют собой рак простаты, рак груди, эндометриоз, маточную лейомиому и доброкачественную гипертрофию предстательной железы. Кроме того, настоящее изобретение включает применение пропан-1,3-дионового соединения для получения антагониста рецептора GnRH, содержащего в качестве активного ингредиента пропан-1,3-дионовое соединение, представленное приведенной выше общей формулой (I), или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель.
Преимущества изобретения
Так как соединение настоящего изобретения имеет прекрасную доступность при пероральном введении, в дополнение к сильному антагонизму в отношении GnRH рецепторов можно ожидать, что это соединение будет оказывать сильное лекарственное действие в живом организме и что оно будет полезно при лечении заболеваний, зависящих от половых гормонов, в особенности GnRH-связанных заболеваний, таких как рак простаты, рак груди, эндометриоз и маточная лейомиома (С. Huddins & C.V. Hogdes, Cancer Res., 1, 293-297 (1941); L. Bokser et al., Proc. Natl. Acad. Sci, USA, 87, 7100-7104 (1990)), доброкачественная гипертрофия предстательной железы (J. Clin. Endocrinol. Metab., 83, 3826-3931, 1998) и т.д. Кроме того, так как соединение настоящего изобретения обладает прекрасной метаболической стабильностью в организме человека и имеет незначительные свойства лекарственного взаимодействия, указанное соединение имеет более желаемые свойства в качестве лекарственного средства, которое используется в случае перечисленных выше заболеваний.
Наилучший способ осуществления изобретения
Предпочтительные варианты осуществления изобретения представлены ниже.
(1) Производное пропан-1,3-диона или его фармацевтически приемлемая соль, где в общей формуле (I) кольцо А представляет собой бензольное кольцо, которое может быть замещено атомом галогена или низшим алкилом, кольцо В представляет собой бензольное кольцо, R1 представляет собой Н, R2 представляет собой ОН, R3 представляет собой Н и Х представляет собой низший алкилен, который может быть замещен.
(2) Производное пропан-1,3-диона формулы (I) или его фармацевтически приемлемая соль, где Х представляет собой метилен, который может быть замещен.
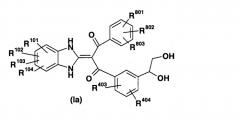
(3) Производное пропан-1,3-диона, представленное общей формулой (Ia), или его фармацевтически приемлемая соль:
(символы в формуле имеют следующие значения,
R801, R802 и R803: могут быть одинаковыми или отличаются друг от друга и каждый из них представляет собой атом галогена или низший алкил, и
R403 и R404: могут быть одинаковыми или отличаются друг от друга и каждый из них представляет собой Н, атом галогена или низший алкил; такие же значения будут использоваться в данном описании и далее).
(4) Производное пропан-1,3-диона или его фармацевтически приемлемая соль по п.4, которые представляют собой, по меньшей мере, одно соединение, выбранное из группы, включающей:
2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-1-[3-(1,2-дигидроксиэтил)фенил]-3-(3,4,5-трифторфенил)пропан-1,3-дион;
1-{2-бутил-3-[(1R)-1,2-дигидроксиэтил]фенил}-2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-3-(3-фторфенил)пропан-1,3-дион;
1-(3,5-дифторфенил)-2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-3-[5-(1,2-дигидроксиэтил)-2-фторфенил]пропан-1,3-дион;
1-(3,5-дифторфенил)-2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-3-{3-[(1R)-1,2-дигидроксиэтил]-2-метилфенил}пропан-1,3-дион;
2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-1-{3-{(1R)-1,2-дигидроксиэтил]-2-метилфенил}-3-(2-фторфенил)пропан-1,3-дион;
2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-1-[3-(1,2-дигидроксиэтил)фенил]-3-(2,3,5-трифторфенил)пропан-1,3-дион;
2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-1-{3-[(1R)-1,2-дигидроксиэтил]-2-метилфенил}-3-(3-метилфенил)пропан-1,3-дион;
1-{2-хлор-3-[(1R)-1,2-дигидроксиэтил]фенил}-2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-3-(3-фторфенил)пропан-1,3-дион);
2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-1-{3-[(1R)-1,2-дигидроксиэтил]фенил}-3-(3-фторфенил)пропан-1,3-дион;
1-(3,5-дифторфенил)-2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-3-[3-(1,2-дигидроксиэтил)-2-фторфенил]пропан-1,3-дион;
1-(3,5-дифторфенил)-2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-3-[3-(1,2-дигидроксиэтил)-4-фторфенил]пропан-1,3-дион;
1-{2-хлор-3-[(1R)-1,2-дигидроксиэтил]фенил}-3-(3,5-дифторфенил)-2-(1,3-дигидро-2Н-бензимидазол-2-илиден)пропан-1,3-дион);
2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-1-{3-[(1R)-1,2-дигидроксиэтил]-2-фторфенил}-3-(3-фторфенил)пропан-1,3-дион;
1-{2-хлор-3-[(1R)-1,2-дигидроксиэтил]фенил}-3-(3-хлорфенил)-2-(1,3-дигидро-2Н-бензимидазол-2-илиден)пропан-1,3-дион).
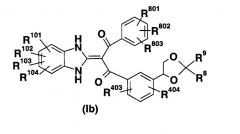
(5) Производное пропан-1,3-диона, представленное общей формулой (Ib), или его фармацевтически приемлемая соль:
(символы в формуле означают следующее:
R8 и R9: могут быть одинаковыми или отличаются друг от друга и каждый из них представляет собой Н, низший алкил, низший алкенил или -О-низший алкил; такие же значения будут использоваться в данном описании и далее).
(6) Производное пропан-1,3-диона общей формулы (Ib) или его фармацевтически приемлемая соль, где R801, R802 и R803 могут быть одинаковыми или отличаются друг от друга и каждый представляет собой Н или атом галогена.
(7) Производное пропан-1,3-диона или его фармацевтически приемлемая соль, которое представляет собой, по меньшей мере, одно соединение, выбранное из группы, включающей:
2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-1-(3-фторфенил)-3-[3-(2-метокси-1,3-диоксолан-4-ил)фенил]пропан-1,3-дион;
2-(1,3-дигидро-2Н-бензимидазол-2-илиден)-1-(3-фторфенил)-3-[3-(2-метокси-2-метил-1,3-диоксолан-4-ил)фенил]пропан-1,3-дион,
или его фармацевтически приемлемую соль.
Далее изобретение описано подробно.
В качестве примера «атома галогена» можно назвать атомы фтора, хлора, брома или йода.
«Низший алкил» представляет собой линейный или разветвленный насыщенный С1-6алкил, предпочтительно метил, этил, изопропил, гексил или т.п.
«Низший алкилен» представляет собой линейный или разветвленный насыщенный С1-6алкилен, предпочтительно метилен, этилен, изопропилен или т.п.
«Бензол, который может быть замещен» или «пиридин, который может быть замещен» представляют собой бензольное кольцо или пиридиновое кольцо, которые могут быть замещены 1-3 замещающими группами, где замещающие группы представляют собой атом галогена, CN, низший алкил, который может быть замещен галогеном, -О-низший алкил, -СО-О-низший алкил или аминогруппу, предпочтительно атом галогена или низший алкил, который может быть замещен атомом галогена.
«Имидазолил, который может быть замещен», представляет собой имидазолил, который может быть замещен 1 или 2 замещающими группами, и в качестве замещающей группы предпочтителен низший алкил.
«Диоксолан, который может быть замещен», представляет собой диоксолан, который может быть замещен 1 или 2 замещающими группами, и в качестве замещающей группы предпочтителен низший алкил, низший алкенил, -О-низший алкил или морфолино-низший алкил.
«Низший алкил, который может быть замещен», представляет собой низший алкил, который может быть замещен 1 или 2 замещающими группами, и в качестве замещающей группы предпочтительны аминогруппа или моно- или ди(низший алкил)аминогруппа.
«Низший алкилен, который может быть замещен» представляет собой алкилен, который может быть замещен 1 или 2 замещающими группами, и примерами предпочтительных замещающих групп могут быть ОН, СООН, -СО-О-низший алкил, атом галогена, CN, фенил, -О-низший алкил, -О-СО-низший алкил, аминогруппа, моно- или ди(низший алкил)аминогруппа, -CO-NH2, -CO-моно- или ди(низший алкил)аминогруппа и циклоалкил.
«Циклоалкил» означает С3-6-моноциклическую насыщенную углеводородную кольцевую группу и предпочтительно представляет собой циклопропил, циклобутил, циклопентил или циклогексил.
«Циклоалкандиил» означает двухвалентную группу, производную С3-6-моноциклического насыщенного углеводородного кольца, и предпочтительно представляет собой циклопропандиил, циклобутандиил, циклопентандиил, циклогександиил или т.п., из которых особенно предпочтителен циклопропандиил.
Определение «доступность» означает свойство, при котором перорально введенный агент абсорбируется пищеварительным трактом, проявляет эффект начального прохождения через печень и затем поступает в кровь.
Соединение, в котором гидроксильная группа заменена группой, образующей пролекарство, также относится к соединению настоящего изобретения.
Примерами образующей пролекарство группы являются группы, описанные в публикации Prog. Med., 5, 2157-2161 (1985) и "Iyakuhin no Kaihatsu (Development of Medicaments)" vol.7 (Hirokawa Shoten, 1990) Bunshi Sekkei (Molecular Desing), pp.163-198.
В соединениях настоящего изобретения присутствуют таутомеры. Их можно описать, например, следующим образом.
Отдельные формы указанных изомеров или их смеси также входят в настоящее изобретение. Кроме того, соединения настоящего изобретения могут иметь асимметричный атом или аксиальную асимметрию, зависящие от типа группы-заместителя, так что могут быть получены изомеры на основе асимметричного атома или т.п. Смеси указанных оптических изомеров и их отдельные формы также включены в настоящее изобретение. Кроме того, соединения, в которых соединения настоящего изобретения мечены радиоактивными изотопами, также входят в изобретение.
Также соединение, в котором геометрическая изомерия, связанная с двойной связью в положении 2 пропана, как показано ниже, может претерпевать взаимные превращения через таутомерию, показанную выше, присутствует среди соединений настоящего изобретения. Пример представлен ниже.
Кроме того, соединение настоящего изобретения иногда образует кислотно-аддитивную соль или в зависимости от типа группы-заместителя соль с основанием, и такая соль входит в объем настоящего изобретения при условии, что она является фармацевтически приемлемой солью. Иллюстративными примерами соли являются кислотно-аддитивная соль с хлористоводородной кислотой, бромистоводородной кислотой, йодистоводородной кислотой, серной кислотой, азотной кислотой, фосфорной кислотой и подобными неорганическими кислотами, или с муравьиной кислотой, уксусной кислотой, пропионовой кислотой, щавелевой кислотой, малоновой кислотой, янтарной кислотой, фумаровой кислотой, малеиновой кислотой, молочной кислотой, яблочной кислотой, винной кислотой, лимонной кислотой, метансульфоновой кислотой, этансульфоновой кислотой, п-толуолсульфоновой кислотой, аспарагиновой кислотой, глутамовой кислотой и подобными органическими кислотами, соли с натрием, калием, магнием, кальцием, алюминием и подобными неорганическими основаниями, или с метиламином, этиламином, этаноламином, лизином, орнитином и подобными органическими основаниями, аммонийная соль и т.д. Различные гидраты и сольваты и вещества, проявляющие полиморфизм, соединения настоящего изобретения и его фармацевтически приемлемой соли также входят в настоящее изобретение.
Способы получения
Соединение настоящего изобретения и его фармацевтически приемлемая соль могут быть получены с использованием различных общеизвестных способов синтеза, исходя из характеристик его основного ядра или типа замещающих групп.
В некоторых случаях в зависимости от типа функциональной группы с точки зрения методик получения эффективно заменять указанную функциональную группу подходящей защитной группой (группой, которая легко превращается в указанную функциональную группу) на стадии от исходных до промежуточных соединений. Примерами такой функциональной группы являются аминогруппа, гидроксильная группа, карбоксильная группа и т.п., и защитные группы, описанные в "Protective groups in Organic Synthesis (3-rd Edition)" (Ed. Greene and Wuts, JOHN WILEY & SONS, 1991), и подобные группы, могут быть приведены в качестве защитных групп, которые необязательно могут быть выбраны с учетом реакционных условий. С помощью таких способов рассматриваемые соединения могут быть получены путем проведения реакции после введения указанной защитной группы и затем снятием защитной группы, как того требуют обстоятельства.
Конкретные способы получения соединения настоящего изобретения описаны ниже. Однако способы получения настоящего изобретения не ограничены примерами, представленными ниже.
Используемые в данном описании сокращения имеют следующие значения:
ДМФА - N,N-диметилформамид;
ДМСО - диметилсульфоксид;
ТГФ - тетрагидрофуран;
Tol - толуол;
ДХЭ - 1,2-дихлорэтан;
ТЭА - триэтиламин;
Диглим - диметиловый эфир диэтиленгликоля;
LiTMP - 2,2,6,6-тетраметилпиперидат лития;
LDA - диизопропиламид лития;
WSCHCl - гидрохлорид 3-(3-диметиламинопропил)-1-этилкарбодиимида;
OHBt - 1-гидроксибензотриазол;
CDI - 1,1'-карбонилдиимидазол.
Способы получения
Первый способ получения
(Символы на реакционной схеме имеют следующие значения.
R: низший алкил; R401, R402, R101, R102, R103 и R104 необязательно могут быть защищены защитной группой. (Такие же значения будут использоваться в данном описании и далее.)
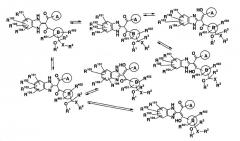
Данный способ получения представляет собой способ получения соединения (I) настоящего изобретения. Способом, который основан на способе получения 4, описанном в патентной ссылке 1, из 1,2-диаминобензольного соединения (II) получают 2-метилимидазольное соединение (III); указанное соединение (III) подвергают взаимодействию с ацильным соединением (IV), и полученную в результате реакционную смесь обрабатывают при комнатной температуре при нагревании в присутствии морфолина или подобного органического основания в инертном для реакции растворителе, получая таким образом имидазольное соединение (VI). Указанное ацильное соединение (IV) может быть получено, например, путем хлорирования соответствующей карбоновой кислоты тионилхлоридом, хлорангидридом щавелевой кислоты или подобным хлорирующим агентом, в дихлорметане или подобном растворителе, инертном в реакции, при комнатной температуре или при нагревании в присутствии или в отсутствие ДМФА или подобного катализатора. Тионилхлорид или т.п. могут быть непосредственно использованы в качестве растворителя. Полученную в результате реакционную смесь можно очистить азеотропной обработкой с толуолом или подобным растворителем, и дополнительную очистку можно проводить или не проводить. Кроме того, промежуточное соединение (V) и т.п. может быть выделено или его можно не выделять.
Далее, промежуточное соединение (VIIIa) и подобное соединение получают, подвергая имидазольное соединение (VI) и ацильное соединение (VII) реакции ацилирования в диглиме или подобном инертном в реакции растворителе в присутствии или в отсутствие ТЭА или аналогичного основания при температуре от комнатной температуры до нагревания; и затем соединение (I) настоящего изобретения получают добавлением карбоновой кислоты (VIIa) в количестве, соответствующем реакции с указанным соединением (VIIIa), или соответствующего реакции количества воды и нагреванием смеси. Ацильное соединение (VII) может быть получено способом, аналогично способу получения соединения (IV). Кроме того, промежуточные соединения (VIIIa) и аналогичные соединения могут быть выделены или их можно не выделять.
Второй способ получения
Приведенный способ получения представляет собой способ особенно подходящий для получения соединений (Ia) и (Ia-i) настоящего изобретения. По данному способу оптически активные соединения настоящего изобретения могут быть получены селективно при использовании в качестве исходных соединений оптически активных соединений (VIId) и (VIIe).
Стадия 1: Указанная стадия представляет собой общеизвестный способ, относящийся к защите 1,2- или 1,3-дигидрокси-соединения. В зависимости от условий реакции необязательно могут быть выбраны защитные группы, описанные в "Protective groups in Organic Synthesis (3-rd Edition)" (Ed. Greene and Wuts, JOHN WILEY & SONS, 1991), и подобные группы.
В этом случае, когда оптически активные 1,2-дигидрокси-соединения (VIId) и (VIIe) используются в качестве исходных веществ вместо соединения (VIIb), указанные соединения (VIId) и (VIIe) могут быть получены известным способом согласно приведенной ниже реакции.
(1): Данная стадия представляет собой способ, общеизвестный как реакция сочетания по Стиле (например, J.K. Stille at al., J. Org. Chem., 52, 422-424, 1987). Более конкретно, реакцию проводят, подвергая галогенарильное соединение или арилтрифталатное соединение, предпочтительно бромарильное соединение (XI) или йодарильное соединение, взаимодействию с соответствующим реакции количеством трибутил(винил)олова или подобного оловоорганического реагента в толуоле или подобном инертном в реакции растворителе при температуре от комнатной температуры до нагревания, в присутствии трис(дибензилиденацетон)дипалладия или подобного палладиевого катализатора и три(трет-бутил)фосфина или подобного фосфинового соединения, также предпочтительно в атмосфере аргона.
(2) Данная стадия представляет собой общеизвестный способ асимметричного дигидроксилирования олефинового соединения (XII). Например, реакцию проводят способом, описанным "Sharpless K.B., et al., Chem. Rev., 94, 1994, 2483-2547", например, путем окисления олефинового соединения с помощью AD-mix (Aldrich, USA) в смешанном растворителе (трет-бутанол)-вода или подобном инертном в реакции растворителе. Реакцию проводят при температуре от охлаждения льдом до нагревания, предпочтительно от 0°C до комнатной температуры. Оптически активные 1,2-дигидрокси-соединения (VIId) и (VIIe), имеющие желаемую абсолютную конфигурацию, могут быть соответственно получены при использовании реагентов AD-mix-альфа и AD-mix-бета. См. приведенную ниже схему химической реакции.
Стадия 2: Данная стадия представляет собой общеизвестную реакцию гидролиза, которую осуществляют путем проведения реакции в ТГФ, метаноле или подобном инертном в реакции растворителе в присутствии гидроксида натрия или подобного органического основания предпочтительно при комнатной температуре.
Стадия 3: Данную стадию проводят общеизвестным способом (K.G. Akamanchi et al., Synlett, 1999, 11, 1763-1785). Например, реагент, образующий хлорангидрид кислоты, получают из тионилхлорида и 1Н-бензотриазола в дихлорметане или подобном инертном в реакции растворителе; и ацильное соединение (Х) получают, подвергая указанный реагент взаимодействию с соответствующей карбоновой кислотой (IX), растворенной в дихлорметане или подобном инертном в реакции растворителе, при охлаждении льдом, при комнатной температуре или при нагревании. Полученное в результате соединение (X) может быть очищено азеотропной обработкой с толуолом или подобным растворителем, и дополнительную очистку можно проводить или не проводить.
Стадия 4: Данную стадию проводят в соответствии с первым способом получения.
Стадия 5: Данная стадия представляет собой способ получения дигидрокси-соединения (Ia-i) путем проведения общеизвестной реакции снятия защиты с защищенного ацетонидом соединения (Ib-i) 1,2- или 1,3-дигидрокси-соединения. Указанный способ может быть проведен в условиях реакции и т.д., описанных в "Protective groups in Organic Synthesis (3-rd Edition)", Ed. Greene and Wuts (JOHN WILEY & SONS, 1991).
Кроме того, когда винильная группа олефинового соединения (XII) расположена в ортоположении к атому фтора, как в случае этилового эфира 3-винил-2-фторбензойной кислоты, или расположена в ортоположении к замещающей группе, обладающей способностью к расщеплению, винильная группа указанного соединения также может быть введена с помощью металларильного соединения. Например, такое соединение также может быть синтезировано путем получения металларильного соединения обработкой этилового эфира 2-фторбензойной кислоты LiTMP, LDA или подобным металлорганическим основанием в ТГФ или подобном инертном в реакции растворителе при низкой температуре, предпочтительно при -78°С, с последующим получением этилового эфира 3-формил-2-фторбензойной кислоты, подвергая указанное соединение взаимодействию с соединением, которое используется как источник ДМФА или подобной формильной группы, при низкой температуре, предпочтительно при -78°С, и затем превращением формильной группы в винильную группу общеизвестной реакцией Виттига. Более конкретно, реакцию Виттига проводят взаимодействием альдегидного соединения и соответствующего реакции количества реагента, фосфониевой соли, в ТГФ или подобном инертном в реакции растворителе в присутствии гидрида натрия, алкиллития, трет-бутоксида калия или подобного основания предпочтительно при температуре от охлаждения льдом до комнатной температуры и также предпочтительно в атмосфере аргона.
Третий способ получения
(В реакционной схеме заместители Ra и Rb могут быть одинаковыми или отличаются друг от друга и каждый представляет собой Н или низший алкил, CH2NMe2, СН2ОМе, CN, Ph, CO2Et, CF3 или циклоалкил, или Ra и Rb вместе могут образовывать циклоалкил, и Rcпредставляет собой Н или низший алкил. Такие же определения будут использоваться в данном описании и далее).
Имидазольное соединение (XIV), полученное из соединения (VI), полученного в первом способе получения, и ацильного соединения (XIII) в соответствии с первым способом получения может быть превращено в соединение (Ia-ii) общеизвестным способом дигидроксилирования олефинового соединения (ed. J. March, "ADVANCED ORGANIC CHEMISTRY" (JOHN WILEY & SONS, 1992). Более предпочтительно, указанную реакцию проводят окислением олефинового соединения тетраоксидом осмия в смеси ТГФ-вода или подобном инертном в реакции растворителе в присутствии N-метилморфолин-N-оксида или подобного соокислителя. Реакцию проводят при температуре от охлаждения льдом до нагревания предпочтительно при комнатной температуре.
Соединение (Ia-ii) в качестве 1,2-гидрокси-соединения может быть превращено в кеталь (Ib-ii) или сложный ортоэфир общеизвестным способом с использованием эквивалентного кетону соединения или ортоэфирного соединения. Такую реакцию можно рассматривать как защитную реакцию 1,2-дигидрокси-соединения, и она может быть проведена с использованием условий реакций и т.п., описанных в приведенной выше "Protective groups in Organic Synthesis (3-rd Edition)".
Четвертый способ получения
(Символы на схеме имеют следующие значения.
L1: атом галогена или подобная уходящая группа;
Nu: нуклеофильный реагент;
Y: кетон или -С(R3)(OR1)-;
Rd: замещающая группа на низшем алкилене, соответствующая Х в общей формуле (I); и
R201: -S(O)m-низший алкил; -N3, N(R6)R7, -OCO-низший алкил или атом галогена. Такие же значения будут использоваться в данном описании и далее).
Данный способ получения проводят, подвергая соединение (XV), имеющее уходящую группу L1, полученное из соединения (VI) в соответствии с первым способом получения, и соответствующее реакции количество нуклеофильного реагента реакции замещения Sn2-типа в ТГФ, ацетоне, ДМФА, ацетонитриле, дихлорметане, метаноле, ДМСО или подобном инертном в реакции растворителе в присутствии карбоната калия или подобного неорганического основания или ТЭА или подобного органического основания в зависимости от обстоятельств в условиях охлаждения, от комнатной температуры до нагревания или при кипении с обратным холодильником. В качестве примеров нуклеофильного реагента можно назвать ацетат калия, азид натрия, тиометоксид натрия и подобные анионные соединения или аминные соединения и подобные основные соединения, хлорид-ионы и т.п.
Когда Y в соединении (XV) представляет собой кетон, соединение кетона (XVII), полученное из соединения (VI) в соответствии с первым способом получения, подвергают взаимодействию с бромом или бромистым водородом в уксусной кислоте или подобном инертном в реакции растворителе с превращением в α-бромкетон (XVIII), и указанное соединение (XVIII) может быть подвергнуто указанной выше реакции замещения Sn2-типа. Полученное таким образом замещенное соединение может быть превращено в соединение (I-i) восстановлением кетона по реакции восстановления, описанной ниже.
Когда нуклеофильный реагент представляет собой группу S-низший алкил, тиоалкильная группа полученного соединения может быть окислена до сульфоксидного соединения или сульфонового соединения с использованием окисляющего агента в соответствии с 10-м способом получения патентной ссылки 1. В качестве окисляющего агента более предпочтительно использовать м-хлорнадбензойную кислоту или перекись водорода.
Пятый способ получения
(В реакционной схеме Х2 представляет собой атом галогена, и кольцо D означает пиридин или имидазол, которые могут быть замещены.)
Данный способ получения представляет собой способ, в котором гидрокси-соединение (I-ii) получают, подвергая соответствующее реакции количество альдегидного соединения (XIX) взаимодействию с литийорганическим соединением (XXI), полученным из азотсодержащего галогенарильного соединения (ХХ) с использованием н-бутиллития или подобного органического основания в ТГФ или подобном инертном в реакции растворителе при температуре от -78°С до комнатной температуры.
Шестой способ получения
Данный способ получения проводят, подвергая дитиоацеталь (XXII) и диаминное соединение (XXIII) реакции конденсации в EtOH или подобном инертном в реакции растворителе при температуре от комнатной температуры до нагревания, предпочтительно нагревания в условиях кипячения с обратным холодильником.
(В реакционной схеме R111 и R112 представляют собой низший алкил, или R111 и R112 вместе образуют цикл, и замещающая группа в кольце В может быть защищена соответствующей защитной группой).
Кроме того, соединения настоящего изобретения и его фармацевтически приемлемые соли могут быть получены путем использования следующих общеизвестных способов превращения замещающей группы, учитывая типы замещающей группы.
1. Реакция восстановления
Восстановление кетогруппы до гидроксильной группы, восстановление азидогруппы в аминогруппу, восстановление ненасыщенной алкильной группы до насыщенной алкильной группы и аналогичные реакции могут быть проведены в соответствии с 4 способом получения патентной ссылки 1. Примерами более подходящих способов являются способ, в котором используют боргидрид натрия, боргидрид лития, диизобутилалюминийгидрид, литийалюминийгидрид или подобный восстанавливающий агент, и способ, в котором каталитическое восстановление проводят с использованием палладия (Pd), платины (Pt), никеля (Ni) или т.п. в атмосфере водорода или формиата аммония или подобного донора водорода.
2. Реакция ацилирования гидроксильной группы или аминогруппы
Реакцию ацилирования гидроксильной группы или аминогруппы проводят, подвергая гидрокси-соединение или амино-соединение взаимодействию с соответствующим реакции количеством хлорангидрида кислоты или ангидрида кислоты в дихлорметане, ДХЭ, пиридине, ТГФ, толуоле или подобном инертном в реакции растворителе в присутствии или в отсутствие диметиламинопиридина или т.п. при температуре от комнатной температуры до нагревания. Альтернативно реакция также может быть проведена, подвергая взаимодействию гидрокси-соединение и соответствующее реакции количество карбоновой кислоты в ДМФА или подобном инертном в реакции растворителе в присутствии или в отсутствие WSCHCl, OHBt, CDI или подобного конденсирующего агента, диметиламинопиридина или подобного ускорителя реакции и ТЭА или подобного органического основания в условиях от комнатной температуры до нагревания. Когда присутствуют две или несколько гидроксильных групп, реакция может быть проведена селективно по желаемому положению путем необязательного использования защитной группы. Дигидрокси-соединение также может быть превращено в соединение циклической угольной кислоты (циклический карбонат) путем использования CDI или т.п. В случае соединения, имеющего две или несколько гидроксильных групп и аминогрупп, могут быть ацилированы все такие группы или часть указанных групп.
3. Реакция гидролиза
Реакция гидролиза сложноэфирного соединения до гидрокси-соединения и карбоновой кислоты может быть проведена в соответствии с 8-м способом получения патентной ссылки 1. В качестве более предпочтительного способа реакцию проводят в ТГФ с использованием гидроксида натрия, гидроксида калия или подобного основания.
4. Превращение 1,2-дигидрокси-соединения в альдегид
Реакцию превращения 1,2-дигидрокси-соединения в альдегид проводят окислительным расщеплением 1,2-дигидроксиэтильной группы в ТГФ, воде, метаноле или подобном инертном в реакции растворителе с использованием перйодноватой кислоты или ее соли, тетраацетата свинца или подобного окисляющего агента. Полученное таким образом альдегидное соединение может быть превращено в амино-соединение в дихлорметане или подобном инертном в реакции растворителе в соответствии с 5-м способом получения патентной ссылки 1.
Соединения настоящего изобре