Производные ациламинотиазола, их получение и их применение в качестве ингибиторов продукции бета-амилоидного пептида
Иллюстрации
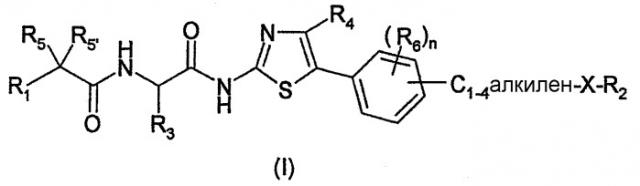
Показать всеИзобретение относится к новым соединениям формулы (I). Соединения настоящего изобретения могут найти применение в качестве лекарственного средства для лечения патологии, в которой является полезным ингибитор образования β-амилоидного пептида β-А4. В общей формуле (I):
Х обозначает атом кислорода; R1 обозначает С1-10-алкил, в случае необходимости замещенный фенилом, тиенилом; или R1 обозначает С3-7-циклоалкил, тиенил, пиридинил; тиенильные группы в случае необходимости могут быть замещены 1-2 C1-3-алкильными группами; фенил может быть в случае необходимости замещен 1-2 атомами галогена; R2 обозначает C1-6-алкил; или R2 обозначает С3-7-циклоалкил, фенил или пиридинил; фенил в случае необходимости может быть замещен одним или несколькими атомами галогена или группами CN, C1-3-алкила, C1-3-алкоксила, C1-3-фторалкоксила; R3 обозначает C1-6-алкил; R4 обозначает атом водорода или C1-6-алкил; R5 и R5' обозначают, независимо один от другого, атом водорода, гидроксил; или R5 и R5' вместе образуют оксо-группу; n обозначает целое число от 0 до 3; и R6 обозначает, независимо один от другого, атом водорода, галогена, C1-3-алкил, C1-3-алкоксил. Изобретение также относится к способу получения соединений, фармацевтической композиции, применению соединений для получения лекарственного средства. 6 н. и 2 з.п. ф-лы, 1 табл.
Реферат
Объектом изобретения являются производные ациламинотиазола, их получение и их применение в терапии.
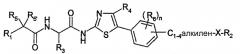
Первым объектом изобретения являются соединения, отвечающие общей формуле (I):
в которой:
X обозначает атом кислорода или серы;
R1 обозначает С1-10-алкил, в случае необходимости замещенный C3-7-циклоалкилом, фенилом, тиенилом; или R1 обозначает C3-7-циклоалкил, тиенил, пиридинил, пиримидинил;
тиенильные группы в случае необходимости могут быть замещены 1-3 С1-3-алкильными группами; фенил может быть в случае необходимости замещен 1-5 атомами галогена или C1-3-алкильными группами, C1-3-алкокси-группами, С1-3-фторалкильными группами, С1-3-фторалкокси-группами;
R2 обозначает C1-6-алкил, в случае необходимости замещенный C3-7-циклоалкилом, фенилом, C1-3-алкоксилом, гидроксилом; или R2 обозначает С3-7-циклоалкил, пиперидинил, фенил или пиридинил;
C3-7-циклоалкил и пиперидинил в случае необходимости могут быть замещены одной или несколькими группами C1-3-алкила, C1-3-алкоксила, гидроксила, C1-3-фторалкила, C1-3-фторалкоксила;
фенил и пиридинил в случае необходимости могут быть замещены одним или несколькими атомами галогена или группами CN, C1-3-алкила, C1-3-алкоксила, гидроксила, Cl-3-фторалкила, C1-3-фторалкоксила;
R3 обозначает атом водорода или С1-6-алкил, который может быть замещен С3-7-циклоалкилом;
R4 обозначает атом водорода или С1-6-алкил;
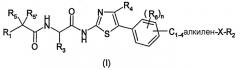
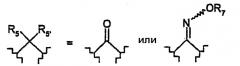
R5 и R5' обозначают, независимо один от другого, атом водорода, галогена, гидроксил, C1-3-алкил; или R5 и R5' вместе образуют оксо-группу или оксимную группу, такую как:
где R7 обозначает атом водорода или C1-3-алкил;
n обозначает целое число от 0 до 3; и
R6 обозначает, независимо один от другого, когда n=2 или 3, атом водорода, галогена, гидроксил, C1-3-алкил, С1-3-алкоксил, C1-3-фторалкил или C1-3-фторалкоксил.
Из соединений общей формулы (I), подгруппа предпочтительных соединений представлена соединениями, в которых:
- X обозначает атом кислорода или серы; и/или
- R1 обозначает C1-5-алкил, предпочтительно, метил, этил, 1-метилэтил, 1,1-диметилэтил, пропил, 1-метилпропил, 2-метилпропил, 1-этилпропил, которые могут быть замещены фенилом, тиенилом; или R1 обозначает C3-7-циклоалкил, предпочтительно, циклогексил, тиенил, пиридинил; тиенильные группы могут быть замещены одним или двумя C1-3-алкильными, предпочтительно, метильными группами; фенил может быть замещен одним или двумя атомами галогена, предпочтительно, хлора или фтора; и/или
- R2 обозначает C1-6-алкил, предпочтительно, этил, 1-метилэтил; или R2 обозначает C3-7-циклоалкил, предпочтительно, циклогексил, фенил или пиридинил; причем фенил может быть замещен 1-3 группами CN, C1-3-алкилами, предпочтительно, метилом, этилом, C1-3-алкоксилами, предпочтительно, метокси, этокси, гидроксилами, фторалкоксилами, предпочтительно, трифторметокси, или атомами галогена, предпочтительно хлора, фтора; и/или
- R3 обозначает C1-6-алкил, предпочтительно, метил, этил, пропил; и/или
- R4 обозначает атом водорода или C1-6-алкил, предпочтительно, метил или 4-метилпентил; и/или
- R5 и R5' обозначают, независимо один от другого, атом водорода, гидроксил; или R5 и R5' вместе образуют оксо-группу; и/или
- R6 обозначает атом водорода, галогена, предпочтительно, хлора или фтора, C1-3-алкил, предпочтительно, метил, C1-3-алкоксил, предпочтительно, метокси или этокси; и/или
- n=0 или 1.
Соединения, в которых одновременно X, R1, R2, R3, R4, R5, R5', R6 и n имеют значения, определенные выше для подгруппы предпочтительных соединений, являются особенно предпочтительными, и наиболее предпочтительными среди них являются соединения, в которых:
X обозначает атом кислорода; и/или
C1-4-алкилен является метиленом; и/или
атом углерода, несущий группу R3 имеет конфигурацию (S).
В качестве примера предпочтительных соединений можно назвать следующие соединения:
1. (2S)-2-{[(2R)-2-циклогексил-2-гидроксиацетил]амино}-N-(5-{2-[(циклогексилокси)метил]фенил}-1,3-тиазол-2-ил)пентанамид;
2. (2S)-2-{[(2S)-2-циклогексил-2-гидроксиацетил]амино}-N-(5-{2-[(циклогексилокси)метил]фенил}-1,3-тиазол-2-ил)пентанамид;
3. (2S)-N-(5-{2-[(циклогексилокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[2-(3-пиридинил)ацетил]амино}пентанамид;
4. N-((1S)-1-{[(5-{2-[(циклогексилокси)метил]фенил}-1,3-тиазол-2-ил)амино]карбонил}бутил)-2-гидрокси-4-метилпентанамид;
5. (2S)-N-{5-[2-(изопропоксиметил)фенил]-4-метил-1,3-тиазол-2-ил}-2-{[2-(3-тиенил)ацетил]амино}пентанамид;
6. (2S)-N-{5-[2-(изопропоксиметил)фенил]-1,3-тиазол-2-ил}-2-{[2-(3-тиенил)ацетил]амино}пентанамид;
7. (2S)-N-{5-[2-(изопропоксиметил)фенил]-1,3-тиазол-2-ил}-2-{[3-(3-тиенил)пропаноил]амино}пентанамид;
8. (2S)-N-{5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}-2-{[2-(3-тиенил)ацетил]амино}пентанамид;
9. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-{5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
10. (2S)-N-{5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}-2-{[2-(2-тиенил)ацетил]амино}бутанамид;
11. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-{5-[2-(изопропоксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
12. (2S)-N-{5-[2-(изопропоксиметил)фенил]-1,3-тиазол-2-ил}-2-{[2-(2-тиенил)ацетил]амино}пентанамид;
13. (2S)-2-[(3,3-диметилбутаноил)амино]-N-{5-[2-(изопропоксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
14. N-{(1S)-1-[({5-[2-(изопропоксиметил)фенил]-1,3-тиазол-2-ил}амино)карбонил]бутил}-3-метил-2-оксопентанамид;
15. (2S)-N-{5-[2-(этоксиметил)фенил]-1,3-тиазол-2-ил}-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
16. (2S)-2-{[2-(2,5-диметил-3-тиенил)ацетил]амино}-N-{5-[2-(этоксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
17. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-[5-(2-{[3-(трифторметокси)фенокси]метил}фенил)-1,3-тиазол-2-ил]пентанамид;
18. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-{5-[4-метокси-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
19. (2S)-N-(5-{2-[(2-фторфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
20. (2S)-N-(5-{2-[(2-этилфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
21. (2S)-2-{[3-(2,4-дихлорфенил)пропаноил]амино}-N-{5-[2-{феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
22. (2S)-2-{[2-(5-метил-2-тиенил)ацетил]амино}-N-{5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
23. (2S)-N-{5-{2-[(2,3-диметоксифенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
24. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-[5-(2-{[2-(трифторметокси)фенокси]метил}фенил)-1,3-тиазол-2-ил]пентанамид;
25. (2S)-N-(5-{2-[(3,5-диметоксифенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
26. (2S)-N-(5-{2-[(2,3-диметилфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
27. (2S)-N-(5-{2-[(3,4-диметилфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
28. (2S)-N-(5-{2-[(2,6-диметилфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
29. (2S)-N-(5-{2-[(3-хлорфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
30. (2S)-N-(5-{2-[(3,4-диметоксифенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
31. (2S)-N-(5-{2-[(2,6-диметоксифенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
32. (2S)-N-(5-{2-[(2,4-диметилфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
33. (2S)-N-(5-{2-[(2,5-диметилфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
34. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-{4-метил-5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
35. (2R)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-{5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
36. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-(5-{2-[(2-метилфенокси)метил]фенил}-1,3-тиазол-2-ил}пентанамид;
37. (2S)-2-{[(2S)-2-гидрокси-3-метилбутаноил]амино}-N-{5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
38. (2S)-2-[(2-гидрокси-3,3-диметилбутаноил)амино]-N-(5-{2-[(2-метоксифенокси)метил]фенил}-1,3-тиазол-2-ил)пентанамид;
39. (2S)-N-(5-{2-[(2-этоксифенокси)метил]фенил}-1,3-тиазол-2-ил)-2-[(2-гидрокси-3,3-диметилбутаноил)амино]пентанамид;
40. (2S)-2-[(2-гидрокси-3-фенилпропаноил)амино]-N-{5-[2-(феноксиметил)-фенил]-1,3-тиазол-2-ил}пентанамид;
41. (2S)-N-(5-{2-[(2,6-дихлорфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-[(2-гидрокси-3,3-диметилбутаноил)амино]пентанамид;
42. (2R)-3-этил-2-гидрокси-N-{(1S)-1-[({5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}амино)карбонил]бутил}пентанамид;
43. (2S)-3-этил-2-гидрокси-N-{(1S)-1-[({5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}амино)карбонил]бутил}пентанамид;
44. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-{5-[2-(изопропоксиметил)-4-метоксифенил]-1,3-тиазол-2-ил}пентанамид;
45. (2S)-N-(5-{2-[(2-(хлор-6-метилфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
46. (2S)-N-(5-{2-[(2,6-дифторфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
47. (2S)-N-{5-[4-хлор-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
48. (2S)-N-{5-[4-фтор-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
49. (2S)-2-{[(2S)-2-гидрокси-3-метилбутаноил]амино}-N-{5-[4-метокси-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
50. (2S)-N-(5-{2-[(3,4-дихлорфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
51. (2S)-N-((1S)-1-{[(5-{2-[(циклогексилокси)метил]фенил}-1,3-тиазол-2-ил}амино]карбонил}бутил)-2-гидрокси-4-метилпентанамид;
52. (2S)-N-{5-[4-этокси-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
53. (2S)-N-{5-[4-этокси-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}-2-{[(2S)-2-гидрокси-3-метилбутаноил]амино}пентанамид;
54. (2S)-N-{5-[5-фтор-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
55. (2S)-N-{5-[5-хлор-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
56. (2S)-N-{5-[5-фтор-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}-2-{[(2S)-2-гидрокси-3-метилбутаноил]амино}пентанамид;
57. (2S)-N-(5-{2-[(циклогексилокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
58. (2S)-2-гидрокси-3,3-диметил-N-[(1S)-1-метил-2-оксо-2-({5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}амино)этил]бутанамид;
59. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-{5-[4-метил-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
60. (2S)-2-{[(2S)-2-гидрокси-3-метилбутаноил]амино}-N-{5-[5-метил-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
61. (2S)-N-(5-{2-[(3-цианофенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
62. (2S)-N-(5-{2-[(3-фторфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
63. (2S)-N-(5-{2-[(3-фторфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3-метилбутаноил]амино}пентанамид;
64. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-{5-[5-метил-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
65. (2S)-2-{[(2S)-2-гидрокси-3-метилбутаноил]амино}-N-{5-[4-метил-2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид;
66. (2S)-N-((1S)-2-{[(5-{2-[(циклогексилокси)метил]фенил}-1,3-тиазол-2-ил}-амино]-1-метил-2-оксоэтил}-2-гидрокси-3,3-диметилбутанамид;
67. (2S)-N-(5-{2-[(2-хлор-5-метилфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
68. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-(5-{2-[(3-метилфенокси)метил)фенил}-1,3-тиазол-2-ил)пентанамид
69. (2S)-N-(5-{2-[(2-цианофенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
70. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-(5-{2-[(4-пиридинилокси)метил]фенил}-1,3-тиазол-2-ил)пентанамид;
71. (2S)-N-(5-{2-[(2-хлор-4,5-диметилфенокси))метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
72. (2S)-N-(5-{2-[(4-хлор-3-метилфенокси))метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
73. (2S)-N-(5-{2-[(2,3-дихлорфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
74. (2S)-N-(5-{2-[(2,3-дифторфенокси)метил]фенил}-1,3-тиазол-2-ил)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}пентанамид;
75. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-{4-(4-метилпентил)-5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил)пентанамид.
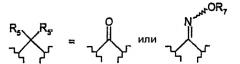
Объектом изобретения также являются, среди соединений общей формулы (I), соединения общей формулы (I'):
(I')
в которой:
X обозначает атом кислорода или серы;
R1 обозначает C1-10-алкил, в случае необходимости замещенный C3-7-циклоалкилом, фенилом, тиенилом; или R1 обозначает C3-7-циклоалкил, тиенил, пиридинил, пиримидинил;
тиенильные группы в случае необходимости могут быть замещены 1-3 С1-3-алкильными группами; фенил может быть в случае необходимости замещен 1-5 атомами галогена или C1-3-алкильными группами, C1-3-алкокси-группами, С1-3-фторалкильными группами, С1-3-фторалкокси-группами;
R2 обозначает C1-6-алкил, в случае необходимости замещенный C3-7-циклоалкилом, фенилом, C1-3-алкоксилом, гидроксилом; или R2 обозначает С3-7-циклоалкил, пиперидинил, фенил или пиридинил;
C3-7-циклоалкил и пиперидинил в случае необходимости могут быть замещены одной или несколькими группами C1-3-алкила, C1-3-алкоксила, гидроксила, C1-3-фторалкила, C1-3-фторалкоксила;
фенил и пиридинил в случае необходимости могут быть замещены одним или несколькими атомами галогена или группами C1-3-алкила, C1-3-алкоксила, гидроксила, C1-3-фторалкила, C1-3-фторалкоксила;
R3 обозначает атом водорода или С1-6-алкил, который может быть замещен С3-7-циклоалкилом;
R4 обозначает атом водорода или С1-4-алкил;
R5 и R5' обозначают, независимо один от другого, атом водорода, галогена, гидроксил, C1-3-алкил; или R5 и R5' вместе образуют оксо-группу или оксимную группу, такую как:
где R7 обозначает атом водорода или C1-3-алкил;
n обозначает целое число от 0 до 3; и
R6 обозначает, независимо один от другого, когда n=2 или 3, атом водорода, галогена, гидроксил, C1-3-алкил, C1-3-алкоксил, C1-3-фторалкил или C1-3-фторалкоксил.
Из соединений общей формулы (I') подгруппа предпочтительных соединений представлена соединениями, в которых:
- X обозначает атом кислорода или серы; и/или
- R1 обозначает C1-5-алкил, предпочтительно, метил, этил, 1-метилэтил, 1,1-диметилэтил, пропил, 1-метилпропил, 2-метилпропил, 1-этилпропил, которые могут быть замещены фенилом, тиенилом; или R1 обозначает C3-7-циклоалкил, предпочтительно, циклогексил, тиенил, пиридинил; тиенильные группы могут быть замещены одним или двумя C1-3-алкильными, предпочтительно, метильными группами; фенил может быть замещен одним или двумя атомами галогена, предпочтительно, хлора или фтора; и/или
- R2 обозначает C1-6-алкил, предпочтительно, этил, 1-метилэтил; или R2 обозначает C3-7-циклоалкил, предпочтительно, циклогексил, или фенил;
причем фенил может быть замещен одним или двумя C1-3-алкильными, предпочтительно, метильными, этильными, C1-3-алкокси-, предпочтительно, метокси-, этокси-, гидроксильными, фторалкокси-, предпочтительно, трифторметокси-, группами или одним или двумя атомами галогена, предпочтительно хлора, фтора; и/или
- R3 обозначает C1-6-алкил, предпочтительно, этил, пропил; и/или
- R4 обозначает атом водорода или C1-4-алкил, предпочтительно, метил; и/или
- R5 и R5' обозначают, независимо один от другого, атом водорода, гидроксил; или R5 и R5' вместе образуют оксо-группу; и/или
- R6 обозначает атом водорода, галогена, предпочтительно, хлора или фтора, C1-3-алкоксил, предпочтительно, метокси; и/или
- n=0 или 1.
В рамках изобретения понимают под:
- Ct-z, где t и z могут принимать значения от 1 до 10, углеродную цепь, которая может содержать от t до z атомов углерода, например, С1-3-углеродную цепь, которая может содержать от 1 до 3 атомов углерода, С3-6-углеродную цепь, которая может содержать от 3 до 6 атомов углерода, …;
- алкилом, прямую или разветвленную насыщенную алифатическую группу, например, С1-6-алкил обозначает прямую или разветвленную углеродную цепь из 1-6 атомов углерода, в частности, метил, этил, пропил, 1-метилэтил, бутил, 1-метилпропил, 2-метилпропил, 1,1-диметилэтил, …, предпочтительно, метил, этил, пропил или 1-метилэтил;
- алкиленом, двухвалентную алкильную группу;
- циклоалкилом, циклическую алкильную группу, например, C3-7-циклоалкил обозначает углеродный цикл из 3-7 атомов углерода, в частности, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, предпочтительно, циклопентил или циклогексил;
- алкоксилом, -О-алкильную группу, где алкил имеет указанные выше значения;
- фторалкилом, алкильную группу, в которой один или несколько атомов водорода замещены атомом фтора;
- фторалкоксилом, алкокси-группу, в которой один или несколько атомов водорода замещены атомом фтора; и
- атомом галогена, фтор, хлор, бром или иод.
Соединения общей формулы (I) могут содержать один или несколько асимметрических атомов углерода. Таким образом, они могут существовать в форме энантиомеров или диастереоизомеров. Эти энантиомеры, диастереоизомеры, а также их смеси, включая рацемические смеси, составляют часть изобретения.
Соединения формулы (I) могут существовать в виде оснований или солей присоединения с кислотами. Такие соли присоединения составляют часть изобретения.
Эти соли предпочтительно получают с фармацевтически приемлемыми кислотами, однако, соли с другими кислотами, пригодными, например, для очистки или выделения соединений формулы (I), также составляют часть изобретения.
Соединения общей формулы (I) могут находиться в форме гидратов или сольватов, а именно, в форме ассоциаций или комбинаций с одной или несколькими молекулами воды или с растворителем. Такие гидраты и сольваты также составляют часть изобретения.
В дальнейшем описании под отделяемой группой понимают группу, которая может быть легко отщеплена от молекулы с удалением электронной пары, путем разрыва гетеролитической связи. Эта группа может, таким образом, быть легко заменена на другую группу, например, в ходе реакции замещения. Такими отделяемыми группами являются, например, галогены или активированная гидроксильная группа, такая как мезилатная, тозилатная, трифлатная, ацетильная группы… и т.д. Примеры отделяемых групп, а также источники, в которых описано их получение, приведены в Advanced Organic Chemistry, J. March, 3rd Edition, Wiley Interscience, p 310-316.
Под защитной группой понимают группу, которая позволяет устранить реакционоспособность функциональной группы или положения в ходе химической реакции, которая может ее (его) затронуть, и которая приводит к исходной молекуле после отщепления известными специалисту методами. Примеры защитных групп, а также методы установления и снятия защиты, приведены, в числе прочих, Protective groups in Organic Synthesis, Greene et al., 2nd Ed. (John Wiley & Sons, Inc., New York).
Вторым объектом изобретения являются способы получения соединений формулы (I).
Так, эти соединения могут быть получены способами, иллюстрируемыми нижеследующими схемами, рабочие условия которых являются обычными известными специалисту.
Схема 1
Согласно схеме 1, соединение формулы (I) может быть получено пептидным связыванием амина формулы (XI) с кислотой формулы (XII) в условиях, известных специалисту, например, в присутствии гексафторфосфата бензотриазол-1-илокси-трис(диметиламино) фосфония (ВОР) и N-этилморфолина или N-метилморфолина в инертном растворителе, таком как диметилформамид, ацетонитрил или дихлорметан при температуре в интервале от 0°C до комнатной температуры.
Амин формулы (XI) получают пептидным связыванием амина формулы (VIII) с аминокислотой формулы (IX), в которой Pg обозначает защитную группу, в условиях, описанных выше, с получением соединения формулы (X). Аминокислоту формулы (IX) защищают, например, при помощи N-трет.-бутилоксикарбонила (Boc). Затем удаляют защиту с соединения (X) известными специалисту методами, получая амин формулы (XI). Например, если используемой защитной группой является Boc, ее удаляют с помощью кислотного гидролиза в присутствии безводной газообразной соляной кислоты.
Соединение формулы (VIII) может быть получено согласно схеме 2.
Схема 2
Согласно этой схеме, аралкил формулы (II), в которой Y обозначает отделяемую группу, предпочтительно, атом галогена, такой как атом брома, и Z обозначает атом галогена, такой как атом брома, конденсируют с алкоголятом или тиолатом щелочного металла, например, формулы R2X-Na+, где Х обозначает атом кислорода или серы. Реакцию проводят в инертном растворителе, таком как диметилформамид, при температуре от 0°C до 50°C, получая соединение формулы (III). Арил формулы (III) превращают в бороновую кислоту формулы (IV) способом, являющимся адаптацией способа, описанного Schoevaars, J. Am. Chem. Soc., 1999, 121, 9550-9561. Это превращение может, например, быть осуществлено путем предварительного образования аниона соединения (III), например, действием сильного основания, такого как бутиллитий, в эфирном растворителе, таком как тетрагидрофуран, при температурах от -50°C до -80°C. Этот анион затем вводят в реакцию с боратом, таким как триметилборат, с получением, в результате гидролиза, бороновой кислоты формулы (IV).
Связывание бороновой кислоты (IV) с 5-бромтиазолом формулы (VI), в которой Pg обозначает защитную группу, такую как иминогруппа, например, дифенилкетонимин, может быть осуществлено в соответствии с реакцией по Suzuki, с помощью способа, являющегося адаптацией способа, описанного Wolfe, J. Org. Chem., 1997, 62, 4943-4948, с получением 5-фенилтиазола формулы (VII). Связывание осуществляют, например, в эфирном растворителе, таком как диоксан, в присутствии тригидрата фосфата трикалия и катализатора, такого как тетракис(трифенилфосфин) палладия (0), при температуре в интервале от комнатной температуры до температуры кипения растворителя. С полученного таким образом 5-фенилтиазола формулы (VII) удаляют защитную группу известными специалисту методами, получая 5-фенил-2-аминотиазол формулы (VIII).
5-бромтиазол формулы (VI) получают, устанавливая защиту аминогруппы соответствующего соединения формулы (V). Предпочтительно, ее защищают в форме дифенилкетонимина в известных специалисту условиях.
Исходные соединения, в частности соединения формул (II), (V), (IX) и (XII), если способ их получения не описан, доступны на рынке или известны из литературы, или могут быть получены описанными в ней способами, или известны специалисту.
Например, 5-бром-2-амино-тиазол (V) может быть получен бромированием соответствующего 2-амино-тиазола согласно способу, являющемуся адаптацией способа, описанного Kaye, J. Chem. Soc. Perkins I, 1981, 2335-2339.
Например, соединение формулы (XII) может быть получено способом, являющимся адаптацией способа, описанного Middleton et al., J. Org. Chem., 45, 14, 1980, 2883-2887 и Miyamoto et al., J. Amer. Chem. Soc., 114, 15, 1992, 6256-6257.
Значения X, R1, R2, R3, R4, R5, R5', R6 и n в соединениях формул (II)-(XII) соответствуют значениям, определенным для соединений формулы (I).
В следующих примерах описано получение некоторых соединений согласно изобретению. Эти примеры не являются ограничительными и служат только для иллюстрации изобретения. Номера соединений, представленных в примерах, соответствуют номерам в следующей далее таблице. Микроанализы элементарного состава и спектры ЯМР, ИК или масс-спектры подтверждают структуру полученных соединений.
Пример 1 (соединение 9)
(2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-{5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид
1.1. 1-бром-2-(феноксиметил)бензол
К 20,2 г фенола в растворе в 150 мл диметилформамида добавляют порциями при 5°C 1,2 г гидрида натрия (в виде 50%-й суспензии в масле). Перемешивают при комнатной температуре и вводят при 5°C 37,2 г 2-бромбензилбромида в растворе в 15 мл диметилформамида. Через 2 часа при 20°C реакционную среду выливают на смесь воды со льдом и экстрагируют этилацетатом. Органическую фазу высушивают над безводным сульфатом натрия и концентрируют, получая 36 г масла.
ЯМР 1H δ в ч.млн (ДМСО d6): 5,22 (с, 2H); 7,09-7,67 (мультиплет, 9H).
1.2. 2-(феноксиметил)фенилбороновая кислота
К 36 г 1-бром-2-(феноксиметил)бензола, полученного на стадии 1.1, в растворе в 150 мл тетрагидрофурана, добавляют по каплям при -70°C, 90 мл n-бутиллития (1,6 M) в растворе в гексане. Через 2 часа при -70°C по каплям добавляют 16 мл триметилбората. Дают температуре среды подняться до -30°C. Осуществляют гидролиз с помощью насыщенного раствора хлорида аммония, затем экстрагируют этилацетатом и высушивают органическую фазу безводным сульфатом натрия. После упаривания получают 33 г твердого вещества белого цвета.
ЯМР 1H δ в ч.млн (ДМСО d6): 5,25 (с, 2H); 6,85-7,67 (мультиплет, 11H).
1.3. 5-бром-N-(дифенилметилен)-1,3-тиазол-2-амин
К 34 г 5-бром-1,3-тиазол-2-аминбромгидрата в суспензии в 300 мл 1,2-дихлорэтана добавляют 26 г бензофенонимина. Смесь кипятят в течение 18 часов с обратным холодильником. Отфильтровывают сформировавшийся осадок и концентрируют фильтрат, получая 37,2 г твердого вещества.
Т.пл.=109°C.
ЯМР 1H δ в ч.млн (ДМСО d6): 7,34 (м, 2H); 7,50-7,76 (мультиплет, 9H).
1.4. 5-{2-[(фенокси)метил]фенил}-N-(дифенилметилен)-1,3-тиазол-2-амин
В 14,8 г 2-(феноксиметил)фенилбороновой кислоты, полученной на стадии 1.2, в растворе 250 мл 1,4-диоксана последовательно вводят 15 г дигидрата фосфата трикалия, 10,5 г 5-бром-N-(дифенилметилен)-1,3-тиазол-2-амина, полученного на стадии 1.3, 1,5 г тетракис(трифенилфосфина) палладия (0) и кипятят 1 час с обратным холодильником. Реакционную среду упаривают досуха, помещают в этилацетат и промывают водой. Органическую фазу высушивают над безводным сульфатом натрия и концентрируют растворители. Остаток хроматографируют на колонке с силикагелем, используя в качестве элюента дихлорметан, и получают 35 г масла желтого цвета.
ЯМР 1H δ в ч.млн: 4,81 (с, 2H); 7,17-7,83 (мультиплет, 20H).
1.5. 5-{2-[(фенокси)метил]фенил}-1,3-тиазол-2-амин
К 35 г 5-{2-[(фенокси)метил]фенил}-N-(дифенилметилен)-1,3-тиазол-2-амина, полученного на стадии 1.4, в растворе в 250 мл метанола, добавляют 150 мл водного раствора соляной кислоты (1 M) и перемешивают 18 часов при 20°C. Упаривают досуха, помещают остаток в диэтиловый эфир и промывают водным раствором гидроксида натрия (0,5 M). Органическую фазу высушивают над безводным сульфатом натрия и концентрируют. Остаток хроматографируют на колонке с силикагелем, используя в качестве элюента смесь дихлорметан/метанол 98/2 (об./об.), получая 15 г твердого вещества бежевого цвета.
Т.пл.=154°C.
ЯМР 1H δ в ч.млн (ДМСО d6): 5,07 (с, 2H); 6,98-7,65 (мультиплет, 10H).
1.6. трет.-бутил-(1S)-1-[({5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}-амино)карбонил]бутилкарбамат
К 3,35 г (2S)-2-[(трет.-бутилоксикарбонил)амино]пентановой кислоты в растворе в 35 мл диметилформамида добавляют при 0°C 7,1 г гексафторфосфата бензотриазол-1-илокси-трис(диметиламино)фосфония, затем, по каплям, 2,1 мл N-метилморфолина. Через 15 минут при 0°C вводят 4 г 5-{2-[(фенокси)метил]фенил}-1,3-тиазол-2-амина, полученного на стадии 1.5, и перемешивают 18 часов при комнатной температуре. Среду помещают в этилацетат и промывают 2 раза водой. Органическую фазу высушивают над безводным сульфатом натрия и концентрируют. Остаток хроматографируют на колонке с силикагелем, используя в качестве элюента смесь дихлорметан/метанол 98/2 (об./об.), получая 5,2 г бесцветного масла.
ЯМР 1H δ в ч.млн (ДМСО d6): 0,88 (т, 3H); 1,22-1,65 (мультиплет, 13H); 4,24 (кв, 1H); 5,09 (с, 2H); 6,94-7,67 (мультиплет, 10H) 12,23 (с, 1H).
1.7. гидрохлорид (2S)-2-амино-N-(5-{2-[(фенокси)метил]фенил}-1,3-тиазол-2-ил)пентанамида
К 5 г трет.-бутил-(1S)-2-[(5-{2-[(фенокси)метил]фенил}-1,3-тиазол-2-ил)амино]-1-пропил-2-оксоэтилкарбамата, полученного на стадии 1.6, в растворе в 60 мл этилацетата, добавляют по каплям при 0°C 25 мл раствора газообразной соляной кислоты (4,5 М) в этилацетате. Среду перемешивают 18 часов при 20°C. Сформировавшийся осадок отфильтровывают, промывают 2 раза диэтиловым эфиром и высушивают, получая 3 г твердого вещества белого цвета.
Т.пл.=148°C.
ЯМР 1H δ в ч.млн (ДМСО d6): 0,90 (т, 3H); 1,39 (м, 2H); 1,85 (м, 2H); 4,18 (кв, 1H); 5,08 (с, 2H); 6,94-7,68 (мультиплет, 10H); 8,65 (с, 3H).
1.8. (2S)-2-{[(2S)-2-гидрокси-3,3-диметилбутаноил]амино}-N-{5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид
К 0,32 г (2S)-2-гидроксил-3,3-диметилбутановой кислоты в растворе в 25 мл диметилформамида при 0°C последовательно добавляют 1,36 г гексофторфосфата бензотриазол-1-илокситрипирролидинфосфония и 0,7 мл N-этилморфолина. Через 20 минут при 0°C вводят 0,88 г гидрохлорида (2S)-2-амино-N-(5-{2-[(фенокси)метил]фенил}-1,3-тиазол-2-ил)пентанамида, полученного на стадии 1.7, и перемешивают в течение 18 часов при комнатной температуре. Реакционную среду помещают в этилацетат и промывают водой. Органическую фазу высушивают над безводным сульфатом натрия и концентрируют. Остаток хроматографируют на колонке с силикагелем, используя в качестве элюента смесь дихлорметан/метанол 99/1 (об./об.), получая после кристаллизации в изопропиловом эфире 0,83 г твердого вещества белого цвета.
Т.пл.=84°C.
ЯМР 1H δ в ч.млн (ДМСО d6): 0,89 (т, 3H); 0,93 (с, 9H); 1,33 (м, 2H); 1,71 (кв, 21H); 3,57 (д, 1H); 4,61 (кв, 1H); 5,09 (с, 2H); 5,61 (д, 1H); 6,97-7,02 (мультиплет, 3H); 7,28-7,67 (мультиплет, 7H); 7,81 (д, 1H); 12,28 (с, 1H).
[α]D 20=-81,8 (c=1/CH3OH).
Пример 2 (соединение 16)
(2S)-2-{[2-(2,5-диметил-3-тиенил)ацетил]амино}-N-{5-[2-(этоксиметил)-фенил]-1,3-тиазол-2-ил}пентанамид
2.1. 2-(2,5-диметил-3-тиенил)-1-(4-морфолинил)-1-этантион
К 5 г 2,5-диметил-3-ацетилтиофена добавляют 1,68 г серы, 6,5 мл морфолина и кипятят 10 часов с обратным холодильником. Охлаждают до 20°C и выливают в водный раствор соляной кислоты (1 н.). Среду экстрагируют этилацетатом. Органическую фазу высушивают над безводным сульфатом натрия и концентрируют. Остаток очищают хроматографией на колонке с силикагелем, используя в качестве элюента смесь циклогексан/этилацетат 8/2 (об./об.), получая 6,8 г масла оранжевого цвета.
ЯМР 1H δ в ч.млн (ДМСО d6): 2,30 (с, 3H); 2,34 (с, 3H); 3,47 (т, 2H); 3,65 (м, 4H); 4,07 (с, 2H); 4,20 (т, 2H); 6,56 (с, 1H).
2.2. 2-(2,5-диметил-3-тиенил)уксусная кислота
2-(2,5-диметил-3-тиенил)уксусную кислоту получают способом, описанным в Heterocycl. Chem; EN; 25; 1988; 1571-1581.
К 6,7 г 2-(2,5-диметил-3-тиенил)-1-(4-морфолинил)-1-этантиона, полученного на стадии 2.1, в растворе в 70 мл метанола добавляют 21 мл водного раствора гидроксида натрия (50 мас.%) и кипятят 6 часов с обратным холодильником. После выпаривания метанола остаток разбавляют водой и подкисляют водным раствором соляной кислоты (6 н.). Сформировавшийся осадок отфильтровывают, затем хроматографируют на колонке с силикагелем, используя в качестве элюента дихлорметан, и получают 3,6 г кристаллов бежевого цвета.
Т.пл.=65°C.
ЯМР 1H δ в ч.млн (ДМСО d6): 2,26 (с, 3H); 2,34 (с, 3H); 3,39 (с, 2H); 6,56 (с, 1H).
2.3. (2S)-2-{[(2,5-диметил-3-тиенил)ацетил]амино}-N-{5-[2-(этоксиметил)фенил]-1,3-тиазол-2-ил}пентанамид
Действуют аналогично стадии 1.8 примера 1, заменяя (2S)-2-гидрокси-3,3-диметилбутановую кислоту 2-(2,5-диметил-3-тиенил) уксусной кислотой, полученной на стадии 2.2. Получают 0,67 г кристаллов белого цвета.
Т.пл.=84°C.
ЯМР 1H δ в ч.млн (ДМСО d6): 0,89 (т, 3H); 1,16 (т, 3H); 1,29 (м, 2H); 1,65 (м, 2H); 2,25 (с, 3H); 2,30 (с, 3H); 3,33 (м, 2H); 3,47 (кв, 2H); 4,44 (с, 2H); 4,49 (кв, 1H); 4,55 (с, 1H); 7,35-7,55 (мультиплет, 5H); 8,32 (д, 1H); 12,28 (с, 1H).
[α]D 20=-103 (c=1/CH3OH).
Пример 3 (соединение 22)
(2S)-2-{[2-(5-метил-2-тиенил)ацетил]амино}-N-{5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид
3.1. 2-(5-метил-2-тиенил)-1-(4-морфолинил)-1-этантион
2-(5-метил-2-тиенил)-1-(4-морфолинил)-1-этантион получают способом, аналогичным способу, описанному в примере 2.1.
ЯМР 1H δ в ч.млн (ДМСО d6): 2,40 (с, 3H); 3,49 (т, 2H); 3,64 (т, 2H); 3,81 (т, 2H); 4,19 (т, 2H); 4,40 (с, 2H); 6,49 (д, 1H); 6,77 (д, 1H).
3.2. 2-(5-метил-2-тиенил)уксусная кислота
2-(5-метил-2-тиенил)уксусную кислоту получают способом, аналогичным способу, описанному в примере 2.2.
Т.пл.=54°C.
ЯМР 1H δ в ч.млн (ДМСО d6): 2,38 (с, 3H); 3,72 (с, 3H); 6,61 (д, 1H); 6,69 (д, 1H).
3.3. (2S)-2-{[2-(5-метил-2-тиенил)ацетил]амино}-N-{5-[2-(феноксиметил)фенил]-1,3-тиазол-2-ил}пентанамид
Действуют аналогично стадии 1.8 примера 1, заменяя (2S)-2-гидрокси-3,3-диметилбутановую кислоту 2-(5-метил-2-тиенил) уксусной кислотой, полученной на стадии 3.2. Получают 0,73 г кристаллов бежевого цвета.
Т.пл.=81°C.
ЯМР 1H δ в ч.млн (ДМСО d6): 0,87 (т, 3H); 1,32 (м, 2H); 1,64 (м, 2H); 2,36 (с, 3H); 3,62 (кв, 2H); 4,48 (кв, 1H); 5,07 (с, 2H); 6,59 (д, 1H); 6,67 (д, 1H); 6,95-7 (мультиплет, 3H); 7,27-7,73 (мультиплет, 7H); 8,41 (д, 1H); 12,30 (с, 1H).
[α]D 20=-91,7 (c=1/CH3OH).
Пример 4 (соединение 7)
(2S)-N-{5-[2-(изопропоксиметил)фенил]-1,3-тиазол-2-ил}-2-{[3-(3-тиенил)пропаноил]амино}пентанамид
4.1. (E)-3-(3-тиенил)-2-пропеновая кислота
К 25 г 3-тиенальдегида в растворе 100 мл пиридина добавляют 46 г малоновой кислоты, 2 мл пиперидина и нагревают при 100°C в течение 4 часов. Реакционную среду охлаждают до 30°C и выливают в водный раствор соляной кислоты (2 н.). Сформировавшийся осадок отфильтровывают и промывают изопропиловым эфиром, получая после высушивания 30 г твердого вещества белого цвета.
Т.пл.=152°C.
ЯМР 1H δ в ч.млн (ДМСО d6): 6,36 (д, 1H); 7,51-7,62 (мультиплет, 3H); 7,93 (д, 1H); 12,27 (с, 1H).
4.2. Этил-(E)-3-(3-тиенил)-2-пропеноат
К 11 г (E)-3-(3-тиенил)-2-пропеновой кислоты, полученной на стадии 4.1, в растворе в 50 мл диметилформамида добавляют 11,5 г карбоната калия, 6,8 мл иодэтана и перемешивают в течение 48 часов при 20°C. Среду помещают в этилацетат и промывают водой. Органическую фазу высушивают над безводным сульфатом натрия и концентрируют, получая 12,5 г масла.
ЯМР 1H δ в ч.млн (ДМСО d6): 1,26 (т, 3H); 4,17 (кв, 2H); 6,47 (д, 1H); 7,57-7,71 (мультиплет, 3H); 8,01 (д, 1H).
4.3. Этил-3-(3-тиенил)-2-пропаноат
К 12,5 г этил-(E)-3-(3-тиенил)-2-пропеноата, полученного на стадии 4.2, в растворе в 100 мл этанола, добавляют 4 г 10%-ого палладия на угле и перемешивают в течение 24 часов при 60°C под давлением водорода 5 бар. Отфильтровывают катализатор и концентрируют фильтрат, получая 11 г масла.
ЯМР 1H δ в ч.млн (ДМСО d6): 1,20 (т, 3H); 2,62 (т, 2H); 2,88 (т, 2H); 4,07 (кв, 2H); 7,02 (д, 1H); 7,18 (м, 1H); 7,45 (м, 1H).
4.4. 3-(3-тиенил)пропановая кислота
К 11 г этил-3-(3-тиенил)-2-пропаноата, полученного на стадии 4.3, в растворе в 100 мл этанола добавляют 75 мл водного раствора гидроксида натрия (2 н.). Перемешивают в течение 18 часов при 20°C. После выпаривания растворителей остаток подкисляют. Сформировавшийся осадок отфильтровывают и высушивают в вакууме, получая 6,3 г твердого вещества бежевого цвета.
Т.пл.=59°C.
ЯМР 1H δ в ч.млн (ДМСО d6): 2,56 (т, 2H); 2,85 (т, 2H); 7,02 (т, 1H); 7,18 (с, 1H); 7,45 (м, 1H); 12,14 (с, 1H).
4.5. (2S)-N-{5-[2-изопропоксиметил)фенил]-1,3-тиазол-2-ил}-2-{[3-(3-тиенил)пропаноил]амино}пентанамид
Действуют аналогично стадии 1.8 примера 1, заменяя (2S)-2-гидрокси-3,3-диметилбутановую кислоту 3-(3-тиенил)пропановой кислотой, полученной на стадии 4.4. Получают 0,75 г кристаллов бежевого цвета.
Т.пл.=101°C.
ЯМР 1H δ в ч.млн (ДМСО d6): 0,87 (т, 3H); 1,13 (д, 6H); 1,33 (м, 2H); 1,62 (м, 2H); 2,48 (т, 2H); 2,82 (т, 2H); 3,67 (м, 1H); 4,45 (с, 2H); 4,54 (кв, 1H); 6,98 (д, 1H); 7,12 (д, 1H); 7,35-7,57 (мультиплет, 6H); 8,21 (д, 1H); 12,26 (с, 1H).
[α]D 20=-71(c=1/CH3OH).
Пример 5
(2R)-3-этил-2-гидрокси-N-{(1S)-1-[({5-[2-(феноксиметил) фенил]-1,3-тиазол-2-ил}амино)карбонил]бутил}пентанамид (соединение n 42) и
(2S)-3-этил-2-гидрокси-N-{(1S)-1-[({5-[2-(феноксиметил) фенил]-1,3-тиазол-2-ил}амино)карбонил]бутил}пентанамид (соединение 43)
5.1. 3-этил-2-гидроксипентановая кислота
К раствору 1,24 мл 2-этилбутиральдегида в 18 мл безводного дихлорметана осторожно добавляют 1,5 мл триметилсилилцианида, затем каталитическое количество иодида цинка. Реакционную среду перемешивают в течение 2 часов при комнатной температуре, затем в течение 3,5 часов при 60°C. Реакционную среду охлаждают до 0°C и добавляют 3,5 мл концентрированной соляной кислоты. Реакционную среду перемешивают в течение 18 часов при комнатной температуре, затем 1 час при кипячении с обратным холодильником. После охлаждения реакционную смесь выливают в воду