Инъецируемые стержни из фосфата кальция для доставки остеогенных белков
Иллюстрации
Показать всеНастоящее изобретение относится к медицине и касается доставки остеогенных белков путем инъецирования в форме твердого стержня. Композиции содержат кальций-фосфатный материал, остеогенный белок и необязательные добавки, например такие, как ингибитор резобции кости. Описаны также способы приготовления фармацевтических композиций и способы применения остеогенных композиций для лечения дефектов кости. Изобретение обеспечивает снижение тяжести остеопороза и количество остеопоротических поражений, заживление переломов, восстановление хрящей, заживление несрастающихся дефектов и артродез, стимуляцию роста костей. 4 н. и 24 з.п. ф-лы, 1 табл., 2 ил.
Реферат
Родственные заявки
[0001] Данная заявка испрашивает приоритет согласно предварительной заявке США №60/502493, поданной 12 сентября 2003 г., описание которой включено в данную заявку по ссылке.
Область изобретения
[0002] Предлагаемое изобретение относится к области остеогенных белков и содержащих их фармацевтических составов.
Предпосылки создания изобретения
[0003] Идиопатический остеопороз - это заболевание неизвестной этиологии, характеризующееся прогрессирующей потерей костной массы и повышенной хрупкостью костей, которые приводят к значительному увеличению подверженности переломам. Остеопороз входит в число самых распространенных заболеваний опорно-двигательного аппарата. Он поражает пятьдесят шесть процентов женщин старше 45 лет. Praemer et al., "Musculoskeletal Conditions in the United States" (Заболевания опорно-двигательного аппарата в Соединенных Штатах), Amer. Acad. of Orthopaedic Surgeons, Park Ridge, IL (1992). Поскольку число случаев остеопороза увеличивается с возрастом и процент заболеваемости среди пожилых лиц в популяции растет, со временем остеопороз станет более распространен. Местное лечение остеопороза затруднительно, и на сегодняшний день не существует известного средства или способа лечения. Наконец, и это является наиболее существенным, остеопороз связан со значительными заболеваемостью и смертностью. Наиболее серьезным видом переломов, причина которых - остеопороз, является перелом проксимальной части бедренной кости в области тазобедренного сустава. Переломы костей тазобедренного сустава, число случаев которых составляет более 300000 в год, в настоящее время являются самыми распространенными переломами среди пожилых людей. Каждая шестая женщина европеоидной расы в течение жизни переносит перелом костей тазобедренного сустава (Cummingset al., Arch. Intern. Med., vol. 149, pp.2455-2458 (1989)), а среди женщин, достигших возраста 96 лет, такой перелом переносит каждая третья.
[0004] Кроме лечения пораженных остеопорозом костей, существует потребность в способах лечения или профилактики связанных с остеопорозом переломов, например путем местного введения остеогенных белков. Остеогенные белки представляют собой белки, способные стимулировать формирование хряща и/или кости или способствовать стимуляции.
В последние годы было выделено и описано большое количество таких остеогенных белков, а некоторое количество было получено рекомбинантными методами.
[0005] Кроме того, были разработаны разнообразные лекарственные формы для доставки остеогенных белков в участок, где желательно стимулировать формирование кости.
[0006] Однако, несмотря на значительные усилия, прилагаемые в данной области, все еще остается потребность в эффективном способе восстановления и/или лечения пораженных остеопорозом или остеопенией костей, а также минимизации или снижения количества случаев или тяжести связанных с остеопорозом переломов.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0007] Настоящее изобретение относится к композициям для доставки остеогенных белков путем инъекции, т.е. к остеогенным композициям. Эти композиции могут иметь форму твердого стержня, предпочтительно цилиндрического твердого стержня, или отверждающейся пасты. Композиции содержат остеогенный кальций-фосфатный материал.
[0008] В некоторых предпочтительных вариантах реализации настоящего изобретения остеогенный белок может являться членом семейства «костных морфогенетических белков» (BMP), более предпочтительно - одним из белков BMP-2, BMP-4, BMP-5, BMP-6, BMP-7, BMP-10, BMP-12 и BMP-13, а наиболее предпочтительно - белком BMP-2. Остеогенный белок предпочтительно присутствует в количестве, варьирующемся в пределах от приблизительно 1% до приблизительно 90%, более предпочтительно - от приблизительно 15% до приблизительно 40% от массы твердых стержней согласно данному изобретению, и в количестве, варьирующемся в пределах от приблизительно 0.01% до приблизительно 2%, более предпочтительно - от приблизительно 0.03% до приблизительно 1% от массы пасты согласно данному изобретению.
[0009] В некоторых предпочтительных вариантах реализации настоящего изобретения кальций-фосфатный материал содержит материал, выбранный из аморфного фосфата кальция типа апатита, слабокристаллизованного фосфата кальция типа апатита, гидроксиапатита, трикальция фосфата, фторапатита и их комбинаций. Наиболее предпочтительно кальций-фосфатный материал представляет собой слабокристаллизованный фосфат кальция типа апатита. Кальций-фосфатный материал предпочтительно присутствует в количестве, варьирующемся в пределах от приблизительно 10% до приблизительно 99%, более предпочтительно - от приблизительно 40% до приблизительно 60% от массы остеогенной композиции в форме стержня, и в количестве, варьирующемся в пределах от приблизительно 30% до приблизительно 70%, более предпочтительно - от приблизительно 45% до приблизительно 55% от массы остеогенной композиции в форме отверждающейся пасты.
[0010] Дополнительные варианты реализации настоящего изобретения относятся к остеогенным композициям, которые содержат также ингибитор резорбции кости. Ингибитор резорбции кости предпочтительно представляет собой бифосфонат, выбранный из алендроната (alendronate), цимадроната (cimadronate), клодроната (clodronate), ЕВ 1053, этидронатов (etidronates), ибандроната (ibandronate), неридроната (neridronate), олпадроната (olpadronate), памидроната (pamidronate), резидроната (risedronate), тилудроната (tiludronate), YH 529, золедроната (zoledronate) и их фармацевтически приемлемых солей, эфиров, кислот, а также их смесей.
[0011] Другие варианты реализации настоящего изобретения относятся к остеогенным композициям, которые содержат также какую-либо добавку, выбранную из фармацевтически приемлемых солей, полисахаридов, пептидов, белков, аминокислот, синтетических полимеров, природных полимеров, поверхностно-активных веществ, а также их комбинаций, более предпочтительно выбранную из карбоксиметилцеллюлозы, гидроксипропилметилцеллюлозы, метилцеллюлозы, полимера молочной кислоты (полилактида), полиэтиленгликоля, поливинилпирролидона, полиоксиэтилена оксида, карбоксивинилового полимера, поливинилового спирта, декстрана сульфата и их комбинаций. Добавка предпочтительно присутствует в количестве, варьирующемся в пределах от приблизительно 1% до приблизительно 90%, более предпочтительно - от приблизительно 20% до приблизительно 40% от массы остеогенной композиции в форме стержня, и в количестве, варьирующемся в пределах от приблизительно 1% до приблизительно 90%, более предпочтительно - от приблизительно 10% до приблизительно 20% от массы остеогенной композиции в форме отверждающейся пасты.
[0012] В случае, когда остеогенная композиция согласно настоящему изобретению имеет форму твердого цилиндрического стержня, диаметр этого цилиндрического стержня предпочтительно лежит в пределах от приблизительно 0.1 мм до приблизительно 3.0 мм, более предпочтительно - составляет приблизительно 1.0 мм, а длина цилиндрического стержня предпочтительно лежит в пределах от приблизительно 0.5 см до предпочтительно 5.0 см.
[0013] Еще один вариант реализации настоящего изобретения относится к способу приготовления композиции в форме стержня для доставки остеогенных белков путем инъекции, при этом композиция содержит остеогенный белок и калций-фосфатный материал, а способ включаюет следующие этапы: (a) смешивание сухой формы остеогенного белка с сухой формой фосфата кальция, в результате которого получают сухую смесь; (b) восстановление сухой смеси путем добавления водного буфера, в результате которого получают пасту; (c) формовка пасты, в результате которой получают композицию в форме стержня; и (d) сушка композиции в форме стержня, полученной на этапе (c), в результате которой получают композицию в форме стержня для доставки остеогенных белков путем инъекции. В предпочтительных способах реализации водный буфер выбирают из фосфатного буферного раствора, физиологического раствора, буферов на основе глицина и глутаминовой кислоты и их комбинаций. Отношение объем: масса (мл:г) водного буфера к сухой смеси лежит в пределах от приблизительно 0.5:1 до приблизительно 2:1. Формовку предпочтительно выполняют путем формовки, экструзии, прессования, сверления или комбинаций этих операций. В некоторых предпочтительных способах реализации композицию в форме стержня нарезают перед этапом (d) или после него.
[0014] Еще один вариант реализации настоящего изобретения относится к способу приготовления композиции в форме пасты для доставки остеогенных белков путем инъекции, при этом композиция содержит остеогенный белок и кальций-фосфатный материал, а способ включает этап смешивания сухой формы кальций-фосфатного материала с водным буфером, содержащим остеогенный белок, с получением пасты. В предпочтительных вариантах реализации настоящего изобретения водный буфер выбирают из фосфатного буферного раствора, физиологического раствора, буферов на основе глицина и глутаминовой кислоты и их комбинаций. Отношение водного буфера к кальций-фосфатному материалу варьируется от приблизительно 0.5:1 до приблизительно 2:1.
[0015] Дальнейшие варианты реализации настоящего изобретения относятся к способам лечения млекопитающих, страдающих дефектами костей, включающим введение в участок дефекта кости эффективного количества описанной здесь композиции для доставки остеогенных белков путем инъекции. Дальнейшие варианты реализации настоящего изобретения относятся к способам лечения млекопитающих, страдающих дефектами костей, включающим следующие этапы: (a) введение в участок дефекта кости эффективного количества описанной здесь композиции для доставки остеогенных белков путем инъекции, и (b) введение в участок дефекта кости эффективного количества ингибитора резорбции кости. Введение ингибитора резорбции кости можно проводить до этапа (a), после этапа (a) или одновременно с этапом (a).
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
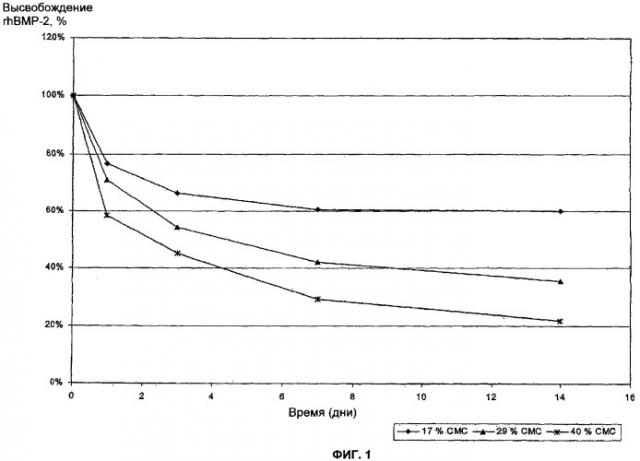
[0016] Фигура 1 представляет собой график, показывающий кинетику высвобождения rhВМР-2 из стержней α-BSM in vitro при использовании 1251-rhBMP-2 в качестве метки.
[0017] Фигура 2 представляет собой график, показывающий местное удержание rhBMP-2 из стержней α-BSM in vivo при использований 251-rhBMP-2 в качестве метки.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0018] В целом, способы и составы согласно настоящему изобретению относятся к регенерации костной ткани и сопутствующему увеличению костной массы, плотности костей и прочности костей. Более конкретно, предложенное изобретение включает инъецируемые твердые стержни и пасты, содержащие остеогенный белок, кальций-фосфатный носитель и, факультативно, добавки и активные вещества, такие как ингибитор резорбции кости, а также способы приготовления таких остеогенных композиций и способы лечения, в которых применяются такие остеогенные композиции. Кальций-фосфатные твердые стержни и отверждающиеся пасты согласно настоящему изобретению подходят для внутрикостной доставки остеогенных белков. Посредством применения способов и композиций согласно настоящему изобретению можно успешно снизить тяжесть остеопороза и количество остеопоротических поражений, что, в конечном счете, приведет к уменьшению числа случаев переломов костей. Другие способы применения в клинике включают заживление переломов, восстановление хрящей, заживление несрастающихся дефектов и артродез. Инъецируемые твердые стержни и отверждающиеся пасты согласно настоящему изобретению можно также применять для стимуляции роста костей, что необходимо при использовании имплантантов для замещения суставов, согласно описанию предварительной заявки США №60/502526 ("Promotion of Bone growth in Joint Replacement Implants Using Osteogenic Proteins″ - Стимуляция роста кости в имплантах для замещения суставов); описание этой предварительной заявки включено в настоящую заявку во всей полноте путем ссылки.
[0019] Первый вариант реализации настоящего изобретения относится к композициям в форме стержней для доставки остеогенных белков путем инъекции, содержащим остеогенный белок и кальций-фосфатный материал. Композиция согласно этому первому варианту реализации настоящего изобретения может факультативно включать другие добавки (связующие вещества, наполнители) и/или активные вещества, такие как ингибитор резорбции кости.
[0020] Эти композиции в форме твердых стержней подходят для местной внутрикостной доставки и, следовательно, их можно вводить путем инъекции непосредственно в участок, пораженный остеопорозом или остеопенией, для эффективной стимуляции образования и/или сохранения кости. Кроме того, инъецируемые композиции в форме стержней демонстрируют замедленный характер высвобождения остеогенного белка, доставляемого таким способом. Твердые стержни согласно настоящему изобретению предпочтительно являются цилидрическими и имеют диаметр, варьирующийся от приблизительно 0.1 мм до приблизительно 3.0 мм, более предпочтительно, составляющий приблизительно 1.0 мм, что делает возможной доставку при помощи иглы размера 16G. Кроме того, твердые стержни предпочтительно имеют длину, варьирующуюся от приблизительно 1.0 мм до приблизительно 5.0 см.
[0021] В отличие от существующих инъецируемых составов остеогенные композиции согласно этому первому варианту реализации настоящего изобретения вводят в твердой форме, что позволяет избежать трудностей, связанных с жидкими или вязкими составами. Например, при использовании жидких или гелеобразных составов жидкости организма могут преждевременно разбавить остеогенное вещество до достижения эффекта стимулирования костей. Настоящее изобретение позволяет избежать эффекта разбавления благодаря применению твердого носителя, который медленно разрушается in vivo, обеспечивая, таким образом, отложенное, замедленное высвобождение активного вещества (веществ).
Кроме того, в отличие от жидких или вязких составов, которые могут мигрировать из места введения, твердые композиции согласно настоящему изобретению удерживаются и остаются в участке желательного роста кости, где они вызывают стимуляцию роста кости. Такие композиции также позволяют более точно размещать твердый стержень путем инъекции в зоны потери костной массы. Обычно композиция должна оставаться в этом участке от приблизительно 5 дней до приблизительно 2 месяцев. В случае преждевременного разрушения композиции либо не будет иметь место желаемый эффект стимуляции роста кости, либо образовавшаяся кость не будет обладать желаемой прочностью. Наконец, хотя остеогенную композицию согласно этому способу реализации настоящего изобретения вводят в твердой форме, ее предпочтительно формуют в виде цилиндрического стержня, что делает ее подходящей как для введения путем инъекции, так и для имплантирования в организм. Безусловно, при желании можно использовать другие формы стержней, например шестигранные, квадратные или полукруглые. Кроме того, применение твердых стержней в значительной степени подавляет хорошо известное хирургическое осложнение, связанное с возникновением эмболии в ходе процедуры внутрикостной инъекции (по сравнению с жидкими или гелеобразными формами). Поскольку объем вводимого путем инъекции высококонцентрированного твердого стержня намного меньше того, который требуется для распределения той же дозы в жидкой или гелеобразной форме, уменьшается риск возможного смещения внутрикостных фрагментов кости, жира или эмболии, вызываемых инъекцией большого объема жидкого/гелеобразого носителя под давлением. Данную композицию можно применять в участке желательного роста кости любым удобным способом, включая введение при помощи обычной иглы для подкожных инъекций или шприца.
[0022] Второй способ реализации настоящего изобретения относится к способу приготовления композиции в форме твердого стержня для доставки остеогенных белков путем инъекции. На первом этапе сухую форму остеогенного белка смешивают с сухой формой кальций-фосфатного материала, получая в результате сухую смесь. Другими словами, сначала для образования сухой смеси применяют порошкообразные или сухие формы как остеогенного белка, так и фосфата кальция. В случае, когда в композицию включены добавки и/или дополнительные активные вещества, эти материалы также можно применять в сухой или порошкообразной форме и включать в сухую смесь.
[0023] На втором этапе сухую смесь восстанавливают путем добавления водного буфера, получая в результате пасту. Подходящие водные буферы включают, без ограничения, фосфатный буферный раствор, физиологический раствор, буферы на основе глицина и их комбинации.
В случае, когда в качестве остеогенного белка применяют ВМР-2, предпочтительно применяют буфер на основе глицина с рН, приблизительно равным 4.5; более предпочтительно - буфер на основе глицина, имеющий следующий состав: 5 ммоль L-глутаминовой кислоты, 2.5% глицина, 0.5% сахарозы, 5 ммоль NaCl и 0. 01% полисорбата polysorbate 80.
[0024] Отношение объем : масса (мл:г) водного буфера к сухой смеси варьирует от приблизительно 0.5:1 до приблизительно 2:1. Однако нижний предел этого массового отношения ограничивает лишь один принцип: количество добавляемой к сухой смеси жидкости должно быть достаточным для образования пасты, которую можно формовать путем выдавливания из шприца или другим способом. Кроме того, верхний предел этого массового отношения также ограничивает лишь один принцип: количество добавляемой к сухой смеси жидкости должно быть настолько большим, чтобы после последующего высушивания полученная форма, т.е. форма стержня, нарушалась; другими словами, если использовать слишком много жидкости, образованная на третьем этапе форма стержня после сушки остеогенного соединения будет нарушена.
[0025] Этот этап проводят в условиях, при которых происходит практически равномерное смешивание. В процессе смешивания компоненты объединяются, и его можно использовать для контроля реакций между компонентами. Хотя предпочтительно, чтобы сухая смесь содержала все желаемые компоненты, также возможно добавлять добавку или дополнительное активное вещество непосредственно перед началом смешивания или перед завершением смешивания. Такие добавка или активное вещество предпочтительно имеют сухую форму, однако также возможно добавлять к пасте добавку или дополнительное активное вещество в гидратированной форме.
[0026] На третьем этапе способа согласно настоящему изобретению пасту формуют, в результате чего образуется композиция в форме стержня. Формовку или придание формы можно выполнять, применяя одну из ряда известных методик, таких как формовка, экструзия, прессование, сверление и/или резка. В предпочтительном способе реализации этого изобретения пастой заполняют шприц для подкожный инъекций и экструдируют ее через носик для иглы. В этом случае вставляют шток шприца и прикладывают достаточное давление, чтобы экструдировать непрерывный длинный отрезок пасты на какую-либо сухую поверхность. Затем при помощи какого-либо режущего инструмента, такого как бритва, скальпель, нож и т.п., наносят разрезы, в результате чего образуются инъецируемые композиции в форме стержней. Резку можно также проводить после описанного ниже этапа сушки. В качестве альтернативы, пасту можно поместить в цилиндрическую форму, катетер, воздухо- или газопроницаемую трубку (например, из силикона или Теflоn®/FЕР (фторированный этилен-пропилен)) или любое другое приспособление экструзионного типа.
[0027] На последнем этапе полученную на предыдущем этапе композицию в форме стержня сушат или отверждают, в результате чего образуется композиция в форме стержней для доставки остеогенных белков путем инъекции согласно настоящему изобретению (первый способ реализации). Сушку можно проводить путем высушивания на воздухе или инкубации при повышенных температурах, т.е. по меньшей мере 37°С. Температура сушки ограничивается лишь заботой о том, чтобы не произошло разрушения остеогенного белка, которое обычно происходит где-то в диапазоне от 55°С до 60°С.
При проведении сушки в сушилке на 37°С сушка занимает приблизительно по меньшей мере один час, а предпочтительно сушку проводят в течение ночи. Остаточная влажность композиции в форме стержня составляет предпочтительно менее 10%.
[0028] Третий способ реализации настоящего изобретения относится к композиции в форме отверждающейся пасты для доставки остеогенных белков путем инъекции, содержащей остеогенный белок и кальций-фосфатный материал. Композиция согласно этому третьему способу реализации настоящего изобретения может факультативно включать другие добавки (связующие вещества, наполнители) и/или активные вещества, такие как ингибитор резорбции костей.
[0029] Эта паста подходит для местной внутрикостной доставки, и, следовательно, ее можно вводить путем инъекции непосредственно в участок, пораженный остеопорозом или остеопенией, после чего эта паста затвердевает до образования твердой формы и эффективно стимулирует образование и/или сохранение кости. Поскольку после введения паста затвердевает в условиях по меньшей мере 37°С, т.е. в организме млекопитающего, устраняются многие недостатки, связанные с применением жидких и гелеобразных композиций. Аналогично описанным выше инъецируемым композициям в форме твердых стержней композиция в форме затвердевшей пасты демонстрирует замедленный характер высвобождения остеогенного белка. Время жизни инъецируемой отверждающейся пасты (т.е. время, в течение которого пасту возможно вводить путем инъекции) можно продлить путем охлаждения пасты.
[0030] Четвертый вариант реализации настоящего изобретения относится к способу приготовления композиции в форме пасты для доставки остеогенных белков путем инъекции. В этом способе сухую форму кальций-фосфатного вещества смешивают с водным буфером, содержащим остеогенный белок, в результате чего образуется паста. В случае, когда в композицию включены добавки и/или дополнительные активные вещества, эти материалы также можно либо применять в сухой форме и смешивать их предварительно с сухой формой кальций-фосфатного материала, либо смешивать непосредственно с водным буфером и кальций-фосфатным материалом. Смешивание проводят в условиях, при которых происходит практически равномерное смешивание. В процессе смешивания компоненты объединяются, и его можно использовать для контроля реакций между компонентами.
[0031] Подходящие водные буферы включают, без ограничения, фосфатный буферный раствор, физиологический раствор, буферы на основе глицина и их комбинации. В случае, когда в качестве остеогенного белка применяют ВМР-2, применяют предпочтительно буфер на основе глицина с рН, приблизительно равным 4.5; более предпочтительно - буфер на основе глицина, имеющий следующий состав: 5 ммоль L-глутаминовой кислоты, 2.5% глицина, 0.5% сахарозы, 5 ммоль NaCl и 0.01% полисорбата polysorbate 80. Массовое отношение водного буфера к сухому фосфату кальция варьируется от приблизительно 0.5:1 до приблизительно 2:1.
[0032] В качестве альтернативы сухую форму остеогенного белка смешивают с сухой формой кальций-фосфатного материала, получая в результате сухую смесь. Затем эту сухую смесь восстанавливают путем добавления водного буфера, получая пасту. Эти этапы идентичны первому и второму этапам способа приготовления композиции в форме твердого стержня (второй способ реализации) за исключением того, что массовое отношение водного буфера к сухому фосфату кальция варьируется от приблизительно 0.5:1 до приблизительно 2:1.
[0033] Ниже приведено более подробное описание активного вещества, носителя, добавок и ингибиторов резорбции кости, подходящих для применения в настоящем изобретении.
АКТИВНОЕ ВЕЩЕСТВО
[0034] Активное вещество, присутствующее в остеогенных композициях согласно настоящему изобретению, предпочтительно выбирают из семейства белков, известного как надсемейство белков «трансформирующих факторов роста бета» (TGF-β). Это семейство включает активины, ингибины и «костные морфогенетические белки» (BMPs). Эти белки BMP включают ВМР-белки ВМР-2, BMP-3, BMP-4, BMP-5, BMP-6 и ВМР-7, раскрытые, например, в Патентах США №5108922, 5013649, 5116738, 5106748, 5187076 и 5141905, BMP-8, раскрытый в РСТ WO 91/18098, BMP-9, раскрытый в РСТ WO 93/00432, BMP-10, раскрытый в РСТ WO 94/26893, BMP-11, раскрытый в РСТ WO 94/26892, BMP-12 и BMP-13, раскрытый в РСТ WO 95/16035, BMP-15, раскрытый в Патенте США № 5635372, и BMP-16, раскрытые в Патенте США №6331612. Другие белки ТФР-бета (TGF-β), которые можно применять в настоящем изобретении в качестве активных веществ, включают Vgr 2 (Jones et al., Mol. Endocrinol., vol. 6, pp.1961 1968 (1992)), а также любые другие факторы роста и дифференцировки (growth and differentiation factor, GDF), включая описанные в РСТ WO 94/15965, WO 94/15949, WO 95/01801, WO 95/01802, WO 94/21681, WO 94/15966, WO 95/10539, WO 96/01845, WO 96/02559 и др. В настоящем изобретении также можно использовать BIP, раскрытый в WO 94/01557, НР00269, раскрытый в JP 7 250688, и МР52, раскрытый в РСТ WO 93/16099. Описания всех указанных выше патентов, публикаций в журналах и опубликованных международных заявок включены в настоящую заявку по ссылке.
[0035] Предпочтительно активное вещество включает по меньшей мере один белок, выбранный из подкласса белков, широко известных как BMP, у которых была обнаружена остеогенная активность и другие типы ростовой и дифференцировочной активности. Субпопуляция белков BMP, предпочтительных в настоящий момент для применения в настоящем изобретении, включает BMP-2, BMP-4, BMP-5, BMP-6, BMP-7, BMP-10, BMP-12 и BMP-13, наиболее предпочтителен ВМР-2, последовательность которого раскрыта в Патенте США №5013649, описание которого включено в настоящую заявку по ссылке
[0036] Активное вещество может представлять собой вещество, полученное рекомбинантными способами или выделенное из белковой композиции (очищенное). Активное вещество, например TGF-β, такой как BMP, или другой димерный белок, может представлять собой гомодимер или гетеродимер с другими BMP (например, гетеродимер, образованный одним мономером BMP-2 и одним мономером ВМР-6) или с другими членами надсемейства TGF-β, такими как антивины, ингибины и TGF-β1 (например, гетеродимер, образованный одним мономером BMP и одним мономером родственного члена надсемейства T4F-β). Примеры таких гетеродимерных белков описаны, например, в РСТ WO 93/09229, описание которой включено в настоящую заявку по ссылке. Активное вещество может содержать ДНК, кодирующую белки BMP, и клетки, трансдуцированные или трансфецированные генами, кодирующими ВМР-белки.
[0037] Активное вещество может, кроме того, содержать дополнительные вещества, такие как белки Hedgehog, Frazzled, Chordin, Noggin, Cerberus и Follistatin. Эти семейства белков описаны в общих чертах в Sasai et al., Cell, vol. 79, pp.779-790 (1994) (Chordin); РСТ WO 94/05800 (Noggin); и Fukui et al., Dev. Biol., vol. 159, pp.131-139 (1993) (Follistatin). Белки Hedgehog описаны в РСТ WO 96/16668, WO 96/17924 и WO 95/18856. Семейство белков Frazzled представляет собой сравнительно недавно открытое семейство белков, обладающих высокой гомологией с внеклеточным доменом рецепторных белков семейства, известного как frizzled. Семейство генов и белков Frizzled описано в Wang et al., J. Biol. Chem., vol. 271, pp.4468-4476 (1996). Активное вещество может также включать другие растворимые рецепторы, такие как укороченные растворимые рецепторы, раскрытые в PCT WO 95/07982.
Из описания WO 95/07982 специалисту в данной области будет понятно, что можно приготовить укороченные растворимые рецепторы для множества других рецепторных белков. Приготовленные таким образом укороченные рецепторы также включены в настоящее изобретение. Указанные выше публикации включены в настоящую заявку по ссылке.
[0038] Количество активного вещества, применяемое здесь, представляет собой количество, достаточное (эффективное) для стимуляции повышенной остеогенной активности существующего или инфильтрирующего предшественника (клетка-предшественник остеобластов) или других клеток (здесь и далее «эффективное количество»). Оно будет зависеть от размера и природы дефекта, который подвергают лечению, а также от состава применяемого кальций-фосфатного носителя. Обычно количество остеогенного белка, присутствующее в остеогенной композиции в форме твердого стержня согласно настоящему изобретению, варьирует от приблизительно 1% до приблизительно 90%, более предпочтительно - от приблизительно 15% до приблизительно 40% от массы остеогенной композиции. Обычно количество остеогенного белка, присутствующее в остеогенной композиции в форме отверждающейся пасты согласно настоящему изобретению, варьирует от приблизительно 0.01% до приблизительно 2%, более предпочтительно - от приблизительно 0.03% до приблизительно 1% от массы остеогенной композиции.
НОСИТЕЛЬ
[0039] Согласно всем примерам реализации настоящего изобретения в качестве носителя применяют кальций-фосфатный материал. «Кальций-фосфатный материал» означает здесь любой синтетический материал, замещающий кость, содержащий в качестве основного компонента фосфат кальция, т.е. материал, не менее 90% массы которого может быть отнесено на счет кальция и/или фосфата. Кальций-фосфатный материал согласно настоящему изобретению может представлять собой любой биосовместимый кальций-фосфатный материал, известный в данной области.
Подходящие фосфатно-кальциевые материалы могут быть получены любым из разнообразных способов, при использовании любых подходящих исходных компонентов, либо приобретены.
[0040] В некоторых предпочтительных примерах реализации настоящего изобретения кальций-фосфатный материал присутствует в количествах, варьирующих от приблизительно 10% до приблизительно 99%, более предпочтительно - от приблизительно 40% до приблизительно 60% от массы остеогенной композиции в форме твердого стержня согласно настоящему изобретению. В некоторых других предпочтительных способах реализации настоящего изобретения кальций-фосфатный материал присутствует в количестве, варьирующем от приблизительно 30% до приблизительно 70%, более предпочтительно - от приблизительно 45% до приблизительно 55% от массы остеогенной композиции в форме отверждающейся пасты согласно настоящему изобретению. Предпочтительно, кальций-фосфатный материал применяют в сухой, т.е. порошкообразной форме.
[0041] Формы фосфата кальция, подходящие для применения в этом изобретении, включают без ограничения аморфный фосфат кальция типа апатита (АСР, АФК), слабокристаллизованный фосфат кальция типа апатита (СКА, РСА), гидроксиапатит (ГА), трикальция фосфат и фторапатит. В предпочтительном примере реализации кальций-фосфатный материал представляет собой твердый слабокристаллизованный фосфат кальция типа апатита, имеющий отношение кальций-к-фосфату (Ca/Р), сравнимое с отношением встречающихся в природе минеральных компонентов костей, более предпочтительно - имеющий отношение кальций-к-фосфату ниже, чем приблизительно 1:1.5, наиболее предпочтительно - приблизительно 1:1.4.
[0042] Подходящие РСА-материалы можно идентифицировать путем смешивания предшественников РСА, гидрирования ограниченным количеством воды (с образованием замазки или пасты), формования в стержни цилиндрической формы, после чего сформованный материал оставляют для затвердевания до состояния РСА-материала. Желательные предшественники способны к затвердеванию во влажной среде при температуре, равной или приблизительно равной температуре тела, в течение менее чем 5 часов, а предпочтительно - в пределах 10-30 минут.
[0043] Согласно настоящему изобретению кальций-фосфатный носитель может содержать любой замещающий кость материал, который содержит одну из указанных выше форм фосфата кальция в качестве основного компонента, т.е. по меньшей мере 90% массы которого может быть отнесено на счет кальция и/или фосфата. Замещающий кость материал может содержать только одну из указанных выше форм фосфата кальция, с дополнительными компонентами или без них, или же замещающий кость материал может содержать комбинацию описанных выше форм фосфата кальция с дополнительными компонентами или без них. Кроме того, для приготовления кальций-фосфатного материала, подходящего для применения в настоящем изобретении, можно использовать одну или более из указанных выше форм фосфата кальция.
Способы изготовления таких материалов хорошо известны в данной области. Однако подойдет любой способ, результатом которого является получение сухого кальций-фосфатного материала, т.е. порошкообразного.
[0044] «Аморфный» означает здесь материал, в значительной степени обладающий свойством аморфности. «Значительная степень аморфности» подразумевает содержание аморфного вещества более 75%, предпочтительно - более 90% и характеризуется широкой, лишенной характерных особенностей дифрактограммой.
[0045] Термины "Слабокристаллизованный фосфат кальция типа апатита", "РСА-фосфат кальция" и "РСА-материал" используются здесь для описания синтетического слабокристаллизованного фосфата кальция типа апатита. Слабокристаллизованный материал типа апатита не ограничивается единственной фазой фосфата кальция, при условии, что он обладает характеристическими спектрами рентгеновской дифракции (XRD) и инфракрасными спектрами Фурье (FITR). Фосфат кальция РСА обладает практически таким же спектром рентгеновской дифракции, что и кость. Спектр рентгеновской дифракции обычно характеризуется лишь двумя широкими пиками в области 20-35Е, причем центр одно приходится на 26Е, а другого - на 32Е. ИК спектр Фурье характеризуется пиками на 563 см-1, 1034 см-1, 1638 см-1 и 3432 с см-1 (±2 см-1); крутые склоны наблюдаются при 603 см-1 и 875 см-1, причем дублет имеет максимумы при 1422 см-1 и 1457 см-1. Материалы РСА, предпочтительные для применения в настоящем изобретении, описаны в Патентах США №№5650176, 5683461 и 6214368, описание каждого из которых включено в данную заявку по ссылке. Подходящие материалы описаны также в серии родственных заявок, озаглавленных "Delivery Vehicle" (Носитель для доставки) "Conversion of Amorphous Calcium Phosphate to Form a Novel Bioceramic" (Переработка аморфного фосфата кальция с целью образования нового биокерамического материала), "Orthopedic and Dental Ceramic Implants" (ортопедические и стоматологические керамические имплантаты) и "Bioactive Ceramic Composites" (биоактивные керамические композиты), при этом все указанные патенты поданы 16 октября 1997 на имя корпорации ЕТЕХ Corporation (Кембридж, Массачусетс) и включены в настоящую заявку по ссылке. Учитывая полноту описания этих вышеупомянутых патентных документов, мы не будем подробно описывать детали приготовления подходящих материалов РСА. Обзора свойств РСА будет достаточно. Материал РСА отличается способностью к биорезорбции (рассасыванию) и минимальной кристалличностью. Кристалличность РСА практически совпадает с кристалличностью костей. Также материал РСА биосовместим и не причиняет вреда организму, в который его вводят.
[0046] Кристаллический гидроксиапатит (ГА, НА) описан, например, в патентах США №№33221 и 33161, каждый из которых включен в настоящую заявку по ссылке. В этих патентах описано, как готовить реминерализующие кальций-фосфатные композиции и тонкокристаллический, некерамический, постепенно рассасывающийся материал-носитель из гидроксиапатита на основе тех же кальций-фосфатных композиций.
Аналогичная кальций-фосфатная система, которая состоит из тетракальций фосфата (ТТСР) и монокальций фосфата (МСР) или его моногидратной формы (МСРМ), описана в патентах США №5053212 и 5129905, каждый из которых включен в описание настоящей заявки по ссылке. Дополнительные кристаллические НА-материалы, широко известные как даллиты, описаны в патенте США №5962028, описание которого включено в настоящую заявку по ссылке.
ДОБАВКИ
[0047] В остеогенных композициях согласно настоящему изобретению можно применять добавки. Многие подобные связующие вещества, которые повышают когезионную способность (способность к сцеплению), и наполнители, которые стабилизируют и/или регулируют высвобождение активных компонентов, хорошо известны специалистам в области составления рецептур. Подходящие добавки включают, без ограничения, фармацевтически приемлемые соли, полисахариды, пептиды, белки, аминокислоты, синтетические полимеры, природные полимеры и/или поверхностно-активные вещества. Подходящие полимеры включают, например, полимеры, описанные в Патенте США №5171579, описание которого полностью включено в настоящую заявку по ссылке. Предпочитаемые добавки включают материалы типа целлюлозы, такие как карбоксиметилцеллюлоза (КМЦ, CMC), гидроксипропилметилцеллюлоза (ГПМЦ, НРМС) и метилцеллюлоза (МЦ, МС), синтетические полимеры, такие как полимеры молочной кислоты (полилактиды) и по