Производные пирролопиримидина, применяемые для лечения пролиферативных заболеваний
Иллюстрации
Показать всеИзобретение относится к новым соединениям формулы I
,
в которой R1 обозначает фенил; G обозначает С1-С7-алкилен; Q обозначает -NH-; и Х обозначает С1-С7-алкилен, или к его солям. Изобретение также относится к фармацевтической композиции, к применению соединения формулы I по любому из п.п.1-5, а также к способу получения соединения формулы I. Технический результат - получение новых биологически активных соединений, обладающих способностью ингибировать протеинтирозинкиназу. 4 н. и 4 з.п. ф-лы.
Реферат
Настоящее изобретение относится к производным 7H-пирроло[2,3-d]пиримидина и к способу их получения, к фармацевтическим композициям, содержащим такие производные, и к применению таких производных - по отдельности или в комбинации с одним или большим количеством других фармацевтически активных соединений - для приготовления фармацевтических композиций, предназначенных для лечения предпочтительно - пролиферативного заболевания, такого как опухоль.
Настоящее изобретение относится к производным 7H-пирроло[2,3-d]пиримидина формулы I
,
в которой
R1 обозначает гетероциклический радикал, или незамещенный, или замещенный ароматический радикал;
G обозначает С1-С7-алкилен, -С(=O)- или С1-С6-алкилен-С(=O)-, в котором карбонильная группа присоединена к пиперазиновому фрагменту;
Q обозначает -NH- или -О-, при условии, что Q обозначает -О-, если G обозначает -С(=O)- или С1-С6-алкилен-С(=O)-; и
Х или отсутствует, или обозначает С1-С7-алкилен, при условии, что гетероциклический радикал R1 присоединен через циклический атом углерода, если Х отсутствует;
или к соли указанных соединений.
Общие термины, используемые выше и ниже в настоящем изобретении, в контексте настоящего раскрытия предпочтительно обладают указанными ниже значениями, если не указано иное:
Если для соединений, солей и т.п. используется форма множественного числа, это означает также и одно соединение, соль и т.п.
Если указаны соединения формулы I, которые могут образовать таутомеры, это означает включение и таутомеров таких соединений формулы I. В частности, таутомерия проявляется, например, у соединений формулы I, которые содержат 2-гидроксипиридильный радикал. В таких соединениях 2-гидроксипиридильный радикал также может содержаться в виде пирид-2(1H)-онила.
Асимметрические атомы углерода, которые необязательно содержатся в соединении формулы I, могут находиться в (R), (S) или (R, S) конфигурации, предпочтительно - в (R) или (S) конфигурации. Заместитель двойной связи или кольца могут находиться в цис- (=Z-) или транс (=Е-) форме. Таким образом, соединения могут содержатся в виде смеси изомеров или, предпочтительно, - в виде чистых изомеров.
Приставка "низш." обозначает радикал, содержащий от 1 атома углерода и максимально до 7 атомов углерода включительно, предпочтительно - максимально до 4 атомов углерода включительно, указанные радикалы являются линейными или разветвленными и содержат одно или несколько разветвлений.
Низш. алкил, например, означает метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, н-гексил или н-гептил.
Низш. алкоксигруппа означает, например, этокси- или метокси-, предпочтительно - метоксигруппу.
Замещенный низш. алкил предпочтительно представляет собой низш. алкил, определенный выше, который может содержать один или большее количество, предпочтительно - один заместитель, такой как, например, аминогруппа, N-низш. алкиламиногруппа, N,N-ди-низш. алкиламиногруппа, N-низш. алканоиламиногруппа, N,N-ди-низш. алканоиламиногруппа, гидроксигруппа, низш. алкоксигруппа, низш. алканоил, низш. алканоилоксигруппа, цианогруппа, нитрогруппа, карбоксигруппа, низш. алкоксикарбонил, карбамоил, N-низш. алкилкарбамоил, N,N-ди-низш. алкилкарбамоил, амидиновая, гуанидиновая, уреидная группа, меркаптогруппа, низш. алкилтиогруппа, галоген или гетероциклический радикал.
Гетероциклический радикал предпочтительно содержит вплоть до 20 атомов углерода и предпочтительно представляет собой насыщенный или ненасыщенный моноциклический радикал, содержащий от 4 до 8 атомов цикла и от 1 до 3 гетероатомов, которые предпочтительно выбраны из группы, включающей азот, кислород и серу, или би- или трициклический радикал, в котором, например, 1 или 2 карбоциклических радикала, таких как, например, бензольные радикалы, аннелированы (сконденсированы) с указанным моноциклическим радикалом. Если гетероциклический радикал содержит конденсированный карбоциклический радикал, то гетероциклический радикал также может быть присоединен к остальной части молекулы формулы I через кольцевой атом конденсированного карбоциклического радикала. Гетероциклический радикал (включая конденсированный карбоциклический радикал(ы), если он содержится) необязательно содержит один или большее количество, предпочтительно - один радикал, такой как, например, незамещенный или замещенный низш. алкил, аминогруппа, N-низш. алкиламиногруппа, N,N-ди-низш. алкиламиногруппа, N-низш. алканоиламиногруппа, N,N-ди-низш. алканоиламиногруппа, гидроксигруппа, низш. алкоксигруппа, низш. алканоил, низш. алканоилоксигруппа, цианогруппа, нитрогруппа, карбоксигруппа, низш. алкоксикарбонил, карбамоил, N-низш. алкилкарбамоил, N,N-ди-низш. алкилкарбамоил, амидиновая, гуанидиновая, уреидная группа, меркаптогруппа, низш. алкилтиогруппа или галоген.
Наиболее предпочтительным гетероциклическим радикалом является пирролидинил, пиперидил, низш. алкилпиперазинил, ди-низш. алкилпиперазинил, морфолинил, тетрагидропиранил, пиридил, пиридил, замещенный гидроксигруппой или низш. алкоксигруппой, и бензодиоксолил, предпочтительно - пирролидинил, пиперидил, низш. алкилпиперазинил, ди-низш. алкилпиперазинил или морфолинил.
Гетероциклический радикал R1 является таким, как определено выше для гетероциклического радикала, при условии, что он связан с Q через кольцевой атома углерода, если Х отсутствует. Предпочтительным гетероциклическим радикалом R1 является бензодиоксолил, пиридил, замещенный гидроксигруппой или низш. алкоксигруппой, или, особенно предпочтительно - индолил, замещенный галогеном и низш. алкилом. Если R1 обозначает пиридил, замещенный гидроксигруппой, то гидроксигруппа предпочтительно присоединена к кольцевому атому углерода, соседнему с кольцевым атомом азота.
Незамещенный или замещенный ароматический радикал R1 содержит вплоть до 20 атомов углерода и является незамещенным или замещенным, например, в каждом случае незамещенным или замещенным фенилом.
Предпочтительно незамещенный ароматический радикал R1 обозначает фенил. Замещенный ароматический радикал R1 предпочтительно обозначает фенил, содержит один или большее количество заместителей, независимо друг от друга выбранных из группы, включающей незамещенный или замещенный низш. алкил, алкиламиногруппу, N,N-ди-низш. алкиламиногруппу, N-низш. алканоиламиногруппу, N,N-ди-низш. алканоиламиногруппу, гидроксигруппу, низш. алкоксигруппу, низш. алканоил, низш. алканоилоксигруппу, цианогруппу, нитрогруппу, карбоксигруппу, низш. алкоксикарбонил, карбамоил, N-низш. алкилкарбамоил, N,N-ди-низш. алкилкарбамоил, амидиновую, гуанидиновую, уреидную группу, меркаптогруппу, низш. алкилтиогруппу и галоген. Наиболее предпочтительный замещенный или замещенный ароматический радикал R1 обозначает фенил, замещенный одним или большим количеством радикалов, независимо друг от друга выбранных из группы, включающей низш. алкил, аминогруппу, гидроксигруппу, низш. алкоксигруппу, галоген и бензилоксигруппу.
Галоген предпочтительно означает фтор, хлор, бром или йод, наиболее предпочтительно - фтор, хлор или бром.
С1-С7-Алкилен может быть разветвленными или неразветвленным и предпочтительно обозначает C1-С3-алкилен.
С1-С7-Алкилен G предпочтительно обозначает С1-С3-алкилен, наиболее предпочтительно - метилен (-СН2-).
Если G не обозначает С1-С7-алкилен, то он предпочтительно обозначает -С(=O)-.
С1-С7-Алкилен Х предпочтительно обозначает С1-С3-алкилен, наиболее предпочтительно - метилен (-СН2-) или этан-1,1-диил (-СН(СН3)-).
Q предпочтительно обозначает -NH-.
Соли предпочтительно являются фармацевтически приемлемыми солями соединений формулы I.
Такие соли образуются, например, в виде молекулярных солей с кислотами, предпочтительно - с органическими или неорганическими кислотами, из соединений формулы I, содержащих основной атом азота, предпочтительно фармацевтически приемлемые соли.
В присутствии отрицательно заряженных радикалов, таких как карбоксигруппа или сульфогруппа, соли также могут образоваться с основаниями, например, соли металла или аммония, такие как соли щелочного металла или щелочноземельного металла, или соли аммония с аммиаком или подходящими органическими аминами, такими как третичные моноамины.
Если в одной молекуле содержатся и основная группа, и кислотная группа, то соединения формулы I также может образовывать внутренние соли.
Для выделения или очистки также можно использовать фармацевтически неприемлемые соли, например, пикраты или перхлораты. Однако для терапевтических целей можно использовать только фармацевтически приемлемые соли свободных соединение (если это необходимо для фармацевтических композиций), и поэтому такие соли являются предпочтительными.
Вследствие близкого родства соединений в свободной форме и в виде их солей, включая соли, которые можно использовать в качестве промежуточных продуктов, например при очистке или идентификации соединений, предлагаемых в настоящем изобретении, то выше и ниже любое указание на свободные соединения следует понимать, как относящееся и к соответствующим солям, если это является подходящим и целесообразным.
Соединения формулы I обладают ценными, фармакологически полезными характеристиками. В частности, они обладают специфической ингибирующей активностью, представляющей интерес для фармакологии. Они особенно эффективны в качестве ингибиторов протеинтирозинкиназы и/или (кроме того) в качестве ингибиторов серин/треонинпротеинтирозинкиназ; они способны, например, эффективно ингибировать активность тирозинкиназы рецептора эпидермального фактора роста (EGF-R) и ErbB-2 киназы. Эти 2 рецептора протеинтирозинкиназы вместе с представителями их группы ЕrbВ-3 и ЕrbВ-4 играют ключевую роль в передаче сигналов в большом количестве клеток млекопитающих, включая клетки человека, в особенности эпителиальные клетки, клетки иммунной системы и клетки центральной и периферической нервной системы. Например, в различных типах клеток индуцированная EGF активация связанной с рецептором протеинтирозинкиназы является необходимым условием деления клетки и, следовательно, пролиферации группы клеток. Наиболее важно то, что сверхэкспрессия EGF-R (HER-1) и/или ЕrbВ-2 (HER-2) наблюдалась в значительной части многих опухолей человека. Например, обнаружено, что EGF-R сверхэкспрессируется при немелкоклеточном раке легких, плоскоклеточной карциноме (головы и шеи), раке молочной железы, желудка, ободочной кишки и предстательной железы, а также глиомах. Обнаружено, что ЕrbВ-2 сверхэкспрессируется при немелкоклеточном раке легких, плоскоклеточной карциноме (головы и шеи), раке молочной железы, желудка и яичника, а также глиомах.
В дополнение к ингибированию активности тирозинкиназы EGF-R, соединения формулы I в различной степени ингибируют другие протеинтирозинкиназы, которые участвуют в передаче сигналов, опосредуемой трофическими факторами, в особенности рецепторов группы эндотелиального фактора роста сосудов (VEGF), (например, KDR, Flt-1, Flt-3), а также abl киназы, в особенности v-abi, киназ группы Src, в особенности c-Src, Lck и Fyn, других представителей группы рецепторов EGF, таких как ЕrbВ-3 (HER-3) и ЕrbВ-4 (HER-4), CSF-1, Kit, рецептора FGF и циклинзависимых киназ CDK1 и CDK2, каждая из которых играет роль в регуляции роста и превращениях в клетках млекопитающих, включая клетки человека.
Ингибирование активности тирозинкиназы EGF-R можно продемонстрировать с помощью известных методик, например, с помощью рекомбинантного внутриклеточного домена рецептора EGF [EGF-R ICD; см., например, публикацию Е.McGlynn и др., Europ. J.Biochem. 207. 265-275 (1992)]. По сравнению с контролем без ингибитора соединения формулы I ингибируют активность фермента на 50% (IС50), например, при концентрации, составляющей от 0,0005 до 0,5 мкМ, предпочтительно - от 0,001 до 0,1 мкМ.
Одновременно или вместо ингибирования активности тирозинкиназы EGF-R соединения формулы I также ингибируют других представителей этой группы рецепторов, таких как ЕrbВ-2. Ингибирующая активность (IС50) находится в примерном диапазоне, составляющем от 0,001 до 0,5 мкМ. Ингибирование тирозинкиназы ErbB-2 (HER-2) можно определить, например, по методикам, аналогичным использующимся для протеинкиназы EGF-R [см. публикацию С.House и др., Europ. J. Biochem. 140, 363-367 (1984)]. Киназу ErbB-2 можно выделить и определить ее активность по методикам, которые сами по себе известны, например, в соответствии с публикацией Т.Akiyama и др., Science 232, 1644 (1986).
Согласно изобретению неожиданно обнаружено, что соединения формулы I в особенности весьма активно ингибируют активность тирозинкиназы рецепторов группы VEGF. Поэтому соединения, предлагаемые в настоящем изобретении, являются весьма эффективными двойными ингибиторами рецепторов групп EGF и VEGF. Ингибирование KDR и Flt-1 и ингибирование индуцированной фактором роста пролиферации HUVECS описано в публикации J.Wood и др., Cancer Res. 60, 2178-2189 (2000). Соединения формулы I ингибируют, например, активность тирозинкиназы KDR со значениями IС50, составляющими от примерно 1 нМ до примерно 1 мкМ, предпочтительно - от примерно 5 нМ до примерно 0,5 мкМ.
Воздействие соединений формулы I на индуцируемое EGF фосфорилирование EGF-R можно определить в линии клеток эпителиальной карциномы человека А431 с помощью ELISA (твердофазный иммуноферментный анализ), что описано в публикации U.Trinks и др., J. Med. Chem. 37:7. 1015-1027 (1994). В этом последнем анализе (EGF-R ELISA) соединения формулы I обладают значениями IC50, составляющими примерно от 0,001 до 1 мкМ.
Соединения формулы I активно ингибируют рост сверхэкспрессирующих EGF-R клеток NCI-H596 немелкоклеточного рака легких [см., например, публикацию W.Lei, и др., Anticancer Res. 19 (1А), 221-228 (1999)] со значениями IС50, составляющими примерно от 0,01 до 1 мкМ. В таком же диапазоне активности соединения формулы I также активно ингибируют рост сверхэкспрессирующих ЕrbВ-2 клеток ВТ474 рака молочной железы человека. Использовали модифицированные методики исследования публикации Т.Meyer и др., Int. J. Cancer 43, 851 (1989). Ингибирующую активность соединений формулы I, вкратце, определяют следующим образом: клетки NCI-H596 (планшет с лунками объемом 10000 мкл) помещают в 96-луночные планшеты для микротитрования. Исследуемые соединения [растворенные в диметилсульфоксиде (ДМСО)] прибавляют в серии концентраций (серийное разведение) таким образом, чтобы конечная концентрация ДМСО не превышала 1% (об./об.). После прибавления планшеты инкубируют в течение 3 дней и за это время контрольные культуры, не содержащие исследуемых соединений, способны претерпеть по меньшей мере 3 цикла деления клеток. Рост клеток NCI-H596 определяют с помощью окрашивания метиленовым голубым: после инкубации клетки фиксируют глутаровым альдегидом, промывают водой и окрашивают 0,05% метиленовым голубым. После стадии промывки краситель элюируют с помощью 3% НСl и оптическую плотность (ОП) в пересчете на лунку планшета для микротитрования измеряют прибором Titertek Multiskan (Titertek, Huntsville, AL, USA) при 665 нм. Значения IC50 определяют с помощью компьютерной программы по формуле:
В этих экспериментах значения IC50 приводятся в виде такой концентрации рассматриваемого исследуемого соединения, которая приводит к количеству клеток, которое на 50% меньше полученного для контроля без прибавления ингибитора. Соединения формулы I обладают ингибирующей активностью со значениями IC50, находящимися в диапазоне от примерно 0,01 до 1 мкМ.
Соединения формулы I также способны подавлять рост опухолевых клеток и in vivo, как это показывает, например, описанное ниже исследование: исследование основано на подавлении роста клеток плоскоклеточной карциномы легких линии NCI-H596 [АТСС НТВ 178; American Type Culture Collection, Rockville, Maryland, USA; см. публикацию Santon, J.B., и др., Cancer Research 46, 4701-4705 (1986) и публикацию Ozawa, S., и др., Int. J.Cancer 40, 706-710 (1987)], которые трансплантированы самкам голых мышей линии BALB/c (Bomholtgard, Denmark). Эта карцинома обнаруживает рост, который коррелирует со степенью экспрессирования EGF-R. Опухоли выявлены после подкожной инъекции клеток [минимально 2×106 клеток в 100 мкл забуференного фосфатом физиологического раствора (ЗФФ) или среды] мышам (4-8 мышей). Инъекции проводили подкожно в левый бок мыши посередине между хвостом и головой. До начала лечения для полученных опухолей проводили серийный пассаж не менее чем для трех последовательных трансплантаций. В течение этого времени скорости роста опухолей стабилизировались. Пассаж опухолей проводили не более 12 раз. В экспериментах по лечению фрагменты опухолей массой примерно 25 мг трансплантировали подкожно в левый бок животных с использованием игольчатого троакара №12 при анестезии с помощью Forene® (Abbott, Schwitzerland). Рост опухолей и массы тела определяли 2 раза в неделю. Лечение всегда начинали после того, как объем опухоли становится равным от 100 до 250 мм. Объемы опухолей рассчитывали по известной формуле: Длина×диаметр2×π/6 [см. публикацию Evans, B.D., и др., Brit. J. Cancer 45, 466-8 (1982)]. Противоопухолевую активность представляли в виде Т/С % (среднее увеличение объемов опухолей у подвергнутых лечению животных, деленное на среднее увеличение объемов опухолей у контрольных животных и умноженное на 100%). При дозе активного ингредиента, составляющей от 3 до 100 мг/кг, обнаружено явное подавление роста опухолей, например, Т/С %, составляющее менее 50.
Соединения формулы I могут ингибировать другие протеинтирозинкиназы, которые участвуют в передаче сигналов, опосредуемой трофическими факторами, например, abl киназы, в особенности такой как v-abl киназа (IС50 составляет, например, от 0,01 до 5 мкМ), киназ группы src, в особенности таких как c-src киназа (IС50 составляет, например, от 0,1 до 10 мкМ) и серин/треонинкиназ, например, протеинкиназы С, каждая из которых участвует в регуляции роста и превращениях в клетках млекопитающих, включая клетки человека.
Указанное выше ингибирование тирозинкиназы v-abl исследуют по методикам, описанным в публикации N.Lydon и др., Oncogene Research 5, 161-173 (1990) и в публикации J.F.Geissler и др., Cancer Research 52, 4492-4498 (1992). В этих методиках в качестве субстратов используют [Val5]-ангиотензин II и [γ-32P]-АТР.
Поэтому соединения формулы I, которые ингибируют активность тирозинкиназы EGF-R или других указанных протеинтирозинкиназ, применимы, например, при лечении доброкачественных или злокачественных опухолей. Соединения формулы I, например, способны одновременно подавлять рост опухолей с нарушенной регуляцией активности EGF-R и/или ЕrbВ-2, а также подавлять васкуляризацию солидных опухолей, стимулируемую посредством VEGF. Эта комбинированная активность приводит к улучшенному противоопухолевому эффекту (см. также WO 02/41882). Кроме того, применение двойного ингибитора уменьшает риск лекарственных взаимодействий и дополнительное уменьшает полную лекарственную нагрузку по сравнению с комбинированной терапией. Соединения формулы I способны замедлить рост опухоли или привести к регрессии опухоли и предупреждению образования метастазов опухоли и роста метастазов. Их предпочтительно можно применять в случае эпидермальной гиперпролиферации (псориаза), для лечения неоплазий эпителиального характера, например, карцином молочной железы и при лейкозах. Кроме того, соединения формулы I можно применять для лечения таких нарушений иммунной системы, в которых участвует несколько протеинтирозинкиназ или, предпочтительно, отдельные протеинтирозинкиназы и/или (кроме того) серин/треонинпротеинкиназы; соединения формулы I также можно применять для лечения таких нарушений центральной или периферической нервной системы, при которых в передаче сигналов участвуют несколько протеинтирозинкиназ или, предпочтительно, одна протеинтирозинкиназа и/или (кроме того) серин/треонинпротеинкиназы.
В целом настоящее изобретение также относится к применению соединений формулы I для ингибирования указанных выше протеинкиназ, предпочтительно - к их применению для двойного ингибирования представителей групп рецепторов EGF и VEGF.
Соединения, предлагаемые в настоящем изобретении, можно применять и поодиночке, и в комбинации с другими фармакологически активными соединениями, например, совместно с ингибиторами ферментов синтеза полиаминов, ингибиторами протеинкиназы С, ингибиторами других тирозинкиназ, цитокинами, регуляторами отрицательного роста, например, TGF-β или IFN-β, ингибиторами ароматазы, антиэстрогенами и/или цитостатическими лекарственными средствами.
В группах предпочтительных соединений формулы I, указанных ниже в настоящем изобретении, определения заместителей, приведенные выше в настоящем изобретении, целесообразно использовать, например, для замены более общих определений, например, для замены более общих определений на более конкретные определения или, предпочтительно, на определения, описанные, как являющиеся предпочтительными.
Предпочтение отдается соединению формулы I, в которой
R1 обозначает гетероциклический радикал или незамещенный или замещенный ароматический радикал;
G обозначает С1-С7-алкилен;
Q обозначает -NH- или -О-; и
Х или отсутствует, или обозначает С1-С7-алкилен, при условии, что гетероциклический радикал R1 присоединен через циклический атом углерода, если Х отсутствует;
или его соли.
Предпочтение также отдается соединению формулы I, в которой
R1 обозначает гетероциклический радикал, или незамещенный, или замещенный ароматический радикал;
G обозначает С1-С7-алкилен;
Q обозначает -NH-; и
Х или отсутствует, или обозначает С1-С7-алкилен, при условии, что гетероциклический радикал R1 присоединен через циклический атом углерода, если Х отсутствует;
или его соли.
Особое предпочтение отдается соединению формулы I, в которой
R1 обозначает гетероциклический радикал, содержащий вплоть до 20 атомов углерода, или незамещенный, или замещенный ароматический радикал, содержащий вплоть до 20 атомов углерода;
G обозначает C1-С3-алкилен;
Q обозначает -NH-; и
Х или отсутствует, или обозначает C1-С3-алкилен, при условии, что гетероциклический радикал R1 присоединен через циклический атом углерода, если Х отсутствует;
или его соли.
Особое предпочтение также отдается соединению формулы I, в которой
R1 обозначает фенил, бензодиоксолил, пиридил, замещенный гидроксигруппой или низш. алкоксигруппой, индолил, замещенный галогеном и низш. алкилом, или фенил, замещенный одним или большим количеством радикалов, независимо друг от друга выбранных из группы, включающей низш. алкил, гидроксигруппу, низш. алкоксигруппу, галоген и бензилоксигруппу;
G обозначает -СН2- или -С(=O)-;
Q обозначает -NH- или -О-, при условии, что Q обозначает -О-, если G обозначает -С(=O)-; и
Х или отсутствует, или обозначает -СН2- или -СН(СН3)-, при условии, что замещенный пиридил или индолил R1 присоединен через циклический атом углерода, если Х отсутствует;
или его соли.
Особое предпочтение также отдается соединению формулы I, в которой
R1 обозначает фенил, бензодиоксолил, пиридил, замещенный гидроксигруппой или низш. алкоксигруппой, или фенил, замещенный одним или большим количеством радикалов, независимо друг от друга выбранных из группы, включающей низш. алкил, гидроксигруппу, низш. алкоксигруппу, галоген и бензилоксигруппу;
G обозначает -СН2-;
Q обозначает -NH-; и
Х или отсутствует, или обозначает -СН2- или -СН(СН3)-, при условии, что замещенный пиридил R1 присоединен через циклический атом углерода, если Х отсутствует;
или его соли.
Особое предпочтение также отдается соединению формулы I в которой С1-С7-алкилен G присоединен к фенилу в положении 3 или 4, наиболее предпочтительно - в положении 4.
Наибольшее особое предпочтение также отдается соединению формулы I, указанному ниже в примерах, или его соли, предпочтительно - фармацевтически приемлемой соли.
Также особенно предпочтительными являются соединения формулы I, которые - по данным описанных выше анализов ингибирования тирозинкиназы - ингибируют HER-1, HER-2 и KDR при значениях IС50, составляющих менее 300 нМ, наиболее предпочтительно - составляющих менее 100 нМ.
Наибольшее особое предпочтение также отдается соединениям формулы I, которые ингибируют активность тирозинкиназы по меньшей мере одного представителя группы рецепторов EGF и одновременно по меньшей мере одного представителя группы рецепторов VEGF (двойное ингибирование представителей групп рецепторов EGF и VEGF) при значениях IС50, по данным описанных выше анализов ингибирования тирозинкиназы находящихся в диапазоне от 0,5 нМ до 0,5 мкМ, предпочтительно - в диапазоне от 1 нМ до 300 нМ.
Особенно предпочтительными дополнительно являются соединения формулы I, в которой G обозначает С1-С7-алкилен, поскольку аминогруппа таких соединений позволяет образовать фармацевтически приемлемые соли этих соединений, что обычно приводит к увеличенной растворимости и улучшенным физико-химическим характеристикам.
В предпочтительном варианте осуществления настоящее изобретение относится к изолированным соединениям формулы I, предпочтительно - к изолированному соединению ((R)-1-фенилэтил)-[6-(4-пиперазин-1-илметилфенил)-7H-пирроло[2,3-d]пиримидин-4-ил]-амину или к его солям, предпочтительно - фармацевтически приемлемым солям.
Термин "изолированное" соединение означает, что соединение удалено из своей первоначальной среды (например, природной среды, если оно находится в природе, включая организм человека или животного, который, например вырабатывает такое соединение после введения другого соединения). Например, природное соединение, находящееся в своей природной среде, не является изолированным, но то же соединение, отделенное от некоторых или всех находящихся совместно с ним в природной среде материалов, является изолированным даже если оно затем повторно вводится в природную систему. Такие соединения могут являться частью композиции и все же быть изолированными в том смысле, что такие композиции не являются частью их природной среды. Таким образом, соединение является по меньшей мере частично очищенным по сравнению с состоянием в природной среде, в которой оно обнаруживается, и поэтому не является природным продуктом.
В важном варианте осуществления изолированное соединение обладает чистотой, достаточной, чтобы допустить его применение для фармацевтических целей, в частности, для приготовления фармацевтической композиции.
Соединения формулы I или его соли можно получить по известным методикам (см., например, WO 03/013541 А1, опубликованную 20 февраля 2003 г.), предпочтительно - по методике, в которой
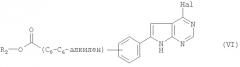
а) для получения соединения формулы I, в которой G обозначает С1-С7-алкилен, соединение формулы II
,
в которой Hal обозначает галоген, G обозначает С1-С7-алкилен и R1, Q и X обладают значениями, указанными для соединения формулы I, вводят в реакцию с пиперазином;
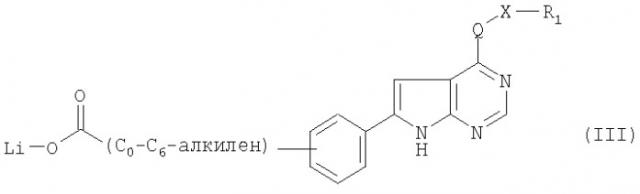
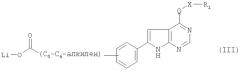
б) для получения соединения формулы I, в которой G обозначает -С(=O)- или С1-С6-алкилен-С(=O)-, в котором карбонильная группа присоединена к пиперазиновому фрагменту, соединение формулы III
в которой заместители и символы обладают значениями, указанными для соединения формулы I, вводят в реакцию с пиперазином; или
в) для получения соединения формулы I, в которой G обозначает С1-С7-алкилен, соединение формулы I, в которой G обозначает -С(=O)- или C1-С6-алкилен-С(=O)-, в котором карбонильная группа присоединена к пиперазиновому фрагменту, вводят в реакцию с восстановительным реагентом для получения соответствующего соединения, в котором G обозначает С1-С7-алкилен;
в которой функциональные группы, которые содержатся в исходных соединениях способов а)-в) и не предназначены для участия в реакции, при необходимости находятся в защищенной форме, и защитные группы, которые содержатся, отщепляются, причем указанные исходные соединения также могут находиться в форме солей, при условии, что содержится солеобразующая группы и возможна реакция с солью;
и, если это необходимо, полученное таким образом соединение формулы I превращают в другое соединение формулы I, свободное соединение формулы I превращают в соль, полученную соль соединения формулы I превращают в свободное соединение или другую соль, и/или смесь изомерных соединений формулы I разделяют на отдельные изомеры.
Описание вариантов способа:
Для способа а):
Реакцию между соединением формулы II и пиперазином (предпочтительно - защищенным по одному из его кольцевых атомов азота, таким как предпочтительно N-трет-бутоксикарбонилпиперазин) предпочтительно проводят в подходящем инертном растворителе, предпочтительно - N,N-диметилформамиде, в присутствии основания, такого как карбонат калия, при температурах от комнатной температуры (КТ) до 100°C. Альтернативно, реакцию между соединением формулы II и пиперазином (предпочтительно - в защищенной форме, таким как N-трет-бутоксикарбонилпиперазин) проводят в подходящем растворителе, например, низш. спиртах, таких как этанол, в присутствии, например, подходящего катализатора, такого как NaI, предпочтительно - при температуре кипения использованного растворителя. В соединении формулы II Hal предпочтительно обозначает хлор.
Для способа б):
Реакцию соединения формулы III с пиперазином (предпочтительно - защищенным по одному из его кольцевых атомов азота, таким как предпочтительно N-трет-бутоксикарбонилпиперазин) предпочтительно проводят в подходящем инертном растворителе, таком как N,N-диметилформамид, и в инертной атмосфере, например, в атмосфере аргона или азота, в присутствии диэтилцианофосфоната, предпочтительно - примерно при 0°C.
Для способа в):
Восстановительный реагент, применяющийся в способе в), предпочтительно представляет собой алюмогидрид лития или диизобутилалюминийгидрид. Реакцию предпочтительно проводят при условиях, описанных в примере 79 или 141 в WO 03/013541 А1 соответственно.
Дополнительные стадии способа
В дополнительных стадиях способа, проводимых при необходимости, функциональные группы исходных соединений, которые не должны участвовать в реакции, могут содержаться в незащищенной форме или могут быть защищены, например, одной или большим количеством защитных групп. 3атем защитные группы полностью или частично удаляют по одной из известных методик, предпочтительно - по методикам, описанным в примерах.
Защитные группы и пути их введения и удаления описаны, например, в публикации "Protective Groups in Organic Chemistry", Plenum Press, London, New York 1973, и в публикации "Methoden der organischen Chemie", Houben-Weyl, 4th edition, Vol.15/1, Georg-Thieme-Verlag, Stuttgart 1974 и в публикации Theodora W. Greene, "Protective Groups in Organic Synthesis", John Wiley & Sons, New York 1981. Особенностью защитных групп является то, что их можно удалить легко, т.е. без протекания нежелательных вторичных реакций, например, путем сольволиза, восстановления, фотолиза или, альтернативно, при физиологических условиях.
Однако конечные продукты формулы I также могут содержать заместители, которые также можно использовать в качестве защитных групп для исходных веществ, предназначенных для получения других конечных продуктов формулы I. Таким образом, в объеме настоящего описания только легко удаляемая группа, которая не является компонентом конкретного искомого конечного продукта формулы I) называется "защитной группой ", если в контексте не указано иное.
Общие условия осуществления способа
Приведенные ниже положения применимы в целом ко всем способам, указанным выше и ниже в настоящем изобретении, когда являются предпочтительными условия проведения реакций, специально указанные выше или ниже:
Все стадии способа, описанные в настоящем изобретении, можно выполнить при известных условиях проведения реакций, предпочтительно - при специально указанных, при отсутствии или обычно в присутствии растворителей или разбавителей, предпочтительно - растворителей или разбавителей, которые инертны по отношению к используемым реагентам и растворяют их, при отсутствии или в присутствии катализаторов конденсации или нейтрализующих реагентов, например, ионообменников, обычно катионообменников, например, в Н+ форме, в зависимости от природы реакции и/или реагентов при пониженной, нормальной или повышенной температуре, например, при температуре в диапазоне от примерно -100 до примерно 190°С; предпочтительно - от примерно -80 до примерно 150°С, например, от -80 до -60°С, при КТ, от -20 до 40°С, от 0 до 100°С или при температуре кипения используемого растворителя, при атмосферном давлении или в закрытом сосуде, когда это целесообразно, то под давлением и/или в инертной атмосфере, например, в атмосфере аргона или азота.
Настоящее изобретение также относится к таким вариантам осуществления способа, при которых в качестве исходного вещества используется соединение, получаемое на любой стадии в качестве промежуточного продукта, и проводят пропущенные стадии, или останавливают способ на любой стадии, или получают исходное вещество при условиях проведения реакции, или используют указанное исходное вещество в виде реакционноспособного производного или соль, или получают соединение, получаемое способом, предлагаемым в настоящем изобретении, при этих условиях проведения реакции, и затем обрабатывают указанное соединение in situ. В предпочтительном варианте осуществления используют такие исходные вещества, которые приводят к соединениям, описанным выше в настоящем изобретении в качестве предпочтительных.
В предпочтительном варианте осуществления соединение формулы I получают с помощью способа и стадий способа, описанных в примерах.
Соединения формулы I, включая их соли, также можно получить в виде гидратов, или их кристаллы могут включать, например, растворитель, использованный для кристаллизации (содержатся в виде сольватов).
Исходные вещества
Новые исходные вещества и/или промежуточные продукты, а также способы их получения также являются объектами настоящего изобретения. В предпочтительном варианте осуществления используют такие исходные вещества и выбирают такие условия проведения реакций, чтобы можно было получить предпочтительные соединения.
Исходные вещества, применяющиеся в описанных выше способах а)-в), являются известными, их можно получить по известным методикам (см. также ЕР 682027, WO 97/02266, WO 97/27199, WO 98/07726 и WO 03/013541 A1), или они имеются в продаже; в частности, их можно получить по методикам, описанным в примерах.
При получении исходных веществ имеющиеся функциональные группы, которые не должны участвовать в реакции, при необходимости должны быть защищены. Предпочтительные защитные группы, их введение и их удаление описаны выше или в примерах. Вместо соответствующих исходных веществ и промежуточных продуктов в реакции также можно использовать их соли при условии, что содержится солеобразующая группы и возможна реакция с солью. Когда выше и ниже в настоящем изобретении используется термин исходные вещества, всегда включаются их соли, если это целесообразно и возможно.
Соединение формулы II можно получить, например, по реакции соединения формулы IV
в которой G обозначает С1-С7-алкилен и R1, Q и Х обладают значениями, указанными для соединения формулы I, например, с тионилгалогенидом, предпочтительно - тионилхлоридом, в присутствии или при отсутствии пиридина, в инертном растворителе, например, толуоле или в смеси состава 1:1 ацетонитрила с диоксаном, предпочтительно - при температуре от -10 до 0°C или при КТ.
Соединение формулы IV можно получить, например, по реакции соединения формулы V
в которой R2 обозначает низш. алкил, предпочтительно - метил или этил, и R1, Q и Х обладают значениями, указанными для соединения формулы I, с
алюмогидридом лития, в инертном растворителе, предпочтительно - про