Соли и полиморфные модификации ингибитора vegf-r
Иллюстрации
Показать всеИзобретение относится к соли N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]
бензофуран-3-карбоксамида, а именно бисмалеату N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]
бензофуран-3-карбоксамида, обладающей противоопухолевой активностью. Изобретение также относится к фармацевтическим композициям на основании этой соли и способу лечения таких нарушений, как рак. 4 н. и 7 з.п. ф-лы, 35 ил., 9 табл.
Реферат
Данная заявка устанавливает приоритет заявки на патент США № 60/706332, поданной 8 августа 2005 г., и заявки на патент США № 60/750189, поданной 14 декабря 2005 г., из которых обе включены в настоящее описание в качестве ссылки.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Данное изобретение относится к формам соли и полиморфным модификациям N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида, который применим для лечения патологического роста клеток, такого как рак у млекопитающих. Данное изобретение также относится к композициям, включающим такие соли и полиморфные модификации, и к способам применения таких композиций для лечения патологического роста клеток у млекопитающих, главным образом, у людей.
Соединение N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида, представленное структурной формулой 1 в форме свободного основания, является
сильнодействующим селективным ингибитором рецептора 2 фактора васкулярного эндотелиального роста (VEGF-R2). Он сильно ингибирует активность тирозинкиназы рецептора VEGF-R2 и селективно блокирует, стимулируемый VEGF, рецептор аутофосфорилирования, а также продолжительность жизни эндотелиальных клеток. Исследования in vivo показали, что это соединение существенно ингибирует васкулярную проницаемость опухолевого ангиогенеза и роста опухолей ксенографтов человека. Это соединение было описано в опубликованной заявке на патент США 2005-0137395, опубликованной 23 июня 2005 г., описание которой включено сюда в качестве ссылки. Способы получения соединения 1 в форме свободного основания также описаны в предварительной заявке США 60/742847, озаглавленной “Methods of Preparing a VEGF-R Inhibitor”, поданной 5 декабря 2005 г.
Преимуществом является наличие соли и полиморфных форм, обладающих такими улучшенными характеристиками, как улучшенные степень кристалличности и растворимость и/или сниженная гигроскопичность, при сохранении стабильности и химических свойств энантиомеров.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
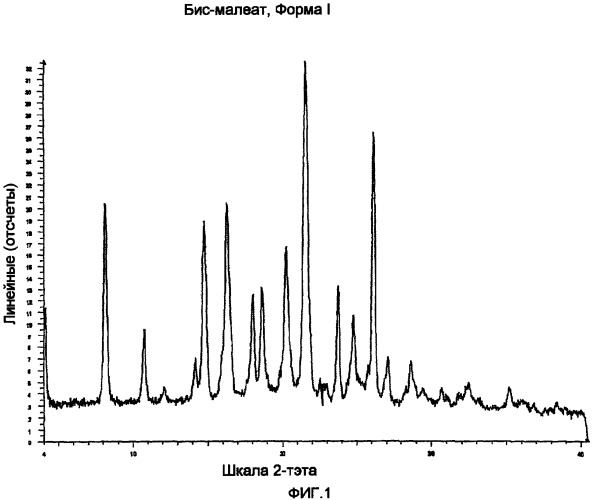
В одном варианте осуществления изобретения, настоящее изобретение предлагает соль бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида. В отдельных аспектах этого варианта осуществления изобретения, соль является безводной. В следующем аспекте, соль является кристаллической. В следующем аспекте соль представляет собой безводную кристаллическую соль. В следующем аспекте соль представляет собой, по существу, чистый полиморф бисмалеата, форму I. В следующем аспекте, соль имеет порошковую дифракционную рентгенограмму, имеющую пик при угле дифракции (2θ), составляющий 18,6±0,1. В следующем аспекте, соль имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 4,0±0,1; 18,1±0,1 и 18,6±0,1. В следующем аспекте, соль имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 4,0±0,1; 8,1±0,1; 18,1±0,1; 18,6±0,1; 21,6±0,1 и 26,2±0,1. В следующем аспекте, соль имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), по существу, такие же, как показано на Фиг. 1. В следующем аспекте, соль имеет спектр ЯМР твердых тел, где химический сдвиг 13C составляет 148,0±0,1 м.д. В следующем аспекте, соль имеет спектр ЯМР твердых тел, где химические сдвиги 13C составляют 148,0±0,1 и 162,5±0,1 м.д. В следующем аспекте, соль имеет спектр ЯМР твердых тел, где химические сдвиги 13C составляют 148,0±0,1; 118,0±0,1; 124,2±0,1; 143,9±0,1 и 162,5±0,1 м.д. В следующем аспекте, соль имеет спектр ЯМР твердых тел, где химические сдвиги 13C располагаются, по существу, как показано на Фиг. 2. В следующем аспекте, соль имеет спектр комбинационного рассеяния, имеющий смещения частот у 1589±1, 1402±1 и 755±1 cм-1. В следующем аспекте, соль имеет спектр комбинационного рассеяния, имеющий смещения частот, находящихся в положениях, по существу, аналогичных показанным на Фиг. 4.
Следующий вариант осуществления изобретения представляет собой соль бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида, где соль является сольватом. В отдельном варианте осуществления изобретения соль является гидратом. В следующем аспекте варианта осуществления изобретения соль представляет собой кристаллогидрат. В следующем аспекте, соль является, по существу, чистым полиморфом бисмалеата, формой III. В следующем аспекте, соль имеет порошковую дифракционную рентгенограмму, имеющую пик при угле дифракции (2θ), составляющий 12,7±0,1. В следующем аспекте, соль имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 6,4±0,1; 12,7±0,1 и 17,3±0,1. В следующем аспекте соль имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 6,4±0,1; 12,7±0,1; 17,3±0,1; 21,3±0,1 и 25,9±0,1. В следующем аспекте соль имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), по существу, аналогичные показанным на Фиг. 6. В следующем аспекте, соль имеет спектр ЯМР твердых тел, где химический сдвиг 13C составляет 132,8±0,1 м.д. В следующем аспекте, соль имеет спектр ЯМР твердых тел, где химические сдвиги 13C составляют 99,2±0,1; 125,8±0,1; и 132,8±0,1 м.д. В еще одном аспекте, в спектре ЯМР твердых тел соли химические сдвиги 13C составляют 99,2±0,1, 125,8±0,1, 132,8±0,1, 142,2±0,1 и 166,1±0,1 м.д. В еще одном аспекте, соль имеет спектр ЯМР твердых тел, где химические сдвиги 13C находятся в положениях, по существу, аналогичных показанным на Фиг. 7. В следующем аспекте соль имеет спектр комбинационного рассеяния, имеющий смещения колебательных частот, находящихся у 761±1, 1405±1 и 1595±1 cм-1. В следующем аспекте соль имеет спектр комбинационного рассеяния, имеющий смещения колебательных частот, находящихся в положениях, по существу, аналогичных показанным на Фиг. 9.
В следующем варианте осуществления изобретения, изобретение предлагает кристаллическую соль бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида, где соль представляет собой смесь бисмалеата формы I и бисмалеата формы III. Предпочтительно, когда смесь представляет собой, по существу, беспримесную смесь бисмалеата формы I и бисмалеата формы III, где, по существу, беспримесная смесь бисмалеата форм I и III включает в себя менее 10%, предпочтительно, менее 5%, предпочтительно, менее 3%, предпочтительно, менее 1% по массе любых других физических форм соли бисмалеата.
В следующем варианте осуществления, изобретение предлагает аморфную форму соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида. Например, аморфная форма может иметь порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), по существу, аналогичных углам, показанным на Фиг. 34.
В следующем варианте осуществления, изобретение предлагает кристаллическую форму свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида. В определенном варианте осуществления изобретения, кристаллическая форма свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида является безводной. В еще одном варианте осуществления изобретения, кристаллическая форма свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида является гидратом.
В следующем варианте осуществления изобретения, кристаллическая форма является полиморфом свободного основания формы 1. В частности, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 19,9±0,1 и 22,0±0,1. Еще более конкретно, кристаллическая форма имеет порошковую рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 13,5±0,1; 19,1±0,1; 19,9±0,1; 22,0±0,1 и 24,1±0,1. Еще более конкретно, кристаллическая форма имеет порошковую рентгенограмму, имеющую пики при углах дифракции (2θ), по существу, аналогичные углам, показанным на Фиг. 11.
В еще одном варианте осуществления изобретения, кристаллическая форма является полиморфом свободного основания формы 2. В частности, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 10,6±0,1 и 15,3±0,1. Еще более конкретно, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 10,6±0,1; 14,0±0,1; 15,3±0,1 и 16,9±0,1. Наиболее конкретно, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), по существу, аналогичные углам, показанным на Фиг. 12.
В еще одном варианте осуществления изобретения, кристаллическая форма является полиморфом свободного основания формы 3. В частности, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 12,5±0,1 и 21,6±0,1. Еще более конкретно, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 12,5±0,1; 21,2±0,1; 21,6±0,1 и 24,0±0,1. Наиболее конкретно, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), по существу, аналогичные углам, показанным на Фиг. 13.
В еще одном варианте осуществления изобретения, кристаллическая форма является полиморфом свободного основания формы 4. В частности, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 6,5±0,1 и 16,0±0,1. Еще более конкретно, кристаллическая форма имеет порошковую рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 5,6±0,1, 6,5±0,1, 16,0±0,1 и 19,5±0,1. Наиболее конкретно, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), по существу, аналогичные углам, показанным на Фиг. 14.
В еще одном варианте осуществления изобретения, кристаллическая форма является полиморфом свободного основания формы 5. В частности, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 22,6±0,1 и 23,4±0,1. Еще более конкретно, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 12,1±0,1; 18,4±0,1; 21,0±0,1; 22,6±0,1 и 23,4±0,1. Наиболее конкретно, кристаллическая форма имеет порошковую рентгенограмму, имеющую пики при углах дифракции (2θ), по существу, аналогичные углам, показанным на Фиг. 15.
В еще одном варианте осуществления изобретения, кристаллическая форма является полиморфом свободного основания формы 6. В частности, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 8,4±0,1 и 14,7±0,1. Еще более конкретно, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), составляющие 8,4±0,1; 14,7±0,1; 17,5±0,1 и 19,6±0,1. Наиболее конкретно, кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), по существу, аналогичные углам, показанным на Фиг. 16.
В следующем варианте осуществления, настоящее изобретение относится к кристаллической форме свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида, где кристаллическая форма имеет спектр комбинационного рассеяния, имеющий смещения колебательных частот, по существу, аналогичные показанным на любой из фигур 17-22.
В следующем варианте осуществления изобретения, настоящее изобретение относится к аморфной форме свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида. Например, аморфная форма может иметь порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), по существу, аналогичные углам, показанным на Фиг. 35.
Настоящее изобретение, кроме того, относится к бисгидробромиду соли N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида. В одном варианте осуществления изобретения, соль представляет собой безводную кристаллическую форму. В следующем варианте осуществления изобретения, соль является, по существу, чистым полиморфом бис-HBr формы I. В следующем варианте осуществления изобретения кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), по существу, аналогичные углам, показанным на Фиг. 29. В следующем варианте осуществления изобретения соль находится в форме кристаллогидрата. В следующем варианте осуществления изобретения соль представляет собой, по существу, чистый полиморф бис-HBr формы II. В следующем варианте осуществления изобретения кристаллическая форма имеет порошковую дифракционную рентгенограмму, имеющую пики при углах дифракции (2θ), по существу, аналогичные углам, показанным на Фиг. 30.
В настоящем изобретении, кроме того, предлагают фармацевтическую композицию, содержащую соль бисмалеата, соль бисгидробромида или формы свободного основания соединения формулы 1 в любой из описанных здесь форм, кристаллической или аморфной. В настоящем изобретении, кроме того, предлагают капсулу, содержащую любую из фармацевтических композиций по настоящему изобретению. В отдельных аспектах этого варианта осуществления изобретения, капсула содержит количество соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида, эквивалентное 0,1-50 мг свободного основания. В следующем аспекте, капсула содержит количество соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида, эквивалентное 0,5-25 мг свободного основания. В следующем аспекте капсула содержит 0,1-50 мг свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида. В следующем аспекте капсула содержит 0,5-25 мг свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида. В следующем аспекте капсула содержит количество бисгидробромида соли N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида, эквивалентное 0,1-50 мг свободного основания. В следующем аспекте, капсула содержит количество бисгидробромида соли N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида, эквивалентное 0,5-25 мг свободного основания.
В еще одном варианте осуществления, изобретение предлагает способ лечения рака у млекопитающих, включая человека, способ включает введение млекопитающему терапевтически эффективного количества любой из фармацевтических композиций по настоящему изобретению, здесь описанных.
В еще одном варианте осуществления изобретения, изобретение предлагает способ лечения рака у млекопитающих, способ включает введение млекопитающим, включая человека, любой из капсул по настоящему изобретению, описанных здесь.
В отдельном аспекте любого из способов по предшествующим вариантам осуществления изобретения способ дополнительно включает в себя введение одного или нескольких противоопухолевых агентов, агентов, препятствующих ангиогенезу, ингибиторов трансдукции сигнала, или агентов, препятствующих пролиферации.
Изобретение также относится к способу лечения патологического роста клеток у млекопитающих, включая человека, включающему в себя введение указанному млекопитающему соединения формулы 1, определенного выше, или его фармацевтически приемлемых соли или сольвата в количестве, эффективном для лечения патологического роста клеток. В одном варианте осуществления данного способа по изобретению, патологический рост клеток является раком, включая, но без ограничения, рак легкого, костный рак, рак поджелудочной железы, рак кожи, рак головы или шеи, кожную или внутриглазную меланому, рак матки, рак яичников, рак прямой кишки, рак анальной области, рак желудка, рак толстой кишки, рак грудной железы, маточный рак, карциному фаллопиевых труб, карциному эндометрия, цервикальную карциному, карциному влагалища, карциному женских половых органов, болезнь Ходжкина, рак пищевода, рак тонкой кишки, рак эндокринной системы, рак щитовидной железы, рак паращитовидной железы, рак надпочечника, саркому мягких тканей, рак уретры, рак полового члена, рак простаты, хроническую или острую лейкемию, лимфоцитарные лимфомы, рак мочевого пузыря, рак почки или мочеточника, карциному ренальных клеток, карциному почечной лоханки, неоплазмы центральной нервной системы (ЦНС), первичную лимфому ЦНС, спинальные осевые опухоли, глиому ствола мозга, аденому гипофиза, или сочетание одного или нескольких из приведенных выше видов рака. В еще одном варианте осуществления указанного способа по изобретению, указанный патологический рост клеток представляет собой доброкачественное пролиферативное заболевание, включающее, но без ограничения, псориаз, доброкачественную гипертрофию предстательной железы или рестеноз.
Данное изобретение также относится к способу лечения патологического роста клеток у млекопитающих, который включает в себя введение указанному млекопитающему количества соединения формулы 1, или его фармацевтически приемлемых соли или сольвата, которое является эффективным при лечении патологического роста клеток, в комбинации с противоопухолевым агентом, выбираемым из группы, состоящей из митотических ингибиторов, алкилирующих агентов, антиметаболитов, включающих антибиотик, ингибиторов фактора роста, ингибиторов клеточного цикла, ферментов, ингибиторов топоизомеразы, модификаторов биологической ответной реакции, антител, цитотоксического агента, антигормонов, антиандрогенов.
Это изобретение также относится к фармацевтической композиции для лечения патологического роста клеток у млекопитающих, включая человека, содержащей эффективное при лечении патологического роста клеток количество соединения формулы 1, определенного выше, или его фармацевтически приемлемых соли или сольвата, и фармацевтически приемлемый носитель. В одном варианте осуществления указанной композиции, указанный патологический рост клеток представляет собой рак, включающий, но без ограничения, рак легкого, костный рак, рак поджелудочной железы, рак кожи, рак головы или шеи, кожную или внутриглазную меланому, рак матки, рак яичника, ректальный рак, рак анальной области, рак желудка, рак толстой кишки, рак грудной железы, маточный рак, карциному фаллопиевых труб, карциному эндометрия, цервикальную карциному, карциному влагалища, карциному женских половых органов, болезнь Ходжкина, рак пищевода, рак тонкой кишки, рак эндокринной системы, рак щитовидной железы, рак паращитовидной железы, рак надпочечника, саркому мягких тканей, рак уретры, рак полового члена, рак простаты, хроническую или острую лейкемию, лимфоцитарные лимфомы, рак мочевого пузыря, рак почки или мочеточника, карциному клеток мочеточника, карциному почечной лоханки мочеточника, неоплазмы центральный нервной системы (ЦНС), первичную лимфому ЦНС, спинальные осевые опухоли, глиому ствола мозга, аденому гипофиза, или комбинацию одного или нескольких из вышеприведенных видов рака. В еще одном варианте осуществления указанной фармацевтической композиции, указанный патологический рост клеток является доброкачественным пролиферативным заболеванием, включающим, но без ограничения, псориаз, доброкачественную гипертрофию предстательной железы или рестеноз.
Изобретение также относится к фармацевтической композиции, предназначенной для лечения патологического роста клеток у млекопитающих, включая человека, которая содержит количество соединения формулы 1, определенного выше, или его фармацевтически приемлемых соли или сольвата, эффективное при лечении патологического роста клеток, в комбинации с противоопухолевым агентом, выбираемым из группы, состоящей из митотических ингибиторов, алкилирующих агентов, антиметаболитов, включающих антибиотик, ингибиторов фактора роста, ингибиторов клеточного цикла, ферментов, ингибиторов топоизомеразы, модификаторов биологической ответной реакции, антигормонов и антиандрогенов.
Данное изобретение также относится к способу лечения нарушения, связанного с ангиогенезом у млекопитающих, включая человека, включающему в себя введение указанному млекопитающему соединения формулы 1, определенного выше, или его фармацевтически приемлемых соли или сольвата, в количестве, эффективном для лечения указанного нарушения. Такие нарушения включают в себя ракoвые опухоли, такие как меланома; глазные нарушения, такие как возрастная дегенерация желтого пятна, установленный синдром глазного гистоплазмоза, и ретинальная реваскуляризация из-за пролиферативной диабетической ретинопатии; ревматоидный артрит; нарушения, связанные с потерей костной массы, такие как остеопороз, болезнь Педжета, злокачественное развитие гуморальной гиперкальциемии, гиперкальциемия, вследствие метастаза опухолей в кость, и остеопороз, вызванный лечением глюкокортикоидным гормоном; коронарный рестеноз; и некоторые микробные инфекции, включающие в себя инфекции, связанные с микробными патогенными микроорганизмами, выбираемыми из аденовируса, хантавирусов, Borrelia burgdorferi, Yersinia spp., Bordetella pertussis и группы A стрептокока.
Данное изобретение также относится к способу и к фармацевтической композиции, предназначенным для лечения патологического роста клеток у млекопитающих, включающему введение соединения формулы 1 или его фармацевтически приемлемых соли или сольвата, и одного или нескольких веществ, выбираемых из агентов, противодействующих ангиогенезу, ингибиторов трансдукции сигнала и агентов, препятствующих пролиферации, в количествах, эффективных при совместном использовании для лечения указанного патологического роста клеток у млекопитающих.
В способах и фармацевтических композициях, описанных здесь, агенты, противодействующие ангиогенезу, такие как ингибиторы MMP-2 (матрикс-металлопротеиназы 2), ингибиторы MMP-9 (матрикс-металлопротеиназы 9) и ингибиторы COX-II (циклооксигеназы II) могут быть использованы совместно c соединением формулы 1 или его фармацевтически приемлемыми солью или сольватом. Примеры применимых ингибиторов COX-II включают в себя CELEBREX™ (алекоксиб), вальдекоксиб и рофекоксиб. Примеры пригодных ингибиторов матрикс-металлопротеиназы описаны в заявках WO 96/33172 (опубликованной 24 октября 1996 г.), WO 96/27583 (опубликованной 7 марта 1996 г.), Европейской заявке на патент № 973049711 (поданной 8 июля 1997 г.), Европейской заявке на патент № 993086172 (поданной 29 октября 1999 г.), WO 98/07697 (опубликованной 26 февраля 1998 г.), WO 98/03516 (опубликованной 29 января 1998 г.), WO 98/34918 (опубликованной 13 августа 1998 г.), WO 98/34915 (опубликованной 13 августа 1998 г.), WO 98/33768 (опубликованной 6 августа 1998 г.), WO 98/30566 (опубликованной 16 июля 1998 г.), публикации Европейского патента 606046 (опубликованной 13 июля 1994 г.), публикации Европейского патента 931788 (опубликованной 28 июля 1999 г.), WO 90/05719 (опубликованной 31 мая 1990 г.), WO 99/52910 (опубликованной 21 октября 1999 г.), WO 99/52889 (опубликованной 21 октября 1999 г.), WO 99/29667 (опубликованной 17 июня 1999 г.), PCT Международной заявке № PCT/IB98/01113 (поданной 21 июля 1998 г.), Европейской заявке на патент № 99302232.1 (поданной 25 марта 1999 г.), заявке Великобритании на патент номер 9912961.1 (поданной 3 июня 1999 г.), предварительной заявке США № 60/148464 (поданной 12 августа 1999 г.), патенте США 5863949 (выданном 26 января 1999 г.), патенте США 5861510 (выданном 19 января 1999 г.), публикации Европейского патента 780386 (опубликованной 25 июня 1997 г.), из которых все включены полностью в настоящее описание в качестве ссылки. Предпочтительными ингибиторами MMP-2 и MMP-9 являются такие, которые обладают малой ингибирующей активностью по отношению MMP-1 или вообще не обладают такой активностью. Более предпочтительными ингибиторами являются такие ингибиторы, которые селективно ингибируют матрикс-металлопротеиназы MMP-2 и/или MMP-9 относительно других матрикс-металлопротеиназ (т.e. MMP-1, MMP-3, MMP-4, MMP-5, MMP-6, MMP-7, MMP-8, MMP-10, MMP-11, MMP-12 и MMP-13).
Некоторыми конкретными примерами MMP ингибиторов, применимых в комбинации с соединениями по настоящему изобретению, являются AG-3340, RO 32-3555, RS 13-0830, и соединения, перечисленные в нижеследующем списке:
3-[[4-(4-фторфенокси)бензолсульфонил]-(1-гидроксикарбамоилциклопентил)амино]пропионовая кислота; гидроксиамид 3-экзо-3-[4-(4-фторфенокси)бензолсульфониламино]-8-оксабицикло[3.2.1]октан-3-карбоновой кислоты; гидроксиамид (2R, 3R) 1-[4-(2-хлор-4-фторбензилокси)бензолсульфонил]-3-гидрокси-3-метилпиперидин-2-карбоновой кислоты; гидроксиамид 4-[4-(4-фторфенокси)бензолсульфониламино]-тетрагидропиран-4-карбоновой кислоты; 3-[[4-(4-фторфенокси)бензолсульфонил]-(1-гидроксикарбамоилциклобутил)амино]пропионовая кислота; гидроксиамид 4-[4-(4-хлорфенокси)бензолсульфониламино]тетрагидропиран-4-карбоновой кислоты; гидроксиамид 3-[4-(4-хлорфенокси)бензолсульфониламино]тетрагидропиран-3-карбоновой кислоты; гидроксиамид (2R, 3R) 1-[4-(4-фтор-2-метилбензилокси)бензолсульфонил]-3-гидрокси-3-метилпиперидин-2-карбоновой кислоты; 3-[[4-(4-фторфенокси)бензолсульфонил]-(1-гидроксикарбамоил-1-метилэтил)амино]пропионовая кислота; 3-[[4-(4-фторфенокси)бензолсульфонил]-(4-гидроксикарбамоилтетрагидропиран-4-ил)амино]пропионовая кислота; гидроксиамид 3-экзо-3-[4-(4-хлорфенокси)бензолсульфониламино]-8-оксабицикло[3.2.1]октан-3-карбоновой кислоты; гидроксиамид 3-эндо-3-[4-(4-фторфенокси)бензолсульфониламино]-8-оксабицикло[3.2.1]октан-3-карбоновой кислоты и гидроксиамид 3-[4-(4-фторфенокси)бензолсульфониламино]тетрагидрофуран-3-карбоновой кислоты; и фармацевтически приемлемые соли, сольваты и пролекарства указанных соединений.
Соединения формулы 1 и их фармацевтически приемлемые соли и сольваты также могут быть использованы в комбинации с ингибиторами трансдукции сигнала, такими как агенты, которые способны ингибировать ответные реакции EGFR (рецептора фактора эпидермального роста), такие как антитела EGFR, антитела EGF, и молекулы, которые являются ингибиторами EGFR; ингибиторы VEGF (фактора васкулярного эндотелиального роста); и ингибиторы рецептора erbB2, такие как органические молекулы или антитела, которые связываются с erbB2 рецептором, например, HERCEPTIN™ (Genentech, Inc. of South San Francisco, California, USA).
Ингибиторы EGFR описаны, например, в WO 95/19970 (опубликованной 27 июля 1995 г.), WO 98/14451 (опубликованной 9 апреля 1998 г.), WO 98/02434 (опубликованной 22 января 1998 г.) и в патенте США 5747498 (выданном 5 мая 1998 г.). Ингибирующие EGFR агенты включают, но без ограничения, моноклональные антитела C225 и анти-EGFR 22Mab (ImClone Systems Incorporated of New York, New York, USA), соединения ZD-1839 (АstraZeneca), BIBX-1382 (Boehringer Ingelheim), MDX-447 (Medarex Inc. of Annandale, New Jersey, USA), и OLX-103 (Merck & Co. of Whitehouse Station, New Jersey, USA), VRCTC-310 (Ventech Research) и токсин слияния EGF (Seragen Inc. of Hopkinton, Massachusetts).
Ингибиторы VEGF, например SU-5416 и SU-6668 (Pfizer Inc.), также могут быть объединены с соединением формулы 1 или его фармацевтически приемлемыми солью или сольватом. Например, ингибиторы VEGF описаны в заявке WO 99/24440 (опубликованной 20 мая 1999 г.), PCT международной заявке PCT/IB99/00797 (поданной 3 мая 1999 г.), в заявке WO 95/21613 (опубликованной 17 августа 1995 г.), в WO 99/61422 (опубликованной 2 декабря 1999 г.), в патенте США 5834504 (выданном 10 ноября 1998 г.), WO 98/50356 (опубликованной 12 ноября 1998 г.), патенте США 5883113 (выданном 16 марта 1999 г.), патенте США 5886020 (выданном 23 марта 1999 г.), патенте США 5792783 (выданном 11 августа 1998 г.), WO 99/10349 (опубликованной 4 марта 1999 г.), WO 97/32856 (опубликованной 12 сентября 1997 г.), WO 97/22596 (опубликованной 26 июня 1997 г.), WO 98/54093 (опубликованной 3 декабря 1998 г.), WO 98/02438 (опубликованной 22 января 1998 г.), WO 99/16755 (опубликованной 8 апреля 1999 г.) и WO 98/02437 (опубликованной 22 января 1998 г.), из которых все включены в настоящее описание полностью в качестве ссылки. Другими примерами некоторых конкретных ингибиторов VEGF являются IM862 (Cytran Inc. of Kirkland, Washington, USA); анти-VEGF моноклональное антитело от Genentech, Inc. of South San Francisco, California; и синтетический рибозим, ангиозим, от Ribozyme (Boulder, Colorado) и Chiron (Emeryville, California).
Ингибиторы ErbB2 рецептора, такие как GW-282974 (Glaxo Wellcome plc) моноклональные антитела AR-209 (Aronex Pharmaceuticals Inc. of The Woodlands, Texas, USA) и 2B-1 (Chiron), могут быть введены в комбинации с соединением формулы 1 или его фармацевтически приемлемой солью или сольватом. Такие ингибиторы erbB2 включают в себя ингибиторы, описанные в WO 98/02434 (опубликованной 22 января 1998 г.), WO 99/35146 (опубликованной 15 июля 1999 г.), WO 99/35132 (опубликованной 15 июля 1999 г.), WO 98/02437 (опубликованной 22 января 1998 г.), WO 97/13760 (опубликованной 17 апреля 1997 г.), WO 95/19970 (опубликованной 27 июля 1995 г.), в патенте США 5587458 (выданном 24 декабря 1996 г.) и патенте США 5877305 (выданном 2 марта 1999 г.), каждый из которых полностью включен в настоящее описание в качестве ссылки. Ингибиторы ErbB2 рецептора, применимые в настоящем изобретении, описаны также в предварительной заявке США № 60/117341, поданной 27 января 1999 г., и в предварительной заявке США № 60/117346, поданной 27 января 1999 г., из которых обе заявки включены в настоящее описание полностью в качестве ссылки.
Другие агенты, препятствующие пролиферации, которые могут быть использованы в комбинированных способах по настоящему изобретению, включают в себя ингибиторы фермента фарнезилпротеинтрансферазы и ингибиторов рецептора тирозинкиназы PDGFr, включая соединения, описанные и заявленные в нижеследующих заявках на патент США: 09/221946 (поданной 28 декабря 1998 г.); 09/454058 (поданной 2 декабря 1999 г.); 09/501163 (поданной 9 февраля 2000 г.); 09/539930 (поданной 31 марта 2000 г.); 09/202796 (поданной 22 мая 1997 г.); 09/384339 (поданной 26 августа 1999 г.) и 09/383755 (поданной 26 августа 1999 г.); и соединения, описанного и заявленного в нижеследующих предварительных заявках на патент США: 60/168207 (поданной 30 ноября 1999 г.); 60/170119 (поданной 10 декабря 1999 г.); 60/177718 (поданной 21 января 2000 г.); 60/168217 (поданной 30 ноября 1999 г.) и 60/200834 (поданной 1 мая 2000 г.). Каждая из вышеприведенных заявок на патент и предварительных заявок на патент включена в настоящее описание полностью в качестве ссылки.
Соединение формулы 1 или его фармацевтически приемлемые соль или сольват также могут быть использованы вместе с другими агентами, применимыми при лечении патологического роста клеток или рака, включающими, но без ограничения, агенты, способные усиливать противоопухолевые иммунные ответные реакции, такие как CTLA4 (цитотоксичный лимфоцитарный антиген 4) антитела, и другие агенты, способные блокировать CTLA4 и агенты, препятствующие пролиферации, такие как другие ингибиторы фарнезилпротеинтрансферазы, например ингибиторы фарнезилпротеинтрансферазы, описанные ранее в ссылках, цитированных в разделе “Предпосылки изобретения”, выше. Конкретные CTLA4 антитела, которые могут быть использованы в настоящем изобретении, включают в себя антитела, описанные в предварительной заявке США 60/113647 (поданной 23 декабря 1998 г.), которая полностью включена в настоящее описание в качестве ссылки.
Термин “лечение”, используемый здесь, означает, если не оговорено иначе, возвращение к прежнему состоянию, ослабление, торможение прогресса или предотвращение нарушения или состояния, к которому применяют этот термин, или же одного или нескольких симптомов такого нарушения или состояния. Термин “лечение”, используемый здесь, если не оговорено иначе, относится к проведению лечения, как непосредственно определено выше.
Термин “по существу, чистый (беспримесный)”, используемый здесь, относящийся к отдельной полиморфной или аморфной форме, означает, что полиморфная аморфная форма включает менее чем 10% по массе, предпочтительно, менее чем 5%, предпочтительно менее чем 3%, предпочтительно менее чем 1% любых других физических форм соединения.
Термин “по существу, одинаковый” используемый здесь, относящийся к положениям пиков рентгеновской дифракции, означает, что учитывают положение типичного пика и вариабельность интенсивности. Например, специалист в данной области поймет, что положения пика (2θ) показывает некоторую внутриприборную вариабельность, обычно на величину 0,1°. Более того, специалист в данной области поймет, что относительные интенсивности пиков покажут внутриприборную вариабельность, а также изменение, обусловленное степенью кристалличности, предпочтительной ориентацией, предварительной обработкой поверхности образца и другими факторами, известными специалисту в данной области, но которые следует рассматривать только как качественные критерии. Аналогично, термин “по существу, одинаковый” используемый здесь, относящийся к ЯМР спектру твердого тела и к спектру комбинационного рассеяния, также предназначен охватить вариабельность, связанную с техникой анализа, которая известна специалистам в данной области. Например, химические сдвиги 13C, измеряемые методом ЯМР твердого тела, как правило, будут меняться на 0,1 м.д., тогда как смещения в КР спектре обычно измеряют в cм-1.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1 показана порошковая дифракционная рентгенограмма соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы I.
На фиг. 2 показан спектр ЯМР твердых тел соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы I.
На фиг. 3 показана термограмма, полученная посредством дифференциальной сканирующей калориметрии (ДСК) соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы I.
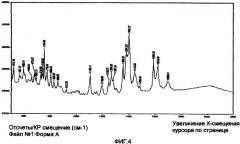
На фиг. 4 показан спектр комбинационного рассеяния соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы I.
На фиг. 5 показан динамический профиль сорбции пара соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы I.
На фиг. 6 показана порошковая дифракционная рентгенограмма соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы III.
На фиг. 7 показан спектр ЯМР твердых тел соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы III.
На фиг. 8 показана термограмма, полученная посредством дифференциальной сканирующей калориметрии (ДСК) соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы III.
На фиг. 9 показан спектр комбинационного рассеяния соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы III.
На фиг. 10 показан спектр комбинационного рассеяния соли бисмалеата N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы III.
На фиг. 11 показана порошковая дифракционная рентгенограмма свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы 1.
На фиг. 12 показана порошковая дифракционная рентгенограмма свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы 2.
На фиг. 13 показана порошковая дифракционная рентгенограмма свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы 3.
На фиг. 14 показана порошковая дифракционная рентгенограмма свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы 4.
На фиг. 15 показана порошковая дифракционная рентгенограмма свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы 5.
На фиг. 16 показана порошковая дифракционная рентгенограмма свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы 6.
На фиг. 17 показан спектр комбинационного рассеяния свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы 1.
На фиг. 18 показан спектр комбинационного рассеяния свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы 2.
На фиг. 19 показан спектр комбинационного рассеяния свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы 3.
На фиг. 20 показан спектр комбинационного рассеяния свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бензофуран-3-карбоксамида полиморфной формы 4.
На фиг. 21 показан спектр комбинационного рассеяния свободного основания N,2-диметил-6-[7-(2-морфолиноэтокси)хинолин-4-илокси]бе