Слитые белки il-7
Иллюстрации
Показать всеИзобретение относится к биотехнологии. Описан слитый белок, включающий цепочку иммуноглобулина и молекулу IL-7 или ее фрагмент, проявляющий активность, присущую IL-7, которая является модифицированной по сравнению с IL-7 дикого типа, где модификация в IL-7 представляет собой аминокислотные остатки в положениях 70 и 91, которые являются гликозилированными, а аминокислотный остаток в положении 116 является негликозилированным. Предложена фармацевтическая композиция, содержащая описанный белок. Представлен способ получения описанного слитого белка, включающий трансформацию клетки-хозяина с помощью ДНК, кодирующей описанный слитый белок IL-7, культивирование клетки-хозяина и сбор слитого белка IL-7. Изобретение может быть использовано при лечении расстройств, сопровождающихся иммунными дефицитами, и, в частности, заболеваний, которые вовлекают дефициты Т-клеток. 6 н. и 21 з.п. ф-лы, 16 ил., 1 табл.
Реферат
[0001] Изобретение относится к слитым белкам интерлейкина-7 (IL-7), способам их получения и к их применению. Слитые белки включают иммуноглобулиновую часть, слитую непосредственно или опосредованно с IL-7, которая может быть модифицирована в специфических положениях по сравнению с IL-7 дикого типа для того, чтобы улучшить биологические и фармацевтические свойства. Белки в соответствии с изобретением являются особенно полезными при лечении расстройств, сопровождающихся иммунодефицитами, и, в частности, заболеваний, которые вовлекают дефициты Т-клеток.
Предпосылки изобретения
[0002] Разнообразные расстройства и способы лечения вовлекают дефицит иммунных клеток. Например, инфекция ВИЧ приводит к потере CD4+ Т-клеток, в то время как способы лечения, такие как химиотерапия и радиационная терапия, обычно приводят к потере широкого разнообразия клеток крови. Были сделаны попытки обеспечить специфические белковые препараты, которые могут пополнить специфические типы иммунных клеток, теряемых в результате заболевания или терапии. Например, в раковой химиотерапии эритропоэтин используется для пополнения красных клеток крови, колониестимулирующий фактор гранулоцитов (G-CSF) используется для пополнения гранулоцитов, а колониестимулирующий фактор гранулоцитов и макрофагов (GM-CSF) используется для пополнения гранулоцитов и макрофагов. Эти белковые лекарственные средства несмотря на то, что являются полезными, имеют относительно короткий период полураспада в сыворотке крови, так что пополнение иммунных клеток часто является неэффективным. Более того, в клиническом применение в настоящее время не существует никакого специфического лечения для специфической стимуляции развития Т- или В-клеток, даже несмотря на то, что потеря этих клеток в результате заболевания или после определенных миелоабляционных способов лечения известна как явление, которое является особенно вредным для здоровья пациента. Таким образом, существует потребность в области техники, которая заключается в развитии стимуляторов и восстановителей иммунной системы, в частности лимфоцитов, которые имеют продолжительный период полураспада в сыворотке крови.
Короткое изложение сущности изобретения
[0003] Настоящее изобретение направлено на слитые белки интерлейкина-7 (IL-7), которые имеют улучшенные биологические свойства по сравнению с соответствующими белками IL-7 дикого типа. Более того, настоящее изобретение основывается, частично, на обнаружении того факта, что слитые белки IL-7, обладающие особенными структурными свойствами, имеют улучшенные биологические свойства по сравнению с рекомбинантным IL-7 дикого типа.
[0004] Соответственно, в одном аспекте изобретение характеризует белок слияния, который включает одну часть, содержащую цепь иммуноглобулина (Ig), и вторую часть, содержащую интерлейкин-7 (IL-7), где слитый белок IL-7 имеет повышенную биологическую активность, такую как длительный период полураспада в сыворотке крови или улучшение выживания или роста иммунных клеток по сравнению с IL-7 дикого типа.
[0005] В одном воплощении изобретение характеризует белок слияния, который включает одну часть, содержащую цепь иммуноглобулина (Ig), и вторую часть, содержащую IL-7, где аминокислотные остатки в положениях 70 и 91 IL-7 являются гликозилированными, а аминокислотный остаток в положении 116 IL-7 является негликозилированным. Повсюду в этом документе аминокислотные положения IL-7 относятся к соответствующим положениям в последовательности зрелого человеческого IL-7. В одном воплощении аминокислотный остаток в положении 116 IL-7 представляет собой аспарагин. В другом воплощении аминокислотный остаток в положении 116 IL-7 является измененным таким образом, что он не служит сайтом гликозилирования. В одном воплощении остаток IL-7 включает дисульфидную связь между Cys2 и Cys92, Cys34 и Cys129, и Cys47 и Cys141 IL-7.
[0006] В другом воплощении изобретение предусматривает слитый белок, содержащий одну часть, которая включает цепь Ig, и вторую часть, включающую IL-7, где IL-7 включает дисульфидную связь между Cys2 и Cys92, Cys34 и Cys129, и Cys47 и Cys141 IL-7. В одном воплощении аминокислотный остаток в положении 116 IL-7 является негликозилированным. В другом воплощении аминокислотный остаток в положении 116 IL-7 представляет собой аспарагин или является измененным таким образом, что он не служит сайтом гликозилирования. В другом воплощении аминокислотные остатки в положениях 70 и 91 IL-7 являются гликозилированными.
[0007] Цепь Ig обычно представляет собой интактное антитело или его часть, такую как участок Fс. Цепь Ig слитого белка IL-7 может иметь происхождение от любого известного изотипа Ig и может включать, по крайней мере, часть одного или более константных доменов. Например, константный домен может быть выбран из группы, которая состоит из участка СН1, шарнирного участка антитела, участка СН2 и участка СН3. В одном воплощении остаток Ig включает шарнирный участок, участок СН2 и участок СН3. Цепь Ig необязательно является связанной с частью IL-7 с помощью линкера.
[0008] Остатки Ig одного изотипа антитела, такие как IgG1 или IgG2, и гибридные участки Ig разрешаются в данном изобретении. Например, в одном воплощении остаток Ig включает шарнирный участок, который имеет происхождение от одного изотипа (то есть IgG2), и участок СН, полученный от другого изотипа (то есть IgG1). Цепь Ig, включающая часть Fc IgG1, может преимущественно быть модифицирована для включения мутаций Asn297Gln и Тyr296Аlа. Кроме того, цепь Ig, включающая часть Fc IgG2, может быть преимущественно модифицирована для включения мутаций Asn297Gln и Phe296Ala.
[0009] IL-7 часть слитого белка IL-7, описанного выше, может включать зрелую часть IL-7 части. В одном воплощении IL-7 часть может дополнительно включать делецию, такую как внутренняя делеция. В одном примере IL-7 может включать делецию восемнадцати аминокислот от аминокислоты 96 до 114 SEQ ID NO: 1.
[0010] В других воплощениях изобретение включает очищенные нуклеиновые кислоты, кодирующие белки слияния IL-7, описанные выше, и культивируемые хозяйские клетки, включающие эти нуклеиновые кислоты.
[0011] В другом аспекте изобретение включает способ получения слитого белка IL-7, включающего экспрессию в хозяйской клетке нуклеиновой кислоты, описанной выше, и выделение слитого белка.
[0012] В другом аспекте изобретение включает композицию, такую как фармацевтическая композиция, содержащая слитый белок, описанный выше.
[0013] В другом аспекте изобретение включает способ лечения пациента путем введения слитых белков Fc-IL-7.
Краткое описание чертежей
[0014] Фигура 1 показывает аминокислотную последовательность человеческого IL-7 (SEQ ID NO:1). Сигнальная последовательность представлена жирным шрифтом. Восемнадцать аминокислот, которые могут быть делетированы из IL-7 последовательности, представлены жирным шрифтом и курсивом.
[0015] Фигура 2 показывает аминокислотную последовательность коровьего IL-7 (SEQ ID NO:2). Сигнальная последовательность представлена жирным шрифтом.
[0016] Фигура 3 показывает аминокислотную последовательность бараньего IL-7 (SEQ ID NO:3). Сигнальная последовательность представлена жирным шрифтом.
[0017] Фигура 4 показывает аминокислотную последовательность зрелого человеческого Fcγ1-IL-7 (SEQ ID NO:4).
[0018] Фигура 5 показывает аминокислотную последовательность зрелого человеческого Fcγ2(h) (FN>AQ)-IL-7 (SEQ ID NO:5).
[0019] Фигура 6 показывает аминокислотную последовательность зрелого человеческого Fcγ1 (линкер 1)-IL-7 (SEQ ID NO:6).
[0020] Фигура 7 показывает аминокислотную последовательность зрелого человеческого Fcγ1 (YN>AQ) (линкер2)-1Е-7 (SEQ ID NO:7).
[0021] Фигура 8 показывает аминокислотную последовательность зрелого человеческого Fcγ1 (YN>AQ,d) (линкер2)-IL-7 (SEQ ID NO:8).
[0022] Фигура 9 представляет собой последовательность нуклеиновой кислоты для участка Fc человеческого Fcγ1-IL-7 (SEQ ID NO:22).
[0023] Фигура 10 представляет собой последовательность нуклеиновой кислоты для участка Fc человеческого Fcγ1 (YN>AQ)-IL-7 (SEQ ID NO:21).
[0024] Фигура 11 представляет собой последовательность нуклеиновой кислоты для участка Fc человеческого Fcγ2(h)-IL-7 (SEQ ID NO:20).
[0025] Фигура 12 представляет собой последовательность нуклеиновой кислоты для участка Fc человеческого Fcγ2(h) (FN>AQ)-IL-7 (SEQ ID NO:19).
[0026] Фигура 13 представляет собой графическое изображение фармакокинетического профиля рекомбинантного человеческого IL-7 (незаштрихованные квадраты) и слитого белка Fcγ2(h) (FN>AQ)-IL-7 (незаштрихованные ромбы) Примера 7. Концентрации в сыворотке введенных слитых белков IL-7 (в нг/мл) измеряли в течение времени (в часах).
[0027] Фигура 14 представляет собой графическое изображение восстановления В-клеток у облученных мышей с пересаженным костным мозгом и обработанных с помощью рекомбинантного человеческого IL-7 (незаштрихованные символы), человеческого Fc-IL-7 (заштрихованные символы) или ФБР (X). Белки вводили через день (квадраты) и один раз в неделю (треугольники). Пунктирная линия представляет концентрацию В-клеток у донорной мыши.
[0028] Фигура 15 представляет собой графическое изображение восстановления Т-клеток у облученных мышей с пересаженным костным мозгом и обработанных с помощью рекомбинантного человеческого IL-7 (незаштрихованные символы), человеческого Fc-IL-7 (заштрихованные символы) или ФБР (X). Белки вводили через день (квадраты) и один раз в неделю (треугольники). Пунктирная линия представляет концентрацию Т-клеток у донорной мыши.
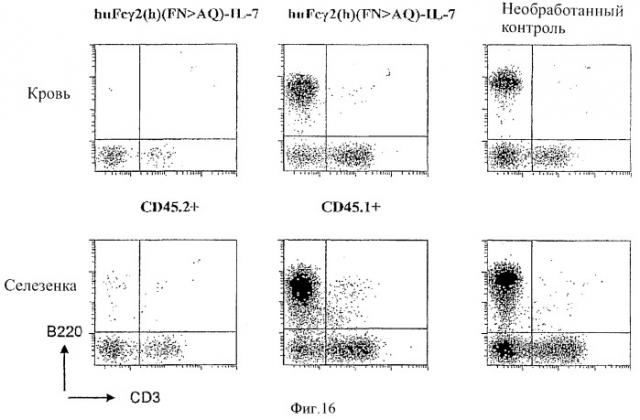
[0029] Фигура 16 представляет собой точечную схему, иллюстрирующую популяции лимфоцитов образцов крови (верхний ряд) и селезенки (нижний ряд) у облученных мышей с пересаженным костным мозгом и обработанных с помощью huFcγ2(h) (FN>AQ)-IL-7 (первые две колонки), необработанных контролей (последняя колонка). Первая колонка представляет восстановленные эндогенные лимфоциты (CD45.2+), а вторая колонка представляет восстановленные донорные лимфоциты (CD45.1+). Т-лимфоциты определяли как CD3 позитивные клетки, показанные в расположенном нижнем правом квадранте. В-лимфоциты определяли как В220 позитивные клетки, показанные в расположенном верхнем левом квадранте.
Подробное описание изобретения
[0030] Изобретение обеспечивает слитые белки IL-7, которые обладают улучшенной биологической активностью по сравнению с белками IL-7 дикого типа. В частности, изобретение обеспечивает слитые белки IL-7, которые включают иммуноглобулиновую часть (Ig). Эти Ig-IL-7 слитые белки обладают улучшенной биологической активностью, такой как более продолжительный период полураспада в сыворотке крови по сравнению с белками IL-7 дикого типа, что делает их приемлемыми для применения при лечении состояний, сопровождающихся дефицитом иммунных клеток, таких как дефициты лимфоцитов.
[0031] Изобретение также частично основывается на открытии того факта, что слитые белки IL-7, которые обладают особыми структурными характеристиками, также имеют улучшенные биологические свойства. Несмотря на то что аминокислотная последовательность IL-7 млекопитающих является хорошо известной, информация о структуре белков IL-7, имеющих происхождение от эукариотических клеток, в том числе, например, каким образом происходит сборка белков и каким является влияние его предсказанных N-связанных сайтов гликозилирования на его биологическую структуру, является слабо изученным. Например, человеческий белок IL-7 имеет цистеин в положениях 2, 34, 47, 92, 129 и 141 зрелого белка и три потенциальных N-связанных сайта гликозилирования в положениях аспарагин (Asn)70, Asn91 и Asn116. Однако точная структура IL-7, синтезированного при культивировании эукариотических клеток, является неизвестной.
[0032] Настоящее изобретение включает слитые белки IL-7, которые имеют особые структурные формы и повышенную биологическую активность. Например, слитые белки IL-7, имеющие дисульфидную модель связывания Cys2-Cys92, Cys34-Cys129 и Cys47-141, являются более активными in vivo, чем рекомбинантный белок IL-7 дикого типа.
[0033] Более того, изобретение обеспечивает форму слитого белка IL-7, в которой два или три потенциальных N-связанных сайта гликозилирования IL-7 являются гликозилированными. В частности, Asn70 и Asn91 зрелого белка являются гликозилированными, в то время как предсказанный N-связанный сайт гликозилирования в положении Asn116 IL-7 не является гликозилированным. Такой слитый белок IL-7 является более активным in vivo, чем рекомбинантный IL-7 дикого типа.
[0034] Изобретение также включает слитые белки IL-7, в которых остаток IL-7 содержит делецию и которые сохраняют сравнимую активность по сравнению с соответствующими немодифицированными слитыми белками IL-7. Например, изобретение обеспечивает форму Ig-IL-7, в которой остаток IL-7 содержит делецию восемнадцати внутренних аминокислот, соответствующую последовательности VKGRKPAALGEAQPTKSL (SEQ ID NO:9).
Слитые белки интерлейкина-7
[0035] Обычно IL-7 часть белка сливают с белком носителя. В одном воплощении белок носителя располагается на N-терминальном конце слитого белка, а белок IL-7 располагается на С-терминальном конце. В другом воплощении слитый белок IL-7 располагается на N-терминальном конце слитого белка, а белок носителя располагается на С-терминальном конце.
[0036] Как используется в данной заявке, термин «интерлейкин-7» или «IL-7» означает полипептиды IL-7 и их производные и аналоги, которые имеют существенную идентичность аминокислотной последовательности с зрелым человеческим IL-7 дикого типа и существенно эквивалентую биологическую активность, например, в стандартных биоанализах или анализах связывающей аффинности рецептора IL-7. Например, IL-7 относится к аминокислотной последовательности рекомбинантного или нерекомбинантного полипептида, который имеет аминокислотную последовательность i) нативного или существующего в природе аллельного варианта полипептида IL-7, ii) биологически активного фрагмента полипептида IL-7, iii) биологически активного полипептидного аналога полипептида IL-7, или iv) биологически активного варианта полипептида IL-7. Полипептиды IL-7 в соответствии с изобретением могут быть получены из любых видов, например человека, коровы или овцы. Последовательность нуклеиновой кислоты и аминокислотная последовательность IL-7 являются хорошо известными в области техники. Например, аминокислотная последовательность человеческого IL-7 имеет депозитный номер в Genbank NM 000880 (SEQ ID NO:1), она показана на Фигуре 1; аминокислотная последовательность мышиного IL-7 имеет депозитный номер в Genbank NM 008371; аминокислотная последовательность IL-7 крысы имеет депозитный номер в Genbank AF 367210; аминокислотная последовательность IL-7 коровы имеет депозитный номер в Genbank NM 173924 (SEQ ID NO:2), она показана на Фигуре 2; а IL-7 аминокислотная последовательность овцы имеет депозитный номер в Genbank 1110089 (SEQ ID NO: 3), она показана на Фигуре 3. Сигнальная последовательность для полипептида каждого вида выделена жирным шрифтом на каждой из Фигур и обычно не включается в случае, если IL-7 часть слита своей С-терминальной частью с белком носителя.
[0037] «Вариант» белка IL-7 определяется как аминокислотная последовательность, которая изменена в одной или более аминокислотах. Вариант имеет «консервативные» изменения в том случае, если заменяющая аминокислота обладает подобными структурными или химическими свойствами, например замена лейцина изолейцином. Более редко вариант может иметь «неконсервативные» изменения, например замену глицина триптофаном. Подобные минорные вариации могут также включать делеции аминокислот или инсерции, или и то, и другое. Руководство по поводу определения, какая и как много аминокислотных остатков могут быть заменены, встроены или делетированы без устранения биологической активности, могут быть найдены при использовании компьютерных программ, которые являются хорошо известными в области техники, например, программного обеспечения для молекулярного моделирования или для получения выравнивания. Варианты IL-7 белков, входящие в объем данного изобретения, включают белки IL-7, которые сохраняют активность IL-7. Полипептиды IL-7, которые включают добавления, замены или делеции, также включаются в данное изобретение до тех пор, пока они сохраняют существенно эквивалентную биологическую активность IL-7. Например, укороченные варианты IL-7, которые сохраняют сравнимую биологическую активность, что и форма полной длины белка IL-7, включаются в данное изобретение. Активность белка IL-7 может быть измерена при использовании in vitro анализов клеточной пролиферации, таких как описано в Примере 6 выше. Активность вариантов IL-7 в соответствии с изобретением поддерживает биологическую активность, по крайней мере, 10%, 20%, 40%, 60%, но более предпочтительно 80%, 90%, 95% и даже более предпочтительно 99% по отношению с IL-7 дикого типа.
[0038] Варианты белков IL-7 также включают полипептиды, которые обладают, по крайней мере, приблизительно 70%, 75%, 80%, 85%, 90%, 92%, 95%, 96%, 97%, 98%, 99% или более идентичностью последовательности с последовательностью IL-7 дикого типа. Для определения процента идентичности двух аминокислотных последовательностей или двух последовательностей нуклеиновых кислот эти последовательности выравниваются для целей оптимального выравнивания (например, в первую аминокислотную последовательность или последовательность нуклеиновой кислоты могут быть введены пробелы для оптимального выравнивания со второй аминокислотной последовательностью или последовательность нуклеиновой кислоты). Процент идентичности между двумя последовательностями представляет собой функцию номера идентичных положений, общих для последовательностей (то есть % гомологии = число идентичных положений/общее число положений·100 раз). Определение процента гомологии между двумя последовательностями может быть осуществлено при использовании математического алгоритма. Предпочтительный неограничивающий пример математического алгоритма, используемого для сравнения двух последовательностей, представляет собой алгоритм Karlin и Altschul (1990) Proc. Natl. Acad. Sci. USA 87: 2264-68, модифицированного в соответствии с Karlin и Altschul (1993) Proc. Natl. Acad. Sci. USA 90: 5873-77. Такой алгоритм введен в программы NBLAST и XBLAST Altschul, и др., (1990) J. Mol. Biol. 215: 403-10. BLAST нуклеотидный поиск может быть осуществлен с помощью программы NBLAST, шкала = 100, разрядность = 12. BLAST белковый поиск может быть осуществлен с помощью программы XBLAST, шкала = 50, разрядность = 3. Для получения выравнивания, содержащего пробелы, для целей сравнения может быть использована программа Gapped BLAST, как описано у Altschul и др,. (1997) Nucleic Acids Research 25(17): 3389-3402. При использовании программ BLAST и Gapped BLAST можно использовать параметры по умолчанию соответствующих программ (например, XBLAST и NBLAST).
[0039] Потенциальные Т-клеточные или В-клеточные эпитопы в остатке IL-7 могут быть удалены или модифицированы в Fc-IL-7 слитые белки в соответствии с изобретением. Примеры остатков IL-7 с устраненной иммуногенностью раскрыты в во временной заявке США под названием «Варианты IL-7 со сниженной иммуногенностью» (Номер дела патентного поверенного LEX-035PR), которая была подана в Ведомство США по патентам и товарным знакам 9 декабря 2004 года.
Белок носителя
[0040] Белок носителя может представлять собой любой остаток, ковалентно слитый с белком IL-7. В одном воплощении белок носителя представляет собой альбумин, например человеческий сывороточный альбумин. В другом воплощении белок носителя представляет собой остаток иммуноголобулина (Ig), такой как тяжелая цепь Ig. Цепь Ig может быть получена из IgA, IgD, IgE, IgG или IgM. В соответствии с изобретением остаток Ig может образовывать интактное антитело и может нацеливать слитый белок IL-7 на специфические целевые сайты в организме. Слитые белки, использующие нацеливание антител, являются известными для специалиста в данной области. В другом воплощении остаток Ig носителя дополнительно включает легкую цепь Ig.
[0041] В одном воплощении остаток Ig включает участок Fc. Как используется в данной заявке, термин «Fc часть» охватывает домены, которые имеют происхождение от константного участка иммуноглобулина, предпочтительно человеческого иммуноглобулина, в том числе фрагмента, аналога, варианта, мутанта или производной константного участка. Приемлемые иммуноглобулины включают IgG1, IgG2, IgG3, IgG4 и другие классы. Константный участок иммуноглобулина определяется как природный или синтетически полученный полипептид, гомологичный иммуноглобулину С-терминального участка, он может включать домен СН1, шарнирный участок, СН2 домен, СН3 домен или СН4 домен, отдельно или в любой комбинации. В данном изобретении часть Fc обычно включает СН2 домен. Например, Fc часть может включать шарнир-СН2-СН3. Альтернативно, Fc часть может включать весь или часть шарнирного участка, СН2 домен и/или СН3 домен и/или СН4 домен.
[0042] Константный участок иммуноглобулина является ответственным за множество важных функций антитела, в том числе связывание с рецептором Fc (FcR) и фиксацию комплемента. Существует пять основных классов константных участков тяжелой цепи, которые классифицируются как IgA., IgG, IgD, IgE и IgM. Например, IgG подразделяется на четыре подкласса: 1, 2, 3 и 4, которые также известны как IgG1, IgG2, IgG3 и IgG4 соответственно.
[0043] Молекулы IgG взаимодействуют с многочисленными классами клеточных рецепторов, в том числе тремя классами рецепторов Fсγ (FcγR), специфичных для IgG класса антител, а именно FcγRI, FcγRII и FcγRIII. Важные последовательности для связывания IgG с рецепторами FcγR, как было сообщено, расположены в доменах СН2 и СН3. Период полураспада антитела в сыворотке крови находится под влиянием способности этого антитела связываться с рецептором Fc (FcR). Подобно этому, период полураспада слитых белков иммуноглобулина также находится под влиянием способности связываться с такими рецепторами (Gillies и др., (1999) Cancer Res. 59: 2159-66). По сравнению с таковыми IgG1, СН2 и СН3, домены IgG2 и IgG4 имеют биохимически невыявляемую или пониженную связывающую аффинность к рецепторам Fc. Было показано, что слитые белки иммуноглобулина, содержащие СН2 и СН3 домены IgG2 или IgG4, имеют более длительные периоды полураспада по сравнению с соответствующими слитыми белками, содержащими СН2 и СН3 домены IgG1 (Патент США №5,541,087; Lo и др., (1998) Protein Engineering, 11: 495-500). В соответствии с определенными воплощениями данного изобретения предпочтительные СН2 и СН3 домены получены из изотипа антитела со сниженными связывающей аффиностью антитела и эффекторными функциями, таких как, например, IgG2 или IgG4. Более предпочтительно СН2 и СН3 домены являются полученными из IgG2.
[0044] Шарнирный участок обычно располагается С-терминально по отношению к СН1 домену константного участка тяжелой цепи. В изотипах IgG дисульфидные связи обычно возникают внутри этого шарнирного участка, что позволяет образовывать тетрамерную молекулу антитела. В этом участке доминирующими являются пролины, серины и треонины. В рамках настоящего изобретения шарнирный участок является обычно, по крайней мере, гомологичным природному участку иммуноглобулина, который включает остатки цистеина для образования дисульфидных связей, связывающих два остатка Fc. Характерные последовательности шарнирных участков для иммуноглобулинов человека и мыши являются известными в области техники и могут быть найдены у Borrebaeck, ред., (1992) Antibody Engineering. A Practical Guide. W.H. Freeman и Со. Приемлемые шарнирные участки для настоящего изобретения могут быть получены из IgG1, IgG2, IgG3, IgG4 и других классов иммуноглобулинов.
[0045] Шарнирный участок IgG1 содержит три цистеина, второй и третий из которых являются вовлеченными в дисульфидные связи между двумя тяжелыми цепями иммуноглобулина. Эти одинаковые два цистеина позволяют осуществлять эффективное и стойкое дисульфидное связывание части Fc. Таким образом, предпочтительный шарнирный участок в соответствии с настоящим изобретением получен из IgG1, более предпочтительно из человеческого IgG1, в котором первый цистеин является предпочтительно мутированным до другой аминокислоты, предпочтительно серина.
[0046] Шарнирный участок изотипа IgG2 содержит четыре дисульфидные связи, которые имеют тенденцию к усилению олигомеризации и возможному неправильному дисульфидному связыванию при секреции в рекомбинантных системах. Приемлемые шарнирные участки могут быть получены из шарнирного участка IgG2; при этом каждый из двух первых цистеинов является предпочтительно мутированными до другой аминокислоты.
[0047] Шарнирный участок IgG4 известен как такой, который формирует неэффективные внутрицепочечные дисульфидные связи. Однако приемлемый шарнирный участок для настоящего изобретения может быть получен из шарнирного участка IgG4, предпочтительно содержащего мутацию, которая способствует правильному формированию дисульфидных связей между остатками тяжелых цепей (Angal и др., (1993) Mol. Immunol., 30: 105-8).
[0048] В соответствии с настоящим изобретением часть Fc может содержать СН2 и/или СН3 и/или СН4 домены и шарнирный участок, который имеет происхождение от различных изотипов антитела, то есть является гибридной Fc частью. Например, в одном воплощении, Fc часть содержит СН2 и/или СН3 домены, полученные из IgG2 или IgG4, и мутантный шарнирный участок, полученный из IgG1. Как используется в данной заявке, Fcγ2(h) относится к воплощению, в котором шарнирный участок имеет происхождение от IgG1, a остальные константные домены происходят из IgG2. Альтернативно, мутантный шарнирный участок, полученный из другого подкласса IgG, используется в гибридной части Fc. Например, может использоваться мутантная форма шарнира IgG4, которая позволяет осуществлять эффективное дисульфидное связывание между двумя тяжелыми цепями. Мутантный шарнирный участок может также иметь происхождение от шарнирного участка IgG2, в котором каждый из двух первых цистеинов является мутированным до другой аминокислоты. Такие гибридные части Fc способствуют экспрессии на высоком уровне и улучшают правильную сборку Fc-IL-7 слитых белков. Сборка таких гибридных Fc частей является известной в области техники и была описана в опубликованной патентной заявке США №2003-0044423.
[0049] В некоторых воплощениях Fc часть содержит модификации аминокислот такие, которые обычно удлиняют период полураспада Fc слитого белка в сыворотке крови. Такие аминокислотные модификации включают мутации, существенно снижающие или устраняющие Fc связывание с рецептором или активность в отношении фиксации комплемента. Например, сайт гликозилирования в пределах Fc части тяжелой цепи иммуноглобулина может быть удален. В IgG1 сайт гликозилирования представляет собой Asn297 в пределах аминокислотной последовательности Gln-Tyr-Asn-Ser (SEQ ID NO:30). В других изотипах иммуноглобулина сайт гликозилирования соответствует Asn297 IgG1. Например, в IgG2 и IgG4 сайт гликозилирования представляет собой аспарагин в пределах аминокислотной последовательности Gln-Phe-Asn-Ser (SEQ ID NO:29). В соответствии с этим мутация Asn297 IgG1 удаляет сайт гликозилирования в Fc части, имеющей происхождение от IgG1. В одном воплощении Asn297 является замененным на Gln. В другом воплощении тирозин в пределах аминокислотной последовательности Gln-Tyr-Asn-Ser (SEQ ID NO:30) является дополнительно мутированным для устранения потенциального эпитопа, не принадлежащего Т-клеткам, полученного в результате мутации аспарагина. Как используется в данной заявке, эпитоп Т-клеток представляет собой полипептидную последовательность в белке, которая взаимодействует с или связывается с молекулами МНС класса II. Например, аминокислотная последовательность Gln-Tyr-Asn-Ser (SEQ ID NO:30) в пределах IgG1 тяжелой цепи может быть заменена на аминокислотную последовательность Gln-Ala-Gln-Ser (SEQ ID NO:28). Подобно этому, мутация аспарагина в пределах аминокислотной последовательности Gln-Phe-Asn-Ser (SEQ ID NO:29) в IgG2 или IgG4 устраняет сайт гликозилирования в Fc части, имеющей происхождение от тяжелой цепи IgG2 или IgG4. В одном воплощении аспарагин заменяется глутамином. В других воплощениях фенилаланин в пределах аминокислотной последовательности Gln-Phe-Asn-Ser (SEQ ID NO:29) является дополнительно мутированным для устранения потенциального эпитопа, не принадлежащего Т-клеткам, полученного в результате мутации аспарагина. Например, аминокислотная последовательность Gln-Phe-Asn-Ser (SEQ ID NO: 29) в пределах тяжелой цепи IgG2 или IgG4 может быть заменена аминокислотной последовательностью Gln-Ala-Gln-Ser (SEQ ID NO: 28).
[0050] Как показали наблюдения, изменение аминокислот поблизости соединения части Fc и не-Fc части может значительно повысить период полураспада в сыворотке крови слитого белка Fc (опубликованная патентная заявка США №2002-0147311). Соответственно, участок соединения слитого белка Fc-IL-7 или IL-7-Fc в соответствии с настоящим изобретением может также содержать изменения, которые соответствуют природным последовательностям тяжелой цепи иммуноглобулина и IL-7 и предпочтительно лежат в пределах приблизительно 10 аминокислот точки соединения. Эти аминокислотные изменения могут вызывать повышение гидрофобности путем, например, изменения С-терминального лизина Fc части на гидрофобную аминокислоту, такую как аланин или лейцин. Еще в одном воплощении в соответствии с изобретением С-терминальный лизин и предшествующий глицин части Fc являются делетированными.
[0051] В других воплощениях Fc часть содержит изменения аминокислот сегмента Leu-Ser-Leu-Ser поблизости С-терминального конца Fc части тяжелой цепи иммуноглобулина. Аминокислотные замены сегмента Leu-Ser-Leu-Ser (SEQ ID NO:27) устраняют потенциальные соединительные эпитопы Т-клеток. В одном воплощении аминокислотная последовательность Leu-Ser-Leu-Ser (SEQ ID NO:27) поблизости С-терминального конца Fc части заменяется на аминокислотную последовательность Ala-Thr-Ala-Thr (SEQ ID NO:26). В других воплощениях аминокислоты в пределах сегмента Leu-Ser-Leu-Ser (SEQ ID NO:27) заменяются на другие аминокислоты, такие как глицин или пролин. Подробно способы осуществления аминокислотных замен сегмента Leu-Ser-Leu-Ser (SEQ ID NO:27) поблизости С-терминального конца IgG1, IgG2, IgG3, IgG4 или других классов молекул иммуноглобулина, а также другие примеры модификаций для изменения соединительных эпитопов Т-клеток, были описаны в опубликованной заявке США №2003-0166877.
Спейсер
[0052] В одном воплощении спейсерный или линкерный пептид является встроенным между белком носителя и слитым белком IL-7. Например, спейсер размещается непосредственно С-терминально по отношению к последней аминокислоте константного участка Ig. Спейсерный или линкерный пептид является предпочтительно незаряженным и более предпочтительно неполярным или гидрофобным. Длина спейсерного или линкерного пептида предпочтительно составляет от 1 до приблизительно 100 аминокислот, более предпочтительно от 1 до приблизительно 50 аминокислот, или от 1 до приблизительно 25 аминокислот, и даже более предпочтительно от 1 до приблизительно 15 аминокислот, и даже более предпочтительно менее чем 10 аминокислот. В одном воплощении спейсер содержит последовательность (G4S)n, где n является меньшим чем 5. В предпочтительном воплощении спейсер содержит последовательность G4SG4 (SEQ ID NO: 25). Еще в одном воплощении спейсер содержит фрагмент, который узнается как N-связанный сайт гликозилирования. Еще в одном воплощении спейсер содержит фрагмент, который узнается сайт-специфическим агентом расщепления. В альтернативном воплощении изобретения белок носителя и слитый белок IL-7 разделены синтетическим спейсером, например, PNA спейсером, который предпочтительно является незаряженным и более предпочтительно неполярным или гидрофобным.
Получение слитых белков IL-7
[0053] Неограничивающие способы для синтеза полезных воплощений в соответствии с изобретением описаны в Примерах данной заявки, как и анализы, полезные для определения in vitro свойств, фармакокинетики и in vivo активности на животных моделях.
[0054] Слитые белки IL-7 в соответствии с изобретением могут быть получены при использовании рекомбинантных экспрессионных векторов, известных в области техники. Термин «экспрессионные векторы» относится к способной к репликации конструкции ДНК, которая кодирует желаемый слитый белок IL-7 и которая содержит транскрипционную единицу, включающую объединение (1) генетического(их) элемента(ов), который(ые) играет (играют) регуляторную роль в генной экспрессии, например, промоторов, операторов или энхансеров, оперативно связанного(ых) с (2) последовательностью ДНК, кодирующей желаемый слитый белок IL-7, который транскрибируется в мРНК и транслируется в белок, и (3) приемлемые последовательности инициации транскрипции и трансляции, а также терминации транскрипции и трансляции. Выбор промотора или других регуляторных элементов обычно варьирует в зависимости от намеченной хозяйской клетки. Предпочтительный экспрессионный вектор в соответствии с изобретением представляет собой Fc экспрессионный вектор, полученный из PdCs-huFc экспрессионного вектора, описанного у Lo и др., Protein Engineering (1998) 11: 495.
[0055] В предпочтительном примере нуклеиновая кислота, кодирующая слитый белок IL-7, трансфецируется в хозяйскую клетку при использовании методик рекомбинантной ДНК. В контексте настоящего изобретения чужеродная ДНК включает последовательность, кодирующую белки в соответствии с изобретением. Приемлемые хозяйские клетки включают прокариотические, дрожжевые и высшие эукариотические клетки. Предпочтительные хозяйские клетки представляют собой эукариотические клетки.
[0056] Рекомбинантные слитые белки IL-7 могут быть экспрессированы в дрожжевых хозяевах, предпочтительно из видов Saccharomyces, таких как S. cerevisiae. Могут также использоваться дрожжи других родов, таких как Pichia или Kluyveromyces. Дрожжевые векторы будут обычно содержать источник репликации из дрожжевой плазмиды или автономно реплицирующуюся последовательность (ARS), промотор, ДНК, кодирующую слитый белок IL-7, последовательности для полиаденилирования и терминации транскрипции, а также гены для селекции. Приемлемые промоторные последовательности в дрожжевых векторах включают промоторы для металлотионеина, 3-фосфоглицераткиназы или других гликолитических ферментов, таких как энолаза, глицеральдегид-3-фосфатдегидрогеназа, гексокиназа, пируватдекарбоксилаза, фосфофруктокиназа, глюкоза-4-фосфатизомераза, 3-фосфоглицератмутаза, пируваткиназа, триозафосфатизомераза, фосфоглюкозоизомераза и глюкокиназа.
[0057] Различные системы культур клеток млекопитающих или насекомых могут использоваться для экспрессии рекомбинантного белка. Бакуловирусные системы для получения белков в клетках насекомых являются хорошо известными в области техники. Примеры приемлемых хозяйских клеток млекопитающих включают клетки NS/0, L клетки, С127, 3Т3, клетки яичника китайского хомячка (СНО), линии клеток HeLa и ВНК. Дополнительные приемлемые хозяйские клетки млекопитающих включают клетки CV-1 (ATCC CCL70) и клетки COS-7, которые получены из почки обезьян. Другая приемлемая линия клеток почки обезьян, CV-1/EBNA, была получена путем трансфекции клеточной линии CV-1 с помощью гена, кодирующего ядерный антиген-1 вируса Эпштейна-Барр (EBNA-1) и с помощью вектора, содержащего регуляторные последовательности цитомегаловируса (CMV) (McMahan и др., (1991) EMBO J. 10: 2821). Ген EBNA-1 позволяет осуществлять эписомальную репликацию экспрессионных векторов, таких как HAV-EO или pDC406, которые содержат EBV источник репликации.
[0058] Экспрессионные векторы млекопитающих могут включать нетранскрибируемые элементы, такие как источник репликации, приемлемый промотор и энхансер, связанные с геном, который подвергают репликации, и другие 5' или 3' фланкирующие нетранскрибируемые последовательности, а также 5' или 3' нетранслируемые последовательности, такие как необходимые сайты связывания рибосом, сайты полиаденилирования, донорные и акцепторные сайты сплайсинга и последовательности терминации транскрипции. Обычно используемые промоторы и энхансеры являются такими, которые получены из вируса полиомы, аденовируса 2, обезьяньего вируса 40 (SV40) и цитомегаловируса человека. ДНК последовательности, полученные из вирусного генома SV40, например, SV40 источник, ранний и поздний промоторы, энхансеры, сплайсер и сайты полиаденилирования, могут использоваться для получения других генетических элементов, необходимых для экспрессии гетерологичной последовательности ДНК.
[0059] Для секреции слитого белка IL-7 из хозяйской клетки экспрессионный вектор включает ДНК, кодирующую сигнальный и лидерный пептиды. В настоящем изобретении можно использовать ДНК, кодирующую нативную сигнальную последовательность IL-7, или альтернативно, можно использовать ДНК, кодирующую гетерологичную сигнальную последовательность, такую как сигнальная последовательность из другого интерлейкина или из молекулы секретируемого Ig.
[0060] Настоящее изобретение также обеспечивает способ для получения рек