Твердый состав с улучшенными растворимостью и стабильностью и способ его получения
Иллюстрации
Показать всеНастоящее изобретение относится к области лекарственных средств, в частности к твердым составам для улучшения растворимости в воде фармацевтически активного ингредиента, включающим (1) фармацевтически активный ингредиент представляет собой 2-(2-{3-диметилкарбамоил-4-[(4′-трифторметилбифенил-2-карбонил)амино]фенил}ацетоксиметил)-2-фенилмалоновой кислоты диэтиловый эфир или его соль, (2) водорастворимое полимерное вещество (поливинилпирролидон или гидроксипропилцеллюлоза), (3) неорганическое пористое (безводную кремниевая кислота), при этом фармацевтически активный ингредиент образует твердую дисперсию в форме частиц вместе с водорастворимым полимерным веществом, и водорастворимое полимерное вещество в форме частиц поддерживается в состоянии, способном адсорбироваться и/или приклеиваться к поверхности неорганического пористого вещества. Также изобретение относится к способам получения указанных составов. Такие составы обеспечивают улучшение растворимости активного компонента и улучшение стабильности. 4 н. и 18 з.п. ф-лы, 2 ил., 2 табл.
Реферат
Область техники
Настоящее изобретение относится к твердому составу с улучшенными растворимостью и стабильностью и способу получения указанного состава.
Более конкретно, настоящее изобретение относится к твердому составу, обладающему улучшенной растворимостью в воде, который включает химическое вещество, плохо растворимое в воде, в качестве фармацевтически активного ингредиента, водорастворимое полимерное вещество и неорганическое пористое вещество, отличающемуся тем, что
(1) химическое вещество, плохо растворимое в воде, образует твердую дисперсию совместно с водорастворимым полимерным веществом,
(2) водорастворимое полимерное вещество, образующее твердую дисперсию, находится в форме мелких частиц, и
(3) водорастворимое полимерное вещество находится в форме мелких частиц и поддерживается в состоянии, способном адсорбироваться и/или приклеиваться к поверхности неорганического пористого вещества,
и к способу получения указанного состава.
Твердый состав настоящего изобретения демонстрирует прекрасную растворимость и высокую биодоступность и способен полностью проявлять достаточную исходную активность в качестве фармацевтически активного ингредиента при предельно низкой дозировке. Следовательно, твердый состав настоящего изобретения при введении больному мало обременяет больного и может также снижать опасение в отношении возникновения побочных эффектов. Более того, твердый состав имеет прекрасную стабильность и может быть получен крайне эффективно и легко с помощью способа настоящего изобретения.
Твердый состав настоящего изобретения может легко и полностью абсорбироваться организмом и, соответственно, когда данную методику применяют к веществам, ингибирующим микросомальный белок транспорта триглицеридов (MTP) и т.д., это не просто приводит к снижению дозировки и улучшению биодоступности, но может быть использовано в качестве прекрасного терапевтического или профилактического агента для гиперлипидемии, артериального склероза, заболевания коронарных артерий, ожирения, сахарного диабета или гипертензии, при которых побочные эффекты, такие как ожирение печени, снижены за счет избирательного ингибирования целевого MTP тонкого кишечника.
Уровень техники
Далее описывается уровень техники приготовления составов для улучшения растворимости в воде химического вещества, которое плохо растворяется в воде и служит в качестве фармацевтически активного ингредиента, а также уровень техники в отношении веществ, ингибирующих MTP, которые рассматриваются как один из примеров фармацевтических продуктов, к которым больше всего подходит применение твердого фармацевтического состава настоящего изобретения.
1. Способы приготовления составов
1-1. Растворимость и стабильность лекарственного вещества
При создании твердого фармацевтического состава, в частности пероральной формы, считается важным в отношении эффективности фармацевтических продуктов добиться достаточно высокой биодоступности.
Много факторов влияет на биодоступность при пероральном введении. Хотя эти факторы включают растворимость в воде, всасывание лекарственного вещества в пищеварительном тракте в целом, величину дозировки и эффект первого прохождения, полагают, что растворимость в воде является наиболее важным и доминирующим фактором при разработке фармацевтических продуктов, так как скорость растворения является определяющей скорость стадией поглощения, особенно для фармацевтических агентов, плохо растворимых в воде.
К сожалению, однако, многие химические вещества для фармацевтических продуктов плохо растворимы в воде и только очень маленькая доза переносится и поглощается кровью и, таким образом, они обладают недостатком в виде крайне низкой биодоступности.
Сообщается, что 338 фармацевтических соединений, продаваемых для перорального введения, за исключением белковых фармацевтических продуктов, подвергали тесту на растворимость Фармакопеи Японии и результаты суммировали, классифицируя по категориям от «предельно растворимых» до «плохо растворимых», и в результате 150 анализируемых соединений, которые составляли 40% суммарных образцов, были классифицированы как «плохо растворимые» соединения, обладающие растворимостью не более 0,1 мг/мл.
Хотя лекарственное вещество должно иметь высокую биодоступность, другими словами, высокую растворимость, так, чтобы проявлялась его эффективность, как указано выше, с другой стороны, его стабильность также очень важна, так как лекарственные вещества хранятся в течение продолжительного периода времени.
Обычно кристаллические химические вещества более стабильны, но хуже растворяются по сравнению с аморфными формами этих веществ. В этом случае решение в отношении растворимости и решение в отношении стабильности находятся в несовместимом сочетании друг с другом, и решение проблем стабильности и растворимости одновременно является предельно трудной задачей.
1-2. Улучшение растворимости плохо растворимых лекарственных веществ
Различные фармацевтические подходы, такие как превращение в солевые формы, образование сольватов, полиморфизм кристаллов, распыление лекарственного вещества в тонкие порошки, смешивание и измельчение с наполнителем, были осуществлены для того, чтобы улучшить растворимость этих плохо растворимых лекарственных веществ.
Однако способы приготовления составов, которые поддерживают стабильность при улучшении растворимости, особенно способы, которые могут обычно применяться к любым лекарственным веществам, не были найдены.
Твердую дисперсию широко использовали в качестве средства улучшения растворимости плохо растворимых лекарственных веществ, и ряд плохо растворимых лекарственных веществ был внедрен в практику в виде твердых дисперсий фармацевтических продуктов. Твердую дисперсию определяют как «дисперсию, в которой один или более активных ингредиентов диспергируется в находящемся в твердом состоянии инертном носителе или его матриксе, получаемую с помощью способа сплавления, способа растворения или способа сплавления-растворения» (см. непатентный документ 1).
Твердая дисперсия представляет собой твердую смесь, получаемую с помощью способов растворения лекарственного вещества в органическом растворителе совместно с носителем, состоящим из неорганического пористого вещества или полимерного вещества, с образованием однородной жидкой фазы с последующим высушиванием или способами сплавления полимерного вещества и лекарственного вещества, за которыми следует их отверждение, и лекарственное вещество однородно диспергируется в матриксе носителя или на его поверхности в виде микрокристаллов или частиц молекулярного размера, что означает состояние в виде одиночных молекул. Обычно аморфное вещество находится в состоянии с более высокой энергией и соответственно имеет улучшенную скорость растворения и повышенный уровень лекарственного вещества в водном растворе по сравнению с кристаллом и, в результате, обладает повышенным всасыванием и способностью к повышению концентрации в крови (например, см. патентные документы 1 и 2).
1-3. Способ получения твердой дисперсии
Несколько типов способов предлагалось в качестве способов получения твердой дисперсии и особенно практичные способы включают способ растворения, способ сплавления, способ распылительной сушки, способ смешивания и измельчения. Из них ниже описываются способ сплавления и способ растворения.
(A) Способ сплавления
Способ сплавления представляет собой способ нагревания и плавления лекарственного вещества, которое является активным ингредиентом, совместно с носителем, состоящим из неорганического пористого вещества и полимерного вещества, и получением в результате этого твердой дисперсии. Например, сообщалось о способе получения твердой дисперсии, состоящей из итраконазола и неорганического пористого вещества, который отличается смешиванием итраконазола, противогрибкового агента триазолового типа и неорганического пористого вещества, выбранного из группы, состоящей из силиката кальция, легкой безводной кремниевой кислоты, силиката магния, алюмосиликата магния, алюмометасиликата магния, силиката алюмомагния, синтетического силиката алюминия и гидратированного диоксида кремния, с последующим нагреванием и плавлением смеси и охлаждением полученного расплава (например, см. патентный документ 3). Независимо от этого сообщалось о способе плавления с экструзией смеси, содержащей итраконазол и водорастворимый полимер, и последующего растирания смеси, полученной с помощью плавления с экструзией (например, см. патентный документ 4).
(B) Способ растворения
Способ растворения представляет собой способ растворения лекарственного вещества и носителя, который является водорастворимым полимером, в растворителе, таком как органический растворитель, и последующего выпаривания растворителя с получением твердой дисперсии. Считается, что растворимость и биодоступность могут быть улучшены, так как лекарственное вещество, плохо растворимое в воде, растворяется в растворителе, и в результате этого лекарственное вещество становится аморфным и диспергированным в носителе, как таковом (например, см. патентный документ 5).
В качестве конкретного примера известен так называемый способ распылительной сушки, при котором жидкость, содержащая растворенный нифедипин, который представляет собой лекарственное вещество, плохо растворимое в воде, и полимерный матрикс, такой как поливинилпирролидон, гидроксипропилметилцеллюлоза, метилцеллюлоза, в органическом растворителе, распыляют и высушивают на тонком порошке лактозы и затем гранулируют с водорастворимым полимером, таким как гидроксипропилцеллюлоза, и в результате этого получают твердую дисперсию (например, см. патентные документы 6 и 7).
Сообщалось также, что лекарственное вещество, плохо растворимое в воде, такое как циклогептадины, и водорастворимый полимер и т.п., такой как поливинилпирролидон, гидроксипропилметилцеллюлоза и гидроксипропилцеллюлоза, растворяют в системе вода/спирт и затем распыляют и гранулируют на лактозе и в результате этого получают твердую дисперсию (например, см. патентный документ 5).
Сообщалось также, что «в отношении конкретного лекарственного вещества, плохо растворимого в воде, известны некоторые способы, при которых лекарственное вещество растворяют в органическом растворителе и смешивают с неорганическим пористым веществом или полимерным веществом, и затем растворитель выпаривают, давая тем самым лекарственному веществу адсорбироваться на неорганическом пористом веществе или диспергироваться в полимерном веществе. Такие способы, однако, не могут применяться ко всем плохо растворимым лекарственным веществам и, кроме того, физические свойства плохо растворимого лекарственного вещества должны быть подробно проверены так, чтобы определить наиболее подходящие вещества с помощью проб и ошибок.» (например, см. патентный документ 8).
Известны также фармацевтическая композиция с улучшенной растворимостью и всасываемостью и способ ее получения, придающие возможность 3-бис-(4-метоксифенил)метилен-2-индолинону становиться аморфным в присутствии полимерного вещества и/или неорганического пористого вещества, и, кроме того, в качестве конкретных способов получения известны также способ получения аморфного продукта с помощью метода нагревания-сплавления или метода растворения с применением TAS-301 в качестве неорганического пористого вещества и способ получения аморфного продукта с помощью метода с использованием полимерного вещества. Однако техническая задача одновременного применения как полимерного вещества, так и неорганического пористого вещества, совсем не была специально известна (например, см. патентный документ 8).
(C) Носитель для твердой дисперсии
Существует два типа носителей для твердой дисперсии, т.е. полимерное вещество и неорганическое пористое вещество.
В качестве полимерного вещества может быть использовано такое, которое может растворяться в воде или в слабо основном или сильно основном буфере и является фармацевтически приемлемым, но его тип конкретно не ограничивается. Например, могут применяться гидроксипропилметилцеллюлоза (Shin-Etsu Chemical: торговая марка TC-5), гидроксипропилцеллюлоза, фталат гидроксипропилметилцеллюлозы, сукцинат гидроксипропилметилцеллюлозы ацетата, метилцеллюлоза, карбоксиметилэтилцеллюлоза, поливинилпирролидон (BASF AG: торговая марка Colidone), полиэтиленгликоль, сополимер этилакрилат-метилметакрилат или сополимер метакриловой кислоты или их смеси (например, см. патентный документ 8).
С другой стороны, неорганическое пористое вещество представляет собой мелкие частицы или порошок, имеющие ряд тонких пор, и оно особенно не ограничивается до тех пор, пока оно является стабильным при нагревании до температуры плавления активного ингредиента, и, например, применяются силикат кальция, легкая безводная кремниевая кислота, силикат магния, алюмосиликат магния, алюмометасиликат магния, силикат алюмомагния, синтетический силикат алюминия, гидратированный диоксид кремния и т.п. Размер частиц составляет от 0,01 мкм до 100 мкм и в среднем от 0,1 до 10 мкм.
Количество применяемого полимерного вещества и/или неорганического пористого вещества особенно не ограничивается и варьируется в зависимости от типа применяемого лекарственного вещества и носителя, но считается, что во многих случаях вещество удобно использовать в количестве, 0,5-5-кратном от лекарственного вещества по массе (например, см. патентный документ 8).
Кроме того, известны составы, содержащие в смеси гидрофобный наполнитель, стабилизирующий агент и разрыхляющий агент.
Например, известны гранулированные частицы, отличающиеся тем, что содержат (a) твердый раствор аморфного и фармацевтически активного лекарственного вещества, которое является кристаллическим в нормальных условиях и слегка водорастворимым при давлении окружающей среды и температуре окружающей среды, и фармацевтически приемлемого гидрофобного наполнителя, (b) стабилизирующий агент, включая полиэтиленгликоль, сахар, сорбит, маннит, поливинилпирролидон или один или более эфиров целлюлозы, и (c) разрыхляющий агент, включая натриевую соль кроскармеллозы, крахмалгликолят натрия, кросповидон или поперечно сшитый полиакрилат (например, см. патентные документы 9 и 10).
(D) Соотношение смешиваемых лекарственных веществ и носителя в твердой дисперсии
Что касается отношения лекарственного вещества и матрикса (носителя) в твердой дисперсии, сообщалось, например, что в случае нифедипина, который представляет собой один из антагонистов кальция, обычно применяемый для профилактики и лечения стенокардии и гипертензии, отношение полимерного вещества (гидроксипропилметилцеллюлозы) к лекарственному веществу (нифедипину) составляет обычно от 1,5 до 3 частей по массе. Причина выбора такого соотношения смеси заключается в том, что, если смешиваемое количество матрикса составляет не более 1 массовой части на 1 массовую часть нифедипина, композиция в форме твердой дисперсии не может быть получена, а в случае 7 частей по массе или более объем композиции увеличивается и состав, получаемый с помощью применения этого соотношения, является недопустимо большим по объему (например, см. патентный документ 11).
Указанный выше способ получения твердой дисперсии является прекрасным способом, но даже этот способ для твердой дисперсии не является абсолютным и не всегда обеспечивает аморфное вещество, и в результате может не увеличивать скорость растворения лекарственного вещества. Например, некоторые параметры, такие как взаимодействие между полимером и активным ингредиентом, их соотношения и применяемый способ производства влияют на химические и физические характеристики полученной твердой дисперсии. В этом отношении существует сообщение о том, что необходимо выбирать как полимер, так и применяемые условия для конкретного активного ингредиента, соответственно, для того, чтобы получить дисперсию, которая осуществит превращение в аморфную форму и сохранит аморфную форму продукта (например, см. патентный документ 12).
Кроме того, когда применяется либо указанный выше способ сплавления, либо способ растворения, полученная этим способом твердая дисперсия должна быть измельчена, просеяна и смешана с другими веществами, как это требуется, и преобразована в состав, такой как гранула или таблетка (например, см. патентный документ 13). В частности, способ растворения может приводить к пленкообразному дисперсному продукту в зависимости от условий получения, и в этом случае необходимо порезать пленку на кусочки.
4-4. Стабильность
Стабильность состава представляет собой один из важных факторов обеспечения эффективности и качества фармацевтического продукта.
При рассмотрении заявки на фармацевтический продукт тесты на стабильность, такие как тест на длительную сохранность, тест на ускорение и жесткий тест лекарственного вещества и его состава, требуются для того, чтобы получить информацию, необходимую для определения способа консервации и периода оценки качества фармацевтического продукта.
Обычно химическое вещество является более стабильным в кристаллическом состоянии, чем в аморфном состоянии. С точки зрения растворимости, однако, проблема состоит в том, что лекарственное вещество, которое образует более стабильный кристалл, более трудно растворить.
2. MTP
Примеры ингибиторов абсорбции липидов, в частности веществ, ингибирующих MTP, описываются ниже в качестве примера лекарственного вещества, плохо растворимого в воде.
MTP экспрессируется как в печени, так и в тонком кишечнике, и представляет собой транспортный белок, катализирующий миграцию триглицеридов, эфиров холестерина и фосфатидилхолина между малым монослоем цитоплазматических мембран и участвующий в образовании липопротеинов.
Таким образом MTP может не только ввести липиды в Апо B-100, вновь синтезированный в печени, но также вводит липиды в Апо B-48, вновь синтезированный в кишечнике.
Следовательно, каждый будет создавать липидные частицы, обогащенные триглицеридами, такие как ЛОНП (липопротеин очень низкой плотности) и хиломикрон. Таким образом, можно ожидать, что вещество, ингибирующее MTP, и/или вещество, ингибирующее секрецию Апо B, будет снижать уровень ЛНП-c и триглицеридов и обладать эффектом снижения всасывания липидов в кишечнике.
Соответственно, вещество, ингибирующее MTP, и/или вещество, ингибирующее секрецию Апо B, может быть использовано для лечения инсулиннезависимого сахарного диабета, недостаточности коронарных артерий сердца, панкреатита, холестеринемии, гипертриглицеридемии, гиперлипидемии, смешанной дислипидемии, гиперлипидемии после приема пищи, атеросклероза и ожирения.
2-1. MTP и Апо B и липиды крови
Ранее указывалось, что гиперлипидемия, сахарный диабет, гипертензия и т.п. являются факторами риска склероза артерий. Гиперлипидемия относится к состоянию, когда уровень липидов, таких как холестерин, аномально увеличивается в крови, и причины этого включают первичную гиперлипидемию, возникающую в результате генетических аномалий фермента и белка, участвующих в метаболизме липопротеинов низкой плотности (ЛНП), рецепторов липопротеинов и т.п., вторичную гиперлипидемию, происходящую из-за различных типов заболеваний и введения лекарственных веществ, и приобретенную гиперлипидемию, возникающую на основе чрезмерного потребления пищи.
Липиды, поступающие с пищей, поглощаются в тонком кишечнике под действием желчных кислот и поступают в кровь через лимфатический проток в виде хиломикронов. Что касается секретируемого хиломикрона, его триглицеридная (TG) часть разрушается до свободных жирных кислот под действием липопротеинлипазы (LPL), присутствующей в сосудистых капиллярах, и он превращается в остаточный хиломикрон, имеющий высокое содержание сложного эфира холестерина (CE), и захватывается печенью с помощью печеночного рецептора ремнантного хиломикрона. Более того, ремнантный хиломикрон, захваченный печенью, превращается в CE и TG и связывается с аполипопротеином B, синтезируемым на шероховатом эндоплазматическом ретикулуме и образует ЛОНП. Этот ЛОНП переносится в аппарат Гольджи, секретируется из клетки после модификации и превращается в липопротеин промежуточной плотности (ЛПП) под действием LPL, затем в ЛНП под действием печеночной триглицеридлипазы (HTGL), и липид распределяется в периферических тканях.
На присутствие белка, обладающего способностью к транспорту TG и CE в тонком кишечнике и микросомальной фракции печени, указывалось в прошлом во время образования хиломикронов в тонком кишечнике или образования ЛОНП в печени, и белок микросомальной фракции печени быка, т.е. MTP, был выделен и очищен из печени и кишечника Wetterau et al. в 1985 г. (см. непатентный документ 2). Однако этот MTP не привлекал внимание в отношении клинической медицины до появления в 1993 г. сообщения о том, что причиной а-β-липопротеинемии является дефицит MTP. Это означает, что это заболевание характеризуется тем, что хотя не существует аберрации в гене, относящемся к аполипопротеину B, аполипопротеин B почти не определяется в сыворотке, сывороточный холестерин составляет не более 50 мг/дл, сывороточные триглицериды выявляются на предельно низком уровне и, кроме того, в крови совсем не выявляется липопротеин, содержащий аполипопротеин B, такой как хиломикрон, ЛОНП и ЛНП. Это указывает на то, что MTP является белком, необходимым для ассоциации аполипопротеина B с TG и CE и образования ЛОНП и хиломикрона, и что он играет существенную роль в их секреции.
Так как липиды по сути не растворимы в воде, липиды в крови связаны с гидрофильным белком, называемым аполипопротеином, и существуют в виде так называемых липопротеинов. Каждый из ЛОНП, ЛПП, ЛНП или хиломикрона, участвующих в гиперлипидемии, представляет собой липопротеин. MTP присутствует в клетках печени и микросомальной фракции эпидермальных клеток тонкого кишечника и отвечает за транспорт TG и CE в клетку. В печени и в тонком кишечнике как только аполипопротеин B (аполипопротеин B100 в печени и аполипопротеин B48 в тонком кишечнике) синтезируется, TG и CE связываются с соответствующим аполипопротеином B за счет транспортного действия MTP, и образуется ЛОНП или хиломикрон. В результате эти липопротеины выходят из клетки в виде ЛОНП из печени и в виде хиломикрона из тонкого кишечника.
MTP, можно сказать, необходим для создания этого липопротеина. Это значит, что транспорт липидов, таких как TG и CE, к аполипопротеину ингибируется при ингибировании активности MTP, и образование липопротеина ингибируется.
Затем было выяснено, что ЛНП непосредственно участвует в развитии склероза артерий в целом, и ЛНП поступает в эндотелий сосудов и откладывается на межклеточном матриксе сосудистой стенки, где он окисляется и денатурирует, и перекисный липид и денатурированный белок вызывают серию воспалительных реакций, вызывая в результате инвазию макрофагов, отложение и вспенивание липидов, миграцию и пролиферацию гладкомышечных клеток и увеличение внеклеточного матрикса и т.д., и в сосудистой стенке образуется атеросклеротическая бляшка. Следовательно, считается, что профилактика или лечение атеросклероза, заболевания коронарных артерий и гипертензии может быть осуществлено с помощью снижения ЛНП.
Этим способом MTP не может ввести липиды только в Апо B-100, вновь синтезированный в печени, но также вводит липиды в Апо B-48, вновь синтезированный в кишечнике.
Следовательно, можно предположить, что вещество, ингибирующее MTP, и/или вещество, ингибирующее секрецию Апо B, будет ингибировать образование липопротеинов, таких как хиломикрон, ЛОНП, ЛНП, снижать в плазме уровень ЛНП-c и триглицеридов и, кроме этого, снижать поглощение липидов в кишечнике и, таким образом, предполагается, что оно может служить в качестве нового типа профилактического или терапевтического агента для гиперлипидемии, атеросклероза, заболевания коронарных артерий, сахарного диабета, ожирения или гипертензии и дополнительно в качестве профилактического или терапевтического агента для панкреатита, холестеринемии, гипертриглицеридемии.
По мере развития разработки ингибиторов MTP указывалось на то, что хотя вещество, ингибирующее MTP, оказывало эффект в отношении снижения липидов в крови, оно обладало способностью вызывать ожирение печени (жировое перерождение печени), и приходилось беспокоиться о возникновении гепатотоксичности. Следовательно, если MTP только в тонком кишечнике может быть избирательно и немедленно ингибирован перед тем, как он достигнет печени, уровень триглицеридов и холестерин крови может быть существенно снижен, без возникновения побочных эффектов, таких как ожирение печени.
В этих условиях весьма желателен новый ингибитор MTP без побочных эффектов, таких как ожирение печени, и улучшенный состав на его основе.
2-2. Вещество, ингибирующее MTP
В виде вещества, ингибирующего MTP, и/или ингибитора секреции Апо B, как указано выше, особенно в виде вещества, ингибирующего MTP, уже известны следующие вещества.
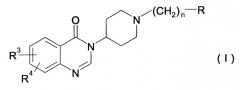
(A) Следующие 3-пиперидил-4-оксохиназолиновые производные описаны в выложенном патенте Японии, публикация No. 11-228569 (см. патентный документ 14).
В этой формуле R имеет формулу (i):
где R1 и R2 могут быть одинаковыми или различными и каждый представляет собой атом водорода; низшую алкильную группу, имеющую от 1 до 4 углеродных атомов; аралкильную группу; бензоильную группу; циклоалкильную группу, имеющую от 3 до 7 углеродных атомов; арильную группу; или гетероарильную группу, содержащую от 1 до 3 гетероатомов, выбранных из атома азота, атома серы и атома кислорода, где циклоалкильная группа, арильная группа или гетероарильная группа могут быть замещены от 1 до 3 заместителями, выбранными из атома галогена; низшей алкильной группы, имеющей от 1 до 4 углеродных атомов; низшей галогеналкильной группы, имеющей от 1 до 4 углеродных атомов; нитрогруппы; низшей алкоксигруппы, имеющей от 1 до 4 углеродных атомов; аминогруппы; аминогруппы, замещенной низшей алкильной группой, имеющей от 1 до 4 углеродных атомов; гидроксильной группой; феноксигруппой; и сульфогруппой, и, по меньшей мере, один из R1 и R2 не является атомом водорода; или формулу (ii):
где A и B могут быть одинаковыми или различными и каждый представляет собой ароматическое углеводородное кольцо; ароматический гетероцикл, содержащий от 1 до 3 гетероатомов, выбранных из атома азота, атома серы и атома кислорода; циклоалкановое кольцо, имеющее от 3 до 7 углеродных атомов; или циклоалкеновое кольцо, имеющее от 5 до 7 углеродных атомов, где ароматическое углеводородное кольцо, ароматический гетероцикл, циклоалкановое кольцо или циклоалкеновое кольцо могут быть замещены от 1 до 3 заместителями, выбранными из атома галогена; низшей алкильной группы, имеющей от 1 до 4 углеродных атомов; низшей галогеналкильной группы, имеющей от 1 до 4 углеродных атомов; гидроксильной группы; нитрогруппы; низшей алкоксигруппы, имеющей от 1 до 4 углеродных атомов; аминогруппы; аминогруппы, замещенной низшей алкильной группой, имеющей от 1 до 4 углеродных атомов; и сульфогруппы), и X представляет собой простую связь; низшую алкильную группу с линейной или разветвленной цепью, имеющую от 1 до 4 углеродных атомов; низшую алкениленовую группу с линейной или разветвленной цепью, имеющую от 2 до 4 углеродных атомов, где низшая алкильная группа или низшая алкениленовая группа могут быть замещены группой, выбранной из атома галогена; гидроксильной группы; нитрогруппы; низшей алкоксигруппы, имеющей от 1 до 4 углеродных атомов; аминогруппы; и сульфогруппы; атом кислорода; атом серы; иминогруппу, которая может быть замещена низшей алкильной группой, имеющей от 1 до 4 углеродных атомов; карбонильную группу; -O-Z-; -Z-O-; -S-Z-; -Z-S-; -NH-Z-; -NR5-Z-; -Z-NH-; или -Z-NR5-, где Z представляет собой низшую алкильную группу, имеющую от 1 до 4 углеродных атомов; или карбонильную группу, и R5 представляет собой низшую алкильную группу, имеющую от 1 до 4 углеродных атомов, и Y, который представляет собой простую связь; низшую алкильную группу с линейной или разветвленной цепью, имеющую от 1 до 4 углеродных атомов; или карбонильную группу, n является целым числом, выбранным от 1 до 4; R3 и R4 могут быть одинаковыми или различными, и каждый представляет собой атом водорода; низшую алкильную группу, имеющую от 1 до 4 углеродных атомов; атом галогена; низшую галогеналкильную группу, имеющую от 1 до 4 углеродных атомов; гидроксильную группу; аминогруппу; или нитрогруппу.
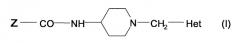
(B) Вещество, ингибирующее MTP, состоящее из бензамидного соединения, обладающего пиперидиновым кольцом, как указано ниже, описывается в национальной публикации международной патентной заявки No. 2004-514676 (WO 2002/042291) (см. патентный документ 15).
В формуле Z представляет собой бифенил, который может быть необязательно замещен одной или более группами заместителей, выбранными из тригалогенметила и тригалогенметокси в положении 2', положении 3', положении 4', положении 5' и положении 6', и Het представляет собой хинолил, или хиноксалил, или пиридил, которые могут быть необязательно замещены одной или более группами заместителей, выбранными из галогена, циано, нитро, C1-C6 алкила, C6-C12 арила,
C1-C6 алкокси, гидроксила, C1-C6 тиоалкокси, карбоксила и C1-C6 алкоксикарбонила.
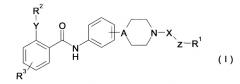
(C) Вещество, ингибирующее MTP, состоящее из бензамидного производного, представленного следующей формулой, описывается в национальной публикации международной патентной заявки No. 2003-535900 (WO 01/097810) (см. патентный документ 16).
В формуле
A представляет собой N или CH;
X выбран из следующих групп: (i) -C1-6 алкилена-, необязательно содержащего одну или две двойных связи и необязательно замещенного одним или более гидрокси,
C1-6 алкилом, C1-6 алкокси, C1-6 ацилом или C1-6 ацилокси группами, (ii) оксо, сульфонила, тиоксо, (iii) -C1-6 алкиленкарбонила-, -C1-6 алкиленсульфонила-, -C1-6 алкилентиоксо-, (iv) -C2-6 алкиленокси-, -C2-6 алкилентио-, -C2-6 алкилен (N-H или N-C1-6 алкил)амино-, (v) -C1-6 алкиленкарбокси-, -C1-6 алкилентиоамидо-, -C1-6 алкилен (N-H или N-C1-6 алкил)карбоксамидо- и (vi) -C2-6 алкиленоксикарбонила-, -C2-6 алкилентиокарбонила-, -C2-6 алкилен (N-H или N-C1-6 алкил)аминокарбонила-;
Z представляет собой прямую связь или -C1-6 алкилен-, необязательно содержащий одну двойную связь и необязательно замещенный одним или более гидрокси, C1-6 алкилом, C1-6 алкокси, C1-6 ацилом или C1-6 ацилокси группами;
R1 выбран из следующих групп: (i) водорода, C1-3 перфторалкила, (ii) C6-10 арила,
C3-8 циклоалкила и их конденсированных бензопроизводных, C7-10 полициклоалкила, C4-8 циклоалкенила, C7-10 полициклоалкенила, (iii) гетероциклила, выбранного из группы, состоящей из моноциклических радикалов и конденсированных полициклических радикалов, где указанные радикалы содержат суммарно от 5 до 14 атомов кольца, где указанные радикалы содержат суммарно от 1-4 гетероатомов кольца, независимо выбранных из кислорода, азота и серы, и где индивидуальные кольца указанных радикалов могут быть независимо насыщенными, частично ненасыщенными или ароматическими, и (iv) где либо X представляет собой C1-6 алкилен и Z представляет собой прямую связь, либо Z представляет собой C1-6 алкилен, R1 дополнительно может представлять собой галоген, циано, нитро или C1-6 ацильную группу,
где когда R1 содержит одно или более колец, указанные кольца, каждое, могут независимо иметь от 0 до 4 заместителей, независимо выбранных из (i) галогена, гидрокси, циано, формила, C1-6 алкилсульфониламино, (ii) C1-6 алкила, C3-8 циклоалкила, C1-3 перфторалкила, (iii) C1-6 алкокси, метилендиокси, C1-3 перфторалкокси, C1-6 алкилтио, (iv) амино, C1-6 алкиламино, ди-C1-6 алкиламино, (v) фенила, фенокси, фенилтио, галогенфенилтио, бензила, бензилокси, (vi) гидроксикарбонила, C1-6 алкоксикарбонила, (vii) аминокарбонила, C1-6 алкиламинокарбонила, ди-C1-6 алкиламинокарбонила,
ди-C1-6 алкиламинокарбонил C1-6 алкокси, C1-3 перфторалкиламинокарбонила, (viii) C1-6 ацила, C1-6 ацилокси, C1-6 ацилокси C1-6 алкила, C1-6 ациламино, и (ix) ароматического гетероцикла, состоящего из моноциклических радикалов, где указанные радикалы содержат 5-6 атомов кольца, где указанные радикалы содержат суммарно от 1 до 4 гетероатомов кольца, независимо выбранных из кислорода, азота и серы, и где каждая из указанных гетероциклических групп необязательно замещена одной или более группами, независимо выбранными из галогена, C1-4 алкила, C1-4 алкокси, C1-3 перфторалкила и C1-3 перфторалкокси;
Y представляет собой прямую или окси связь, -C1-6 алкилен-, -окси C1-6 алкилен- или гетероциклил, содержащий моноциклические радикалы, где указанные радикалы содержат 5 атомов кольца, и где указанные радикалы содержат от 1 до 4 гетероатомов кольца, независимо выбранных из кислорода, азота и серы, и где кольцо может быть независимо насыщенным, частично ненасыщенным или ароматическим;
R2 представляет собой фенил, C3-8 циклоалкил или гетероциклил, состоящий из моноциклических радикалов, где указанные радикалы содержат суммарно от 5 до 6 атомов кольца, где указанные радикалы содержат суммарно от 1 до 4 гетероатомов кольца, независимо выбранных из кислорода, азота и серы, где кольцо может быть независимо насыщенным, частично ненасыщенным или ароматическим, и где каждый R2 необязательно замещен одной или более группами, независимо выбранными из галогена, C1-4 алкила, C1-4 алкокси, C3-8 циклоалкила, C1-3 перфторалкила, C1-3 перфторалкокси, гидроксикарбонила, C1-6 алкоксикарбонила, циано, нитро, C1-4 алкиламиносульфонила; и
R3 представляет собой водород или одну или более групп, независимо выбранных из галогена, C1-4 алкила, C1-4 алкокси, C1-3 перфторалкила или C1-3 перфторалкокси.
(D) Вещество, ингибирующее MTP, состоящее из замещенного пиперазинового производного, представленного следующей формулой, описывается в национальной публикации международной патентной заявки No. 2003-521484 (WO 01/047898) (см. патентный документ 17).
В формуле m представляет собой число 2 или 3, n представляет собой число 1, 2, 3, 4 или 5, X представляет собой углерод-углеродную связь, атом кислорода, метилен, этилен, имино или N-(C1-3-алкил)иминогруппу, Ra представляет собой би- или трициклический ароматический углеводород, где ангулярная метиновая группа может быть замещена атомом азота, би- или трициклический гетероароматический углеводород, связанный с группой пиперазино через атом углерода, состоящий из 5-членного гетероарильного кольца, содержащего один или два атома азота, и циклопентадиенильного кольца, конденсированного через виниленовую группу, где дополнительно метиновая группа может быть замещена атомом азота, и/или ангулярная метиновая группа может быть замещена атомом азота, 5-членное гетероарильное кольцо, которое содержит иминогруппу, необязательно замещенную
C1-3-алкилом, фенил-C1-3-алкилом, фенилом, пиридинилом, пиридазинилом, пиримидинилом или пиразинильной группой, или атомом кислорода или серы и фенилом, или 6-членное гетероарильное кольцо, конденсированное через одну или две доступных виниленовых группы, содержащее один, два или три атома азота, где конденсированные кольца могут быть одинаковыми или различными, или нафтильное кольцо, конденсированное через одну или две доступные виниленовые группы, где дополнительно в бициклической или трициклической группе, образован