Производные пиримидина, обладающие ингибирующим действием в отношении 11b-hsd1
Иллюстрации
Показать всеИзобретение относится к новым соединениям формулы (I) и их фармацевтически приемлемым солям и эфирам, обладающим ингибирующим действием в отношении фермента 11бета-гидроксистероиддегидрогеназы 1 (11bHSD1). Соединения могут быть использованы для лечения и профилактики заболеваний, связанных с активностью указанного фермента, таких как диабет, ожирение, заболеваний связанных с приемом пищи, дислипидемии и гипертензии. В общей формуле (I)
R1 представляет собой метил, этил, циклопропил, циклобутил, изопропил, трет-бутил, метоксиметил, циклопропилметоксиметил, 2-метилтиазолил, морфолинилметил или фенил; R2 представляет собой водород, С1-4алкил или фенил;
R3 представляет собой водород, С1-4алкил или фенил; R4 представляет собой фенил, нафтил, тиофенил, хинолил или пиперидил, где фенил, нафтил, тиофенил, хинолил и пиперидил необязательно замещены от 1-3 заместителями, независимо выбранными из С1-4алкила, галогена, С1-4алкокси, циано, трифторметила, фенила, фенил-С1-4алкила, фенилокси, оксазолила и пиридинила; R5 представляет собой водород, C1-4алкил, фенил-С1-4алкил, С3-6циклоалкил-С1-4алкил или аминокарбонил-С1-4алкил. 2 н. и 15 з.п. ф-лы, 1 табл.
Реферат
Настоящее изобретение относится к новым производным пиримидина, пригодным в качестве ингибиторов 11b-HSD1 (T2D).
Настоящее изобретение относится, в частности, к соединениям формулы I и к их фармацевтически приемлемым солям и эфирам:
где R1 представляет собой алкил, циклоалкил, циклоалкилалкокси, алкоксиалкил, циклоалкилалкоксиалкил, гетероциклил, гетероциклилалкил, арил, арилалкил, арилоксиалкил, амино или аминоалкил;
R2 представляет собой водород, алкил или арил;
R3 представляет собой водород, алкил или арил;
R4 представляет собой фенил, нафтил, тиофенил, хинолил, пиперидил, морфолил или тиоморфолил, где фенил, нафтил, тиофенил, хинолил, пиперидил, морфолил и тиоморфолил необязательно замещены одним или несколькими заместителями, независимо выбранными из алкила, циклоалкила, галогена, алкокси, циано, трифторметила, арила, арилалкила, арилокси, оксазолила, пиридинила, пиримидинила, пиразолила, имидазолила и тиазолила;
R5 представляет собой водород, алкил, аралкил, циклоалкилалкил или аминокарбонилалкил
и где исключаются
N-(2,6-диметил-4-пиримидинил)бензолсульфонамид;
2-хлор-N-(2-метил-4-пиримидинил)-п-толуолсульфонамид;
N-(2-(диметиламино)-6-метил-5-пропил-4-пиримидинил)бензолсульфонамид и 2,4,5-трихлор-N-(2,6-диметил-4-пиримидинил)бензолсульфонамид.
Глюкокортикоиды (кортизол у человека, кортикостерон у мышей и крыс) представляют собой важный класс адренокортикостероидов, которые регулируют множество метаболических и гомеостатических процессов и образуют ключевой компонент реакции на стресс. Глюкокортикоиды действуют посредством внутриклеточных глюкокортикоидных рецепторов и, в некоторых тканях, минералокортикоидных рецепторов; при этом оба вида относятся к факторам транскрипции ядра. Действие глюкокортикоидов на ткани мишени зависит не только от циркулирующих концентраций стероида и клеточной экспрессии рецепторов, но также и от внутриклеточных ферментов, которые в основном определяют, в какой степени глюкокортикоиды получают доступ к рецепторам в активных формах. 11бета-гидроксистероиддегидрогеназы (11бета-HSD) катализируют взаимное превращение в основном активного 11-гидроксиглюкокортикоида (кортизол у человека) в его неактивные 11-кетометаболиты (кортизон у человека).
Фермент 11бета-гидроксистероиддегидрогеназа типа 1 (11бета-HSD1) взаимопревращается из неактивных в активные глюкокортикоиды, тем самым играя основную роль в локальной модуляции концентрации клеточного агониста и таким образом вызывая активацию кортикостероидных рецепторов в тканях-мишенях. В недавнем исследовании, проведенном F.Hoffmann-La Roche, были проанализированы различия в экспрессии гена у худощавых и полных людей, используя технологию генного набора для того, чтобы идентифицировать специфические изменения в экспрессии гена, которая может быть связана с резистентностью к инсулину или измененным метаболизмом. Это исследование показало, что мРНК для 11бета-HSD1 приблизительно в два раза сильнее регулируется в жировой ткани у полных людей. Более того, сверхэкспрессия 11бета-НSD1 в адипоцитах мыши приводит к висцеральному ожирению и к синдрому-Х подобного фенотипа (Masuzaki H. и др., Science, 2001, Dec 7; 294 (5549), сс. 2166-70). Вместе с этим, эти данные убедительно показывают важную роль бетаHSD1 в индукции ожирения и ослаблении гомеостаза глюкозы и липидных параметров. Таким образом, селективное ингибирование этого фермента могло бы понизить уровни глюкозы в крови у пациентов с диабетом типа 2, нормализовать повышенные липидные параметры и/или понизить вес полных пациентов.
Первым фармакологическим указанием на то, что ингибирование 11бета-HSD1 у человека может иметь благоприятные эффекты, были получены с помощью карбеноксолона, противоязвенного лекарственного препарата, который ингибирует как 11бета-HSD1, так и связанный с ним фермент 11бета-HSD2. Лечение карбеноксолоном приводит к увеличению чувствительности к инсулину, что указывает на то, что ингибирование 11бета-HSD1 может уменьшать уровни кортизола в клетке и, следовательно, уменьшать некоторые его вредные воздействия (Walker и др., J. Clin. Endocrinol. Metab., 1995; 80, сс.3155-3159).
11бета-HSD1 экспрессируется во многих тканях, включая печень, жировую ткань, гладкую мускулатуру, поджелудочную железу и головной мозг. Его активность зависит от НАДФ(Н) и он имеет относительно низкое сродство со своим субстратом (по сравнению с 11бета-HSD2). 11бета-HSD1 в гомогенатах ткани и после очистки является двунаправленным, проявляя реакции как 11бетадегидрогеназы, так и 11бетаредуктазы, с повышенной устойчивостью к активности дегидрогеназы (P.M.Stewart и Z.S.Krozowski, Vitam. Horm., 1999, 57, сс.249-324). Однако, когда активность фермента проверяли на интактных клетках, преобладала активность 11бетаредуктазы, которая вырабатывает активные глюкокортикоиды из инертных 11-кетоформ. Такая выработка глюкокортикоида будет повышать эффективные внутриклеточные уровни глюкокортикоида, тем самым повышая активность глюкокортикоида. Это и есть повышение клеточной концентрации кортизола, которое может привести к повышению выработки глюкозы в печени, дифференциации адипоцитов и резистентности к инсулину.
Ингибирование 11бета-НSD1 должно не только уменьшать типичные симптомы синдрома Х/диабетов, а также быть безопасным и не обладать сильными побочными эффектами. Исследования неспецифического ингибитора карбеноксолона подчеркивают важность разработки специфических ингибиторов 11бета-HSD1. Ингибирование фермента 11бета-НSD2 трудно осуществляется и приводит к повышению кровяного давления. В отличие от этого, ингибирование 11бета-HSD1 должно хорошо переноситься, поскольку было обнаружено, что 11бета-HSD1 обработанные мыши являются здоровыми и устойчивыми к гипергликемии, вызванной ожирением или стрессом (Kotelevtsev Y. и др., Рrос Natl Acad Sci U S A, 1997, Dec 23; 94 (26), сс.14924-9). Аналогично, при голодании эти мыши имеют пониженную активацию ключевых ферментов печени, которые вовлечены в глюконеогенез. Кроме того, эти мыши имеют повышенные липидные и липопротеиновые профили, предполагающие, что ингибирование HSD1 может быть высоко эффективным и безопасным. Последние исследования показали, что ингибиторы 11бета-HSD1 также могут быть полезны для снижения высокого кровяного давления (Masuzaki H. и др., J Clin Invest., 2003, July; 112(1), сс.83-90; Rauz S. и др., QJM, 2003, July; 96(7), сс.481-90) для улучшения когнитивной способности (Sandeep TC. и др., Рrос Natl Acad Sci USА, 2004, Apr. 27; 101 (17), сс.6734-9) или для устранения нарушений, связанных с болезнью Альцгеймера. Вместе с этим, ингибирование 11бета-HSD1 может быть безопасным и эффективным подходом для лечения симптомов диабетов, ожирения и других заболеваний.
Соединения формулы I и их фармацевтически приемлемые соли и эфиры являются новыми и имеют ценные фармакологические свойства. В частности, они являются ингибиторами 11b-HSD1 (T2D) и они проявляют селективность в отношении фермента, связанного с 11бета-НSD2. Следовательно, соединения, которые являются специфическими ингибиторами 11бета-HSD1 (T2D) представляют подход, например, к снижению уровней глюкозы в крови и нормализации липидных параметров у пациентов с диабетом типа 2 путем модулирования локальной концентрации активного глюкокортикоида кортизола в ткани-мишени (печень, жировая ткань).
Соединения настоящего изобретения могут использоваться для профилактики и/или лечения метаболических заболеваний, ожирения, дислипидемии, гипертензии и/или диабетов, особенно диабетов типа 2.
Соединения настоящего изобретения могут также использоваться для профилактики и/или лечения высокого глазного давления, когнитивной способности, болезни Альцгеймера и/или нейродегенерации.
Объектами настоящего изобретения являются соединения формулы I и их указанные выше соли и эфиры как таковые и их применение в качестве терапевтически активных веществ, способ получения указанных соединений, промежуточные соединения, фармацевтические композиции, лекарственные средства, содержащие указанные соединения, их фармацевтически приемлемые соли и эфиры, применение указанных соединений, эфиров и солей для профилактики и/или лечения заболеваний, особенно для лечения или профилактики заболеваний, связанных с приемом пищи, ожирения, дислипидемии, гипертензии и/или диабетов, особенно диабетов типа 2, и применение указанных соединений, солей и эфиров для изготовления лекарственных средств для лечения или профилактики метаболических заболеваний, ожирения, дислипидемии, гипертензии и/или диабетов, особенно диабетов типа 2.
Соединения настоящего изобретения могут также объединяться с агонистами PPAR (альфа, гамма, дельта), DHEA (дегидроэпиандростерон), ингибиторами DPPIV, инсулином и/или ингибиторами липазы, особенно орлистатом.
В настоящем описании термин "алкил", отдельно или в комбинации, обозначает линейную или разветвленную алкильную группу, содержащую от 1 до 8 атомов углерода, предпочтительно линейную или разветвленную алкильную группу, содержащую от 1 до 6 атомов углерода, и особенно предпочтительно линейную или разветвленную алкильную группу, содержащую от 1 до 4 атомов углерода. Примерами линейных и разветвленных C1-C8 алкильных групп являются метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, изомеры пентила, изомеры гексила, изомеры гептила и изомеры октила, предпочтительно метил и этил и наиболее предпочтительно метил.
Термин "циклоалкил", отдельно или в комбинации, обозначает циклоалкильное кольцо, содержащее от 3 до 8 атомов углерода, и предпочтительно циклоалкильное кольцо, содержащее от 3 до 6 атомов углерода. Примерами С3-C8 циклоалкила являются циклопропил, метилциклопропил, диметилциклопропил, циклобутил, метилциклобутил, циклопентил, метилциклопентил, циклогексил, метилциклогексил, диметилциклогексил, циклогептил и циклооктил, предпочтительно циклопропил.
Термин "алкокси", отдельно или в комбинации, обозначает группу формулы алкил-O-, в которой термин "алкил" имеет описанное ранее значение, такой как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси и трет-бутокси, предпочтительно метокси и этокси и наиболее предпочтительно метокси.
Термин "арил", отдельно или в комбинации, обозначает фенильную или нафтильную группу, предпочтительно фенильную группу, которая необязательно замещена одним или несколькими заместителями, предпочтительно 1-3, каждый из которых независимо выбран из галогена, трифторметила, трифторметокси, амино, алкила, алкокси, алкилкарбонила, циано, карбамоила, алкоксикарбамоила, метилендиокси, карбокси, алкоксикарбонила, аминокарбонила, алкиламинокарбонила, диалкиламинокарбонила, гидрокси, нитро, алкил-SO2-, амино-SO2-, циклоалкила и им подобных. Предпочтительным является фенил или нафтил, особенно фенил, необязательно замещенный 1-3, предпочтительно одним или двумя, заместителями, независимо выбранными из алкила, галогена, алкокси, трифторметокси, нитро и трифторметила. Особенно предпочтительным является фенил.
Термин "арилокси", отдельно или в комбинации, обозначает группу арил-O-, в которой термин "арил" имеет описанное ранее значение.
Термин "аралкил", отдельно или в комбинации, обозначает арилалкильную группу, в которой термины "арил" и "алкил" имеют описанные ранее значения.
Термин "гетероциклил", отдельно или в комбинации, обозначает насыщенный, частично ненасыщенный или ароматический 5-10-членный гетероцикл, который содержит один или несколько гетероатомов, выбранных из азота, кислорода и серы. При необходимости, он может быть замещен в одном или нескольких атомах углерода, например, галогеном, алкилом, алкокси, оксо и т.д. и/или на вторичном атоме азота (то есть -NH-) алкилом, циклоалкилом, аралкоксикарбонилом, алканоилом, фенилом или фенилалкилом, или на третичном атоме азота (то есть =N-) оксидо, причем галоген, алкил, циклоалкил и алкокси являются предпочтительными. Примерами таких гетероциклильных групп являются пирролидинил, пиперидинил, пиперазинил, морфолинил, тиоморфолинил, пиразолил, имидазолил (например, имидазол-4-ил и 1-бензилоксикарбонилимидазол-4-ил), пиразолил, пиридил, пиразинил, пиримидинил, гексагидропиримидинил, фурил, тиенил, тиазолил, оксазолил, индолил (например, 2-индолил), хинолил (например, 2-хинолил, 3-хинолил и 1-оксидо-2-хинолил), изохинолил (например, 1-изохинолил и 3-изохинолил), тетрагидрохинолил (например, 1,2,3,4-тетрагидро-2-хинолил), 1,2,3,4-тетрагидроизохинолил (например, 1,2,3,4-тетрагидро-1-оксоизохинолил) и хиноксалинил. Предпочтительными примерами являются тиофенил, хинолил, пиперидил, морфолил, тиоморфолил, оксазолил, пиридинил, пиримидинил, пиразолил, имидазолил и тиазолил.
Термин "амино", отдельно или в комбинации, обозначает первичную, вторичную или третичную аминогруппу, присоединенную через атом азота, где вторичная аминогруппа имеет алкильный или циклоалкильный заместитель и третичная аминогруппа имеет два одинаковых или различных алкильных или циклоалкильных заместителя, или два заместителя у атома азота вместе образуют цикл, такие как, например, -NH2, метиламино, этиламино, диметиламино, диэтиламино, метилэтиламино, пирролидин-1-ил или пиперидино и т.д., предпочтительно первичный амино, диметиламино и диэтиламино и особенно диметиламино.
Термин "галоген", отдельно или в комбинации, обозначает фтор, хлор, бром или йод, предпочтительно фтор, хлор или бром.
Термин "карбонил", отдельно или в комбинации, обозначает группу - С(O)-.
Термин "окси", отдельно или в комбинации, обозначает группу -О-.
Термин "нитро", отдельно или в комбинации, обозначает группу -NO2.
Термин "циано", отдельно или в комбинации, обозначает группу -CN.
Термин "фармацевтически приемлемые соли" обозначает те соли, которые сохраняют биологическую эффективность и свойства свободных оснований или свободных кислот, которые не являются биологически или иначе неприемлемыми. Соли образуются с неорганическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и им подобные, предпочтительно хлористоводородная кислота, и органическими кислотами, такими как уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, малеиновая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота, N-ацетилцистеин и им подобные. Помимо этого, соли могут быть получены путем добавления неорганического основания или органического основания к свободной кислоте. Соли, полученные из неорганического основания, включают, но не ограничиваются ими, соли с натрием, калием, литием, аммонием, кальцием, магнием и им подобным. Соли, полученные из органических оснований, включают, но не ограничиваются ими, соли с первичными, вторичными и третичными аминами, замещенными аминами, включая природные замещенные амины, циклическими аминами и основными ионообменными смолами, такими как изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин, этаноламин, лизин, аргинин, N-этилпиперидин, пиперидин, полиминовые смолы и им подобные. Соединение формулы I также может присутствовать в форме цвиттерионов. Особенно предпочтительными фармацевтически приемлемыми солями соединений формулы I являются гидрохлориды.
Соединения формулы I также могут быть сольватированы, например гидратированы. Сольватация может осуществляться в ходе способа получения или может происходить, например, вследствие гигроскопических свойств первоначально безводного соединения формулы I (гидратация). Термин фармацевтически приемлемые соли также включает физиологически приемлемые сольваты.
"Фармацевтически приемлемые эфиры" обозначают, что из соединений общей формулы (I) могут быть получены производные по функциональным группам с получением производных, которые способны превращаться обратно в исходные соединения in vivo. Примеры таких соединений включают физиологически приемлемые и метаболически лабильные эфирные производные, такие как метоксиметильные эфиры, метилтиометильные эфиры и пивалоилоксиметильные эфиры. Кроме того, любые физиологически приемлемые эквиваленты соединений общей формулы (I), аналогичные метаболически лабильным эфирам, которые способны превращаться в исходные соединения общей формулы (I) in vivo, также входят в объем настоящего изобретения.
Соединения формулы I могут содержать несколько асимметрических центров и могут существовать в форме оптически чистых энантиомеров, смесей энантиомеров, таких как, например, рацематы, оптически чистых диастереоизомеров, смесей диастереоизомеров, диастереоизомерных рацематов или смесей диастереоизомерных рацематов.
Предпочтительными являются соединения формулы I и их фармацевтически приемлемые соли, особенно соединения формулы I.
Предпочтительными являются соединения формулы I, где
R1 представляет собой алкил, циклоалкил, алкоксиалкил, циклоалкилалкоксиалкил, гетероциклил, гетероциклилалкил, арил, арилалкил, арилоксиалкил, амино или аминоалкил;
R2 представляет собой водород или алкил;
R3 представляет собой водород или алкил;
R4 представляет собой фенил, нафтил, тиофенил, хинолил, пиперидил, морфолил или тиоморфолил, где фенил, нафтил, тиофенил, хинолил, пиперидил, морфолил и тиоморфолил необязательно замещены одним или несколькими заместителями, независимо выбранными из алкила, циклоалкила, галогена, алкокси, циано, трифторметила, арила, арилалкила, арилокси, оксазолила, пиридинила, пиримидинила, пиразолила, имидазолила и тиазолила;
R5 представляет собой водород или алкил;
и их фармацевтически приемлемые соли и эфиры
и где исключаются
N-(2,6-диметил-4-пиримидинил)бензолсульфонамид;
2-хлор-N-(2-метил-4-пиримидинил)-п-толуолсульфонамид;
N-(2-(диметиламино)-6-метил-5-пропил-4-пиримидинил)бензолсульфонамид и
2,4,5-трихлор-N-(2,6-диметил-4-пиримидинил)бензолсульфонамид.
Другими предпочтительными являются соединения формулы I, где R1 представляет собой алкил, циклоалкил, алкоксиалкил, циклоалкилалкоксиалкил, гетероциклил, гетероциклилалкил или арил.
Особенно предпочтительными являются соединения формулы I, где R1 представляет собой метил, этил, циклопропил, циклобутил, изопропил, трет-бутил, метоксиметил, циклопропилметоксиметил, 2-метилтиазолил, морфолинилметил или фенил.
Также предпочтительными являются соединения формулы I, где R2 представляет собой водород.
Другим предпочтительным вариантом осуществления настоящего изобретения являются соединения формулы I, где R2 представляет собой метил.
Предпочтительными являются соединения формулы I, где R3 представляет собой водород.
Другим предпочтительным вариантом осуществления настоящего изобретения являются соединения формулы I, где R5 представляет собой водород.
Другими предпочтительными являются соединения формулы I, где R5 представляет собой метил.
Также предпочтительными являются соединения формулы I, где R4 представляет собой фенил, нафтил, тиофенил, хинолил или пиперидил, где фенил, нафтил, тиофенил, хинолил и пиперидил необязательно замещены одним или несколькими, предпочтительно 1-3 заместителями, независимо выбранными из алкила, галогена, алкокси, трифторметила, арила, оксазолила и пиридинила.
Другими предпочтительными являются соединения формулы I, где R4 представляет собой фенил, замещенный одним или несколькими, предпочтительно 1-3 заместителями, независимо выбранными из алкила, циклоалкила, галогена, алкокси, трифторметила, фенила и оксазолила.
Предпочтительными являются соединения формулы I, где R4 представляет собой фенил, нафтил, хинолил или пиперидил.
Также предпочтительными являются соединения формулы I, где R4 представляет собой тиофенил, морфолил или тиоморфолил, где тиофенил, морфолил и тиоморфолил необязательно замещены одним или несколькими, предпочтительно 1 -3 заместителями, независимо выбранными из алкила, циклоалкила, галогена, алкокси, циано, трифторметила, арила, арилалкила, арилокси, оксазолила, пиридинила, пиримидинила, пиразолила, имидазолила и тиазолила.
Примерами предпочтительных соединений формулы (I) являются:
1) 3-хлор-2-метил-N-(2-метилпиримидин-4-ил)бензолсульфонамид;
2) 3-хлор-N-(2-циклопропилпиримидин-4-ил)-2-метилбензолсульфонамид;
3) N-(2-циклопропилпиримидин-4-ил)-2,5-дифторбензолсульфонамид;
4) (2-циклопропилпиримидин-4-ил)амид нафтален-2-сульфоновой кислоты;
5) (2-циклопропилпиримидин-4-ил)амид бифенил-4-сульфоновой кислоты;
6) (2-циклопропилпиримидин-4-ил)амид хинолин-8-сульфоновой кислоты;
7) N-(2-циклопропилпиримидин-4-ил)бензолсульфонамид;
8) N-(2-циклопропилпиримидин-4-ил)-5-фтор-2-метилбензолсульфонамид;
9) N-(2-циклопропилпиримидин-4-ил)-3-метоксибензолсульфонамид;
10) N-(2-циклопропилпиримидин-4-ил)-2-метокси-5-метилбензолсульфонамид;
11) 3-хлор-N-(2-циклопропилпиримидин-4-ил)-4-метоксибензолсульфонамид;
12) 5-хлор-N-(2-циклопропилпиримидин-4-ил)-2-метоксибензолсульфонамид;
13) 5-фтор-N-(2-изопропилпиримидин-4-ил)-2-метилбензолсульфонамид;
14) 3,4-дихлор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
15) N-(2-изопропилпиримидин-4-ил)-4-(1,3-оксазол-5-ил)бензолсульфонамид;
16) 2,4-дихлор-N-(2-изопропилпиримидин-4-ил)-6-метилбензолсульфонамид;
17) 2,3-дихлор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
18) (2-изопропилпиримидин-4-ил)амид 4,5-дихлортиофен-2-сульфоновой кислоты;
19) (2-изопропилпиримидин-4-ил)амид 5-пиридин-2-илтиофен-2-сульфоновой кислоты;
20) 3-хлор-N-(2-изопропилпиримидин-4-ил)-2-метилбензолсульфонамид;
21) N-(2-изопропилпиримидин-4-ил)-3-трифторметилбензолсульфонамид;
22) N-(2-изопропилпиримидин-4-ил)-2-трифторметилбензолсульфонамид;
23) (2-изопропилпиримидин-4-ил)амид 5-хлортиофен-2-сульфоновой кислоты;
24) N-(2-изопропилпиримидин-4-ил)-4-трифторметилбензолсульфонамид;
25) (2-изопропилпиримидин-4-ил)амид пиперидин-1-сульфоновой кислоты;
26) (2-изопропилпиримидин-4-ил)амид нафтален-2-сульфоновой кислоты;
27) (2-изопропилпиримидин-4-ил)амид бифенил-4-сульфоновой кислоты;
28) 2,5-дифтор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
29) N-(2-изопропилпиримидин-4-ил)-3,4-диметоксибензолсульфонамид;
30) N-(2-трет-бутилпиримидин-4-ил)-3,4-дихлорбензолсульфонамид;
31) N-(2-трет-бутилпиримидин-4-ил)-5-фтор-2-метилбензолсульфонамид;
32) (2-трет-бутилпиримидин-4-ил)амид нафтален-2-сульфоновой кислоты;
33) N-(2-трет-бутилпиримидин-4-ил)-2,5-дифторбензолсульфонамид;
34) N-(2-трет-бутилпиримидин-4-ил)-4-(1,3-оксазол-5-ил)бензолсульфонамид;
35) 3-хлор-N-(2-этилпиримидин-4-ил)-2-метилбензолсульфонамид;
36) 2,4-дихлор-N-(2-этилпиримидин-4-ил)-6-метилбензолсульфонамид;
37) 4-хлор-N-(2-этилпиримидин-4-ил)-2,5-диметилбензолсульфонамид;
38) 3-хлор-N-(2-циклобутилпиримидин-4-ил)-2-метилбензолсульфонамид;
39) (2-циклобутилпиримидин-4-ил)амид нафтален-2-сульфоновой кислоты;
40) (2-циклобутилпиримидин-4-ил)амид 5-пиридин-2-илтиофен-2-сульфоновой кислоты;
41) 2,4-дихлор-N-(2-циклобутилпиримидин-4-ил)-6-метилбензолсульфонамид;
42) 3,4-дихлор-N-(2-метоксиметилпиримидин-4-ил)бензолсульфонамид;
43) 3-хлор-N-(2-циклопропилметоксиметилпиримидин-4-ил)-
2-метилбензолсульфонамид;
44) 3-хлор-2-метил-N-(2-морфолин-4-илметилпиримидин-4-ил)бензолсульфонамид;
45) (2,6-диметилпиримидин-4-ил)амид нафтален-2-сульфоновой кислоты;
46) 3-хлор-N-(2-циклопропилпиримидин-4-ил)-2-N-диметилбензолсульфонамид;
47) 3,4-дихлор-N-(2-изопропилпиримидин-4-ил)-N-метилбензолсульфонамид;
48) 3-хлор-2-метил-N-(2-фенилпиримидин-4-ил)бензолсульфонамид и
49) 3-хлор-2-метил-N-[2-(2-метилтиазол-4-ил)пиримидин-4-ил]бензолсульфонамид.
Другими примерами предпочтительных соединений являются:
50) 3-хлор-N-(2-метоксиметилпиримидин-4-ил)-2-метилбензолсульфонамид;
51) (2,5,6-триметилпиримидин-4-ил)амид нафтален-2-сульфоновой кислоты;
52) 4,5-дихлор-2-фтор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
53) 2,4-дифтор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
54) 2-хлор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
55) 4-хлор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
56) 3-хлор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
57) 2,4-дихлор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
58) 2,4-дихлор-N-(2-изопропилпиримидин-4-ил)-5-метилбензолсульфонамид;
59) 2,5-дихлор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
60) (2-изопропилпиримидин-4-ил)амид 3-бром-5-хлортиофен-2-сульфоновой кислоты;
61) 2,4-дихлор-N-(2-циклопропилпиримидин-4-ил)-6-метилбензолсульфонамид;
62) 4-хлор-N-(2-циклопропилпиримидин-4-ил)-2,5-диметилбензолсульфонамид;
63) N-(2-циклопропилпиримидин-4-ил)-2,4-диметоксибензолсульфонамид;
64) 3-хлор-N-(2-циклопентилпиримидин-4-ил)-2-метилбензолсульфонамид;
65) (2-циклопропилпиримидин-4-ил)амид 5-фенилтиофен-2-сульфоновой кислоты;
66) 3-хлор-N-(2-циклопропилметоксипиримидин-4-ил)-2-метилбензолсульфонамид;
67) 2-[(3,4-дихлорбензолсульфонил)-(2-изопропилпиримидин-4-ил)
амино]-N,N-диметилацетамид;
68) N-бензил-3-хлор-N-(2-циклопропилпиримидин-4-ил)-2-метилбензолсульфонамид;
69) 3-хлор-N-циклопропилметил-N-(2-циклопропилпиримидин-4-ил)-2-метилбензолсульфонамид и
70) 3-хлор-2-метил-N-(6-фенилпиримидин-4-ил)бензолсульфонамид.
Примерами особенно предпочтительных соединений формулы (I) являются:
3-хлор-2-метил-N-(2-метилпиримидин-4-ил)бензолсульфонамид;
3-хлор-N-(2-циклопропилпиримидин-4-ил)-2-метилбензолсульфонамид;
N-(2-циклопропилпиримидин-4-ил)-2,5-дифторбензолсульфонамид;
(2-циклопропилпиримидин-4-ил)амид нафтален-2-сульфоновой кислоты;
(2-циклопропилпиримидин-4-ил)амид бифенил-4-сульфоновой кислоты;
5-фтор-N-(2-изопропилпиримидин-4-ил)-2-метилбензолсульфонамид;
3,4-дихлор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
N-(2-изопропилпиримидин-4-ил)-4-(1,3-оксазол-5-ил)бензолсульфонамид;
2,4-дихлор-N-(2-изопропилпиримидин-4-ил)-6-метилбензолсульфонамид;
2,3-дихлор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
(2-изопропилпиримидин-4-ил)амид 5-пиридин-2-илтиофен-2-сульфоновой кислоты;
3-хлор-N-(2-изопропилпиримидин-4-ил)-2-метилбензолсульфонамид;
N-(2-изопропилпиримидин-4-ил)-3-трифторметилбензолсульфонамид;
N-(2-изопропилпиримидин-4-ил)-2-трифторметилбензолсульфонамид;
(2-изопропилпиримидин-4-ил)амид 5-хлортиофен-2-сульфоновой кислоты;
N-(2-изопропилпиримидин-4-ил)-4-трифторметилбензолсульфонамид;
(2-изопропилпиримидин-4-ил)амид нафтален-2-сульфоновой кислоты;
(2-изопропилпиримидин-4-ил)амид бифенил-4-сульфоновой кислоты;
2,5-дифтор-N-(2-изопропилпиримидин-4-ил)бензолсульфонамид;
N-(2-изопропилпиримидин-4-ил)-3,4-диметоксибензолсульфонамид;
N-(2-трет-бутилпиримидин-4-ил)-4-оксазол-5-илбензолсульфонамид;
3-хлор-N-(2-этилпиримидин-4-ил)-2-метилбензолсульфонамид;
2,4-дихлор-N-(2-этилпиримидин-4-ил)-6-метилбензолсульфонамид;
3-хлор-N-(2-циклобутилпиримидин-4-ил)-2-метилбензолсульфонамид;
(2-циклобутилпиримидин-4-ил)амид нафтален-2-сульфоновой кислоты;
(2-циклобутилпиримидин-4-ил)амид 5-пиридин-2-илтиофен-2-сульфоновой кислоты;
2,4-дихлор-N-(2-циклобутилпиримидин-4-ил)-6-метилбензолсульфонамид;
3-хлор-N-(2-циклопропилпиримидин-4-ил)-2-N-диметилбензолсульфонамид и
3,4-дихлор-N-(2-изопропилпиримидин-4-ил)-N-метилбензолсульфонамид.
Способы получения соединений формулы I являются объектом изобретения.
Получение соединений формулы I настоящего изобретения может осуществляться последовательным или конвергентным способами синтеза. Синтезы по изобретению показаны на следующих схемах. Навыки, необходимые для проведения реакции и очистки конечных продуктов, известны специалисту в данной области техники. Заместители и указания, используемые в следующем описании процессов, имеют значения, указанные выше, если конкретно не указано иное.
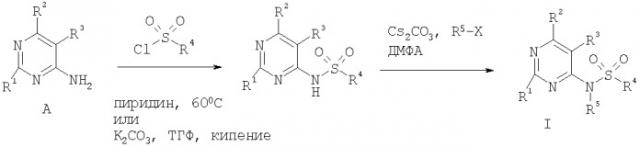
Обычно, соединения типа I легко получают сульфонилированием соответствующим образом замещенных 4-аминопиримидинов А сульфонилхлоридами при различных условиях, которые известны специалисту в данной области техники. Примерами таких условий являются, как показано на схеме ниже, например, пиридин при повышенных температурах или ТГФ при кипении в присутствии основания, такого как карбонат калия, карбонат натрия, гидрид натрия, триэтиламин или им подобные.
Соединения I с R5=Н, полученные таким способом, необязательно далее могут быть замещены при атоме азота сульфонамидной группы обработкой основанием, таким как гидрид натрия, карбонат цезия, карбонат калия или им подобные, в растворителе, таком как ДМФА или ТГФ, с последующим алкилированием полученного аниона алкилгалогенидом, таким как метилйодид, этилбромид, бензилбромид или им подобные, для введения желаемого заместителя R5.
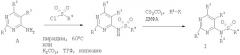
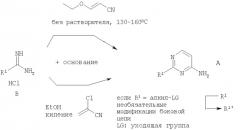
Подходящим образом замещенные 4-аминопиримидины А являются либо коммерчески доступными, известными из уровня техники, либо могут быть получены аналогично известным источникам из известных исходных материалов. В обычном способе синтеза используют амидины или соли амидина в качестве исходных материалов, которые - после высвобождения свободного амидина обработкой основанием, таким как триэтиламин, этоксид натрия, карбонат калия или им подобные, если в качестве исходных материалов используют соли амидина - обрабатывают акрилонитрилом, таким как 2-хлоракрилонитрил или 3-этоксиакрилонитрил в условиях, которые уже были описаны ранее (например, J. Heterocyclic Chem., 1977, 14, сс.1413-1414). Другие альтернативные подходы для получения подходящим образом замещенных 4-аминопиримидинов также доступны из уровня техники.
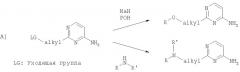
В присутствии подходящим образом замещенной боковой цепи в положении 2 4-аминопиримидинового промежуточного соединения А, например, в случае присутствия уходящей группы, такой как галогенид в боковой цепи, возможны дополнительные, но необязательные модификации. Например, уходящая группа может быть заменена обработкой подходящего исходного материала а) спиртами и основанием для получения арильных или алкильных эфиров или б) аминами для получения аминоалкильных производных, как показано на схеме А ниже. Когда уходящая группа присоединена непосредственно к пиримидиновому ядру в положении 2, возможны аналогичные реакции со спиртами с получением О-замещенных 2-гидрокси-4-аминопиримидинов (схема Б).
Превращение соединения формулы I в фармацевтически приемлемую соль может осуществляться обработкой такого соединения неорганической кислотой, например галогенводородной кислотой, такой как, например, хлористоводородная кислота или бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.д., или органической кислотой, такой как, например, уксусная кислота, лимонная кислота, малеиновая кислота, фумаровая кислота, винная кислота, метансульфоновая кислота или п-толуолсульфоновая кислота. Соответствующие соли карбоновых кислот также могут быть получены из соединений формулы I обработкой физиологически приемлемыми основаниями.
Превращение соединений формулы I в фармацевтически приемлемые эфиры или амиды может осуществляться, например, обработкой подходящих аминогрупп или гидроксильных групп, присутствующих в молекулах, карбоновой кислотой, такой как уксусная кислота, конденсирующим агентом, таким как гексафторфосфат бензотриазол-1-илокси-трис(диметиламино)фосфония (ВОР) или N,N-дициклогексилкарбодиимид (DCCI) с получением эфира карбоновой кислоты или амида карбоновой кислоты.
Предпочтительный способ получения соединения формулы I, как определено выше, включает реакцию соединения формулы:
в присутствии соединения формулы:
где R1-R5 являются такими, как определено выше. Особенно предпочтительным является указанный выше способ, например, в пиридине или ТГФ, особенно в присутствии основания, такого как, например, карбонат калия, карбонат натрия, гидрид натрия или триэтиламин. Очень предпочтительной является указанная выше реакция в присутствии пиридина при температуре от 50°С до 70°С. Еще более предпочтительным является указанный выше способ в присутствии ТГФ в условиях кипения с обратным холодильником.
Предпочтительными промежуточными соединениями являются:
2-циклопропилпиримидин-4-иламин;
2-изопропилпиримидин-4-иламин;
2-трет-бутилпиримидин-4-иламин;
2-этилпиримидин-4-иламин;
2-циклобутилпиримидин-4-иламин;
2-метоксиметилпиримидин-4-иламин;
2-циклопропилметоксиметилпиримидин-4-иламин;
2-морфолин-4-илметилпиримидин-4-иламин;
2-фенилпиримидин-4-иламин и
2-(2-метилтиазол-4-ил)пиримидин-4-иламин.
Описанные выше соединения формулы I для применения в качестве терапевтически активного вещества являются другим объектом настоящего изобретения.
Также объектом настоящего изобретения являются соединения, как описано выше, для изготовления лекарственных средств для профилактики и лечения заболеваний, которые вызваны нарушениями, связанными с ферментом 11бета-гидроксистероиддегидрогеназа 1 (11bHSD1).
Аналогично, объектом изобретения являются фармацевтические композиции, содержащие соединение формулы I, как описано выше, и терапевтически инертный носитель.
Другим предпочтительным вариантом осуществления настоящего изобретения является применение соединения формулы I, как описано выше, для изготовления лекарственных средств для лечения и профилактики диабетов, ожирения, заболеваний, связанных с приемом пищи, дислипидемии и гипертензии.
Особенно предпочтительным является применение соединения формулы I, как описано выше, для изготовления лекарственных средств для лечения и профилактики диабетов типа II.
Другой объект настоящего изобретения относится к соединению формулы I, как описано выше, полученному в соответствии с любым одним из описанных выше способов.
Также объектом изобретения является способ лечения и профилактики диабетов, ожирения, заболеваний, связанные с приемом пищи, дислипидемии и гипертензии, который включает введение эффективного количества соединения формулы I, как описано выше.
Особенно предпочтительным является способ лечения и профилактики диабетов типа II, который включает введение эффективного количества соединения формулы I, как описано выше.
Методики анализа
Переходная экспрессия и частичная очистка
кДНК, кодирующую белок 11бета-HSD1 человека, клонировали в вектор экспрессии pcDNA3 (Stratagene). Эту конструкцию (более подробно см. Alex Odermatt и др. J. Biol Chem., 1999, Т.274, вып.40, сс.28762-28770) использовали для переходной экспрессии белка в клетках НЕК293 (номер АТСС: CRL-1573, описанный Graham, F.L., Smiley, J., Russell, W.C., Nairn, R. (1977)), используя липофектамин. Через 48 ч после трансфекции клетки дважды промывали охлажденным льдом PBS (забуференный фосфатом соляной раствор). К 1 объему клеточной суспензии в PBS добавляли 2 объема охлажденного льдом буфера для лизиса (50 мМ Tris; pH 7,5; 1 мМ EDTA; 100 мМ NaCl). Клетки подвергали лизису с помощью гомогенизации Potter (20 ходов). Полученный гомогенизат обрабатывали ультразвуком с помощью ультразвукового шунта (10% выход; 2×30 сек) и очищали низкоскоростным центрифугированием (10 мин ×9000 g; 4°C). Микросомальную фракцию собирали с помощью высокоскоростного центрифугирования (60 мин ×110'000 g). Полученный остаток повторно суспендировали в буфере для хранения (20 мМ Tris; pH 7,5; 1 мМ EDTA; 10% глицерин) и повторяли центрифугирование. Полученный остаток, содержащий микросомальную фракцию, снова помещали в буфер для хранения и аликвоты хранили замороженными в жидком азоте до применения.
Выработка стабильных клеточных линий, экспрессирующих 11бета-HSD1
Такую же конструкцию, применяющуюся для переходной экспрессии 11бета-HSD1 человека, также использовали для установления стабильности клеточных линий, экспрессирующих белок. Вкратце, (НЕК293) клетки трансфицировали с помощью конструкции 11бета-HSD1, используя реагент липофектамин (Gibco BRL) в соответствии с инструкцией производителя. Через два дня после трансфекции инициировали выбор генетицина (0,8 мг/мл) и выделяли нескол