Полиморфная модификация соединения {6,7-бис(2-метоксиэтокси)хиназолин-4-ил}-(3e)
Иллюстрации
Показать всеИзобретение относится к кристаллической полиморфной модификации гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина. Кристаллическая полиморфная модификация имеет порошковую рентгеновскую дифрактограмму, в которой имеются характеристические максимумы, выраженные в градусах угла 2-тэта ±0,2 градуса: 5,7; 9,7; 10,1; 11,3; 17,0; 17,4; 18,9; 19,6; 21,3; 22,8; 23,6; 24,2; 24,7; 25,4; 26,2; 26,7; 29,3. Изобретение также относится к способу получения кристаллической полиморфной модификации, к фармацевтической композиции, обладающей ингибирующим действием в отношении тирозинкиназных ферментов, включающей кристаллическую полиморфную модификацию, к применению кристаллической полиморфной модификации для получения лекарственных средств. 7 н. и 5 з.п. ф-лы, 6 ил.
Реферат
Соединение гидрохлорид [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина формулы (I) используется для лечения гиперпролиферативных нарушений и расстройств, например таких, как рак у млекопитающих.
В международной заявке WO 96/30347, которая включена в описание настоящей заявки в полном объеме в качестве ссылки, раскрыто получение гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, а также использование этого соединения. В частности, это соединение является ингибитором тирозинкиназных ферментов, таких как рецепторы эпидермального фактора роста, и может быть использовано для лечения и/или профилактики заболеваний, которые связаны с тирозинкиназными ферментами, такими как рецепторы эпидермального фактора роста, например, для лечения и/или профилактики таких заболеваний, как рак, в особенности таких, как немелкоклеточный рак легкого, колоректальный рак, трудноизлечимый немелкоклеточный рак легкого, рак поджелудочной железы, рак яичника, рак молочной железы, глиома, злокачественные опухоли на голове или злокачественные опухоли на шее.
Недавно в международной заявке WO 01/34574, которая включена в описание настоящей заявки в полном объеме в качестве ссылки, были описаны две различных полиморфных модификации гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, обозначаемые как полиморфная модификация А и полиморфная модификация В.
Полиморфизм (наличие полиморфных модификаций) определяется как способность вещества кристаллизоваться с образованием более чем одного типа кристаллической решетки. Тип полиморфной модификации (полиморфная форма) может влиять на многие свойства, проявляемые лекарственным средством в твердом состоянии. Различные кристаллические модификации соединения могут значительно отличаться друг от друга во многих отношениях, включая растворимость, скорость растворения и биодоступность. Всестороннее исследование вопросов, связанных с полиморфизмом (образованием полиморфных модификаций), формированием молекулярных кристаллов и с их ролью в фармацевтике приведено в: Byrn S.R., Pfeiffer R.R., Stowell J.G., „Solid-State Chemistry of Drugs", SSCI Inc., West Lafayette, Indiana, 1999), Brittain H.G., „Polymorph modificationism in Pharmaceutical Solids", Marcel Dekker, Inc., New York, Basel, 1999); Bernstein (Bernstein J., Polymorph modificationism in Molecular Crystals", Oxford University Press, 2002).
Что касается двух полиморфных модификаций, описанных в международной заявке WO 01/34574, то полиморфная модификация В термодинамически более стабильна, чем полиморфная модификация А, в то время как полиморфная модификация А обладает лучшей растворимостью и более высокой скоростью растворения, чем полиморфная модификация В. Однако, рассматривая известные полиморфные модификации А и В гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, представляет интерес получить такую модификацию этого соединения, которая, являясь более термодинамически стабильной, чем полиморфная модификация А, также обладала бы лучшей растворимостью и более высокой скоростью растворения, чем полиморфная модификация В.
Неожиданно было обнаружено, что гидрохлорид [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина существует в виде третьей полиморфной модификации, обозначенной как полиморфная модификация Е, которая термодинамически более стабильна, чем известная полиморфная модификация А, обладает лучшей растворимостью и более высокой скоростью растворения, чем известная полиморфная модификация В.
Таким образом в соответствии с настоящим изобретением предлагается новая кристаллическая полиморфная модификация гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, которая неожиданно обладает лучшей растворимостью и более высокой скоростью растворения, чем полиморфная модификация В, и более термодинамически стабильна по сравнению с полиморфной модификацией А. Следовательно, полиморфная модификация согласно настоящему изобретению будет более подходящей для использования в фармакологии, чем известные полиморфные модификации А и В.
В том случае когда не указано иное, приведенные ниже определения используются для иллюстрации и определения значения и объема различных терминов, используемых для описания настоящего изобретения.
Термин ″кристаллическая полиморфная модификация" относится к кристаллической модификации, которая может быть охарактеризована аналитическими методами, например, такими как порошковая дифракция рентгеновских лучей, ИК-спектроскопия или температура плавления.
Термин ″полиморфная модификация Е″ относится к кристаллической полиморфной модификации гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина согласно настоящему изобретению. Термины ″полиморфная модификация А″ и ″полиморфная модификация В″ относятся к различным кристаллическим полиморфным модификациям гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, как описано в международной заявке WO 01/34574.
Сокращение „ИК" означает инфракрасный.
Описание чертежей:
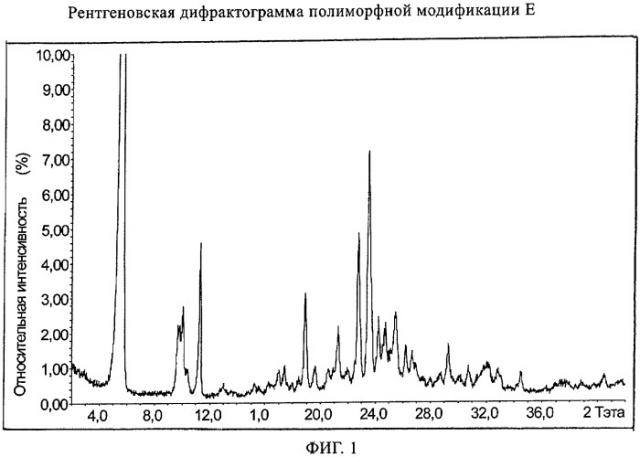
Фиг.1: рентгеновская дифрактограмма полиморфной модификации Е.
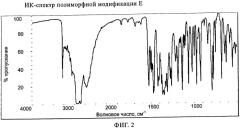
Фиг.2: ИК-спектр полиморфной модификации Е.
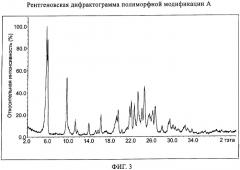
Фиг.3: рентгеновская дифрактограмма полиморфной модификации А.
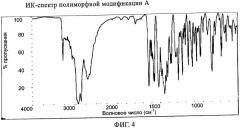
Фиг.4: ИК-спектр полиморфной модификации А.
Фиг.5: рентгеновская дифрактограмма полиморфной модификации В.
Фиг.6: ИК-спектр полиморфной модификации В.
Более конкретно, настоящее изобретение относится к кристаллической полиморфной модификации гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, характеризующейся порошковой рентгеновской дифрактограммой, на которой имеются характеристические максимумы, выраженные в градусах 2-тэта, при приблизительно:
| угол 2-тэта, градусы | |
| 5,7 | |
| 9,7 | |
| 10,1 | |
| 11,3 | |
| 17,0 | |
| 17,4 | |
| 18,9 | |
| 19,6 | |
| 21,3 | |
| 22,8 | |
| 23,6 | |
| 24,2 | |
| 24,7 | |
| 25,4 | |
| 26,2 | |
| 26,7 | |
| 29,3 |
Термин ″приблизительно″ в данном контексте означает, что имеется некоторая погрешность в определении градусов 2-тэта, составляющая ±0,2 (выражено в градусах 2-тэта).
Предпочтительно, кристаллическая полиморфная модификация, описанная выше, характеризуется порошковой рентгеновской дифрактограммой, на которой имеются характеристические максимумы, выраженные в градусах 2-тэта, как указывалось выше, с относительной интенсивностью, составляющей приблизительно
| Угол 2-тэта, градусы | Относительная интенсивность |
| 5,7 | 100 |
| 9,7 | 2,7 |
| 10,1 | 3,3 |
| 11,3 | 4,4 |
| 17,0 | 1,2 |
| 17,4 | 1,4 |
| 18,9 | 3,9 |
| 19,6 | 1,2 |
| 21,3 | 2,6 |
| 22,8 | 5,1 |
| 23,6 | 9,0 |
| 24,2 | 3 |
| 24,7 | 2,7 |
| 25,4 | 3,2 |
| 26,2 | 2,2 |
| 26,7 | 1,8 |
| 29,3 | 2 |
Термин ″приблизительно″ в данном контексте означает, что имеется некоторая погрешность в определении относительной интенсивности. Специалисту в данной области техники известно, что погрешность в определении относительной интенсивности зависит исключительно от условий измерения. Значения относительной интенсивности могут, например, отличаться на ±30% или, предпочтительно, на ±10%.
Предпочтительной является такая кристаллическая полиморфная модификация, как описано выше, которая характеризуется порошковой рентгеновской дифрактограммой, приведенной на фигуре 1.
Таким образом, кристаллическая полиморфная модификация, описанная выше, может быть охарактеризована ее ИК-спектром. В соответствии с другим предпочтительным вариантом осуществления настоящее изобретение относится к кристаллической полиморфной модификации гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил](3-этинилфенил)амина, которая характеризуется ИК-спектром поглощения, в котором имеются характеристические максимумы, выраженные в см-1, при приблизительно 3277 см-1, 3057 см-1, 1627 см-1, 1070 см-1, 1022 см-1, 892 см-1, 873 см-1, 850 см-1, 780 см-1, 745 см-1, 725 см-1, 652 см-1. Термин „приблизительно" в данном контексте означает, что значения, выраженные в см-1, могут отличаться на ±2 см, предпочтительно на ±1 см. Такая кристаллическая полиморфная модификация, как описано выше, которая характеризуется ИК-спектром поглощения, приведенным на фигуре 2, представляет предпочтительный вариант осуществления настоящего изобретения.
В дополнение, кристаллическая полиморфная модификация, описанная выше, может быть охарактеризована ее температурой плавления. Таким образом, настоящее изобретение также включает кристаллическую полиморфную модификацию гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, которая характеризуется температурой плавления, составляющей от 211°С до 214°С.
Кроме того, настоящее изобретение, в частности, относится к компаунду гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, в котором по меньшей мере 70% представлено в виде кристаллической полиморфной модификации, которая определена выше, в частности, по меньшей мере 90% представлено в виде кристаллической полиморфной модификации, которая определена выше, более предпочтительно, по меньшей мере 95% представлено в виде кристаллической полиморфной модификации, как определено выше, и даже, в особенности, по меньшей мере 99% представлено в виде кристаллической полиморфной модификации, которая определена выше.
Кроме того, настоящее изобретение относится к способу получения кристаллической полиморфной модификации, как описано выше, указанный способ включает взаимодействие соединения формулы (II)
с соединением формулы (III)
в (α,α,α)-трифтортолуоле. Соединение формулы (II) представляет собой 3-этиниланилин, который также называют 3-этиниламинобензолом, а соединение формулы (III) представляет собой 4-хлор-6,7-бис(2-метоксиэтокси)-хиназолин. Исходные продукты формулы (II) и (III) могут быть получены в соответствии с методиками, известными из предшествующего уровня техники, например, из опубликованной международной заявки WO 01/34574. Описанное выше взаимодействие можно проводить в условиях, известных специалисту в данной области техники. Например, подходящая температура может составлять от 30 до 100°С, предпочтительно от 50 до 80°С, более предпочтительно от 70 до 80°С. Согласно предпочтительному варианту осуществления изобретения взаимодействие проводят в присутствии HCl. После осуществления взаимодействия кристаллическая полиморфная модификация гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, которая описана выше, выпадает в осадок из (α,α,α)-трифтортолуола и может быть выделена в соответствии с методиками, известными специалисту в данной области техники, например, посредством фильтрации или центрифугирования. Молярное соотношение соединения формулы (II) к соединению формулы (III) может варьироваться, например, в интервале от 0,5 до 1,5. Предпочтительно, молярное соотношение находится в интервале от 0,9 до 1,1. Более предпочтительно, молярное соотношение составляет приблизительно 1, наиболее предпочтительно 1.
Кроме того, настоящее изобретение относится к кристаллической полиморфной модификации, как определено выше, полученной способом, который определен выше.
Как описано выше, полиморфная модификация согласно настоящему изобретению представляет собой фармацевтически активное соединение и ингибирует ферменты - тирозинкиназы, в особенности, такие как рецепторы эпидермального фактора роста, и может быть использовано для лечения и/или профилактики заболеваний, которые связаны с тирозинкиназными ферментами, в частности, такими как рецепторы эпидермального фактора роста, например, может быть использовано для лечения и/или профилактики таких заболеваний как рак, в особенности, немелкоклеточный рак легкого, колоректальный рак, трудноизлечимый немелкоклеточный рак, рак поджелудочной железы, рак яичника, рак молочной железы, глиома, злокачественные опухоли на голове или злокачественные опухоли на шее. Предпочтительным показанием для профилактики и/или лечения является немелкоклеточный рак легкого.
Настоящее изобретение также относится к фармацевтическим композициям, включающим кристаллическую полиморфную модификацию, которая определена выше, и фармацевтически приемлемый носитель и/или вспомогательное вещество.
Кроме того, в объем настоящего изобретения входит кристаллическая полиморфная модификация, которая описана выше, предназначенная для применения в качестве терапевтически активного соединения, предпочтительно, в качестве терапевтически активного соединения для лечения и/или профилактики заболеваний, которые связаны с тирозинкиназными ферментами, в частности, такими как рецепторы эпидермального фактора роста, например, для лечения и/или профилактики таких заболеваний как рак (злокачественные опухоли), в особенности, таких как немелкоклеточный рак легкого, колоректальный рак, трудноизлечимый немелкоклеточный рак легкого, рак поджелудочной железы, рак яичника, рак молочной железы, глиома, злокачественные опухоли на голове или злокачественные опухоли на шее, в частности, такого заболевания как немелкоклеточный рак легкого.
В соответствии с другим предпочтительным вариантом осуществления настоящее изобретение относится к способу терапевтического и/или профилактического лечения заболеваний, которые связаны с тирозинкиназными ферментами, в частности, такими как рецепторы эпидермального фактора роста, в частности, для терапевтического и/или профилактического лечения рака, например, такого как немелкоклеточный рак легкого, колоректальный рак, трудноизлечимый немелкоклеточный рак легкого, рак поджелудочной железы, рак яичника, рак молочной железы, глиома, злокачественные опухоли на голове или злокачественные опухоли на шее, особенно такого как немелкоклеточный рак легкого, указанный способ включает введение кристаллической полиморфной модификации, которая определена выше, человеку или животному.
Настоящее изобретение также включает применение кристаллической полиморфной модификации, которая определена выше, для терапевтического и/или профилактического лечения заболеваний, которые связаны с тирозинкиназными ферментами, в частности, такими как рецепторы эпидермального фактора роста, в частности, для терапевтического и/или профилактического лечения рака, в частности, такого как немелкоклеточный рак легкого, колоректальный рак, трудноизлечимый немелкоклеточный рак легкого, рак поджелудочной железы, рак яичника, рак молочной железы, глиома, злокачественные опухоли на голове или злокачественные опухоли на шее, в особенности, такого как немелкоклеточный рак легкого.
Настоящее изобретение также относится к применению кристаллической полиморфной модификации, которая описана выше, для получения лекарственных средств для терапевтического и/или профилактического лечения заболеваний, которые связаны с тирозинкиназными ферментами, в частности, такими как рецепторы эпидермального фактора роста, в частности, для терапевтического и/или профилактического лечения рака, в частности, такого как немелкоклеточный рак легкого, колоректальный рак, трудноизлечимый немелкоклеточный рак легкого, рак поджелудочной железы, рак яичника, рак молочной железы, глиома, злокачественные опухоли на голове или злокачественные опухоли на шее, в особенности, такого как немелкоклеточный рак легкого. Эти лекарственные средства включают соединение, которое описано выше.
В случае композиций, применения и способов, которые описаны выше, вместо полиморфной модификации, которая определена выше, может быть использовано соединение гидрохлорид [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, которое по меньшей мере на 70% представляет собой кристаллическую полиморфную модификацию, которая определена выше, в частности, соединение, которое по меньшей мере на 90% представляет собой кристаллическую полиморфную модификацию как определено выше, в особенности, соединение, которое по меньшей мере на 95% представляет собой кристаллическую полиморфную модификацию, которая определена выше, и даже, в особенности, по меньшей мере на 99% представляет собой кристаллическую полиморфную модификацию.
Полиморфная модификация согласно настоящему изобретению может быть использована в виде лекарственного средства, например, в виде фармацевтического препарата для энтерального, парентерального или местного введения. Лекарственное средство может быть введено, например, перорально, например, в виде таблеток, таблеток с покрытием, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий, ректально, например, в виде суппозиториев, парентерально, например, в виде растворов для инъекций или суспензий или растворов для инфузии, или местно, например, в виде мазей, кремов или масел.
Получение фармацевтических препаратов может быть осуществлено способами, хорошо известными специалистам в данной области техники, при введении описанной полиморфной модификации необязательно в комбинации с другими терапевтически значимыми соединениями в лекарственную форму, вместе с подходящими нетоксичными, инертными, терапевтически совместимыми твердыми или жидкими носителями, и если это необходимо, вместе с обычными фармацевтическими вспомогательными веществами.
Подходящие носители представляют собой не только неорганические вещества-носители, но и органические вещества-носители. Таким образом, например, лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли могут быть использованы в качестве носителя для таблеток, таблеток с покрытием, драже, твердых и мягких желатиновых капсул. Подходящие вещества-носители для мягких желатиновых капсул представляют собой, например, растительные масла, воски, жиры и полутвердые и жидкие полиолы (однако в зависимости от природы активного ингредиента мягких желатиновых капсул носитель может не использоваться). Подходящие вещества-носители для получения растворов и сиропов представляют собой, например, воду, полиолы, сахарозу, инвертный сахар и подобные им носители. Подходящие вещества-носители для растворов для инъекций представляют собой, например, воду, спирты, полиолы, глицерин и растительные масла. Подходящие вещества-носители для суппозиториев представляют собой, например, природные или отвержденные масла, воски, жиры и полужидкие или жидкие полиолы. Подходящие вещества-носители для местного применения представляют собой глицериды, полусинтетические и синтетические глицериды, гидрогенированные масла, жидкие воски, жидкие парафины, жидкие жирные спирты, стеролы, полиэтиленгликоли и производные целлюлозы.
В качестве вспомогательных веществ следует рассматривать обычно используемые в фармацевтике стабилизаторы, консерванты, агенты, улучшающие смачиваемость, и эмульгирующие агенты, агенты, улучшающие консистенцию, агенты, улучшающие вкус и запах, соли для регулирования осмотического давления, буферные вещества, солюбилизаторы, подкрашивающие вещества и маскирующие агенты, а также антиоксиданты.
Дозировка соединений формулы I может варьироваться в широких пределах в зависимости от заболевания, которое подлежит контролю, возраста, индивидуального состояния пациента и способа введения, и безусловно должна в каждом конкретном случае соответствовать индивидуальным требованиям. Для взрослых пациентов следует рассматривать дневную дозировку, составляющую приблизительно от 1 до 7000 мг, в особенности, приблизительно от 5 до 2500 мг, предпочтительно от 5 до 200 мг. В зависимости от степени выраженности симптомов заболевания и фармакокинетического профиля соединение можно вводить в виде одной или нескольких дневных дозировок, например, в виде 1-3 дозированных единиц.
Фармацевтические препараты подходящим образом содержат приблизительно 1-1000 мг, предпочтительно 5-200 мг соединения формулы I.
Приведенные ниже примеры служат для более подробной иллюстрации изобретения. Однако они никаким образом не ограничивают объем настоящего изобретения. Кристаллические полиморфные модификации А и В гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина могут быть получены в соответствии с методиками, описанными в опубликованной международной заявке WO 01/34574.
Примеры
Пример 1
Реактор с рубашкой, емкость 500 мл, продувают азотом и помещают в него 30 г 4-хлор-6,7-бис(2-метоксиэтокси)хиназолина и 130 г (α,α,α)-трифтортолуола. К белой суспензии добавляют 12,55 г 3-этиниланилина, растворенного в 180 г (α,α,α)-трифтортолуола. После добавления 0,18 г HCl (37%) реакционную смесь перемешивают дополнительно в течение 15 мин при комнатной температуре, после чего нагревают до температуры образования флегмы. После завершения реакции суспензию охлаждают до комнатной температуры и отфильтровывают. Выделенные кристаллы гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина промывают этанолом и высушивают при 60°С /10 мбар в течение ночи. Полученный продукт характеризуют методом порошковой рентгеновской дифракции и методом ИК-спектроскопии как модификацию Е. Кристаллы плавятся при температуре приблизительно 213°С (Tonset, измерено методом дифференциальной сканирующей калориметрии).
Пример 2
Рентгеновские порошковые дифрактограммы индивидуальных кристаллических полиморфных модификаций Е, А и В гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина регистрируют, используя дифрактометр «Bruker D8 diffractometer» (геометрия: Брэгг-Брентано; излучение: CuKα 1,54184 Å; второй графитовый монохроматор; детектор: сцинтилляционный счетчик, 2δ ступенчатое сканирование с величиной шага 0,02° и временем измерения, составляющим 1,0 с для одного шага). Образцы (приблизительно 200 мг) получают и анализируют без какой-либо дополнительной обработки соединения (например, такой как размол или просеивание). Порошковые рентгеновские дифрактограммы индивидуальных кристаллических полиморфных модификаций Е, А и В гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина приведены на фиг.1, 3 и 5, соответственно.
Пример 3
ИК-спектры индивидуальных кристаллических полиморфных модификаций Е, А и В гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина регистрировали с использованием пленки суспензии в нуйоле (Nujol), состоящей из приблизительно 15 мг образца и приблизительно 15 мг нуйола между двумя пластинками из хлорида натрия, используя ИК-спектрометр с преобразованием Фурье - ИК-ПФ-спектрометр (Nicolet 20SXB или эквивалентный ему) при поглощении (разрешение 2 см-1, 200 или более циклов сканирования, МСТ-детектор). ИК-спектры индивидуальных кристаллических полиморфных модификаций Е, А и В гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина приведены на фигурах 2, 4 и 6, соответственно.
Пример 4
Значения температуры плавления индивидуальных кристаллических полиморфных модификаций Е, А и В гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина измеряют методом дифференциальной сканирующей калориметрии (как описано, например, в: P.J. Haines, ed., "Principles of Thermal Analysis and Calorimetry", Royal Society of Chemistry, Cambridge, UK, 2002):
| Тип полиморфной модификации | Температура плавления (Tonset), [°С] |
| полиморфная модификация Е | от 211 до 214 |
| полиморфная модификация А | от 205 до 208 |
| полиморфная модификация В | от 227 до 231 |
Пример 5
Термодинамическую стабильность индивидуальных кристаллических полиморфных модификаций Е, А и В гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина измеряют с использованием методик, известных из предшествующего уровня техники, например, описанных в: Byrn, S.R., Pfeiffer, R.R., Stowell, J.G., „Solid-State Chemistry of Drugs", SSCI Inc., West Lafayette, Indiana, 1999. Измерения температуры плавления, теплоты растворения, а также эксперименты по достижению равновесного состоянии в суспензии свидетельствуют о том, что полиморфная модификация Е является термодинамически более стабильной, чем полиморфная модификация А, а также о том, что полиморфная модификация В является более стабильной, чем полиморфные модификации Е и А.
| Тип полиморфной модификации | Температура плавления (Tonset), [°С] | Теплота растворения, этанол/вода (45:55 г/г, 45°С), [кДж/моль] |
| полиморфная модификация Е | от 211 до 214 | от 56,9 до 58,4 |
| полиморфная модификация А | от 205 до 208 | от 50,0 до 55,6 |
| полиморфная модификация В | от 227 до 231 | от 61,2 до 62,4 |
Пример 6
Данные о растворимости полиморфных модификаций А, В и Е, измеренной после достижения равновесия, через 20 мин при 20°С либо в воде, либо в водном буферном растворе (рН 1), приведены в следующей таблице:
| Тип полиморфной модификации | Вода | Водный буферный раствор (рН 1) |
| полиморфная модификация Е | 0,191% | 0,011% |
| полиморфная модификация А | 0,194% | 0,017% |
| полиморфная модификация В | 0,098% | 0,003% |
Пример А
Таблетки с пленочным покрытием, содержащие следующие ингредиенты, могут быть приготовлены общепринятым образом:
| Ингредиенты | На таблетку | |
| Ядро: | ||
| Соединение формулы (I) | 10,0 мг | 200,0 мг |
| Микрокристаллическая целлюлоза | 23,5 мг | 43,5 мг |
| Водная лактоза | 60,0 мг | 70,0 мг |
| Повидон (Povidone) K30 | 12,5 мг | 15,0 мг |
| Гликолят натриевой соли крахмала | 12,5 мг | 17,0 мг |
| Стеарат магния | 1,5 мг | 4,5 мг |
| (Масса ядра) | 120,0 мг | 350,0 мг |
| Пленочное покрытие: | ||
| Гидроксипропилметилцеллюлоза | 3,5 мг | 7,0 мг |
| Полиэтиленгликоль 6000 | 0,8 мг | 1,6 мг |
| Тальк | 1,3 мг | 2,6 мг |
| Оксид железа (желтый) | 0,8 мг | 1,6 мг |
| Диоксид титана | 0,8 мг | 1,6 мг |
Активный ингредиент просеивают и смешивают с микрокристаллической целлюлозой и затем полученную смесь гранулируют, используя раствор поливинилпирролидона в воде. Гранулят смешивают с гликолятом натриевой соли крахмала и стеаратом магния и прессуют, получая при этом ядро таблетки размером 120 или 350 мг, соответственно. На ядро затем наносят пленочное покрытие, используя водный раствор/суспензию вышеуказанных компонентов для получения пленочного покрытия.
Пример Б
Капсулы, содержащие следующие ингредиенты, могут быть получены обычным образом:
| Ингредиенты | На капсулу |
| Соединение формулы (I) | 25,0 мг |
| Лактоза | 150,0 мг |
| Кукурузный крахмал | 20,0 мг |
| Тальк | 5,0 мг |
Компоненты просеивают, смешивают и помещают в капсулы размера 2.
Пример В
Пакетики, содержащие указанные ниже ингредиенты, могут быть приготовлены обычным образом:
| Соединение формулы (I) | 50,0 мг |
| Лактоза, мелкодисперсный порошок | 1015,0 мг |
| Микрокристаллическая целлюлоза (AVICEL РН 102) | 1400,0 мг |
| Натриевая соль карбоксиметилцеллюлозы | 14,0 мг |
| Поливинилпирролидон К 30 | 10,0 мг |
| Стеарат магния | 10,0 мг |
| Добавки, улучшающие вкус и запах | 1,0 мг |
Активный ингредиент смешивают с лактозой, микрокристаллической целлюлозой и натриевой солью карбоксиметилцеллюлозы и гранулируют, используя поливинилпирролидон в воде. Полученный гранулят смешивают со стеаратом магния и добавками, улучшающими вкус и запах, расфасовывают в маленькие пакетики.
1. Кристаллическая полиморфная модификация гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, которая характеризуется порошковой рентгеновской дифрактограммой, в которой имеются характеристические максимумы, выраженные в градусах угла 2-тэта ±0,2 градуса:
| 2-тэта, градусы | |
| 5,7 | |
| 9,7 | |
| 10,1 | |
| 11,3 | |
| 17,0 | |
| 17.4 | |
| 18,9 | |
| 19,6 | |
| 21,3 | |
| 22,8 | |
| 23,6 | |
| 24,2 | |
| 24,7 | |
| 25,4 | |
| 26,2 | |
| 26,7 | |
| 29,3 |
2. Кристаллическая полиморфная модификация по п.1, которая характеризуется порошковой рентгеновской дифрактограммой, приведенной на фигуре 1.
3. Кристаллическая полиморфная модификация гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, которая характеризуется ИК-спектром поглощения, в котором имеются характеристические максимумы, выраженные в см-1, 3277 см-1, 3057 см-1, 1627 см-1, 1070 см-1, 1022 см-1, 892 см-1, 873 см-1, 850 см-1, 780 см-1, 745 см-1, 725 см-1, 652 см-1 ±2 см-1.
4. Кристаллическая полиморфная модификация по п.3, которая характеризуется ИК-спектром поглощения, приведенным на фигуре 2.
5. Кристаллическая полиморфная модификация гидрохлорида [6,7-бис(2-метоксиэтокси)хиназолин-4-ил]-(3-этинилфенил)амина, которая характеризуется температурой плавления, составляющей от 211 до 214°С.
6. Способ получения кристаллической полиморфной модификации по любому из пп.1-5, включающий взаимодействие соединения формулы (II) с соединением формулы (III) в (α,α,α)-трифтортолуоле.
7. Кристаллическая полиморфная модификация по любому из пп.1-5, полученная взаимодействием соединения формулы (II) с соединением формулы (III) в (α,α,α)-трифтортолуоле.
8. Фармацевтическая композиция, обладающая ингибирующим действием в отношении тирозинкиназных ферментов, включающая кристаллическую полиморфную модификацию, по любому из пп.1-5 в качестве активного компонента и фармацевтически приемлемый носитель и/или вспомогательное вещество.
9. Кристаллическая полиморфная модификация по любому из пп.1-5, обладающая ингибирующим действием в отношении тирозинкиназных ферментов.
10. Кристаллическая полиморфная модификация по любому из пп.1-5 для применения в качестве терапевтически активного соединения для получения лекарственных средств, предназначенных для терапевтического и/или профилактического лечения и/или профилактики заболеваний, которые связаны с рецепторами эпидермального фактора роста.
11. Применение кристаллической полиморфной модификации по любому из пп.1-5 для получения лекарственных средств для терапевтического и/или профилактического лечения заболеваний, которые связаны с рецепторами эпидермального фактора роста.
12. Применение кристаллической полиморфной модификации по любому из пп.1-5 для получения лекарственных средств для терапевтического и/или профилактического лечения рака.