Способ получения метионина
Иллюстрации
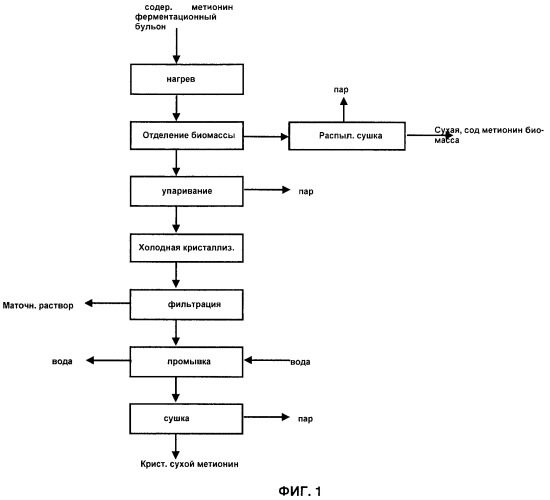
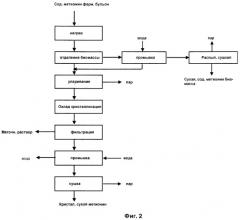
Показать всеИзобретение относится к биотехнологии, а именно к способу выделения ферментативно полученного метионина. Способ включает нагревание ферментационного бульона, содержащего метионин и биомассу, образовавшегося при ферментации микроорганизма-продуцента метионина, с последующим отделением от ферментационного бульона биомассы с получением жидкой фазы, обогащенной метионином, причем отделенную биомассу промывают водой, и образовывающийся раствор объединяют с упомянутой жидкой фазой. Полученный метионин выкристаллизовывают. Изобретение позволяет повысить эффективность выделения метионина. 13 з.п. ф-лы, 4 ил.
Реферат
Настоящее изобретение касается способа ферментативного получения метионина, способа выделения образованного при этом метионина, полученной при выделении биомассы, содержащей метионин, ее применения для получения корма или добавки к корму, а также применения выделенного метионина для получения пищевых продуктов или кормов, или добавок к пищевым продуктам или кормам.
Метионин применяют в различных сферах, включая пищевую промышленность, производство кормов, косметическую и фармацевтическую промышленность.
До настоящего времени техническое значение имеют только химические способы получения D,L-метионина. Исходными веществами для осуществления такого синтеза являются сероводород, метилмеркаптан, акролеин, синильная кислота или метилмеркаптопропиональдегид (см. Ullmann's Encyclopedia of Industrial Chemistry (1985), Vol.A2, стр.71).
Метионин получают также естественными клеточными процессами обмена веществ. Его получение в промышленных масштабах целесообразнее всего осуществлять при помощи бактериальных культур, которые выращивают для получения и выделения больших количеств желаемого вещества. С этой целью особенно подходящими организмами являются непатогенные булавообразные бактерии.
Известно, что метионин может быть получен ферментацией штаммов булавообразных бактерий, в частности, Corynebacterium glutamicum. Ввиду большого значения специалисты постоянно работают над усовершенствованием способов получения. К методам усовершенствования могут, например, относится ферментативно-технические мероприятия, которые касаются композиции питательной среды или важных функциональных свойств самого микроорганизма.
Для усовершенствования функциональных свойств этих микроорганизмов в отношении выработки соответствующей молекулы могут быть использованы методы мутагенеза, селекции и отбора мутантов или методы рекомбинантных ДНК для усовершенствования штаммов, вырабатывающих аминокислоту, таких как, например, Corynebacterium, путем увеличения концентрации или исключения отдельных генов биосинтеза аминокислоты, что способствует улучшению выработки аминокислоты.
Так, например, WO-A-02/10209 и DE-A-10136986 описывают способ ферментативного получения L-метионина при использовании генетически модифицированных булавообразных бактерий, вырабатывающих L-метионин. В частности, там описан способ получения L-метионин, включающий ферментацию бактерий, накопление аминокислоты в среде или в бактериях и выделение аминокислоты. Кроме того, описан способ получения содержащей L-метионин добавки к кормам животных из ферментационного бульона, который включает такие стадии: а) ферментацию вырабатывающих L-метионин микроорганизмов; b) концентрацию ферментационного бульона, например, выпариванием; с) отделение биомассы (от 0 до 100%), например, центрифугированием; и d) сушку, например, сублимационную или распылительную сушку, распылительную грануляцию.
Swapan и др. в J. Microbial Biotechnology, 4 (1), 35-41 (1989) описывают выработку метионина мутантом Bacillus megaterium путем выделения клеток из ферментационного бульона, установления значения pH, равного 5, обработки активированным углем и ионообменной хроматографии.
Из DE-A-3533198 известен способ ферментативного получения L-лейцина при помощи специальных термофильных бактерий. Ферментацию осуществляют непрерывно при +60°С путем удерживания биомассы, отделения содержащей продукт истощенной среды, охлаждения (до +2°С) в кристаллизаторе, выделения выкристаллизованной аминокислоты и возвращения маточного щелока в реактор. Однако ферментативное получение метионина там не описано.
Описанные до настоящего времени способы выработки метионина микроорганизмами не отвечают требованиям получения в технических масштабах. Причиной этого, с одной стороны, является ограниченная растворимость метионина в водной ферментационной среде, в результате чего при высокой продуктивности биосинтеза метионин выпадает в осадок в ферментационный бульон, что осложняет очистку. Другой причиной является тот факт, что при осуществлении способа согласно уровню техники скапливается значительное количество побочных продуктов, удаление которых требует больших затрат.
Краткое описание изобретения
Таким образом, задача данного изобретения состояла в разработке усовершенствованного способа выделения ферментативно полученного метионина, который мог бы быть применим для ферментационных бульонов, содержащих метионин частично в кристаллической форме. Следующая задача состояла в разработке способа обработки содержащих метионин ферментационных бульонов, при осуществлении которого не образовывались бы практически никакие побочные продукты и который был бы особенно рентабельным.
Неожиданном образом поставленная выше задача была решена способом обработки, при осуществлении которого целенаправленно используют свойства растворимости метионина для отделения биомассы. При осуществлении данного способа кристаллизацию используют как метод очистки ферментативно полученного L-метионина. В результате получают два различных продукта, используемых в качестве добавки к корму (низко- и высококонцентрированный продукт). В предпочтительных вариантах практически не образуются никакие побочные продукты, что позволяет осуществлять особенно рентабельное получение метионина в технических масштабах.
Подробное описание изобретения
А) Общие определения
„Метионин" в рамках данного изобретения включает в себя L- или D-метионин, смеси этих изомеров, такие как, например, рацематы, предпочтительно L-метионин.
Растворимость метионина в воде при 20°С составляет приблизительно 30 г/л, при 70°С она превышает 90 г/л. В ферментационном бульоне при таких условиях наблюдают растворимости сравнимого порядка.
Процессы, такие как „концентрирование", „отделение", „промывка" „сушка" в рамках данного изобретения включают в себя все известные специалистам способы. Так, например, под „концентрированием" подразумевают выпаривание жидкой фазы при атмосферном давлении или в вакууме. „Концентрирование" можно, например, осуществлять при использовании известных технологий, таких как обратный осмос или нанофильтрация, или общеупотребительных устройств, таких как выпарной аппарат или ротационный выпарной аппарат, или их комбинаций. „Отделение" может, например, включать в себя центрифугирование, фильтрацию, декантацию или комбинацию этих способов. „Промывка" может означать, например, отфильтровывание твердого вещества и одно- или многоразовое промывание, в случае необходимости, после взмучивания фильтрационного осадка. „Сушка" может, например, включать в себя сушку вымораживанием, распылительную сушку, распылительную грануляцию, сушку в псевдоожиженном слое или комбинацию этих способов.
В) Предпочтительные формы осуществления изобретения
Первым объектом данного изобретения является способ выделения ферментативно полученного метионина, причем
a) содержащую метионин водную фракцию, образующуюся при ферментации вырабатывающего метионин микроорганизма, которая, в частности, содержит метионин в частично нерастворенной форме, нагревают до температуры, достаточной для повышения растворимости метионина в водной фазе, предпочтительно с целью в основном полного растворения метионина,
b) из нее выделяют жидкую фазу, обогащенную метионином, и
c) метионин выкристаллизовывают, в случае необходимости, после концентрирования обогащенной водной фазы.
Выражение „в основном" полностью растворенный означает, что метионин, например, на более чем 95%, более чем 98%, в частности до 100%, в пересчете на общее содержание метионина, растворен в жидкой фазе.
Содержащая метионин „жидкая фракция", как правило, представляет собой полученный в процессе ферментации бульон, который, в частности, содержит метионин в частично нерастворенной форме и который, в случае необходимости, может содержать другие твердые компоненты, обычно содержащиеся в ферментационных бульонах; или производную от него, например, полученную при соответствующей предварительной обработке жидкость. „Предварительная обработка" может заключаться, например, в концентрировании выпариванием или добавлении веществ. Так, например, в бульон можно добавлять содержащие метионин фракции более ранних стадий обработки или добавки (см. ниже), которые способствуют дальнейшей обработке или применению продукта по назначению (например, в качестве добавки к корму).
Содержание нерастворенного метионина в, в случае необходимости, насыщенном ферментационном бульоне в пересчете на общий вес ферментационного бульона составляет приблизительно от 1 до 10 вес.%, предпочтительно приблизительно от 3 до 8 вес.% или в пересчете на общий вес твердого вещества приблизительно от 30 до 80 вес.%, предпочтительно от 50 до 57 вес.%.
Так, например, содержание метионина, полученного при осуществлении ферментации согласно изобретению, может составлять приблизительно 96 г/л, из которых при обычной температуре ферментации приблизительно 46 г/л являются растворенными, а приблизительно 50 г/л - нерастворенными.
Содержание метионина в обогащенной жидкой фазе, в пересчете на ее сухие остатки, составляет приблизительно от 60 до 100 вес.% или приблизительно от 90 до 100 вес.%, например, приблизительно от 75 до 85 вес.% или приблизительно от 95 до 100 вес.%, в пересчете на сухую массу.
С целью в основном полного растворения метионина на стадии а) раствор нагревают до температуры приблизительно от 60 до 120°С, предпочтительно приблизительно от 70 до 100°С, в зависимости от количества подлежащего растворению продукта. При этом, в случае необходимости, можно работать при незначительно повышенном давлении, например, от 1 до 5 атм.
Предпочтительно на стадии а) в качестве жидкой фракции используют содержащий биомассу ферментационный бульон без дальнейшей предварительной обработки.
Обогащенную метионином жидкую фазу стадии b) получают предпочтительно путем выделения биомассы из обогащенного растворенным метионином нагретого ферментационного бульона. Чтобы избежать преждевременного выкристаллизовывания метионина, во время выделения биомассы также работают при повышенной температуре, предпочтительно при температуре в указанном выше диапазоне.
Согласно предпочтительной форме осуществления изобретения
d) выкристаллизованный метионин отделяют,
e) отделенный твердый, предпочтительно кристаллический метионин, в случае необходимости, промывают и
f) в случае необходимости, сушат.
Согласно другому предпочтительному варианту осуществления способа отделенную на стадии b) биомассу
g1) в случае необходимости, промывают, причем используемую для промывания жидкость, в случае необходимости, нагревают и
g3) сушат.
Нагревание жидкости для промывки может быть необходимым в том случае, если, например, твердый метионин должен содержаться в отделенной фракции биомассы, при этом желательно получать метионин из фракции биомассы в как можно более широких масштабах.
Во избежание побочных продуктов, предпочтительно
g2) образовывающуюся на стадии g1) промывную жидкость объединяют с обогащенной метионином жидкой фазой стадии b).
Полученные описанными выше способами жидкие фазы стадии b), содержащие метионин, концентрируют, например, выпариванием при нагревании и, в случае необходимости, в вакууме. Содержание метионина в образующемся при этом концентрате составляет приблизительно от 10 до 40 вес.%, в пересчете на общий вес концентрата. При этом отделение метионина осуществляют предпочтительно кристаллизацией при охлаждении. С этой целью раствор охлаждают до температуры от 0 до 20°С. После завершения кристаллизации твердый метионин промывают холодной промывной жидкостью, например водой, и, в случае необходимости, при легком нагревании сушат.
Согласно другому варианту осуществления способа образующийся на стадии d) маточный раствор
d1) объединяют с содержащей метионин жидкой фракцией, выделенной из другой ферментационной смеси, содержащей вырабатывающий метионин микроорганизм;
или
d2) добавляют в биомассу, выделенную из той же или другой ферментационной смеси, содержащей вырабатывающий метионин микроорганизм, перед сушкой согласно стадии g3).
Согласно следующему варианту осуществления способа полученную на стадии е) промывную жидкость
е1) объединяют с содержащей метионин жидкой фракцией, выделенной из другой ферментационной смеси, содержащей вырабатывающий метионин микроорганизм; или
е2) добавляют в биомассу, выделенную из той же или другой ферментационной смеси, содержащей вырабатывающий метионин микроорганизм, перед сушкой согласно стадии g3).
Путем возврата маточного раствора и промывной жидкости удается еще более эффективно препятствовать образованию побочных продуктов.
Кроме того, согласно изобретению сушку согласно стадии g3) осуществляют предпочтительно в виде распылительной сушки.
Следующим объектом данного изобретения является способ ферментативного получения метионина, причем известным способом ферментируют естественный или рекомбинантный микроорганизм, после чего полученный метионин выделяют описанным выше способом.
Согласно предпочтительной форме осуществления изобретения способы согласно изобретению проводят при использовании вырабатывающего метионин микроорганизма, выбранного из естественных или рекомбинантных бактерий вида Corynebacterium.
Кроме того, изобретение касается также применения полученного на описанной выше стадии g3) высушенного материала для получения корма или добавки к корму.
Объектом данного изобретения является также применение выделенного согласно изобретению метионина для получения пищевых продуктов или кормов, или добавок к пищевым продуктам или кормам.
Кроме того, изобретение касается также содержащей метионин высушенной биомассы, получаемой описанным выше способом; добавок к кормам, включающих такую биомассу; а также композиций кормов, которые наряду с обычными компонентами кормов содержат также такую добавку.
Ниже описаны другие варианты выполнения изобретения.
С) Используемые согласно изобретению клетки-хозяин
Для осуществления способа согласно изобретению используют предпочтительно булавообразные бактерии. Предпочтительно ими являются бактерии вида Corynebacterium. В частности следует назвать род Corynebacterium glutamicum, который известен специалистам своей способностью вырабатывать L-аминокислоту.
Примерами подходящих штаммов являются:
из вида Corynebacterium:
Corynebacterium glutamicum ATCC 13032, Corynebacterium acetoglutamicum ATCC 15806, Corynebacterium acetoacidophilum ATCC 13870, Corynebacterium thermo-aminogenes FERM BP-1539, Corynebacterium melassecola ATCC 17965; Corynebacterium glutamicum KFCC10065; или Corynebacterium glutamicum ATCC21608
из вида Brevibacterium:
Brevibacterium flavum ATCC 14067; Brevibacterium lactofermentum ATCC 13869 и Brevibacterium divaricatum ATCC 14020;
(KFCC=Korean Federation of Culture Collection (Корейская Федерация Коллекции Культур); ATCC = American Type Culture Collection (Американская Коллекция Видов Культур); FERM BP = Sammlung des National institute of Bioscience and Human-Technology, Agency of Industrial Science and Technology, Japan (собрание Национального Института Биологической Науки и Гуманитарной Технологии, Агентство Промышленной Науки и Технологии, Япония))
При этом штаммы бактерий могут быть использованы в естественной форме или генетически модифицированы. Так, например, могут быть использованы микроорганизмы, в которых увеличена концентрация генов биосинтеза метионина, так что клетка содержит большее количество метионина. Альтернативно или дополнительно могут быть исключены или ослаблены те гены, которые участвуют в разлагающем метионин обмене веществ. Подходящие стратегии усовершенствования способов выработки метионина известны из уровня техники и описаны, например, в WO-A-02/10209, DE-A-10217058, DE-A-10239308, DE-A-10239073, DE-A-10239082 и DE-A-10222858, на которые тут существуют определенные ссылки.
С целью снижения активности или количества фермента, который может уменьшать содержание метионина, специалисты могут применять различные отдельные меры или их комбинации. Снижение транскрипционной способности гена, который кодирует белок согласно изобретению, может уменьшать концентрацию соответствующего белка. Специалисты могут достигать этого путем изменения или замены региона промотора или регулятора, а также места присоединения рибосом кодирующего гена. Вдоль кодирующего региона специалист может менять терминаторы или вводить последовательности, которые уменьшают стабильность транскрипта. Эти меры, уменьшающие продолжительность жизни мРНК, дают возможность снизить экспрессию соответствующего белка, а также его концентрацию.
На уровне экспрессии фермента объединенные последовательности могут приводить к повышению уровня распада и, таким образом, к снижению концентрации белка. Кроме того, благодаря целенаправленному или нецеленаправленному мутагенезу кодирующего гена специалисты могут изменять активность, сродство и специфичность субстратов. Мутации в соответствующих генах могут таким образом влиять на активность ферментов, что приводит к частичному или полному снижению скорости ферментативной реакции. Примеры таких мутаций известны специалистам (Motoyama Н. Yano Н. Terasaki Y. Anazawa Н. Applied & Environmental Microbiology. 67:3064-70, 2001, Eikmanns BJ. Eggeling L. Sahm Н. Antonie van Leeuwenhoek. 64:145-63, 1993-94). Мутанты белка могут также уменьшать или предотвращать гомо- или гетеромультиметамеризация ферментативных комплексов и таким образом ухудшать ферментативные свойства.
Модифицированные таким образом гены могут быть интегрированы в плазмиды или предпочтительно в хромосому. При этом дополнительно может содержаться также первичный не модифицированный ген, который, однако, предпочтительно заменяют модифицированным геном.
С целью снижения активности фермента в булавообразной бактерии достаточным может оказаться осуществление экспрессии генов, кодирующих функциональные эквиваленты, такие как синтетически полученные мутанты или естественные гомологи из других организмов. При этом первичный ген также может присутствовать, однако, предпочтительно его заменяют модифицированным или гомологичным геном.
Кроме того, для бактериальной выработки менионина предпочтительным может быть увеличение концентрации одного или нескольких ферментов биосинтеза метионина, обмена веществ цистеина, синтеза аспартатсемиальдегида, гликолиза, репарации, обмена веществ пентоза-фосфата, цикла лимонной кислоты или переноса аминокислоты.
Так, для получения метионина может быть увеличена концентрация одного или нескольких следующих ген:
- ген lysC, кодирующий аспартаткиназу (ЕР 1108790 А2; ДНК-SEQ №281),
- ген asd, кодирующий аспартат-семиальдегид (ЕР 1108790 А2; ДНК-SEQ №282),
- ген gap, кодирующий глицеринальдегид-3-фосфат (Eikmanns (1992), Journal of Bacteriology 174: 6076-6086),
- ген pgk, кодирующий 3-фосфоглицкрат киназу (Eikmanns (1992), Journal of Bacteriology 174: 6076-6086),
- ген рус, кодирующий пируват карбоксилазу (Eikmanns (1992), Journal of Bacteriology 174: 6076-6086),
- ген tpi, кодирующий триозафосфат изомеразу (Eikmanns (1992), Journal of Bacteriology 174:6076-6086),
- ген metA, кодирующий гомосерин O-ацетилтрансферазу (ЕР 1108790 А2; ДНК-SEQ №725),
- ген metB, кодирующий цистатионин-гамма-синтазу (ЕР 1108790 А2; ДНК-SEQ №3491),
- ген metC, кодирующий цистатионин-гамма-лиазу (ЕР 1108790 А2; ДНК-SEQ №3061),
- ген metH, кодирующий цистатионин-синтазу (ЕР 1108790 А2; ДНК-SEQ №1663),
- ген glyA, кодирующий серин-гидроксиметилтрансферазу (ЕР 1108790 А2; ДНК-SEQ №1110),
- ген metY, кодирующий O-ацетилгомосерин-сульфгидрилазу (ЕР 1108790 А2; ДНК-SEQ №726),
- ген metF, кодирующий метилентетрагидрофолат-редуктазу (ЕР 1108790 А2; ДНК-SEQ №2379),
- ген serC, кодирующий фосфосерин-аминотрансферазу (ЕР 1108790 А2; ДНК-SEQ №928),
- ген serB, кодирующий фосфосерин-фосфатазу (ЕР 1108790 А2; ДНК-SEQ №334, ДНК-SEQ №467, ДНК-SEQ №2767)
- ген cysE, кодирующий серии ацетил-трансферазу (ЕР 1108790 А2; ДНК-SEQ №2818),
- ген cysK, кодирующий цистеин-синтазу (ЕР 1108790 А2; ДНК-SEQ №2817),
- ген hom, кодирующий гомосерин-дегидрогеназу (ЕР 1108790 А2; ДНК-SEQ №1306).
Дополнительно предпочтительной для получения метионина согласно изобретению может быть мутация, по меньшей мере, одного из перечисленных ниже ген таким образом, что метаболиты обмена веществ незначительно или совсем не влияют на активность соответствующих белков по сравнению с немутированными белками или их специфическая активность повышается:
- ген lysC, кодирующий аспартаткиназу (ЕР 1108790 А2; ДНК-SEQ №281),
- ген рус, кодирующий пируват карбоксилазу (Eikmanns (1992), Journal of Bacteriology 174: 6076-6086),
- ген metA, кодирующий гомосерин O-ацетилтрансферазу (ЕР 1108790 А2; ДНК-SEQ №725),
- ген metB, кодирующий цистатионин-гамма-синтазу (ЕР 1108790 А2; ДНК-SEQ №3491),
- ген metC, кодирующий цистатионин-гамма-лиазу (ЕР 1108790 А2; ДНК-SEQ №3061),
- ген metH, кодирующий метионин-синтазу (ЕР 1 108 790 А2; ДНК-SEQ №1663),
- ген glyA, кодирующий серин-гидроксиметилтрансферазу (ЕР 1108790 А2; ДНК-SEQ №1110),
- ген metY, кодирующий O-ацетилгомосерин-сульфгидрилазу (ЕР 1108790 А2; ДНК-SEQ №726),
- ген metF, кодирующий метилентетрагидрофолат-редуктазу (ЕР 1108790 А2; ДНК-SEQ №2379),
- ген serC, кодирующий фосфосерин-аминотрансферазу (ЕР 1108790 А2; ДНК-SEQ №928),
- ген serB, кодирующий фосфосерин-фосфатазу (ЕР 1108790 А2; ДНК-SEQ №334, ДНК-SEQ №467, ДНК-SEQ №2767),
- ген cysE, кодирующий серин ацетил-трансферазу (ЕР 1108790 А2; ДНК-SEQ №2818),
- ген cysK, кодирующий цистеин-синтазу (ЕР 1108790 А2; ДНК-SEQ №2817),
- ген hom, кодирующий гомосерин-дегидрогеназу (ЕР 1108790 А2; ДНК-SEQ №1306)
Кроме того, предпочтительным для выработки метионина может оказаться ослабление одного или нескольких указанных ниже генов, в частности, снижение их экспрессии, или их исключение:
- ген metK, кодирующий S-аденосилметионин-синтазу (Е.С.2.5.1.6),
- ген thrB, кодирующий гомосерин-киназу (ЕР 1108790 А2; ДНК-SEQ №3453),
- ген ilvA, кодирующий треонин дегидратазу (ЕР 1108790 А2; ДНК-SEQ №2328),
- ген thrC, кодирующий треонин синтазу (ЕР 1108790 А2; ДНК-SEQ №3486),
- ген ddh, кодирующий мезо-диаминопимелат D-дегидрогеназу (ЕР 1108790 А2; ДНК-SEQ №3494),
- ген pck, кодирующий фосфоэнопируват-карбоксикиназу (ЕР 1108790 А2; ДНК-SEQ №3157),
- ген pgi, кодирующий глюкоза-6-фосфат-6-изомеразу (ЕР 1108790 А2; ДНК-SEQ №950),
- ген рохВ, кодирующий пируват-оксидазу (ЕР 1 108 790 А2; ДНК-SEQ №2873),
- ген dapA, кодирующий дигидродипиколинат синтазу (ЕР 1108790 А2; ДНК-SEQ №3476),
- ген dapB, кодирующий дигидродипиколинат редуктазу (ЕР 1108790 А2; ДНК-SEQ №3477),
- ген lysA, кодирующий диаминопиколинат декарбоксилазу (ЕР 1108790 А2; ДНК-SEQ №3451)
Кроме того, предпочтительной для выработки метионина может быть мутация, по меньшей мере, одного из указанных выше генов metK, thrB, ilvA, thrC, ddh, pck, pgi, рохВ, dapA, dapB, lysA, что частично или полностью снижает ферментативную активность соответствующего белка.
Кроме того, предпочтительным для выработки метионина может оказаться исключение других нежелательных побочных реакций (Nakayama: "Breeding of Amino Acid Producing Microorganisms", in: Overproduction of Microbial Products, Krumphanzl, Sikyta, Vanek (eds.). Academic Press, London, UK, 1982).
Для достижения сверхэкспрессии специалисты могут применять различные отдельные меры или их комбинацию. Так, например, можно увеличивать число копий соответствующих генов или подвергать мутации регион промотора или регулятора или место присоединения рибосом, которое располагается вверх по направлению к структурному гену. Подобным образом действуют экспрессионные кассеты, встроенные вверх по направлению к структурному гену. Благодаря индуцируемым промоторам дополнительно можно увеличивать экспрессию в процессе ферментативной выработки L-метионина. Кроме того, экспрессия улучшается также при увеличении продолжительности существования мРНК. Предотвращая распад ферментативного белка, также можно увеличить ферментативную активность. Гены или генные конструкты могут находиться в плазмидах с различным количеством копий или быть интегрированными в хромосому и усилены. Альтернативно сверхэкспрессии соответствующих генов можно достигать изменением композиции среды и водом культуры.
В этой связи необходимые указания приведены, например, в таких литературных источниках под редакцией Martin и др. (Biotechnology 5, 137-146 (1987)), Guerrero и др. (Gene 138, 35-41 (1994)), Tsuchiya и Morinaga (Biotechnology 6, 428-430 (1988)), Eikmanns и др. (Gene 102, 93-98 (1991)), в ЕР 0472869, US 4,601,893, Schwarzer и Pünier (Biotechnology 9, 84-87 (1991)), Remscheid и др. (Applied and Environmental Microbiology 60,126-132 (1994)), LaBarre и др. (Journal of Bacteriology 175, 1001-1007 (1993)), в WO 96/15246, Malumbres и др. (Gene 134, 15-24 (1993)), в JP-A-10-229891, в Jensen и Hammer (Biotechnology and Bioengineering 58, 191-195 (1998)), Makrides (Microbiological Reviews 60:512-538 (1996)) и известных учебниках по генетике и молекулярной биологии.
D) Осуществление ферментации согласно изобретению
Полученные согласно изобретению микроорганизмы могут быть непрерывно или периодически культивированы периодическим способом (периодическая культивация) или способом подпитки (способ темперирования), или способом неоднократной подпитки (способ циклического темперирования) для выработки метионина. Информация о известных методах культивации приведена в пособии по редакцией Chmiel (Bioprozeβtechnik 1. Einführung in die Bioverfahrenstechnik (Gustav Fischer Verlag, Stuttgart, 1991)) или в учебнике под редакцией Storhas (Bioreaktoren und periphere Einrichtungen (Vieweg Verlag, Braunschweig/Wiesbaden, 1994)).
Используемая культурная среда должна определенным образом соответствовать требованиям соответствующих штаммов. Культурная среда различных микроорганизмов описана в справочнике "Manual of Methods fur General Bacteriology" der American Society für Bacteriology (Washington D.C., USA, 1981).
Эти среды, которые могут быть использованы согласно изобретению, как правило, включают один или несколько источником углерода, источников азота, неорганических солей, витаминов и/или микроэлементов.
Предпочтительными источниками углерода являются сахара, такие как моно-, ди- или полисахариды. Особенно предпочтительными источниками углерода являются например, глюкоза, фруктоза, манноза, галактоза, рибоза, сорбоза, рибулоза, лактоза, мальтоза, сахароза, раффиноза, крахмал или целлюлоза. Кроме того, сахар можно также добавлять в среду в виде комплексных соединений, таких как меласса, или других побочных продуктах рафинирования сахара. Предпочтительным также может быть добавление смесей различных источников углерода. Другими возможными источниками углерода являются масла и жиры, такие как, например, соевое масло, подсолнечное масло, арахисовое масли и кокосовое масло; жирные кислоты, такие как, например, пальмитиновая, стеариновая или линолевая кислота; спирты, такие как, например, глицерин, метанол или этанол; и органические кислоты, такие как, например, уксусная кислота или молочная кислота.
Источниками азота являются, как правило, органические или неорганические соединения азота, материалы, которые содержат эти соединения. Примерами источников азота являются газообразный аммиак или аммониевые соли, такие как сульфат аммония, хлорид аммония, фосфат аммония, карбонат аммония или нитрат аммония, нитраты, карбамиды, аминокислоты или комплексные источники азота, такие как кукурузный экстракт, соевая мука, соевый белок, дрожжевой экстракт, мясной экстракт и другие. Источники азота могут быть использованы отдельно или в виде смеси.
Неорганические соединения солей, которые могут содержаться в среде, включают хлориды, фосфаты или сульфаты кальция, магния, натрия, кобальта, молибдена, калия, марганца, цинка, меди и железа.
В качестве источника серы для получения метионина могут быть использованы неорганические, содержащие серу соединения, такие как, например, сульфаты, сульфиты, дитиониты, тетратиониты, тиосульфаты, сульфиды, а также органические соединения серы, такие как меркаптаны и тиолы.
Источником фосфора могут быть фосфорная кислота, гидрофосфат калия или двукалиевая соль ортофосфорной кислоты или соответствующие содержащие натрий соли.
В среду можно также добавлять хелатирующий агент с целью удерживания ионов металла в растворе. Особенно предпочтительными хелатирующими агентами являются дигидроксифенолы, такие как пирокатехин или протокатеховая кислота, или органические кислоты, такие как лимонная кислота.
Применяемые согласно изобретению ферментационные среды содержат, как правило, и другие обычные факторы роста, такие как витамины или стимуляторы роста, к которым, например, принадлежит биотин, рибофлавин, тиамин, фолиевая кислота, никотиновая кислота, пантотенат и пиридокасин. Факторы роста и соли входят в состав комплексных компонентов среды, таких как дрожжевой экстракт, меласса, кукурузный экстракт и т.п. Кроме того, в культурную среду могут быть добавлены подходящие предстадии. Точный состав соединений среды большей частью зависит от соответствующего эксперимента и для каждого случая выбирается индивидуально. Информация, касающаяся оптимизации среды, приведена в "Applied Microbiol. Physiology, A Practical Approach" (Hrsg. P.M. Rhodes, P.F.Stanbury, IRL Press (1997) S. 53-73, ISBN 0 19 963577 3). Среды роста могут быть приобретены у коммерческих оферентов, например, Standard 1 (Merck) или BHI (Brain heart infusion, DIFCO) и т.п.
Все компоненты среды стерилизуют термически (20 мин при 1,5 бар и 121°С) или стерилизацией при фильтровании. Компоненты могут быть стерилизованы вместе или, в случае необходимости, отдельно. На начальной стадии культивации можно использовать все компоненты среды или, в случае необходимости, добавлять их непрерывно или периодически.
Температура культуры, как правило, составляет от 15°С до 45°С, предпочтительно от 25°С до 40°С, она может быть постоянной при проведении эксперимента или может меняться. Значение pH среды должно составлять от 5 до 8,5, предпочтительно около 7,0. Значение pH в процессе выращивания можно контролировать добавлением основных соединений, таких как гидроксид натрия, гидроксид калия, аммиак или аммиачная вода, или кислотных соединений, таких как фосфорная кислота или серная кислота. Для контролирования пенообразования могут быть использованы антивспениватели, такие как, например, полигликолевые эфиры жирных кислот. Для поддержания стабильности плазмид в среду могут быть введены соответствующие вещества селективного действия, такие как, например, антибиотики. Для поддержания аэробных условий в культуру добавляют кислород или содержащие кислород газовые смеси, такие как, например, окружающий воздух. Культуру используют до тех пор, пока не образуется максимальное количество желаемого продукта. Как правило, для этого требуется от 10 до 160 часов.
Содержание высушенной массы в полученных таким образом содержащих метионин ферментационных бульонах, как правило, составляет от 7,5 до 25 вес.%.
Кроме того, предпочтительным является способ, согласно которому ферментацию, по меньшей мере, в конце, в частности, по меньшей мере, после осуществления 30% процесса ферментации проводят при ограничении количества сахара. Это означает, что в течение этого времени концентрацию пригодного для использования сахара держат на уровне от ≥0 до 3 г/л или снижают.
Е) Очистка метионина
Если полученный выкристаллизацией согласно изобретению метионин не имеет желаемую чистоту, то его можно очистить. С этой целью продукт в растворенной форме подвергают хроматографии на соответствующей смоле, причем желаемый продукт или примеси полностью или частично остаются в хроматографической смоле. Такое хроматографирование, в случае необходимости, может быть осуществлено повторно, причем используют одни и те же или разные хроматографические смолы. Специалисты хорошо знакомы с выбором соответствующей хроматографической смолы и ее эффективным применением. Очищенный продукт можно концентрировать фильтрацией или ультрафильтрацией и сохранять при температуре, при которой достигается максимальная стабильность продукта.
Идентичность и чистоту выделенного соединения можно определять известными методами. Они включают высокоэффективную жидкостную хроматографию (ВЭЖХ), спектроскопические способы, способы окрашивания, тонкослойную хроматографию, БИКС, ферментивный анализ или микробиологические исследования. Эти способы анализа описаны в: Patek др. (1994) Appl. Environ. Microbiol. 60:133-140; Malakhova et al. (1996) Biotekhnologiya 11 27-32-, и Schmidt и др. (1998) Bioprocess Engineer. 19:67-70. Ulmann's Encyclopedia of Industrial Chemistry (1996) Bd. A27, VCH: Weinheim, S. 89-90, S. 521-540, S. 540-547, S. 559-566, 575-581 и S. 581-587; Michal, G (1999) Biochemical Pathways: An Atlas of Biochemistry and Molecular Biology, John Wiley and Sony, Fallon, A. и др. (1987) Applications of HPLC in Biochemistry in: Laboratory Techniques in Biochemistry and Molecular Biology, Bd. 17.
F) Сушка биомассы
После завершения ферментации, содержащий метионин, ферментационный бульон можно непосредственно перерабатывать на готовую сухую добавку к корму. Согласно предпочтительной форме осуществления изобретения сначала из ферментационного бульона полностью или частично, предпочтительно полностью, выделяют часть биомассы, например, центрифугированием и перерабатывают на добавку к корму согласно изобретению. Полученная биомасса содержит дополнительно определенное количество метионина, которое, в случае необходимости, можно уменьшать подключением промежуточной стадии промывки.
Переработку биомассы согласно изобретению на соответствующий высушенный продукт можно осуществлять различными известными из уровня техники способами. В частности, подходящими являются способы сушки, такие как распылительная сушка, распылительная грануляция, контактная сушка, сушка в псевдоожиженном слое или сушка вымораживанием. Соответствующие способы описаны, например, в: О.Krischer, W.Kast, Trocknungstechnik Erster Band, "Die wissenschaftlichen Grundlagen der Trocknungstechnik″, Springer-Verlag 1978; Krischer/Kröll, Trocknungstechnik Zweiter Band, ″Trockner und Trocknungsverfahren", Springer-Verlag 1959; К. Kröll, W. Kast, Trocknungstechnik Dritter Band, "Trocknen und Trockner in der Produktion″, Springer-Verlag 1989; К.Masters, "Spray Drying Handbook", Longman Scientific & Technical 1991, 725 Seiten; H. Uhlemann, L. Mörl, "Wirbelschicht - Sprühgranulation″, Springer-Verlag 2000; Gefriertrocknung: Georg-Wilhelm Oetjen. ″Gefriertrocknen″, VCH 1997, а также ЕР-А-0809940. На эти публикации тут существуют определенные ссылки.
Особенно предпочтительно стадию сушки согласно изобретению осуществляют в виде распылительной сушки, например распылительной сушки с интегрированным псевоожиженным слоем, или распылительной грануляции.
При желании сушку можно осуществлять в присутствии подходящего для корма носителя, использование которого, в частности, может улучшить сыпучесть и таким образом качество продукта.
В качестве подходящих для корма носителей могут быть использованы обычные инертные носители. "Инертный" носитель не должен вступать ни в какое нежелательное взаимодействие с содержащимися в добавке пищевыми добавками и должен быть особенно выгодно использован в качестве вспомогательного вещества в добавках к кормам. Как примеры подходящих носителей следует назвать: неорганические или органические соединения естественного или синтетического происхождения. Примерами подходящих низкомолекулярных неорганических носителей являются соли, такие как хлорид натрия, карбонат кальция, сульфат натрия и сульфат магния, или кремниевая кислота. Примерами подходящих органических носителей являются, в частности, сахара, такие как, например, глюкоза, фруктоза, сахароза, а также декстрин и продукты крахмала. Примерами высокомолекулярных органических носителей соединения крахмала и целлюлозы, такие как, в частности, кукурузный крахмал, мука из зерна злаковых культур, например, мука из пшеницы, ржи, ячменя и овса, или их смеси или отруби шлифовочно-размольных систем. Носитель может содержаться в препарате, в пересчете на высушенный материал, в количестве приблизительно от 5 до 85 вес.%, например, приблизительно от 10 до 30 вес.%, от 20 до 40 вес.% или от 50 до 85 вес.%.
Ниже в общих чертах коротко описаны некоторые предпочтительные технологии сушки.
Распылительную сушку можно осуществлять таким образом, что сначала еще влажную биомассу закачивают в распылитель башни для распылительной сушки. Распыление осуществляют, например, при помощи распыляющего сопла (однокомпонентное сопло), двухкомпонентного сопла или центробежного распылителя. Сушку капель осуществляют с помощью подаваемого для распылительной сушки потока горячего воздуха. При использовании центробежных распылителей сушку осуществляют предпочтительно прямотоком. В случае сопел сушку можно осуществлять также противотоком или пульсирующим током. Высушенный порошок можно выгружать из башни или подавать в поток воздуха и выделять из циклона и/или фильтра. В зависимости от продукта и методов действия необходимой может быть дополнительная сушка, которую можно осуществлять в интерном, прифланцованном к устройству распылительной сушки или экстерном псевдоожиженном слое.
Согласно другому варианту осуществления способа сушки согласно изобретению к стадии сушки, в частности, распылительной сушки, последовательно присоединена стадия непрерывной или периодический агломерации в псевдоожиженном слое. С этой целью в сушилку с псевдоо