Фармацевтические композиции замедленного высвобождения, содержащие аплиндор и его производные
Иллюстрации
Показать всеИзобретение относится к области фармацевтики и касается лекарственного средства для перорального применения для лечения расстройств допаминергической системы, включающего аплиндор и один или несколько замедляющих высвобождение полимеров. Лекарственное средство обеспечивает снижение побочных эффектов от введения аплиндора. 6 н. и 36 з.п. ф-лы, 13 табл.
Реферат
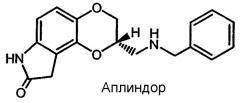
Настоящее изобретение относится к фармацевтическим композициям замедленного высвобождения допаминергических соединений, включающих S-2-[(бензиламино)метил]-2,3,8,9-тетрагидро-7H-1,4-диоксино[2,3-e]индол-8-он (аплиндор) и его фармацевтически приемлемые соли.
Сообщалось, что соединения, имеющие структуру 2-(аминометил)-2,3,8,9-7Н4-диоксино[2,3-e]индол-8-она, обладают значительной активностью в отношении допаминового рецептора, а также способностью модулировать синтез допамина. См. патент США 5756532, введенный посредством ссылки во всей его полноте для всех целей. Эти соединения полезны для лечения и профилактики различных допаминергических расстройств, включающих шизофрению, шизоаффективное расстройство, симптомы болезни Паркинсона, синдром Туретта, психоз при болезни Льюиса-Боди, психоз при болезни Альцгеймера, гиперлактинемию, наркоманию и острую манию при биполярных расстройствах. Мощный и селективный частичный агонист D2/D3 аплиндор (S-2-[(бензиламино)метил]-2,3,8,9-тетрагидро-7H-1,4-диоксино[2,3-e]индол-8-он) был идентифицирован как лекарственное средство для больных шизофренией.
Введение аплиндора приводит к высоким начальным концентрациям лекарственного средства. Такая картина "немедленного” высвобождения может создать трудности, которые включают невозможность поддерживать оптимальные уровни воздействия во времени и неприятные побочные эффекты ввиду наличия слишком большой начальной дозы. Таким образом, имеется значительная потребность в композициях аплиндора регулируемого высвобождения, способных к повышению Тмакс и/или уменьшению Смакс без снижения суммарного воздействия лекарственного средства. Данное изобретение направлено на достижение этих, а также других важных целей.
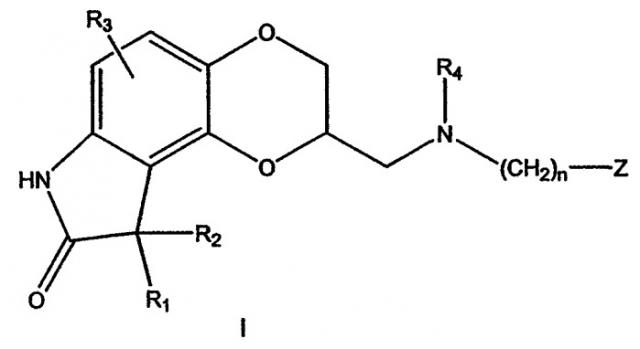
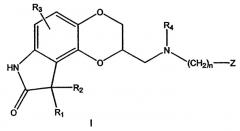
В некоторых вариантах осуществления настоящее изобретение предлагает лекарственные препараты регулируемого высвобождения, содержащие соединение формулы I:
в которой:
R1 и R2 независимо представляют водород, алкил с 1-6 атомами углерода, фенил или бензил;
или R1 и R2, взятые вместе, представляют бензилиден, необязательно замешенный R3, который определен ниже, или алкилиден, имеющий до 6 атомов углерода;
или R1 и R2, взятые вместе с атомом углерода, к которому они присоединены, образуют карбонильный фрагмент или циклоалкильную группу, имеющую от 3 до 6 атомов углерода;
R3 представляет водород, гидрокси, галоген, трифторметил, трифторметокси, алкил с 1-6 атомами углерода, алкокси с 1-6 атомами углерода, арилалкокси с 7-12 атомами углерода, алканоилокси с 2-6 атомами углерода, аминогруппу, моно- или диалкиламиногруппу, в которой каждая алкильная группа имеет от 1 до 6 атомов углерода, алканамидо с 2-6 атомами углерода или алкансульфонамидо с 1-6 атомами углерода;
R4 представляет водород или алкил с 1-6 атомами углерода;
n равно одному из целых чисел 0, 1, 2, 3, 4, 5 или 6;
Z представляет водород, гидрокси, алкил с 1-6 атомами углерода, алкенил с 2-6 атомами углерода, алкинил с 2-6 атомами углерода, алкокси с 1-6 атомами углерода, циклоалкил с 3-8 атомами углерода, полициклический алкил с 7-15 атомами углерода, фенил, необязательно замещенный R3, как определено выше, феноксигруппу, необязательно замещенную R3, как определено выше, нафтил, необязательно замещенный R3, как определено выше, или нафтилоксигруппу, необязательно замещенную R3, как определено выше, гетероарил или гетероарилоксигруппу, в которой гетероциклическое кольцо гетероарильной или гетероарилоксигруппы выбрано из тиофена, фурана, пиридина, пиразина, пиримидина, индола, индазола, имидазола, хромана, кумарина, карбостирила, хинолина, бензиоксазола, бензоксазола, пиразола, пиррола, тиазола, оксазола или изоксазола и гетероциклическое кольцо необязательно замещено R3, как определено выше,
или его фармацевтически приемлемую соль.
В некоторых предпочтительных вариантах осуществления настоящего изобретения соединением является 2-[(бензиламино)метил]-2,3,8,9-тетрагидро-7H-1,4-диоксино[2,3-e]индол-8-он или его фармацевтически приемлемая соль. В некоторых особо предпочтительных вариантах осуществления настоящего изобретения соединением является S-2-[(бензиламино)метил]-2,3,8,9-тетрагидро-7H-1,4-диоксино[2,3-e]индол-8-он (аплиндор) или его фармацевтически приемлемая соль.
В некоторых предпочтительных вариантах осуществления настоящего изобретения каждым из описываемых лекарственных препаратов регулируемого высвобождения соединением является аплиндора фумарат.
В некоторых вариантах осуществления настоящего изобретения лекарственный препарат регулируемого высвобождения представляет собой пероральную дозированную композицию.
В некоторых вариантах осуществления настоящего изобретения препарат содержит одну или несколько микрочастиц, которые могут быть, например, пилюлями, бусинами, таблетками, сфероидами или сочетанием двух или более из них.
В некоторых вариантах осуществления лекарственных препаратов регулируемого высвобождения для перорального применения настоящего изобретения соединение высвобождается из указанной дозированной формы со скоростью, эффективной для того, чтобы увеличить время достижения максимальной терапевтической концентрации (т.е. Тмакс) по сравнению с Тмакс лекарственного препарата мгновенного высвобождения, например, так, чтобы Тмакс композиции регулируемого высвобождения было по меньшей мере примерно в 1,5 раза, 2 раза, 3 раза, 4 раза, 5 раз или 6,5 раз больше, чем Тмакс лекарственного препарата мгновенного высвобождения.
В некоторых вариантах осуществления настоящего изобретения соединение высвобождается из указанной дозированной формы со скоростью, эффективной для того, чтобы снизить максимальную терапевтическую концентрацию указанного соединения (т.е. Смакс) по сравнению с Смакс лекарственного препарата мгновенного высвобождения, например, так, чтобы Смакс препарата регулируемого высвобождения была меньше, чем примерно 0,75, 0,60, 0,50 или 0,40 от Смакс лекарственного препарата мгновенного высвобождения.
В некоторых вариантах осуществления лекарственных препаратов регулируемого высвобождения для перорального применения настоящего изобретения соединение высвобождается из препарата со скоростью, эффективной для того, чтобы увеличить фармацевтически эффективную концентрацию соединения в млекопитающем в течение периода времени (т.е. площадь под кривой (ППК) зависимости концентрации в плазме (сыворотке или крови) от времени, такая как ППК0-12) относительно лекарственного препарата мгновенного высвобождения, например, так, чтобы ППК0-12 препарата регулируемого высвобождения было по меньшей мере примерно в 1,05 раз, 1,2 раза, 1,3 раза или 1,4 раза больше чем ППК0-12 лекарственного препарата мгновенного высвобождения.
В некоторых вариантах осуществления настоящего изобретения соединение высвобождается из 0,1 мг дозированной формы со скоростью, эффективной для обеспечения площади под кривой (ППК) зависимости концентрации в плазме (сыворотке или крови) от времени от нуля до 12 часов (ППК0-12) примерно от 260 пкг*ч/мл до примерно 2400 пкг*ч/мл, тогда как для других таких вариантов осуществления ППК0-12 составляет примерно от 290 пкг*ч/мл до примерно 1300 пкг*ч/мл. ППК может быть измерена так, как описано в Principles of Drug Action: The Basis of Pharmacology, 3rd Ed., W.B. Pratt & P. Taylor, eds. (Churchill Livingstone: New York) 1990. В некоторых вариантах осуществления настоящего изобретения 5 мг соединения обеспечивают ППКss (площадь под кривой в стационарном состоянии от 0 до 12 часов) примерно от 36000 пкг*ч/мл до примерно 109000 пкг*ч/м, тогда как другие обеспечивают ППКss примерно от 36000 пкг*ч/мл до примерно 75000 пкг*ч/мл. В некоторых вариантах осуществления настоящего изобретения 30 мг соединения обеспечивают ППК0-12 примерно от 121000 пкг*ч/мл до примерно 890000 пкг*ч/мл, тогда как другие такие осуществления настоящего изобретения обеспечивают ППК0-12 примерно от 170000 пкг*ч/мл до примерно 760000 пкг*ч/мл.
В некоторых вариантах осуществления настоящего изобретения соединение высвобождается из 0,1 мг дозированной формы со скоростью, эффективной для обеспечения максимальной концентрации в плазме (сыворотке или крови) (Смакс) примерно от 40 пкг/мл до примерно 190 пкг/мл, и в других таких вариантах осуществления примерно от 40 пкг/мл до примерно 180 пкг/мл. Максимальную концентрацию в плазме измеряли так, как описано в Principles of Drug Action: The Basis of Pharmacology, 3rd Ed., W.B. Pratt & P. Taylor, eds. (Churchill Livingstone: New York) 1990; Human Pharmacology: Molecular to Clinic, K. Kist, ed. (Mosby-Year Books: Philadelphia, 1991. В некоторых вариантах осуществления настоящего изобретения 5 мг соединения обеспечивают Смакс примерно от 4000 пкг/мл до примерно 14000 пкг/мл, тогда как в других таких вариантах осуществления Смакс составляет примерно от 6000 пкг/мл до примерно 12000 пкг/мл. В некоторых вариантах осуществления настоящего изобретения 30 мг соединения обеспечивают Смакс примерно от 18000 пкг/мл до примерно 110000 пкг/мл; в других таких вариантах осуществления Смакс составляет примерно от 20000 пкг/мл до примерно 92000 пкг/мл.
В некоторых вариантах осуществления настоящего изобретения дозы постепенно увеличивали (т.е. титровали) во времени (например, сутки или недели) до желаемой дозы, чтобы избежать или уменьшить тяжесть возможных побочных эффектов, таких как тошнота или другие проявления непереносимости у пациента. Например, некоторые варианты осуществления настоящего изобретения предлагают вводить увеличивающиеся дозы с постепенным приращением, где начальная доза находится в интервале примерно от 0,05 мг до примерно 0,4 мг в сутки. В других вариантах осуществления дозы увеличивают с постепенным приращением за период времени до конечной дозы, какова она есть, или в каждый последующий день вводят более высокую дозу, которая может находиться в интервале, например, от 2 мг до 75 мг в сутки. В других вариантах осуществления период титрования дозы до достижения конечной дозы составляет по меньшей мере около 3 суток, по меньшей мере около 5 суток, по меньшей мере около 12 суток или по меньшей мере около 15 суток.
В других вариантах осуществления применяют набор дозированных форм регулируемого высвобождения, который содержит множество отдельных дозированных форм регулируемого высвобождения, где две или более из указанных отдельных дозированных форм содержат различные количества соединения. Отдельная дозированная форма может быть одной единичной дозой (например, одной таблеткой или капсулой) или может включать многократные единичные дозы (например, 2 или более таблеток или капсул). В некоторых вариантах осуществления настоящего изобретения набор дозированных форм регулируемого высвобождения имеет 2 или более отдельных дозированных форм регулируемого высвобождения, содержащих начальную дозу и конечную дозу (где конечную дозу или дозу с большим количеством вводят по дням позднее, и конечная доза выше начальной дозы). Например, набор может содержать две или более различные отдельные дозированные формы регулируемого высвобождения, в диапазоне примерно от 0,05 мг до примерно 30 мг соединения. В других вариантах осуществления набор лекарственных препаратов регулируемого высвобождения имеет по меньшей мере две или более отдельных дозированных форм, выбранных из 0,05 мг, 0,1 мг, 0,2 мг, 0,25 мг, 0,3 мг, 0,4 мг, 0,5 мг, 0,6 мг, 0,75 мг, 1 мг, 1,5 мг, 2 мг, 3 мг, 4 мг, 5 мг, 6 мг, 8 мг, 10 мг, 11 мг, 12 мг, 13 мг, 14 мг, 15 мг, 16 мг, 17 мг, 20 мг, 23 мг, 24 мг, 25 мг, 26 мг или 30 мг указанного соединения.
В некоторых вариантах осуществления настоящего изобретения набор дозированных форм регулируемого высвобождения имеет по меньшей мере две отдельные дозированные формы регулируемого высвобождения, содержащие различное количество соединения, причем количество соединения в каждой из различных дозированных форм отличается по меньшей мере на десять процентов, и, более предпочтительно, по меньшей мере на 20 процентов. В других вариантах осуществления каждая из отдельных дозированных форм обеспечивает ППК0-12 в интервале примерно от 260 пкг*ч/мл до примерно 890000 пкг*ч/мл.
В некоторых вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения содержат по меньшей мере некоторое количество микрочастиц, которые включают инертное ядро, слой активного соединения, отложенный на инертное ядро, и покрытие, включающее по меньшей мере один регулирующий скорость высвобождения полимер, нанесенное на слой соединения. В некоторых вариантах осуществления настоящего изобретения все микрочастицы включают инертное ядро, слой соединения и покрытие.
В некоторых вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения содержат по меньшей мере некоторое количество микрочастиц, которые включают инертное ядро, слой покрытия, нанесенный на инертное ядро, слой покрытия, включающий соединение и по меньшей мере один регулирующий скорость высвобождения полимер. В некоторых вариантах осуществления настоящего изобретения все микрочастицы включают инертное ядро и покрывающий слой.
В следующих вариантах осуществления препараты регулируемого высвобождения для перорального применения содержат по меньшей мере некоторое количество микрочастиц, которые включают ядро, которое включает активное соединение, и слой покрытия, нанесенный на ядро, включающий по меньшей мере один регулирующий скорость высвобождения полимер. В некоторых вариантах осуществления настоящего изобретения все микрочастицы включают ядро, которое содержит соединение, и покрывающий слой.
В некоторых вариантах осуществления лекарственных препаратов регулируемого высвобождения для перорального применения настоящего изобретения процентное содержание по массе активного соединения в композиции составляет примерно от 1% до примерно 25%, предпочтительно примерно от 2% до примерно 15%, предпочтительно примерно от 5% до примерно 10%.
В некоторых вариантах осуществления лекарственных препаратов регулируемого высвобождения для перорального применения настоящего изобретения препарат включает капсулы, содержащие микрочастицы. В некоторых вариантах осуществления настоящего изобретения микрочастицы спрессованы в таблетку или пилюлю.
В некоторых вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения включают одну или несколько гранул. В некоторых вариантах осуществления настоящего изобретения гранулы дополнительно включают покрытие, которое дополнительно включает по меньшей мере один регулирующий скорость высвобождения полимер. В некоторых вариантах осуществления настоящего изобретения гранулы содержатся внутри капсулы.
В некоторых вариантах осуществления лекарственных препаратов регулируемого высвобождения для перорального применения настоящего изобретения препарат дополнительно содержит один или несколько ингредиентов, выбранных из наполнителей, дезинтегрантов, эксципиентов и сочетаний двух или нескольких из них. В некоторых вариантах осуществления настоящего изобретения гранулы и ингредиенты спрессовывают в таблетки.
В некоторых вариантах осуществления лекарственных препаратов регулируемого высвобождения для перорального применения настоящего изобретения процентное содержание по массе активного соединения в препарате составляет примерно от 1% до примерно 25%, предпочтительно примерно от 2% до примерно 15%, предпочтительно примерно от 5% до примерно 10%.
В некоторых вариантах осуществления лекарственных препаратов регулируемого высвобождения для перорального применения настоящего изобретения препарат включает восковую матрицу, предпочтительно, когда препарат представляет собой таблетку. В некоторых вариантах осуществления настоящего изобретения воск присутствует в количестве по массе примерно от 10 до примерно 60%, предпочтительно примерно от 20% до примерно 40%.
В некоторых вариантах осуществления настоящего изобретения воск включает воск карнаба, цетостеариловый спирт, жирные кислоты или смесь двух или нескольких из них. В некоторых вариантах осуществления настоящего изобретения содержащее воск средство дополнительно включает по меньшей мере один регулирующий скорость высвобождения полимер.
В некоторых вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения включают полиэтиленоксидную матрицу, предпочтительно, когда форма представляет собой таблетку. В некоторых вариантах осуществления настоящего изобретения таблетка включает полиэтиленоксидную матрицу.
В некоторых вариантах осуществления настоящего изобретения полиэтиленоксид присутствует в количестве по массе примерно от 5 до примерно 40%, предпочтительно примерно от 10% до примерно 20% от средства.
В некоторых вариантах осуществления настоящего изобретения лекарственный препарат регулируемого высвобождения представляет собой таблетку, которая включает по меньшей мере один регулирующий скорость высвобождения полимер. В некоторых предпочтительных вариантах осуществления настоящего изобретения дозированная форма представляет собой совместно спрессованную таблетку. В некоторых предпочтительных вариантах осуществления настоящего изобретения совместно спрессованная таблетка включает ядро и внешнее спрессованное покрытие, где ядро включает активное соединение и по меньшей мере один регулирующий скорость высвобождения полимер. В следующих вариантах осуществления совместно спрессованная таблетка включает ядро и внешнее спрессованное покрытие, где спрессованное покрытие включает по меньшей мере один регулирующий скорость высвобождения полимер. В некоторых предпочтительных вариантах осуществления настоящего изобретения совместно спрессованная таблетка включает ядро и внешнее спрессованное покрытие, где каждое из ядра и спрессованного покрытия включает активное соединение и по меньшей мере один независимо выбранный регулирующий скорость высвобождения полимер. В некоторых предпочтительных вариантах осуществления настоящего изобретения ядро и внешнее спрессованное покрытие каждое содержит по меньшей мере одну образующую матрицу гидроксипропилметилцеллюлозу высокой вязкости, и по меньшей мере одну образующую матрицу гидроксипропилметилцеллюлозу низкой вязкости. Предпочтительно, образующий матрицу полимер низкой вязкости включает гидроксипропилметилцеллюлозу, выбранную из Methocel K100LV, Methocel E50LV, Methocel E5, Methocel E15LV или комбинации двух или нескольких из них, и образующий матрицу полимер высокой вязкости включает гидроксипропилметилцеллюлозу, выбранную из Methocel K4M, Methocel K15M, Methocel K100M, Methocel E4M или комбинаций двух или нескольких из них. В некоторых особо предпочтительных вариантах осуществления настоящего изобретения образующий матрицу полимер низкой вязкости включает Methocel K100LV, и образующий матрицу полимер высокой вязкости включает Methocel K4M.
В некоторых вариантах осуществления лекарственных препаратов регулируемого высвобождения для перорального применения настоящего изобретения препарат включает по меньшей мере один образующий матрицу полимер, который предпочтительно выбирают из восков, смол, гидроксипропилметилцеллюлоз, гтдроксиэтилцеллюлоз, гидроксипропилцеллюлоз, карбаполов, полиметилакрилатов, полиэтиленоксидов и комбинаций двух или нескольких из них.
В некоторых вариантах осуществления лекарственных препаратов регулируемого высвобождения для перорального применения настоящего изобретения активное соединение содержится в количестве примерно от 0,02% до примерно 16 мас.%, предпочтительно примерно от 0,02% до примерно 4% от массы препарата.
В некоторых вариантах осуществления лекарственных препаратов регулируемого высвобождения для перорального применения настоящего изобретения препараты включают одну гидроксипропилметилцеллюлозу высокой вязкости и одну гидроксипропилметилцеллюлозу низкой вязкости. Предпочтительно образующий матрицу полимер высокой вязкости включает гидроксипропилметилцеллюлозу, выбранную из Methocel K4M, Methocel K15M, Methocel K100M, Methocel E4M и комбинаций двух или нескольких из них. Предпочтительно гидроксипропилметилцеллюлоза присутствует в количестве по массе примерно от 15% до примерно 80%, предпочтительно примерно от 25% до примерно 50%, и предпочтительно представляет собой Methocel K4M. Предпочтительно гидроксипропилметилцеллюлоза низкой вязкости включает Methocel K100LV, Methocel E50LV, Methocel E5, Methocel E15LV или комбинацию двух или нескольких из них, предпочтительно в количестве по массе примерно от 15% до примерно 80%, предпочтительно примерно от 20% до примерно 50%, и предпочтительно представляет собой Methocel K100LV.
В некоторых вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения могут содержать водорастворимый эксципиент, предпочтительно в количестве по массе вплоть до 50%, предпочтительно в количестве по массе примерно от 2% до примерно 25%. В некоторых предпочтительных вариантах осуществления эксципиентом является сахар.
В некоторых вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения могут включать диспергируемый в воде эксципиент, которым предпочтительно является микрокристаллическая целлюлоза, коллоидальная двуокись кремния, силицированная микрокристаллическая целлюлоза, крахмал, сверхдезинтегрант или комбинация двух или нескольких из них. Предпочтительно диспергируемый в воде эксципиент присутствует в количестве по массе примерно от 2% до примерно 50%, предпочтительно примерно от 5% до примерно 25%.
В некоторых вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения включают один или несколько антиоксидантов, стабилизаторов, хелатирующих агентов, модификаторов кислотного рН, модификаторов щелочного рН или комбинации двух или нескольких из них.
В некоторых вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения включают одно или несколько связующих, агентов, повышающих текучесть, лубрикантов или модификаторов растворимости, которыми может являться поверхностно-активное вещество, кислотное соединение или щелочное соединение.
В некоторых вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения включают покрытие, которое включает водорастворимый полимер и краситель и/или рН-зависимый полимер, регулирующий скорость высвобождения, рН-независимый полимер, регулирующий скорость высвобождения, или их комбинацию.
В некоторых из предшествующих лекарственных препаратов регулируемого высвобождения для перорального применения дозированная форма включает один или несколько регулирующих скорость высвобождения полимеров, которыми могут быть, например, один или несколько из полиметилакрилатов, сополимеров метакриловой кислоты - эфира метакриловой кислоты, фталата ацетата целлюлозы, этилцеллюлозы, фталата поливинилацетата, фталата гидроксипропилметилцеллюлозы или комбинаций двух или нескольких из них. В некоторых предпочтительных вариантах осуществления настоящего изобретения регулирующим скорость высвобождения полимером может быть один или несколько из полиметилакрилатов, сополимеров метакриловой кислоты - эфира метакриловой кислоты, этилцеллюлозы или комбинаций двух или нескольких из них.
В следующих вариантах осуществления регулирующий скорость высвобождения полимер выбирают из образующих матрицу гидроксипропилметилцеллюлоз высокой вязкости, и из образующих матрицу гидроксипропилметилцеллюлоз низкой вязкости
В некоторых вариантах осуществления настоящего изобретения образующую матрицу гидроксипропилметилцеллюлозу высокой вязкости выбирают из Methocel K4M, Methocel K15M, Methocel K100M, Methocel E4M и комбинаций двух или нескольких из них.
В некоторых вариантах осуществления настоящего изобретения образующую матрицу гидроксипропилметилцеллюлозу низкой вязкости выбирают из Methocel K100LV, Methocel E50LV, Methocel E5, Methocel E15LV и комбинаций двух или нескольких из них.
В некоторых вариантах осуществления настоящего изобретения регулирующий скорость высвобождения полимер включает один или несколько из Eugradit RS, Eugradit RL, сюрелеазы или комбинацию двух или нескольких из них.
В некоторых вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения содержат один или несколько из модификаторов растворимости, например поверхностно-активных веществ, кислотных соединений, основных соединений и их комбинации.
В некоторых вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения содержат один или несколько из антиоксидантов, модификаторов рН, агентов, образующих хелаты металлов, или комбинации двух или нескольких из них.
В следующих вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения могут содержать один или несколько из наполнителей, дезинтегрантов, связующих или комбинации двух или нескольких из них.
В некоторых вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения содержат один или несколько наполнителей, связующих, дезинтегрантов, лубрикантов, стабилизаторов, модификаторов рН, антиоксидантов или комбинации двух или нескольких из них.
В некоторых предпочтительных вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения содержат фармацевтически эффективное количество активного соединения, гидроксипропилметилцеллюлозу высокой вязкости в количестве примерно от 20% до примерно 60 мас.%, и гидроксипропилметилцеллюлозу низкой вязкости в количестве примерно от 20% до примерно 60 мас.%.
В некоторых следующих вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения содержат фармацевтически эффективное количество активного соединения, водорастворимый компенсирующий эксципиент в количестве примерно от 0,5% до примерно 5 мас.%, диспергируемый в воде эксципиент в количестве примерно от 5% до примерно 30 мас.%, гидроксипропилметилцеллюлозу высокой вязкости в количестве примерно от 20% до примерно 60 мас.%, и гидроксипропилметилцеллюлозу низкой вязкости в количестве примерно от 20% до примерно 60 мас.% и, необязательно, лубрикант в количестве примерно от 0,1 до примерно 1 мас.%.
В некоторых следующих предпочтительных вариантах осуществления препараты регулируемого высвобождения для перорального применения настоящего изобретения содержат фармацевтически эффективное количество активного соединения, диспергируемый в воде эксципиент в количестве примерно от 10% до примерно 30 мас.%, гидроксипропилметилцеллюлозу высокой вязкости в количестве примерно от 20% до примерно 40 мас.% и гидроксипропилметилцеллюлозу низкой вязкости в количестве примерно от 20% до примерно 40 мас.% и, необязательно, лубрикант в количестве примерно от 0,1 до примерно 1 мас.%.
В некоторых вариантах осуществления настоящее изобретение предоставляет способы лечения расстройства допаминэргической системы, которые включают введение нуждающемуся в таком лечении пациенту лекарственного препарата регулируемого высвобождения согласно изобретению.
В некоторых следующих вариантах осуществления настоящее изобретение предоставляет способы лечения шизофрении, шизоаффективного расстройства, болезни Паркинсона, синдрома Туретта, психоза при болезни Льюиса-Боди, психоза при болезни Альцгеймера, гиперлактинемии, наркомании и острой мании при биполярных расстройствах, включающие введение нуждающемуся в таком лечении пациенту лекарственного препарата регулируемого высвобождения согласно изобретению.
В некоторых следующих вариантах осуществления настоящее изобретение предлагает способы лечения симптомов болезни Паркинсона, включающие введение нуждающемуся в таком лечении пациенту лекарственного средства регулируемого высвобождения согласно изобретению.
Настоящее изобретение предоставляет также способы получения предлагаемых лекарственных препаратов и продукты этих способов.
Настоящее изобретение предоставляет лекарственные препараты регулируемого высвобождения, которые содержат в качестве активного ингредиента соединение формулы I:
в которой составляющие переменные являются такими, как описано выше.
Термин "активное соединение”, как использовано в данном описании, предназначен для обозначения соединений формулы I и, в частности, 2-[(бензиламино)метил]-2,3,8,9-тетрагидро-7H-1,4-диоксино[2,3-e]индол-8-она, S-2-[(бензиламино)метил]-2,3,8,9-тетрагидро-7H-1,4-диоксино[2,3-e]индол-8-она (аплиндора) и их фармацевтически приемлемых солей, предпочтительно, но без ограничения, фумаратных солей, и пролекарств предшествующих соединений.
Описанные в данном описании лекарственные препараты обеспечивают регулируемое высвобождение активных соединений у млекопитающего при различных путях введения, включая пероральное введение. В некоторых предпочтительных вариантах осуществления настоящего изобретения лекарственные препараты включают соединение S-2-[(бензиламино)метил]-2,3,8,9-тетрагидро-7H-1,4-диоксино[2,3-e]индол-8-он, называемое аплиндором, предпочтительно, его фумаратную соль.
Аплиндор может образовывать фармацевтически приемлемые соли с различными кислотами, включая неорганические кислоты, такие как хлористоводородная кислота, бромистоводородная кислота, фосфорная кислота, хлорная кислота, азотная кислота, йодистая кислота и т.п., а также органические кислоты, такие как щавелевая кислота, фумаровая кислота, янтарная кислота, уксусная кислота, бензойная кислота, гликолевая кислота, яблочная кислота, лимонная кислота, метансульфоновая кислота, бензолсульфоновая кислота, салициловая кислота, паратолуолсульфоновая кислота, адипиновая кислота и т.п. Композиции, включающие все такие соли, входят в объем настоящего изобретения.
Термин "пролекарство”, как использовано в данном описании, имеет привычное значение ковалентно модифицированного производного соединения или его фармацевтически приемлемой соли, где такая модификация дает в результате производное, которое является метаболически лабильным и после ввода млекопитающему приводит в результате к высвобождению родительского соединения в кишечнике, плазме или ткани. Такие производные могут быть получены этерификацией, ацилированием или модификацией соединения иным способом так, чтобы ввести физиологически подвижную группу.
Аплиндор содержит один хиральный центр и используется преимущественно в виде S-изомера. Однако активность присуща также и R-изомеру. Лекарственные препараты настоящего изобретения включают оба изомера и не ограничены одним энантиомером или конкретной энантиомерной смесью.
Для целей данного изобретения термины "мгновенное высвобождение”, "форма мгновенного высвобождения” относятся к лекарственным препаратам, которые обеспечивают быстрое и непостепенное высвобождение активного соединения из препарата, т.е. к лекарственным препаратам, которые содержат активное соединение и быстро растворяющийся носитель, который не замедляет высвобождение активного соединения из препарата. Такой лекарственный препарат мгновенного высвобождения или не имеет регулирующих скорость высвобождения полимеров или других веществ, которые замедляют высвобождение активного соединения из препарата, или содержит такие полимеры и вещества в количествах, которые достаточно малы, чтобы высвобождение активного соединения из препарата не замедлялось относительно других, во всем остальном идентичных лекарственных препаратов, лишенных таких полимеров или веществ. Одним из примеров такого препарата "мгновенного высвобождения” является активное соединение, примешанное к микрокристаллической целлюлозе Avicel, что дает в результате более чем 75%-ное растворение аплиндора или его фармацевтически приемлемой соли в 0,1N растворе HCl за менее чем 0,25 часа, как описано ниже.
Термины "медленное высвобождение”, "умеренное высвобождение” и "быстрое высвобождение” представляют препараты регулируемого высвобождения, которые описаны выше, которые высвобождают активное соединение со скоростью, являющейся медленной, умеренной или быстрой в отношении друг другу.
Термины "регулируемое высвобождение”, "форма регулируемого высвобождения”, "лекарственный препарат регулируемого высвобождения” и т.п. относятся к препаратам, которые содержат средства, замедляющие высвобождение активного соединения из препарата относительно препарата "мгновенного высвобождения”, который описан выше, например, относительно во всем остальном идентичного препарата, лишенного регулирующих скорость высвобождения полимеров или других замедляющих высвобождение веществ. Таким образом, термин "регулируемое высвобождение” может прилагаться к любому числу лекарственных препаратов продолжительного высвобождения и должен рассматриваться как по существу синоним высвобождению с задержкой, высвобождению во времени, пролонгированному высвобождению, программированному во времени высвобождению, высвобождающимся во времени, высвобождению с временным покрытием, замедленному высвобождению, медленному действию, длительному действию, действию с задержкой, разнесенному высвобождению, разнесенному во времени высвобождению, продленно действующему, продленному действию и т.п.
Должно быть понятно, что препараты регулируемого высвобождения могут привести в результате к высвобождению активного соединения из дозированной формы со скоростью, эффективной для увеличения времени, которое требуется, чтобы достичь максимальной терапевтической концентрации
(т.е. Тмакс) по сравнению с Тмакс лекарственного препарата мгновенного высвобождения, так, например, что Тмакс препарата регулируемого высвобождения составляет по меньшей мере примерно 1,5, 2, 2,5, 3, 4,5 или 5,5 Тмакс лекарственного препарата мгновенного высвобождения. Препараты регулируемого высвобождения могут также приводить в результате к высвобождению активного соединения из дозированной формы со скоростью cнижения максимальной терапевтической концентрации указанного соединения (т.е. Смакс) по сравнению с Смакс лекарственного препарата мгновенного высвобождения, например, так, что Смакс препарата регулируемого высвобождения составляет менее чем примерно 0,75, 0,60, 0,50 или 0,40 от Смакс лекарственного препарата мгновенного высвобождения. Препараты регулируемого высвобождения могут также давать в результате высвобождение активного соединения из дозированной формы со скоростью, эффективной для повышения фармацевтически эффективной концентрации соединения у млекопитающего за период времени (т.е. площади под кривой, ППК, зависимости концентрации в плазме (сыворотке или крови) от времени, такой
как ППК0-12) относительно лекарственного препарата мгновенного высвобождения, например, так, что ППК0-12 препарата регулируемого высвобождения составляет по меньшей мере примерно 1,05, 1,1, 1,2, 1,3 или 1,4 от ППК0-12 лекарственного препарата мгновенного высвобождения.
Величины "Смакс", "Тмакс” и "ППК”, приведенные в данном описании, если не указано, что они являются "средними" значениями, относятся к значениям, наблюдавшимся у отдельного пациента. Кроме того, величины Смакс, Тмакс и ППК, если не указано иное, могут быть значениями, наблюдавшимися в стационарном состоянии при дозировании через регулярные промежутки времени (например, каждые 12 часов) в течение многих дней (например, введение многократных доз) или значениями при однократном введении.
Термин "регулирующий скорость высвобождения полимер”, как использован