Полинуклеотид, кодирующий ацилтрансферазу, отвечающую за модификацию платенолида в положении 3 (варианты), полипептид, представляющий собой ацилтрансферазу, отвечающую за модификацию платенолида в положении 3 (варианты), бактериальный экспрессионный вектор (варианты), бактериальная экспрессионная система, бактериальная клетка-хозяин, способ продуцирования полипептида, штамм streptomyces ambofaciens, применение полинуклеотида (варианты), клетка бактерии streptomyces ambofaciens, клетка-хозяин streptomyces ambofaciens и способ получения полипептида
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, конкретно к выделению и идентификации новых генов пути биосинтеза спирамицинов и к новым полипептидам, участвующим в этом биосинтезе, и может быть использовано для получения ацилтрансферазы, отвечающей за модификацию платенолида в положении 3. Полинуклеотидом, кодирующим ацилтрансферазу, которая отвечает за модификацию платенолида в положении 3, трансформируют клетки бактерии рода Streptomyces и получают штамм-продуцент целевого полипептида. Изобретение позволяет повысить степень продуцирования и чистоту продуцируемого спирамицина. 18 н. и 8 з.п. ф-лы, 41 ил., 44 табл.
Реферат
Настоящее изобретение относится к выделению и идентификации новых генов пути биосинтеза спирамицинов и к новым полипептидам, участвующим в этом биосинтезе. Оно также относится к применению этих генов с целью увеличения степени продуцирования и чистоты получаемого спирамицина.
Изобретение относится также к применению этих генов для конструкции мутантов, которые могут приводить к синтезу новых антибиотиков или к производным формам спирамицинов. Изобретение относится также к молекулам, продуцируемым за счет экспрессии этих генов, и, наконец, к фармакологически активным композициям, включающим молекулу, продуцируемую за счет экспрессии таких генов.
Streptomyces представляют собой грамположительные филаментозные бактерии почвы. Они играют важную роль в деструкции и минерализации органических материалов благодаря большому разнообразию расщепляющих ферментов, которые они выделяют. Они обладают явлениями единственных в своем роде морфологических дифференцировок в прокариотах, сопровождающихся метаболической дифференцировкой, характеризующейся продуцированием вторичных метаболитов, обладающих огромным разнообразием химических структур и биологических активностей. Среди этих метаболитов находят спирамицины, продуцируемые в нативном состоянии бактерией Streptomyces ambofaciens.
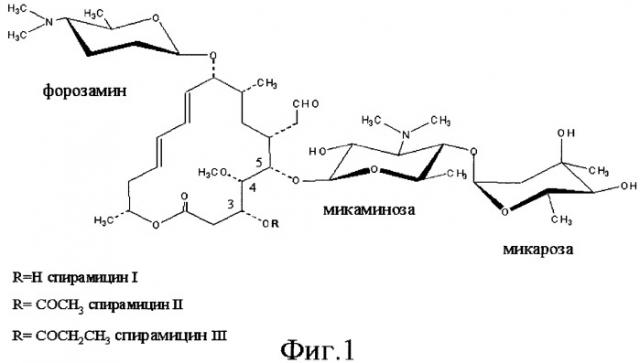
Спирамицин представляет собой антибиотик семейства макролидов, пригодный как в ветеринарии, так и в медицине. Макролиды характеризуются наличием лактонового цикла, к которому привиты один или несколько сахаров. Streptomyces ambofaciens в нативном состоянии продуцирует спирамицины I, II и III (см. фиг.1), однако, антибиотическая активность спирамицина I отчетливо выше таковой спирамицинов II и III (Liu и др., 1999). Молекула спирамицина I образована лактоновым макроциклом, называемым платенолидом, и тремя сахарами: форозамином, микаминозой и микарозой (см. фиг.1). Антибиотическая активность спирамицинов возникает вследствие ингибирования протеинового синтеза в прокариотах за счет механизма, приводящего к связыванию антибиотика с бактериальной рибосомой.
Некоторые соединения, являющиеся членами семейства макролидов и имеющие также лактоновый цикл, можно использовать в области антибиотиков. Так, продукт FK506 обладает иммуносупрессорными эффектами и открывает перспективы терапевтического использования в области трансплантации органов, ревматоидного артрита и, вообще, в случае патологий, связанных с аутоиммунными реакциями. Другие макролиды, как авермектин, обладают инсектицидными и антигельминтными активностями.
Многочисленные пути биосинтеза, касающиеся антибиотиков, принадлежащих к различным классам, а также других вторичных метаболитов (согласно обзору, Chater K., 1990), на сегодняшний день уже изучены в случае Streptomyces. Однако знание путей биосинтеза спирамицинов в настоящее время является только очень частичным.
Биосинтез спирамицинов представляет собой сложный процесс, включающий многочисленные стадии и опосредуемый многочисленными ферментами (Omura и др., 1979а; Omura и др., 1979b). Спирамицины относятся к большому классу поликетидов, который объединяет комплексные молекулы, особенно изобилующие в микроорганизмах почвы. Эти молекулы объединяют не по аналогии структуры, а по некоторому подобию на уровне стадий пути их биосинтеза. В самом деле, поликетиды продуцируются комплексным рядом реакций, но в пути их биосинтеза совместно обладают рядом реакций, катализируемых ферментом или ферментами, называемыми “поликетидсинтазами” (PKS). В случае Streptomyces ambofaciens биосинтез лактонового макроцикла спирамицинов (платенолид) протекает через ряд из восьми модулей, кодируемых пятью разными генами PKS (Kuhstoss S., 1996; патент США 5945320). Спирамицины образуются из этого лактонового цикла. Однако различные стадии и ферменты, участвующие в синтезе сахаров, а также их связывание с лактоновым циклом и модификация этого цикла для получения спирамицинов на сегодняшний день остаются еще неизвестными.
В патенте США 5514544 описывается клонирование последовательности, называемой srmR, в Streptomyces ambofaciens. В этом патенте высказывается гипотеза, что ген srmR кодирует протеин-регулятор транскрипции генов, участвующих в биосинтезе макролидов.
В 1987 г. Richardson и сотрудники (Richardson и др, 1987) показали, что резистентность к спирамицину S. ambofaciens придается по меньшей мере тремя генами, причем эти последние были названы srmA, srmB и srmC. В патенте США 4886757 в особенности описывается характеристика фрагмента ДНК S. ambofaciens, содержащего ген srmC. Однако последовательность этого гена не была представлена. В 1990 г. Richardson и сотрудники (Richardson и др., 1990) предложили гипотезу о существовании трех генов биосинтеза спирамицина, близких к srmB. В патенте США 5098837 сообщается о клонировании пяти генов, потенциально участвующих в биосинтезе спирамицина. Эти гены были названы srmD, srmE, srmF, srmG и srmH.
Одна из больших трудностей при получении таких соединений, как спирамицины, заключается в том, что для получения относительно незначительного количества продукта необходимы очень большие объемы при ферментации. Следовательно, желательно иметь возможность повышать эффективность получения таких молекул в целях снижения издержек производства.
Путь биосинтеза спирамицинов представляет собой сложный процесс и желательно идентифицировать и ликвидировать паразитические реакции, которые могут протекать во время этого процесса. Целью такой манипуляции является получение более чистого антибиотика и/или повышение производительности. По этому поводу, Streptomyces ambofaciens в нативном состоянии продуцирует спирамицины I, II и III (см. фиг.1), однако, антибиотическая активность спирамицина I отчетливо выше таковой спирамицинов II и III (Liu и др., 1999). Следовательно, желательно иметь возможность располагать штаммами, продуцирующими только спирамицин I.
Ввиду коммерческого интереса к макролидным антибиотикам проводятся интенсивные исследования в отношении получения новых производных, в частности, аналогов спиромицинов, обладающих предпочтительными свойствами. Желательно иметь возможность генерировать в достаточном количестве медиаторы пути биосинтеза спирамицинов или производных спирамицинов, в частности, с целью получения гибридных антибиотиков, происходящих от спирамицинов.
Общее описание изобретения
Настоящее изобретение основано на клонировании генов, продукт которого участвует в биосинтезе спирамицинов. Изобретение относится, прежде всего, к новым генам пути биосинтеза спирамицинов и новым полипептидам, участвующим в этом биосинтезе.
Были клонированы гены пути биосинтеза и ассоциированные кодирующие последовательности и была определена последовательность ДНК каждого. Клонированные кодирующие последовательности в дальнейшем обозначают как orf1*c, orf2*c, orf3*c, orf4*c, orf5*, orf6*, orf7*c, orf8*, orf9*, orf10*, orf1, orf2, orf3, orf4, orf5, orf6, orf7, orf8, orf9c, orf10, orf11c, orf12, orf13c, orf14, orf15c, orf16, orf17, orf18, orf19, orf20, orf21c, orf22c, orf23c, orf24c, orf25c, orf26, orf27, orf28c, orf29, orf30c, orf31, orf32c, orf33 и orf34c. Функция протеинов, кодируемых этими последовательностями, в пути биосинтеза спирамицинов раскрывается в нижеприводимом обсуждении, которое поясняется фиг.4, 5, 6 и 8.
1) Первый объект изобретения относится к полинуклеотиду, кодирующему полипептид, участвующий в биосинтезе спирамицинов, отличающемуся тем, что последовательность вышеуказанного полинуклеотида представляет собой:
(а) одну из последовательностей SEQ ID № 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 28, 30, 34, 36, 40, 43, 45, 47, 49, 53, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 107, 109, 111, 113, 115, 118, 120, 141, 143, 145, 147 и 149,
(b) одну из последовательностей, образованных вариантами последовательностей (а);
(с) одну из последовательностей, происходящих от последовательностей (а) и (b) в соответствии с вырожденностью генетического кода.
2) Объектом настоящего изобретения также является полинуклеотид, гибридизующийся в условиях гибридизации высокой жесткости по меньшей мере с одним из полинуклеотидов согласно вышеприведенному п.1).
3) Изобретение относится также к полинуклеотиду, обладающему по меньшей мере 70%, 80%, 85%, 90%, 95% или 98% идентичности по нуклеотидам с полинуклеотидом, включающим по меньшей мере 10, 12, 15, 18, 20-25, 30, 40, 50, 60, 70, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1050, 1100, 1150, 1200, 1250, 1300, 1350, 1400, 1450, 1500, 1550, 1600, 1650, 1700, 1750, 1800, 1850 или 1900 последовательных нуклеотидов полинуклеотида согласно вышеприведенному п.1).
4) Изобретение также относится к полинуклеотиду согласно вышеприведенному п.2) или 3), отличающемуся тем, что он выделен из бактерии рода Streptomyces.
5) Изобретение относится также к полинуклеотиду по вышеприведенному п.2), 3 или 4, отличающемуся тем, что он кодирует протеин, участвующий в биосинтезе макролида.
6) Изобретение также относится к полинуклеотиду по вышеприведенному п.2), 3) или 4), отличающемуся тем, что он кодирует протеин, обладающий активностью, подобной протеину, кодируемому полинуклеотидом, с которым он гибридизуется или обладает идентичностью.
7) Изобретение также относится к полипептиду, образующемуся в результате экспрессии полинуклеотида по вышеприведенному п.1), 2), 3), 4), 5) или 6).
8) Следующий аспект изобретения относится к полипептиду, участвующему в биосинтезе спирамицинов, отличающемуся тем, что последовательность вышеуказанного полипептида представляет собой:
(а) одну из последовательностей SEQ ID № 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 27, 29, 31, 32, 33, 35, 37, 38, 39, 41, 42, 44, 46, 48, 50, 51, 52, 54, 55, 56, 57, 58, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 108, 110, 112, 114, 116, 117, 119, 121, 142, 144, 146, 148 и 150,
(b) одну из последовательностей, таких как указанные в п.(а), если не считать того, что по всей длине вышеуказанной последовательности одна или несколько аминокислот заменены, встроены или подвергнуты делеции без затрагивания функциональных свойств;
(с) одну из последовательностей, образованных вариантами последовательностей (а) и (b).
9) Другой аспект изобретения относится к полипептиду, обладающему по меньшей мере 70%, 80%, 85%, 90%, 95% или 98% идентичности по аминокислотам с полипептидом, включающим по меньшей мере 10, 15, 20, 30-40, 50, 60, 70, 80, 90, 100, 120, 140, 160, 180, 200, 220, 240, 260, 280, 300, 320, 340, 360, 380, 400, 420, 440, 460, 480, 500, 520, 540, 560, 580, 600, 620 или 640 последовательных аминокислот полипептида согласно вышеприведенному п.8).
10) Еще один аспект изобретения относится к полипептиду по вышеприведенному п.9), отличающемуся тем, что он выделен из бактерии рода Streptomyces.
11) Другой аспект изобретения относится к полипептиду по вышеприведенному п.9) или 10), отличающемуся тем, что он кодирует протеин, участвующий в биосинтезе макролида.
12) Следующий аспект изобретения относится к полипептиду по вышеприведенному п.9), 10) или 11), отличающемуся тем, что он обладает активностью, подобной таковой полипептида, с которым он имеет идентичность.
13) Еще один аспект изобретения относится к рекомбинантной ДНК, отличающейся тем, что она включает по меньшей мере один полинуклеотид по любому из вышеприведенных п.п.1), 2), 3), 4), 5) или 6).
14) Другой аспект изобретения относится к рекомбинантной ДНК по вышеприведенному п.13, отличающейся тем, что указанная рекомбинантная ДНК встроена в вектор.
15) Следующий аспект изобретения относится к рекомбинантной ДНК по вышеприведенному п.14, отличающейся тем, что вышеуказанный вектор выбирают среди бактериофагов, плазмид, фагемид, интегрирующих векторов, фосмид, космид, шаттл-векторов, ВАС или РАС.
16) Другой аспект изобретения относится к рекомбинантной ДНК по вышеприведенному п.15, отличающейся тем, что ее выбирают среди pOS49.1, pOS49.11, pOSC49.12, pOS49.14, pOS49.16, pOS49.28, pOS44.1, pOS44.2, pOS44.4, pSPM5, pSPM7, pOS49.67, pOS49.88, pOS49.106, pOS49.120, pOS49.107, pOS49.32, pOS49.43, pOS49.44, pOS49.50, pOS49.99, pSPM17, pSPM21, pSPM502, pSPM504, pSPM507, pSPM508, pSPM509, pSPM1, pBXL1111, pBXL1112, pBXL1113, pSPM520, pSPM521, pSPM522, pSPM523, pSPM524, pSPM525, pSPM527, pSPM528, pSPM34, pSPM35, pSPM36, pSPM37, pSPM38, pSPM39, pSPM40, pSPM41, pSPM42, pSPM43, pSPM44, pSPM45, pSPM47, pSPM48, pSPM50, pSPM51, pSPM52, pSPM53, pSPM55, pSPM56, pSPM58, pSPM72, pSPM73, pSPM515, pSPM519, pSPM74, pSPM75, pSPM79, pSPM83, pSPM107, pSPM543 и pSPM106.
17) Следующий аспект изобретения относится к экспрессирующему вектору, отличающемуся тем, что он включает по меньшей мере одну нуклеотидную последовательность, кодирующую полипептид по вышепривденному п.7), 8), 9), 10), 11) или 12).
18) Изобретение также относится к экспрессионной системе, включающей соответствующий экспрессирующий вектор и клетку-хозяина, позволяющей осуществлять экспрессию одного или нескольких полипептидов по вышеприведенному п.7), 8), 9), 10), 11) или 12.
19) Изобретение также относится к экспрессионной системе по вышеприведенному п.18, отличающейся тем, что ее выбирают из прокариотных экспрессионных систем или эукариотных экспрессирующих систем.
20) Изобретение также относится к экспрессионной системе по вышеприведенному п.19), отличающейся тем, что ее выбирают из экспрессионных систем бактерии E.coli, бакуловирусных экспрессионных систем, позволяющих осуществлять экспрессию в клетках насекомых, экспрессиионных систем, позволяющих осуществлять экспрессию в дрожжевых клетках, экспрессионных систем, позволяющих осуществлять экспрессию в клетках млекопитающих.
21) Изобретение также относится к клетке-хозяину, в которую введен по меньшей мере один полинуклеотид и/или по меньшей мере одна рекомбинантная ДНК и/или по меньшей мере один экспрессирующий вектор по любому из вышеприведенных п.п.1), 2), 3), 4), 5), 6), 13), 14), 15), 16) или 17.
22) Изобретение также относится к способу продуцирования полипептида по вышеприведенному п.7), 8), 9), 10), 11) или 12), отличающемуся тем, что вышеуказанный способ включает следующие стадии:
а) инсерция по меньшей мере одной нуклеиновой кислоты, кодирующей вышеуказанный полипептид, в соответствующий вектор;
b) культивирование, на соответствующей культуральной среде, клетки-хозяина, предварительно трансформированной или трансфектированной вектором со стадии а);
с) рекуперация кондиционированной культуральной среды или клеточного экстракта;
d) выделение и очистка из вышеуказанной культуральной среды или еще из клеточного экстракта, полученной(ного) на стадии с), вышеуказанного полипептида;
е) в желательном случае, охарактеризовывание продуцированного рекомбинантного полипептида.
23) Другой аспект изобретения относится к микроорганизму, блокируемому на стадии пути биосинтеза по меньшей мере одного макролида.
24) Следующий аспект изобретения относится к микроорганизму по вышеприведенному п.23), отличающемуся тем, что его получают путем инактивации функции по меньшей мере одного протеина, участвующего в биосинтезе этого или этих макролидов в микроорганизме, являющемся продуцентом этого или этих макролидов.
25) Другой аспект изобретения относится к микроорганизму по вышеприведенному п.24), отличающемуся тем, что инактивацию этого протеина или этих протеинов осуществляют путем мутагенеза в гене или генах, кодирующих вышеуказанный или вышеуказанные протеины, или путем экспрессии одной или нескольких антисмысловых РНК, комплементарных РНК или матричным РНК, кодирующим вышеуказанный или вышеуказанные протеины.
26) Другой аспект изобретения относится к микроорганизму по вышеприведенному п.25, отличающемуся тем, что инактивацию этого или этих протеинов осуществляют за счет мутагенеза путем облучения, путем воздействия мутагенного химического агента, путем направленного мутагенеза или путем замены гена.
27) Следующий аспект изобретения относится к микроорганизму по вышеприведенному п.25) или 26), отличающемуся тем, что мутагенез или мутаганезы осуществляют in vitro или in situ путем супрессии, замены, делеции и/или инсерции одного или нескольких оснований в случае рассматриваемого гена или рассматриваемых генов или путем генной инактивации.
28) Еще один аспект изобретения относится к микроорганизму по вышеприведенному п.23), 24), 25), 26) или 27), отличающемуся тем, что вышеуказанным микроорганизмом является бактерия рода Streptomyces.
29) Другой аспект изобретения относится к микроорганизму по вышеприведенному п.23), 24), 25), 26), 27) или 28), отличающемуся тем, что макролидом является спирамицин.
30) Другой аспект изобретения относится к микроорганизму по вышеприведенному п.23), 24), 25), 26), 27), 28) или 29, отличающемуся тем, что вышеуказанным микроорганизмом является штамм S. ambofaciens.
31) Другой аспект изобретения относится к микроорганизму по вышеприведенному п.23), 24), 25), 26), 27), 28), 29) или 30), отличающемуся тем, что мутагенез осуществляют по меньшей мере в гене, включающем последовательность по любому из вышеуказанных п.п.1), 2), 3), 4), 5) или 6).
32) Следующий аспект изобретения относится к микроорганизму по вышеприведенному п.25), 26), 27), 28), 29), 30) или 31, отличающемуся тем, что мутагенез осуществляют в одном или нескольких генах, включающих одну из последовательностей, соответствующих одной или нескольким последовательностям SEQ ID № 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 28, 30, 34, 36, 40, 43, 45, 47, 49, 53, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 107, 109, 111, 113, 115, 118, 120, 141, 143, 145, 147 и 149.
33) Другой аспект изобретения относится к микроорганизму по вышеприведенному п.25), 26), 27), 28), 29), 30), 31) или 32, отличающемуся тем, что мутагенез состоит в генной инактивации гена, включающего последовательность, соответствующую проследовательности SEQ ID № 13.
34) Другой аспект изобретения относится к штамму Streptomyces ambofaciens, отличающемуся тем, что он является штаммом, выбираемым из одного из штаммов, депонированных в Национальной коллекции культур микроорганизмов (CNCM) 10 июля 2002 г. под регистрационным номером I-2909, I-2911, I-2912, I-2913, I-2914, I-2915, I-2916 или I-2917.
35) Следующий аспект изобретения относится к способу получения медиатора биосинтеза макролида, отличающемуся тем, что он включает следующие стадии:
а) культивирование, на соответствующей культуральной среде, микроорганизма по любому из вышеприведенных п.п.23), 24), 25), 26), 27), 28), 29), 30), 31), 32), 33) или 34);
b) рекуперация кондиционированной культуральной среды или клеточного экстракта;
с) выделение и очистка из вышеуказанной культуральной среды или еще из клеточного экстракта, полученной(ного) на стадии b), вышеуказанного медиатора биосинтеза.
36) Другой аспект изобретения относится к способу получения молекулы, происходящей от макролида, отличающемуся тем, что получают медиатор биосинтеза согласно способу по вышеприведенному п.35) и модифицируют таким образом продуцированный медиатор.
37) Следующий аспект изобретения относится к способу получения по вышеприведенному п.36), отличающемуся тем, что вышеуказанный медиатор модифицируют химическим, биохимическим, ферментативным и/или микробиологическим способом.
38) Другой аспект изобретения относится к способу получения по вышеприведенному п.36) или 37), отличающемуся тем, что в вышеуказанный микроорганизм вводят один или несколько генов, кодирующих протеины, способные модифицировать медиатор, служащий для них в качестве субстрата.
39) Следующий аспект изобретения относится к способу получения по вышеприведенному п.36), 37) или 38), отличающемуся тем, что макролидом является спирамицин.
40) Другой аспект изобретения относится к способу получения по вышеприведенному п.36), 37), 38 или 39), отличающемуся тем, что используемым микроорганизмом является штамм S. ambofaciences.
41) Следующий аспект изобретения относится к микроорганизму, продуцирующему спирамицин I, но не продуцирующему спиромицины II и III.
42) Другой аспект изобретения относится к микроорганизму по вышеприведенному п.41), отличающемуся тем, что он включает совокупность генов, необходимых в биосинтезе спирамицина I, однако, ген, включающий последовательность SEQ ID № 13 или один из ее вариантов или одну из последовательностей, происходящих от них в соответствии с вырожденностью генетического кода, и кодирующий полипептид, соответствующий последовательности SEQ ID № 14 или одному из ее вариантов, не экспрессирован или инактивирован.
43) Следующий аспект изобретения относится к микроорганизму по вышеприведенному п.42), отличающемуся тем, что вышеуказанную инактивацию осуществляют путем мутагенеза в гене, кодирующем вышеуказанный протеин, или путем экспрессии антисмысловой РНК, комплементарной матричной РНК, кодирующей вышеуказанный протеин.
44) Другой аспект изобретения относится к микроорганизму по вышеприведенному п.42), отличающемуся тем, что вышеуказанный мутагенез осуществляют в промоторе этого гена, в кодирующей последовательности или в некодирующей последовательности с целью инактивации кодируемого протеина или предотвращения его экспрессии или его трансляции.
45) Следующий аспект изобретения относится к микроорганизму по вышеприведенному п.43) или 44), отличающемуся тем, что мутагенез осуществляют путем облучения, путем воздействия мутагенного химического агента, путем направленного мутагенеза или путем замены гена.
46) Другой аспект изобретения относится к микроорганизму по вышеприведенному п.43), 44) или 45), отличающемуся тем, что мутагенез осуществляют in vitro или in situ путем супрессии, замены, делеции и/или инсерции одного или нескольких оснований в случае рассматриваемого гена или путем генной инактивации.
47) Следующий аспект изобретения относится к микроорганизму по вышеприведенному п.41) или 42), отличающемуся тем, что вышеуказанный микроорганизм получают за счет экспрессии генов пути биосинтеза спирамицина, причем они не включают ген, содержащий последовательность, соответствующую SEQ ID № 13, или один из ее вариантов или одну из последовательностей, происходящих от них в соответствии с вырожденностью генетического кода, и кодирующий полипептид, соответствующий последовательности SEQ ID № 14 или одному из ее вариантов.
48) Другой аспект изобретения относится к микроорганизму по вышеприведенному п.41), 42), 43), 44), 45), 46) или 47), отличающемуся тем, что вышеуказанным микроорганизмом является бактерия рода Streptomyces.
49) Следующий аспект изобретения относится к микроорганизму по вышеприведенному п.41), 42), 43), 44), 45) 46), 47) и 48), отличающемуся тем, что вышеуказанный микроорганизм получают из исходного штамма, продуцирующего спирамицины I, II и III.
50) Другой аспект изобретения относится к микроорганизму по вышеприведенному п.41), 42), 43), 44), 45), 46), 47), 48) или 49), отличающемуся тем, что его получают путем мутагенеза в гене, включающем последовательность, соответствующую SEQ ID № 13, или один из ее вариантов или одну из последовательностей, происходящих от них в соответствии с вырожденностью генетического кода, и кодирующем полипептид, соответствующий последовательности SEQ ID № 14 или одному из ее вариантов, обладающему такой же функцией.
51) Следующий аспект изобретения относится к микроорганизму по вышеприведенному п.41), 42), 43), 44), 45), 46), 47), 48), 49) или 50), отличающемуся тем, что вышеуказанный микроорганизм получают из штамма S. ambofaciens, продуцирующего спирамицины I, II и III, в котором осуществляют генную инактивацию гена, включающего последовательность, соответствующую последовательности SEQ ID № 13, или одну из последовательностей, происходящих от нее в соответствии с вырожденностью генетического кода.
52) Другой аспект изобретения относится к штамму S. ambofaciens, отличающемуся тем, что речь идет о штамме, депонированном в Национальной коллекции культур микроорганизмов (CNCM) 10 июля 2002 г. под регистрационным номером I-2910.
53) Следующий аспект изобретения относится к способу продуцирования спирамицина I, отличающемуся тем, что он включает следующие стадии:
а) культивирование, на соответствующей культуральной среде, микроорганизма по любому из вышеприведенных п.п.41), 42), 43), 44), 45), 46), 47), 48), 49), 50), 51) или 52);
b) рекуперация кондиционированной культуральной среды или клеточного экстракта;
с) выделение и очистка из вышеуказанной культуральной среды или еще из клеточного экстракта, полученной(ного) на стадии b), спирамицина I.
54) Другой аспект изобретения относится к применению полинуклеотида по любому из вышеприведенных п.п.1), 2), 3), 4), 5) или 6) для повышения продуцирования макролидов микроорганизмом.
55) Следующиий аспект изобретения относится к мутантному микроорганизму, являющемуся продуцентом макролида, отличающемуся тем, что он обладает генетической модификацией по меньшей мере в одном гене, включающем последовательность по любому из вышеприведенных п.п.1), 2), 3), 4), 5) или 6), и/или что он сверхпродуцирует по меньшей мере один ген, включающий последовательность по любому из вышеприведенных п.п.1), 2), 3), 4), 5) или 6).
56) Другой аспект изобретения относится к мутантному микроорганизму по вышеприведенному п.55), отличающемуся тем, что генетическая модификация состоит в супрессии, замене, делеции и/или инсерции одного или нескольких оснований в случае рассматриваемого гена или рассматриваемых генов с целью экспрессирования одного или нескольких протеинов, обладающих высшей активностью, или экспрессирования на более высоком уровне этого или этих протеинов.
57) Следующий аспект изобретения относится к мутантному микроорганизму по вышеприведенному п.55), отличающемуся тем, что сверхпродуцирования рассматриваемого гена достигают за счет увеличения числа копий этого гена и/или за счет введения более активного промотора, чем исходный промотор.
58) Другой аспект изобретения относится к мутантному микроорганизму по вышеприведенному п.55) или 57), отличающемуся тем, что сверхпродуцирования рассматриваемого гена достигают за счет трансформации микроорганизма, являющегося продуцентом макролида, с помощью конструкции рекомбинантной ДНК по вышеприведенному п.13, 14 или 17, позволяющей осуществлять сверхпродуцирование этого гена.
59) Следующий аспект изобретения относится к мутантному микроорганизму по вышеприведенному п.55), 56), 57) или 58), отличающемуся тем, что генетическую модификацию осуществляют в одном или нескольких генах, включающих одну из последовательностей, соответствующих одной или нескольким последовательностям SEQ ID № 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 28, 30, 34, 36, 40, 43, 45, 47, 49, 53, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 107, 109, 111, 113, 115, 118, 120, 141, 143, 145, 147 и 149, или один из ее вариантов, или одну из последовательностей, происходящих от них в соответствии с вырожденностью генетического кода.
60) Другой аспект изобретения относится к мутантному микроорганизму по вышеприведенному п.55), 56), 57), 58) или 59), отличающемуся тем, что микроорганизм сверхпродуцирует один или несколько генов, включающих одну из последовательностей, соответствующих одной или нескольким последовательностям SEQ ID № 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 28, 30, 34, 36, 40, 43, 45, 47, 49, 53, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 107, 109, 111, 113, 115, 118, 120, 141, 143, 145, 147 и 149, или один из ее вариантов, или одну из последовательностей, происходящих от них в соответствии с вырожденностью генетического кода.
61) Другой аспект изобретения относится к мутантному микроорганизму по вышеприведенному п.55), 56), 57), 58), 59) или 60), отличающемуся тем, что вышеуказанным микроорганизмом является одна из бактерий рода Streptomyces.
62) Следующий аспект изобретения относится к мутантному микроорганизму по вышеприведенному п.55), 56), 57), 58), 59), 60) или 61), отличающемуся тем, что макролидом является спирамицин.
63) Другой аспект изобретения относится к мутантному микроорганизму по вышеприведенному п.55), 56), 57), 58), 59), 60), 61) или 62), отличающемуся тем, что вышеуказанным микроорганизмом является один из штаммов S. ambofaciens.
64) Следующий аспект изобретения относится к способу продуцирования макролидов, отличающемуся тем, что он включает следующие стадии:
а) культивирование, на соответствующей культуральной среде, микроорганизма по любому из вышеприведенных п.п.55), 56), 57), 58), 59), 60), 61), 62), 63) или 64);
b) рекуперация кондиционированной культуральной среды или клеточного экстракта;
с) выделение и очистка из вышеуказанной культуральной среды или еще из клеточного экстракта, полученной(ного) на стадии b), вышеуказанного продуцированного макролида или вышеуказанных продуцированных макролидов.
65) Другой аспект изобретения относится к применению последовательности и/или рекомбинантной ДНК и/или вектора по любому из вышеприведенных п.п.1), 2), 3), 4), 5), 6), 7), 8), 9), 10), 11), 12), 13), 14), 15), 16) или 17) для получения гибридных антибиотиков.
66) Следующий аспект изобретения относится к применению по меньшей мере одного полинуклеотида и/или по меньшей мере одной рекомбинантной ДНК и/или по меньшей мере одного экспрессирующего вектора и/или по меньшей мере одного полипептида и/или по меньшей мере одной клетки-хозяина по одному из вышеприведенных п.п.1), 2), 3), 4), 5), 6), 7), 8), 9), 10), 11), 12), 13), 14), 15), 16), 17) или 21) для осуществления одной или нескольких биоконверсий.
67) Другой аспект изобретения относится к полинуклеотиду, отличающемуся тем, что речь идет о полинуклеотиде, комплементарном одному из полинуклеотидов по вышеприведенному п.1), 2), 3), 4), 5) или 6).
68) Следующий аспект изобретения относится к микроорганизму, являющемуся продуцентом по меньшей мере одного спирамицина, отличающемуся тем, что он сверхпродуцирует:
- ген, который может быть получен за счет амплификации путем полимеразной цепной реакции (PCR) при использовании пары праймеров, имеющих следующие последовательности: 5' AAGCTTGTGTGCCCGGTGTACCTGGGGAGC 3' (SEQ ID № 138) и 5' GGATCCCGCGACGGACACGACCGCCGCGCA 3' (SEQ ID № 139) и в качестве матрицы космиды pSPM36 или полной ДНК Streptomyces ambofaciens;
- или ген, происходящий от него в соответствии с вырожденностью генетического кода.
69) Другой аспект изобретения относится к микроорганизму по п.68 или 90, отличающемуся тем, что речь идет о бактерии рода Streptomyces.
70) Следующий аспект изобретения относится к микроорганизму по п.68, 69 или 90, отличающемуся тем, что речь идет о бактерии вида Streptomyces ambofaciens.
71) Другой аспект изобретения относится к микроорганизму по п.68, 69, 70 или 90, отличающемуся тем, что сверхпродуцирования вышеуказанного гена достигают путем трансформации вышеуказанного микроорганизма экспрессирующим вектором.
72) Следующий аспект изобретения относится к штамму Streptomyces ambofaciens, отличающемуся тем, что речь идет о штамме OSC2/pSPM75(1) или штамме OSC2/pSPM75(2), депонированном в Национальной коллекции культур микроорганизмов (CNCM), Институт Пастера, 25, rue du Docteur Roux, 75724 Париж, Cedex 15, Франция, 6 октября 2003 г. под регистрационным номером I-3101.
73) Другой аспект изобретения относится к рекомбинантной ДНК, отличающейся тем, что она включает:
- полинуклеотид, который может быть получен за счет амплификации путем полимеразной цепной реакции при использовании пары праймеров, имеющих следующие последовательности: 5' AAGCTTGTGTGCCCGGTGTACCTGGGGAGC 3' (SEQ ID № 138) и 5' GGATCCCGCGACGGACACGACCGCCGCGCA 3' (SEQ ID № 139) и в качестве матрицы космиды pSPM36 или полной ДНК Streptomyces ambofaciens;
- или фрагмент, включающий по меньшей мере 10, 12, 15, 18, 20-25, 30, 40, 50, 60, 70, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1050, 1100, 1150, 1200, 1250, 1300, 1350, 1400, 1450, 1460, 1470, 1480, 1490 или 1500 последовательных нуклеотидов этого полинуклеотида.
74) Следующий аспект изобретения относится к рекомбинантной ДНК по п.73 или 91, отличающейся тем, что речь идет о векторе.
75) Другой аспект изобретения относится к рекомбинантной ДНК по п.73, 74 или 91, отличающейся тем, что речь идет о экспрессирующем векторе.
76) Следующий аспект изобретения относится к клетке-хозяину, в которую введена по меньшей мере одна рекомбинантная ДНК по любому из п.п.73, 74, 75 или 91.
77) Другой аспект изобретения относится к способу продуцирования полипептида, отличающемуся тем, что вышеуказанный способ включает следующие стадии:
а) трансформация клетки-хозяина с помощью по меньшей мере одного экспрессирующего вектора по п.75;
b) культивирование, на соответствующей культуральной среде, вышеуказанной клетки-хозяина;
с) рекуперация кондиционированной культуральной среды или клеточного экстракта;
d) выделение и очистка из вышеуказанной культуральной среды или еще из клеточного экстракта, полученной(ного) на стадии с), вышеуказанного полипептида;
е) в желательном случае, охарактеризовывание продуцированного рекомбинантного полипептида.
78) Следующий аспект изобретения относится к микроорганизму по п.51, отличающемуся тем, что генную инактивацию осуществляют путем делеции полноразмерного гена или части гена, включающего последовательность, соответствующую SEQ ID № 13, или одну из последовательностей, происходящих от нее в соответствии с вырожденностью генетического кода.
79) Другой аспект изобретения относится к микроорганизму по любому из п.п.41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51 или 78, отличающемуся тем, что он, кроме того, сверхпродуцирует:
- ген, который может быть получен за счет амплификации путем полимеразной цепной реакции при использовании пары праймеров, имеющих следующие последовательности: 5' AAGCTTGTGTGCCCGGTGTACCTGGGGAGC 3' (SEQ ID № 138) и 5' GGATCCCGCGACGGACACGACCGCCGCGCA 3' (SEQ ID № 139) и в качестве матрицы космиды pSPM36 или полной ДНК Streptomyces ambofsciens;
- или ген, происходящий от него в соответствии с вырожденностью генетического кода.
80) Следующий аспект изобретения относится к экспрессирующему вектору, отличающемуся тем, что полинуклеотид, соответствующий последовательности SEQ ID № 47, или полинуклеотид, происходящий от него в соответствии с вырожденностью генетического кода, находится под контролем промотора, позволяющего осуществлять экспрессию протеина, кодируемого указанным полинуклеотидом, в Streptomyces ambofaciens.
81) Другой аспект изобретения относится к экспрессирующему вектору по п.80, отличающемуся тем, что он является плазмидой pSPM524 или pSPM525.
82) Следующий аспект изобретения относится к штамму Streptomyces ambofaciens, трансформированному вектором по п.80 или 81.
83. Другой аспект изобретения относится к микроорганизму по любому из п.п.41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 78, 79 или 92, отличающемуся тем, что он, кроме того, сверхпродуцирует ген, соответствующий кодирующей последовательности SEQ ID 47 или кодирующей последовательности, происходящей от нее в соответствии с вырожденностью генетического кода.
84. Следующий аспект изобретения относится к микроорганизму по п.83, отличающемуся тем, что речь идет о штамме SPM502pSPM525, депонированном в Национальной коллекции культур микроорганизмов (CNCM), Институт Пастера, 25, rue du Docteur Roux, 75724 Париж, Cedex 15, Франция, 26 февраля 2003 г. под регистрационным номером I-2977.
85) Другой аспект изобретения относится к способу продуцирования спирамицина (спирамицинов), отличающемуся тем, что он включает следующие стадии:
а) культивирование, на соответствующей культуральной среде, микроорганизма по любому из п.п.68, 69, 70, 71, 72, 78, 79, 82, 83, 84, 90 или 92;
b) рекуперация кондиционированной культуральной среды или клеточного экстракта;
с) выделение и очистка из вышеуказанной культуральной среды или еще из клеточного экстракта, полученной(ного) на стадии b), спирамицинов.
86) Следующий аспект изобретения относится к полипептиду, отличающемуся тем, что его последовательность включает последовательность SEQ ID № 112 или последовательность SEQ ID № 142.
87) Другой аспект изобретения относится к полипептиду, отличающемуся тем, что его последовательность соответствует последовательности, выражаемой кодирующей последовательностью:
- гена, который может быть получен за счет амплификации путем полимеразной цепной реакции (РСR) при использовании пары праймеров, имеющих следующие последовательности: 5' AAGCTTGTGTGCCCGGTGTACCTGGGGAGC 3' (SEQ ID № 138) и 5' GGATCCCGCGACGGACACGACCGCCGCGCA 3' (SEQ ID № 139) и в качестве матрицы космиды pSPM36 или полной ДНК Streptomyces ambofaciens,
- или гена, происходящего от него в соответствии с вырожденностью генетического кода.
88) Следующий аспект изобретения относится к экспрессирующему вектору, позволяющему осуществлять экспрессию полипептида по п.86, 87 или 93 в Streptomyces ambofaciens.
89) Другой аспект изобретения относится к экспрессирующему вектору по п.88, отличающемуся тем, что речь идет о плазмиде pSPM75.
90) Следующий аспект изобретения относится к микроорганизму по п.68, отличающемуся тем, что геном, который может быть получен за счет амплификации путем полимеразной цепной реакции, является ген, соответствующий кодирующей последовательности SEQ ID № 141, или ген, происходящий от него в соответствии с вырожденностью генетического кода.
91) Другой аспект изобретения относится к рекомбинантной ДНК по п.73, отличающейся тем, что полинуклеотидом, который может быть получен за счет амплификации путем полимеразной цепной реакции, является полинуклеотид, соответствующий последовательности SEQ ID № 141.
92) Следующий аспект изобретения относится к микроорганизму по п.79, отличающемуся тем, что геном, который может быть получен за счет амплификации путем полимеразной цепной реакции, является ген, соответствующий кодирующей последовательности SEQ ID № 141, или ген, происходящий от него в соответствии с вырожденностью генетического кода.
93) Другой аспект изобретения относится к полипептиду, отличающемуся тем, что его последовательностью является SEQ ID № 142.
Общие определения