Стереоселективный синтез аналогов витамина д
Иллюстрации
Показать всеНастоящее изобретение относится к промежуточным соединениям, используемым в синтезе кальципотриола или моногидрата кальципотриола, к способам получения упомянутых промежуточных соединений и к способам стереоселективного восстановления упомянутых промежуточных соединений. Способ позволяет повысить выход С-24 гидроксилэпимеров производных кальципотриола. 11 н. и 16 з.п. ф-лы, 1 табл.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
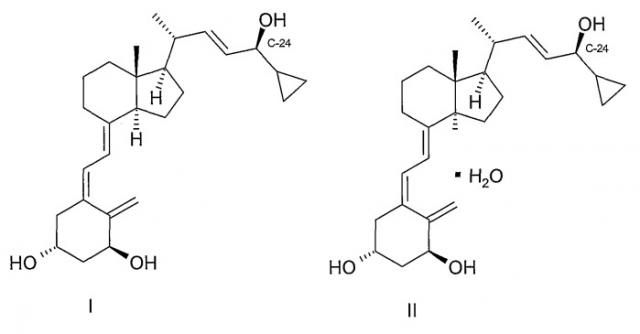
Настоящее изобретение относится к способам получения кальципотриола {(5Z, 7E, 22E, 24S)-24-циклопропил-9,10-секохола-5,7,10(19),22-тетраен-1α-3β-24-триол} или моногидрата кальципотриола стереоселективным восстановлением. Настоящее изобретение дополнительно предлагает новые промежуточные соединения и способы синтеза промежуточных соединений, пригодных для получения кальципотриола или моногидрата кальципотриола.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Кальципотриол или кальципотриен (структура 1) [CAS 112965-21-6] показывает высокую активность в ингибировании нежелательного разрастания эпидермальных кератиноцитов [F.A.C.M. Castelijins, M.J. Gerritsen, I.M. J.J. van Erp, van de Kerkhof; Acta Derm. Venereol. 79, 11,1999]. Эффективность кальципотриола или моногидрата кальципотриола (II) при лечении псориаза была показана в ряде клинических испытаний [D.M.Ashcroft et al.; Brit. Med. J. 320, 963-7, 2000] и кальципотриол используют в нескольких коммерческих лекарственных рецептурах.
В получении кальципотриола необходима специфическая стереохимия гидроксильной группы при С-24 для полного проявления биологической активности. При действующей методологии требуемую стереохимию достигают одним из следующих способов:
(i) недиастереоселективным восстановлением С-24 кетотриенов с последующим разделением диастереомерных смесей С-24 гидроксилэпимеров с помощью хроматографии (WO 87/00834 & M.J. Calverley; Tetrahedron 43 (20), 4609-19, 1987);
(ii) присоединением энантиомерно-чистой С-24-гидроксилсодержащей боковой цепи к скелету витамина Д (M.J. Calverley, Synlett, 157-59, 1990);
(iii) селективной ферментативной этерификацией одного из С-24 гидроксилэпимеров с последующим хроматографическим разделением (WO 03/060094).
Недиастереоселективное восстановление С-24 кетотриенов с последующим разделением эпимерной смеси (i) представляет собой наиболее широко распространенную методику получения желаемого эпимера. Данный процесс восстановления дает, главным образом, нежелательный С-24 эпимерный спирт (обычно примерно 60% нежелательного 24-R эпимера) и в производственном масштабе трудно выделить желаемый S-эпимер из такой смеси с помощью хроматографии.
Стереоселективный синтез (ii) представляет собой неудобный способ для масштабного производства вследствие своей многостадийной природы и стоимости и вследствие факта использования токсичных промежуточных соединений. Способ ферментативной этерификации (iii) имеет неудобство, помимо высокой стоимости применяемых ферментов, способ включает, в зависимости от селективности применяемых ферментов, 1-2 дополнительных реакционных стадий, которые дополнительно увеличивают стоимость процесса.
Стереоселективное восстановление С-24 кетонов непосредственно до желательных С-24 гидроксилэпимеров было, например, описано для производных холестерина в WO 98/24800 и M. Ishiguro et al., J.C.S. Chem. Comm., 115-117,1981. Стереоселективное восстановление тройной связи в боковой цепи аналога кальципотриола c незащищенной триеновой системой, используя S-Alpine Borane, было описано M.J. Calvery et al. в Bioorg. Med. Chem. Lett., 1841-1844 3(9), 1993.
Главная техническая проблема использования способов стереоселективного восстановления для синтеза кальципотриола обусловлен тем, что ненасыщенная триеновая система известных до настоящего времени промежуточных соединений для синтеза кальципотриола химически лабильна в присутствии кислоты Льюиса, промежуточные соединения легко окисляются, и что они не совместимы с применением типичных условий реакции восстановления. Это приводит к уменьшению выхода, загрязнению продуктов и трудозатратным вспомогательным операциям, особенно в крупномасштабном производстве.
Целью данного изобретения является создание альтернативного способа синтеза кальципотриола, который может преодолеть одну или более различных проблем и неудобств, описанных выше.
Настоящее изобретение предлагает новый способ получения диастереомерно обогащенных С-24 гидроксилэпимеров производных кальципотриола с использованием нового пути синтеза, содержащего стадию стереоселективного восстановления. Настоящее изобретение дополнительно предлагает новые химически более устойчивые промежуточные соединения, в которых лабильная триеновая система защищена в виде аддукта с диоксидом серы. При получении диастереомерно обогащенных С-24 гидроксилэпимеров производных кальципотриола выход и эффективность последующего отделения желательного С-24 S-гидроксилэпимера могут быть значительно улучшены.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
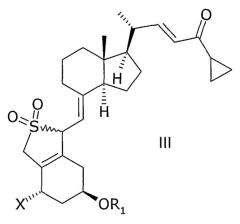
Неожиданно было найдено, что соединение общей структуры III,
в которой Х представляет собой водород или ОR2,
и в которой R1 и R2 могут быть одинаковыми или различными и представляют собой водород или гидроксизащитную группу,
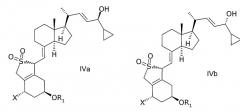
в инертном растворителе с восстановительным агентом или с восстановительным агентом в присутствии хирального вспомогательного вещества образует смесь соединений общей структуры IVa или IVb,
которая обогащена IVa, причем Х, R1 и R2 как определены выше.
В первом аспекте данное соединение относится к способу получения кальципотриола {(5Z, 7E, 22E, 24S)-24-циклопропил-9,10-секохола-5,7,10(19),22-тетраен-1α-3β-24-триол} или моногидрата кальципотриола, содержащему следующие стадии:
(а) восстановление соединения общей структуры III,
в которой Х представляет собой ОR2,
и в которой R1 и R2 могут быть одинаковыми или различными и представляют собой водород или гидроксизащитную группу,
в инертном растворителе с восстановительным агентом или с восстановительным агентом в присутствии хирального вспомогательного вещества для образования смеси соединений общей структуры IVa или IVb, которая обогащена IVa, причем Х, R1 и R2 определены выше;
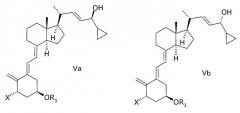
(b) взаимодействие смеси соединений общей структуры IVa или IVb, которая обогащена IVa, в присутствии основания с получением смеси соединений общей структуры Va и Vb, которая обогащена Va,
причем Х, R1 и R2 как определены выше;
(с) выделение соединения общей структуры Va из смеси соединений общей структуры Va и Vb, которая обогащена Va, причем Х, R1 и R2 определены выше;
(d) изомеризация соединения общей структуры Va в соединение общей структуры VIa,
в которой Х, R1 и R2 определены выше; и
(е) когда R1 и/или R2 не является водородом, удаление гидроксизащитной группы R1 и/или R2 соединения общей структуры Va для получения кальципотриола или моногидрата кальципотриола.
В дополнительном аспекте данное изобретение относится к способу получения кальципотриола или моногидрата кальципотриола, содержащему стадии (а)-(b), упомянутые выше, и дополнительно содержащему следующие стадии:
(f) изомеризации смеси соединений общей структуры Va и Vb, причем Х, R1 и R2 как определены в пункте 2, которая обогащена Va до смеси соединений общей структуры VIa и VIb, которая обогащена VIa,
причем Х, R1 и R2 определены выше;
(g) выделение соединения общей структуры VIa из смеси соединений общей структуры VIa и VIb, которая обогащена VIa, причем Х, R1 и R2 определены выше;
(h) когда R1 и/или R2 не является водородом, удаление гидроксизащитной группы R1 и/или R2 соединения общей структуры VIa для получения кальципотриола или моногидрата кальципотриола.
В еще одном дополнительном аспекте данное изобретение относится к способу получения кальципотриола {(5Z, 7E, 22E, 24S)-24-циклопропил-9,10-секохола-5,7,10(19),22-тетраен-1α-3β-24-триол} или моногидрата кальципотриола, содержащему следующие стадии:
(j) восстановление соединения общей структуры III,
в котором Х представляет собой водород,
и в котором R1 представляет собой водород или гидроксизащитную группу, в инертном растворителе с восстановительным агентом или с восстановительным агентом в присутствии хирального вспомогательного вещества для образования смеси соединений общей структуры IVa или IVb,
которая обогащена IVa, причем Х, R1 и R2 определены выше;
(k) взаимодействие смеси соединений общей структуры IVa или IVb, которая обогащена IVa, в присутствии основания с получением смеси соединений общей структуры Va и Vb, которая обогащена Va, причем Х, R1 и R2 определены выше;
(l) выделение соединения общей структуры Va из смеси соединений общей структуры Va и Vb, которая обогащена Va, причем Х, R1 и R2 определены выше;
(m) гидроксилирование соединения общей структуры Va подходящим гидроксилирующим агентом, причем Х и R1 определены выше, с образованием соединения общей структуры Va, причем Х представляет собой ОR2 и R2 представляет собой водород, и при этом R1 определено выше;
(о) изомеризация соединения общей структуры Va в соединение общей структуры VIa,
причем Х, R1 и R2 определены выше; и
(p) когда R1 не является водородом, удаление гидроксизащитной группы R1 соединения общей структуры VIa для получения кальципотриола или моногидрата кальципотриола.
В еще одном дополнительном аспекте данное изобретение относится к способу получения кальципотриола или моногидрата кальципотриола, содержащему стадии (j)-(l) пункта 4 и дополнительно содержащему следующие стадии:
(q) защита С-24 гидроксигруппы соединения общей структуры Va, в которой Х представляет собой водород и в которой R1 представляет собой водород или гидроксизащитную группу, с гидроксизащитной группой;
(r) гидроксилирование С-24 гидроксизащищенного соединения общей структуры Va подходящим гидроксилирующим агентом, причем Х и R1 определены выше, для получения С-24 гидроксизащищенного соединения общей структуры Va, причем Х представляет собой ОR2 и R2 представляет собой водород, и при этом R1 определено выше;
(s) удаление С-24 гидроксизащитной группы соединения общей структуры Va;
(t) изомеризация соединения общей структуры Va в соединение общей структуры VIa,
причем Х, R1 и R2 определены выше; и
(u) когда R1 не является водородом, удаление гидроксизащитной группы R1 соединения общей структуры VIa для получения кальципотриола или моногидрата кальципотриола.
В еще одном дополнительном аспекте данное соединение относится к способу получения соединения общей структуры III,
в которой Х представляет собой или водород, или ОR2, и причем R1 и R2 могут быть одинаковыми или различными и представляют собой водород или гидроксизащитную группу, взаимодействием соединения общей структуры VII или VIII,
причем R1 и R2 как определены выше, с диоксидом серы.
В еще одном дополнительном аспекте данное изобретение относится к способу взаимодействия смеси соединений общей структуры IVa и IVb,
в которой Х представляет собой или водород, или ОR2,
и причем R1 и R2 могут быть одинаковыми или различными и представляют собой водород или гидроксизащитную группу, которая обогащена IVa, в присутствии основания с получением смеси соединений общей структуры Va и Vb, которая обогащена Va, при этом Х, R1 и R2 определены выше.
В еще одном дополнительном аспекте данное изобретение относится к способу получения кальципотриола {(5Z, 7E, 22E, 24S)-24-циклопропил-9,10-секохола-5,7,10(19),22-тетраен-1α-3β-24-триол} или моногидрата кальципотриола, содержащему любой из способов, описанных выше.
В еще одном дополнительном аспекте, данное изобретение относится к соединениям общей структуры IIIa или IIIb, или их смесям,
в которой Х представляет собой или водород, или ОR2,
и причем R1 и R2 могут быть одинаковыми или различными и представляют собой водород или гидроксизащитную группу.
В еще одном дополнительном аспекте данное изобретение относится к соединениям общей структуры IVaa, IVab, IVba, IVbb, IVb или их смесям,
в которой Х представляет собой или водород или ОR2,
и причем R1 и R2 могут быть одинаковыми или различными и представляют собой водород или гидроксизащитную группу.
В еще одном дополнительном аспекте, данное изобретение относится к применению соединений общей структуры IIIa, IIIb, IVaa, IVab, IVba, IVbb в качестве промежуточных соединений в производстве кальципотриола или моногидрата кальципотриола.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
Используемый здесь термин «гидроксизащитная группа» означает любую группу, которая образует производное, которое устойчиво к намеченной реакции, в которой упомянутая гидроксизащитная группа может быть селективно удалена реагентами, которые не атакуют регенерируемую гидроксигруппу. Упомянутое производное может быть получено селективной реакцией гидрокизащитного агента с гидроксигруппой. Силильные производные, такие как силильные эфиры, образующие трет.-бутилдиметилсилил, представляют собой примеры гидроксизащитных групп. Силилхлориды, такие как трет.-бутилдиметилсилилхлорид (ТБСХ), триметилсилилхлорид, триэтилсилилхлорид, дифенилметилсилилхлорид, триизопропилсилилхлорид, и трет.-бутилдифенилсилилхлорид представляют собой примеры гидроксизащитных агентов. Фтористый водород, такой как водный HF в ацетонитриле, или тетра-н-бутиламмонийфторид представляют собой примеры реагентов, которые могут удалять силильные группы. Другие гидроксизащитные группы включают в себя эфиры, такие как тетрагидропираниловый (ТГП) эфир, включая в себя алкоксиалкиловые эфиры (ацетали), такие как метоксиметиловый (МОМ) эфир, или сложные эфиры, такие как хлоруксусный эфир, триметилацетат, ацетат или бензоат. Примеры гидроксизащитных групп и способов защиты и удаления, включенные в рамки данной заявки (но не ограниченные ими) могут, например, быть найдены в “Protective Groups in Organic Synthesis” 3rd ed., T.W. Greene & P.G.M. Wuts eds., John Wiley 1999 и в “ Protecting Groups”, 1st ed., P.J. Kocienski, G. Thieme 2000.
Используемый здесь термин «алкил» означает линейную или разветвленную алкильную группу, которая может быть циклической или ациклической, имеющую от одного до двадцати атомов углерода, предпочтительно от одного до семи атомов углерода. Метильная группа, этильная группа, н-пропильная группа, изопропильная группа, пентильная группа, гексильная группа и трет.-бутилдиметильная группа представляют собой, не ограничиваясь ими, примеры алкильных групп.
Используемый здесь термин «восстановительный агент» означает любой агент, способный к восстановлению, включая в себя энантиоселектиное или диастереоселективное восстановление С-24 кетогруппы соединения общей структуры III, с получением соединения общей структуры IV. В одном варианте осуществления восстановительный агент может восстанавливать С-24 кетогруппу соединения общей структуры III без хирального вспомогательного соединения с образованием смеси соединений общей структуры IV, при этом упомянутая смесь обогащена желательным эпимером IVa (предпочтительно образующим 24-S изомер). В другом варианте осуществления восстановительный агент может восстанавливать С-24 кетогруппу соединения общей структуры III в присутствии хирального вспомогательного соединения с образованием смеси соединений общей структуры IV, при этом упомянутая смесь обогащена желательным эпимером IVa (предпочтительно образующим 24-S изомер). Восстановительный агент может быть хиральным или ахиральным. Примеры восстановительных агентов включают в себя (но не ограничиваются) борановые восстановительные агенты, гидриды металлов, такие как гидрид лития, гидрид алюминия, борогидрид натрия или AlH3, возможно в присутствии солей лантанидов (например, LaCl3, CeBr3, CeCl3) или NaBH3(OAc), Zn(BH4)2 и Et3SiH. Другие восстановительные агенты включают в себя (но не ограничиваются) водород в присутствии катализатора, такого как платина или рутений, натрий в этаноле, изопропиловый спирт и изопропоксид алюминия, и порошок цинка в воде или в спирте.
Используемый здесь термин «борановый восстановительный агент» включает в себя боран или любое производное борана, такое как борановые комплексы с аминами или эфирами. Не ограничивающие примеры борановых восстановительных агентов, например включают в себя N,N-диэтиланилинборан, боран-тетрагидрофуран, 9-боранбициклононан (9-ББН) или борандиметилсульфид.
Используемый здесь термин «хиральное вспомогательное соединение» означает хиральное соединение или оптически активный катализатор, например соединение, содержащее асимметрически замещенный атом углерода или вспомогательные хиральные соединения, или смеси хиральных соединений и/или оптически активных катализаторов, которые будут улучшать выход соединения общей структуры IVa по отношению к его эпимерам (увеличение молярного соотношения IVa:IVb) при восстановлении соединения общей формулы III с упомянутым восстановительным агентом. Упомянутые хиральные вспомогательные соединения могут, таким образом, быть любыми соединениями, которые способны увеличивать стереоселективность в реакции восстановления соединения общей структуры III по сравнению с выходом или стереоселективностью для IVa без присутствия или включения хирального вспомогательного соединения. Неограничивающие примеры хиральных вспомогательных соединений включают в себя хиральные 1,2-аминоспирты, такие как хиральные цис-1-амино-2-инданолпроизводные, такие как (1S,2R)-(-)-цис-1-амино-2-инданол или цис-1-амино-1,2,3,4-тетрагидронафталин-2-ол, такие как (1S,2R)-цис-1-амино-1,2,3,4-тетрагидронафталин-2-ол. Другие примеры представляют собой бинафтилпроизводные, такие как (R)-2,2'-бис(дифенилфосфино)-1,1'-бинафтилрутений ацетат 2,2'-дигидрокси-1,1'-бинафтилпроизводные. Дополнительные примеры включают в себя, но не ограничиваются, (R)-(+)-α,α-дифенил-2-пирролидинметанол,(R)-(+)-2-амино-4-метил-1,1-дифенил-1-пентанол,(R)-(-)-2-амино-3-метил-1,1-дифенил-1-бутанол, (R)-(+)-2-амино-1,1,3-трифенил-1-пропанол и (1S,2R)-(-)-2-амино-1,2-дифенилэтанол.
Используемый здесь термин «инертный растворитель» означает любой органический растворитель, совместимый с упомянутым восстановительным агентом в применяемых условиях реакции, или смеси таких растворителей. Выбор такого растворителя будет зависеть от специфики используемого восстановительного агента. Неограничивающие примеры инертных растворителей включают в себя углеводороды, такие как толуол, и эфиры, такие как трет.-бутилметиловый эфир или тетрагидрофуран.
Смесь соединений общей структуры IVa и IVb, которая обогащена IVa, означает смесь, возможно, содержащую другие соединения или растворители, с молярным соотношением (диастереомерное соотношение) IVa/IVb, равным единице (50:50) или большем, чем единица, таким образом, что смесь содержит, по меньшей мере, 50% соединения общей структуры IVa (с содержанием 50% или меньше соединения общей структуры IVb).
Смесь соединений общей структуры Va и Vb, которая обогащена Va, означает смесь, возможно, содержащую другие соединения или растворители, с молярным соотношением (диастереомерное соотношение) Va/Vb, равным единице (50:50) или большем, чем единица, таким образом, что смесь содержит, по меньшей мере, 50% соединения общей структуры Va (с содержанием 50% или меньше соединения общей структуры Vb).
Смесь соединений общей структуры VIa и VIb, которая обогащена VIa, означает смесь, возможно, содержащую другие соединения или растворители, с молярным соотношением (диастереомерное соотношение) VIa/VIb, равным единице (50:50) или большем, чем единица, таким образом, что смесь содержит, по меньшей мере, 50% соединения общей структуры VIa (с содержанием 50% или меньше соединения общей структуры VIb).
Используемый здесь термин «выделение соединения» включает в себя очистку и/или изоляцию соединения, например, по меньшей мере, 90% чистоты, такого как, по меньшей мере, 95% чистоты, такого как 97% чистоты, 98% чистоты, 99% чистоты. Термин «выделение соединения» также включает в себя значение увеличения концентрации соединения в смеси таких соединений, возможно содержащих растворители, таким образом, что смесь дополнительно обогащается желательным или предпочтительным соединением или изомером, таким как эпимер, после упомянутого выделения.
Варианты осуществления
В наиболее предпочтительном в настоящее время варианте осуществления настоящего изобретения Х представляет собой OR2.
В предпочтительном в настоящее время варианте осуществления настоящего изобретения R1 и/или R2 представляют собой алкилсилил, такой как трет.-бутилдиметилсилил, наиболее предпочтительно, когда R1 и R2 одинаковые.
В другом варианте осуществления настоящего изобретения R1 и R2 представляют собой водород.
В предпочтительном в настоящее время варианте осуществления настоящего изобретения восстановительный агент представляет собой борановый восстановительный агент, такой как N,N-диэтиланилинборан, борантетрагидрофуран, или борандиметилсульфид.
В предпочтительном в настоящее время варианте осуществления настоящего изобретения стадию восстановления проводят с хиральным восстановительным агентом или в присутствии хирального вспомогательного соединения.
В предпочтительном в настоящее время варианте осуществления настоящего изобретения хиральное вспомогательное соединение представляет собой хиральный 1,2-аминоспирт, такой как хиральное производное цис-1-амино-2-инданола, такое как (1S,2R)-(-)-цис-1-амино-2-инданол.
В предпочтительном в настоящее время варианте осуществления настоящего изобретения стадию восстановления проводят в интервале температур от 10 до 20°С, в частности 15-20°С.
В другом варианте осуществления настоящего изобретения молярное соотношение (диастереомерное соотношение IVa/IVb) смеси соединений общей структуры IVa и IVb, которая обогащена IVa, больше, чем 55:45, такое как 56:44, такое как 57:43, такое как 59:41, такое как 60:40, такое как 63:37, такое как 65:35, такое как 68:32, такое как 70:30, такое как 72:28, такое как 73:27, такое как 74:26, такое как 75:25, такое как 76:24, такое как 77:23, такое как 78:22, такое как 79:21, такое как 80:20.
В другом варианте осуществления настоящего изобретения молярное соотношение (диастереомерное соотношение Va/Vb) смеси соединений общей структуры Va и Vb, которая обогащена Va, больше, чем 55:45, такое как 56:44, такое как 57:43, такое как 59:41, такое как 60:40, такое как 63:37, такое как 65:35, такое как 68:32, такое как 70:30, такое как 72:28, такое как 73:27, такое как 74:26, такое как 75:25, такое как 76:24, такое как 77:23, такое как 78:22, такое как 79:21, такое как 80:20.
В другом варианте осуществления настоящего изобретения молярное соотношение (диастереомерное соотношение VIa/VIb) смеси соединений общей структуры VIa и VIb, которая обогащена VIa, больше, чем 55:45, такое как 56:44, такое как 57:43, такое как 59:41, такое как 60:40, такое как 63:37, такое как 65:35, такое как 68:32, такое как 70:30, такое как 72:28, такое как 73:27, такое как 74:26, такое как 75:25, такое как 76:24, такое как 77:23, такое как 78:22, такое как 79:21, такое как 80:20.
В одном варианте осуществления настоящего изобретения соединение общей структуры Va выделено, например, хроматографически из смеси соединений общей структуры Va и Vb, которая обогащена Va, при этом Х, R1 и R2 определены выше в (стадии (с)).
В другом варианте осуществления настоящего изобретения соединение общей структуры VIa выделено, например, хроматографически из смеси соединений общей структуры VIa и VIb, которая обогащена VIa, при этом Х, R1 и R2 определены выше в (стадии (g)).
Способы синтеза
Соединения общей структуры III могут, например, быть синтезированы с помощью реакции Дильса-Альдера при обработке соединения общей структуры VII или VIII диоксидом серы. Используемый диоксид серы может быть жидким, газообразным или растворенным в подходящем растворителе. Подходящие растворители для реакции Дильса-Альдера представляют собой все растворители, которые совместимы с условиями реакции, такие как алканы, такие как гексан или гептан, углеводороды, такие как ксилолы, толуол, эфиры, такие как диэтиловый эфир или метил-трет.-бутиловый эфир (МТБЭ), ацетаты, такие как этилацетат или 2-пропилацетат, галогенированные растворители, такие как дихлорметан или смесь упомянутых растворителей. В предпочтительном варианте осуществления растворитель представляет собой толуол. В другом предпочтительном варианте осуществления растворитель представляет собой смесь не смешивающегося с водой растворителя и воды, такую как толуол и вода. Реакцию также можно проводить в чистом диоксиде серы без растворителя. Подходящая температура реакции способа находится в интервале от -50°С до 60°С, таком как от -30°С до 50°С, таком как от -15°С до 40°С, таком как от -5°С до 30°С, таком как от 0°С до 35°С, таком как от 5°С до 30°С, наиболее часто таком как от 10°С до 25°С, таком как от 15°С до 20°С. В одном варианте осуществления диоксид серы используют в избытке (моль/моль), таком как 5-100 молярный избыток, таком как 7-30 молярный избыток, таком как 10-15 молярный избыток. Любой избыток непрореагировавшего диоксида серы может быть удален из реакционной смеси, например, промывкой с водным основанием, таким как водный гидроксид натрия, или отгонкой диоксида серы, возможно, вместе с растворителем, возможно, при пониженном давлении. Соединения общей структуры III обычно получают как смесь их эпимеров IIIa и IIIb.
Молярное соотношение IIIa/IIIb смеси эпимеров, полученных по реакции Дильса-Альдера будет зависеть от групп Х, R1, R2 и от используемых условий реакции. Настоящее изобретение включает в себя смеси всех возможных композиций (молярное соотношение IIIa/IIIb), таких как 1:99, таких как 2:98, таких как 3:97, таких как 4:96, таких как 5:95, таких как 10:90, таких как 85:15, таких как 80:20, таких как 75:25, таких как 30:70, таких как 35:65, таких как 40:60, таких как 45:55, таких как 50:50, таких как 55:45, таких как 60:40, таких как 65:35, таких как 70:30, таких как 75:25, таких как 80:20, таких как 85:10, таких как 90:10, таких как 95:5, таких как 96:4, таких как 97:3, таких как 98:2, таких как 99:1.
Общая формула III включает в себя смеси всех возможных композиций, как перечислено выше.
В варианте осуществления настоящего изобретения соединения IIIa и IIIb используют как смесь, как показано в общей формуле III в последующей стадии восстановления. Смесь IIIa и IIIb может, но не обязательно, быть очищена или выделена хроматографией или кристаллизацией. В другом варианте осуществления соединение IIIa используют в последующей стадии восстановления. В еще одном варианте осуществления соединение IIIb используют в последующей стадии востановления.
Соединение общей структуры VII может, например, быть синтезировано согласно способам, раскрытым, например, M.J.Calverley, Tetragedron, Vol. 43, № 20, pp.4609-4619, 1987 или в WO 87/00834 и в ссылках, цитируемых там. Например, с соединения VII, в котором Х представляет собой OR2 и как R1, так и R2 представляют собой представляют собой трет.-бутилдиметилсилил, которое описано в данных ссылках, может быть снята защита водной гидрофтористой кислотой в ацетонитриле с получением смеси соединений, в которых Х представляет собой OR2, при этом или R1, или R2 представляют собой водород, или образуют соединение, в котором Х представляет собой OR2, и R1, и R2 - оба представляют собой водород. Данная смесь соединений может, например, быть разделена или хроматографией, или кристаллизацией, как, в общем, здесь описано. При взаимодействии упомянутых соединений общей структуры VII, в которой R1 и/или R2 представляют собой водород, с подходящим защитным агентом, новые группы R1 и/или R2 могут быть введены. В зависимости от стехиометрии используемого защитного агента и условий реакции может быть получена смесь незащищенных, монозащищенных и дизащищенных соединений. Любое промежуточное соединение в смеси, в котором Х представляет собой OR2 и или R1, или R2 представляет собой водород, может быть затем хроматографически выделено и может реагировать с подходящим защитным агентом, отличным от первого используемого агента, образуя соединения общей структуры VII, в которой Х представляет собой OR2 и R1 отличен от R2.
Соединения общей структуры VII, в которой Х представляет собой водород и R1 представляет собой водород или гидроксизащитную группу, могут, например, быть получены, начиная от соединений 7а и/или 7b, описанных M.J. Calverley, Tetrahedron, Vol. 43, № 20, p. 4610, 1987, последующими аналогичными процедурами и общими синтетическими способами, вышеописанным и цитированным выше в ссылках.
Способ восстановления по настоящему изобретению может, например, быть проведен при взаимодействии прохирального кетона общей структуры III с хиральным бораном как восстановительным агентом или с бораном как восстановительным агентом в присутствии хирального вспомогательного соединения. Способ приводит к энантиоселективному/диастереоселективному восстановлению прохирального кетона так, что из двух возможных эпимеров IVa или IVb образуется предпочтительно один соответствующий эпимер. Степень энантиоселективности/диастереоселективности будет зависеть от используемого восстановительного агента, хирального вспомогательного соединения и условий реакции.
Реакция восстановления соединения общей структуры III обычно протекает в температурном интервале от -80°С до 70°С, в таком как от -40°С до 60°С, в таком как от -15°С до 50°С, в таком как от -5°С до 40°С, например от 0°С до 5°С или от 5°С до 35°С. В одном варианте осуществления температурный интервал составляет от 10°С до 30°С, от 15°С до 25°С, от 15°С до 20°С. Оптимум температуры будет зависеть от специфических условий реакции и используемых реагентов. В одном варианте осуществления настоящего изобретения реакционную смесь немедленно охлаждали до 0-10°С после завершения, чтобы избежать образования побочных продуктов. Если N,N-диэтиланилин используют как восстановительный агент, то N,N-диэтиланилин может легко быть удален из реакционной смеси экстракцией с водной соляной кислотой. Одномолярный эквивалент по отношению к основанию, экстрагируемому 1 М соляной кислотой, является предпочтительным.
Восстановительный агент, возможно, растворенный или смешанный с инертным растворителем, может быть добавлен к соединению общей структуры III, возможно, растворенному или смешанному с инертным растворителем, например, в инертной атмосфере, такой как азот. Альтернативно, соединение общей структуры III, возможно, растворенное или смешанное с инертным растворителем, может быть добавлено к восстановительному агенту, возможно, растворенному или смешанному с инертным растворителем (обратный порядок).
В одном варианте осуществления настоящего изобретения восстановительный агент используют в эквимолярном количестве или в молярном избытке относительно соединения общей структуры III. В специфическом варианте осуществления настоящего изобретения молярное соотношение восстановительный агент/соединение общей структуры III составляет 1,0-5,0. В предпочтительном в настоящее время варианте осуществления настоящего изобретения молярное соотношение восстановительный агент/соединение общей структуры III составляет 1,8-3,0, такое как 2,3-3,9, такое как 2,5-2,7.
Хиральное вспомогательное соединение может реагировать с восстановительным агентом до восстановления in situ для образования хирального восстановительного агента или хиральное вспомогательное соединение может, например, служить как хиральный лиганд в комплексе с восстановительным агентом, то есть, например, образовывать хиральный восстановительный агент. Настоящее изобретение включает в себя использование таких хиральных восстановительных агентов или комплексов хиральный лиганд-восстановительный агент, которые получают и выделяют отдельно перед использованием для восстановления соединения общей структуры III.
Термин «восстановительный агент в присутствии хирального вспомогательного соединения», таким образом, включает в себя любой хиральный восстановительный агент. Например, хиральное вспомогательное соединение может реагировать с борановым восстановительным агентом до восстановления in situ с образованием хирального боранового восстановительного агента или хиральное вспомогательное соединение может служить как хиральный лиганд в борановом комплексе. Примеры таких хиральных борановых восстановительных агентов представляют собой хиральные оксаборолидины или оксазаборолидины, такие как хиральные оксазаборолидиновые реагенты, полученные из (1R,2S)-цис-1-aмино-2-инданола,(1S,2R)-цис-1-aмино-2-инданола, (S)-пролинола или B-(3-пинанил)-9-борабицикло[3.3.2]нонан(alpine-borane) или, например, 5,5-дифенил-2-метил-3,4-пропано-1,3,2-оксазаборолидина, (S)-2-метил-CBS-оксазаборолидина, (R)-2-метил-CBS-оксазаборолидина. Настоящее изобретение включает в себя поэтому использование таких хиральных восстановительных агентов как хиральные борановые восстановительные агенты, или как комплексы хиральный лиганд-восстановительный агент, такие как хиральный лиганд-борановые комплексы, которые получают и выделяют перед использованием для восстановления соединения общей структуры III.
Другой пример хирального лиганда в комплексе с восстановительным агентом представляет собой комплекс LiALH4 и 2,2'-дигидрокси-1,1'бинафтила.
Молярное соотношение восстановительный агент/хиральное вспомогательное соединение находится обычно в интервале 0,1-20,0, таком как 0,4-10, таком как 0,3-5,0, таком как 0,5-4,5, таком как 1,0-4,0, таком как 1,9-3,1, таком как 2,1-2,9, таком как 2,3-2,7, например 10,8, 5,4, 2,6, 2,5 или 1,6.
Хиральное вспомогательное соединение может присутствовать в каталитических количествах, таких как субстехиометрические, или в эквимолярных, или в молярном избытке по отношению к соединению общей структуры III или к восстановительному агенту. Например, соотношение хиральное вспомогательное соединение/соединение III может быть 0,25-2,5, таким как 0,5-2,0, таким как 0,8-1,3, таким как 0,9-1,2, таким как 1,0-1,1.
Выбор конкретного энантиомера хирального вспомогательного соединения будет определять стереоселективную ориентацию гидроксигруппы соединения общей структуры IV относительно C-24. Хиральное вспомогательное соединение, которое преимущественно приводит к S-конфигурации, при С-24 является предпочтительным.
Реакции, катализируемые боранами, были, например, рассмотрены Deloux and Srebnik [Chem. Rev.93, 763, 1993]. Примеры эффективных катализаторов, основанных на хирально модифицированных боранах, могут, например, быть найдены в [A.Hirao, J.Chem. Soc. Chem. Commun. 315,1981; E.J. Corey, J. Am. Chem. Soc. 109, 7925, 1987].
Примеры синтеза и/или использования, например, 1,2- и 1,3-аминоспиртов в стереоселективном восстановлении с бораном могут, например, быть найдены в [E.Didier et al.; Tetrahedron 47, 4941-4958, 1991; C.H. Senanayake et al., Tetrahedron Letters, 36(42), 7615-18, 1995, EP 0698028, EP 0640089, EP 0305180, WO 93/23408, WO 94/26751]. Синтез и/или использование хиральных цис-1-амино-2-инданолпроизводных в борановом восстановлении может, например, быть найден в [C.H. Senanayake, Aldrichimica Acta, 31(1), 1-15, 1998; A.K. Ghosh et al., Sinthesis, 937-961, 1998; Y. Hong et al., Tetrahedron Letters, 35(36), 6631-34, 1994; B.Di Simone, Tetrahedron Assimetry, 6(1) 301-06, 1995; Y. Hong et al., Tetrahedron Letters, 36(36), 6631-34, 1994; R. Hett et al., Org. Process. Res. Dev., 2, 96-99, 1998; или EP 0763005] и в ссылках, там цитируемых.
Способы получения кальципотриола, как здесь описаны, могут быть модифицированы в отношении последовательности реакционных стадий, пропуска одной или более реакционных стадий, или ввода дополнительных стадий очистки или взаимодействия на любой стадии последовательности реакций. Настоящее изобретение включает в себя все такие модификации.
Способ получения кальципотриола, как здесь описан, включает в себя дополнительно все варианты, в которых гидроксизащитные группы R1 и/или R2 для соединений или промежуточных соединений, где R1 и/или R2 не являются водородом, удаляются на любой стадии реакционной последовательности. Соединения или промежуточные соединения, в которых R1 и/или R2 представляют собой водород, могут быть защищены защитными агентами на любой стадии реакционной последовательности, вклю